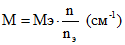СПРАВКА
Источник публикации
М., 1988
Примечание к документу
Документ включен в Перечень международных и региональных (межгосударственных) стандартов (п. п. 15, 63, 67, 70, 1330, 1362, 1366), а в случае их отсутствия - национальных (государственных) стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента Таможенного союза "О безопасности продукции, предназначенной для детей и подростков" (ТР ТС 007/2011) и осуществления оценки соответствия объектов технического регулирования (Решение Коллегии Евразийской экономической комиссии от 14.03.2023 N 31).
Документ включен в Перечень международных и региональных (межгосударственных) стандартов, а в случае их отсутствия - национальных (государственных) стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента Таможенного союза "О безопасности игрушек" (ТР ТС 008/2011) и осуществления оценки соответствия объектов технического регулирования (Решение Комиссии Таможенного союза от 23.09.2011 N 798).
Документ включен в Перечень документов (пункты 3, 7, 50) в области стандартизации, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения технического регламента Таможенного союза "О безопасности продукции, предназначенной для детей и подростков" (ТР ТС 007/2011) и осуществления оценки соответствия объектов технического регулирования (Решение Комиссии Таможенного союза от 23.09.2011 N 797).
Взамен "Методических указаний по санитарно-гигиенической оценке резиновых изделий, применяемых в медицине", утв. Минздравом СССР 26.09.1975.
Название документа
"Методические указания по санитарно-гигиенической оценке резиновых и латексных изделий медицинского назначения"
(утв. Минздравом СССР 19.12.1986, Миннефтехимпромом СССР 25.12.1986)
"Методические указания по санитарно-гигиенической оценке резиновых и латексных изделий медицинского назначения"
(утв. Минздравом СССР 19.12.1986, Миннефтехимпромом СССР 25.12.1986)
Содержание
Начальник управления по внедрению
новых лекарственных средств
и медицинской техники
Минздрава СССР
Ю.Г.БОБКОВ
19 декабря 1986 года
Зам. министра
нефтеперерабатывающей
и нефтехимической
промышленности СССР
Н.Т.ЧЕТВЕРИКОВ
25 декабря 1986 года
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ПО САНИТАРНО-ГИГИЕНИЧЕСКОЙ ОЦЕНКЕ РЕЗИНОВЫХ
И ЛАТЕКСНЫХ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
Методические указания подготовлены Научно-исследовательским институтом резиновых и латексных изделий Миннефтехимпрома под редакцией зам. директора по научной работе, д.т.н. Д.П. Трофимовича, сотрудниками химико-аналитической лаборатории (зав. лаб., к.х.н. Ю.Г. Чикишев, н.о. Е.А. Кузнецова, н.с. Э.З. Ольпинская), токсикологической лаборатории (зав. лаб., к.м.н. Н.И. Шумская, с.н.с., к.м.н. В.Н. Жиленко, м.н.с. Л.Г. Котова), лаборатории медицинских изделий (зав. лаб., к.т.н. Г.К. Мельникова), а также сотрудниками отдела токсикологических исследований и испытаний полимерных, других материалов и изделий медицинского назначения ВНИИИ медицинской техники Минздрава СССР (зав. отделом, к.м.н. В.Г. Лаппо).
Методические указания предназначены для осуществления предварительной гигиенической оценки вновь разрабатываемых резиновых и латексных медицинских изделий с целью получения разрешения Минздрава СССР на возможность их широкого применения по назначению, для проведения контроля <*> выпускаемых резиновых и латексных изделий на заводах-изготовителях, а также в учреждениях, использующих эти изделия.
--------------------------------
<*> Контроль осуществляется по действующей технической документации (ТУ, ГОСТы) до окончания срока их действия. При создании новой технической документации и пересмотре существующей необходимо использовать рекомендации настоящих "Методических указаний..."
В 1975 году впервые были разработаны "Методические указания по санитарно-гигиенической оценке резиновых изделий, применяемых в медицине", утвержденные МЗ СССР 26 сентября 1975 г.
За период 1975 - 85 г.г. получены новые данные по обоснованию методических подходов при изучении биологически активности резиновых материалов, а также разработаны новые и усовершенствованы существующие химические методы анализа веществ, мигрирующих из резин в контактирующие среды. Это послужило основанием для создания нового варианта "Методических указаний по санитарно-гигиенической оценке резин для изготовления изделий медицинского назначения".
В "Методических указаниях" представлены гигиенические требования к резиновым изделиям медицинского назначения, схемы проведения исследований, методы определения соединений, выделяющихся из резин, гигиенические нормативы миграции вещества (ДКМ), перечень ингредиентов, рекомендуемых для использования в рецептурах резиновых смесей.
С опубликованием данных "Методических указаний" теряют силу изданные ранее "Методические указания", М., 1975 г.
1.1. В состав резин, предназначенных для изготовления изделий медицинского назначения, могут вводиться ингредиенты, предусмотренные перечнем рекомендуемых веществ (см. приложение 1).
1.2. Рецептура резины после проведения гигиенических исследований должна быть согласована с органами здравоохранения.
1.3. При использовании импортных материалов необходимо получить документ о разрешении использования его в экспортируемой стране, а также провести проверку соответствия качественного состава материала действующему стандарту на идентичные продукты отечественного производства.
РЕЗИНОВЫХ И ЛАТЕКСНЫХ ИЗДЕЛИЙ
2.1. Санитарно-гигиеническая оценка резиновых изделий должна осуществляться с учетом их назначения и конкретных условий эксплуатации (см. таблицу 5.1).
2.2. Образцы резиновых и латексных изделий должны быть с однородной, гладкой, сухой, нелипкой внутренней и наружной поверхностями.
2.3. Резины не должны выделять в контактирующие среды химические вещества в количестве, превышающем допустимые количества миграции (ДКМ - см. приложение 2), изменять свойства лекарственных препаратов, оказывать токсическое действие на организм человека.
2.4. Импортные образцы резин подлежат санитарно-гигиеническим исследованиям в условиях, аналогичных условиям при испытании отечественных образцов.
3.1. В учреждения, осуществляющие гигиенические исследования, должны направляться образцы резин или изделия из них с указанием следующих данных:
- наименование изделия, область его применения (конкретное назначение), условия эксплуатации (время, температура контакта с биологическими средами и другие);
- сведения о технологии изготовления изделий;
- дата изготовления;
- рецептура резин в массовых частях ингредиентов с указанием на них ГОСТов, ОСТов, ТУ.
3.2. Количество образцов, необходимое для гигиенического исследования, определяется исполнителем (технологами, химиками, токсикологами).
3.3. Организация, выполняющая гигиенические исследования, оформляет полученные результаты в виде гигиенического заключения и представляет его на рассмотрение во ВНИИИМТ.
4.1. Гигиеническая оценка вновь разрабатываемых резиновых изделий медицинского назначения заключается в проведении санитарно-химического и биологического исследования.
4.2. Санитарно-химический контроль резиновых изделий предшествует биологическим исследованиям.
4.3. В случае несоответствия резин санитарно-химическим показателям токсикологические исследования этих образцов не проводится (приложение 2).
И ПРОВЕДЕНИЕ САНИТАРНО-ХИМИЧЕСКИХ ИССЛЕДОВАНИЙ
5.1. Образцы изделий, поступившие на испытания, подвергают предварительной обработке в соответствии с назначением (см. приложение 4).
5.2. Вытяжки готовят в соответствии с условиями моделирования, приведенными в таблице 5.1.
Таблица 5.1
и выбор условий приготовления вытяжек
Номер группы | Наименование группы | Наименование изделий | Условия эксплуатации | Условия приготовления вытяжек | |||||
Среда | Время | Температура, °C | Модельная среда | S/V, см2/см3 | Температура, °C | Время | |||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
1. | Изделия для внутреннего протезирования | Эндопротезы костей и суставов, имплантаты для челюстно-лицевой хирургии, протезы мягких тканей, искусственные клапаны сердца, имплантаты для глазных операций, баллоны для окклюзии сосудов | Внутренние среды организма человека, кровь, лимфа | Пожизненно (постоянно) | 36 - 40 | Дистиллированная вода физиологический раствор | 1:1 | 40 | 30 суток |
2. | Изделия для контакта с кровью | Пробки для укупорки сосудов с кровью, кровезаменителями и другими парентеральными препаратами | Кровь, кровезаменители, инфузионные растворы | Стерилизация 45 мин, хранение от 2 до 5 лет | 120 + 2 | То же | 1:2 | Автоклавирование | |
120 | 30 мин | ||||||||
Настаивание | |||||||||
25 | 5 суток | ||||||||
Трубки медицинские для переливания крови | То же | 1 - 3 суток | 36 - 40 | -"- | 1:2 | 40 | 24 ч | ||
Трубки латексные для систем переливания крови (одноразового пользования) | -"- | 4 - 6 ч | 36 - 40 | -"- | 1:2 | 40 | 8 ч | ||
Детали к аппаратам АИК и АИП | -"- | до 24 ч | 36 - 40 | -"- | 1:2 | 40 | 24 ч | ||
3. | Фармацевтические изделия | Пробки для укупорки антибиотиков, биологических и эндокринных препаратов | Порошкообразные и жидкие стерильные препараты, водные, спиртовые | Стерилизация 1 час, хранение от 2 до 5 лет | 120 | Дистиллированная вода, физиологический раствор, спиртовой раствор | 1:2 | Автоклавирование | |
120 | 30 мин | ||||||||
Настаивание | |||||||||
не выше 25 | 25 | 5 суток | |||||||
Детали к инъекторам | Биосреды: вакцины, сыворотки, бактериальные и вирусные препараты | Кратковременно | 25 | Дистиллированная вода, физиологический раствор | 1:2 | 40 | 1 ч | ||
Трубки медицинские вакуумно-бактериологические | То же | Кратковременно (на потоке) | 120 | То же | 1:2 | 40 | 8 ч | ||
Колпачки латексные к медицинским пипеткам | Контакт через воздух с лекарственными препаратами жидкими | Кратковременно | 25 | Воздух | 1:5 | 25 | 2 ч | ||
4. | Изделия, используемые для гастроэнтерологии, урологии, акушерства и анестезиологии | Зонды различных типов, оболочки эндоскопов, катетеры урологические различных типов, трубки ректальные, латексные комплектующие детали к зондам, баллонам и катетерам, маточные кольца, изделия N 2 | Внутренние среды организма человека: желудочный сок, желчь, слизь, слюна, моча | От 15 мин до 1 суток | 36 - 40 | 1:2 | 40 | 8 ч | |
Трубки интубационные разных типов, в том числе латексные армированные, катетеры для бронхографии и отсасывания слизи, канюли к интубационным трубкам (герметизир) | Слюна, слизь, воздух, газовоздушные смеси | От 1 ч до 3 суток | 36 - 40 | Дистиллированная вода, воздух | 1:2 | 40 | 24 ч | ||
1:2,75 (для воздуха) | 25 | 24 ч | |||||||
Дренажи желчных путей типа Кера и другие, катетеры самоудерживающиеся крупноголовчатые типа Петнера и Малеко, катетеры-дренажи типа Фолея, трубки дренажные | Внутренние среды организма человека, кровь, лимфа | От 1 суток до 15 суток | 36 - 40 | Дистиллированная вода, физиологический раствор, дистиллированная вода подкисленная (pH 4,0) или подщелоченная (pH 9,0) | 1:2 | 40 | 24 ч | ||
Изделия санитарии и гигиены ухода за больными | Кружки Эсмарха, грелки, спринцовки, каплесчитатели, пузыри для льда, жгуты Эсмарха, губка туалетная | Кожа, слизистые покровы, лекарственные препараты | До 1 ч | 36 - 40 <*> | Дистиллированная вода, физиологический раствор | 1:2 | 40 | 1 ч | |
Кало-мочеприемники, подкладные круги, бинты Мартинса, гигиенические пояса, хирургические и анатомические перчатки, напальчники и др. (подушки кислородные) | Воздух, обогащенный кислородом | До 24 ч. | 36 - 40 | Дистиллированная вода, воздух | 1:2 | 40 | 1 ч | ||
до 25 | 1:2,75 (для воздуха) | 25 | 24 ч | ||||||
6. | Комплектующие детали к наркозно-дыхательной аппаратуре и к диагностическим приборам | Маски наркозные, в том числе латексные для новорожденных, детали к аппаратам ручной искусственной вентиляции легких, мешки и меха (гофрированные) дыхательные, трубки гофрированные дыхательные, формовые детали к приборам и аппаратам (диафрагмы, переходники, уплотнители, пробки и т.д.) | Воздух, обогащенный кислородом | До 24 ч | 36 - 40 | Дистиллированная вода, воздух | 1:2 | 40 | 1 ч |
до 25 | 1:2,75 (для воздуха) | 25 | 24 ч | ||||||
Трубки слуховые, трубки соединительные, детали к операционным столам, баллоны к медицинским приборам | Кожа | Кратковременно | 25 | Дистиллированная вода | 1:2 | 25 | 1 ч | ||
--------------------------------
<*> При применении грелки для обогрева тела температура может доходить до 95 °C, но контакт тогда только через ткань.
В стеклянный сосуд с притертой пробкой или плотно закрывающейся пластинкой, заполненный модельной средой необходимой температуры, помещают исследуемый образец так, чтобы его поверхность со всех сторон соприкасалась с жидкостью. При приготовлении автоклаватов колбу из нейтрального стекла с притертой пробкой, в которую помещен образец с модельным раствором, стерилизуют в автоклаве при температуре 120 + 2 °C и давлении 1,1 атм.
5.3. Гигиеническую оценку образцов проводят по схеме в следующем порядке:
- органолептическое исследование образцов резин и вытяжек из них;
- определение миграции химических веществ в воздух, дистиллированную воду и модельные среды в соответствии с рецептурой и областью применения;
- биологическое исследование резин в соответствии с назначением и условиями эксплуатации.
ОБРАЗЦОВ РЕЗИН И ВЫТЯЖЕК ИЗ НИХ <*>
--------------------------------
<*> Органолептические исследования производственными лабораториями не проводятся.
Для проведения органолептических испытаний привлекаются лица, которые могут четко различать запах, вкус и привкус образцов. Дегустаторов должно быть не менее 5 человек. Каждый дегустатор заносит результаты в индивидуальную карту и подписывает ее.
Отбор дегустаторов проводится на основании их способности определять вкус следующих растворов в концентрации г на 100 см3:
- сладкий | - сахароза | 0,8 |
- соленый | - хлористый натрий | 0,25 |
- кислый | - лимонная или | 0,03 |
винная кислота | 0,018 | |
- горький | - кофеин или хинин (хлоргидрат) | 0,002 |
и запах:
- уксусная кислота | 0,09% |
- хлороформ | 0,05% |
- водный раствор этилацетата | 0,007% |
Для дегустации пригодны лица, определяющие указанные эталоны.
При органолептическом исследовании образцов отмечают: характер поверхности (сухая, липкая, гладкая, наличие трещин и т.д.); характер запаха (например: запах резины, фенольный, ароматический и т.д.).
Целью органолептических исследований является определение наличия, интенсивности и характера запаха воздуха, создаваемого химическими веществами, выделяющимися из исследуемого материала.
Оценка интенсивности запаха проводится по 5-ти балльной шкале /1/.
Таблица 6.1
Количественная оценка в баллах | Характеристика запаха |
0 | Не отмечается ни одним из дегустаторов |
1 | Едва заметный; обнаруживается наиболее чувствительными лицами |
2 | Слабый, не привлекающий внимания, но обнаруживаемый, если указать на него |
3 | Отчетливый, легко обнаруживаемый дегустаторами |
4 | Обращающий на себя внимание и вызывающий отрицательный отзыв |
5 | Настолько сильно, что вызывает неприятное ощущение |
Вытяжки из резин готовят согласно п. 5 и таблицы 5.1.
При органолептическом исследовании вытяжки отмечают:
- характер привкуса характеризуется словами: горьковатый, щиплющий, нефтепродуктов, посторонний неопределенный.
Интенсивность привкуса выражают словами: слабый привкус, ясно выраженный, сильный;
- мутность вытяжек характеризуют описательно: слабая опалесценция, заметная опалесценция, сильная опалесценция, слабая муть, сильная муть;
- осадок характеризуют по его величине: незначительный, большой. Кроме того, отмечают его свойства: кристаллический, аморфный и т.п.; отмечают цвет осадка: белый, серый, бурый и т.п.
6.3.1. Запах и его интенсивность определяют сразу же после окончания соответствующей экспозиции во всех вытяжках из исследуемого образца при комнатной температуре и температурах, предусмотренных условиями моделирования по п. 5.1 путем закрытой дегустации.
6.3.2. Вкус и привкус определяют только в модельных растворах из исследуемого изделия при комнатной температуре и при температуре около 40 °C по сравнению с контролем, методом закрытой дегустации, аналогично определению запаха.
6.3.3. Для исследования запаха и привкуса вытяжек в четыре колбы с притертыми пробками вместимостью до 100 см3 вносят: в три колбы по 50 см3 контрольной пробы, а в одну - 50 см3 исследуемой пробы. Предварительно каждому дегустатору предлагают открыто ознакомиться с запахом контрольного раствора. Для этого одну из 3-х колбочек с контрольным раствором тщательно взбалтывают, открывают пробку и предлагают слегка втянуть в нос воздух из колбы у самого горлышка. После этого проводят закрытую дегустацию растворов в оставшихся трех колбочках, чтобы выявить наличие запаха исследуемой пробы.
6.3.4. Для определения привкуса набирают в рот 10 - 15 см3 заведомо известной контрольной пробы, держат во рту несколько секунд, а затем сплевывают. Точно так же поступают с остальными растворами.
6.3.5. В соответствии с табл. 6.2 оценивают интенсивность запаха и привкуса вытяжек из изделий, контактирующих с полостью рта. Из всех полученных результатов определения интенсивности запаха и привкуса выводят среднее арифметическое значение, выраженное целым числом и его десятыми долями. Образец считается удовлетворительным, если интенсивность запаха образца (табл. 6.1) не превышает трех баллов, а интенсивность запаха и привкуса вытяжек (табл. 6.2) - не более двух баллов.
Таблица 6.2
Интенсивность в баллах | Степень изменений | Определение изменений |
0 | Запах, привкус отсутствуют | Различия не обнаружены ни одним дегустатором |
1 | Слабый запах или привкус Различия между опытными образцами незначительны | Различия заметны и установлены 50% дегустаторов |
2 | Заметный запах или привкус | Различия легко определяемые всеми дегустаторами |
3 | Сильный запах или привкус | Изменения, явно заметные и вызывают отрицательный отзыв |
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущены опечатки: имеются в виду пункты 5.1 и 5.2, а не 6.1 и 6.2 соответственно. |
Для анализа используются реактивы квалификации "о ч", "ч.д.а.", "х.ч.". Подготовку образцов к исследованию и приготовление вытяжек проводят согласно п.п. 6.1, 6.2 в соответствии с табл. 5.1.
К интегральным показателям относятся определение величины pH, окисляемости, сухого остатка. Эти показатели дают возможность установить общее количество мигрирующих веществ из изделий медицинского назначения в вытяжки.
Приборы и посуда
1. Потенциометр pH-340 или др. марки.
2. Нефелометр НФМ или НФР.
3. Сушильный шкаф лабораторный по ГОСТ 7365-65.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-80 с 1 января 1989 года Постановлением Госстандарта СССР от 23.06.1988 N 2472 введен в действие ГОСТ 24104-88. Взамен ГОСТ 24104-88 с 1 июля 2002 года Постановлением Госстандарта России от 26.10.2001 N 439-ст введен в действие ГОСТ 24104-2001. |
4. Весы аналитические типа ВЛА-200 по ГОСТ 24104-80Е и др.
5. Эксикатор без крана по ГОСТ 25336-82Е
(Заполненный прокаленным хлористым кальцием).
6. Горелки газовые, лабораторные или электроплитки.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 10394-72 Постановлением Госстандарта СССР от 15.07.1982 N 2670 с 1 января 1984 года введен в действие ГОСТ 25336-82. |
7. Стаканы стеклянные по ГОСТ 10394-72, вместимостью 100 - 500 см3.
8. Колбы конические Эрленмейра по ГОСТ 10394-72, вместимостью 100 - 350 см3.
9. Холодильник Либиха по ГОСТ 25336-82Е.
10. Бюретки по ГОСТ 20292-74, вместимостью 25 см3 с притертым краном.
11. Колбы измерительные до ГОСТ 1770-74, вместимостью 25 - 1000 см3.
12. Стекла часовые.
13. Кварцевые чашки, вместимостью 100 см3.
14. Пипетки, вместимостью 5 - 100 см3 по ГОСТ 1770-74.
Величина pH характеризует кислотность или основность вытяжек из резин или из изделий. Величину pH измеряют потенциометрически. Допускается изменение величины pH вытяжки не более +/- 1,0 по отношению к pH "холостой" пробы.
--------------------------------
<*> Показатель используется только при оценке резин для контакта с инъекционными и диффузионными препаратами. Предельно допустимая величина окисляемости для указанных резин должна быть не более  .
.
 .
.Необходимые реактивы
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 4527-65, а не ГОСТ 4527-81. |
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 4527-65 Постановлением Госстандарта СССР от 11.02.1975 N 389 с 1 марта 1975 года введен в действие ГОСТ 20490-75. |
1. Калий марганцевокислый по ГОСТ 4527-71, 0,01Н раствор; 0,1Н раствор - реактив "а" (готовят в день проведения анализа из 0,1Н раствора).
2. Щавелевая кислота <**> по ГОСТ 5873-68, перекристаллизованная, 0,1Н раствор; 0,01Н раствор - реактив "б" (готовят в день проведения анализа из 0,1Н раствора).
--------------------------------
<**> Для более длительной сохранности 0,1Н раствора щавелевой кислоты рекомендуется при приготовлении его (перед доведением раствора в мерной колбе до метки) добавить 0,1Н раствора серной кислоты из расчета 20 см3 0,1Н раствора серной кислоты на 1 дм3 0,1Н раствора щавелевой кислоты.
3. Кислота серная по ГОСТ 4204-77, в разведении 1:3 по объему (реактив "в").
Проверка серной кислоты для проведения анализа
Исходную химически чистую серную кислоту предварительно проверяют на наличие восстанавливающих веществ. С этой целью проводят следующую пробу: в химический стакан или колбу из бесцветного стекла вместимостью 150 см3 наливают 60 см3 дистиллированной воды, 20 см3 испытуемой концентрированной серной кислоты и 5 см3 0,01Н раствора перманганата калия.
Параллельно ставят контрольную пробу - 60 см3 дистиллированной воды, 20 см3 испытуемой концентрированной серной кислоты. Затем в течение 5 минут ведут наблюдение за окраской жидкости в первой пробе при сравнении ее с контрольной пробой. Розовая окраска в первой колбе должна сохраняться не менее 5 минут. Исследуемая серная кислота непригодна для определения окисляемости, если окраска исчезает раньше.
4. Вода дистиллированная по ГОСТ 6709-72.
7.1.2.1. Ход определения
Для определения окисляемости всегда берут 100 см3 жидкости. Вначале проводят определение окисляемости в "холостой" пробе на проверку титра 0,01Н раствора перманганата калия. Затем определяют окисляемость испытуемой вытяжки.
В колбу при помощи пипетки наливают 100 см3 "холостой" пробы и 5 см3 серной кислоты (реактив "в"), опускают капилляры для равномерного кипения, колбу закрывают часовым стеклом, ставят на сетку и содержимое ее нагревают с таким расчетом, чтобы до момента закипания прошло около 7 минут. Отмечают момент закипания. Колбу снимают с огня и в кипящую жидкость из бюретки быстро приливают 15 см3 0,01Н раствора перманганата калия (реактив "в"). Затем колбу вновь ставят на сетку, соединяют с холодильником и кипятят ровно 15 минут, считая с отмеченного момента первоначального закипания. При этом нужно следить, чтобы кипение было равномерным, спокойным. По истечении 15 минут колбу снимают с огня, в нее из бюретки при помешивании быстро приливают 15 см3 0,01Н раствора щавелевой кислоты (реактив "б"), избыток которой тотчас же оттитровывают перманганатом (реактив "а"). Необходимо подчеркнуть, что титровать перманганатом можно только обесцветившуюся жидкость. При титровании избытка щавелевой кислоты в "холостой" пробе должно затрачиваться не более 1 см3 0,01Н раствора перманганата калия. Большее количество перманганата указывает на недостаточную чистоту дистиллированной воды. В этом случае определение следует прекратить, и приготовить вытяжку и контроль на свежей порции дистиллированной воды.
Определение окисляемости испытуемой вытяжки проводят так же, как и "холостой" пробы. В случае необходимости вытяжку берут в разведении: определенное количество вытяжки (10, 20, 40 см3 и т.д.) доводят до 100 см3 при помощи "холостой" пробы. Рекомендуется начинать определение с 50 см3 вытяжки + 50 см3 "холостой" пробы. Если при кипении в течение 8 - 10 минут (считая с момента первоначального закипания) цвет жидкости не изменяется, и она остается прозрачной, следует поставить определение с большим количеством вытяжки. В случае же сильного помутнения и побурения или обесцвечивания жидкости определение ставят с меньшим количеством жидкости <*>.
--------------------------------
<*> Рекомендуется во всех случаях проводить определение в 50 см3 вытяжки до конца для того, чтобы ориентировочно рассчитать количество вытяжки, которое нужно взять для определения.
Количество вытяжки, взятое для определения, должно в конечном счете быть таково, чтобы на титрование избытка щавелевой кислоты в испытуемой пробе пошло перманганата в 3 - 3,5 раза больше, чем в "холостой" пробе.
Определение следует проводить не менее, чем в двух параллельных пробах (из одной и той же вытяжки или "холостой" пробы). Расхождение между параллельными пробами не должно превышать 0,1 см3 0,01Н раствора перманганата калия.
Пример: на титрование избытка щавелевой кислоты в испытуемой пробе (50 см3 вытяжки + 50 см3 "холостой" пробы) пошло 4 см3 раствора перманганата калия, на титрование в "холостой" пробе - 0,8 см3 перманганата калия.
Нужно взять такое количество вытяжки, чтобы на титрование избытка щавелевой кислоты в нем пошло 2,4 + 2,8 см3 0,01Н раствора перманганата калия. Составляем пропорцию:
50 см3 | - 4,0 см3 0,01Н раствора |
X см3 | - 2,4 см3 0,01Н раствора |
X = 30 см3 | |
Значит для определения нужно взять около 30 см3 испытуемой вытяжки (соответственно доводя объем жидкости до 100 см3 при помощи "холостой" пробы).
Расчет
Окисляемость (x) выражают в миллиграммах кислорода, затраченного на окисление, в пересчете на 100 см2 общей поверхности резины, контактирующей с модельной средой и вычисляют по следующей формуле:
 ,
,где: а - количество 0,01Н раствора перманганата калия, пошедшего на титрование избытка щавелевой кислоты в испытуемой пробе, см3;
б - количество 0,01Н раствора перманганата калия, пошедшего на титрование избытка щавелевой кислоты в "холостой" пробе, см3;
к - коэффициент поправки для 0,01Н раствора перманганата калия;
В - объем испытуемой вытяжки, см3;
г - объем взятой для определения пробы испытуемой жидкости, см3;
д - общая поверхность определяемого образца, взятого для приготовления вытяжки; см2;
0,08 - количество миллиграмм кислорода, соответствующее 1 см3 0,01Н раствора перманганата калия.
7.1.3. Определение сухого остатка в водных вытяжках /1/
100 см3 вытяжки и контрольного раствора помещают в кварцевую чашку, предварительно доведенную до постоянного веса при температуре 100 +/- 3 °C. Постоянный вес считается достигнутым, если два последних взвешивания после высушивания в течение 1 часа дают разницу в 0,0005 г. Перед взвешиванием чашку помещают в эксикатор для охлаждения на 30 - 50 минут. Чашку с исследуемой вытяжкой помещают в сушильный шкаф с температурой 100 +/- 3 °C и выдерживают там до полного удаления жидкости. Взвешивание чашки с сухим остатком проводят с интервалом в 1 час до достижения постоянного веса. С учетом величины контрольного раствора остаток исследуемой вытяжки не должен превышать 5 мг.
Расчет сухого остатка (x) в % проводят по формуле:
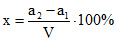 ,
,где: а1 - вес пустой чашки, г;
а2 - вес чашки с сухим остатком, г;
V - объем вытяжки, взятой для анализа, см3.
Определение следует проводить не менее, чем в 2-х параллельных пробах.
7.2. Метод тонкослойной хроматографии (ТСХ) для определения уровня миграции индивидуальных химических соединений <*>
--------------------------------
<*> В производственных лабораториях обязательным считается определение индивидуальных химических соединений (в зависимости от рецептуры), вошедших в приложение N 2.
Данный метод используется для определения уровня миграции ускорителей, стабилизаторов, пластификаторов и других соединений в вытяжке из резин.
Тонкослойная хроматография занимает особое место среди методов разделения, благодаря простоте и доступности оборудования. ТСХ - вид жидкостной хроматографии, в которой роль подвижной фазы (ПФ) выполняет жидкая фаза, а разделение смеси веществ происходит на тонком слое сорбента по мере ее продвижения. Анализируемые вещества наносят на линию старта на расстоянии 1,5 - 2 см от края хроматографической пластинки в виде концентрированных пятен диаметром не более 0,5 см или полосок длиной 8 - 10 мм, шириной 2 - 4 мм. Справа и слева от пробы наносят растворы "свидетелей" - аликвотные части стандартных растворов искомых веществ в количествах, соответствующих диапазону определяемых концентраций анализируемых соединений. Разделение проводят в хроматографической камере, на дно которой налит слой ПФ толщиной 0,5 см. После подъема ПФ примерно на 10 см пластинку вынимают, отмечают границу подъема ПФ (линия фронта растворителя) и сушат на воздухе. Определяемые вещества на пластинке обнаруживают двумя способами:
1) пластинку просматривают в УФ свете при длинах волн 254 или 366 нм, отмечая цвет и контуры светящихся пятен;
2) пластинку опрыскивают (проявляют) соответствующим для каждого класса соединений проявляющим реагентом. Определяемые вещества проявляются в виде окрашенных пятен. Положение пятен на хроматограмме характеризуется величиной Rf.
Rf - является качественной характеристикой положения вещества, специфичной для него в выбранных хроматографических условиях. Rf - это отношение расстояния между стартом и центром зоны (пятна) к расстоянию от старта до фронта растворителя. На рис. 1 представлена хроматограмма и расчет величины Rf.

А - линия старта;
Б и Б1 - центры локализации зон (пятен) веществ;
В - линия фронта;
1, 2 - точки нанесения индивидуальных веществ ("свидетелей");
3 - точка нанесения смеси веществ 1 и 2

Идентификацию веществ проводят путем сравнения окраски пятен и величины Rf пробы с окраской пятен и величины Rf "свидетелей". Наличие на пластинке при хроматографировании пробы пятна, совпадающего по величине Rf и окраске с пятном свидетеля" указывают на присутствие искомого соединения.
Определение проводится по результатам не менее 2-х параллельных опытов. Содержание вещества в пробе по хроматограмме определяют двумя путями.
1) По графику зависимости между логарифмом количества вещества в пробе и корнем квадратным из площади пятна 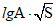 . Для построения градуировочного графика готовят серию растворов с точно известной концентрацией (5 - 6 концентраций). Растворы наносят на пластинку, хроматографируют и проявляют. На проявленную пластинку помещают прозрачную бумагу (кальку) и обрисовывают контуры пятен. Затем с помощью миллиметровой бумаги подсчитывают площадь пятен и строят калибровочный график. По построенному графику рассчитывают содержание вещества в исследуемой пробе.
. Для построения градуировочного графика готовят серию растворов с точно известной концентрацией (5 - 6 концентраций). Растворы наносят на пластинку, хроматографируют и проявляют. На проявленную пластинку помещают прозрачную бумагу (кальку) и обрисовывают контуры пятен. Затем с помощью миллиметровой бумаги подсчитывают площадь пятен и строят калибровочный график. По построенному графику рассчитывают содержание вещества в исследуемой пробе.
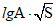 . Для построения градуировочного графика готовят серию растворов с точно известной концентрацией (5 - 6 концентраций). Растворы наносят на пластинку, хроматографируют и проявляют. На проявленную пластинку помещают прозрачную бумагу (кальку) и обрисовывают контуры пятен. Затем с помощью миллиметровой бумаги подсчитывают площадь пятен и строят калибровочный график. По построенному графику рассчитывают содержание вещества в исследуемой пробе.
. Для построения градуировочного графика готовят серию растворов с точно известной концентрацией (5 - 6 концентраций). Растворы наносят на пластинку, хроматографируют и проявляют. На проявленную пластинку помещают прозрачную бумагу (кальку) и обрисовывают контуры пятен. Затем с помощью миллиметровой бумаги подсчитывают площадь пятен и строят калибровочный график. По построенному графику рассчитывают содержание вещества в исследуемой пробе.2) Путем сравнения размера пятна и интенсивности окраски анализируемого вещества с интенсивностью окраски и величиной пятен "свидетелей", хроматографируемых рядом с пробой в одинаковых условиях (полуколичественная оценка). Содержание вещества в анализируемом растворе выражают в мг/дм3 по формуле:
 ,
,где: А - содержание вещества в вытяжке, мг/дм3;
а - содержание вещества в исследуемой пробе, мг;
V - объем вытяжки, взятой для экстракции, см3.
Количественное определение можно также осуществлять по измерению интенсивности отраженного света с помощью денситометрии по калибровочному графику или калибровочному коэффициенту. Для этой цели используют приборы - денситометры типа ERL-65 m (производство ГДР), БИАН-170 (отечественного производства) и др. Запись спектрограмм ведут согласно инструкции, прилагаемой к прибору.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду пункт 5, а не 6. |
Необходимые приборы и посуда:
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-80 с 1 января 1989 года Постановлением Госстандарта СССР от 23.06.1988 N 2472 введен в действие ГОСТ 24104-88. Взамен ГОСТ 24104-88 с 1 июля 2002 года Постановлением Госстандарта России от 26.10.2001 N 439-ст введен в действие ГОСТ 24104-2001. |
1. Весы аналитические типа ВЛА-200 по ГОСТ 24104-80Е и др.
2. Шкаф сушильный, лабораторный по ГОСТ 7365-65.
3. Эксикатор без крана по ГОСТ 25336-82Е.
4. Прибор для отгонки при нормальных условиях и в вакууме все на шлифах (круглодонные колбы, вместимостью 100 - 200 см3 по ГОСТ 25336-82Е; насадка Вюрца по ГОСТ 25336-82Е; холодильник Либиха по ГОСТ 25336-82Е; аллонж по ГОСТ 25336-82Е; капилляр).
5. Баня водяная по ГОСТ 9147-80.
6. Цилиндры измерительные по ГОСТ 1770-74Е, вместимостью 10 - 250 см3.
7. Ступки фарфоровые по ГОСТ 9147-73.
ИС МЕГАНОРМ: примечание. ГОСТ 2823-73 утратил силу с 1 апреля 1989 года. Действовал ГОСТ 27544-87 ("ИУС", N 4, 1989). Взамен ГОСТ 27544-87 Постановлением Госстандарта СССР от 30.03.1990 N 691 с 1 января 1991 года введен в действие ГОСТ 28498-90. |
8. Термометры лабораторные по ГОСТ 2823-73 до 100 °C с ценой деления 1 °C.
9. Насос водоструйный по ГОСТ 25336-82Е.
10. Делительные воронки по ГОСТ 25336-82Е, вместимостью 200 - 500 см3.
11. Лампа с максимумом ультрафиолетового излучения 253,7 нм со светофильтрами типа БС-3 (пропускание до 270 нм), БС-4 (пропускание до 280 нм) и УФС-3 (пропускание до 366 нм) по нормативно-технической документации.
12. Камера для хроматографирования - прямоугольный или цилиндрический сосуд с притертой крышкой, размеры камеры должны обеспечивать размещение в ней необходимых для проведения испытаний хроматографических пластин.
13. Опрыскиватель с тонким распылителем (пульверизатор).
14. Микрошприц или микропипетка с оттянутым капиллярным концом, вместимостью 0,01 см3, капилляры стеклянные для нанесения проб.
15. Пипетки градуированные по ГОСТ 20292-74, вместимостью от 0,1 до 100 см3.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 10394-72 Постановлением Госстандарта СССР от 15.07.1982 N 2670 с 1 января 1984 года введен в действие ГОСТ 25336-82. |
16. Стаканы стеклянные по ГОСТ 10394-72, вместимостью 100 - 500 см3.
17. Колбы измерительные по ГОСТ 1770-74, вместимостью 25 - 1000 см3.
18. Сита по ГОСТ 3584-73 (не менее 100 - 120 меш.).
19. Пробирки стеклянные по ГОСТ 25336-82Е.
20. Камера для опрыскивания пластинок - стеклянный колпак для насоса с кнопкой и рантом или другой, диаметром 200 - 500 мм.
21. Колбы конические Бунзена по ГОСТ 25336-82Е, толстостенные с боковым отводом (для фильтрования).
22. Стеклянные сосуды с притертой пробкой или плотно закрывающейся стеклянной пластинкой (емкости для приготовления вытяжек из резин).
23. Колбы конические Эрленмейра по ГОСТ 10394-72, вместимостью 250 см3.
24. Фотоэлектроколориметр (ФЗК 56М или другого типа).
25. Спектрофотометр (СФ-4, 16, 26, "Спекорд" и др.).
26. Пластинки с тонким слоем сорбента.
В практике работы методом тонкослойной хроматографии (ТСХ) используют пластинки с тонким слоем сорбента, выпускаемые промышленностью и приготовленные в лабораторных условиях.
26.1. Пластинки типа "Силуфол", выпускаемые ЧССР и другие.
26.2. Приготовление пластинок в лабораторных условиях:
26.2.1. С тонким слоем силикагеля. В ступке смешивают 6,9 г предварительно растертого и просеянного через сито 100 меш. силикагеля КСК (ГОСТ 3956-76), 0,7 г медицинского гипса с 18 см3 дистиллированной воды, которую добавляют небольшими порциями при перемешивании. Смесь тщательно растирают до получения сметанообразной массы и приготовленную сорбционную массу равномерно наносят на чистую сухую поверхность стеклянных пластин <*> (примерно три - пять штук) размером 90x120 мм или 120x180 мм. Сушат пластинки на воздухе при комнатной температуре на горизонтальной поверхности в течение суток. Хранят в эксикаторе над слоем силикагеля.
--------------------------------
<*> Стеклянные пластины тщательно моют водой, содой, хромовой смесью, дистиллированной водой и сушат в вертикальном положении.
26.2.2. С тонким слоем оксида алюминия.
25 г оксида алюминия (для хроматографии II степени активности) и 1,25 г гипса, предварительно просеянного через сито 100 меш смешивают в ступке и растирают с 50,0 см3 дистиллированной воды до получения однородной массы. Массу наносят равномерными слоем на 10 - 12 стеклянных пластинок и сушат на воздухе на горизонтальной поверхности.
Для извлечения и концентрирования отдельных компонентов из вытяжки применяют метод экстракции. Определенный объем вытяжки экстрагируют органическим растворителем в делительной воронке. Условия экстракции индивидуальных соединений, все необходимые для анализа реактивы и подвижные фазы представлены в методиках определения индивидуальных веществ.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду пункт 7.2, а не 8.2. |
При изготовлении медицинских резин и изделий из них наиболее широко применяют следующие классы ускорителей вулканизации: тиурам и дитиокарбаминаты (производные дитиокарбаминовой кислоты), тиазолы, сульфенамиды, гуанидины (дифенилгуанидин). В данном разделе представлены методики определения ускорителей и некоторых продуктов их превращения в вытяжках из резин (приготовление вытяжек п. 5 табл. 5.1 методом ТСХ (п. 8.2).
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду таблица 7.1, а не 8.1. |
Краткая характеристика ускорителей представлена в табл. 8.1.
Таблица 7.1
NN пп | Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Температура плавления, °C | |
1. | Тиурам Д | Тетраметилтиурамдисульфид |  | 240,41 | Порошок белый с серым оттенком | 145 | Растворим: в хлороформе, скипидаре, бензоле, сероуглероде |
2. | Тиурам Е | Тетраэтилтиурамдисульфид |  | 296,52 | Порошок белого цвета | 173 | Растворим: в хлороформе, бензоле; ограниченно в бензине, спирте |
3. | Тиурам ЭФ | Диэтилдифенилтиурамдисульфид |  | 292,61 | Порошок белого цвета с кремовым оттенком | 174 | Растворим: в бензоле, ацетоне, хлороформе |
4. | Цимат | Диметилдитиокарбамат цинка |  | 318,86 | Порошок белого цвета | 248 - 250 | Растворим: в разбавленных щелочах, плохо растворим в ароматических и хлорированных растворах |
5. | Этилцимат | Диэтилдитиокарбаминат цинка |  | 361,89 | Порошок белого цвета | 173 - 174 | Растворим: в хлороформе, бензоле |
6. | Вулкацит-П-экстра-Н | Этилфенилдитиокарбаминат цинка |  | 457,99 | Порошок белого цвета | 205 - 208 | Растворим: в бензоле, хлороформе |
В резинах, содержащих тиурамные ускорители, при вулканизации в присутствии окиси цинка образуются цинковые соли дитиокарбаминовой кислоты, соответствующие введенному ускорителю. При термическом распаде ускорителей, производных дитиокарбаминовой кислоты, возможно образование вторичных аминов.
Необходимые реактивы:
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Диоксан по ГОСТ 10455-80.
3. Циклогексан по ГОСТ 14198-78.
4. Четыреххлористый углерод ГОСТ 20288-74.
ИС МЕГАНОРМ: примечание. ГОСТ 10165-79 утратил силу с 1 января 1990 года (ИУС "Государственные стандарты", N 8, 1989). |
5. Дитизон по ГОСТ 10165-79, 0,05% раствор в четыреххлористом углероде.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 9968-73 Постановлением Госстандарта СССР от 19.12.1986 N 4123 с 1 января 1988 года введен в действие ГОСТ 9968-86. |
6. Метилен хлористый по ГОСТ 9968-73.
7. Гексан по ТУ 6-09-3375-78.
8. Бензол по ГОСТ 5955-75.
ИС МЕГАНОРМ: примечание. Здесь и далее в официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 22300-76, а не ГОСТ 2.2300-76. |
9. Эфир диэтиловый (серный) по ГОСТ 2.2300-76.
10. Натр едкий по ГОСТ 2263-79, 40% раствор.
11. Медь сернокислая по ГОСТ 4165-78, 5% раствор.
12. Висмут азотнокислый основной по ГОСТ 1021-76.
13. Кислота уксусная по ГОСТ 61-75 - ледяная, 10% раствор.
14. Калий иодистый по ГОСТ 4232-74.
15. Кислота соляная по ГОСТ 3118-77.
16. 2,6-дихлорхинон-4-хлоримид по ТУ 6-09-05-889-78, 1% раствор спиртовый.
17. Нингидрин по ТУ 6-09-2737-75.
18. Кадмий уксуснокислый по ГОСТ 5824-79.
19. Медь азотнокислая по ТУ ГКХ-РУ-1816-62.
20. Спирт этиловый по ГОСТ 18300-72.
21.1. Смесь диоксана и циклогексана (3:7).
21.2. Смесь бензола и хлористого метилена (или хлороформа) (4:1).
21.3. Смесь гексана и хлористого метилена (2:3).
21.4. Смесь четыреххлористого углерода и диэтилового эфира (24:1).
21.5. Метилен хлористый или хлороформ (2-х-ступенчатое хроматографирование).
22.1. Дитизон - 0,05% раствор в четыреххлористом углероде.
Реактив А. Растворяют 3,85 г основного азотнокислого висмута в 55 см3 дистиллированной воды и 25 см3 ледяной уксусной кислоты.
Реактив Б. Растворяют 8 г иодистого калия в 20 см3 дистиллированной воды.
Смешивают растворы А и Б. Полученный раствор устойчив в течение нескольких месяцев.
Реактив В. Готовят непосредственно перед употреблением: к 7 см3 смеси растворов А и Б добавляют 50 см3 дистиллированной воды, 10 см3 ледяной уксусной кислоты и затем по каплям концентрированную соляную кислоту, пока раствор не станет прозрачным.
Реактив В используют для проявления хроматограммы, устойчив несколько дней.
22.3. 2,6-дихлорхинон-4-хлоримид - 1% спиртовой раствор.
Способ приготовления:
I. Раствор 1 - 0,1 г нингидрина растворяют в 50 см3 этилового спирта и добавляют 10 см3 ледяной уксусной кислоты.
Раствор 2 - 0,5 г меди азотнокислой растворяют в 50 см3 этилового спирта.
Перед употреблением смешивают растворы 1 и 2 в соотношении 50:3.
II. 0,5 г нингидрина и 0,5 г кадмия уксуснокислого растворяют в 100 см3 10%-ного раствора уксусной кислоты в этиловом спирте.
22.5. Медь сернокислая - 5%-ный водный раствор.
23. Стандартные растворы ускорителей в хлороформе с концентрацией 100 мкг/см3.
Ход определения
Для определения ускорителей 50 см3 вытяжки экстрагируют в делительной воронке 3 раза по 5 минут, используя 10 см3 хлороформа на каждую экстракцию. После каждой экстракции смеси дают расслоиться. Объединенные хлороформенные экстракты собирают в колбу для отгонки растворителя или в выпарительную чашку, профильтровав их через сухой бумажный фильтр. Затем из экстракта удаляют растворитель до объема 0,1 - 0,3 см3 (из колбы растворитель отгоняют с холодильником Либиха на водяной бане с температурой 85 °C, из чашки - испарением на воздухе при комнатной температуре в вытяжном шкафу).
Хроматографирование на пластинках (силикагель + гипс) или типа "Силуфол" проводят по п. 7.2.1, используя при этом ПФ и окрашивающие реагенты, представленные в пунктах 21, 22 перечня необходимых реактивов и сводной табл. 7.2. Количественное определение осуществляется по п. 7.2.2. Предел обнаружения 0,025 мг/дм3.
Таблица 7.2
производных дитиокарбаминовой кислоты -
методом тонкослойной хроматографии
Определяемое соединение | Сорбент | Величина Rf в подвижных фазах | Окраска пятен на хроматограмме с проявляющим реагентом | |||||||
Бензол - Хлористый метилен (хлороформ) 4:1 | Гексан - хлористый метилен 2:3 | Диоксан-циклогексан 3:7 | Хлористый метилен или хлороформ <*> 2-х ступенчатое хроматографирование | Хлористый метилен, бензол, гексан 1:1:0,5 | Дитизон | Модифицированный нингидринный реагент | Реактив Драгендорфа | 2,6-дихлорхинон-4-хлоримид прогрев при 100 - 105 °C в течение 10 мин | ||
Тиурам Д | Силикагель + гипс, "Силуфол" | 0,24 +/- 0,04 | - | - | 0,32 +/- 0,04 | - | - | зеленая | красная | красно-коричневая |
Цимат | 0,51 +/- 0,04 | - | 0,40 +/- 0,02 | 0,56 +/- 0,04 | - | малиновая | зелено-коричневая | |||
Тиурам Е | 0,41 +/- 0,04 | - | - | - | - | - | зеленая | |||
Этилцимат | 0,71 +/- 0,04 | - | 0,60 +/- 0,02 | - | - | малиновая | зелено-коричневая | |||
Тиурам ЭФ | - | 0,34 +/- 0,02 | - | - | 0,30 +/- 0,02 | - | желто-зеленая | |||
Вулкацит-П-экстра-Н | - | 0,49 +/- 0,02 | 0,54 +/- 0,02 | - | 0,45 +/- 0,02 | малиновая | зелено-коричневая | |||
В табл. 7.3 представлена характеристика вторичных аминов - продуктов термического распада ускорителей - производных дитиокарбаминовой кислоты (тиурама Д и цимата - диметиламина; тиурама Е и этилцимата - диэтиламина; тиурама ЭФ и вулкацита-П-экстра-Н - моноэтиланилина).
Таблица 7.3
Химическое название | Структурная формула | Молекул. масса | Агрегатное состояние | Температура кипения, °C | Растворимость | Примечание |
1 | 2 | 3 | 4 | 5 | 6 | 7 |
Диметиламин |  | 45 | Бесцветный газ с резким запахом | 6,9 | Хорошо растворим в воде и органических растворителях | Образует кристаллические соли с кислотами. Выпускается 33%-ным водным раствором |
Диэтиламин |  | 81 | Бесцветная жидкость с резким запахом | 55 | Легко растворим в воде, спирте, эфире | Образует кристаллические соли с кислотами |
Моноэтиланилин |  | 109 | Жидкость от желтого до светло-коричневого цвета | 204 | Растворим в органических растворителях, умеренно - в воде, не растворим в щелочах |
Необходимые реактивы:
1. Кислота серная по ГОСТ 4204-77.
2. Метиловый спирт (метанол) по ГОСТ 6995-77.
3. Кислота уксусная, ледяная, по ГОСТ 61-75.
4. Ацетон по ГОСТ 2603-79.
5. Вода дистиллированная по ГОСТ 6709-72.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
6. Хлороформ по ГОСТ 20015-74.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 9968-73 Постановлением Госстандарта СССР от 19.12.1986 N 4123 с 1 января 1988 года введен в действие ГОСТ 9968-86. |
7. Метилен хлористый по ГОСТ 9968-73.
8. Бензол по ГОСТ 5955-75.
9. Нингидрин по ТУ 6-09-737-73.
10. 2,6-дихлорхинон-4-хлоримид по ТУ 6-09-05-889-78.
11. п-нитроанилин по ТУ 6-09-258-77.
12. Натрий азотистокислый (нитрит натрия) по ГОСТ 4197-74.
13. Кислота соляная по ГОСТ 3118-77.
14. Системы подвижных фаз:
ИС МЕГАНОРМ: примечание. Нумерация фаз дана в соответствии с официальным текстом документа. |
15. Проявляющие (окрашивающие) реагенты.
15.1. Раствор нингидрина. Способ приготовления: 0,1 г нингидрина растворяют в 50 см3 этилового спирта и добавляют 10 см3 ледяной уксусной кислоты.
15.2. 2,6-дихлорхинон-4-хлоримид - 1%-ный спиртовой раствор.
15.3. Диазотированный п-нитроанилин.
Способ приготовления: 0,7 г п-нитроанилина растворяют в 9 см3 концентрированной соляной кислоты и затем доводят объем раствора до 100 см3 дистиллированной водой. Непосредственно перед употреблением 4 см3 раствора п-нитроанилина по каплям и при охлаждении добавляют к 5 см3 1%-ного раствора нитрита натрия.
Определение диметил- и диэтиламинов
Диметил- и диэтиламины определяют в водных вытяжках после предварительной экстракции ускорителей хлороформом по п. 7.3.2.1. Водный слой переносят в прибор для отгонки растворителя в вакууме или в выпарительную чашку и добавляют 0,1 см3 0,01Н раствора серной кислоты. Раствор концентрируют до 0,1 - 0,3 см3 путем отгонки воды на водяной бане из чашки при температуре 85 - 90 °C, из колбы - в вакууме водоструйного насоса при температуре водяной бани 40 - 45 °C. Весь сконцентрированный раствор (0,1 - 0,3 см3) в виде сернокислых солей диметил- и диэтиламинов переносят на хроматографическую пластинку в соответствии с п. 7.2.1 и хроматографируют, используя систему подвижных фаз I и II перечня необходимых реактивов, а в качестве окрашивающего реагента раствор нингидрина. После опрыскивания проявляющим реагентом пластинку выдерживают в термостате при температуре 95 - 97 °C в течение 3 - 5 мин. Амины проявляются в виде ярко-розовых пятен.
Количественное определение проводят по п. 7.2.2.
Предел обнаружения аминов 0,02 мг/дм3.
Определение моноэтиланилина
Экстрагирование моноэтиланилина из вытяжек проводят как и при определении ускорителей по п. 7.3.2. Вытяжки кислого характера перед экстракцией подщелачивают 40%-ным раствором едкого натра до pH 10 - 11 по универсальной индикаторной бумаге. Сконцентрированный до 0,1 - 0,2 см3 хлороформенный раствор моноэтиланилина переносят на хроматографическую пластинку, хроматографируют в подвижной фазе III и проявляют раствором диазотированного п-нитроанилина или 2,6-дихлорхинон-4-хлоримида. Предел обнаружения 0,05 мг/дм3.
В табл. 7.4 представлены условия хроматографического определения исследуемых аминов.
Таблица 7.4
методом тонкослойной хроматографии
Определяемый амин | Сорбент | Величина Rf в подвижных фазах | Окраска пятен на хроматограмме с проявляющим реагентом | Примечание | ||||
Метанол-ацетон-вода-ледяная уксусная кислота 40:30:20:7 | Ацетон-вода-ледяная уксусная кислота 60:10:2,5 | Бензол-хлористый метилен-хлороформ 30:10:10 | Нингидрин | 2,6-дихлорхинон-4-хлоримид | Диазотированный п-нитроанилин | |||
Диметиламин | Силикагель + гипс, "Силуфол" | 0,03 +/- 0,02 | 0,18 +/- 0,02 | - | розовая | - | - | |
Диэтиламин | 0,31 +/- 0,02 | 0,31 +/- 0,02 | - | розовая | - | - | ||
Моноэтиланилин | - | - | 0,55 +/- 0,02 | - | синяя | оранжевая | ||
К производным 2-меркаптобензтиазола относятся ускорители вулканизации класса тиазолов и сульфенамидов. В табл. 7.5 дана краткая характеристика применяемых ускорителей - производных 2-меркаптобензтиазола.
Таблица 7.5
производных 2-меркаптобензтиазола
Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Температура плавления, °C | Растворимость |
Каптакс | 2-меркаптобензтиазол |  | 167,25 | Порошок от светло-желтого до желтого цвета | 170 | Растворим: в бензоле, хлороформе, ацетоне, щелочах; не растворим: в холодной воде; слабо растворим в горячей воде |
Альтакс | Ди-(2-бензтиазолил)-дисульфид |  | 332,5 | Порошок от белого до светло-желтого цвета | 170 | Растворим: в бензоле, толуоле, хлороформе, сероуглероде. Слабо растворим: в спирте, воде, разбавленных кислотах |
Сульфенамид Ц | N-циклогексид-2-бензтиазолил-сульфенамид |  | 263 | Порошок кремового или желто-белого цвета | 103 | Растворим: почти во всех органических растворителях. Не растворим: в воде, разбавленных растворах кислот и щелочей |
В процессе вулканизации резин, содержащих ускорители класса тиазолов и сульфенамидов, наиболее вероятными продуктами их превращения являются каптакс и альтакс. Эти соединения необходимо определять при исследовании резин, в рецептуре которых используются ускорители - производные 2-меркаптобензтиазола.
Необходимые реактивы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 9968-73 Постановлением Госстандарта СССР от 19.12.1986 N 4123 с 1 января 1988 года введен в действие ГОСТ 9968-86. |
2. Метилен хлористый по ГОСТ 9968-73.
3. Висмут азотнокислый основной по ГОСТ 10217-76.
4. Кислота уксусная ледяная по ГОСТ 61-75.
5. Вода дистиллированная по ГОСТ 6709-72.
6. 2,6-дихлорхинон-4-хлоримид по ТУ 6-09-05-889-78.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду стандарт ГОСТ 4166-76, а не ГОСТ 4155-76. |
7. Натрий сернокислый безводный по ГОСТ 4155-76.
9.1. Реактив Драгендорфа (способ приготовления см. п. 7.3.2, п.п. 22.2).
9.2. 2,6-дихлорхинон-4-хлоримид - 1%-ный спиртовой раствор.
10. Стандартный раствор каптакса, альтакса и сульфенамида Ц в хлороформе с концентрацией 100 мкг/см3.
Ход определения
Экстрагирование из вытяжек соединений класса 2-меркаптобензтиазола и идентификация их с помощью метода ТСХ осуществляется по п. 7.3.2 с использованием ПФ и проявляющих реагентов, указанных в пунктах 8, 9 перечня реактивов и растворов, а количественное определение по п. 7.2.2.
В табл. 7.6 представлены условия хроматографического определения ускорителей - производных 2-меркаптобензтиазола.
Таблица 7.6
ускорителей - производных 2-меркаптобензтиазола
Определяемое соединение | Сорбент | Величина Rf в подвижной фазе | Окраска пятен с проявляющими реактивами | Предел обнаружения, мг/дм3 | Примечание | |
2,6-дихлорхинон-4-хлоримид | Реактив Драгендорфа | |||||
Каптакс | Силикагель + гипс, "Силуфол" | 0,26 +/- 0,02 | оранжево-красная | красно-оранжевая | 0,05 + 0,07 | Пластинка, проявленная 2,6-дихлорхинон-4-хлоримидом, выдерживается в течение 5 - 10 мин при температуре 100 - 105 °C |
Альтакс | 0,40 +/- 0,02 | желтая | красно-оранжевая | 0,05 + 0,07 | ||
Сульфенамид Ц | 0,49 +/- 0,02 | желто-оранжевая | малиновая | 0,05 + 0,07 | ||
Дитиодиморфолин (ДТДМ) относится к классу серосодержащих ускорителей и используется в латексных и резиновых смесях. ДТДМ - химическое название N,N-дитиодиморфолин - имеет структурную формулу:

с М.м. 236
белый порошок с температурой плавления 120 - 124 °C. Растворяется в ацетоне, спирте, а также при нагревании в дихлорэтане, хлороформе, бензоле, эфире, практически не растворим в воде.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Гексан по ТУ 6-09-3375-78.
3. Нингидрин по МРТУ 6-09-2726-65.
4. Спирт этиловый по ГОСТ 18300-72.
5. Уксусная кислота ледяная по ГОСТ 61-75.
6. Медь азотнокислая по ТУ ГКХ-РУ-1816-62.
7. Калий иодистый по ГОСТ 4232-74.
8. Крахмал растворимый по ГОСТ 10163-76.
9. Перманганат калия по ГОСТ 4527-2-65.
10. Кислота соляная по ГОСТ 3118-77.
11. Дитиодиморфолин, перекристаллизованный.
12. Стандартный раствор дитиодиморфолина в хлороформе с концентрацией 100 мкг/см3.
13. Система подвижных растворителей смесь хлороформа с гексаном в соотношения 1,75:1.
Проявляющие реагенты:
14.1. Модифицированный раствор нингидрина (приготовление по п. 7.3.2.1 п.п. 22.4).
14.2. Калий-иодкрахмальный реагент
Способ приготовления:
Раствор А. 0,25 г иодистого калия растворяют в 25 см3 дистиллированной воды.
Раствор Б. 0,75 г крахмала растворимого заваривают в 25 см3 кипящей дистиллированной воды.
Растворы смешивают перед употреблением в соотношения 1:1.
15. Хлорная камера: в эксикатор с притертой крышкой и фарфоровой вставкой заливают смесь водных растворов перманганата калия (3%) и соляной кислоты (10%) в соотношения 1:1 так, чтобы раствор находился ниже уровня фарфоровой вставки не менее, чем 2 см.
16. Дистиллированная вода по ГОСТ 6709-72.
Ход определения
Экстрагирование и хроматографирование дитиодиморфолина из вытяжек проводят по п. 7.3.2, используя ПФ и растворы, указанные в перечне реактивов. При использовании калий-иодкрахмального реагента пластинку перед обработкой последним помещают на 5 минут в камеру с хлором, а затем сушат на воздухе до полного исчезновения запаха хлора. Дитиодиморфолин обнаруживается при этом в виде пятен темно-синего цвета. При использовании нингидрина пятна препарата окрашены в ярко малиновый цвет.
Rf дитиодиморфолина 0,35 +/- 0,03. Предел обнаружения 0,02 мг/дм3. Количественное определение проводят по п. 7.2.2.
В табл. 7.7 представлена краткая характеристика дифенилгуанидина (наиболее распространенного ускорителя класса гуанидинов) и анилина - продукта термического распада дифенилгуанидина.
Таблица 7.7
Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Температура плавления или кипения, °C | Растворимость |
Гуанид Ф | N,N'-дифенилгуанидин |  | 211,26 | Кристаллический порошок белого цвета | 151,5 | Растворим в хлороформе, толуоле, ацетоне, спирте. Практически не растворим в воде, бензине, бензоле |
Анилин | Аминобензол |  | 93 | Жидкость желтого цвета | 184 кипения | Растворим в воде (3,7 г в 100 г воды), спирте, ацетоне, эфире, бензоле и других органических растворителях |
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Спирт этиловый по ГОСТ 18300-72.
3. Аммиак водный по ГОСТ 3760-79, 25% раствор.
4. Углерод четыреххлористый по ГОСТ 20288-74.
5. Ацетон по ГОСТ 2603-79.
6. Кали едкое по ГОСТ 24363-80.
7. Натрий углекислый кристаллический по ГОСТ 84-76.
8. Кислота уксусная ледяная по ГОСТ 61-75.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 3118-77, а не ГОСТ 1318-78. |
9. Кислота соляная по ГОСТ 1318-78, раствор в воде 1:1.
10. Вода дистиллированная по ГОСТ 6709-72.
11. Стандартные растворы дифенилгуанидина и анилина в хлороформе с концентрацией 100 мкг/см3.
12. Подвижные фазы:
12.1. Смесь ацетона и аммиака (99:1,0).
12.2. Смесь четыреххлористого углерода, ацетона, аммиака (4:1:1,0).
13. Проявляющие (окрашивающие) реагенты:
13.1. 2,6-дихлорхинон-4-хлоримид, 1% спиртовой раствор.
13.2. Гипохлорид натрия.
СПОСОБ ПРИГОТОВЛЕНИЯ
100 г хлорной извести и 100 см3 дистиллированной воды перемешивают в течение 15 минут, добавляя при перемешивании раствор углекислого натрия (70 г углекислого натрия в 170 см3 дистиллированной воды), после этого масса густеет, а затем разжижается. Раствор дважды фильтруют через обеззоленный фильтр. Хранят раствор в темной склянке.
Ход определения
Для определения 100 см3 вытяжки экстрагируют в делительной воронке 3 раза по 5 минут, используя 15 см3 хлороформа на каждую экстракцию. Объединенные хлороформенные экстракты собирают в колбу для отгонки растворителя или выпарительную чашку, профильтровав их через сухой бумажный фильтр.
Вытяжки кислого характера перед экстракцией подщелачивают по универсальной индикаторной бумаге до pH 10 - 11. Затем из экстракта удаляют растворитель до объема 0,1 - 0,3 см3 (из колбы растворитель отгоняют с холодильником Либиха на водяной бане с температурой 85 °C, из чашки - испарением на воздухе при комнатной температуре в вытяжном шкафу. Хроматографирование на пластинках силикагель + гипс или типа "Силуфол" осуществляется по п. 7.2.1. Идентификация и количественное определение дифенилгуанидина осуществляется до п.п. 7.2.2, 7.3.2, используя ПФ и окрашивающие реагенты, представленные в перечне реактивов и таблице 7.8.
Таблица 7.8
дифенилгуанидина и анилина
Определяемое соединение | Сорбент | Величина Rf в подвижных фазах | Окраска пятна на хроматограмме с проявляющим реагентом | Предел обнаружения, мг/дм3 | ||
ацетон:аммиак (99:1) | четыреххлористый углерод:ацетон:аммиак (4:1:0,1) | Гипохлорид натрия | 2,6-дихлорхинон-4-хлоримид | |||
Дифенилгуанидин | Силикагель (КСК) + гипс, "Силуфол" | 0,36 +/- 0,03 | - | коричневая | синяя | 0,05 |
Анилин | - | 0,55 +/- 0,03 | - | серо-синяя | 0,01 | |
Определение анилина в вытяжках
Экстракцию анилина из вытяжки хлороформом проводят аналогично экстракции дифенилгуанидина, только вытяжку предварительно подщелачивают едким кали (1 - 3 г) до pH 9 - 10 по универсальной индикаторной бумаге. На каждую экстракцию расходуют 20 см3 хлороформа.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду пункт 7.2.2, а не 7.22. |
При анализе спирто-водных вытяжек последние подкисляют 2 - 3 каплями уксусной кислоты и отгоняют спирт в вакууме водоструйного насоса при температуре водяной бани не выше 50 °C, после чего экстрагируют, как указано выше. Объединенные хлороформенный экстракт подкисляют 3 каплями уксусной кислоты и концентрируют путем отгонки растворителя на водяной бане при температуре не выше 80 °C до объема 0,3 - 0,4 см3. Идентификацию и количественное определение проводят по п.п. 7.22, 7.3.2.
Стабилизаторы применяются для защиты резин и каучуков от различных видов старения и деструкции. В качестве стабилизаторов применяют соединения фенольного и аминного типа. В процессе эксплуатации резин стабилизаторы, как и возможные продукты их превращения, могут мигрировать в контактирующие среды.
Характеристика наиболее широко применяемых стабилизаторов в резинах медицинского назначения представлена в табл. 7.9.
Таблица 7.9
в резинах медицинского назначения
Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Температура плавления, °C | Растворимость |
Агидол-2 (противостаритель НГ-2246) | 2,2-метилен-бис-(4-метил-6-третбутилфенол) |  | 340,50 | Кристаллический порошок белого цвета | 133 | Растворяется в большинстве органических растворителей, не растворяется в воде |
Нафтам-2 (неозон Д) |  |  | 219,20 | Кристаллический порошок от белого до бежевого цвета | 108 | Растворяется в большинстве органических растворителей |
Необходимые реактивы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Гексан по ТУ 6-09-3375-78.
3. Этиловый эфир уксусной кислоты по ГОСТ 22300-76.
4. Кислота фосфорномолибденовая по ТУ 46-09-3540-79.
5. Спирт этиловый по ГОСТ 18300-72.
6. Подвижная фаза: смесь гексана с этиловым эфиром уксусной кислоты 9:1.
7. Проявляющий реагент: 10% спиртовой раствор фосфорномолибденовой кислоты.
8. Аммиак водный по ГОСТ 3760-79, 25% раствор.
Ход определения
50 см3 вытяжки экстрагируют дважды по 5 минут 15 см3 хлороформа. Концентрирование и хроматографирование по п. 7.2.1. Идентификацию и количественное определение проводят по п.п. 7.2.2 и 7.3.2 с использованием в качестве проявляющего реагента спиртового раствора фосфорномолибденовой кислоты с последующим выдерживанием пластинки в парах аммиака. НГ-2246 обнаруживается на пластинке в виде синих пятен с Rf 0,39 +/- 0,03. Предел обнаружения 0,06 мг/дм3.
Необходимые реактивы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Гексан по ТУ 6-09-3375-78.
3. Ацетон по ГОСТ 2603-79.
4. Натрий азотистокислый по ГОСТ 4197-74.
5. п-нитроанилин по ТУ 6-09-258-77.
6. 2,6-дихлорхинон-4-хлоримид по ТУ 6-09-05-889-78.
ИС МЕГАНОРМ: примечание. Здесь и далее в официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 3118-77, а не ГОСТ 3118-78. |
7. Кислота соляная по ГОСТ 3118-78.
8. Подвижные фазы:
а) смесь гексана:ацетона в соотношении 9:1
б) хлороформ.
9. Реагенты для обнаружения:
а) 1% спиртовой раствор 2,6-дихлорхинон-4-хлоримида (устойчив в течение 2-х недель, хранить в темном месте);
б) диазотированный п-нитроанилин.
Способ приготовления
0,7 г п-нитроанилина растворяют в 9 см3 концентрированной соляной кислоты и затем объем раствора доводят водой до 100 см3. Перед опрыскиванием пластинки к 4 см3 исходного раствора по каплям и при охлаждении льдом, добавляют 5 см3 1% водного раствора азотистокислого натрия.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 11078-78, а не ГОСТ 11073-78. |
10. Натр едкий по ГОСТ 11073-78.
Ход определения
50 см3 вытяжки экстрагируют дважды по 5 минут 15 см3 хлороформа (для вытяжек нейтрального и щелочного характера). Вытяжку кислого характера перед экстракцией подщелачивают 40% раствором едкого натра до pH 8,0. Хроматографирование проводят по п. 7.2.1. Идентификацию и количественное определение по п.п. 7.2.2 и 7.3.2. При использовании в качестве проявляющего реагента спиртового раствора 2,6-дихлорхинон-4-хлоримида неозон Д обнаруживается на пластинке в виде сине-фиолетовых пятен с Rf = 0,73 +/- 0,02; при использовании диазотированного п-нитроанилина окраска пятен малиновая. Предел обнаружения 0,03 мг/дм3.
--------------------------------
<*> Допускается определение ДОФ и ДБФ методом газовой хроматографии.
Краткая характеристика пластификаторов представлена в табл. 7.10.
Таблица 7.10
Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Растворимость |
ДБФ | Дибутилфталат |  | 278,34 | Бесцветная маслянистая жидкость | Растворим в этаноле, хлороформе, ацетоне и других растворителях |
ДОФ | Диоктилфталат |  | 393,40 | То же | То же |
Необходимые реактивы и растворы
1. Н-гептан по ГОСТ 25828-83.
2. Натрий сернокислый б/в по ГОСТ 4166-76.
3. Эфир диэтиловый (серный) по ГОСТ 2.2300-76.
4. Кислота серная по ГОСТ 4204-77.
5. Диметиламинобензальдегид - пара по МРТУ 6-09-684-63.
6. Бензол по ГОСТ 5955-75.
7. Этилацетат по ГОСТ 22300-76.
8. Подвижная фаза: смесь бензола и этилацетата в соотношении 95:5.
9. Проявляющий реагент - свежеприготовленный п-диметиламинобензальдегид в смеси эфира и серной кислоты 1:1.
Способ приготовления: 0,25 г п-диметиламинобензальдегида растворяют в 50 см3 смеси концентрированной серной кислоты и диэтилового эфира (1:1).
10. Стандартные растворы ДБФ и ДОФ в гептане с концентрацией 100 мкг/см3.
Ход определения
20 см3 вытяжки трижды экстрагируют н-гептаном порциями по 5 см3 на каждую экстракцию, гептановый экстракт сушат сернокислым натрием "б/в" и концентрируют до 0,2 - 0,3 см3, удаляя растворитель на водяной бане. Аналогично проводят экстракцию "холостой" пробы (модельной среды). Хроматографирование проводят по п. 7.2.1, используя пластины приготовленные по п. 7.3 п.п. 26.2.1, и ПФ-смесь бензола и этилацетата (95:5), бензола. Идентификацию и количественное определение проводят по п. 7.2.2 и 7.3.2. Для обнаружения фталатов пластинку, перед опрыскиванием проявляющим реагентом, выдерживают в сушильном шкафу при температуре 150 - 160 °C в течение 5 - 10 мин, затем обрабатывают раствором п-диметиламинобензальдегида и вновь выдерживают в течение 20 мин. при той же температуре. При наличии фталатов появляются пятна красно-бурого цвета с Rf = 0,40 +/- 0,02 для ДБФ и Rf = 0,57 +/- 0,02 для ДОФ. Предел обнаружения 0,1 мг/дм3.
Используя пластины "Силуфол" с люминесцентным индикатором (для УФ 254 нм) хроматографирование проводят в тех же условиях, а определяют фталаты облучая пластину УФ светом. Фталаты обнаруживаются в виде темных пятен на флюоресцирующем фоне. Предел обнаружения 0,1 мг/дм3
Бензойная кислота - бесцветные, блестящие, шелковистые листочки или иглы с молекулярной массой 122,12, температурой плавления 122 °C, и структурной формулой: 

Легко сублимируется при температуре выше 100 °C. Растворяется в хлороформе, четыреххлористом углероде, бензоле, ацетоне.
Необходимые реактивы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
2. Вода дистиллированная по ГОСТ 6709-72.
3. Гексан по ТУ 6-09-3375-78.
4. Кислота бензойная по ТУ 6413-77.
5. Кислота уксусная ледяная по ГОСТ 61-75.
6. Индикатор бромкрезоловый зеленый по ТУ ГКХ 1815-62.
7. Кислота серная по ГОСТ 4204-77, 0,1Н раствор.
8. Стандартный раствор бензойной кислоты в хлороформе с концентрацией 100 мкг/см3:
9. Натрий гидрофосфат по ГОСТ 4172-76.
10. Калий дегидрофосфат по ГОСТ 4198-75.
11. Буфер фосфатный с pH 6,0 - 6,2.
Способ приготовления
а) раствор N 1 - 11,866 г гидрофосфата натрия (Na2HPO4 2H2O) растворяют в 1000 см3 воды;
б) раствор N 2 - 9,073 г дегидрофосфата калия (KH2PO4) растворяют в 1000 см3 воды.
В мерную колбу вместимостью 100 см3 вносят 18,4 см3 раствора N 1 и доводят раствором N 2 до метки.
12. Подвижная фаза:
гексан:ледяная уксусная кислота (95:5).
13. Хроматографические пластинки.
Способ приготовления
0,4 г силикагеля "КСК" растирают в фарфоровой ступке с 5 см3 0,25% раствора бромкрезолового зеленого в буферном растворе с pH 6,0 - 6,2. Суспензию переносят на стеклянную пластинку, равномерно распределяют по поверхности пластинки. Пластинку помещают на горизонтальную поверхность, сушат при комнатной температуре в течение 1 часа, затем при температуре 100 °C в течение 20 - 30 минут в сушильном шкафу. Приготовленная пластинка может храниться в течение 2 дней при комнатной температуре. Перед употреблением ее необходимо выдержать 15 минут при температуре 100 °C.
Ход определения
50 см3 вытяжки подкисляют 0,1Н раствором серной кислоты до pH 2,5 (~ 0,1 см3) и экстрагируют дважды по 5 минут 10 см3 хлороформа. Экстракты переносят в фарфоровую чашку и концентрируют до объема 0,2 - 0,3 см3 при комнатной температуре. Хроматографируют по п. 7.2.2, 7.3.2. Для обнаружения бензойной кислоты пластинку после хроматографирования высушивают на воздухе до удаления запаха уксусной кислоты и затем помещают в термостат на 15 - 30 минут при температуре 100 °C. Бензойная кислота проявляется в виде желтых пятен на сине-зеленом фоне с Rf = 0,2 +/- 0,02. Предел обнаружения 0,01 мг/дм3.
В качестве вулканизующих агентов при изготовлении силиконовых резин применяются пероксиды: перекись дикумила, пероксимон Г-40. В данном разделе представлены методики определения перекиси дикумила и продукта его разложения - ацетофенона.
Краткая характеристика данных соединений представлена в табл. 7.11.
Таблица 7.11
Техническое название | Химическое название | Структурная формула | Молекулярная масса | Агрегатное состояние | Температура плавления, °C | Растворимость |
Перекись дикумила |  |  | 270,37 | Белый, светло-желтый, кристаллический порошок, плотность 1530 кг/дм3 | 39,42 | Растворима в ацетоне, спиртах, хлороформе. Не растворима в воде |
Ацетофенон | ацетилбензол |  | 120,0 | Жидкость со специфическим запахом уд. вес 1,033 | 202 (кипения) | Растворим в ацетоне, спиртах, хлороформе и других органических растворителях |
Необходимые реактивы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
1. Хлороформ по ГОСТ 20015-74.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 5955-75, а не ГОСТ 5855-75. |
2. Бензол по ГОСТ 5855-75.
3. Ксилол по ТУ 6-09-3829-74.
4. Стандартные растворы пероксида и ацетофенона в хлороформе, концентрацией 100 мкг/см3 (устойчив в течение 10 дней).
5. Ацетон по ГОСТ 2603-79.
6. Аммоний роданистый по СТ СЭВ 222-75.
7. Железо сернокислое по ГОСТ 9485-74.
8. 2,4-динитрофенилгидразин солянокислый по ТУ 09-2394.
9. Кислота соляная по ГОСТ 3118-78.
10. Подвижные фазы:
а) ксилол
б) бензол
в) бензол:ацетон (4:1)
11. Проявляющие (окрашивающие) реагенты
1. Раствор роданистого аммония в ацетоне, содержащий сульфат железа.
Способ приготовления: 10 см3 свежеприготовленного 2% раствора роданистого аммония в ацетоне смешивают перед употреблением с 0,07 г сульфата железа;
2. 2,4-динитрофенилгидразин солянокислый.
Способ приготовления: 150 мг 2,4-динитрофенилгидразина растворяют в смеси 22 см3 концентрированной соляной кислоты и 25 см3 воды. Смесь разбавляют до 100 см3 водой.
Ход определения
50 см3 вытяжки экстрагируют дважды по 5 минут, используя 20 см3 хлороформа на каждую экстракцию. Дальнейшее определение проводят по п. 7.2.1. Идентификация и количественное определение осуществляются по п.п. 7.2.2 и 7.3.2. Подвижные фазы, величины Rf, проявляющие реагенты и окраска пятен представлены в табл. 7.12. Для перекиси дикумила, после хроматографирования и высушивания пластинки на воздухе до полного удаления растворителя, пластинку помещают на 1 минуту в сушильный шкаф при температуре 135 °C, вынимают и сразу опрыскивают проявляющим реагентом. Предел обнаружения 0,01 - 0,02 мг/дм3.
Таблица 7.12
и ацетофенона методом хроматографии в тонком слое сорбента
Определяемое соединение | Сорбент | Величина Rf в подвижных фазах | Окраска пятна на хроматограмме с окрашивающим реагентом | Предел обнаружения, мг/дм3 | Примечание | |||
Ксилол | Бензол | бензол-ацетон (4:1) | Раствор роданистого аммония в ацетоне содержащий сульфат железа | 2,4-динитрофенилгидразин солянокислый | ||||
Перекись дикумила | "Силуфол" | 0,76 | 0,95 | - | красно-коричневая | - | 0,01 | |
Ацетофенон | "Силуфол" | - | - | 0,68 | - | желто-оранжевая | 0,01 | |
7.4.1. Определение 2,4-дихлорбензойной (или бензойной) кислоты в вытяжках из резин на основе силиконового каучука
В процессе вулканизации силиконовых резин из перекиси бензоила или 2,4-дихлорбензоила образуются кислоты, которые могут переходить в вытяжку из резин.
Необходимые реактивы
1. Вода дистиллированная по ГОСТ 6709-72.
2. Натрий хлористый по ГОСТ 4233-77, 0,9%-ный раствор (физиологический раствор).
3. Уранил азотнокислый по ВТУ-РУ-966-63, 1% раствор в этаноле.
4. Родамин C по ВТУ-РУ-856-53, насыщенный раствор в бензоле.
5. Кислота бензойная по ТУ 6413-77.
6. Кислота 2,4-дихлорбензойная (перекристаллизованная).
7. Стандартный раствор бензойной или 2,4-дихлорбензойной кислоты с содержанием 100 мкг/в см3.
8. Спирт этиловый по ГОСТ 18300-72.
Построение калибровочного графика
В цилиндры с притертыми пробками емкостью 0,5 см3 последовательно переносят 0,10; 0,20; 0,30 и т.д. см3 стандартного раствора кислоты, добавляют 2 - 3 капли 1% раствора азотнокислого (или уксуснокислого) уранила и объем доводят дистиллированной водой до 3,0 см3. Раствор осторожно перемешивают и добавляют 1,5 см3 насыщенного раствора родамина C в бензоле. Раствор встряхивают в течение 2 - 3 минут и оставляют стоять до расслоения фаз, после чего верхний слой осторожно переносят пипеткой в кювету с толщиной слоя 3 мм и фотометрируют со светофильтром N 6 относительно дистиллированной воды на ФЭК-56М в ультрафиолетовой области (ртутно-кварцевая лампа СВД-120А). Калибровочный график строят в координатах оптическая плотность - концентрация кислоты в растворе (мкг/см3).
Ход определения
2 см3 вытяжки переносят в цилиндр емкостью 5 см3, добавляют 2 - 3 капли 1% раствора азотнокислого (или уксуснокислого) уранила и объем доводят до 3 см3 дистиллированной водой. Раствор осторожно перемешивают и добавляют 1,5 см3 насыщенного раствора родамина C в бензоле. Раствор тщательно перемешивают (встряхивают) в течение 2 - 3 минут и оставляют до полного расслоения фаз. Верхний бензольный слой переносят в кювету с толщиной слоя 3 мм и фотометрируют на ФЭК-56М со светофильтром N 6 в ультрафиолетовой области спектра.
По калибровочному графику находят содержание 2,4-дихлорбензойной (или бензойной) кислоты и пересчитывают на весь объем вытяжки. Результаты определения выражают в мг/дм3.
Методика основана на образовании сернокислого бария в результате взаимодействия с серной кислотой.
Необходимые реактивы
1. Кислота соляная по ГОСТ 3118-77, 10% раствор.
2. Кислота серная по ГОСТ 4204-77, концентрированная.
Ход определения
50 см3 вытяжки переносят в фарфоровую чашку и выпаривают досуха на водяной или песочной бане. Сухой остаток озоляют в муфеле при температуре 550 - 600 °C (до получения золы белого или светло-кремового цвета). Охлажденную золу растворяют в 3 см3 10% раствора соляной кислоты (если раствор мутный, его фильтруют), переносят в пробирку и добавляют 1 - 2 капли концентрированной серной кислоты. Появление мути или осадка указывает на присутствие бария (сернокислого бария).
Предел обнаружения - 3 мг/л.
Метод основан на фотометрировании окрашенного комплекса бария с нитхромазо в видимой области спектра.
Необходимые реактивы и растворы
1. Вода дистиллированная по ГОСТ 6709-72.
2. Спирт этиловый по ГОСТ 18300-72.
3. Кислота соляная по ГОСТ 3118-77 - 1Н раствор.
4. Барий азотнокислый по ГОСТ 3777-76.
5. Нитхромазо по ТУ 5-096514-70, раствор 10-3 М.
Способ приготовления: 0,17 г нитхромазо растворяют в 50 см3 дистиллированной воды и раствор пропускают через колонку с ионообменной смолой КУ-2 в H+ форме.
Элюат собирают в мерную колбу, вместимостью 200 см3 и после того, как колонка будет полностью отмыта от реагента, доводят до метки дистиллированной водой.
6. Модельные растворы, имитирующие слюну - физиологический раствор (0,9%-ный раствор хлористого натрия), подкисленный и подщелоченный.
7. Стандартный раствор соли бария
Способ приготовления: точную навеску 0,0239 г азотнокислого бария растворяют в дистиллированной воде в мерной колбе вместимостью 500 см3. В 1 см3 приготовленного раствора содержится 25 мкг бария.
8. Фильтры обеззоленные синяя лента по ТУ 6-09-1678-77.
Построение калибровочного графика
В мерные колбы, вместимостью 25 см3, последовательно переносят 0,5; 1,0; 1,5 см3 и т.д. стандартного раствора бария. В каждую колбу добавляют 1 см3 нитхромазо (10-3 М), 0,5 см3 1Н раствора соляной кислоты, 10 см3 этанола или 10 см3 ацетона и доводят раствор до метки дистиллированной водой и тщательно перемешивают. Определяют оптическую плотность на спектрофотометре (СФ-16, 26, "Спекорд" и др.) относительно холостой пробы при длине волны  . Калибровочный график строят в координатах оптическая плотность - содержание бария в растворе, мкг/см3. Предел обнаружения - 0,3 мг/дм3.
. Калибровочный график строят в координатах оптическая плотность - содержание бария в растворе, мкг/см3. Предел обнаружения - 0,3 мг/дм3.
 . Калибровочный график строят в координатах оптическая плотность - содержание бария в растворе, мкг/см3. Предел обнаружения - 0,3 мг/дм3.
. Калибровочный график строят в координатах оптическая плотность - содержание бария в растворе, мкг/см3. Предел обнаружения - 0,3 мг/дм3.Ход определения <*>
--------------------------------
<*> Для обеспечения контроля испытуемой вытяжки на присутствие ионов бария по величине ДКМ, анализируемую вытяжку (100 см3) концентрируют, путем упаривания на песчаной бане до объема 2 - 3 см3 и проводят определение.
В мерную колбу вместимостью 25 см3 переносят 2 - 3 см3 фильтрованного раствора вытяжки, добавляют последовательно 1 см3 нитхромазо (10-3 М), 0,5 см3 1 Н раствора кислоты, 10 см3 этанола или ацетона, доводят раствор до метки дистиллированной водой и тщательно перемешивают. После 20-минутной выдержки раствор вновь доводят до метки дистиллированной водой, перемешивают и фотометрируют в кювете с толщиной слоя 10 мм при длине волны 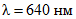 . Содержание бария находят по калибровочному графику и выражают в мг/дм3.
. Содержание бария находят по калибровочному графику и выражают в мг/дм3.
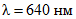 . Содержание бария находят по калибровочному графику и выражают в мг/дм3.
. Содержание бария находят по калибровочному графику и выражают в мг/дм3.--------------------------------
<*> Определяется только в вытяжках, приготовленных на дистиллированной воде.
Метод основан на фотометрировании окрашенного комплекса родаминцинката, образующегося при взаимодействии ионов цинка с родамином C или B.
Необходимые растворы и реактивы
1. Вода дистиллированная по ГОСТ 6709-72.
2. Уротропин по ГОСТ 1381-73 - 5% водный раствор.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 199-68 Постановлением Госстандарта СССР от 09.02.1978 N 415 с 1 января 1978 года введен в действие ГОСТ 199-78. |
3. Натрий уксуснокислый по ГОСТ 199-68.
4. Родамин C (или B) - 0,02% раствор.
5. Кислота уксусная ледяная по ГОСТ 61-75.
ИС МЕГАНОРМ: примечание. Постановлением Госстандарта России от 27.06.1996 N 433 с 1 января 1997 года введен в действие ГОСТ 3640-94. |
6. Цинк металлические по ГОСТ 3640-65.
7. Аммоний роданистый по ГОСТ 19582-74 - 20% раствор.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 11293-78 Постановлением Госстандарта СССР от 26.12.1989 N 4152 с 1 июля 1991 года введен в действие ГОСТ 11293-89. |
8. Желатин по ГОСТ 11293-78 - 0,5% раствор.
Способ приготовления: навеску желатина переносят в холодную дистиллированную воду, в течение 1 - 1,5 часов желатин набухает, затем раствор нагревают, чтобы растворился желатин (но не доводя до кипения).
9. Кислота соляная по ГОСТ 3118-77.
10. Ацетатный буферный раствор.
Способ приготовления: в мерную колбу вместимостью 100 см3 помещают 3 см3 концентрированной уксусной кислоты и 15 г уксуснокислого натрия, доводят до метки дистиллированной водой.
11. Стандартный раствор цинка.
Способ приготовления: растворяют 0,1 г металлического цинка в 2 см3 концентрированной соляной кислоты. Раствор осторожно переносят в мерную колбу вместимостью 1000 см3 и доводят до метки дистиллированной водой. Затем 25 см3 полученного раствора переносят в мерную колбу вместимостью 100 см3 и доводят до метки дистиллированной водой. В 1 см3 приготовленного раствора содержится 25 мкг цинка.
12. Хлоридно-аммиачный буфер (при полярографическом определении).
Способ приготовления: в мерную колбу вместимостью 200 см3 помещают 60 см3 8 - 10% раствора аммиака (полученного насыщением дистиллированной воды аммиаком в закрытом сосуде) и 20 г хлористого аммония особой чистоты. Растворы доводят до метки дистиллированной водой.
Построение калибровочного графика
В мерную колбу вместимостью 25 см3 последовательно переносят 0,5; 1,0; 1,5; 2,0 см3 и т.д. стандартного раствора цинка, добавляют последовательно 0,1 - 0,2 см3 5% раствора уротропина (нейтрализуют до pH 4,5 - 5,0), 3 см3 ацетатного буферного раствора, 1 см3 0,5% раствора желатина и 1,3 см3 20% раствора роданистого аммония. Раствор хорошо перемешивают, добавляют 2,5 см3 0,02% раствора родамина и доводят дистиллированной водой до метки (тщательно перемешивают). Через 25 минут раствор фотометрируют в кювете с толщиной слоя 50 мм и светофильтром N 9  относительно холостой пробы (смесь реагентов). Калибровочный график строят в пределах концентраций от 0,5 до 2 мкг/см3 в координатах оптическая плотность - содержание цинка в растворе мкг или мг/дм3.
относительно холостой пробы (смесь реагентов). Калибровочный график строят в пределах концентраций от 0,5 до 2 мкг/см3 в координатах оптическая плотность - содержание цинка в растворе мкг или мг/дм3.
 относительно холостой пробы (смесь реагентов). Калибровочный график строят в пределах концентраций от 0,5 до 2 мкг/см3 в координатах оптическая плотность - содержание цинка в растворе мкг или мг/дм3.
относительно холостой пробы (смесь реагентов). Калибровочный график строят в пределах концентраций от 0,5 до 2 мкг/см3 в координатах оптическая плотность - содержание цинка в растворе мкг или мг/дм3.Определение цинка в водной вытяжке
В мерную колбу вместимостью 25 см3 переносят 2 - 10 см3 вытяжки и последовательно прибавляют 0,1 - 0,2 см3 уротропина, 3 см3 ацетатного буферного раствора, 1 см3 0,5% раствора желатина и 1,3 см3 20% раствора роданистого аммония. Раствор осторожно, хорошо перемешивают, добавляют 2,5 см3 0,02% раствора родамина и доводят до метки водой. Тщательно перемешивают. Через 25 минут фотометрируют на колориметре ФЭК-56М в кювете с толщиной слоя 50 мм с красным светофильтром  относительно раствора холостой пробы. Содержание цинка в растворе определяют по калибровочному графику и пересчитывают на весь объем полученной вытяжки. Предел обнаружения - 0,25 мг/дм3.
относительно раствора холостой пробы. Содержание цинка в растворе определяют по калибровочному графику и пересчитывают на весь объем полученной вытяжки. Предел обнаружения - 0,25 мг/дм3.
 относительно раствора холостой пробы. Содержание цинка в растворе определяют по калибровочному графику и пересчитывают на весь объем полученной вытяжки. Предел обнаружения - 0,25 мг/дм3.
относительно раствора холостой пробы. Содержание цинка в растворе определяют по калибровочному графику и пересчитывают на весь объем полученной вытяжки. Предел обнаружения - 0,25 мг/дм3.Приготовление стандартного раствора цинка
Растворяют 1 г металлического цинка "хч" (без мышьяка) в 1,0 - 2,0 см3 10 н азотной кислоты. Раствор доводят до 1000 см3 в мерной колбе. 1,0 см3 приготовленного раствора содержит 0,001 г цинка.
Построение калибровочного графика
Для построения калибровочного графика в сосуд для полярографии помещают 5 см3 хлоридно-аммиачного фона и различные количества стандартного раствора цинка: 0,1; 0,3; 0,5; 0,7; 1,0; 2,0; 3,0; 4,0; 5,0 см3; 3 капли 1% раствора желатина. Объем доводят дистиллированной водой точно до 10 см3. Освобождают раствор от кислорода, продувая аргон особой чистоты через раствор в течение 5 минут. Скорость подачи газа 10 пузырьков за 7 секунд; регулируется микровинтом. Затем снимают вольтамперную кривую. Значение высоты волны в зависимости от изменения концентрации цинка наносится на систему координат, где по оси абсцисс откладывают концентрацию цинка в г на 10 см3 раствора, а по оси ординат высоту волны в мм.
Ход определения
К 5 см3 исследуемой вытяжки прибавляют 5 см3 хлоридно-аммиачного фона и 3 капли 1% раствора желатина. Раствор освобождают от кислорода, продувая аргон в течение 5 минут. Затем раствор полярографируют. Полученная вольтамперная кривая, выраженная с хорошо обозначенными верхней и нижней площадками. Содержание цинка в 1 см3 вытяжки определяют методом калибровочных кривых при чувствительности прибора 5, 2, 1. Чувствительность определения цинка составляет 10-7 г/дм3 при чувствительности 1.
Определение основано на взаимодействии сульфид-иона с ацетатом свинца.
Реактивы и аппаратура
1. Фотоэлектроколориметр 56М или другой марки.
2. Свинец уксуснокислый по ГОСТ 1027-67, 0,1% раствор.
3. Вода дистиллированная по ГОСТ 6709-72.
4. Уксусная кислота, ледяная по ГОСТ 61-75.
5. Натрия сульфид по ГОСТ 2053-77.
6. Кадмий уксуснокислый по ГОСТ 5824-79.
Растворяют 5 г ацетата кадмия в 30 см3 уксусной кислоты 96% (d = 1,06) и 65 см3 дистиллированной воды.
7. Иод по ГОСТ 4159-79, 0,01Н раствор.
8. Натрий тиосульфат по ГОСТ 244-76, 0,01Н раствор.
9. Кислота фосфорная по ГОСТ 5653-75.
Растворяют 124 см3 ортофосфорной кислоты 85% (d = 1,71) в 500 см3 дистиллированной воды.
10. Кислота соляная по ГОСТ 3118-77.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 10163-62 Постановлением Госстандарта СССР от 17.02.1976 N 420 с 1 января 1977 года введен в действие ГОСТ 10163-76. |
11. Крахмал, водорастворимый по ГОСТ 10163-62, 0,5% раствор.
12. Колбы мерные вместимостью 25, 50, 100, 1000 см3 по ГОСТ 1770-74.
Приготовление раствора ацетата свинца
1,831 г Pb(CH3COO)2·3H2O растворяют в дистиллированной воде, содержащей 1 см3 ледяной уксусной кислоты, в колбе на 1000 см3 и доводят до метки дистиллированной водой.
Приготовление стандартного раствора сульфида натрия
а) Основной раствор - 0,1 г Na2S·9H2O растворяют в 50 см3 дистиллированной воды и добавляют 50 см3 глицерина в мерной колбе на 1000 см3, а затем доводят дистиллированной водой до метки. Точное содержание сульфид-иона в этом растворе определяется иодометрическим титрованием. 200 см3 основного раствора сульфида натрия помещают в колбу с притертой пробкой, добавляют 20 - 30 см3 раствора ацетата кадмия и 50 см3 концентрированной соляной кислоты. Не менее чем через 5 часов фильтруют осадок сульфида кадмия через асбест, промывают дистиллированной водой, растворяют в избытке раствора иода (50 см3 или более) и подкисляют 20 см3 фосфорной кислоты. Через 20 минут оттитровывают избыток иода 0,01Н раствором тиосульфата натрия, используя крахмальный раствор-индикатор.
Расчет
1 см3 0,01Н иода = 0,1603 мг S-2

где: а - количество добавленного 0,01Н раствора иода, см3;
б - количество пошедшего на титрование 0,01Н раствора тиосульфата натрия, см3;
с - объем основного раствора сульфида натрия, см3.
После точного определения концентрации сульфид-иона в основном растворе, из него приготавливают рабочий раствор, с содержанием сульфид-иона 0,01 мг в 1 см3. Рабочий раствор готовят перед началом определения.
Ход определения
20 см3 испытуемого раствора (водной вытяжки) помещают в мерную колбу на 25 см3 и прибавляют 5 см3 ацетата свинца (аналогичным способом готовят холостой раствор). В присутствии сульфидов или гидросульфидов раствор темнеет по сравнению с холостым раствором. Окрашенный раствор через 10 минут фотометрируют на ФЭК-56М при светофильтре N 2 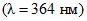 в кювете 50 мм относительно холостой пробы. Содержание сульфид-иона находят по калибровочному графику, представляющему собой зависимость величины оптической плотности от концентрации сульфид-иона.
в кювете 50 мм относительно холостой пробы. Содержание сульфид-иона находят по калибровочному графику, представляющему собой зависимость величины оптической плотности от концентрации сульфид-иона.
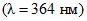 в кювете 50 мм относительно холостой пробы. Содержание сульфид-иона находят по калибровочному графику, представляющему собой зависимость величины оптической плотности от концентрации сульфид-иона.
в кювете 50 мм относительно холостой пробы. Содержание сульфид-иона находят по калибровочному графику, представляющему собой зависимость величины оптической плотности от концентрации сульфид-иона.Построение калибровочного графика
Для построения калибровочного графика готовят серию растворов с точно известным содержанием сульфид-иона (от 1 до 15 мкг в пробе). В мерные колбы на 25 см3 помещают по 20 см3 дистиллированной воды и последовательно приливают 0,1 см3, 0,3 см3, 0,5 см3, 1,0 см3, 1,5 см3 рабочего раствора с содержанием сульфид-иона 0,01 мг/см3. Затем в каждую колбу прибавляют по 5 см3 ацетата свинца, тщательно перемешивают и через 10 минут фотометрируют в кювете 50 мм со светофильтром N 2. По результатам измерений строят калибровочный график. При концентрации сульфид-иона в пределах от 1 до 15 мкг в пробе наблюдается прямая зависимость оптической плотности от концентрации. Предел обнаружения - 1 мг/дм3.
Принцип метода
Метод /6/ заключается в термостатировании 10 см3 водной, солевой или другой вытяжки из медицинской резины в стеклянной герметично закрытой емкости до установления равновесия между жидкой и газовой фазами с последующим газохроматографическим анализом паровой фазы.
Предел обнаружения при определении акрилонитрила - 0,03 мг/дм3.
Реактивы и аппаратура
1. Акрилонитрил "ч" ТУ 6-09-1168-71.
2. Стандартные растворы акрилонитрила в воде.
3. Сжатые газы: азот особой чистоты или гелий, водород, воздух.
4. Газовый хроматограф с пламенно-ионизационным детектором.
5. Шприц медицинский типа "Рекорд" емкостью 5 см3.
6. Ультратермостат.
7. Склянки <*> вместимостью 40 см3, закрывающиеся навинчивающейся крышкой, в которой просверлено отверстие для взятия пробы шприцем. Для уплотнения в крышку вставляется прокладка из инертной термостойкой резины. Снизу резиновой прокладки помещается тефлоновая пленка для предотвращения процессов сорбции-десорбции между резиновой и исследуемой пробой.
--------------------------------
<*> На практике можно использовать аптечные склянки емкостью 40 см3.
Условия термостатирования
- объем (масса) пробы | - 10 см3 (10 г) |
- температуре, °C | - 92 |
- Время, мин | - 15 |
- объем анализируемого пара, см3 | - 5 |
Условия хроматографирования
Колонка металлическая или стеклянная (3 м x 33 мм), заполненная ПЭГА (10%), нанесенным на сферохром (0,20 - 0,25 мм) <**>.
--------------------------------
<**> В НИИРе используется стеклянная колонка (2,4 м x 4 мм), заполненная карбоваксом 20М (15%), нанесенным на хроматон-N-AW-ДМСS (0,16 - 0,20 мм).
Температура | колонки | - 110 °C |
испарителя | - 200 °C | |
Скорость потока, см3/мин: | ||
газа-носителя | - 30 | |
водорода | - 30 | |
воздуха | - 300 | |
Приготовление стандартных растворов акрилонитрила в воде и построение калибровочного графика.
В мерную колбу вместимостью 25 см3 вносят 10 - 15 см3 дистиллированной воды, взвешивают с точностью до 0,0002 г. После добавления 1 - 2 капель акрилонитрила, колбу взвешивают вновь и доводят объем раствора до метки дистиллированной водой.
Для построения градуировочного графика готовят стандартные растворы с концентрацией акрилонитрила 0,03; 0,05; 0,1; 0,2; 0,3 мг/дм3.
В склянку вместимостью 40 см3 вносят 10 см3 (10 г) модельного раствора и плотно завинчивают крышкой, снабженной резиновой и тефлоновой прокладками. Склянку помещают в ультратермостат и выдерживают в течение 15 мин при 92 °C. Отбирают 5 см3 паровоздушной смеси заранее подогретым шприцем "Рекорд" (для этого в промежутках между анализами шприц кладут на ультратермостат) и хроматографируют. Перед отбором каждой последующей пробы шприц трехкратно промывают анализируемым паром внутри склянки. Отобрав пробу пара, необходимо ее сразу же ввести в испаритель хроматографа, не допуская конденсации пара на стенках шприца.
Строят график зависимости площади пика (S, мм2) от концентрации раствора (C, мг/дм3): S = f (c).
Ход определения
Отбирают пипеткой 10 см3 водной, солевой или другой вытяжки, переносят в склянку вместимостью 40 см3, плотно завинчивают крышку. Затем анализ проводят так же, как при построении калибровочного графика. Концентрацию акрилонитрила определяют по градуировочному графику.
Важнейшим условием успешного применения парофазного ГХ метода анализа является строгое соблюдение тождественности условий термостатирования, дозирования проб и всех параметров хроматографирования при калибровке и анализе вытяжек.
Принцип метода
Метод заключается в экстрагировании водной вытяжки гептаном, упаривании экстракта досуха, растворения в этиловом спирте с последующим газохроматографированием.
Реактивы и аппаратура
1. Диоктилфталат по МРТУ 6-09-851-63.
2. Дибутилфталат по ГОСТ 8728-77.
3. Хроматограф газовый с детектором ионизации в пламени.
4. Сжатые газы:
- азот по ГОСТ 9293-74;
- водород по ГОСТ 3023-80;
- воздух по ГОСТ 11882-73.
5. Микрошприц МШ-10.
6. Делительные воронки по ГОСТ 25336-82Е, вместимостью 100 см3
7. Фарфоровый тигель по ГОСТ 9147-80, вместимостью 20 - 25 см3.
8. п-гептан по ГОСТ 25828-83.
Ход анализа
25 см3 вытяжки экстрагируют 2 раза 10 см3 гептана. Объединенные экстракты упаривают досуха под тягой в фарфоровом тигле. В фарфоровый тигель с полученным сухим остатком экстракта добавляют 0,1 см3 этилового спирта, тщательно перемешивают. Микрошприцем отбирают 2 - 3 мкл раствора и хроматографируют.
Условия хроматографирования
Колонка стеклянная (0,8 м x 3 мм)
Сорбент: 5% Е-30 <*> на хроматоне N-AW-ДМСS (0,16 - 0,20 мм).
--------------------------------
<*> Возможно использование и других неподвижных фаз (карбовакс 20М, полиэтиленгликольадипинат и т.д.)
Температура колонки | - 220 °C |
Температура испарителя | - 250 °C |
Скорость потока, см3/мин: | |
газа-носителя | - 30 |
водорода | - 30 |
воздуха | - 300 |
Для количественного определения ДОФ и ДБФ используют метод внешнего стандарта. Этот метод заключается в хроматографировании 2 - 3 мкл раствора ДОФ или ДБФ с точно известной концентрацией.
Рассчитывают содержание определяемого вещества в вытяжке относительно стандарта.
Пример расчета.
Находим на хроматограмме площади пика определяемого вещества - S (мм2) и внешнего стандарта - S1 (мм2). Затем определяем количество анализируемого вещества в пробе.
 ,
,где: X - количество определяемого вещества в пробе (мг);
а - количество стандартного вещества (мг).
Затем определяем содержание вещества во всем анализируемом объеме (количество вытяжки, взятое для анализа).
 ,
,где: X - количество определяемого вещества в пробе (мг);
Vоб - 0,1 см3 спирта, взятого для растворения сухого остатка в тигле;
Vm - объем пробы, введенной в хроматограф (см3).
Затем пересчитывают содержание пластификатора на 1 дм3 вытяжки.
В этом разделе приведены методы, которые необходимо проводить в вытяжках независимо от рецептуры резины, согласно требованиям, предъявляемым к данным группам резин.
Мутность водных вытяжек определяют нефелометрическим методом, используя нефелометры марки НФМ, НФР.
Ход определения
Для приготовления прибора к работе в камеру нефелометра заливают дистиллированную воду, предварительно профильтрованную через воронку фильтрирующих с величиной пор 3 - 10 мкм (фильтр стеклянный с пористой перегородкой N 4). Мутность исследуемой вытяжки (приготовленной согласно таблице 5.1 и п. 5.2) и контрольной воды измеряют на нефелометре:
НФР - при избирательном поглотителе N 2 

НФМ - при зеленом светофильтре К-4  и рассеивателе N 4,
и рассеивателе N 4,
 и рассеивателе N 4,
и рассеивателе N 4,в цилиндрической кювете с внутренним диаметром 18 мм (подробно методика измерения изложена в описании к приборам).
По черной шкале правого измерительного барабана производят отсчет величины пропускания. Затем измеряют величину пропускания эталонной призмы мутности.
Величину мутности контрольной воды и вытяжки рассчитывают по формуле:
где: Мэ - мутность эталонной призмы, указанная в паспорте;
n - отсчет по черной шкале для исследуемой вытяжки;
nэ - отсчет по черной шкале для эталонной призмы.
7.6.2. Определение качества фармацевтических пробок, контактирующих с антибиотиком, по величине опалесценции (мутности) водных растворов антибиотика.
Методика основана на выдерживании резиновых пробок в контакте с порошком антибиотика (стрептомицина при температуре 40 °C, пенициллина - 100 °C) в течение 1 часа и последующего растворения антибиотика в дистиллированной воде для определения опалесценции раствора на нефелометре.
Допустимая величина опалесценции:
для стрептомицина - 0,0080 см-1, пенициллина - 0,0060 см-1.
Реактивы и аппаратура
1. Антибиотики (стрептомицин, пенициллин, отвечающие требованиям X Госфармакопеи СССР).
2. Вода дистиллированная по ГОСТ 6709-72.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 9775-69 Постановлением Госстандарта СССР от 15.07.1982 N 2670 с 1 января 1984 года введен в действие ГОСТ 25336-82. |
3. Воронка фильтрующая по ГОСТ 9775-69 с величиной пор 3 - 10 мкм (фильтры стеклянные с пористой перегородкой N 4).
4. Колбы конические с притертыми пробками по ГОСТ 25336-82Е, вместимостью 100 - 150 см3.
5. Нефелометр типа НФР, НФМ.
Ход определения
3 навески стрептомицина по 4,2 г каждая, взятые на аналитических весах с точностью 0,0002 г и по 12 резиновых пробок (предварительно обработанные и высушенные (см. приложение 4) помещают в три конические колбы с притертыми пробками вместимостью 100 - 150 см3. Резиновые пробки тщательно пересыпают порошком антибиотика. Колбы выдерживают в термостате при температуре 38 - 40 °C в течение 1 часа.
Затем колбы охлаждают при комнатной температуре в течение 5 минут и растворяют стрептомицин в 15 см3 дистиллированной воды, которую предварительно фильтруют через стеклянный фильтр N 4.
Приготовленный раствор (с пробками) выдерживают при комнатной температуре до полного растворения, после чего определяют опалесценцию (мутность) на нефелометре:
НФР - при избирательном поглотителе N 2  ,
,
 ,
,НФМ - при зеленом светофильтре К-4 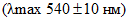 и рассеивателе N 4,
и рассеивателе N 4,
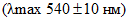 и рассеивателе N 4,
и рассеивателе N 4,в цилиндрической кювете с внутренним давлением 18 мм (подробно методика измерения изложена в описании к приборам).
По черной шкале правого измерительного барабана производят отсчет величины пропускания.
После измерения опалесценции раствора антибиотика в тех же условиях определяют величину пропускания эталонной призмы мутности (призмы светорассеяния) и величину опалесценции антибиотика без пробок.
Расчет величины опалесценции (мутности) проводят по формуле, приведенной в п. 7.6.1.
Из 3-х параллельных определений рассчитывают среднюю величину опалесценции. Одновременно определяют величину опалесценции стрептомицина (без пробок).
При использовании пенициллина берут навеску 1,75 г и 5 резиновых пробок. Колбы выдерживают в термостате при температуре 100 - 105 °C в течение 1 часа, охлаждают 15 - 20 минут, растворяют в 25 см3 дистиллированной воды. Дальнейший ход определения такой же как для стрептомицина.
7.6.3. Колориметрическое определение ионов хлора /6/
Определение основано на связывании иона хлора нитратом серебра с образованием взвешенной мути хлорида серебра в водной вытяжке.
Определению мешают другие галогены.
Предел обнаружения - 0,2 мг/дм3.
Допустимая концентрация миграции - 4 мг/дм3.
Необходимые реактивы <*>
--------------------------------
<*> Растворы готовят на дистиллированной воде, свободной от ионов хлора.
1. Стандартный раствор N 1, содержащий 100 мкг/см3 ионов хлора, готовят растворением 0,0204 г хлорида калия в 100 см3 дистиллированной воды (раствор пригоден к работе в течение 6 месяцев).
2. Стандартный раствор N 2, содержащий 10 мкг/см3 ионов хлора, готовят из стандартного раствора N 1 разведением в 10 раз дистиллированной водой. Раствор N 2 сохраняется в течение двух недель.
3. Дистиллированная вода, свободная от ионов хлора. К 5 см3 воды добавляют 0,5 см3 азотной кислоты и 1 см3 1% раствора нитрата серебра, раствор не должен давать опалесценции.
4. Азотная кислота по ГОСТ 4461-77, 10% раствор.
5. Нитрат серебра по ГОСТ 1277-75, 1% раствор. Раствор хранят в темной склянке.
6. Комплект колориметрических пробирок по ГОСТ 1770-74.
Ход определения
а) Визуальное определение ионов хлора
В колориметрическую пробирку вносят от 0,5 до 5,0 см3 водной вытяжки. Одновременно готовят стандартную шкалу с содержанием от 0 до 10 мкг иона хлора с интервалом 1 мкг, используя стандартный раствор N 2 согласно табл. 7.13.
Таблица 7.13
Реактив | Номер стандарта | ||||||||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | |
Стандартный раствор N 2, см3 | 0 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | 1,0 |
Дистиллированная вода см3 | 5,0 | 4,9 | 4,8 | 4,7 | 4,6 | 4,5 | 4,4 | 4,3 | 4,2 | 4,1 | 4,0 |
Содержание ионов Cl-, мкг | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
Во все пробирки шкалы и пробы приливают по 1 см3 раствора азотной кислоты и 1 см3 раствора нитрата серебра. После тщательного перемешивания пробирки с содержимым выдерживают в темноте. Спустя 10 мин интенсивность помутнения пробы сравнивают со стандартной шкалой на черном фоне.
Концентрация иона хлора в анализируемой вытяжке X (в мг/дм3) рассчитывается по формуле:
 ,
,где: а - количество вещества, найденное в анализируемом объеме вытяжки, мг;
V - объем жидкости, взятый для анализа (0,5 - 5) см3.
б) Количественное определение ионов хлора фотометрическим методом
В мерную колбу вместимостью 25 см3 приливают 20 см3 пробы, затем добавляют 5 капель азотной кислоты (1:1) и 0,5 см3 5% раствора азотнокислого серебра. Через 10 минут появляется характерное помутнение. Раствор переливают в кювету с толщиной слоя 20 мм и измеряют оптическую плотность при  . Содержание ионов хлора находят по калибровочному графику, для построения которого готовят стандартную шкалу в интервале 0,1 - 20 мкг/см3.
. Содержание ионов хлора находят по калибровочному графику, для построения которого готовят стандартную шкалу в интервале 0,1 - 20 мкг/см3.
 . Содержание ионов хлора находят по калибровочному графику, для построения которого готовят стандартную шкалу в интервале 0,1 - 20 мкг/см3.
. Содержание ионов хлора находят по калибровочному графику, для построения которого готовят стандартную шкалу в интервале 0,1 - 20 мкг/см3.7.6.4. Определение аммиака /6/
К 10 см3 исследуемого раствора прибавляют 0,15 см3 реактива Несслера, перемешивают и через 5 минут сравнивают с эталоном, состоящим из 10 см3 0,0002% раствора аммиака в воде и такого же количества реактива, какое добавлено к испытуемому раствору.
Наблюдение проводят в пробирках одинакового диаметра и высоты.
Интенсивность окраски, появившейся в испытуемом растворе, не должна превышать эталон.
Предел обнаружения - 0,3 мг/дм3.
Допустимая концентрация миграции - 2 мг/дм3.
К 10 см3 испытуемого раствора прибавляют 0,5 см3 8% соляной кислоты, 1 см3 5% раствора хлористого бария, перемешивают и через 10 минут сравнивают с эталоном, состоящим из 10 см3 0,001% раствора сульфат-иона и такого же количества реактивов, которое добавлено к испытуемому раствору.
Наблюдение проводят в пробирках одинакового объема и высоты.
Мутность испытуемого раствора не должна превышать мутность эталона.
Чувствительность определения 3 мг SO4-2/дм3.
Реакция основана на образовании окрашенного комплекса ионов свинца с сульфарсазеном.
Необходимые реактивы и растворы
1. Калий железистосинеродистый по ГОСТ 4207-75, 1% раствор.
2. Натрий титреборнокислый (бура) по ГОСТ 4199-76, 0,05М раствор.
3. Сульфарсазен, по ВТУ МГ УХП 546-60, 0,05% раствор в 0,05М растворе буры.
4. Дистиллированная вода по ГОСТ 6709-72.
Ход определения
100 см3 вытяжки упаривают до 1 см3, затем прибавляют 0,1 - 0,2 см3 1% раствора железистосинеродистого калия (для связывания цинка), 2 - 3 см3 раствора сульфарсазена в буре и 2 - 3 см3 раствора буры. В присутствии ионов свинца образуется оранжево-красное окрашивание.
Предел обнаружения - 0,15 мг/дм3.
Реакция основана на образовании окрашенного комплекса ионов кальция с индикатором кальционом.
Необходимые реактивы и растворы
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 2603-71 Постановлением Госстандарта СССР от 17.04.1979 N 1404 с 1 июля 1980 года введен в действие ГОСТ 2603-79. |
1. Ацетон по ГОСТ 2603-71.
2. Натр едкий по ГОСТ 11078-78, 0,5Н раствор.
3. Кальцион по МРТУ 6-09-3812-67, 0,002% раствор.
4. Вода дистиллированная по ГОСТ 6709-72.
Ход определения
100 см3 вытяжки упаривают до 1 см3, затем приливают 2 - 3 см3 дистиллированной воды, 0,8 см3 ацетона, 0,6 см3 раствора едкого натрия и 5 - 6 капель раствора кальциона, в присутствии Ca++ синий цвет переходит в розовый с малиновым оттенком.
Предел обнаружения 1 мг/дм3.
Определение мышьяка основано на способности соединений мышьяка под действием атомарного водорода восстанавливаться в мышьяковистый водород, который, соприкасаясь с бумагой, пропитанной бромной ртутью, окрашивает ее в коричневый или желтый цвет.
Необходимые реактивы
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 4232-74, а не ГОСТ 5232-74. |
1. Калий иодистый по ГОСТ 5232-74, 10% раствор.
2. Олово хлористое по ГОСТ 4780-78, 10% раствор в разбавленной (1:9) соляной кислоте.
Способ приготовления:
Хлорид олова растворяют при нагревании в концентрированной соляной кислоте, а затем разбавляют дистиллированной водой.
3. Ртуть бромная по ГОСТ 5508-50, 5% спиртовой раствор.
4. Индикаторная бумага.
Способ приготовления:
В свежеприготовленный 5% спиртовой раствор бромида ртути погружают на 30 минут кусочки фильтровальной бумаги, тонкой и плотной, диаметром 20 мм. Затем их вынимают из раствора и помещают на часовое стекло и высушивают на воздухе. Индикаторную бумагу хранят в банке из темного стекла. Срок годности 1 неделя.
5. Свинец уксуснокислый по ГОСТ 1027-67, 10% раствор.
6. Вата или бумага, пропитанная раствором ацетата свинца.
Способ приготовления:
Кусочки фильтровальной бумаги (2,5 x 4 см) или ваты выдерживают в течение 30 минут в 10% растворе ацетата свинца, затем вынимает и высушивают при температуре 105 °C.
7. Цинк металлический (не содержащий мышьяка) по ГОСТ 989-75.
8. Стандартный раствор мышьяка, 1 мг/см3 As+3.
Способ приготовления:
1,3200 г трехокиси мышьяка растворяют в 20 см3 2 Н раствора едкого натра, раствор разбавляют 20 см3 воды и подкисляют 30 см3 2 Н раствором соляной кислоты и количественно переносят в мерную колбу вместимостью 1000 дм3 и доводят дистиллированной водой до метки.
9. Кислота серная, концентрированная по ГОСТ 4204-77.
10. Прибор Гутцайта (см. рис.).
Прибор для определения мышьяка

Прибор для определения мышьяка состоит из трех разъемных частей, соединенных между собой шлифами. Нижняя часть прибора колба 1, в которую помещают исследуемый раствор, кислоту и цинк. Высота колбы 90 мм, диаметр - 60 мм. Колба закрывается стеклянной пришлифованной пробкой - 2 (куда помещают вату - 5, пропитанную раствором ацетата свинца), которая переходит в трубку 3 с внутренним диаметром 1,5 мм и высотой 60 мм. Трубка посередине разрезана, края ее в этом месте разбортованы и притерты. Между этими шлифами зажимается индикаторная бумага - 4. Верхний конец трубки по притертой пробке 7 укрепляется в стеклянном кожухе - 6.
Ход определения
Построение стандартной шкалы
Приготавливают серию стандартных растворов, которые в 25 см3 дистиллированной воды содержат от 0,5 - 5 мкг мышьяка. В склянку прибора переносят 25 см3 раствора известной концентрации мышьяка, прибавляют 5 - 6 капель хлорида олова, 3 - 3,2 см3 концентрированной серной кислоты, 5 см3 раствора иодида калия, 1 - 2 гранулы цинка и тотчас же закрывают склянку насадкой, в которой закреплен кружок фильтровальной бумаги, пропитанной раствором бромной ртути, а в шлифе пробирки 2 помещают кусочки ваты, 5, пропитанной ацетатом свинца. По окончании выделения водорода (45 мин) извлекают кружок бумаги с образовавшимся окрашенным пятном. Серия стандартных растворов должна включать 5 известных концентраций. Нулевой стандарт представляет холостой опыт. Кружочки бумаги с образовавшимися окрашенными пятнами целесообразно запарафинить для дальнейшего сравнения с исследуемыми растворами для количественного определения мышьяка. Срок хранения стандартов 1 месяц.
Ход определения
25 см3 исследуемой пробы переносят в склянку прибора и проводят определение как описано при построении стандартной шкалы. Содержание мышьяка находят путем сравнения интенсивности окраски пятна исследуемого раствора с пятнами стандартной шкалы и пересчитывают на весь объем вытяжки.
Предел обнаружения мышьяка - 0,008 мг/дм3.
Условия приготовления газовоздушной среды для исследования резиновых изделий, применяемых в медицинской практике осуществляют согласно таблице 5.1.
Анализируемый образец закладывается в эксикатор и выдерживается при соответствующих условиях. По истечении указанного срока воздух в эксикаторе подвергают химическому анализу. На каждое определение индивидуального соединения необходимо брать новый образец резины. В воздухе, контактировавшем с изделием, определяют: мономеры (в соответствии с используемым каучуком), сероводород, сероуглерод, амины, формальдегид, фенолы и др.
Необходимые приборы
1. Хроматограф газовый с детектором ионизации в пламени (типа ЛХМ-80 и др. марок).
2. Электроаспиратор М-822, ЭА-30 и др.
3. Поглотительные сосуды Полежаева, Зайцева и др. по ГОСТ 25336-82Е.
4. Микрошприц МШ-10.
5. Лупа измерительная с ценой деления 0,1 мм.
7.7.1.1. Определение акрилонитрила /21/
Акрилонитрил (нитрил акриловой кислоты) - бесцветная жидкость с молекулярной массой 53,06, температурой кипения 78 - 79 °C, структурной формулой CH2 = CH - CN, растворим в воде, хорошо растворим в спирте, эфире.
Необходимые реактивы
1. Диметилформамид по ГОСТ 20289-74.
2. Акрилонитрил (перегнанный).
3. Стандартный раствор акрилонитрила в диметилформамиде с концентрацией 100 мкг/см3.
4. Сжатые газы:
ИС МЕГАНОРМ: примечание. Здесь и далее в официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 9293-74, а не ГОСТ 9393-74. |
- азот по ГОСТ 9393-74
- водород по ГОСТ 3022-80
- воздух по ГОСТ 11882-73.
5. Носитель - хроматон N-AW-ДМСS, зернение 0,2 - 0,25 мм.
6. Неподвижная фаза - карбовакс - 1500.
Отбор проб
3 дм3 воздуха аспирируют со скоростью 0,1 дм3/мин через два поглотительных сосуда Полежаева, содержащих по 1 см3 диметилформамида, при охлаждении льдом.
Ход анализа
Для анализа из каждого поглотительного сосуда берут по 5 мкл пробы и вводят в хроматограф через мембрану испарителя.
Условия хроматографирования
Колонка стальная (3,0 м x 3 мм).
Сорбент: 15% карбовакс-1500 на хроматоне N-AW-ДМСS (0,2 - 0,25 мм).
Температура испарения | - 200 °C |
Температура колонки | - 110 °C |
Скорость потока, см3/мин: | |
газ-носитель | - 30 |
водород | - 30 |
воздух | - 250 |
Скорость движения диаграммной ленты - 600 мм/ч.
Количественное определение акрилонитрила проводят методом абсолютной калибровки путем измерения площади пика.
Для калибровки готовят рабочие стандартные растворы с концентрацией от 1 до 100 мкг/см3 и хроматографируют в тех же условиях, что и пробы. По полученным данным строят градуировочный график в координатах: площадь пика (см2) - концентрация (мкг/см3), рассчитывают по формуле:
 ,
,где: C - концентрация вещества, найденная по графику, мкг/см3;
V - общий объем пробы, см3;
V20 - объем отобранного воздуха, приведенный к стандартным условиям, дм3.
Общее количество находят как сумму определенного акрилонитрила в двух поглотительных сосудах.
Предел обнаружения - 3,5·10-9 г/см3.
Изопрен (2-метил-1,3-бутадиен) - бесцветная жидкость с молекулярной массой 68,12 и температурой кипения 34,067 °C, структурной формулой 

не растворим в воде, хорошо растворим в спирте, эфире.
Необходимые реактивы
1. Спирт этиловый по ГОСТ 18300-72.
2. Изопрен
3. Стандартный раствор изопрена в этиловом спирте с концентрацией 100 мкг/см3.
4. Сжатые газы:
- азот по ГОСТ 9393-74
- водород по ГОСТ 3022-80
- воздух по ГОСТ 11882-73.
5. Носитель - хроматон N-AW-ДМСS, зернение 0,25 - 0,31 мм.
6. Неподвижная фаза - полиэтиленгликольадипинат.
Отбор проб
5 дм3 воздуха аспирируют со скоростью 0,5 дм3/мин через два поглотительных сосуда, содержащих по 2 см3 этилового спирта, при охлаждении льдом.
Ход анализа
Для анализа из каждого поглотительного сосуда берут по 5 мкл пробы и вводят в хроматограф через мембрану испарителя.
Условия хроматографирования
Колонка стеклянная (0,8 м x 5 мм).
Сорбент: 15% полиэтиленгликольадипинат, нанесенный на хроматоне N-AW-ДМСS (0,25 - 0,31 мм).
Температура колонки - 60 °C
Температура испарителя - 90 °C
Скорость потока, см3/мин:
газ-носитель (азот) | - 30 |
водород | - 30 |
воздух | - 300 |
Скорость движения диаграммной ленты 600 мм/ч.
Количественное определение изопрена проводят методом абсолютной калибровки путем измерения площади пика.
Для калибровки готовят рабочие стандартные растворы с концентрацией от 1 до 100 мкг/см3 и хроматографируют в тех же условиях, что и пробы. По полученным данным строят градуировочный график в координатах: площадь пика (см2) - концентрация (мкг/см3).
Содержание изопрена рассчитывают по формуле:

где: C - концентрация вещества, найденная по графику, мкг/см3;
V - общий объем пробы, см3;
V20 - объем отобранного воздуха, приведенный к стандартным условиям, дм3.
Общее количество находят как сумму определенного изопрена в двух поглотительных сосудах.
Предел обнаружения - 4·10-8 г/см3.
Необходимые приборы и посуда
1. Фотоэлектроколориметр ФЭК-56М или другого типа.
2. Электроаспираторы М-822, ЭА-30 и др.
3. Поглотительные приборы (малые) со стеклянной пористой пластинкой N 1, типа Зайцева и др.
4. Пробирки обычные вместимостью 5 и 10 см3 по ГОСТ 25336-82Е.
5. Пипетки вместимостью 1, 2, 3, 5, 10 см3 с ценой деления 0,01 см3, по ГОСТ 20292-74.
6. Колбы измерительные, вместимостью 25, 50, 100, 500 и 1000 см3 по ГОСТ 1770-74.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 10394-72 Постановлением Госстандарта СССР от 15.07.1982 N 2670 с 1 января 1984 года введен в действие ГОСТ 25336-82. |
7. Колбы конические Эрленмейра, вместимостью 100 - 200 см3 по ГОСТ 10394-72.
8. Пробирки колориметрические, вместимостью 5, 10, 15 см3, по ГОСТ 1770-74.
Определение сероводорода основано на реакции его с нитратом серебра.
Предел обнаружения - 1,0 мг/м3.
Предельно допустимая концентрация - 10,0 мг/м3.
Необходимые реактивы и растворы
1. Нитрат серебра по ГОСТ 1277-75, 0,05%-ный раствор в 10%-ной серной кислоте.
2. Кислота серная по ГОСТ 4204-77, 10% раствор (по объему).
3. Крахмал по ГОСТ 10163-76, 0,5% раствор.
4. Тиосульфат натрия по ГОСТ 244-76, 0,1Н раствор.
5. Стандартный раствор тиосульфата натрия.
Способ приготовления:
В мерную колбу вместимостью 1000 см3 вносят 3 см3 0,1Н тиосульфата натрия и доводят объем дистиллированной водой до метки, 1 см3 раствора соответствует 0,01 мг сероводорода.
Описание определения
1. Отбор проб
Исследуемый воздух протягивают со скоростью 25 см3/мин. через два поглотительных раствора, заполненные 2 см3 раствора нитрата серебра в серной кислоте с одной каплей раствора крахмала.
2. Построение калибровочного графика
В колориметрические пробирки вместимостью 5 см3 готовят стандартную шкалу согласно табл. 7.14.
Таблица 7.14
Реактив | Норма стандартов | |||||||||
0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | |
Стандартный раствор см3 | 0 | 0,05 | 0,10 | 0,20 | 0,30 | 0,40 | 0,50 | 0,60 | 0,70 | 0,80 |
Раствор крахмала | По одной капле в каждую пробирку | |||||||||
Поглотительный раствор, см3 | 2,00 | 1,95 | 1,90 | 1,80 | 1,70 | 1,60 | 1,50 | 1,40 | 1,30 | 1,20 |
Содержание сероводорода, мкг | 0 | 0,5 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Содержимое пробирки перемешивают и колориметрируют при длине волны  в кювете с толщиной слоя 3 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероводородов.
в кювете с толщиной слоя 3 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероводородов.
 в кювете с толщиной слоя 3 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероводородов.
в кювете с толщиной слоя 3 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероводородов.3. Ход определения
Испытуемую пробу переносят в кювете с толщиной слоя 3 мм и колориметрируют при длине волны 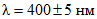 . Затем рассчитывают содержание сероводорода в воздухе (в мг/м3) по формуле:
. Затем рассчитывают содержание сероводорода в воздухе (в мг/м3) по формуле:
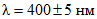 . Затем рассчитывают содержание сероводорода в воздухе (в мг/м3) по формуле:
. Затем рассчитывают содержание сероводорода в воздухе (в мг/м3) по формуле: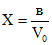 ,
,где: в - количество вещества, найденное во всем объеме исследуемого раствора, мкг;
V0 - объем исследуемого воздуха, приведенный к нормальным условиям, дм3.
Метод основан на взаимодействии сероуглерода с диэтиламином и ацетоном меди с образованием дитиокарбамата меди, окрашивающего раствор в желто-бурый цвет. Содержание сероуглерода определяется колориметрически по калибровочному графику.
Предел обнаружения 0,5 мг/м3.
Предельно допустимая концентрация - 1 мг/м3.
Необходимые реактивы и растворы
1. Медь уксуснокислая по ГОСТ 5852-79, 0,05% раствор в этиловом спирте, свежеприготовленный.
2. Сероуглерод, перегнанный, по ГОСТ 19213-73.
3. Диэтиламин по ГОСТ 9875-73, 1,5% раствор в этиловом спирте, свежеприготовленный.
4. Этиловый спирт по ГОСТ 18300-72.
5. Стандартный раствор сероуглерода.
Способ приготовления:
В мерную колбу вместимостью 25 см3 наливают 20 см3 раствора диэтиламина. Колбу закрывают пробкой и взвешивают на аналитических весах. Затем прибавляют 1 - 2 капли сероуглерода и вторично взвешивают. Содержимое колбы доводят раствором диэтиламина до метки, закрывают пробкой, хорошо перемешивают и рассчитывают содержание сероуглерода в 1 см3 раствора. Соответствующим разбавлением раствором диэтиламина получают стандартный раствор с содержанием сероуглерода 0,01 мг/см3.
Ход определения
1. Отбор проб
2 - 3 дм3 исследуемого воздуха со скоростью 30 дм3/ч протягивают через два последовательно соединенных поглотительных прибора, содержащих по 10 см3 раствора диэтиламина и помещенных в сосуд с охлаждающей смесью (лед + соль).
2. Построение калибровочного графика
В колориметрических пробирках вместимостью 5 см3 приготавливают стандартную шкалу согласно табл. 7.15.
Таблица 7.15
Реактивы | Номера стандартов | ||||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | |
Стандартный раствор сероуглерода, см3 | 0 | 0,1 | 0,3 | 0,5 | 0,7 | 1,0 | 1,5 |
Раствор диэтиламина | 5,0 | 4,9 | 4,7 | 4,5 | 4,3 | 4,0 | 3,5 |
Раствор ацетата меди | Во все пробирки по 0,5 см3 | ||||||
Содержание сероуглерода, мг | 0 | 0,001 | 0,003 | 0,005 | 0,007 | 0,01 | 0,015 |
Содержимое пробирок встряхивают и через 5 минут колориметрируют при длине волны  в кювете с толщиной слоя 10,0 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероуглерода.
в кювете с толщиной слоя 10,0 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероуглерода.
 в кювете с толщиной слоя 10,0 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероуглерода.
в кювете с толщиной слоя 10,0 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация сероуглерода.Ход определения
Содержимое поглотительных приборов анализируют отдельно. 1 и 5 см3 исследуемого раствора из первого поглотительного прибора и 5 см3 из второго прибора переносят в колориметрические пробирки. Недостающий объем доводят поглотительным раствором до 5 см3, затем прибавляют по 0,5 см3 раствора ацетата меди. Содержимое пробирки встряхивают и через 5 минут колориметрируют при длине волны  в кювете с толщиной слоя 10,0 мм относительно холостой пробы. Затем рассчитывают содержание сероуглерода в воздухе (в мг/м3) по формуле:
в кювете с толщиной слоя 10,0 мм относительно холостой пробы. Затем рассчитывают содержание сероуглерода в воздухе (в мг/м3) по формуле:
 в кювете с толщиной слоя 10,0 мм относительно холостой пробы. Затем рассчитывают содержание сероуглерода в воздухе (в мг/м3) по формуле:
в кювете с толщиной слоя 10,0 мм относительно холостой пробы. Затем рассчитывают содержание сероуглерода в воздухе (в мг/м3) по формуле: ,
,где: а - общий объем поглотительного раствора, см3;
в - количество сероуглерода, найденное в анализируемом объеме пробы, мг;
с - объем поглотительного раствора, взятый для определения, см3;
V0 - объем исследуемого воздуха, приведенный к нормальным условиям, дм3.
При наличии сероуглерода во втором поглотителе результаты суммируются.
Метод позволяет определить суммарное содержание аминов. Амины определяются по реакции с 2,4-динитрохлорбензолом. Предел обнаружения 0,7 мг/м3.
Необходимые реактивы и растворы
1. 2,4-динитрохлорбензол, ТУ 6-09-2983-73, 5% спиртовой раствор.
2. Карбонат натрия по ГОСТ 83-79, 8% раствор.
3. Кислота соляная, по ГОСТ 3118-77, 5% раствор.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 20015-74 Постановлением Госстандарта СССР от 22.12.1988 N 4454 с 1 января 1991 года введен в действие ГОСТ 20015-88. |
4. Хлороформ, по ГОСТ 20015-74.
5. Стандартный раствор
Способ приготовления:
В мерную колбу вместимостью 50 см3 помещают 0,05 г амина (диэтиламина) и доводят водой до метки. Путем разбавления водой готовят стандартные растворы (содержание амина 0,1 и 0,01 мг/см3).
Описание определения
1. Отбор проб
15 дм3 исследуемого воздуха со скоростью 0,5 дм3/мин протягивают через поглотительный прибор, содержащий 3 см3 воды.
2. Построение калибровочного графика
В колориметрические пробирки вместимостью 5 см3 переносят раствор, содержащий определенное количество амина и проводят определение согласно приведенной в табл. 7.16 стандартной шкале для определения аминов.
Таблица 7.16
Реактивы | Номера стандартов | |||||||
0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | |
Стандартный раствор, содержание амина 0,01 мг/см3 см3 | 0 | 0,25 | 0,5 | - | - | - | - | - |
Стандартный раствор, содержание амина 0,1 мг/см3, см3 | - | - | - | 0,1 | 0,2 | 0,4 | 0,6 | 0,8 |
Вода, см3 | 1,0 | 0,75 | 0,5 | 0,9 | 0,8 | 0,6 | 0,4 | 0,2 |
Раствор карбоната натрия | Во все пробирки по 0,1 см3 | |||||||
Динитрохлорбензол | Во все пробирки по 0,2 см3 После 5-минутного нагревания и охлаждения | |||||||
Раствор соляной кислоты | Во все пробирки по 0,5 см3 | |||||||
Хлороформ | Во все пробирки по 1,0 см3 | |||||||
Содержание амина, мкг | 0 | 0,0025 | 0,005 | 0,01 | 0,02 | 0,04 | 0,06 | 0,08 |
В присутствии амина в нижнем хлороформенном слое сразу появляется желтая окраска, которую колориметрируют в кювете с толщиной слоя 1,0 мм при длине волны  . По полученной оптической плотности хлороформенного раствора и концентрации амина строят график.
. По полученной оптической плотности хлороформенного раствора и концентрации амина строят график.
 . По полученной оптической плотности хлороформенного раствора и концентрации амина строят график.
. По полученной оптической плотности хлороформенного раствора и концентрации амина строят график.Ход определения
Содержимое поглотительного прибора переносят в пробирки, прибор промывают 2 раза по 1 см3 водой и доводят водой раствор в пробирке до 5 см3.
Для анализа отбирают по 1 см3, в колориметрические пробирки добавляют по 1 см3 раствора карбоната натрия и по 0,2 см3 раствора динитрохлорбензола. Пробирки помещают на 5 минут в кипящую водяную баню и после охлаждения в них добавляют по 0,5 см3 соляной кислоты, затем по 1 см3 хлороформа и энергично взбалтывают.
Хлороформенный слой колориметрируют в кювете с толщиной слоя 1,0 мм при длине волны 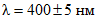 .
.
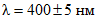 .
.Концентрацию амина в воздухе (X) в мг/м3 вычисляют по формуле:
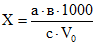 ,
,где: а - общий объем вытяжки, см3;
в - количество амина, найденное в анализируемом объеме пробы, мг;
с - объем вытяжки, взятой для определения, см3;
V0 - объем исследуемого воздуха, приведенный к нормальным условиям, дм3.
Формальдегид реагирует в кислой среде с хромотроповой кислотой, образуя соединение, окрашивающее раствор в фиолетовый цвет.
Чувствительность метода 0,3 мг/м3.
Предельно допустимая концентрация - 0,5 мг/м3.
Необходимые реактивы и растворы
1. Серная кислота по ГОСТ 4204-77, d = 1,83 и разбавленная (1:3).
2. Натр едкий, по ГОСТ 4328-77, 20% раствор.
3. Иод, по ГОСТ 4159-79, 0,1Н раствор.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 244-76, а не ГОСТ 255-76. |
4. Тиосульфат натрия, по ГОСТ 255-76, 0,1Н раствор.
5. Крахмал водорастворимый, по ГОСТ 10163-76, 0,5% раствор.
6. Хромотроповая кислота, по ТУ 6-09-3749-74 или ее динатриевая соль, 1% раствор.
7. Стандартный раствор формальдегида.
Готовят 1% раствор и количество формальдегида определяют титрометрически. В колбу вместимостью 200 см3 вводят 1 см3 1%-ного формалина, приливают 10 см3 воды и добавляют из бюретки 10 см3 раствора иода. Затем по каплям прибавляют раствор едкого натрия до получения светло-желтого окрашивания. Оставляют на 10 мин, затем добавляют 2 см3 10% раствора соляной кислоты до полного выделения иода, опять оставляют на 10 мин и оттитровывают раствор тиосульфатом натрия с крахмалом в качестве индикатора. В таких же условиях оттитровывается и контрольный раствор. Разность между объемами раствора тиосульфата, пошедшего на контрольное титрование и на титрование раствора формалина, позволяет вычислить количество иода, пошедшее на окисление формальдегида. 1 см3 0,1Н раствора иода соответствует 1,5 мг формальдегида. Определив количество формальдегида в растворе, соответствующим разбавлением готовят стандартный раствор, содержащий формальдегида 2 мг/см3, а из него готовят раствор, содержащий 0,01 мг/см3.
Ход определения
1. Отбор проб
5 дм3 исследуемого воздуха со скоростью 20 дм3/мин протягивают через два поглотительных прибора, содержащих по 5 см3 воды.
2. Построение калибровочного графика
В колориметрических пробирках вместимостью 5 см3 приготавливают стандартную шкалу, согласно табл. 7.17.
Таблица 7.17
Реактивы | Номера стандартов | ||||||
0 | 1 | 2 | 3 | 4 | 5 | 6 | |
Стандартный раствор, содержащий формальдегида 0,01 мг/см3, см3 | 0 | 0,05 | 0,1 | 0,15 | 0,25 | 0,35 | 0,45 |
Вода, см3 | 2,7 | 2,65 | 2,60 | 2,55 | 2,45 | 2,35 | 2,25 |
Хромотроповая кислота | Во все пробирки по 0,4 см3 | ||||||
Серная кислота d = 1,83 | Во все пробирки по 1,9 см3 | ||||||
Содержание формальдегида, мг | 0 | 0,0005 | 0,001 | 0,0015 | 0,0025 | 0,0035 | 0,0045 |
Содержимое пробирок встряхивают, закрывают пробками и помещают на 30 мин в кипящую водяную баню. По охлаждении через 40 - 50 минут интенсивность фиолетовой окраски колориметрируют в кюветах с толщиной слоя 10 мм, при длине волны  . Калибровочный график строят в координатах оптическая плотность - концентрация формальдегида.
. Калибровочный график строят в координатах оптическая плотность - концентрация формальдегида.
 . Калибровочный график строят в координатах оптическая плотность - концентрация формальдегида.
. Калибровочный график строят в координатах оптическая плотность - концентрация формальдегида.Ход определения
В колориметрическую пробирку вносят 3,0 см3 исследуемого раствора, добавляют 0,4 см3 хромотроповой кислоты и 1,9 см3 серной кислоты (d = 1,83). Пробирку закрывают пробкой и помещают на 30 мин в кипящую водяную баню, через 40 - 50 мин после охлаждения колориметрируют в кюветах с толщиной слоя 10 мм при длине волны  .
.
 .
.Содержание формальдегида в воздухе в мг/м3 вычисляют по формуле:
 ,
,где: а - общий объем вытяжки, см3;
в - количество формальдегида, найденное в анализируемом объеме пробы, мг;
с - объем вытяжки, взятой для определения, см3;
V0 - объем исследуемого воздуха, приведенный к нормальным условиям, дм3.
Метод позволяет определять суммарное содержание фенолов. Фенолы определяются по реакции с 4-аминоантипирином в щелочной среде в присутствии феррицианида калия, являющегося окислителем. При этом образуются соединения типа индофенола, окрашенные в интенсивно красный цвет.
Предел обнаружения - 0,1 мг/дм3.
Необходимые реактивы и растворы
1. 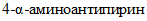 ,
,
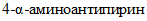 ,
,2% водный раствор.
2. Феррицианид калия по ГОСТ 6816-79E, 8% водный раствор.
3. Аммоний хлористый по ГОСТ 2210-73.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: стандарт имеет номер ГОСТ 3760-79, а не ГОСТ 3.7.60-79. |
4. Аммиак концентрированный по ГОСТ 3.7.60-79.
5. Кислота серная по ГОСТ 2184-77, разбавленный раствор (1:3 по объему).
6. Буферный раствор с pH = 9,8.
Способ приготовления:
20 г хлорида аммония растворяют в 100 см3 концентрированного раствора аммиака.
7. Натр едкий по ГОСТ 4328-77, 10% раствор.
8. Стандартный раствор фенола.
В мерную колбу вместимостью 50 см3 наливают 10 - 15 см3 дистиллированной воды, взвешивают на аналитических весах, затем помещают в нее кристаллик свежеперегнанного фенола, взвешивают вторично и доводят объем водой до метки. Рассчитывают содержание фенола в 1 см3 раствора. Из полученного основного раствора соответствующим разведением готовят непосредственно перед его использованием раствор, содержащий 5 мкг/см3 фенола.
Описание определения
1. Отбор проб
10 дм3 исследуемого воздуха пропускают со скоростью 0,5 дм3/мин, через поглотительный прибор, содержащий 5 см3 дистиллированной воды.
2. Построение калибровочного графика
В колориметрическую пробирках вместимостью 5 см3 приготавливают стандартную шкалу согласно табл. 7.18.
Таблица 7.18
Реактивы | Номера стандартов | |||||||
0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | |
Стандартный раствор фенола, см3 | 0 | 0,25 | 0,5 | 0,75 | 1,0 | 1,25 | 1,5 | 1,75 |
Дистиллированная вода, см3 | 5,0 | 4,75 | 4,5 | 4,25 | 4,0 | 3,75 | 3,5 | 3,25 |
Буферный раствор | Во все пробирки по 0,5 см3 | |||||||
Раствор феррицианида калия | Во все пробирки по 0,2 см3 | |||||||
Раствор 4-аминоантипирина | Во все пробирки по 0,2 см3 | |||||||
Содержание фенола, мкг | 0 | 1,25 | 2,5 | 3,75 | 5,0 | 6,25 | 7,5 | 8,75 |
Пробирки с раствором тщательно перемешивают после добавления каждого реактива и колориметрируют при длине волны 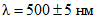 в кювете с толщиной слоя 10 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация фенола.
в кювете с толщиной слоя 10 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация фенола.
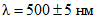 в кювете с толщиной слоя 10 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация фенола.
в кювете с толщиной слоя 10 мм относительно холостого опыта. Калибровочный график строят в координатах оптическая плотность - концентрация фенола.Ход определения
Пробу переносят в пробирку и нейтрализуют по индикаторной бумаге растворами едкого натра или серной кислоты затем добавляют 0,5 см3 буферного раствора, 0,2 см3 раствора феррицианида калия и 0,2 см3 раствора 4-аминоантипирина. Пробирки с раствором тщательно перемешивают и колориметрируют в кюветах с толщиной слоя 10 мм при длине 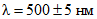 .
.
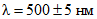 .
.Содержание фенола в воздухе в мг/м3 вычисляют по формуле:
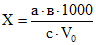 ,
,где: а - общий объем вытяжки, см3;
в - количество фенола, найденное в анализируемом объеме пробы, мг;
с - объем вытяжки, взятый для определения, см3;
V0 - объем исследуемого воздуха, приведенный к нормальным условиям, дм3.
Биологические исследования не проводятся, если резина не может быть разрешена на основании органолептических и санитарно-химических исследований.
Необходимость исследования биологической активности резин возникает при:
1. Разработке новых видов материалов по вновь разработанной рецептуре.
2. Введении новых ингредиентов в ранее разрешенные резиновые смеси.
3. Изменении технологии изготовления материала или изделия из него.
Методы биологических исследований обусловлены принадлежностью резин или изделий из них к определенной группе классификации, приведенных в приложении 7.
К изделиям этой группы предъявляются следующие требования: не вызывать изменения тканей, прилегающих к протезам, общего биологического действия и отдаленных последствий длительного контакта протезов с организмом.
Исследование протезов осуществляется в два этапа: при введении вытяжки в брюшную полость и при имплантации образцов изделий.
Опыты проводят на 40 белых крысах с массой тела 180 - 200 г и 30 белых мышах с массой тела 18 - 22 г. Испытуемую вытяжку вводят внутрибрюшинно поочередно в правую и левую паховые области через день, всего 25 введений в дозе 10 мл/кг.
Параллельно контрольным животным того же пола и массы тела вводят раствор, используемый в качестве экстрагента (0,9% физиологический раствор или дистиллированная вода) в той же дозе, что и вытяжки из резиновых изделий.
Наблюдение за животными проводят в динамике на протяжении эксперимента (после 5, 15, 25 введений) и спустя месяц по его окончании.
Выбор показателей интоксикации в каждом конкретном случае определяется составом резиновой смеси и результатами санитарно-химических анализов вытяжки из резинового изделия. Обязательными является определение массы тела, массовых коэффициентов внутренних органов, состояния нервной системы, функции печени и почек, состава периферической крови, активности ряда специфических ферментов, состояния надпочечников (см. приложение 8).
Оценка результатов исследований вытяжки осуществляется по количественным критериям вредности, приведенным в разделе 8.7.
Масса имплантируемого образца протеза в экспериментах вычисляется, исходя из массы протеза для человека (в мг/кг), допуская не более 10-кратной аггравации. Опыт проводят на беспородных крысах-самцах или самках с исходной массой тела 200 - 250 г. Количество животных в группе должно быть не менее 50 на один образец. Контролем служат аналогичные по массе и форме образцы заведомо биологически инертного тефлона. Перед операцией все образцы стерилизуются согласно технологическому регламенту.
В брюшную полость имплантаты вводят через разрез кожи и мышц живота под общим нембуталовым наркозом. Операционная полость перед наложением внутренних и внешних швов обрабатывается антибиотиками.
Подкожно образцы имплантируются двумя способами (п/к).
а) При введении материалов, предназначенных для протезов твердых тканей, вырезаются узкие полоски шириной не более 1 мм и длиной 15 мм. Количество вводимых полос зависит от массы протеза (от 2 до 4 шт на 1 животное). Каждая пластинка вставляется в просвет широкой иглы, которая надевается на шприц с 3 мл 2% раствора новокаина. Игла вводится под кожу животного, и полоска силикона выталкивается раствором новокаина резким движением поршня шприца.
б) Второй способ имплантации под кожу используется при испытании объемных образцов, чаще округлой формы, характерной для протезов мягких тканей (например, молочной железы). В этом случае имплантаты материала вводятся через надрез кожи в подкожный или внутримышечный карман с последующим наложением швов. Процедура проводится под общим эфирным ингаляционным наркозом.
С целью выявления общетоксического эффекта животные с имплантатами обследуются на протяжении хронического эксперимента через 1, 3, 6, 9, 12 и 18 месяцев после операции. Оценка физиологического состояния животных проводится с использованием тестов, приведенных в приложении 8.
По окончании опыта животных забивают. При вскрытии проводят визуальное исследование внутренних органов и их морфологическое исследование с целью выявления патологических органных изменений.
Оценка результатов общего токсикологического действия протезов проводится по обобщенному показателю, суммирующему число статистически достоверных отклонений показателей состояния организма подопытных животных по сравнению с контрольными (см. раздел 8.7).
Местная реакция тканей, непосредственно прилегающих к имплантатам, изучается в динамике: через 14, 21 день, 6, 12, 18 месяцев после операции. Для морфологических исследований берется кожа с подкожной клетчаткой вместе с образцом силикона, фиксируется в формалине, заливается в парафин. Перед проводкой образец извлекается из тканей. Срезы толщиной 5 - 7 микрон окрашиваются гематоксилин-эозином и пикрофуксином по Ван-Гизон.
Регистрируется в течение процессов капсулообразования: ширина капсулы, качественный состав клеток (наличие зрелых или молодых фибробластов, присутствие макрофагов, эозинофилов, плазматических клеток, лимфоидных инфильтратов). Ткани, окружающие капсулу, исследуются с целью выявления воспалительных, сосудистых, аллергических опухолевых процессов.
Оценка местной реакции тканей, окружающих имплантаты, сравнивается с реакцией тканей на имплантацию инертного материала (тефлона). В случае удовлетворительных результатов зрелая капсула вокруг имплантата не должна значительно отличаться от капсулы, сформированной вокруг биологически инертного тефлона, т.е. должна быть тонкой, состоять из плотно прилегающих друг к другу зрелых концентрических пучков коллагеновых волокон, содержать очень небольшое количество клетчатых элементов (фиброцитов, единичных лимфоцитов). В околокапсульном пространстве не должно быть выраженных воспалительных сосудистых, аллергических проявлений признаков предопухолевой пролиферации. При имплантации инертного материала полное формирование капсулы и затухание воспалительных реакций происходит к 6-месячному сроку пребывания имплантата в организме.
Изучение и оценка отдаленных последствий длительного контакта протезов с организмом (гонадотропное, мутагенное действие) осуществляется в соответствии с методическими рекомендациями: "Методы экспериментального исследования по установлению порогового действия промышленных ядов на генеративную функцию с целью гигиенического нормирования" М., 1978, утверждено зам. главного санитарного врача СССР N 1744-77 от 10.07.77.
При изучении и оценке бластомогенного эффекта используются "Методические рекомендации по исследованию канцерогенных свойств химических веществ и биологических продуктов в хронических опытах на животных" М - Л., 1981, утверждено МЗ СССР N 2453-81 от 09.10.81.
Основным требованием, предъявляемым к изделиям этой группы, является отсутствие загрязнений контактирующих сред токсическими примесями в количествах, оказывающих вредное действие на организм.
В токсикологическом эксперименте используются вытяжки, приготовленные в соответствии с табл. 5.1. Оценка токсичности вытяжек осуществляется на животных по схеме, приведенной в приложениях 1, 2, раздел 8.7 для резин группы II. Исследования включают введение вытяжки в брюшную полость, в вену, внутрикожно, а также определение гемолитической активности вытяжки в опытах "in vitro".
Оценка токсичности вытяжек при введении в брюшную полость проводится по п. 8.1.1 раздела 8.1.
Опыты проводят на 20 белых мышах с исходной массой тела 18 - 20 г. Испытуемую вытяжку, приготовленную на физиологическом растворе, вводят внутривенно в хвостовую вену в дозе 10 мл/кг ежедневно, всего 5 введений.
Контрольным животным того же пола и веса вводят физиологический раствор в той же дозе, что и вытяжки из резиновых изделий.
По окончании эксперимента животных обследуют по показателям, характеризующим общее состояние организма и отдельных органов и систем (масса тела, массовые коэффициенты внутренних органов, состояние нервной системы, состав периферической крови, патоморфологические изменения внутренних органов (см. приложение 8).
Для оценки полученных результатов используются количественные критерии биологической активности резин (см. раздел 8.7).
В качестве дополнительного показателя для получения более полной характеристики биологических свойств резины используется внутрикожный тест.
Опыты проводят на 3 здоровых серых кроликах массой 2,5 - 3 кг, не бывших ранее в опытах. Предварительно выстригают шерсть с 2-х сторон спины животного вдоль позвоночника размером 4x6 см.
Вытяжка из резинового изделия, приготовленная на физиологическом растворе, в количестве 0,2 мл вводится внутрикожно в 5-ти участках кожи с одной стороны от позвоночника на расстоянии 1 см друг от друга. В кожу другой стороны вводят равное количество физиологического раствора. За местной реакцией наблюдают через 3, 6, 24 и 72 часа после инъекции.
Результаты проб оценивают по интенсивности воспалительной реакции кожи в баллах.
I - эритема диаметром до 5 мм;
II - эритема диаметром более 5 мм и небольшой отек;
III - выраженная инфильтрация;
IV - появление некроза.
Если введение физиологического раствора вызывает видимую реакцию кожи в те же сроки наблюдения, то аналогичную ей реакцию на введение вытяжки оценивали как отрицательную.
Гемолитический тест направлен на выявление возможного неблагоприятного действия полимерного материала непосредственно на кровь. Определение гемолитического действия при воздействии вытяжки проводится в опытах "in vitro" в соответствии с "Методикой, рекомендованной СЭВ для стерильных полимерных систем для взятия, переливания крови".
Исследование включает 3 этапа:
1. Приготовление вытяжки из изделий. Вытяжка должна быть приготовлена на физиологическом растворе.
2. Приготовление суспензии эритроцитов. Цитратную донорскую кровь, заготовленную на цитрате 3,9% в соотношении 1:9, центрифугируют в течение 5 минут при 1500 оборотов в минуту (срок хранения крови 24 часа, T = +4 °C). Плазму отделяют, осадок дважды промывают стерильным 0,9% раствором хлорида натрия, после каждого промывания центрифугируют 5 минут при 1500 об/мин. При отсутствии донорской крови суспензия эритроцитов может быть приготовлена на цитратной крови собаки. 1,0 мл осадка смешивают с 9,0 мл 0,9% раствора хлорида натрия.
Полученную суспензию эритроцитов следует хранить не более 24 часов в холодильнике (T = +4 - 5 °C).
3. Постановка эксперимента и оценка результатов. 5,0 мл вытяжки смешивают с 1,0 мл суспензии эритроцитов. Смесь выдерживают 1 час при температуре 37 °C, а затем центрифугируют в течение 20 минут при 1500 об/мин. В качестве контроля используется смесь 5,0 мл стерильного 0,9% раствора хлорида натрия и 1,0 мл суспензии эритроцитов. Все манипуляции по отношению к контролю проводятся параллельно с опытными пробами. Если надосадочная жидкость в контрольной пробе окажется окрашенной - исследование проводится повторно. При обнаружении окрашивания надосадочной жидкости провести определение содержания гемоглобина при длине волны 540 нм, кювета 1 см, отсчет по шкале светопропускания T.
Если величина опыта превышает значение контроля более чем на 5%, считать вытяжку "гемолитически активной", а сам полимерный материал - токсичным.
Исследуемый материал свободен от гемолитически действующих веществ, если надосадочная жидкость опытной пробы по сравнению с контрольной не превышает 5%.
К изделиям этой группы предъявляется такие же требования, что и к изделиям для контакта с кровью.
Условия приготовлений вытяжки для токсикологического эксперимента изложены в табл. 5.1.
Токсикологический эксперимент с экстрактами из фармацевтических изделий проводят в соответствии с рекомендациями, данными в приложении 7 для резин группы III. Эти исследования включают введение вытяжки в брюшную полость и внутрикожно. Способы введения осуществляются по п.п. 8.1.1 и 8.2.2.
Для изделий, предназначенных для контакта с инъекционным и инфузионными растворами, обязательным является определение пирогенности вытяжек, которое проводятся согласно Государственной фармакопее СССР /1/.
Для оценки биологических свойств изделий этой группы из исследуемых образцов готовят вытяжки согласно табл. 5.1.
При изучении изделий, имеющих контакт с желудочно-кишечным трактом, вытяжки животным вводят через рот, в остальных случаях в брюшную полость.
8.4.1. Введение вытяжки в желудок (в/ж)
Водные вытяжки вводят 40 белым крысам с исходной массой 180 - 200 г в желудок в количестве 2% от массы тела животного ежедневно, кроме выходных дней в течение 1 месяца. При увеличении сроков эксперимента до 3-х месяцев и больше водную вытяжку дают животным в виде питья из стеклянных мерных поилок.
В этом случае регистрируется суточное количество водной вытяжки потребляемое животными (утром, перед заливкой новой порции вытяжки).
Контрольные животные в аналогичных условиях получают дистиллированную воду.
Наблюдение за животными и их обследование проводят после 15 и 25 введений вытяжки в рот через зонд или ежемесячно при свободном спаивании. В качестве обязательных показателей интоксикации используются масса тела, массовые коэффициенты внутренних органов, температура тела, состояние нервной системы, состав периферической крови, состояние печени, почек, надпочечников, активность ряда специфических ферментов, патоморфологические изменения во внутренних органах (см. приложение 8).
Для оценки полученных результатов используются количественные критерии биологической активности резин (см. раздел 8.7).
Основные требования к изделиям этой группы, методы проведения эксперимента и их оценки изложены в "Методических указаниях по изучению раздражающих и сенсибилизирующих свойств резин медицинского назначения, предназначенных для контакта с неповрежденной кожей человека и установление санитарных стандартов аллергенов, мигрирующих из них", МЗ СССР, 1985 (см. приложение 10).
Основным требованием, предъявляемым к изделиям этой группы, является отсутствие загрязнения воздушной среды посторонними веществами, не превышающими ПДК для атмосферного воздуха. Гигиеническая оценка изделий осуществляется по результатам санитарно-химических анализов воздушной среды.
Для оценки степени вредного действия резин на организм использованы количественные критерии общего токсического действия, основанные на учете вариабельности изменений реактивности организма при воздействии химического фактора малой интенсивности. Выявленная зависимость частоты отклонений комплекса показателей состояния животных от повреждающего действия резин использована для подсчета суммы статистически достоверных изменений используемых тестов (n) в процентах к общему числу всех регистрируемых показателей (N) на протяжении повторного (в течение 1 - 2,5 месяцев) или хронического - 3 месячного эксперимента: КВ (критерий вредности) равен:
 ,
,где: n - суммарное число статистически достоверных изменений показателей состояния животных;
N - общее количество регистрируемых тестов на протяжении всего эксперимента.
Сформировано следующее определение критерия вредности резин.
Резины относятся к биологически активным, если они сами или вытяжки из них вызывают статистически достоверные отклонения (p < 0,05) разных показателей функционального состояния организма от контроля, суммарное количество которых в измеряемом комплексе в течение многократных определений на протяжении повторного или хронического воздействия составляет больше 5%, хотя наблюдавшиеся изменения находятся в пределах физиологических колебаний (приложение 9).
3. Кибардин С.А., Марков К.А. Тонкослойная хроматография в органической химии. - М.: Химия, 1978.
4. Березкин В.Г., Бочков А.С. Количественная тонкослойная хроматография. - М.: Наука, 1980.
5. Кирхнер Ю. Тонкослойная хроматография. - М: Мир, 1981 - 2 т.
6. Методические рекомендации по определению вредных веществ, выделяющихся из полимерных материалов в воду, модельные среды и пищевые продукты. - Л., 1981.
7. Саноцкий И.В. Методы определения токсичности и опасности химических веществ. - М.: 1970. - 316 с.
9. МЗ СССР 14.04.80 N 2166-80. Методические рекомендации по использованию поведенческих реакций животных в токсикологических исследованиях для целей гигиенического нормирования. - Киев, 1980. - С. 16 - 17.
14. Германова А.Л. Отчет по теме N 800003; АМН СССР, Институт гигиены труда и профзаболеваний. - 1982.
18. Шумская Н.И., Найденко Н.Ф. Токсикология новых промышленных веществ. Медицина. - 1971. - N 12. - С. 124 - 132.
21. Муравьева С.И., Бабина М.Д., Атласов А.Г., Новиков Н.С. Санитарно-химический контроль воздуха промышленных предприятий. - М.: Медицина, 1982.
В РЕЗИНОВЫХ ИЗДЕЛИЯХ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
Раздел I
1. Каучуки, латексы, регенераты
1.1. Каучуки
Содержание в резиновых смесях от 30 до 80% по массе
NN | Наименование | ГОСТ, ТУ | Марка | Примечание |
1 | 2 | 3 | 4 | 5 |
1.1.1. | Натуральный каучук | Инструкция МНХП 1983 (приемка, хранение и испытание НК) | Смокед-шит светлый креп | |
1.1.2. | Бутилкаучук | ТУ 38.003169-74Е изм. 3 ТУ 38.30100-84 | БК 2045М БК 1675Т БК 1675М | |
1.1.3. | Синтетический натрий-бутадиеновый каучук | ОСТ 38.00379-74 | СКБ 35рщ | |
1.1.4. | Синтетический цис-изопреновый | ТУ 38.103241-79 изм. 3 | СКИ-ЗС | |
ТУ 38.103244-81 | СКИ-ЗП | |||
1.1.5. | Термостойкий винилсилоксановый | ОСТ 38.0310-78 | СКТВ кислотный и щелочной | |
ТУ 38.403380-80 | СКТВМ для медицинских изделий | |||
1.1.6. | Термостойкий силоксановый | ГОСТ 14680-79 | СКТ | |
ГОСТ 13835-73 | СКТН низкомолекулярный | |||
1.1.7. | Хлорбутилкаучук | Импортный | НТ-1068 | |
1.1.8. | Бутадиеновый | ТУ 38.40307-81 | СКД-ЛР 1,2 | |
1.1.9. | Бутадиен-нитрильный | ТУ 38.103264-80 изм. 1 | СКН-26М с П-23 | |
1.2. Латексы Содержание в смесях от 80 до 100% по массе | ||||
1.2.1. | Натуральный центрифугированный невулканизованный | Импортный | Квалитекс и другие | |
1.2.2. | Натуральный центрированный сливкоотделением | Импортный | Ревертекс TS | |
1.2.3. | Натуральный вулканизованный | Импортный | Ревультекс LR, MR Квалитекс PV | |
1.3. <*> Регенераты цветные | ||||
1.3.1. | Регенераты цветные | ТУ 38.106142-76 | ЛР-27 ЛР-32 ЛР-35 | |
Раздел II
2. Ингредиенты резиновых и латексных смесей
2.1. Вулканизующие агенты
Общее содержание в резиновых смесях не более 2,5% по массе, в латексных - 3,0% по массе.
NN | Наименование | ГОСТ, ТУ | Марка | Примечание | ||||
1 | 2 | 3 | 4 | 5 | ||||
| ||||||||
2.1.1. | Сера техническая | ГОСТ 127-76 | Молотая высший сорт, класс 1 и 2, 9995, 9996 | |||||
2.1.2. | Перекись бензоила техническая (бензоилпероксид) | ГОСТ 14888-78 | ||||||
2.1.3. | Паста пероксида 2,4-дихлорбензоила | Импортная | ||||||
2.1.4. | Тиурам Д (тетраметилтиурамдисульфид) | |||||||
2.1.5. | Дитиодиморфолин | ТУ 6-14-10-321-79 | ||||||
2.1.6. | Тиурам Е (тетраэтилтиурамдисульфид) | ОСТ 6-14-147-80 | ||||||
2.1.7. | Тиурам ЭФ (тетраэтилфенилтиурамдисульфид) | ТУ 6-14-22-211-82 | ||||||
2.2. Ускорители вулканизации Общее содержание в смесях не более 1,2% по массе | ||||||||
2.2.1. | 2,2'-дибензтиазолдисульфид, тиазол 2-МБС (альтакс)-75 | ГОСТ 7087-75 изм. 1 | ||||||
2.2.2. | Бутилцимат (дибутилдитиокарбамат цинка) | Импортный | ||||||
2.2.3. | Вулкацит-П-экстра-Н (этилфенилдитиокарбамат цинка) | Импортный | ||||||
Hermat | Стандарт ЧССР Д.9058-66 | |||||||
2.2.4. | Дифенилгуанидин (гуанид Ф) | |||||||
порошок | ГОСТ 40-80 | |||||||
гранулы | ТУ 6-14-996-76 | |||||||
2.2.5. | Каптакс (2-меркаптобензтиазол) | изм. 1 | ||||||
2.2.6. | Тиурам Д (тетраметилтиурамдисульфид) | |||||||
2.2.7. | Тиурам Е (тетраэтилтиурамдисульфид) | ОСТ 6-14-147-80 | ||||||
2.2.8. | Тиурам ЭФ (тетраэтилфенилтиурамдисульфид) | ТУ 6-14-22-211-82 | Опытные партии | |||||
2.2.9. | Сульфенамид Ц (N-циклогексилбензтиазолилсульфенамид-2) | ТУ 6-14-868-81 | ||||||
2.2.10. | Ускоритель К-45 (диметилдитиокарбамат диметиламмония) | ТУ 6-14-550-75 | ||||||
2.2.11. | Этилцимат (диэтилдитиокарбамат цинка) | ТУ 6-14-809-77 | ||||||
2.2.12. | Цинкапт (цинковая соль 2-меркаптобензтиазола) | ТУ 6-14-900-77 | ||||||
2.2.13. | Цимат (диметилдитиокарбамат цинка) | ТУ 6-14-915-78 | ||||||
2.3. Активаторы ускорителей Содержание в резиновых смесях не более 5%, в латексных - не более 3% по массе. | ||||||||
2.3.1. | Белила цинковые (оксид цинка) | БЦ-0 БЦ-1 | ||||||
2.3.2. | Белила цинковые сухие муфельные | ГОСТ 5.161-69 | ||||||
2.3.3. | Магнезия жженая | ГОСТ 844-79 | А | |||||
2.3.4. | Тиомочевина | |||||||
2.4. Антискорчинги | ||||||||
| ||||||||
2.4.1. | Бензойная кислота | ГОСТ 6313-77 | ||||||
2.4.2. | Ангидрид фталевый технический | ГОСТ 7119-77 | ||||||
2.5. Противостарители Общее содержание в смесях не более 2% по массе | ||||||||
2.5.1. | Агидол-2 (НГ-2246; 2,2'-метилен-бис-(4-метил-6-третбутилфенол) | ТУ 38.101617-80 | ||||||
2.5.2. | Агидол-40 (2,4,6-трис(3,5-ди-третбутил-4-оксибензил)мезителен | ТУ 38.103217-73 | ||||||
2.5.3. | Нафтам-2 (фенил-2-нафтиламин) | ГОСТ 39-79 | ||||||
2.5.4. | Церезин | М-67, М-80 | ||||||
2.5.5. | Озокерит 60 | ТУ 01-08-386-78 | ||||||
2.5.6. | Сплав АФ-1 (церезин, парафин, петролятум) | ТУ 38.101595-81 | ||||||
2.5.7. | Воск ЗВ-1 (защитный) | ТУ 38.101564-80 | ||||||
2.5.8. | Агидол-1 (ионол) (4-метил-2,6-дитретбутилфенол) | ГОСТ 10894-76 | ||||||
пищевой | ТУ 38.101459-74 | |||||||
2.5.9 <*> | Диафен ФП (4010 NA) N-изопропил-N-фенилфенилендиамин-1,4) сантофлекс IP | импортный ТУ 6-14-817-76 | ||||||
2.5.10. | Воск ЗВ-1 (защитный) | ТУ 38.101564-80 | ||||||
2.6. Наполнители Общее содержание в резиновой смеси не более 80% по массе | ||||||||
2.6.1. | Аэросил А-175 | |||||||
2.6.2. | Барий сернокислый аккумуляторный | ГОСТ 11380-74 | ||||||
2.6.3. | Барий сернокислый реактивный | |||||||
2.6.4. | Барий углекислый технический | ГОСТ 2149-75 | ||||||
2.6.5. | Каолин обогащенный для резино-технических изделий и пластмасс | ГОСТ 19608-74 | ||||||
Каолин парфюмерный | ГОСТ 21285-75 | П-1 | ||||||
2.6.6. | Литопон сухой парфюмерный | Кр | ||||||
ГОСТ 21285-76 | П-1 | |||||||
2.6.7. | Мел химический осажденный | А, Б | ||||||
| ||||||||
2.6.8. | Мел природный обогащенный | ГОСТ 12085-73 | ММС | |||||
| ||||||||
2.6.9. | Сажа белая БС-50, БС-100 | |||||||
2.6.10. | Сажа белая У-333 | ТУ 6-18-184-74 | ||||||
2.6.11. | Тальк медицинский | импортный | ||||||
| ||||||||
2.6.12. | Тальк молотый для производства резиновых изделий и пластических масс | ТРПН - наполнитель ТРПВ - для опудривания | ||||||
Тальк молотый из руд Онотского месторождения (для пищевой промышленности) | ГОСТ 21-25-217-78 | марки А | ||||||
2.6.13. | Углерод технический | ГОСТ 7885-77 изм. N 4 | К 354 П 324 П 514 П 701 П 803 <*> Т 900 <*> | |||||
окисленный | ТУ 38.415106-82 | (ПМО-101М) П 243-0 | ||||||
печной электропроводный | ТУ 38.11518-85 | (ПМЭ-80В) П 366-7 | ||||||
Примечание: <*> Допускается применение только в сочетании с техуглеродом марок ПМ-75, ДГ-100 и электропроводящими марками техуглерода.
печной электропроводный, импортный | СТ СЭВ 3766-82 | |||||||
ацетиленовый элементный | ТУ 14-7-24-73 | |||||||
2.6.14 <*> | Глет свинцовый (оксид свинца) | ГОСТ 5539-78 | ||||||
2.7. Мягчители и пластификаторы Общее содержание в резиновых смесях не более 15% по массе. | ||||||||
| ||||||||
2.7.1. | Масло индустриальное | ГОСТ 20799-75 | И-8А | |||||
2.7.2. | Низкомолекулярный полиэтилен (НМПЭ) | ТУ 6-05-1837-77 | кроме изделий, соприкасающихся с жирами | |||||
| ||||||||
2.7.3. | Кислота стеариновая техническая (стеарин) | ГОСТ 6484-64 | для пробок фармацевтических только сорт особый А, или Б, или сорт 1 | |||||
2.7.4. | Канифоль сосновая | ГОСТ 19113-73 ГОСТ 797-64 | ||||||
| ||||||||
2.7.5. | Парафин нефтяной для пищевой промышленности | ГОСТ 13577-71 | Марка А | |||||
ГОСТ 23683-79 | П-1, П-2 | |||||||
2.7.6. | Дибутилфталат, диоктилфталат | ГОСТ 8728-77 | дибутилфталат | |||||
2.7.7. | Ренацит IV (цинковая соль пентахлортиофенола) | импортный | ||||||
2.7.8. | Масло-мягчитель нетоксол | ТУ 38.101999-84 | ||||||
2.7.9. | Фактис темный | ТУ 38.106257-74 | ||||||
2.7.10. | Канифоль экстракционная модифицированная ЭМ-3 | ТУ 8-105-50-78 | ||||||
2.7.11 <*> | Стабилпласт-62 | ТУ 38.101545-80 | ||||||
| ||||||||
2.7.12. | Синтетические жирные кислоты | ГОСТ 23239-78 | ||||||
2.7.13 <*> | Полипропилен атактический (АПП) | ТУ 6-05-1902-81 | ||||||
2.7.14 <*> | Рубракс (битумы нефтяные) | |||||||
2.8. Поверхностно-активные вещества (эмульгаторы, диспергаторы, стабилизаторы) Общее содержание в латексных смесях не более 4% по массе. | ||||||||
2.8.1. | Дибутилфталат реактивный | ГОСТ 2102-67 | ||||||
2.8.2. | Диспергатор НФ технический | ГОСТ 6848-79 | ||||||
| ||||||||
2.8.3. | Казеин кислотный | ГОСТ 17626-72 | ||||||
| ||||||||
2.8.4. | Кислота олеиновая чистая | ГОСТ 7580-55 изм. 1 ГОСТ 10475-75 | ||||||
2.8.5. | Лигнин сульфатный | ТУ 81-04-145-72 | ||||||
2.9. Стабилизаторы силиконовых смесей Общее содержание в смесях не более 8% по массе | ||||||||
2.9.1. | Дифенилсиландиол | ТУ 6-02-63-71 | ||||||
2.9.2. | Диолы НД-8 (L,W-дигидроксиполиметилсилоксаны) | СТП 38.1440-77 | ||||||
2.10. Пигменты и красители Общее содержание в резиновой смеси не более 2% по массе, в латексной смеси не более 5% по массе. | ||||||||
2.10.1. | Пигмент красный железоокисный марки К | ТУ 6-10-602-77 | ||||||
2.10.2. | Пигмент голубой фталоцианиновый | |||||||
2.10.3. | Пигмент желтый прочный 23 | ТУ 6-14-615-81 | ||||||
2.10.4. | Пигмент зеленый | |||||||
2.10.5. | Пигмент зеленый фталоцианиновый | ТУ 6-14-408-76 | ||||||
2.10.6. | Пигмент золотисто-желтый прочный | ТУ 6-14-744-78 | ||||||
2.10.7. | Пигмент красный 5С | ТУ 6-14-588-79 | ||||||
2.10.8. | Пигмент оранжевый Е | ТУ 6-14-46-81 | ||||||
2.10.9. | Пигмент розовый Н | ТУ 6-14-244-76 | ||||||
2.10.10. | Пигмент чисто-голубой фталоцианиновый | ТУ 6-14-516-80 | ||||||
2.10.11. | Лак оранжевый | ГОСТ 1338-78 | ||||||
2.10.12. | Лак рубиновый СК | ГОСТ 7436-74 | ||||||
2.10.13. | Ультрамарин УС | ОСТ 6-10-404-77 | ||||||
| ||||||||
2.10.14. | Диоксид титана пигментный | ГОСТ 9808-75 | А-1 А-01 | |||||
2.11. Вещества, регулирующие pH латексных смесей Общее содержание в смеси не более 1% по массе. | ||||||||
| ||||||||
2.11.1. | Аммиак водный технический | ГОСТ 9-77 | ||||||
2.11.2. | Калий гидроксид технический | |||||||
2.11.3. | Натр едкий очищенный | |||||||
Раздел III
3.1. Вспомогательные вещества | ||||||||
| ||||||||
3.1.1. | Бензин | ГОСТ 443-76 | БР-1 "Галоша" | |||||
3.1.2. | Ксилол | |||||||
3.1.3. | Толуол | |||||||
3.1.4. | Спирт этиловый ректификованный технический | |||||||
3.1.5. | Полиметилсилоксановая жидкость | ПМС-200 ПМС-300 ПМС-400 ПМС-500 | ||||||
3.1.6. | Резотропин (модификатор РУ) | ТУ 6-14-200-76 | ||||||
| ||||||||
3.1.7. | Сода кальцинированная | ГОСТ 5100-73 | ||||||
3.1.8. | Глицерин | дистиллированный | ||||||
3.1.9. | Натрий карбоксиметилцеллюлоза очищенная | ОСТ 6-05-386-73 | ||||||
| ||||||||
3.1.10. | Кислота соляная | ГОСТ 857-78 | ||||||
3.1.11. | Натрий хлористый | ГОСТ 13830-68 | ||||||
| ||||||||
3.1.12. | Натрий двууглекислый | ГОСТ 4201-66 | ||||||
| ||||||||
3.1.13. | Полиэтиленовая пленка | ГОСТ 10354-73 | ||||||
3.1.14. | Триполифосфат натрия | ГОСТ 13493-77 | ||||||
3.1.15. | Триэтаноламин (чистый) | ТУ 6-09-2448-72 | ||||||
3.1.16. | Углекислый аммоний пищевой | ГОСТ 18916-73 | ||||||
3.1.17. | Углеаммонийные соли технические | |||||||
3.1.18. | Цинк углекислый | ТУ 6-09-01-575-79 | ||||||
3.1.19. | Эмульсия КЭ 10-01 | ТУ 6-02-587-75 | 70%-ная | |||||
3.1.20. | Лутанол М-40 (поливинилметиловый эфир) | импортный | ||||||
3.2. Вспомогательные смеси | ||||||||
3.2.1. | Штепельная краска для маркировки хирургических перчаток | Л-167-3 | Заключение ВНИИИМТ N 51-Т/3307 от 27.04.77 | |||||
3.2.2. | Талько-каолиновая дисперсия для опудривания хирургических перчаток (с добавлением эмульсии ПМС-300) | Заключение ВНИИИМТ N 51-Т/5629 от 01.08.77 | ||||||
3.2.3. | Краска для маркировки резиновых хирургических перчаток | 52-414 52-415 | ||||||
3.2.4. | Краска маркировочная | 52-53 | ВНИИИМТ N 51-Т/5774 от 28.07.75 | |||||
3.2.5. | Краска для маркировки хирургических перчаток | 52-473 52-473а | ВНИИИМТ N 51-Т/4306 от 01.07.74 | |||||
ХИМИЧЕСКИХ ВЕЩЕСТВ ИЗ РЕЗИН
NN пп | Наименование определяемого химического вещества | Величина ДКМ, мг/л | Примечание |
1 | 2 | 3 | 4 |
1. | Изопрен | 0,01 | |
2. | Нитрил акриловой кислоты | 0,05 | |
3. | Агидол 2-(НГ-2246, 2,2-метилен-бис-(4-метил-6-трет-бутилфенол) | 2,00 | |
4. | Агидол 40 (2,4,6-трис-(3,5-ди-трет-бутил-4-оксибензил)-мезитилен | 1,00 | |
5. | Тетраметилтиурамдисульфид (тиурам Д) | 0,05 | Для укупорочных пробок и систем для переливания крови |
0,5 | Для резин, контактирующих с кожей | ||
0,6 | Для остальных резин | ||
6. | Тетраэтилтиурамдисульфид (Тиурам Е) | 0,5 <*> | |
7. | Диэтилдифенилтиурамдисульфид (тиурам ЭФ) | 1,0 | |
8. | Моноэтиланилин | 0,5 | |
9. | Диметилдитиокарбамат цинка (цимат) | 0,05 | Для резин, контактирующих с кровью |
0,6 | Для остальных резин | ||
10. | Диэтилдитиокарбамат цинка (этилцимат) | 0,5 <*> | |
11. | Этилфенилдитиокарбамат цинка | 1,0 | |
12. | Дифенилгуанидин | 0,15 | |
0,5 | Для резин, контактирующих с кожей человека | ||
13. | Альтакс <**> | 0,4 | |
14. | Каптакс <**> (2-меркаптобензтиазол) | 0,4 |
--------------------------------
15. | Сульфенамид Ц <*> (циклогексил-2-бензтиазолсульфенамид) | 0,4 | |
16. | Дибутилфталат | 0,2 | |
17. | Диоктилфталат | 2,0 | |
18. | Неозон Д (нафтам-2, 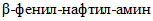 ) ) | 0,2 | |
19. | Дитиодиморфолин | 0,5 | |
20. | Ионы цинка | 1,0 | |
21. | Ионы бария | 0,1 | |
22. | Ацетофенон | 0,1 |
--------------------------------
ПЕРЕЧЕНЬ ВЕЩЕСТВ, КОТОРЫЕ НЕОБХОДИМО ОПРЕДЕЛЯТЬ
В МОДЕЛЬНЫХ СРЕДАХ В ЗАВИСИМОСТИ ОТ РЕЦЕПТУРЫ РЕЗИН
NN пп | Наименование ингредиентов резин | Определяемое химическое вещество |
1 | 2 | 3 |
1. | Каучуки СКИ-ЗС СКИ-ЗП СКИЛ-5 | Изопрен |
2. | Каучук синтетический бутадиен-нитрильный СКН-26М с П-23 | Нитрил акриловой кислоты |
3. | Агидол-2 (НГ-2246, 2,2-метилен-бис-4-метил-6-третбутилфенол) | 2,2'-метилен-бис-4-метил-6-третбутилфенол |
4. | Агидол 40 (2,4,6-трис-(3,5-дитретбутил-4-оксибензил) мезитилен | 2,4,6-трис-(3,5-дитретбутил-4-оксибензил) мезитилен |
5. | Тетраметилтиурамдисульфид (тиурам Д) | тетраметилтиурамдисульфид диметилдитиокарбамат цинка |
6. | Тетраэтилтиурамдисульфид (тиурам Е) | тетраэтилтиурамдисульфид диэтилдитиокарбамат цинка |
7. | Диэтилдифенилтиурамдисульфид (тиурам ЭФ) | диэтилдифенилтиурамдисульфид моноэтиланилин |
8. | Этилфенилдитиокарбамат цинка (вулкацит Р экстра Н) | этилфенилдитиокарбамат цинка моноэтиланилин |
9. | Диэтилдитиокарбамат цинка (этилцимат) | диэтилдитиокарбамат цинка |
10. | Дифенилгуанидин | дифенилгуанидин |
11. | Каптакс (2-меркаптобензтиазол) | 2-меркаптобензтиазол |
12. | Альтакс (2,2-дибензтиазолдисульфид) | 2-меркаптобензтиазол |
13. | Циклогексил-2-бензтиазол-сульфенамид (сульфенамид Ц) | сульфенамид Ц 2-меркаптобензтиазол |
14. | Цинковая соль 2-меркаптобензтиазола (цинкапт) | 2-меркаптобензтиазол |
15. | Дибутилфталат | дибутилфталат |
16. | Диоктилфталат | диоктилфталат |
17. | Неозон Д (нафтам-2, 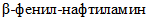 ) ) |  |
18. | Дитиодиморфолин | дитиодиморфолин |
19. | Белила цинковые (оксид цинка) | ионы цинка |
20. | Литопон | ионы бария ионы цинка |
21. | Барий сернокислый, уксуснокислый | ионы бария |
22. | Глет свинцовый <*> | ионы свинца |
23. | Ренацит IV (цинковая соль пентахлортиофенола) | ионы цинка |
--------------------------------
РЕЗИНОВЫХ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
I группа. Изделия для эндопротезирования.
Соотношение поверхности изделия в см2 к объему моющего раствора в мл 1:5.
Двухкратное кипячение в 0,5% растворе натрия кислого углекислого (NaHCO3) в дистиллированной воде по 30 минут.
Двухкратная-трехкратная промывка после каждого кипячения дистиллированной водой комнатной температуры в течение 5 минут.
Кипячение в дистиллированной воде в течение 30 минут.
Автоклавирование изделий в безворсовой (пергаментной) бумаге при температуре 120 +/- 2 °C в течение 45 минут.
II группа. Изделия для контакта с кровью и кровезаменителями.
Соотношение веса изделий в граммах к объему моющего раствора в мл 1:5.
Промывка проточной водопроводной водой в течение 5 минут.
Двухкратное кипячение в 1% растворе натрия углекислого (кальцинированной соды Na2CO3) по 30 минут.
Кипячение в 0,1% растворе соляной кислоты (HCl) в течение 30 минут.
Двухкратное автоклавирование в дистиллированной воде по 60 минут при температуре 120 +/- 2 °C и давлении 1,1 - 1,2 атм для изделий на основе натурального и силиконового каучуков и при температуре 130 +/- 2 °C и давлении 1,8 - 2 атм для изделий на основе бутилкаучука (укупорочные пробки).
После каждого кипячения и автоклавирования трехкратное промывание изделий дистиллированной водой комнатной температуры в течение 5 минут.
III группа. Фармацевтические изделия.
Соотношение веса изделий в граммах к объему моющего раствора в мл 1:5.
Промывка проточной водопроводной водой в течение 5 минут. Двухкратное кипячение в 2% растворе натрия гидрооксида (NaOH) по 10 минут.
Автоклавирование в дистиллированной воде при температуре 120 +/- 2 °C и давлении 1,1 - 1,2 атм в течение 60 минут.
После каждого кипячения и автоклавирования трехкратное промывание изделий дистиллированной водой комнатной температуры в течение 5 минут.
IV группа. Изделия для гастроэнтерологии, урологии, акушерства и анестезиологии.
Соотношение поверхности изделий в см2 к объему моющего раствора в мл 1:5.
Продувание сжатым воздухом для освобождения от талька и резиновой крошки.
Промывание проточной водопроводной водой комнатной температуры в течение 5 минут.
Двухкратное кипячение в 2% растворе натрия кислого углекислого (NaHCO3) или натрия углекислого (Na2CO3) в течение 30 минут.
Двухкратное кипячение в дистиллированной воде в течение 30 минут.
После каждого кипячения трехкратное промывание изделия дистиллированной водой комнатной температуры не менее 5 минут.
V и VI <*> группы. Изделия санитарии и гигиены, ухода за больными. Комплектующие детали к наркозно-дыхательной аппаратуре и другим аппаратам, приборам и оборудованию.
--------------------------------
<*> Указанная обработка не распространяется на кружки и жгуты Эсмарха, грелки, пузыри для льда, бинты Мартенса, напальчники, подушки кислородные и детали к операционным столам.
Соотношение поверхности изделия в см2 к объему моющего раствора в мл 1:5.
Продувание сжатым воздухом для освобождения от талька и резиновой крошки.
Промывание проточной водопроводной водой в течение 5 минут.
Кипячение в 2% растворе натрия кислого углекислого (NaHCO3) или натрия углекислого (Na2CO3) в течение 30 минут.
Трехкратное промывание изделий дистиллированной водой комнатной температуры в течение 1 минуты.
Кипячение в дистиллированной воде в течение 30 минут.
Образец дегустационной карты
Фамилия, имя, отчество ____________________________________
Дата проведения анализа ___________________________________
NN растворов, не отличающихся от контрольного ______________
по запаху __________________ по привкусу ___________________
1. Характер запаха исследуемого (фенольный, ароматический, посторонний, неопределенный и т.д.).
2. Характер привкуса исследуемого раствора (горьковатый, щиплющий, нефтепродуктов, посторонний, неопределенный).
3. Интенсивность запаха и привкуса исследуемого растворов в баллах.
NN растворов | запах в баллах | привкус в баллах |
1. | ||
2. | ||
3. |
Подпись ____________
ФОРМА БЛАНКА ПРОВЕДЕННОГО ХИМИЧЕСКОГО АНАЛИЗА
Анализ N от "___" ______ 198__ г.
по санитарно-химическому контролю резины
марки _________________________, предназначенной для ______________________
______________________ по разрешению МЗ СССР N ____________________________
Образец ___________________________________________________________________
(пластина, изделие)
Дата поступления __________________________________________________________
Режим вулканизации ________________________________________________________
Условия эксплуатации изделий:
Температура эксплуатации, °C ______________________________________________
Соотношение поверхности резины к объему рабочей среды в течение
1 часа ____________________
Давление, МПа _____________
Особые условия обработки изделия перед эксплуатацией ______________________
___________________________________________________________________________
Результаты санитарно-химического контроля
Модельная среда | Условия приготовления вытяжек | Содержание компонентов, мг/л | ||||
Т °C | Экспозиция, час | |||||
заливания | настаивания | каптакс | тиурам | |||
Заключение: приведенные показатели (не) соответствуют ДКМ
Анализ проведен т. ______________________ по инструкции N _________________
(сотрудник)
Зав. лаб.
Группы резин | Вид животного | Способы воздействия на организм | Кол-во животных | Доза | Режим воздействия | Сроки наблюдения, мес. | Исследования |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
I. Изделия для внутреннего протезирования | крысы | 1. Введение вытяжек в/б | 40 | 10 мл/кг | через день, 25 раз | 2 | |
2. Имплантация в/б и п/к | 50 | вес образца | операция | 12 - 18 | |||
3. Бластомогенный эффект | 50 | -"- | -"- | до естеств. гибели | |||
II. Изделия для контакта с кровью | крысы | Введение вытяжек в/б | 40 | 10 мл/кг | через день, 25 раз | 2 | Определение гемолитической активности вытяжек |
мыши | в/в | 20 | 10 мл/кг | ежедневно 5 раз | 2 недели | - | |
кролики | в/к | 6 | 0,2 мл | однократно в 5 точках | 72 часа | ||
крысы | Введение вытяжек в/б | 40 | 10 мл/кг | через день, 25 раз | 2 | - | |
кролики | в/к | 6 | 0,2 мл в 5 точках | однократно | 72 часа | ||
IV. Изделия используемые в гастроэнтерологии, урологии, акушерстве и в анестезиологии | крысы | Введение вытяжки в/ж | 40 | 2% от массы тела | ежедневно | 1 <*> | |
-"- | Введение в/б | 40 | 10 мл/кг | ежедневно 25 раз | 2 | ||
V. Изделия санитарии и гигиены, ухода за больными | морские свинки | Аппликации образца на кожу | 30 | 6,5 см2 поверхности | ежедневно | 1,5 | |
VI. Комплектующие детали к наркозно-дыхательной аппаратуре и диагностическим приборам | крысы | Оценка по результатам сан. химических анализов воздушной среды |
--------------------------------
1. Масса тела /7/
2. Массовые коэффициенты внутренних органов /7/
3. Температура тела
4. Состояние нервной системы:
а) суммационно-пороговый показатель /8/
б) норковый рефлекс /9/
в) ориентировочные реакции /9/
5. Состав периферической крови:
а) гемоглобин /10/
б) эритроциты /11/
в) лейкоциты /11/
г) лейкоцитарная формула /12/
д) состояние гемостаза /13/
6. Состояние печени:
а) гиппуровая кислота /14/
б) общий белок /15/
в) SH-группы в сыворотке крови /16/
7. Состояние почек:
а) диурез /17/
б) белок /18/
ИС МЕГАНОРМ: примечание. Нумерация пунктов дана в соответствии с официальным текстом документа. |
г) хлориды в моче /19/
8. Активность ряда специфических ферментов (церулоплазмина, каталазы) /20/
9. Состояние надпочечников:
а) Содержание аскорбиновой кислоты /21/
б) массовый коэффициент /7/
10. Патоморфологические изменения во внутренних органах.
Класс опасности резин | Степень биологической активности | Критерии вредности | |
Частота изменений комплекса показателей у животных, % | Степень выраженности биологических эффектов у животных | ||
высоко активные | выше 20 | Стойкие, необратимые изменения показателей, носящих системный характер, сочетание функциональных морфологических нарушений | |
умеренно активные | 6 - 20 | Изменения различных показателей, не сохраняющихся в "восстановительном" периоде; но выявляемые с помощью функциональных нагрузок | |
не активные | 0 - 5 | Отсутствие или изменения отдельных показателей, не носящие системный характер, нестойкие, не сохраняющиеся в "восстановительном" периоде и не выявляемые с помощью функциональных нагрузок | |
Первые две группы резин (I и II) не допускаются для широкого использования по назначению. Резины, относящиеся к III группе, рекомендуются для натурных и клинических испытаний.
Утверждаю
Начальник управления по внедрению
новых лекарственных средств
и медицинской техники
Минздрава СССР
Э.А.БАБАЯН
17 сентября 1985 года
Согласовано
И.о. директора ВНИИИМТ
Минздрава СССР, д.т.н.,
профессор
Б.И.ЛЕОНОВ
Зав. отделом
токсикологических исследований
и испытаний полимерных
и других материалов
медицинского назначения,
к.м.н.
В.Г.ЛАППО
Зам. начальника
ВПО "Союзрезинообувь"
Б.К.ГОЛУБЕВ
16 сентября 1985 года
ПО ИЗУЧЕНИЮ РАЗДРАЖАЮЩИХ И СЕНСИБИЛИЗИРУЮЩИХ СВОЙСТВ РЕЗИН
МЕДИЦИНСКОГО НАЗНАЧЕНИЯ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ КОНТАКТА
С НЕПОВРЕЖДЕННОЙ КОЖЕЙ ЧЕЛОВЕКА, И УСТАНОВЛЕНИЮ САНИТАРНЫХ
СТАНДАРТОВ АЛЛЕРГЕНОВ, МИГРИРУЮЩИХ ИЗ НИХ
"Методические указания" разработаны в Научно-исследовательском институте резиновых и латексных изделий Миннефтехимпрома
Составители:
Зав. токсикологической лабораторией, докт. мед. наук Н.И. Шумская; научный сотрудник Л.П. Петрова.
ОБЩИЕ ПОЛОЖЕНИЯ
В связи с возможностью развития заболеваний кожи в результате контакта с резиновыми изделиями, используемыми в медицине (хирургические и анатомические перчатки, напальчники, эластичные бинты, моче- и калоприемники, дренажные трубки, предметы санитарии и гигиены), возникла необходимость предварительной оценки их раздражающих и сенсибилизирующих свойств.
Биологическая активность резин обусловлена мигрирующим из них комплексом химических соединений, зависящим от состава рецептуры и технологического режима синтеза. Многие исходные продукты изготовления резин (хлоропреновый, стирольный, этиленпропиленовый, натрий-бутадиеновый, полисульфидный, фтористый каучуки, тиурам Д, неозон Д, парафенилендиаминовые антиоксиданты, ренацит и др.) обладают раздражающим и сенсибилизирующим действием. Однако, аллергенное действие резины определяется не только свойствами исходных ингредиентов. На резину распространяются закономерности комбинированного действия химических соединений. Кроме того, вновь образующиеся в резине продукты взаимодействия ингредиентов (в основном, каучуков и ускорителей вулканизации) могут придавать резине раздражающее и сенсибилизирующие свойства. Указанная особенность резин послужила основанием для разработки настоящих рекомендаций к постановке исследований резин, предназначенных для непосредственного контакта с кожей человека.
Разработка новых резин и резиновых изделий указанного назначения должна проводиться с учетом установленных гигиенических нормативов для мигрирующих веществ.
Методические указания предназначены для врачей-токсикологов НИИ гигиенического профиля и ведомственных токсикологических лабораторий, занимающихся исследованием резиновых изделий для медицины.
Методические указания включают следующие разделы:
- Исследование раздражающего действия резиновых изделий в эксперименте на животных.
- Исследование раздражающего действия резин на людях-добровольцах.
- Гигиеническое регламентирование аллергенов, мигрирующих из резин.
При направлении на исследование необходимо представить следующие материалы:
- название (марка) материала или изделия и область его применения с указанием характера и длительности контакта с организмом;
- рецептуру композиции с указанием нормативной документации на ингредиенты, их названий и количество;
- краткое описание технологии изготовления изделий с указанием веществ, применяемых в процессе синтеза (катализаторов, инициаторов и т.д.) с результатами определения их остаточных количеств в композиции, а также температурных режимов процессов;
- наименование учреждения-изготовителя;
- предполагаемая продолжительность хранения изделия от момента изготовления до использования, режим хранения;
- вид стерилизации, из числа предусмотренных ОСТом 72-2-2-77.
Представляемые на испытание образцы должны пройти предстерилизационную очистку и (или) стерилизацию.
Для проведения исследований изделий, выпускаемых на импортных ингредиентах или по технологии зарубежных фирм, следует представлять документы, разрешающие применение данного изделия (или материала) в стране-изготовителе.
Количество образцов, необходимое
для проведения гигиенических исследований
Наименование изделий | Количество образцов | |
штук | м2 | |
Бинты Мартинса | - | 0,5 |
Жгуты Эсмарха | - | 0,5 |
Подкладная клеенка | - | 0,5 |
Кало- и мочеприемники | 5 | - |
Подкладные круги | 1 | - |
Напальчники | 20 | - |
Перчатки | 10 | - |
Предварительным и обязательным этапом исследования является ознакомление с рецептурой и технологическим режимом синтеза изучаемого полимера с целью выявления в нем раздражающих веществ и аллергенов. Эти сведения помогают сделать некоторые рекомендации уже в процессе предварительного отбора. Например, не рекомендуется вводить в состав резиновой смеси с невысоким содержанием наполнителя одновременно несколько ингредиентов, обладающих выраженным аллергенным и раздражающим действием на кожу (тиурам Д, каптакс, неозон Д, ионокс, 4010 NA, натуральный каучук "смокед-шит"). Из резин подобного типа (малонаполненных) происходит одновременная миграция нескольких продуктов, что создает опасность усиления биологического эффекта, характерного для комбинированного действия аллергенов.
Об опасности развития повышенной чувствительности к резине можно судить уже по миграции из нее химических соединений, обладающих аллергенными свойствами. Условия проведения санитарно-химических анализов определяются назначением резиновых изделий и режимом их эксплуатации. При контакте резины с кожей поступление химических соединений в организм происходит путем перехода их в жидкие продукты жизнедеятельности кожных желез. Исходя из этого, для проведения исследований резин из них рекомендуется приготовить экстракты на дистиллированной воде и физиологическом растворе. Учитывая односторонний контакт изделия с кожными покровами, при экстрагировании берется соотношение поверхности образца резины к объему экстрагента, равное 1:2 см2/см3.
Приготовление вытяжек проводится в термостате при температуре 37 - 40 °C в течение 24 часов. Указанные условия экстрагирования резин предусматривают некоторую аггравацию с целью осуществления наиболее полного перехода токсичных веществ из резины в контактирующие среды.
Образцы изделий перед испытаниями обрабатывают теплой водой с мылом с последующим ополаскиванием дистиллированной водой или подвергают специальной стерилизации, предусмотренной инструкцией по эксплуатация изделия. Результаты испытаний выражаются в количестве мигрирующего вещества (мг) со 100 см2 поверхности резины.
Набор санитарно-химических показателей зависит от состава резиновой смеси и включает в себя 3 основные группы исследуемых показателей:
1. Исследование вытяжек интегральными методами (определение содержания окисляемых и непредельных соединений, pH среды);
2. Качественное и количественное определение индивидуальных веществ, мигрирующих из резин в модельные среды (компоненты резиновых смесей и продукты их превращения).
3. Идентификация остаточных мономеров каучука, а также продуктов, применяемых при синтезе и технологическом процессе переработки резины.
Проведенные детальные химические анализы могут выявить непригодность резин для применения по назначению. Критериями выбраковки служат содержание в модельных средах токсичных веществ в количествах, превышающих установленные санитарные нормативы ДКМ, а также одновременная миграция из резин несколько аллергеноопасных соединений на уровнях, близких к порогу раздражающего и сенсибилизирующего действия.
В ЭКСПЕРИМЕНТЕ НА ЖИВОТНЫХ
4.1. Способ исследования
Наиболее приемлемой моделью для изучения раздражающего действия резиновых изделий остаются морские свинки-альбиносы или свинки пестрой масти с белыми пятнами на боках.
Нанесение резины на кожу экспериментальных животных осуществляется с помощью фиксирующей бинтовой повязки. Животным прикрепляются кусочки резины площадью 6,5 см2, смоченные физиологическим раствором, на выстриженный участок боковой поверхности туловища.
4.2. Сроки исследования
Общее количество аппликаций зависит от назначения изделий. Изделия, предназначенные для кратковременного одноразового использования, испытываются в течение 5 дней (аггравация на индивидуальную и видовую чувствительность).
Изделия, имеющие длительный повторный контакт с кожей человека перчатки, напальчники, подкладные круги и т.д.), должны исследоваться в течение 20 рабочих дней. Это вызвано тем, что по нашим многолетним наблюдениям резиновые изделия проявляют раздражающее действие после 10 - 15 дневного контакта с кожей. Кроме того, указанные сроки позволяют проводить оценку функционального состояния кожи в динамике. Продолжительность ежедневного воздействия 6 часов.
4.3. Методы исследования
Объективными показателями раздражающего действия являются количественная оценка эритемы и отека кожи. Оценка эритемы в баллах проводится по колориметрической линейке С.В. Суворова и соавторов (1977). Для измерения отека кожи применяется обычно микрометр. Нами предлагается более удобный способ измерения отека с помощью толщиномера ТР-1-10. Толщиномер имеет плоские измерительные поверхности и шкалу часового типа, что создает определенные преимущества его перед микрометром. Проводить измерения может один человек. При работе с прибором следует левой рукой собрать кожу животного в складку и поместить между измерительными поверхностями прибора, который находится в правой руке. Показания читаются на шкале прибора. Рекомендуется проводить на каждом участке кожи по 3 измерения и вычислять среднюю величину. В процессе работы необходимо следить, чтобы внешний край измерительной поверхности прибора совпадал с краем кожной складки.
Наиболее значимыми с гигиенической точки зрения функциональными изменениями кожи, приводящими к развитию дерматитов, являются нарушения ее барьерной функции (pH, нейтрализующей способности, алкилрезистентности). В связи с этим в качестве обязательных показателей рекомендуется проводить измерение pH, устойчивости к щелочам или нейтрализующей способности кожи. Перечисленные методы подробно описаны в литературе (Иевлева Е.А., и соавт., 1977; Колпакова А.И., 1967 и др.). Приводим предложенную нами модификацию методики Burkchardta, изучения нейтрализующей способности кожи. Сущность метода заключается в способности кожи нейтрализовать вещества, обладающие щелочной реакцией. Методика основана на регистрации времени, за которое универсальная индикаторная бумага, пропитанная щелочным раствором, восстановит первоначальный цвет. На участок кожи, слегка увлажненный дистиллированной водой, накладывается отрезок универсальной pH - индикаторной бумаги длиной 1 см, смоченной 0,002Н раствором едкого натра (pH 8,0). По секундомеру отмечается время, за которое зеленый цвет бумаги восстанавливается до первоначального желтого (pH 6,0). В качестве контроля используется участок туловища животного, симметричный опытному. Обследование животных проводится каждые 6 дней.
Для математической обработки результатов исследований применяется общепринятый в токсикологии критерий Стьюдента-Фишера.
Критериями раздражающего действия резиновых изделий служат наличие воспалительной реакции кожи у 50% животных от 0,1 балла и выше (суммарно - по эритеме и отеку), усиление реакции кожи при продолжении воздействия, стойкость функциональных изменений кожи при отсутствии видимой реакции.
НА ЛЮДЯХ-ДОБРОВОЛЬЦАХ
В случае отрицательных результатов испытаний резиновых изделий на животных проводят исследования по оценке первичного раздражающего действия на людях-добровольцах. Для этого подбирают группы волонтеров (не менее 15 человек), включая лиц обоего пола и любого возраста (кроме детей), не имеющих кожных заболеваний в анамнезе.
Образцы резины поверхностью 2x2 см в количестве 3-х штук наносят на внутреннюю поверхность предплечья на расстояния 3 см друг от друга, закрепляя их медицинским лейкопластырем. Количество аппликаций (от 1 до 20) и продолжительностью ежедневной экспозиций (от 6 до 24 часов) колеблются в зависимости от назначения изделия. Реакцию (зуд, чувство жжения, краснота, шелушение, высыпания и пр.) оценивают по окончании ежедневной аппликации и до повторного нанесения образца на следующий день. Возникновение любых изменений на местах нанесения образца служит сигналом к прекращению испытаний.
Образец считается удовлетворительным, если незначительные изменения на коже могут быть отнесены к разряду случайных, то есть появляются на одном месте не более, чем у 2-х человек.
После наблюдений на людях-добровольцах проводятся более продолжительные клинические испытания (совместно с врачами-дерматологами) за лицами, пользующимися изделиями.
6.1. Способ исследования
Эксперимент проводится на морских свинках-альбиносах или с белыми пятнами на боках. Животным с помощью фиксирующей бинтовой повязки прикрепляют резиновые пластинки на правую сторону освобожденной от шерсти боковой поверхности туловища. Площадь резины составляет 6,5 см2. Перед нанесением резину смачивают дистиллированной водой или физиологическим раствором.
6.2. Сроки исследования
Проявление сенсибилизирующих свойств резиновых изделий наблюдается после длительного повторного контакта с организмом человека и связано с миграцией из них химических аллергенов. Относительно низкие уровни миграции химических соединений обусловливают, как правило, слабые сенсибилизирующие свойства резин. В связи с этим продолжительность периода сенсибилизации животных путем повторных накожных аппликаций резин должна составлять не менее 20 дней.
6.3. Методы исследования
В качестве показателей аллергенного действия рекомендуется применять общепринятые в промышленной аллергологии тесты: кожные и конъюнктивные провокационные пробы, реакции выявления клеточных и гуморальных антител in vitro (РСАЛ, РСЛЛ, РСМП) и другие. Подробное описание методик дано в методических указаниях "Постановка исследований по гигиеническому нормированию промышленных аллергенов в воздухе рабочей зоны". Невозможность полной расшифровки химического состава мигрирующего из резин комплекса соединений делает необходимым постановку разрешающего тестирования не только с исходными аллергенами, введенными в резиновую смесь, но и с резиной в целом. Кожные провокационные пробы ставятся путем нанесения резины на участок тела, симметричный подопытному, на 6 часов. В качестве антигенов при конъюнктивальном тестировании и в реакциях in vitro применяются водные вытяжки из резин. Вытяжки готовят на дистиллированной воде или физиологическом растворе в термостате при температуре 37 °C в течение суток. Подбор рабочей концентрации антигена осуществляется варьированием соотношения площади поверхности образца к объему экстрагента и обычно составляет от 5:1 до 8:1 см2/см3.
Для выявления местных аллергических реакций достаточно чувствительным и информативным является метод количественного подсчета тучных клеток (тканевых базофилов) в коже лабораторных животных. Для морфологических исследований кожу фиксируют в 12% формалине, заливают в парафин. Окрашивают срезы гематоксиллинэозином и толуидиновым синим полихромным, окрашивающим тучные клетки в малиновый цвет. На срезах подсчитывают среднее количество тучных клеток в поле зрения микроскопа (увеличение 900), учитывая при этом количество зрелых, незрелых, дегранулированных и опустошенных клеток. Функциональное состояние клеток определяют по индексу созревания  и индексу активности
и индексу активности 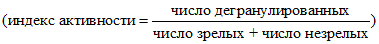 .
.
 и индексу активности
и индексу активности 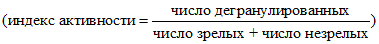 .
.В качестве контроля используют кожу контактных животных. Оптимальным сроком для взятия материала являются пятые сутки после начала аппликаций на кожу. Полученные результаты статистически обрабатываются с помощью критерия Стьюдента-Фишера.
Критериями сенсибилизирующего действия резины служат наличие единичных положительных реакций на антиген у подопытных животных.
МИГРИРУЮЩИХ ИЗ РЕЗИН
7.1. Предварительная оценка опасности вещества по литературным данным
Практически все химические соединения, внедряемые в промышленность, проходят первичную токсикологическую оценку, включающую сведения о их резорбтивном, раздражающем и сенсибилизирующем действии. Вещества, биологический характер действия которых не изучен, могут быть проанализированы по следующему плану: физико-химические свойства (липофильность, растворимость в воде, коэффициент распределения октанол-вода и масло-вода), ориентировочная оценка резорбтивных свойств с использованием расчетных формул (3), принадлежность к известным классам аллергенов (2).
Химические соединения, относящиеся к чрезвычайно опасным по классификации Г.И. Румянцева и соавторов (3) и к сверхкумулятивным по классификации Л.М. Медведя, не должны допускаться к применению в резинах, предназначенных для повторного контакта с кожей человека.
Нормирование по общетоксическому признаку химических соединений, относящихся к классу малоопасных и не кумулирующих в организме, не имеет практического значения.
7.2. Количественная оценка резорбтивного действия
Исследованию подлежат вещества, обладающие высокой степенью липидорастворимости, относящиеся к высоко- и умеренноопасным классам соединений, обладающие выраженными кумулятивными свойствами.
Порядок испытаний изложен в методических указаниях "Оценка воздействия вредных химических соединений на кожные покровы и обоснование предельно допустимых уровней загрязнений кожи" (1).
Оценка резорбтивного действия включает установление среднесмертельных уровней (DL50), среднеэффективного времени гибели животных (To150), порогов острого и хронического действия (Limac и Limch), зон острого и хронического действия (Zac и Zch), коэффициента кумуляции.
7.3. Оценка раздражающего действия
Исследованию подлежат вещества, способные вызывать раздражение кожи в концентрациях от 0,1% и ниже при однократном воздействии (1 класс).
7.3.1. Способ исследования
Вещество испытывается на 2 видах животных (как правило, морских свинках и кроликах) путем нанесения его в виде раствора или взвеси в дистиллированной воде на выстриженный участок боковой поверхности туловища.
7.3.2. Сроки исследования
Число повторных аппликаций не менее 20, что позволяет проследить за функциональным состоянием кожи в динамике, а также выявить накопление раздражающего эффекта.
7.3.3. Методы исследования
Для оценки раздражающего эффекта применяются количественные методы измерения интенсивности эритемы и отека кожи, изменения (функционального состояния кожи: pH, алкалирезистентности нейтрализующей способности.
Критериями для установления пороговой концентрации вещества (Limiz cut) служат наличие воспалительной реакции кожи у 50% животных от 0,1 балла и выше (суммарно по эритеме и отеку) при продолжении воздействия, стойкость функциональных изменений кожи при отсутствии видимой реакции.
7.4. Количественная оценка сенсибилизирующего действия
Исследованию подлежат вещества, относящиеся по химической структуре к известным классам аллергенов. Нормирование по аллергенному действию проводится для вещества, обладающего специфическим сенсибилизирующим эффектом, то есть когда порог общетоксического действия (Lim ch) выше порога аллергенного действия (Lim al). Поэтому начальная концентрация вещества должна быть ниже (Limch) не менее, чем в 2 раза, а каждая последующая уменьшается в 10 раз. Дальнейший ход исследований совпадает с изложенным в этапе 5 первого раздела настоящих "Методических указаний". Величина Limal cut определяется развитием сенсибилизации у отдельных животных, выявляемой положительными реакциями на антиген не менее, чем по двум тестам.
7.5. Установление допустимого количества миграции (ДКМ) химических веществ из резин
Гигиеническая стандартизация резин проводится в 2 этапа:
1. Установление ДКМ для изолированно взятых веществ (исходных или образующихся в резине).
2. Апробация норматива ДКМ на готовых резинах.
7.5.1. Установление ДКМ для химических соединений
Первый этап нормирования основан на результатах исследования биологической активности отдельно взятых химических соединений.
ДКМ для веществ, обладающих специфическим сенсибилизирующим действием, устанавливается, исходя из порога аллергенного действия (Lim al cut). Для нахождения Lim al необходимо определить содержание вещества, способного мигрировать из резин в вытяжку или модельную среду.
Расчет рабочей концентрации вещества, используемой в экспериментальных исследования, осуществляется по формуле:
где: K - рабочая концентрация вещества в %;
A - содержание вещества (г) в вытяжке (л);
S - поверхность резинового материала, используемого для приготовления 1 л модельных растворов (500 см2);
p - поверхность резины, используемая в эксперименте (6,5 см2)
100 - коэффициент для перевода концентрации из г/мл в %;
V - объем рабочего раствора для нанесения вещества на кожу (0,1 мл).
Если миграция ТМТД из резин колеблется в пределах 0,1 - 3,0 мг/л, в формулу вводят наибольшую величину (3,0 мг/л), т.е. используя вышеприведенную формулу, рабочая концентрация ТМТД составит 0,04%.
Наряду с расчетной в опыте используют дополнительно еще две концентрации: на порядок выше и ниже реально существующей (в нашем случае 0,4 и 0,004%).
Допустимое количество миграции (ДКМ) химических веществ (мг/л) рассчитывается по формуле:

где: S - поверхность резинового материала, используемого для приготовления модельных растворов (обычно 500 см2);
K - величина концентрации в %
P - поверхность резины, используемой в эксперименте (6,5 см2);
Jз - индекс запаса.
Величина коэффициента запаса колеблется от 3 до 5 в зависимости от выраженности сенсибилизирующих свойств вещества (в соответствии с методическими рекомендациями "Постановка исследования по гигиеническому нормированию промышленности аллергиков в воздухе рабочей зоны", ДКМ для химических веществ, обладающих специфическим раздражающим действием, устанавливается на уровне в 10 раз ниже порога раздражающего действия.
7.5.2. Гигиеническая регламентация резин (апробация ДКМ, установленного для химического соединения на готовых резинах)
Установленный для отдельно взятого химического вещества гигиенический норматив не всегда гарантирует безопасность резины. Вредное влияние резины на живой организм может быть неидентично с действием ингредиентов, из которых она изготовлена. Это обусловлено возможностью образования в процессе ее изготовления химических соединений, имеющих иную структуру и иные токсические свойства, чем вещества, вводимые в состав смеси. Имеет значение комбинированное действие веществ, придающее резине качественно новые биологические свойства. Наиболее активно взаимодействующими и образующими большинство продуктов превращения в резине являются каучуки, ускорители вулканизации и вулканизующие агенты. Кроме того, большинство ускорителей вулканизации относятся к классу аллергенов и гигиеническое нормирование их остаточных количеств в резине является первоочередной задачей.
Значительное число ингредиентов, доходящее до 20, колебания их процентного содержания в рецептуре затрудняют выявление причины биологической активности резин. Поэтому представляется целесообразным проверять установленные нормативы на модельных композициях. Модельная композиция должна отвечать следующим требованиям: содержать минимальное число компонентов, отвечать технологическим требованиям, предъявляемым к данному типу резин. Проводится сопоставление аллергенной активности модельной резины и изолированно взятого соединения, мигрирующего из резины и для которого ранее была установлена величина ДКМ.
В случаях совпадения эффекта гигиеническая регламентация резин данного типа осуществляется по нормативу, для этого соединения. Тип резины различается по виду каучука, ускорителя вулканизации и вулканизующих агентов. Добавление в рецептуру резин ингредиентов, не обладающих сенсибилизирующими свойствами и не подвергающихся превращению в процессе изготовления, не влияет на аллергенные свойства резин. К таким ингредиентам относятся наполнители, пластификаторы, пигменты.
При усилении аллергических свойств модельной композиции за счет комбинированного действия нескольких аллергенов необходима корректировка гигиенического норматива путем увеличения коэффициента запаса (в 10 и более раз).
В случаях образования в резине нового аллергена (при распаде ускорителя вулканизации, вулканизующего агента или при взаимодействии ускорителя вулканизации с каучуком) необходимо установление ДКМ для выявленного аллергена.
По окончании испытаний составляется гигиеническое заключение о возможности применения изделия по назначению, куда включаются сведения о составе резиновой смеси, результаты санитарно-химических и токсикологических исследований.