СПРАВКА
Источник публикации
"Бюллетень нормативных и методических документов Госсанэпиднадзора", выпуск 3 (89), сентябрь 2022
Примечание к документу
Название документа
"МР 4.2.0292-22. 4.2. Методы контроля. Биологические и микробиологические факторы. Фенотипическая идентификация бактерий рода Yersinia на основе ферментативной активности. Методические рекомендации"
(утв. Роспотребнадзором 30.06.2022)
"МР 4.2.0292-22. 4.2. Методы контроля. Биологические и микробиологические факторы. Фенотипическая идентификация бактерий рода Yersinia на основе ферментативной активности. Методические рекомендации"
(утв. Роспотребнадзором 30.06.2022)
Содержание
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный
санитарный врач
Российской Федерации
А.Ю.ПОПОВА
30 июня 2022 года
4.2. МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ
ФАКТОРЫ
ФЕНОТИПИЧЕСКАЯ ИДЕНТИФИКАЦИЯ БАКТЕРИЙ РОДА YERSINIA
НА ОСНОВЕ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
МР 4.2.0292-22
Методические рекомендации работаны ФБУН "Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера" Роспотребнадзора (Е.А. Воскресенская, Е.А. Богумильчик, Г.И. Кокорина).
1.1. Настоящие методические рекомендации (далее - МР) применяются при проведении исследований с целью идентификации и дифференциации бактерий рода Yersinia для повышения эффективности мониторинга циркулирующих штаммов иерсиний.
1.2. В МР охарактеризованы ферментативные свойства представителей 26 видов рода Yersinia, известных в настоящее время. Представлен комплекс биохимических тестов для определения метаболического профиля выделенных штаммов, использование которого позволяет осуществить внутриродовую и внутривидовую дифференциацию иерсиний, включая выявление патогенных и непатогенных представителей рода.
В МР представлен алгоритм применения коммерческих тестов и тестов с использованием сред и реактивов, приготовленных в лабораторных условиях, с описанием методик.
1.3. МР не распространяются на диагностические исследования по идентификации возбудителя чумы. Биохимические свойства Y. pestis приведены в данных МР для сравнения с остальными представителями рода Yersinia.
1.4. МР предназначены для органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, могут быть использованы научными и медицинскими организациями, осуществляющими исследования бактерий рода Yersinia.
2.1. Род Yersinia в соответствии с современной классификацией включает 26 видов, относится к самостоятельному семейству Yersiniaceae порядка Enterobacteriales: Y. aldovae, Y. aleksiciae, Y. alsatica, Y. artesiana, Y. bercovieri, Y. canariae, Y. enterocolitica, Y. entomophaga, Y. frederiksenii, Y. hibernica, Y. intermedia, Y. kristensenii, Y. massiliensis, Y. mollaretii, Y. nurmii, Y. pekkanenii, Y. pestis, Y. proxima, Y. pseudotuberculosis, Y. rochesterensis, Y. rohdei, Y. ruckeri, Y. similis, Y. thracica, Y. vastinensis, Y. wautersii [19, 40, 47, 48, 49].
2.2. Представители рода различаются по патогенному потенциалу. Три вида отнесены к патогенным для человека и животных: Y. pestis - возбудитель чумы, Y. pseudotuberculosis - возбудитель псевдотуберкулеза и Y. enterocolitica биотипа 1B, 2 - 5 - возбудители кишечного иерсиниоза.
Y. ruckeri вызывает иерсиниоз рыб семейства лососевых и некоторых других - энтерит, септическое заболевание, сопровождающееся покраснением рта ("болезнь красного рта", "enteric red mouth, ERM") [2, 50, 70]. Y. entomophaga является патогеном насекомых [33].
Остальные виды иерсиний в настоящее время рассматриваются как непатогенные для людей и животных. Среди них обширная группа близкородственных Y. enterocolitica (Y. enterocolitica-like) представителей рода Yersinia включает девять видов: Y. aldovae, Y. aleksiciae, Y. bercovieri, Y. frederiksenii, Y. intermedia, Y. kristensenii, Y. massiliensis, Y. mollaretii, Y. rohdei [59, 63]. Данные виды широко распространены в природе, их изолируют из различных объектов внешней среды. Штаммы Y. enterocolitica-like выделяют из испражнений больных с гастроинтестинальными проявлениями при отсутствии других возбудителей кишечных инфекций и факторов неинфекционной природы, вызывающих расстройство кишечника, основным проявлением которого является диарея, а также из мочи и крови [12, 41, 66]. У некоторых представителей данной группы также выявлены отдельные факторы патогенности [3, 34, 35, 52].
Вид Y wautersii вместе с патогенными видами Y. pseudotuberculosis, Y. pestis и непатогенным Y. similis образуют группу, называемую Y. pseudotuberculosis complex [39, 55]. Выделение штаммов Y. wautersii от человека, обнаружение у некоторых из них хромосомных и плазмидных генов вирулентности, свидетельствуют о возможном патогенном потенциале данного вида иерсиний.
2.3. Определение таксономической принадлежности микроорганизма по фенотипическим признакам является комплексным исследованием, включающим выявление ферментативного профиля, изучение культуральных, морфологических, тинкториальных, физиологических, хемотаксономических, антигенных свойств.
2.4. Разнообразие представителей рода Yersinia и гетерогенность отдельных видов осложняет фенотипическую идентификацию иерсиний по совокупности биохимических свойств, особенно видов, близкородственных Y. enterocolitica. Представителей данных видов, являющихся непатогенными, в некоторых случаях некорректно идентифицируют как Y. enterocolitica, возбудителя кишечного иерсиниоза. Существуют проблемы при определении биотипа Y. enterocolitica, что необходимо для дифференциации патогенных (биотипы 1B, 2 - 5) и непатогенных (биотип 1A) представителей вида.
2.5. Характеристика ферментативных свойств может быть недостаточной для корректной дифференциации видов (например, когда различие основывается только на одном биохимическом признаке или при получении атипичного метаболического профиля). Для достоверной идентификации используются генотипические методы исследования (анализ полного генома, мультилокусное сиквенс-типирование корового генома и др.) [56, 40]. Виды иерсиний Y. alsatica, Y. artesiana, Y. canariae, Y. hibernica, Y. proxima, Y. rochesterensis, Y. thracica, Y. vastinensis недостаточно охарактеризованы вследствие изучения единичных штаммов, что не позволяет рассматривать данные об отдельных метаболических свойствах как объективные.
2.6. В качестве метода фенотипической идентификации иерсиний может быть использован метод масс-спектрометрического анализа, сочетающий матрично-активированную лазерную десорбцию/ионизацию (англ. Matrix Assisted Laser Desorption/Ionization) с времяпролетным разделением (англ. Time of Flight) ионов (далее - MALDI-ToF MS). Метод MALDI-ToF MS позволяет корректно установить принадлежность к роду Yersinia и идентифицировать до вида штаммы Y. enterocolitica и Y. pseudotuberculosis [7]. Ограничением в применении MALDI-ToF MS является недостоверная идентификация других видов иерсиний, что обусловлено высокой степенью геномного сходства и недостаточным количеством в таксономических базах эталонных профилей масс-спектров.
2.7. Перечень оборудования, химических реактивов, расходных материалов и средств представлен в приложении 1 к настоящим МР.
рода Yersinia
Признаки рода Yersinia
3.1. Фенотипические характеристики иерсиний, включая ферментативную активность, во многих случаях зависят от температуры, и ряд ферментов активнее вырабатывается штаммами, инкубированными при плюс 25 - 29 °C, чем при плюс 35 - 37 °C [23].
3.2. Иерсинии обладают каталазной активностью, цитохромоксидазная активность (тест на оксидазу) отсутствует.
3.3. К родовым биохимическим признакам иерсиний относится ферментация D-маннозы и D-маннитола. За счет ферментации D-маннитола колонии иерсиний приобретают характерный вид на CIN-агаре (колонии с красным центром, см. пункты 4.10, 4.11). Ферментация D-адонитола и дульцитола у бактерий рода Yersinia отсутствует. Иерсинии ферментируют D-глюкозу до кислоты без газа, что является постоянной характеристикой для Y. pestis и Y. pseudotuberculosis, но у некоторых штаммов других видов может наблюдаться небольшое газообразование. Ферментация других углеводов определяется видовой принадлежностью.
Некоторые представители видов Y. entomophaga, Y. frederiksenii, Y. intermedia, Y. rohdei, Y. canariae, Y. rochesterensis, Y. artesiana, Y. proxima, Y. vastinensis могут ферментировать лактозу [23, 33, 46, 60].
3.4. Y. pseudotuberculosis, Y. enterocolitica и большинство других видов иерсиний гидролизуют мочевину, но наличие уреазы не является родовым признаком, так как штаммы Y. pestis, Y. nurmii, Y. ruckeri, Y. entomophaga не обладают уреазной активностью.
3.5. Иерсинии не утилизируют фенилаланин, триптофан и аргинин. Лизиндекарбоксилазу вырабатывают штаммы Y. ruckeri и некоторые штаммы Y. aleksiciae [61]. Остальные представители рода не декарбоксилируют лизин. Наличие орнитиндекарбоксилазной активности определяется видовой принадлежностью.
3.6. Иерсинии не вырабатывают сероводород.
3.7. Для большинства иерсиний характерна подвижность при температуре инкубации (22 +/- 2) °C и потеря подвижности при температуре роста выше плюс 30 °C, за исключением Y. entomophaga, которые подвижны независимо от температуры инкубации [33]. Некоторые представители Y. ruckeri являются неподвижными при (22 +/- 2) °C [25].
Основные свойства иерсиний различных видов
3.8. По биохимическим свойствам представители вида Y. pseudotuberculosis однородны. Штаммы Y. pseudotuberculosis гидролизуют мочевину, эскулин, ферментируют L-рамнозу, D-ксилозу, мальтозу, трегалозу (приложение 2 к настоящим МР); не ферментируют лактозу, сахарозу, D-сорбитол, раффинозу; не образуют индол, не декарбоксилируют орнитин, не утилизируют цитрат на среде Симмонса [55]. Бактерии данного вида проявляют подвижность в 0,3% полужидком агаре при температуре (22 +/- 2) °C, но неподвижны при температуре (37 +/- 1) °C [9]. Образование ацетоина (реакция Фогеса-Проскауэра) отсутствует при температурах (26 +/- 2) °C и (37 +/- 1) °C.
Основными признаками, которые следует учитывать при идентификации иерсиний вида Y. pseudotuberculosis, являются:
- наличие уреазной активности. В тесте на гидролиз мочевины в жидкой среде у штаммов Y. pseudotuberculosis уже в первые 1 - 2 часа может наблюдаться положительная реакция;
- отсутствие ферментации сахарозы. В табл. 1 перечислены биохимические признаки, по которым дифференцируют иерсинии, не расщепляющие сахарозу. По наличию ферментации L-рамнозы, отсутствию декарбоксилирования орнитина и отрицательной реакции Фогеса-Проскауэра устанавливают принадлежность к виду Y. pseudotuberculosis.
Таблица 1
не ферментирующих сахарозу <1>
--------------------------------
<1> Биохимические свойства Y. aleksiciae, Y. hibernica и Y. thracica не включены в таблицу, так как штаммы данных видов имеют сходный метаболический профиль с Y. kristensenii (приложение 2 к настоящим МР); биохимические свойства Y. pestis не приведены (пункт 1.3).
Субстрат, метаболит <2> Вид | Сахароза | Ацетоин | Мочевина | Орнитин | L-Рамноза | D-Сорбитол | D-Ксилоза | Трегалоза |
Y. aldovae | (-) | + | + | + | + | + | + | + |
Y. pseudotuberculosis | - | - | + | - | + | - | + | + |
Y. similis | - | - | + | - | + | - | + | + |
Y. wautersii | - | - | + | - | + | - | + | + |
Y. pekkanenii | - | - | + | - | - | - | + | + |
Y. kristensenii | - | - | + | + | - | + | + | + |
Y. ruckeri | - | (-) | - | + | - | B | - | + |
Примечание: "+" - положительная реакция у 90 - 100% штаммов; "-" - положительная реакция у 0 - 10% штаммов; "(-)" - положительная реакция у 11 - 25% штаммов; "B" - положительная реакция у 26 - 75% штаммов. Условия инкубации: (26 +/- 2) °C 24 - 48 ч. | ||||||||
--------------------------------
<2> Примечание: здесь и далее в графе "Субстрат, метаболит" перечислены названия субстратов, которые подвергаются ферментативному расщеплению (например, сахароза, мочевина и т.д.), либо метаболиты (продукты), образующиеся в результате биохимических реакций (например, ацетоин, индол и др.).
Для представителей вида Y. pseudotuberculosis установлена вариабельность ферментации мелибиозы: большинство штаммов ферментируют мелибиозу, но есть не ферментирующие мелибиозу штаммы [28, 39, 55].
3.9. Представители вида Y. similis имеют сходный с Y. pseudotuberculosis ферментативный профиль: гидролизуют мочевину, эскулин, ферментируют L-рамнозу, D-ксилозу, трегалозу; не расщепляют орнитин, лизин, сахарозу, раффинозу, D-сорбитол, L-сорбозу, цитрат натрия, не образуют индол и ацетоин [62, 63]. Отличительным признаком является наличие у штаммов Y. similis пиразинамидазной активности и отсутствие способности ферментировать мелибиозу [55].
Дополнительными методами дифференциации штаммов непатогенного вида Y. similis и патогенного Y. pseudotuberculosis являются молекулярно-генетические: секвенирование гена 16S pРНК, мультилокусное сиквенс-типирование, ПЦР [4, 28, 55].
3.10. Вид Y. wautersii выделен из вида Y. pseudotuberculosis [55]. Штаммы Y. wautersii дифференцируют от Y. pseudotuberculosis и Y. similis по способности ферментировать раффинозу. Пиразинамидазной активностью штаммы Y. wautersii не обладают, как и Y. pseudotuberculosis, в отличие от гидролизующих пиразинамид Y. similis. Биохимическая активность представлена в табл. 1 и приложении 2 к настоящим МР.
3.11. Виды Y. wautersii, Y. pseudotuberculosis, Y. pestis и Y. similis входят в Y. pseudotuberculosis complex на основании выраженного генетического родства [39, 55]. Штаммы Y. wautersii, Y. pseudotuberculosis и Y. similis обладают близкими метаболическими свойствами, их различают по пиразинамидазной активности и ферментации раффинозы и мелибиозы [55].
3.12. По биохимическим свойствам представители вида Y. enterocolitica подразделяют на 6 биотипов: 1A, 1B, 2, 3, 4, 5 [74]. Штаммы Y. enterocolitica биотипов 1B, 2 - 5 патогенны для человека и животных, биотипа 1A - непатогенны.
Биохимические свойства, характерные для Y. enterocolitica: наличие уреазы, орнитиндекарбоксилазы, ферментации сахарозы, мальтозы, L-арабинозы, образования ацетоина при (26 +/- 2) °C; отсутствие лизиндекарбоксилазы, ферментации L-рамнозы, раффинозы, мелибиозы, 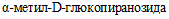 (
(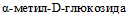 ) (табл. 2 и приложение 2 к настоящим МР).
) (табл. 2 и приложение 2 к настоящим МР).
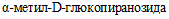 (
(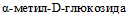 ) (табл. 2 и приложение 2 к настоящим МР).
) (табл. 2 и приложение 2 к настоящим МР).Патогенные и непатогенные Y. enterocolitica дифференцируют по способности к ферментации салицина и гидролизу эскулина. Непатогенные представители биотипа 1A утилизируют салицин и эскулин. Для патогенных Y. enterocolitica (биотипы 1B, 2, 3, 4, 5) характерно отсутствие ферментации салицина и гидролиза эскулина. Фермент 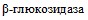 , обеспечивающий утилизацию эскулина и салицина, расщепляет также хромогенные субстраты, которые используются в некоторых хромогенных средах для выделения Y. enterocolitica [37].
, обеспечивающий утилизацию эскулина и салицина, расщепляет также хромогенные субстраты, которые используются в некоторых хромогенных средах для выделения Y. enterocolitica [37].
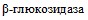 , обеспечивающий утилизацию эскулина и салицина, расщепляет также хромогенные субстраты, которые используются в некоторых хромогенных средах для выделения Y. enterocolitica [37].
, обеспечивающий утилизацию эскулина и салицина, расщепляет также хромогенные субстраты, которые используются в некоторых хромогенных средах для выделения Y. enterocolitica [37].Патогенные и непатогенные Y. enterocolitica дифференцируют по гидролизу пиразинамида [36] (пункты 5.47 - 5.49). Непатогенные Y. enterocolitica биотипа 1A обладают пиразинамидазой. Для патогенных Y. enterocolitica биотипов 1B, 2, 3, 4, 5 характерно отсутствие пиразинамидазной активности.
Патогенных представителей биотипа 1B и остальных патогенных Y. enterocolitica (биотипы 2 - 5) различают на среде с Твин 80 по наличию твинэстеразы (пункты 5.35 - 5.37). Данный фермент есть у патогенных Y. enterocolitica биотипа 1B и у непатогенных Y. enterocolitica биотипа 1A (которые различают по ферментации салицина и эскулина), но отсутствует у штаммов биотипов 2 - 5. По определению способности к индолообразованию, ферментации D-ксилозы, трегалозы, L-сорбозы дифференцируют представителей биотипов 2, 3, 4 и 5 (табл. 2).
Таблица 2
Y. enterocolitica, Y. bercovieri и Y. mollaretii
Субстрат, метаболит: Вид биотип: | Мочевина | Сахароза | Орнитин | Ацетоин (26 +/- 2) °C | Пиразинамид | Эскулин | Салицин | Твин-80 | Индол | D-Ксилоза | Трегалоза | L-Сорбоза | L-Фукоза | |
Y. enterocolitica, биотип | + | + | + | + | + | (+) | + | + | + | + | + | + | + | |
+ | + | + | + | - | - | - | + | + | + | + | + | - | ||
+ | + | + | + | - | - | - | - | B | + | + | + | - | ||
+ | + | + | + | - | - | - | - | - | + | + | + | - | ||
+ | + | + | + | - | - | - | - | - | - | + | + | - | ||
+ | (+) | (+) | (+) | - | - | - | - | - | B | - | - | - | ||
Y. mollaretii | + | + | + | - | + | (-) | (-) | - | - | + | + | + | - | |
Y. bercovieri | + | + | + | - | + | B | (-) | - | - | + | + | - | + | |
Примечание: "+" - положительная реакция у 90 - 100% штаммов; "-" - положительная реакция у 0 - 10% штаммов; "(+)" - положительная реакция у 76 - 89% штаммов; "(-)" - положительная реакция у 11 - 25% штаммов; "B" - положительная реакция у 26 - 75% штаммов. Условия инкубации: (26 +/- 2) °C 24 - 48 ч. | ||||||||||||||
Характеристика биохимической активности штаммов, отнесенных к различным биотипам Y. enterocolitica:
- штаммы Y. enterocolitica биотипа 1A ферментируют салицин, трегалозу, L-сорбозу, D-ксилозу, образуют индол, гидролизуют эскулин и Твин 80;
- штаммы Y. enterocolitica биотипа 1B ферментируют трегалозу, L-сорбозу, D-ксилозу, образуют индол, гидролизуют Твин 80, не ферментируют салицин, не гидролизуют эскулин;
- штаммы Y. enterocolitica биотипа 2 ферментируют трегалозу, L-сорбозу, D-ксилозу, образуют индол (вариабельно), не гидролизуют Твин 80, эскулин, не ферментируют салицин;
- штаммы Y. enterocolitica биотипа 3 ферментируют трегалозу, L-сорбозу, D-ксилозу, не образуют индол, не гидролизуют Твин 80, эскулин, не ферментируют салицин;
- штаммы Y. enterocolitica биотипа 4 ферментируют трегалозу, L-сорбозу, не образуют индол, не гидролизуют Твин 80, эскулин, не ферментируют D-ксилозу и салицин;
- штаммы Y. enterocolitica биотипа 5 не образуют индол, не гидролизуют Твин 80, эскулин, не ферментируют трегалозу, L-сорбозу, салицин, вариабельно ферментируют D-ксилозу.
3.13. В настоящее время близкородственные Y. enterocolitica (Y. enterocolitica-like виды) представители рода Yersinia отнесены к непатогенным микроорганизмам и включают 9 видов (Y. aldovae, Y. aleksiciae, Y. bercovieri, Y. frederiksenii, Y. intermedia, Y. kristensenii, Y. massiliensis, Y. mollaretii, Y. rohdei) [59, 63].
3.14. Иерсинии видов Y. bercovieri и Y. mollaretii ранее являлись представителями Y. enterocolitica биогрупп 3A и 3B соответственно [73]. По биохимическим свойствам иерсинии видов Y. bercovieri и Y. mollaretii похожи на патогенных представителей Y. enterocolitica 2 - 4 биотипов. Биохимическая активность штаммов Y. bercovieri и Y. mollaretii характеризуется наличием уреазы, орнитиндекарбоксилазы, ферментацией сахарозы, мальтозы. Штаммы данных видов не образуют индол, не утилизируют цитрат натрия, не ферментируют салицин (за исключением некоторых штаммов), L-рамнозу, мелибиозу, раффинозу, 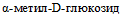 , не гидролизуют Твин 80, не вырабатывают ацетоин при температуре (26 +/- 2) °C (приложение 2 к настоящим МР). Последний признак является основным при дифференциации Y. bercovieri и Y. mollaretii от патогенных Y. enterocolitica (п. 5.29 - 5.31). По ферментации L-сорбозы и L-фукозы различают штаммы Y. bercovieri и Y. mollaretii: наличие ферментации L-сорбозы отмечают у Y. mollaretii, L-фукозу ферментируют Y. bercovieri. Видовые биохимические признаки Y. bercovieri, Y. mollaretii и Y. enterocolitica представлены в табл. 2.
, не гидролизуют Твин 80, не вырабатывают ацетоин при температуре (26 +/- 2) °C (приложение 2 к настоящим МР). Последний признак является основным при дифференциации Y. bercovieri и Y. mollaretii от патогенных Y. enterocolitica (п. 5.29 - 5.31). По ферментации L-сорбозы и L-фукозы различают штаммы Y. bercovieri и Y. mollaretii: наличие ферментации L-сорбозы отмечают у Y. mollaretii, L-фукозу ферментируют Y. bercovieri. Видовые биохимические признаки Y. bercovieri, Y. mollaretii и Y. enterocolitica представлены в табл. 2.
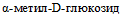 , не гидролизуют Твин 80, не вырабатывают ацетоин при температуре (26 +/- 2) °C (приложение 2 к настоящим МР). Последний признак является основным при дифференциации Y. bercovieri и Y. mollaretii от патогенных Y. enterocolitica (п. 5.29 - 5.31). По ферментации L-сорбозы и L-фукозы различают штаммы Y. bercovieri и Y. mollaretii: наличие ферментации L-сорбозы отмечают у Y. mollaretii, L-фукозу ферментируют Y. bercovieri. Видовые биохимические признаки Y. bercovieri, Y. mollaretii и Y. enterocolitica представлены в табл. 2.
, не гидролизуют Твин 80, не вырабатывают ацетоин при температуре (26 +/- 2) °C (приложение 2 к настоящим МР). Последний признак является основным при дифференциации Y. bercovieri и Y. mollaretii от патогенных Y. enterocolitica (п. 5.29 - 5.31). По ферментации L-сорбозы и L-фукозы различают штаммы Y. bercovieri и Y. mollaretii: наличие ферментации L-сорбозы отмечают у Y. mollaretii, L-фукозу ферментируют Y. bercovieri. Видовые биохимические признаки Y. bercovieri, Y. mollaretii и Y. enterocolitica представлены в табл. 2.3.15. Представители вида Y. aldovae по ферментативной активности схожи со многими видами иерсиний. Штаммы вида Y. aldovae обладают уреазной активностью, декарбоксилируют орнитин, вырабатывают ацетоин (при температуре (26 +/- 2) °C), ферментируют L-рамнозу, D-сорбитол, D-ксилозу, трегалозу; не образуют индол, не утилизируют лизин, раффинозу, мелибиозу, L-сорбозу, 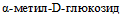 , мальтозу. Большинство штаммов Y. aldovae не ферментируют сахарозу [40, 54, 22, 23, 24, 44, 62, 64]. В этом случае Y. aldovae дифференцируют от иерсиний видов Y. pseudotuberculosis, Y. similis и Y. wautersii по способности утилизировать орнитин и вырабатывать ацетоин (табл. 1). Штаммы Y. aldovae, ферментирующие сахарозу, дифференцируют от иерсиний видов Y. frederiksenii и Y. intermedia по отсутствию индолообразования. Биохимическая активность иерсиний вида Y. aldovae представлена в приложении 2 к настоящим МР.
, мальтозу. Большинство штаммов Y. aldovae не ферментируют сахарозу [40, 54, 22, 23, 24, 44, 62, 64]. В этом случае Y. aldovae дифференцируют от иерсиний видов Y. pseudotuberculosis, Y. similis и Y. wautersii по способности утилизировать орнитин и вырабатывать ацетоин (табл. 1). Штаммы Y. aldovae, ферментирующие сахарозу, дифференцируют от иерсиний видов Y. frederiksenii и Y. intermedia по отсутствию индолообразования. Биохимическая активность иерсиний вида Y. aldovae представлена в приложении 2 к настоящим МР.
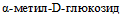 , мальтозу. Большинство штаммов Y. aldovae не ферментируют сахарозу [40, 54, 22, 23, 24, 44, 62, 64]. В этом случае Y. aldovae дифференцируют от иерсиний видов Y. pseudotuberculosis, Y. similis и Y. wautersii по способности утилизировать орнитин и вырабатывать ацетоин (табл. 1). Штаммы Y. aldovae, ферментирующие сахарозу, дифференцируют от иерсиний видов Y. frederiksenii и Y. intermedia по отсутствию индолообразования. Биохимическая активность иерсиний вида Y. aldovae представлена в приложении 2 к настоящим МР.
, мальтозу. Большинство штаммов Y. aldovae не ферментируют сахарозу [40, 54, 22, 23, 24, 44, 62, 64]. В этом случае Y. aldovae дифференцируют от иерсиний видов Y. pseudotuberculosis, Y. similis и Y. wautersii по способности утилизировать орнитин и вырабатывать ацетоин (табл. 1). Штаммы Y. aldovae, ферментирующие сахарозу, дифференцируют от иерсиний видов Y. frederiksenii и Y. intermedia по отсутствию индолообразования. Биохимическая активность иерсиний вида Y. aldovae представлена в приложении 2 к настоящим МР.3.16. У штаммов вида Y. rohdei отмечают замедленный гидролиз мочевины - от 2 до 7 суток [20, 23, 65]. Большинство штаммов декарбоксилируют орнитин, ферментируют мальтозу, утилизация цитрата натрия вариабельная. Иерсинии данного вида ферментируют сахарозу, D-сорбитол, трегалозу, D-ксилозу; не образуют индол, ацетоин, не гидролизуют эскулин, не ферментируют салицин. По ферментации мелибиозы и раффинозы выделяют 2 биотипа Y. rohdei: к биотипу 1 относят штаммы, ферментирующие раффинозу и мелибиозу, к биотипу 2 - не ферментирующие оба углевода [20]. Ключевыми биохимическими свойствами для видовой идентификации Y. rohdei являются отсутствие образования индола и ацетоина. Биохимические характеристики вида представлены в приложении 2 к настоящим МР.
3.17. Вид Y. intermedia является наиболее гетерогенным по биохимическим свойствам среди видов близкородственных Y. enterocolitica и включает 10 биотипов [42]. Представители вида Y. intermedia по сравнению с иерсиниями других видов метаболически наиболее активны, для них характерны следующие признаки: гидролиз мочевины, декарбоксилирование орнитина, ферментация сахарозы, салицина, L-сорбозы, D-сорбитола, трегалозы, D-ксилозы, мальтозы, гидролиз эскулина, гидролиз Твин 80 (вариабельно), образование индола и ацетоина (при (26 +/- 2) °C). Штаммы Y. intermedia вариабельно ферментируют L-рамнозу, раффинозу, мелибиозу, 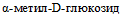 и утилизируют цитрат; разделение Y. intermedia на 10 биохимических вариантов обусловлено различными комбинациями данных свойств (табл. 3). Определение биотипов является необходимым для корректной дифференциации вида Y. intermedia от других видов иерсиний.
и утилизируют цитрат; разделение Y. intermedia на 10 биохимических вариантов обусловлено различными комбинациями данных свойств (табл. 3). Определение биотипов является необходимым для корректной дифференциации вида Y. intermedia от других видов иерсиний.
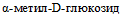 и утилизируют цитрат; разделение Y. intermedia на 10 биохимических вариантов обусловлено различными комбинациями данных свойств (табл. 3). Определение биотипов является необходимым для корректной дифференциации вида Y. intermedia от других видов иерсиний.
и утилизируют цитрат; разделение Y. intermedia на 10 биохимических вариантов обусловлено различными комбинациями данных свойств (табл. 3). Определение биотипов является необходимым для корректной дифференциации вида Y. intermedia от других видов иерсиний.Таблица 3
Y. frederiksenii, Y. intermedia, Y. massiliensis
и Y. enterocolitica биотипа 1A
Субстрат, метаболит: Вид биотип: | Ацетоин | Твин 80 | L-Рамноза | Мелибиоза | Раффиноза | 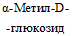 | Цитрат | |
Y. enterocolitica 1A | + | + | - | - | - | - | - | |
Y. massiliensis | - | - | - | - | - | - | B | |
Y. frederiksenii | (+) | B | + | - | - | - | B | |
Y. intermedia, биотип | 1 | + | B | + | + | + | + | + |
2 | + | B | + | + | + | + | - | |
3 | + | B | + | + | + | - | + | |
4 | + | B | - | + | + | + | B | |
5 | + | B | - | + | + | - | B | |
6 | + | B | + | + | - | + | - | |
7 | + | B | + | + | - | - | - | |
8 | + | B | + | - | + | + | + | |
9 | + | B | + | - | - | + | + | |
10 | + | B | + | - | - | + | - | |
Примечание: "+"- положительная реакция у 90 - 100% штаммов; "-" - положительная реакция у 0 - 10% штаммов; "(+)" - положительная реакция у 76 - 89% штаммов; "B" - положительная реакция у 26 - 75% штаммов. | ||||||||
3.18. Представители вида Y. frederiksenii, в отличие от Y. intermedia, не ферментируют мелибиозу и раффинозу. По отношению к другим субстратам иерсинии данного вида также активны: вырабатывают уреазу, орнитиндекарбоксилазу, ферментируют сахарозу, L-рамнозу, салицин, мальтозу, D-ксилозу, трегалозу, D-сорбитол, L-сорбозу, образуют индол, ацетоин, гидролизуют эскулин, вариабельно утилизируют цитрат натрия и Твин 80.
Биохимические свойства Y. frederiksenii представлены в приложении 3 к настоящим МР.
Для корректной идентификации и дифференциации представителей Y. frederiksenii, Y. intermedia и Y. enterocolitica выполняют ряд необходимых тестов [1]. Патогенные Y. enterocolitica биотипов 1B, 2 - 5 не утилизируют салицин и эскулин, в отличие от Y. intermedia, Y. frederiksenii и непатогенных Y. enterocolitica биотипа 1A. Для видовой дифференциации Y. intermedia, Y. frederiksenii и непатогенных Y. enterocolitica биотипа 1A используют комплекс тестов, выявляющих ферментацию L-рамнозы, раффинозы, мелибиозы, 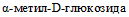 и способность утилизировать цитрат натрия (табл. 3).
и способность утилизировать цитрат натрия (табл. 3).
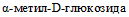 и способность утилизировать цитрат натрия (табл. 3).
и способность утилизировать цитрат натрия (табл. 3).3.19. Штаммы, отнесенные к виду Y. massiliensis, по биохимическим характеристикам близки к представителям Y. frederiksenii, Y. intermedia и непатогенным Y. enterocolitica биотипа 1A: они гидролизуют мочевину, вырабатывают индол, декарбоксилируют орнитин, ферментируют сахарозу, салицин, D-ксилозу, трегалозу, мальтозу, D-сорбитол (приложение 2 к настоящим МР). У штаммов Y. massiliensis в течение первых 48 ч отмечают отрицательную реакцию Фогеса-Проскауэра при (26 +/- 2) °C, после 72 ч инкубации наблюдается слабоположительная продукция ацетоина [43]. Y. massiliensis не ферментируют L-рамнозу, раффинозу, мелибиозу, не гидролизуют Твин 80. В отношении лизиндекарбоксилазы, аргининдигидролазы и триптофандезаминазы разные авторы отмечают как наличие, так и отсутствие у штаммов Y. massiliensis данных ферментов [40, 43, 60]. Биохимические свойства представителей видов Y. massiliensis, Y. frederiksenii, Y. intermedia и Y. enterocolitica биотипа 1A приведены в табл. 3 и приложении 2 к настоящим МР.
3.20. Основные ферментативные характеристики при идентификации представителей вида Y. kristensenii: наличие уреазной и орнитиндекарбоксилазной активности и отсутствие ферментации сахарозы и образования ацетоина при (26 +/- 2) °C. Штаммы Y. kristensenii не ферментируют L-рамнозу, мелибиозу, раффинозу, 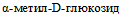 , салицин; ферментируют мальтозу, трегалозу, D-сорбитол, L-сорбозу, D-ксилозу; не утилизируют цитрат натрия, эскулин; образование индола и гидролиз Твин 80 вариабельны. Ферментативные характеристики приведены в табл. 1 и приложении 2 к настоящим МР.
, салицин; ферментируют мальтозу, трегалозу, D-сорбитол, L-сорбозу, D-ксилозу; не утилизируют цитрат натрия, эскулин; образование индола и гидролиз Твин 80 вариабельны. Ферментативные характеристики приведены в табл. 1 и приложении 2 к настоящим МР.
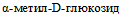 , салицин; ферментируют мальтозу, трегалозу, D-сорбитол, L-сорбозу, D-ксилозу; не утилизируют цитрат натрия, эскулин; образование индола и гидролиз Твин 80 вариабельны. Ферментативные характеристики приведены в табл. 1 и приложении 2 к настоящим МР.
, салицин; ферментируют мальтозу, трегалозу, D-сорбитол, L-сорбозу, D-ксилозу; не утилизируют цитрат натрия, эскулин; образование индола и гидролиз Твин 80 вариабельны. Ферментативные характеристики приведены в табл. 1 и приложении 2 к настоящим МР.3.21. Отмечают выраженное сходство метаболических свойств иерсиний вида Y. aleksiciae и Y. kristensenii, при этом существует внутривидовое различие Y. aleksiciae по способности декарбоксилировать лизин [40, 44, 61]. Биохимические свойства видов Y. aleksiciae и Y. kristensenii приведены в табл. 1 и приложении 2 к настоящим МР. Дифференцировать виды Y. aleksiciae и Y. kristensenii только на основании лизиндекарбоксилазной активности некорректно, а другими биохимическими тестами невозможно. Для дифференциации данных видов применяют масс-спектрометрический метод исследования.
3.22. Вид Y. rochesterensis выделен из вида Y. kristensenii по результатам полногеномного анализа [49]. Отмечают сходство ферментативной активности штаммов данных видов. Y. rochesterensis характеризуются наличием уреазной и орнитиндекарбоксилазной активности, отсутствием лизиндекарбоксилазы, способностью к ферментации D-сорбитола, D-ксилозы, мальтозы, трегалозы, отсутствием образования ацетоина и ферментации сахарозы, L-рамнозы, мелибиозы, раффинозы (приложение 2 к настоящим МР). Большинство штаммов вида Y. rochesterensis образуют индол, липазная и пиразинамидазная активность вариабельна, некоторые штаммы Y. rochesterensis утилизируют цитрат натрия [24, 40, 49].
3.23. Ферментативные свойства иерсиний видов Y. hibernica и Y. kristensenii похожи: для них характерно отсутствие ферментации сахарозы, наличие уреазной и орнитиндекарбоксилазной активности. Y. hibernica утилизируют D-сорбитол, D-ксилозу, не утилизируют цитрат натрия, лизин, L-рамнозу, мелибиозу, не образуют ацетоин и индол (табл. 1, приложение 2 к настоящим МР) [40, 47].
3.24. Штамм, отнесенный к виду Y. canariae, по биохимической активности наиболее близок Y. enterocolitica и характеризуется следующими метаболическими свойствами: гидролизует мочевину, образует индол, ферментирует сахарозу, трегалозу, D-сорбитол и L-арабинозу, не образует ацетоин, не утилизирует орнитин, лизин, L-рамнозу, мелибиозу, цитрат натрия [48] (приложение 2 к настоящим МР). Данный штамм Y. canariae дифференцируют от иерсиний вида Y. enterocolitica по отсутствию образования ацетоина (при (26 +/- 2) °C) и орнитиндекарбоксилазной активности; от иерсиний видов Y. mollaretii и Y. bercovieri - по образованию индола [48].
3.25. По результатам углубленного исследования генома внутри видов Y. kristensenii, Y. enterocolitica и Y. frederiksenii выявлено и охарактеризовано несколько новых видов: Y. thracica (выделен из вида Y. kristensenii), Y. artesiana и Y. proxima (выделены из вида Y. enterocolitica), Y. vastinensis и Y. alsatica (выделены из вида Y. frederiksenii) [40]. Известные ферментативные характеристики штаммов данных видов приведены в приложении 2 к настоящим МР.
3.26. Отличительной характеристикой представителей вида Y. ruckeri от других иерсиний является отсутствие гидролиза мочевины. Дифференцирующими видовыми признаками Y. ruckeri является отсутствие ферментации сахарозы и индолообразования, наличие орнитиндекарбоксилазной активности и у большинства штаммов лизиндекарбоксилазной активности.
По метаболическим свойствам штаммы Y. ruckeri разделены на 2 биотипа: отнесенные к биотипу 1 подвижны и гидролизуют Твин 80, представители биотипа 2 неподвижны и не гидролизуют Твин 80 [25].
Другие биохимические характеристики штаммов вида Y. ruckeri: ферментируют мальтозу и трегалозу, не ферментируют D-ксилозу, салицин, L-рамнозу, мелибиозу, раффинозу, 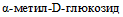 , L-сорбозу. Некоторые штаммы иерсиний данного вида вырабатывают ацетоин (при температуре (26 +/- 2) °C), утилизация D-сорбитола вариабельная (приложение 2 к настоящим МР). Многие штаммы утилизируют цитрат натрия, гидролизуют желатин, реакции могут проходить длительно (от двух до семи суток) [27]. При идентификации Y. ruckeri следует учитывать, что ферментативные свойства Y. ruckeri и бактерий рода Serratia похожи (утилизируют лизин, желатин и др.) [25, 27, 32].
, L-сорбозу. Некоторые штаммы иерсиний данного вида вырабатывают ацетоин (при температуре (26 +/- 2) °C), утилизация D-сорбитола вариабельная (приложение 2 к настоящим МР). Многие штаммы утилизируют цитрат натрия, гидролизуют желатин, реакции могут проходить длительно (от двух до семи суток) [27]. При идентификации Y. ruckeri следует учитывать, что ферментативные свойства Y. ruckeri и бактерий рода Serratia похожи (утилизируют лизин, желатин и др.) [25, 27, 32].
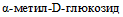 , L-сорбозу. Некоторые штаммы иерсиний данного вида вырабатывают ацетоин (при температуре (26 +/- 2) °C), утилизация D-сорбитола вариабельная (приложение 2 к настоящим МР). Многие штаммы утилизируют цитрат натрия, гидролизуют желатин, реакции могут проходить длительно (от двух до семи суток) [27]. При идентификации Y. ruckeri следует учитывать, что ферментативные свойства Y. ruckeri и бактерий рода Serratia похожи (утилизируют лизин, желатин и др.) [25, 27, 32].
, L-сорбозу. Некоторые штаммы иерсиний данного вида вырабатывают ацетоин (при температуре (26 +/- 2) °C), утилизация D-сорбитола вариабельная (приложение 2 к настоящим МР). Многие штаммы утилизируют цитрат натрия, гидролизуют желатин, реакции могут проходить длительно (от двух до семи суток) [27]. При идентификации Y. ruckeri следует учитывать, что ферментативные свойства Y. ruckeri и бактерий рода Serratia похожи (утилизируют лизин, желатин и др.) [25, 27, 32].3.27. По ферментативной активности представители видов Y. nurmii и Y. entomophaga схожи с Y. ruckeri: не гидролизуют мочевину, декарбоксилируют орнитин, ферментируют трегалозу, не образуют индол, не ферментируют L-рамнозу, D-сорбитол, L-сорбозу, D-ксилозу, салицин, эскулин. В отличие от Y. ruckeri, штаммы данных видов ферментируют сахарозу и не утилизируют лизин. Штаммы видов Y. nurmii, Y. entomophaga и Y. ruckeri не ферментируют L-арабинозу. Метаболические свойства, по которым дифференцируют Y. nurmii и Y. entomophaga, - ферментация мелибиозы и раффинозы [33, 45]. Биохимические признаки иерсиний данных видов представлены в табл. 4 и приложении 2 к настоящим МР.
Таблица 4
Y. entomophaga, Y. nurmii и Y. ruckeri
Субстрат, метаболит: Вид | Мочевина | Лизин | Орнитин | Сахароза | Раффиноза | Мелибиоза |
Y. entomophaga | - | - | + | + | + | + |
Y. nurmii | - | - | + | + | - | - |
Y. ruckeri | - | (+) | + | - | - | - |
Примечание: "+" положительная реакция у 90 - 100% штаммов; "-" - положительная реакция у 0 - 10% штаммов; "(+)" - положительная реакция у 76 - 89% штаммов. Условия инкубации: (26 +/- 2) °C 24 - 48 ч. | ||||||
3.28. По метаболическим свойствам иерсинии вида Y. pekkanenii близки псевдотуберкулезному микробу: гидролизуют мочевину, не утилизируют лизин и орнитин, не образуют ацетоин, индол, не утилизируют цитрат натрия, не ферментируют сахарозу, раффинозу, D-сорбитол, L-сорбозу [44]. Штаммы Y. pekkanenii и Y. pseudotuberculosis различают по ферментации L-рамнозы, D-целлобиозы и гидролизу эскулина. Биохимические свойства Y. pekkanenii приведены в табл. 1 и приложении 2 к настоящим МР.
3.29. Таксономия рода Yersinia с 2005 г. расширилась за счет описания новых видов на основе исследования генома: Y. aleksiciae, Y. alsatica, Y. artesiana, Y. canariae, Y. entomophaga, Y. hibernica, Y. massiliensis, Y. nurmii, Y. pekkanenii, Y. proxima, Y. rochesterensis, Y. thracica, Y. vastinensis. Вследствие изучения единичных штаммов вышеуказанных видов данные об отдельных биохимических свойствах не являются объективными. Для достоверной дифференциации новых и предковых видов, учитывая выраженное сходство их ферментативной активности, следует применять генотипические методы.
и первичной идентификации иерсиний
4.1. При выявлении иерсиний бактериологическим методом исследуемые пробы после предварительной инкубации в средах накопления (этап "холодового" или селективного обогащения) или нативный материал засевают на плотные дифференциально-диагностические питательные среды в соответствии с методическими документами <3>.
--------------------------------
4.2. При проведении исследований используются зарегистрированные и разрешенные для использования на территории Российской Федерации питательные среды, расходные материалы и средства, перечисленные в приложении 1 к настоящим МР, аналогичные им или с лучшими характеристиками. При идентификации иерсиний могут быть использованы имеющиеся в государственных коллекциях тест-штаммы иерсиний отдельных видов.
Дифференциально-диагностическая питательная среда
для выделения возбудителей кишечного иерсиниоза
и псевдотуберкулеза
4.3. Для индикации Y. pseudotuberculosis и Y. enterocolitica применяют дифференциально-диагностическую среду для выделения возбудителей кишечного иерсиниоза и псевдотуберкулеза [14, 15]. Состав и приготовление среды приведены в пункте 1 приложения 1 к настоящим МР.
4.4. Данная среда содержит краситель бромтимоловый синий (среда с бромтимоловым синим (далее СБТС)). Бромтимоловый синий - pH-индикатор, используемый при приготовлении дифференциально-диагностических питательных сред, изменяет окраску от желтого (при pH 6,0) до синего (при pH 7,6) через различные оттенки зеленого цвета; при pH 7,0 имеет характерный травянистый оттенок. При гидролизе мочевины, входящей в состав СБТС, бромтимоловый синий окрашивает среду и колонии микроорганизмов в сине-зеленый (синий) цвет за счет наличия у микроорганизмов фермента уреазы или в желтый - при отсутствии уреазы. Входящая в состав желчь подавляет рост некоторой посторонней микрофлоры.
4.5. На СБТС растут Y. pseudotuberculosis, Y. enterocolitica и другие виды Yersinia. Колонии иерсиний на этой среде имеют характерную морфологию - сухие, матовые, с приподнятым центром, легко дифференцируются от энтеробактерий, не гидролизующих мочевину, приобретающих характерную морфологию колоний - сочные, выпуклые, блестящие. На СБТС Y. pseudotuberculosis образуют на синем фоне среды мелкие колонии 1 - 2 мм в диаметре, круглой формы, выпуклые, имеющие шероховатую сухую поверхность, ровный или неровный (фестончатый) край, пастообразную консистенцию, непрозрачные, сине-зеленого цвета, с выраженным приподнятым центром и матовым налетом. Y. enterocolitica образуют на синем фоне среды колонии среднего размера 1,5 - 3 мм в диаметре, круглой формы, выпуклые, имеющие гладкую или шероховатую сухую поверхность, ровный или неровный край, пастообразную консистенцию, непрозрачные, сине-зеленого цвета, могут быть с приподнятым центром и матовым налетом. Непатогенные представители рода Yersinia образуют на синем фоне среды более крупные колонии 2 - 4 мм в диаметре, сине-зеленые, сухие с матовым налетом или гладкие и блестящие с ровным краем, могут иметь светлый ободок и приподнятый центр.
4.6. Выявление иерсиний на СБТС в некоторых случаях осложняет:
1) обильный рост посторонней микрофлоры (энтеробактерии, псевдомонады);
2) присутствие некоторых энтеробактерий, гидролизующих мочевину (Klebsiella, Proteus);
3) в случае сопутствующего роста гидролизующих мочевину микроорганизмов, которые изменяют цвет среды с зеленого на синий, Hafnia alvei и Pseudomonas spp. образуют сходные по морфологии с иерсиниями колонии.
4.7. Кроме Y. pestis, отсутствие уреазы характерно для представителей видов Y. ruckeri, Y. nurmii, Y. entomophaga. Представители Y. ruckeri и Y. nurmii не меняют цвет среды на сине-зеленый и образуют желтые или желто-зеленые колонии с матовым налетом 2 - 4 мм в диаметре. При исследовании рыбы и рыбных продуктов в целях выявления Y. ruckeri, являющейся патогеном рыб, такие нетипичные для иерсиний колонии отбирают и проводят идентификацию по биохимическим свойствам.
Цефсулодин-иргазан-новобиоцин агар
4.8. Цефсулодин-иргазан-новобиоцин агар ("cefsulodin-irgasan-novobiocin" - далее CIN-агар), является селективной плотной питательной средой, применяемой для выделения возбудителя кишечного иерсиниоза [23, 51, 58, 68, 71]. CIN-агар является оптимальной средой для обнаружения патогенных и непатогенных Y. enterocolitica, особенно когда среда используется после "холодового" обогащения и тщательного отбора предполагаемых колоний с использованием стереомикроскопа [29]. Состав и приготовление среды приведены в пункте 2 приложения 1 к настоящим МР.
4.9. Использование CIN-агара регламентировано Международной организацией по стандартизации (англ. International Organization for Standardization) (далее - ISO) для обнаружения патогенных Y. enterocolitica в пищевых продуктах <4>.
--------------------------------
<4> ГОСТ ISO 10273.
4.10. Среда содержит цефсулодин, иргазан и новобиоцин в качестве селективных противомикробных препаратов, ингибирующих рост многих представителей порядка Enterobacteriales в пользу иерсиний [57]. Среда обладает хорошей селективной способностью, позволяя дифференцировать иерсинии и ряд других грамотрицательных бактерий благодаря характерной морфологии колоний вследствие ферментации D-маннитола [31, 57].
4.11. На CIN-агаре патогенные Y. enterocolitica образуют мелкие колонии 0,5 - 2 мм в диаметре, круглой формы, имеющие гладкую поверхность, ровный край, пастообразную консистенцию, с красным четко очерченным приподнятым центром (вид "жареного яйца"), окруженным чистой прозрачной зоной, центр тонко гранулирован, поверхность колоний блестящая. Непатогенные представители Y. enterocolitica биотипа 1A и виды, близкородственные Y. enterocolitica, образуют на CIN-агаре колонии 1 - 3 мм в диаметре, с более крупным и менее четким красным центром (кроме Y. kristensenii, колонии которых мельче, могут быть с более темным красным центром), окружающая полупрозрачная зона имеет вид матового стекла [30, 51]. Микроорганизмы, которые не ферментируют D-маннитол, образуют бесцветные или бледно-розового цвета полупрозрачные колонии.
4.12. При применении CIN-агара существуют ограничения:
1) некоторые представители родов порядка Enterobacteriales (особенно Serratia и Citrobacter) растут на CIN-агаре, образуя колонии, похожие на Y. enterocolitica и другие виды Yersinia [67];
2) характер колоний на CIN-агаре не позволяет дифференцировать патогенные и непатогенные Y. enterocolitica, патогенные Y. enterocolitica и другие непатогенные иерсинии [30, 31, 38, 72];
3) присутствующий в составе CIN-агара цефсулодин может оказывать ингибирующее действие на штаммы Y. pseudotuberculosis [53, 58, 67, 69]; при наличии роста на CIN-агаре штаммы данного вида иерсиний образуют круглые или слегка неправильной круглой формы колонии с неровным краем, с красным центром, который может быть диффузным без четкой границы, колонии могут быть сухими;
4) на CIN-агаре возможно угнетение роста Y. ruckeri, Y. nurmii [26].
Шигелла-сальмонелла агар с дезоксихолатом натрия
и хлоридом кальция
4.13. В качестве плотной селективной среды для выявления Y. enterocolitica в пробах, прошедших этап селективного обогащения, регламентировано использование модификации сальмонелла-шигелла агара с дезоксихолатом натрия и хлоридом кальция <5> (англ. Salmonella-Shigella Deoxycholate Calcium chloride agar, далее - SSDC-агар). Состав и приготовление среды приведены в пункте 3 приложения 1 к настоящим МР.
--------------------------------
<5> ГОСТ ISO 10273.
4.14. На SSDC-агаре штаммы Y. enterocolitica образуют мелкие до 1 мм колонии круглые, серого цвета, с нечетким, расплывчатым краем, тонко гранулированные при просмотре в косо проходящем свете <6> [26].
--------------------------------
<6> ГОСТ ISO 10273.
4.15. Существуют недостатки применения SSDC-агара для выявления Y. enterocolitica:
1) вид колоний иерсиний на этой среде не всегда характерный и не позволяет дифференцировать их от других микроорганизмов (Morganella, Proteus, Serratia, Aeromonas) [26, 58];
2) краситель бриллиантовый зеленый в составе SSDC-агара может подавлять рост некоторых штаммов патогенных Y. enterocolitica серотипов O:8 и O:9 [57].
Селективные среды, применяемые для выделения энтеробактерий
4.16. Для первичного посева исследуемых проб при индикации иерсиний используют среду Эндо, агар МакКонки, предназначенные для селективного выделения и дифференциации грамотрицательных микроорганизмов кишечной группы в соответствии с методическими документами <7>.
--------------------------------
4.17. На среде Эндо через 24 ч иерсинии образуют мелкие 1 - 2 мм в диаметре выпуклые, гладкие, блестящие ("росинки"), с ровным краем, полупрозрачные лактозонегативные бесцветные колонии. Через 48 ч размер колоний увеличивается, они приобретают светло-розовый оттенок.
4.18. Ограничениями в применении данных сред являются:
1) слабые селективные свойства сред в отношении бактерий рода Yersinia вследствие сходства морфологии колоний иерсиний и других энтеробактерий, не ферментирующих лактозу, и роста сопутствующей микрофлоры [51];
2) ингибирующее действие красителей в составе сред (основной фуксин в среде Эндо и нейтральный красный в агаре МакКонки) на некоторые штаммы Y. enterocolitica, в том числе патогенные, относящиеся к серотипам O:3, O:5,27, O:8, O:9 [57].
Полиуглеводные среды для идентификации энтеробактерий
4.19. На этапе первичной идентификации иерсиний в соответствии с методическими документами <8> применяют комбинированные дифференциально-диагностические питательные среды: двухсахарный агар Клиглера, двухсахарный агар Ресселя, модифицированный агар Клиглера с мочевиной, модифицированный агар Ресселя с мочевиной (по Равич-Биргер), трехсахарный агар с мочевиной И.С. Олькеницкого.
--------------------------------
4.20. Посевы на полиуглеводных средах инкубируют при температуре (37 +/- 1) °C, через 24 ч оценивают способность к расщеплению углеводов и мочевины.
4.21. На полиуглеводных средах Клиглера и двухсахарном агаре Ресселя, содержащих D-глюкозу и лактозу, учитывают результат ферментации углеводов. Скошенная часть среды цвет не меняет, так как иерсинии не расщепляют лактозу, за исключением отдельных штаммов некоторых видов (приложение 2 к настоящим МР). Иерсинии ферментируют D-глюкозу с образованием кислот, в результате окраска столбика среды изменяется в зависимости от внесенного индикатора: при использовании фенолового красного (агар Клиглера) столбик среды меняет красный цвет на желтый, в случае содержания в среде бромтимолового синего (агар Ресселя) столбик среды меняет зеленый цвет на желтый. Штаммы, ферментирующие лактозу, изменяют цвет всей среды.
4.22. На полиуглеводных средах с мочевиной (среда Олькеницкого, модифицированный агар Ресселя по Равич-Биргер) учитывают способность микроорганизмов ферментировать D-глюкозу, лактозу и расщеплять мочевину.
В результате роста на этих средах иерсиний, обладающих ферментом уреаза, продукты распада мочевины смещают pH среды в щелочную сторону. После инкубации скошенная часть среды и столбик приобретают окраску, соответствующую применяемому pH-индикатору в щелочном диапазоне. В среде Олькеницкого феноловый красный окрашивает скошенную поверхность и столбик среды в малиновый цвет. На модифицированной среде Ресселя при использовании в качестве комбинированного индикатора тимолового синего и индикатора Андреде среда приобретает фиолетовую или сине-фиолетовую окраску; при использовании в качестве комбинированного индикатора фенолового красного и метиленового синего столбик среды становится малинового цвета, скошенная поверхность - фиолетового.
В случае роста на данных средах иерсиний, не гидролизующих мочевину, учитывают ферментацию сахаров; цвет среды меняется в зависимости от внесенного индикатора.
4.23. Существуют ограничения использования полиуглеводных сред с мочевиной:
1) у штаммов, гидролизующих мочевину, анализ ферментации сахаров не осуществляют, так как в процессе их роста и скошенная часть среды, и столбик приобретают окраску, соответствующую щелочному pH среды за счет продуктов распада мочевины [17]. Для исследования ферментации углеводов у данных штаммов применяют среды Гисса;
2) при использовании трехсахарного агара с мочевиной Олькеницкого у иерсиний, ферментирующих сахарозу, в ряде случаев затруднен учет гидролиза мочевины неполным окрашиванием столбика среды в малиновый цвет. Для получения полного окрашивания всей среды в малиновый цвет рекомендуют использовать питательную среду с мочевиной на основе агара Клиглера (то есть не содержащую сахарозу) [17].
4.24. На полиуглеводных средах, содержащих соли железа, учитывают способность к образованию сероводорода. Вследствие отсутствия продукции иерсиниями сероводорода черное окрашивание не образуется.
дифференциации бактерий рода Yersinia
5.1. Для изучения биохимических свойств выделенной культуры используют традиционные микробиологические тесты с применением различных дифференциально-диагностических питательных сред, содержащих субстраты, используемые иерсиниями в процессе метаболизма. Исследование ферментативной активности бактерий проводят с применением коммерческих тестов, зарегистрированных и разрешенных для использования на территории Российской Федерации, и (или) тестов с использованием сред и реактивов, приготовленных в лабораторных условиях в соответствии с приложением 1 к настоящим МР. Для контроля специфичности тестов используют референс-штаммы (положительный и отрицательный контроль).
5.2. При исследовании ферментативной активности бактерий, предварительно рассматриваемых в качестве представителей рода Yersinia, с использованием коммерческих тест-систем (или отдельных тестов) и тестов, приготовленных в лабораторных условиях, необходимыми условиями являются возраст культуры бактерий, температурный и временной режимы инкубации. Вследствие психрофильных свойств у представителей рода Yersinia метаболизм некоторых веществ может различаться при (37 +/- 1) °C и (26 +/- 2) °C. Необходимо соблюдать оптимальный для иерсиний температурный режим проведения исследования в соответствии с методическими документами <9> - инкубация суточной (18 - 24 ч) агаровой культуры при (26 +/- 2) °C в течение 24 - 48 часов [21].
--------------------------------
<9> МУК 4.2.3019-12.
5.3. Биохимические тесты, используемые для внутриродовой и внутривидовой дифференциации иерсиний, охарактеризованы в пунктах 5.4 - 5.52. Для каждого теста приведены виды (биотипы) иерсиний, при дифференциации которых рассматриваемый тест является наиболее значимым. Алгоритм дифференциации патогенных и непатогенных видов иерсиний представлен в приложении 3 к настоящим МР.
Гидролиз мочевины
5.4. Микроорганизмы, обладающие ферментом уреазой, гидролизуют мочевину с образованием в виде конечных продуктов аммиака и диоксида углерода (CO2), смещая pH среды в щелочную сторону, что учитывают по изменению цвета индикатора. При проведении теста в планшете для предотвращения выхода аммиака, способного изменять pH среды в соседних лунках, после инокуляции культуры наносят 2 - 3 капли стерильного минерального масла на среду в лунке.
5.5. Для определения гидролиза мочевины используют плотную среду с мочевиной Преуса, агар Кристенсена с мочевиной или его модификацию - жидкую среду с мочевиной.
При использовании жидкой среды с мочевиной (состав и приготовление среды в соответствии с пунктом 4 приложения 1 к настоящим МР) реакцию учитывают через 1 ч, 2 ч и 24 ч инкубации исследуемой культуры при температуре (26 +/- 2) °C. В случае наличия уреазы развивается малиновое окрашивание среды.
При использовании плотной среды с мочевиной Преуса (состав и приготовление среды в соответствии с пунктом 5 приложения 1 к настоящим МР) реакцию учитывают через 24 - 48 ч инкубации исследуемой культуры при температуре (26 +/- 2) °C. Вследствие гидролиза мочевины цвет среды становится синим.
5.6. На этапе первичной идентификации наличие уреазы у иерсиний определяют с использованием полиуглеводных сред: трехсахарного агара с мочевиной Олькеницкого, модифицированной среды Ресселя с мочевиной (по Равич-Биргер), питательной среды с мочевиной на основе агара Клиглера, не содержащего сахарозу [11, 16, 17]. При гидролизе мочевины и скошенная поверхность, и столбик среды приобретают характерную окраску за счет индикатора, при этом анализ ферментации углеводов не проводят (пункты 4.19 - 4.24).
5.7. Определение наличия или отсутствия фермента уреазы является основным тестом для дифференциации бактерий рода Yersinia. Не обладают способностью гидролизовать мочевину иерсинии видов Y. entomophaga, Y. nurmii, Y. pestis и Y. ruckeri. Уреазой обладают представители остальных 22 видов иерсиний: Y. aldovae, Y. aleksiciae, Y. alsatica, Y. artesiana, Y. bercovieri, Y. canariae, Y. enterocolitica, Y. frederiksenii, Y. hibernica, Y. intermedia, Y. kristensenii, Y. massiliensis, Y. mollaretii, Y. pekkanenii, Y. proxima, Y. pseudotuberculosis, Y. rochesterensis, Y. rohdei, Y. similis, Y. thracica, Y. vastinensis и Y. wautersii. Некоторые штаммы данных видов могут давать отрицательную реакцию гидролиза мочевины при температуре (37 +/- 1) °C, поэтому важно определять биохимическую активность иерсиний при температуре (26 +/- 2) °C.
Декарбоксилирование аминокислот
5.8. Используют тесты, направленные на выявление специфических ферментов, способных катализировать декарбоксилирование аминокислот с образованием щелочных продуктов (амин или диамин и CO2), что выявляется по изменению цвета среды за счет индикатора. Для стабилизации продуктов расщепления аминокислот реакцию проводят в анаэробных условиях, для создания которых после инокуляции культуры на среду наносят 2 - 3 капли стерильного минерального масла с образованием слоя толщиной 4 - 5 мм.
5.9. Среда для определения декарбоксилазной активности содержит L-лизин или L-орнитин. Состав и приготовление среды с индикаторами бромкрезоловый пурпурный и крезоловый красный представлены в пункте 6 приложения 1 к настоящим МР. Через 24 - 48 ч при наличии декарбоксилазной активности индикаторная система изменяет цвет среды от желтого к фиолетовому. Если в качестве индикатора используется бромтимоловый синий, готовая среда имеет желтовато-зеленый цвет [9, 16]. При декарбоксилировании аминокислоты среда приобретает синий цвет, при отсутствии утилизации аминокислот среда становится желтой. Цвет контрольной среды (не содержащей аминокислоту) с выросшей культурой изменяется на желтый.
5.10. Представители видов Y. pseudotuberculosis, Y. similis, Y. wautersii, Y. canariae, Y. pekkanenii не декарбоксилируют орнитин. Выявление орнитиндекарбоксилазы используется при определении вида не ферментирующих сахарозу иерсиний, например, при дифференциации Y. pseudotuberculosis от Y. kristensenii и Y. aldovae (таблица 1). По наличию орнитиндекарбоксилазной активности (кроме реакции Фогеса-Проскауэра) дифференцируют штаммы видов Y. enterocolitica и Y. canariae.
5.11. Иерсинии не декарбоксилируют лизин, исключение составляют большинство штаммов Y. ruckeri и некоторые штаммы Y. aleksiciae и Y massiliensis.
Ферментация углеводов
5.12. Для дифференциации бактерий по сахаролитической активности в отношении различных углеводных субстратов применяют углеводные среды (среды Гисса). Иерсинии имеют тип ферментации углеводов с образованием смеси кислот (молочной, уксусной и др.), которые снижают значение pH, что приводит к изменению цвета индикатора среды.
5.13. Для ферментации углеводов используют жидкие или с добавлением агара (0,2 - 0,4%) среды Гисса [9, 13, 18]. Состав и приготовление сред для ферментации углеводов приведены в пункте 7 приложения 1 к настоящим МР.
Готовая среда с индикатором Андреде бесцветная, слегка желтоватая, с индикатором бромтимоловым синим имеет травянисто-зеленый цвет (pH 6,9 - 7,0) или синий с зеленоватым оттенком (pH 7,2 - 7,4).
Посевы инкубируют при температуре (26 +/- 2) °C. Учет результатов проводят через 24 и 48 ч инкубации исследуемой культуры. Ферментация углеводов сопровождается окрашиванием среды в розово-красный цвет в случае применения индикатора Андреде или желтый при использовании бромтимолового синего или фенолового красного.
Для определения способности ферментировать углеводы в качестве альтернативной используют среду, содержащую фосфатный буфер pH 7,6, феноловый красный и углевод [5].
5.14. Определение ферментации сахарозы - один из обязательных тестов для видовой идентификации иерсиний. Сахарозу ферментируют с образованием кислоты представители Y. alsatica, Y. artesiana, Y. bercovieri, Y. canariae, Y. enterocolitica, Y. entomophaga, Y. frederiksenii, Y. intermedia, Y. massiliensis, Y. mollaretii, Y. nurmii, Y. proxima, Y. rohdei, Y. vastinensis. Большинство штаммов Y. aldovae не утилизируют сахарозу [22, 23, 40]. Сахарозу не ферментируют представители Y. aleksiciae, Y. hibernica, Y. kristensenii, Y. pekkanenii, Y. pestis, Y. pseudotuberculosis, Y. rochesterensis, Y. ruckeri, Y. similis, Y. thracica, Y. wautersii. В табл. 1 представлены другие биохимические свойства видов, не ферментирующих сахарозу.
5.15. L-Рамнозу утилизируют представители Y. aldovae, Y. alsatica, Y. frederiksenii, Y. pseudotuberculosis, Y. similis, Y. vastinensis, Y. wautersii и отдельных биотипов Y. intermedia. По отсутствию у представителей Y. enterocolitica способности ферментировать L-рамнозу их дифференцируют от иерсиний вида Y. frederiksenii и Y. intermedia 1 - 3 и 6 - 10 биотипов (табл. 3). По ферментации L-рамнозы дифференцируют Y. pseudotuberculosis и Y. pekkanenii (таблица 1).
5.16. Мелибиозу ферментируют штаммы Y. entomophaga, Y. intermedia 1 - 7 биотипов, Y. wautersii, большинство штаммов Y. pseudotuberculosis и некоторые представители Y. rohdei. Способность к разложению мелибиозы используют для видовой дифференциации штаммов Y. intermedia 1 - 7 биотипов и Y. enterocolitica (табл. 3).
5.17. Раффинозу ферментируют представители Y. entomophaga, Y. wautersii, Y. intermedia 1 - 5, 8 биотипов, некоторые штаммы Y. rohdei. Штаммы Y. wautersii дифференцируют по способности ферментировать раффинозу от штаммов Y. pseudotuberculosis и Y. similis (табл. 1). По отсутствию у представителей Y. enterocolitica способности ферментировать раффинозу их дифференцируют от иерсиний вида Y. intermedia 1 - 5 и 8 биотипов (табл. 3).
5.18. Ферментация 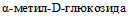 наблюдается только у представителей Y. intermedia, что позволяет дифференцировать не ферментирующие раффинозу и мелибиозу штаммы Y. intermedia 9 и 10 биотипов и Y. frederiksenii (табл. 3).
наблюдается только у представителей Y. intermedia, что позволяет дифференцировать не ферментирующие раффинозу и мелибиозу штаммы Y. intermedia 9 и 10 биотипов и Y. frederiksenii (табл. 3).
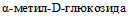 наблюдается только у представителей Y. intermedia, что позволяет дифференцировать не ферментирующие раффинозу и мелибиозу штаммы Y. intermedia 9 и 10 биотипов и Y. frederiksenii (табл. 3).
наблюдается только у представителей Y. intermedia, что позволяет дифференцировать не ферментирующие раффинозу и мелибиозу штаммы Y. intermedia 9 и 10 биотипов и Y. frederiksenii (табл. 3).5.19. Ферментация мальтозы наблюдается у всех иерсиний, за исключением большинства штаммов Y. aldovae и некоторых Y. rohdei. Представители Y. hibernica вариабельно ферментируют мальтозу [40, 47].
5.20. Тест на ферментацию L-сорбозы используют для определения биотипа штаммов Y. enterocolitica (таблица 2). По ферментации L-сорбозы дифференцируют штаммы Y. bercovieri и Y. mollaretii.
5.21. Способность ферментировать салицин используют для определения биотипа штаммов Y. enterocolitica (таблица 2).
5.22. Свойство ферментировать D-ксилозу используют для определения биотипа штаммов Y. enterocolitica (табл. 2). D-Ксилозу не ферментируют штаммы Y. enterocolitica 4 биотипа, некоторые штаммы 5 биотипа и иерсинии видов Y. entomophaga, Y. ruckeri и Y. nurmii.
5.23. Ферментируют трегалозу большинство представителей рода Yersinia. Способность ферментировать трегалозу используют для определения биотипа штаммов Y. enterocolitica: штаммы Y. enterocolitica 5 биотипа не обладают этой способностью (табл. 2). Представители Y. hibernica вариабельно ферментируют трегалозу [40, 47].
5.24. Ферментируют L-арабинозу иерсинии многих видов, за исключением видов Y. entomophaga, Y. nurmii и Y. ruckeri.
5.25. Не ферментируют D-сорбитол большинство представителей Y. enterocolitica 5 биотипа, Y. entomophaga, Y. nurmii, Y. pseudotuberculosis, Y. pekkanenii, Y. similis, Y. wautersii. Представители Y. ruckeri вариабельно ферментируют D-сорбитол. Способность утилизировать D-сорбитол используют для определения биотипа Y. enterocolitica (табл. 2).
Индолообразование
5.26. В тесте на индолообразование у микроорганизмов выявляют фермент триптофаназу, которая расщепляет гетероциклическую аминокислоту L-триптофан с образованием индола, пировиноградной кислоты и аммиака. Содержание индола в среде определяют добавлением тест-реактива Ковача или Эрлиха на основе бензойного альдегида, при взаимодействии с которым индол образует окрашенные в розовый или красный цвет соединения.
5.27. Среду для определения индолообразования готовят на основе триптического перевара казеина (1,2 - 1,4% аминного азота), бульона Хоттингера, к которому добавляют 0,3% L-триптофана, pH среды 6,8 - 6,9 или используют среду Строгова [8, 9].
Состав и приготовление среды Строгова приведены в пункте 8 приложения 1 к настоящим МР. Посевы инкубируют при температуре (26 +/- 2) °C. Через 48 ч инкубации к 1 - 2 мл культуры добавляют 0,5 мл реактива Ковача (пункт 9 приложения 1 к настоящим МР), встряхивают. Наличие индола в среде оценивают по появлению красного кольца на поверхности среды через 1 - 2 мин.
5.28. Тест на индолообразование используют при определении биотипов штаммов Y. enterocolitica (табл. 2), для дифференциации Y. massiliensis от Y. bercovieri, Y. mollaretii и Y. rohdei.
Образование ацетилметилкарбинола
5.29. Для иерсиний некоторых видов характерно анаэробное сбраживание D-глюкозы по пути преобразования метаболита пировиноградной кислоты в ацетилметилкарбинол (ацетоин). Образование ацетоина выявляют по окрашиванию среды в реакции Фогеса-Проскауэра: в щелочной среде в присутствии 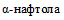 происходит окисление ацетоина до диацетила, который, вступая в реакцию с азотистыми основаниями пептона, образует соединение вишнево-красного цвета.
происходит окисление ацетоина до диацетила, который, вступая в реакцию с азотистыми основаниями пептона, образует соединение вишнево-красного цвета.
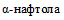 происходит окисление ацетоина до диацетила, который, вступая в реакцию с азотистыми основаниями пептона, образует соединение вишнево-красного цвета.
происходит окисление ацетоина до диацетила, который, вступая в реакцию с азотистыми основаниями пептона, образует соединение вишнево-красного цвета.5.30. Среда для обнаружения образования ацетоина содержит пептон и D-глюкозу (среда Кларка). Состав среды и реактивов для реакции Фогеса-Проскауэра, их приготовление приведены в пунктах 10, 11 приложения 1 к настоящим МР.
Посевы инкубируют в двух пробирках при разной температуре (26 +/- 2) °C и (37 +/- 1) °C в течение 48 ч (возможна инкубация до 5 сут). По истечении не менее 48 ч к 2,5 мл культуры на среде Кларка добавить 0,3 мл реактива 1, тщательно перемешать, затем добавить 0,1 мл реактива 2, пробирку встряхнуть для лучшего доступа кислорода. Соблюдают указанный порядок добавления реактивов. Через 10 - 15 мин оценивают характер окраски. При положительном результате развивается вишнево-красное окрашивание. Другие цвета (медный и др.) среды соответствуют отрицательному результату.
5.31. Продукция ацетоина у иерсиний зависит от температуры инкубации: образование ацетоина наблюдается при температуре (26 +/- 2) °C, но не при (37 +/- 1) °C. Этой способностью обладают представители видов Y. enterocolitica, Y. frederiksenii, Y. intermedia, Y. aldovae, Y. nurmii, Y. entomophaga, Y. alsatica, Y. artesiana, Y. proxima, Y. vastinensis. Представители Y. massiliensis образуют ацетоин, но медленнее: после 24 ч реакция отрицательная, после 72 ч может наблюдаться положительная реакция (плюс 28 °C) [43]. Иерсинии остальных видов не образуют ацетоин. Тест на образование ацетоина применяют для дифференциации штаммов Y. enterocolitica и иерсиний видов Y. mollaretii, Y. bercovieri, Y. rohdei.
Утилизация цитрата на агаре Симмонса
5.32. Тест направлен на выявление способности микроорганизмов использовать цитрат натрия в качестве единственного источника углерода в питательной среде. Иерсинии, обладающие ферментами цитратазами, расщепляют цитрат с образованием диоксида углерода, который, вступая в реакцию с ионами натрия и водой, образует карбонат натрия, сдвигающий pH среды в щелочную сторону. В присутствии индикатора оливково-зеленый цвет среды изменяется на ярко-синий. Иерсинии, не обладающие способностью утилизировать цитрат в качестве единственного источника углерода, на среде Симонса не растут, и цвет среды не меняется.
5.33. Для изучения способности энтеробактерий утилизировать цитрат натрия используют агаризованные среды Симмонса (пункт 12 приложения 1 к настоящим МР).
Засевают скошенную часть и столбик среды суспензией культуры (1081010 м.к./мл), которую готовят в 0,9%-м растворе хлорида натрия, чтобы при посеве не внести вместе с культурой питательные вещества, для исключения ложноположительного результата. Посевы инкубируют при температуре (26 +/- 2) °C в течение 48 ч (возможна инкубация до 5 сут). Появление роста изолированных колоний на поверхности среды и изменение цвета среды на синий указывает на способность утилизировать цитрат, при отрицательном результате рост отсутствует и цвет среды не изменяется.
5.34. Способностью утилизировать цитрат натрия обладают иерсинии видов Y. intermedia (кроме биотипов 2, 6, 7, 10), Y. nurmii, Y. entomophaga, Y. ruckeri. Представители Y. aldovae, Y. alsatica, Y. frederiksenii, Y. massiliensis, Y. proxima, Y. rohdei вариабельно утилизируют цитрат натрия. Тест на утилизацию цитрата используют для определения биотипа Y. intermedia.
Гидролиз Твин 80
5.35. Для определения наличия у иерсиний фермента липазы (твин-эстеразы) в качестве субстрата используют Твин 80 (эфир олеиновой кислоты), гидролитическое расщепление которого сопровождается визуально определяемым изменением среды.
5.36. Для выявления ферментов липаз (эстераз) иерсинии культивируют на средах с липосодержащими субстратами. Состав и приготовление среды для определения гидролиза Твин 80 приведены в пункте 13 приложения 1 к настоящим МР.
Засеять культуру на чашку/сектор чашки Петри штрихом или в форме изолированной бляшки. Инкубировать 24 - 72 ч при температуре (26 +/- 2) °C. Положительным результатом считается появление мутного ореола вокруг колоний, состоящего из кристаллов кальциевого мыла на поверхности и в толще среды.
5.37. Тест на определение способности гидролизовать Твин 80 используют для определения биотипов Y. enterocolitica в комплексе с другими тестами (ферментация салицина или гидролиз эскулина, индолообразование, ферментация D-ксилозы и L-сорбозы). Наличие гидролиза Твин 80 позволяет дифференцировать штаммы Y. enterocolitica биотипа 1 (1A - непатогенные и 1B - патогенные) от патогенных штаммов Y. enterocolitica 2, 3, 4 и 5 биотипов, у которых липаза отсутствует (не гидролизуют Твин 80) (табл. 2). Y. massiliensis не гидролизует Твин 80 в отличие от Y. enterocolitica биотипа 1A (табл. 3).
Гидролиз эскулина
5.38. Данный тест предназначен для выявления у микроорганизмов способности утилизировать эскулин (относится к группе гликозидов - производных сахаров), являющийся субстратом фермента 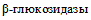 . При выращивании бактерий на среде, содержащей эскулин, продукты его гидролиза, взаимодействуя с цитратом железа, образуют преципитат черного цвета.
. При выращивании бактерий на среде, содержащей эскулин, продукты его гидролиза, взаимодействуя с цитратом железа, образуют преципитат черного цвета.
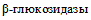 . При выращивании бактерий на среде, содержащей эскулин, продукты его гидролиза, взаимодействуя с цитратом железа, образуют преципитат черного цвета.
. При выращивании бактерий на среде, содержащей эскулин, продукты его гидролиза, взаимодействуя с цитратом железа, образуют преципитат черного цвета.5.39. Для выявления фермента 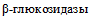 иерсинии культивируют на средах, содержащих эскулин (пункт 14 приложения 1 к настоящим МР).
иерсинии культивируют на средах, содержащих эскулин (пункт 14 приложения 1 к настоящим МР).
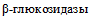 иерсинии культивируют на средах, содержащих эскулин (пункт 14 приложения 1 к настоящим МР).
иерсинии культивируют на средах, содержащих эскулин (пункт 14 приложения 1 к настоящим МР).Учет результатов проводят через 24 и 48 ч инкубации посевов при температуре (26 +/- 2) °C. При гидролизе эскулина наблюдается черный ореол вокруг колоний с образованием осадка.
5.40. Тест на гидролиз эскулина и аналогичный тест на ферментацию другого гликозида - салицина используют при определении биотипа штаммов Y. enterocolitica (таблица 2).
Способность гидролизовать эскулин учитывают при видовой идентификации Y. massiliensis, Y. intermedia, Y. frederiksenii.
Гидролиз желатина
5.41. Тест выявляет протеолитическую активность бактерий. При гидролизе белков желатина протеолитическим ферментом микроорганизмов желатиназой происходит утрата его желирующей способности, которая сопровождается разжижением желатина.
5.42. Состав и приготовление питательной среды с желатином приведены в пункте 15 приложения 1 к настоящим МР. Посевы инкубируют при (22 +/- 2) °C от одного дня до семи суток с ежедневным учетом результата. Положительная реакция - разжижение по крайней мере части среды. При отрицательном результате среда остается равномерно плотной.
Для более быстрого выявления гидролиза желатина тест проводят в бульоне, содержащем диски с активированным углем и желатином [6]. При положительной реакции освободившиеся частицы активированного угля распределяются по всему объему, окрашивая среду. Данный метод применяется в некоторых коммерческих тест-системах.
5.43. Тест на желатиназную активность используют для видовой идентификации Y. ruckeri и Y. nurmii, которые, в отличие от иерсиний других видов, гидролизуют желатин.
Дезаминирование триптофана и фенилаланина
5.44. Тест основан на способности микроорганизмов при росте на питательных средах, содержащих L-триптофан или L-фенилаланин, вырабатывать специфические дезаминазы, которые подвергают аминокислоты окислительному дезаминированию с образованием продуктов, выявляемых при добавлении хлорида железа (III) по изменению окрашивания.
Для определения триптофандезаминазы применяют жидкую среду (состав и приготовление в соответствии с пунктом 16 приложения 1 к настоящим МР) [5].
Посевы инкубируют при температуре (26 +/- 2) °C 24 - 48 ч. После инкубации вносят 1 - 2 капли реактива для определения триптофандезаминазы (пункт 17 приложения 1 к настоящим МР). Наличие фермента выявляется по появлению темно-коричневого или красно-бурого окрашивания среды через 1 - 2 мин после внесения реактива с хлорным железом. При отрицательной реакции цвет среды желтый.
5.46. Иерсинии не дезаминируют фенилаланин и триптофан, исключение составляют некоторые представители вида Y. massiliensis (пункт 3.19 настоящих МР).
Гидролиз пиразинамида
5.47. Вырабатываемый микроорганизмами фермент пиразинамидаза гидролизует амид пиразинкарбоновой кислоты (пиразинамид). Продукт гидролиза (2 пиразинкарбоновая кислота) после взаимодействия с солями железа окрашивает среду в коричневый цвет.
5.48. Для выявления пиразинамидазной активности используют плотную среду, содержащую пиразинамид. Состав и приготовление среды приведены в пункте 18 приложения 1 к настоящим МР.
Культуры, выращенные на обычном питательном агаре при температуре (26 +/- 2) °C, засевают частыми штрихами на поверхность агара с пиразинамидом. Посевы инкубируют при температуре (26 +/- 2) °C в течение 48 ч. После инкубации в пробирки вносят 1,0 - 2,0 мл свежеприготовленного раствора сульфата аммонийного железа (пункт 19 приложения 1 к настоящим МР) и оставляют при комнатной температуре на 15 мин.
Цвет среды с иерсиниями, не обладающими пиразинамидазой, остается без изменения. Цвет среды с иерсиниями, гидролизующими пиразинамид, в присутствии соли железа приобретает выраженный коричневый (красно-коричневый) оттенок. Из-за нечеткого изменения цвета среды визуальный учет пиразинамидазной активности иерсиний может иметь неоднозначную интерпретацию.
5.49. Тест на выявление пиразинамидазы используют в качестве дополнительного к другим тестам, определяющим принадлежность к патогенным или непатогенным видам/биотипам иерсиний. Штаммы Y. pseudotuberculosis, Y. wautersii и патогенных Y. enterocolitica не гидролизуют пиразинамид. Штаммы непатогенных Y. enterocolitica биотипа 1A и Y. similis проявляют пиразинамидазную активность (пункты 3.9, 3.12).
Подвижность
5.50. В тесте на подвижность выявляют способность микроорганизмов к активному перемещению с участием жгутиков.
5.51. Для определения подвижности используют полужидкий питательный агар (состав и приготовление в соответствии с пунктом 20 приложения 1 к настоящим МР) [13].
Посев делают уколом в верхнюю часть столбика среды на глубину около 5 см, инкубируют в двух пробирках при разной температуре (26 +/- 2) °C и (37 +/- 1) °C в течение 1 - 2 суток [9]. Подвижные бактерии образуют диффузное помутнение среды. Неподвижные бактерии растут по ходу укола, среда при этом остается прозрачной.
5.52. Многие виды иерсиний подвижны при температуре (22 +/- 2) °C. При температуре выше плюс 30 °C иерсинии утрачивают подвижность (приложение 2 к настоящим МР). Штаммы, отнесенные к виду Y. entomophaga, подвижны при температуре (22 +/- 2) °C и при температуре (37 +/- 1) °C [33]. Для ряда видов иерсиний свойство подвижности охарактеризовано при температуре плюс 28 °C. Данная информация не включена в приложение 2 к настоящим МР, так как подвижность иерсиний следует определять при температуре (22 +/- 2) °C [9]. Например, Y. wautersii и Y. pekkanenii неподвижны при плюс 28 °C, но нет данных об отсутствии подвижности при плюс 22 °C [40, 44, 55].
Коммерческие тест-системы для биохимической идентификации
и дифференциации энтеробактерий
5.53. Совокупность предлагаемых биохимических тестов определяется производителем тест-системы. В состав различных наборов включены тесты для определения от 12 до 50 биохимических признаков микроорганизмов. Существующие коммерческие тест-системы не позволяют произвести полноценное определение видов и биотипов бактерий рода Yersinia. С учетом имеющихся ограничений в применении их используют в комплексе с отдельными дополнительными тестами, необходимыми для корректной видовой и внутривидовой идентификации бактерий рода Yersinia, описание которых приведено в главе V.
5.54. Примеры идентификации иерсиний представлены в приложении 4 к настоящим МР.
к МР 4.2.0292-22
РАСХОДНЫЕ МАТЕРИАЛЫ
Состав и приготовление питательных сред и реактивов <10>
--------------------------------
<10> Примечание. Допускается использование питательных сред и реактивов с аналогичными или лучшими характеристиками.
1. Дифференциально-диагностическая питательная среда для выделения возбудителей кишечного иерсиниоза и псевдотуберкулеза <11> [9]
--------------------------------
<11> МУ 3.1.1.2438-09.
Состав:
Панкреатический гидролизат рыбной муки | 23,0 г |
Желчь очищенная | 4,0 г |
D-Глюкоза | 10,0 г |
Мочевина | 5,0 г |
Хлорид натрия (NaCl) | 5,4 г |
Бромтимоловый синий | 0,128 г или 8,0 мл 1,6%-го спиртового раствора |
Гидрофосфат калия (K2HPO4) | 1,0 г |
Агар микробиологический | 11,0 г |
Вода дистиллированная | до 1000,0 мл |
Компоненты тщательно перемешать в дистиллированной воде, довести объем до 1 л, нагреть до кипения, кипятить 5 мин. Охладить до плюс 40 °C - плюс 45 °C, разлить в чашки Петри. Хранить среду в течение 7 - 10 суток при температуре (6 +/- 2) °C.
Применяется бромтимоловый синий спирторастворимый (3',3"-бромтимолсульфофталеин) или бромтимоловый синий водорастворимый (натриевая или аммонийная соль 3',3"-бромтимолсульфофталеина), обе формы бромтимолового синего одинаково меняют цвет в одном диапазоне pH: от 6,0 до 7,6. В случае применения 3',3"-бромтимолсульфофталеина индикатор растворяют в спирте (для получения 1,6%-го спиртового раствора 0,16 г бромтимолового синего растворить в 10 мл этанола) или в водном растворе щелочи (для получения 1,6%-го водно-щелочного раствора 0,1 г бромтимолового синего растворить в 3,2 мл 1/20 N гидроксида натрия (концентрация NaOH 2 г/л), затем добавить 3,0 мл дистиллированной воды). При использовании водорастворимого бромтимолового синего растворение в спирте или щелочи не требуется, натриевая (или аммонийная) соль 3,3-бромтимолсульфофталеина хорошо растворима в воде.
2. Цефсулодин-иргазан-новобиоцин агар <12>
--------------------------------
<12> ГОСТ ISO 10273.
Состав основы среды:
Ферментативный гидролизат желатина | 17,0 г |
Ферментативный гидролизат казеина и тканей животных | 3,0 г |
Дрожжевой экстракт | 2,0 г |
D-Маннитол | 20,0 г |
Пируват натрия | 2,0 г |
Хлорид натрия (NaCl) | 2,0 г |
Дезоксихолат натрия | 0,5 г |
Сульфат магния 7-водный | (MgSO4·7H2O) 0,01 г |
Нейтральный красный | 0,03 г |
Кристаллический фиолетовый | 0,001 г |
Агар микробиологический | 12,5 г |
Вода дистиллированная | до 1000,0 мл |
Компоненты основы среды растворить в воде при кипячении, стерилизовать автоклавированием при температуре плюс 121 °C в течение 15 мин, pH среды 7,2 - 7,4.
В стерильную основу среды внести селективную добавку, содержащую цефсулодин, иргазан, новобиоцин. Растворы противомикробных препаратов готовить отдельно.
Растворить 0,4 г иргазана в 100 мл этанола (4 г/л спиртовой раствор), допускается хранение раствора при минус 20 °C не более четырех недель.
Растворить 1,5 г цефсулодина в 100 мл дистиллированной воды (15 г/л). Стерилизовать фильтрацией.
Растворить 0,25 г новобиоцина в 100 мл дистиллированной воды (2,5 г/л). Стерилизовать фильтрацией.
Добавить асептически по 1 мл раствора каждого противомикробного препарата к 997 мл основы среды, охлажденной до плюс 45 °C, перемешать. Разлить в стерильные чашки Петри.
3. Шигелла-сальмонелла агар с дезоксихолатом натрия и хлоридом кальция <13>
--------------------------------
<13> ГОСТ ISO 10273.
Состав:
Мясной экстракт | 5,0 г |
Гидролизат казеина и тканей животных | 5,0 г |
Дрожжевой экстракт | 5,0 г |
Лактоза | 10,0 г |
Желчные соли | 8,5 г |
Дезоксихолат натрия | 10,0 г |
Хлорид кальция (CaCl2·H2O) | 1,0 г |
Цитрат натрия (Na3C6H5O7) | 10,0 г |
Тиосульфат натрия 5-водный | 8,5 г |
Цитрат железа (III) (FeC6H5O7) | 1,0 г |
Бриллиантовый зеленый | 0,0003 г |
Нейтральный красный | 0,025 г |
Агар микробиологический | 15,0 г |
Вода дистиллированная | до 1000,0 мл |
Компоненты растворить в воде, довести объем до 1 л. Нагреть и кипятить в течение минуты. Не стерилизовать, pH среды 7,4.
4. Жидкая среда для определения уреазы [5]
Состав:
1/15 М фосфатный буфер, pH 7,0 | 100,0 мл |
Хлорид натрия (NaCl) | 2,5 г |
Феноловый красный | 2,5 мл 0,4%-го водно-щелочного раствора |
Вода дистиллированная | до 500,0 мл |
Мочевина | 10,0 мл 50%-го водного раствора |
Для приготовления 100 мл 1/15 М фосфатного буфера pH 7,0 в отдельных емкостях подготовить 1/15 М растворы калия дигидрофосфата (9,078 г KH2PO4 на 1 л дистиллированной воды) и натрия гидрофосфата (11,876 г Na2HPO4·2H2O на 1 л дистиллированной воды), смешать 40 мл раствора калия дигидрофосфата и 60 мл раствора натрия гидрофосфата [9]. При необходимости корректировать pH изменением соотношения фосфатов.
Для приготовления 0,4%-го водно-щелочного раствора фенолового красного сухой краситель в количестве 0,1 г растереть в ступке в 5,7 мл 1/20 N раствора щелочи (концентрация NaOH 2 г/л), после растворения добавить дистиллированную воду до 25 мл.
Для приготовления 50%-го раствора мочевины 50,0 г мочевины растворить в 100,0 мл дистиллированной воды, стерилизовать фильтрованием или выдержать раствор 2 - 3 суток для "самостерилизации".
Смешать компоненты среды (кроме мочевины), стерилизовать автоклавированием плюс 121 °C 20 мин, охладить, асептично добавить 10 мл 50%-го раствора мочевины. Среду использовать без повторной стерилизации, хранить при температуре (6 +/- 2) °C.
Состав:
Бульон Хоттингера | 1000,0 мл |
Агар | 15,0 г |
D-Глюкоза | 5,0 г |
Бромтимоловый синий (водорастворимый) | 0,02 г |
Мочевина | 20,0 мл 50%-го водного раствора |
Ингредиенты (кроме мочевины) растворить в бульоне при подогревании, профильтровать, установить pH 6,9 - 7,0. Стерилизовать автоклавированием при плюс 121 °C 20 мин. К стерильной среде асептически добавить раствор мочевины (приготовление согласно пункту 4 приложения 1 к настоящим МР). Разлить в пробирки, охладить в наклонном положении. Цвет готовой среды светло-зеленый (оливковый).
Состав:
Пептон ферментативный | 5,0 г |
D-Глюкоза | 1,0 г |
L-Аминокислота (лизин/орнитин) | 10,0 г |
Бромкрезоловый пурпурный | 0,6 мл 1,6%-го спиртового раствора |
Крезоловый красный | 5,0 мл 0,1%-го спиртового раствора |
Вода дистиллированная | до 1000,0 мл |
Белковая питательная основа может дополнительно содержать 5 г мясного или 3 г дрожжевого экстракта [13, 18].
Компоненты среды растворить в воде, при необходимости профильтровать, установить pH 6,0 - 6,1. Внести растворы индикаторов, перемешать, разлить в пробирки по 2 - 3 мл. Стерилизовать автоклавированием при плюс 112 °C 30 мин. Контрольная среда не содержит аминокислоту.
Состав:
Пептон ферментативный | 10,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Углевод | 5,0 - 10,0 г (0,5 - 1,0%) |
Индикатор | 10,0 мл индикатора Андреде или 1,0 мл 1,6%-го щелочного раствора бромтимолового синего |
Вода дистиллированная | до 1000,0 мл |
Для приготовления индикатора Андреде 1,0 г кислого фуксина растворить в 64 мл 1 N растворе гидроксида натрия (концентрация NaOH 40 г/л), после растворения добавить 400 мл дистиллированной воды, выдержать 24 ч в термостате при (37 +/- 1) °C и затем 48 ч при комнатной температуре на свету. Хранить готовый индикатор в емкости темного стекла с резиновой или притертой пробкой.
В качестве индикатора pH используют бромтимоловый синий в виде 1,6%-го щелочного раствора (пункт 1 приложения 1 к настоящим МР).
Пептон растворить в воде при нагревании, охладить до плюс 50 °C, профильтровать. Добавить хлорид натрия и индикатор, профильтровать, установить pH 7,1 - 7,4, стерилизовать автоклавированием при плюс 121 °C 15 мин.
К стерильной питательной основе добавить соответствующий углевод до конечной концентрации 1% (сахароза), либо 0,5% (L-рамноза, мелибиоза, раффиноза, 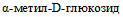 , мальтоза, L-сорбоза, салицин, D-ксилоза, трегалоза, L-арабиноза, D-сорбитол). Среды с углеводами стерилизовать при плюс 112 °C в течение 20 мин [9].
, мальтоза, L-сорбоза, салицин, D-ксилоза, трегалоза, L-арабиноза, D-сорбитол). Среды с углеводами стерилизовать при плюс 112 °C в течение 20 мин [9].
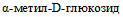 , мальтоза, L-сорбоза, салицин, D-ксилоза, трегалоза, L-арабиноза, D-сорбитол). Среды с углеводами стерилизовать при плюс 112 °C в течение 20 мин [9].
, мальтоза, L-сорбоза, салицин, D-ксилоза, трегалоза, L-арабиноза, D-сорбитол). Среды с углеводами стерилизовать при плюс 112 °C в течение 20 мин [9].Согласно другому способу, углеводы стерилизовать в виде 10%-го водного раствора при плюс 121 °C в течение 10 мин или фильтрацией (диаметр пор мембранного фильтра - не более 0,22 мкм), после стерилизации раствор углевода асептично добавить до конечной концентрации 0,5 - 1,0% к стерильной питательной основе [13, 18].
8. Среда Строгова для определения индолообразования [8]
Состав:
L-Триптофан | 2,5 г (до 0,5%) |
Хлорид натрия (NaCl) | 5,0 г |
Гидрофосфат калия (K2HPO4) | 2,5 г |
Вода дистиллированная | до 1000,0 мл |
Растворить компоненты среды в воде, разлить в пробирки по 2 - 3 мл, стерилизовать автоклавированием при плюс 100 °C в течение 40 мин, pH среды 7,2 - 7,4.
Состав:
Изоамиловый спирт | 75,0 мл |
Пара-диметиламинобензальдегид | 5,0 г |
Соляная кислота (конц.) (HCl) | 25,0 мл |
Растворить 5 г пара-диметиламинобензальдегида в 75 мл амилового спирта, затем медленно добавить 25 мл концентрированной соляной кислоты. Готовый реактив прозрачный желтого цвета. Хранить без доступа света в условиях холодильника не более 3 - 4 недель.
Состав:
Пептон | 5,0 г |
D-Глюкоза | 5,0 г |
Гидрофосфат калия (K2HPO4) | 5,0 г |
Вода дистиллированная | до 1000,0 мл |
Компоненты растворить в воде, профильтровать через бумажный фильтр, установить pH 6,9 - 7,0, разлить по 3 - 5 мл в пробирки. Стерилизовать автоклавированием при плюс 112 °C 20 мин, pH среды 6,9 - 7,0.
Реактив 1
5%-й спиртовой раствор 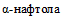 : : | |
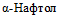 | 5,0 г |
96%-й этиловый спирт | 100,0 мл |
Реактив 2
40%-й раствор гидроксида калия: | |
Гидроксид калия (KOH) | 40,0 г |
Дистиллированная вода | 100,0 мл |
Примечание: готовый раствор 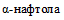 хранить не более 1 года в темной посуде при (26 +/- 2) °C.
хранить не более 1 года в темной посуде при (26 +/- 2) °C.
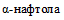 хранить не более 1 года в темной посуде при (26 +/- 2) °C.
хранить не более 1 года в темной посуде при (26 +/- 2) °C.Состав:
Цитрат натрия (Na3C6H5O7) | 2,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Сульфат магния семиводный (MgSO4·7H2O) | 0,2 г |
Дигидрофосфат аммония (NH4H2PO4) | 1,0 г |
Гидрофосфат калия (K2HPO4) | 1,0 г |
Бромтимоловый синий | 0,08 г или 5 мл 1,6%-го спиртового раствора |
Агар микробиологический | 20,0 г |
Дистиллированная вода | до 1000,0 мл |
Соли и индикатор растворить в воде, установить pH 6,9 - 7,0. После добавления агара довести до кипения, тщательно перемешивая среду. Разлить в пробирки по 5 - 7 мл и стерилизовать при плюс 121 °C 15 мин или плюс 112 °C 30 мин. При охлаждении сформировать скошенную поверхность и столбик в соотношении по длине 1,5:1.
--------------------------------
<14> ГОСТ ISO 10273.
Состав:
Пепсиновый гидролизат мяса | 10,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Хлорид кальция (CaCl2·H2O) | 0,1 г |
Агар микробиологический от 9,0 до | 18,0 г |
Дистиллированная вода | до 1000,0 мл |
Добавка для 1 л готовой среды: | |
Эфир олеиновой кислоты (Твин 80) | 10,0 мл |
Компоненты основы среды (кроме Твин 80) растворить при нагревании в 1 л дистиллированной воды. Стерилизовать автоклавированием при плюс 121 °C 30 мин, pH основы 7,2 - 7,6. К 990 мл основы среды, охлажденной до плюс 40 °C - плюс 50 °C, добавить 10 мл стерильного Твин 80 (конечная концентрация Твин 80 в среде 1% по объему). Твин 80 предварительно стерилизовать автоклавированием при плюс 121 °C 15 мин. Аккуратно перемешать до полного растворения Твина, разлить в чашки Петри.
Состав:
Мясной экстракт | 3,0 г |
Пептон | 10,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Эскулин | 1,0 г |
Цитрат железа (III) (FeC6H5O7) | 0,5 г |
Дистиллированная вода | до 1000,0 мл |
Ингредиенты растворить в воде при нагревании. Установить pH 7,0 - 7,1. Разлить по 3 - 4 мл в пробирки, стерилизовать при плюс 121 °C 15 мин или плюс 112 °C 30 мин. При охлаждении сформировать скошенную поверхность.
15. Питательная среда с желатином [13]
Состав:
Мясной экстракт | 3,0 г |
Пептон | 5,0 г |
Желатин | 120,0 г |
Дистиллированная вода | до 1000,0 мл |
Растворить пептон и мясной экстракт в воде. К питательной основе добавить желатин, оставить при комнатной температуре на 1 - 2 ч для набухания, подогреть на водяной бане при плюс 40 °C - плюс 50 °C до полного растворения желатина. Разлить по 8 - 9 мл в стерильные пробирки, стерилизовать автоклавированием при плюс 121 °C в течение 12 мин, охладить пробирки в вертикальном положении.
В качестве другой белковой питательной основы используют бульон Хоттингера [9].
16. Состав среды для определения триптофандезаминазы [5]
Состав:
L-Триптофан | 5,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Пептон | 10,0 г |
Вода дистиллированная | до 1000,0 мл |
Ингредиенты растворить в воде, профильтровать, разлить в пробирки по 2 - 3 мл. Стерилизовать автоклавированием при плюс 121 °C 30 мин.
Состав:
Хлорид железа (III) гексагидрат (FeCl3·6H2O) | 10 г |
Вода дистиллированная | до 100 мл |
Соль растворить в воде для получения 10%-го водного раствора хлорида железа (III). Реактив хранить при (6 +/- 2) °C без доступа света.
Состав среды:
Питательная основа | 30,0 г |
Дрожжевой экстракт | 3,0 г |
Пиразинамид (пиразинкарбоксиамид) | 1,0 г |
0,2 М Трис-малеатный буфер pH 6,0 | до 1000,0 мл |
Состав 0,2 М Трис-малеатного буфера pH 6,0: | |
Раствор 1: | |
Трис(гидроксиметил)аминометан | 24,2 г |
Малеиновая кислота | 23,2 г |
Дистиллированная вода | до 1000,0 мл |
Раствор 2: | |
Гидроксид натрия (NaOH) | 8,0 г |
Дистиллированная вода | до 1000,0 мл |
Для приготовления 0,2 М Трис-малеатного буферного раствора pH 6,0 смешать 250 мл раствора 1 и 130 мл раствора 2, добавить дистиллированную воду до 1000 мл [10].
В буферный раствор добавить питательную основу (по типу агара Хоттингера), дрожжевой экстракт и растворить при нагревании. Добавить пиразинамид. Среду разлить по 5 мл в пробирки, стерилизовать автоклавированием при плюс 121 °C 20 мин. Охладить среду в наклонном положении для формирования скоса длиной 5 - 6 см. Готовую среду хранить при (6 +/- 2) °C.
19. Реактив для выявления пиразинамидазы [13]
Состав:
Сульфат аммонийного железа гексагидрат ((NH4)2Fe(SO4)2·6H2O) | 1,0 г |
Дистиллированная вода | до 100,0 мл |
Растворить в воде навеску соли, использовать в день приготовления.
20. Полужидкий питательный агар для определения подвижности [13]
Состав:
Пептон ферментативный | 10,0 г |
Мясной экстракт | 3,0 г |
Хлорид натрия (NaCl) | 5,0 г |
Агар микробиологический | 4,0 г |
Вода дистиллированная | до 1000,0 мл |
Растворить компоненты в воде, установить pH 7,2 - 7,4; добавить агар, расплавить при нагревании, профильтровать. Готовая среда должна быть прозрачной. Разлить по 8 мл в пробирки, стерилизовать автоклавированием при плюс 121 °C 15 мин, охладить в вертикальном положении.
21. Готовые питательные среды и тест-системы, зарегистрированные и разрешенные для использования на территории Российской Федерации:
- агар Хоттингера;
- бульон Хоттингера;
- агар Шимана (основа селективного агара для иерсиний) и селективная добавка для иерсиний;
- тест-система для идентификации и дифференциации энтеробактерий и других неприхотливых грамотрицательных палочек;
- среда с мочевиной по Преусу;
- агар с мочевиной по Кристенсену;
- бульон с мочевиной по Кристенсену;
- полиуглеводные среды с мочевиной (агар Олькеницкого и др.);
- среда для определения орнитиндекарбоксилазы;
- среда для определения лизиндекарбоксилазы;
- среда Гисса с рамнозой/арабинозой/ксилозой/мальтозой/раффинозой/салицином/сахарозой/сорбитом и др.;
- питательная среда для определения образования индола;
- реактив Эрлиха для определения образования индола;
- бульон для определения уреазы, продукции индола и подвижности;
- среда Кларка для реакции Фогеса-Проскауэра;
- реактив для реакции Фогеса-Проскауэра;
- среда Симмонса (цитратный агар);
- среда для определения подвижности.
Таблица 1
Оборудование для приготовления питательных сред
и проведения исследования
Наименование оборудования | Обозначение и наименование документов, технические характеристики |
Анализатор потенциометрический (pH-метр) | Диапазон измерения pH от 3,0 до 8,0 с точностью +/- 0,01 ед. pH при температуре плюс 25 °C |
Баня водяная с терморегулятором | Диапазон поддерживаемой температуры T окр. +5 ... +100 °C |
Весы электронные | Диапазон измерений до 400 г. Класс точности или погрешность +/- 10 мг ГОСТ 8.520 |
Денситометр для бактериальных суспензий | - |
Механические или электронные одноканальные или многоканальные дозаторы переменного объема | Диапазоны измерений: - 100 - 1000 мкл ССП +/- (1,5 - 1,0)%, СКО 2,0 - 1,0%; - 1000 - 5000 мкл ССП +/- 1,0%, СКО 1,0% ГОСТ 28311 |
Микроскоп биологический стереоскопический | Диапазон увеличения 10x - 80x ТУ 3-3-1210 |
Плита электрическая | - |
Стерилизатор паровой | Рабочее давление пара 2,4 кгс/см2 (или 3,0 кгс/см2), температура (плюс 136 +/- 1) °C |
Термостат электрический суховоздушный | Диапазон рабочих температур: T окр. +5 ... +60 °C, +/- 0,4 °C |
Термостат электрический суховоздушный с охлаждением | Диапазон рабочих температур: +5 ... +60 °C, +/- 1,5 °C (или +5 ... +70 °C, +/- 0,5 °C) |
Холодильник фармацевтический | Диапазон рабочих температур: +2 ... +15 °C, +/- 2 °C |
Шкаф сушильный стерилизационный | Диапазон рабочих температур: +50 ... +200 °C, +/- 4 °C |
Примечание. Допускается использование оборудования с аналогичными или лучшими техническими характеристиками. | |
Таблица 2
Материалы и химические реактивы для приготовления
питательных сред и проведения исследования
Наименование материалов | Обозначение и наименование документов, технические характеристики |
1 | 2 |
Компоненты питательных сред (продукты животного и растительного происхождения и др.): | |
Дрожжевой экстракт | - |
Желатин | |
Желчные соли | - |
Желчь очищенная | - |
Мясной экстракт | - |
Панкреатический гидролизат рыбной муки | - |
Пепсиновый гидролизат мяса | - |
Пептон ферментативный | |
Ферментативный гидролизат желатина | - |
Ферментативный гидролизат казеина и тканей животных | - |
Углеводы, спирты: | |
L-Арабиноза | - |
D-Ксилоза | - |
Мальтоза | - |
Мелибиоза | - |
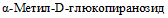 ( (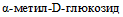 ) ) | - |
L-Рамноза | - |
Раффиноза | - |
Салицин | - |
Сахароза | |
D-Сорбитол (D-сорбит) | - |
L-Сорбоза (L-сорбиноза) | - |
Спирт изоамиловый | |
Спирт этиловый 96% | |
Трегалоза | - |
Эскулин | - |
Аминокислоты: | |
L-Лизин дигидрохлорид | - |
L-Орнитин дигидрохлорид | - |
L-Триптофан | - |
Индикаторы: | |
Бриллиантовый зеленый | - |
Бромкрезоловый пурпурный | - |
Бромтимоловый синий | ТУ 6-09-5423 |
Крезоловый красный | - |
Кристаллический фиолетовый | - |
Нейтральный красный | - |
Феноловый красный | - |
Фуксин кислый | - |
Противомикробные препараты: | |
Иргазан | - |
Новобиоцин | - |
Цефсулодин | - |
Химические реактивы и другие компоненты питательных сред (органические и неорганические соединения и др.): | |
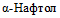 | - |
Аммония дигидрофосфат NH4H2PO4 (фосфорнокислый аммоний, однозамещенный) | ГОСТ 3771 |
Вода дистиллированная | |
Железа аммонийного сульфат шестиводный (NH4)2Fe(SO4)2·6H2O (Соль Мора) | |
Железа хлорид (III) (FeCl3) | |
Железа цитрат (III) FeC6H5O7 (лимоннокислое железо) | - |
Калия гидроксид KOH (гидроокись калия) | |
Калия гидрофосфат K2HPO4 (фосфорнокислый калий двузамещенный) | |
Калия дигидрофосфат KH2PO4 (калий фосфорнокислый однозамещенный) | |
Кальция хлорид CaCl2·H2O | |
Магния сульфат семиводный MgSO4·7H2O (сернокислый магний) | |
Малеиновая кислота H4C4O4 (цис-бутендиовая кислота) | ГОСТ 9803 |
Минеральное масло (вазелиновое масло) | |
Мочевина (NH2)2CO (диамид угольной кислоты) | |
Натрия гидроксид NaOH (гидроокись натрия) | |
Натрия гидрофосфат Na2HPO4 (фосфорнокислый натрий двузамещенный) | |
Натрия дезоксихолат C24H39NaO4 | - |
Натрия пируват C3H3O3Na | - |
Натрия тиосульфат 5-водный Na2S2O3·5H2O (гипосульфит) | |
Натрия хлорид NaCl (хлористый натрий) | |
Натрия цитрат Na3C6H5O7 | |
Пара-диметиламинобензальдегид (CH3)2NC6H4CHO | - |
Пиразинамид | - |
Соляная кислота HCl (конц.) (хлороводородная кислота) | |
Трис(гидроксиметил)аминометан (HOCH2)3CNH2 (трис) | - |
Трис(гидроксиметил)аминометан (HOCH2)3CNH2 (трис) | - |
Эфир олеиновой кислоты (Твин 80) | - |
Примечание. Допускается использование материалов и химических реактивов с аналогичными или лучшими характеристиками. | |
Таблица 3
Вспомогательные расходные материалы для приготовления
питательных сред и проведения исследования
Бумага фильтровальная лабораторная | |||||
| |||||
Вата медицинская гигроскопическая | ГОСТ 2556 | ||||
Мембранные фильтры для стерилизующей фильтрации растворов с диаметром пор 0,2 мкм | - | ||||
Наконечники для дозаторов переменного объема (до 200 мкл, до 1000 мкл, до 5000 мкл) | - | ||||
Отраслевой стандарт для визуальной оценки мутности ОСО 42-28-85 | - | ||||
Пакеты бумажные для стерилизации лабораторных принадлежностей | ТУ 9398-020-11764404 | ||||
Пакеты полимерные для стерилизации лабораторных принадлежностей и обеззараживания отходов | - | ||||
Петли микробиологические диаметром 1 - 4 мм | - | ||||
Пипетки градуированные вместимостью 5,0 мл, 10,0 мл | |||||
Планшеты иммунологические 96-луночные стерильные | - | ||||
Пробирки стеклянные типов П1, П2 | |||||
Пробки силиконовые, целлюлозные, ватно-марлевые для стеклянных колб, флаконов, пробирок | - | ||||
Спиртовка СЛ-2 | |||||
Ступка с пестиком лабораторная | |||||
Термометр ртутный с диапазоном измерения от 0 до 100 °C (цена деления шкалы 1 °C) | |||||
Флаконы и колбы стеклянные вместимостью 250, 500, 1000, 2000 см3 | |||||
Цилиндры мерные по 50, 100, 500 и 1000 мл | |||||
Чашки биологические (Петри) стеклянные или одноразовые из полимерных материалов диаметром 90 или 100 мм | |||||
Штативы для пробирок лабораторных | - | ||||
Примечание. Допускается использование расходных материалов с аналогичными или лучшими техническими характеристиками. | |||||
к МР 4.2.0292-22
(ЗА ИСКЛЮЧЕНИЕМ Y. PESTIS) <15>
--------------------------------
<15> Данные биохимической активности приведены в соответствии с литературными источниками [9, 20, 22, 23, 24, 25, 27, 32, 33, 39, 40, 42, 43, 44, 45, 46, 47, 48, 49, 54, 55, 59, 60, 61, 62, 64, 65, 73, 74].
Вид Биохимические свойства | Y. aldovae | Y. aleksiciae | Y. alsatica <1> | Y. artesiana <1> | Y. bercovieri | Y. canariae <1> | Y. enterocolitica | Y. entomophaga <1> | Y. frederiksenii | Y. hibernica <1> | Y. intermedia | Y. kristensenii | Y. massiliensis <1> | Y. mollaretii | Y. nurmii <1> | Y. pekkanentii <1> | Y. proxima <1> | Y. pseudotuberculosis | Y. rochesterensis <1> | Y. rohdei | Y. ruckeri | Y. similis | Y. thracica <1> | Y. vastinensis <1> | Y. wautersii <1> |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 |
Гидролиз мочевины | + <2> | + | + | + | + <2> | + | + <2> | - | + <2> | + | + <2> | + <2> | + | + <3> | - | + | + | + | + | B <4> | - | + | + | + | + |
Образование индола | - | B | + | + | - | + | B <5> | - | + | - | + | B | + | - | - | - | + | - | [+] | - | - | - | - | + | - |
Образование ацетоина (26 +/- 2) °C | + | - | + | + | - | - | + <6> | + | [+] | - | + | - | - <7> | - | + | - | + | - | - | - | [-] | - | - | + | - |
Образование ацетоина (37 +/- 1) °C | - | нд | нд | нд | - | - | - | нд | - | - | - | - | нд | - | нд | нд | нд | - | нд | - | - | нд | нд | нд | нд |
Орнитиндекарбоксилаза | + <2> | + | B | [-] | + <2> | - | + <6> | + | + | + | + | + | + | + <2> | + | - | B | - | + <2> | [+] <2> | + | - | B | [+] | - |
Лизиндекарбоксилаза | - | B | - | - | - | - | - | - | - | - | - | - | B | - | - | - | - | - | - | - | [+] <2> | - | - | - | - |
Триптофандезаминаза | - | - | - | - | - | - | - | нд | - | - | - | - | нд | - | нд | - | - | - | - | - | - | нд | - | - | - |
Аргининдигидролаза | - | - | - | - | - | - | - | нд | - | - | - | - | нд | - | нд | - | - | - | - | - | - | нд | - | - | - |
Гидролиз эскулина | - | - | + | + | B <3> | B | B <5> | - | + <2> | B | [+] <3> | - | + | [-] | - | - | + | + | - | - | - | + | - | + | + |
Гидролиз желатина | - | - | - | - | - | - | - | нд | - | - | - | - | - | - | + | - | - | - | - | - | [+] <4> | - | - | - | - |
Утилизация цитрата (26 +/- 2) °C | B | - | B | - | - | - | - | + | B | - | B <5> | - | B | - | + | - | B | - | [-] | B <4> | [+] <4> | - | - | - | - |
Подвижность <8> (22 +/- 2) °C | + | нд | нд | нд | + | нд | + | + | + | нд | + | + | нд | + | нд | нд | нд | + | + | + | B <5> | нд | нд | нд | нд |
Подвижность (37 +/- 1) °C | - | нд | нд | нд | - | нд | - | + | - | нд | - | - | - | - | нд | - | нд | - | нд | - | - | нд | нд | нд | нд |
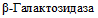 (ОНПГ) (ОНПГ) | B | + | + | + | [+] | + | + <6> | + | + | B | + | + <2> | + | + <3> | + | + | + | + | + <2> | + <2> | + <2> | + | B | + | + |
Липаза (среда с Твин-80) | B | - | + | - | - | + | B <5> | + | B | B | B | B | - | - | + | - | + | - | B | - | B <5> | - | [-] | [-] | - |
Пиразинамидаза | + | + | + | + | + | - | B <5> | + | + | + | + | + | + | + | + | + | + | - | B | + | + | + | + | + | - |
Образование кислоты из: | |||||||||||||||||||||||||
Сахарозы | [-] | - | + | + | + | + | + <6> | + | + | - | + | - | + | + | + | - | + | - | - | + | - | - | - | + | - |
Салицина | - | - | + | + | [-] | B | B <5> | - | + | B | + | - | + | [-] | - | - | + | B | - | [-] | - | B | - | + | B |
D-Ксилозы | + <2> | + | + | + | + | + | B <5> | - | + | + | + | + <2> | + | + <2> | - | + | + | + | + | + <2> | - | + | + | + | + |
D-Сорбитола | + <2> | + | + | + | + | + | B <5> | - | + | + | + | + | + | + | - | - | + | - | + | + | B | - | + | + | - |
Трегалозы | + | + | + | + | + | + | B <5> | + | + | B | + | + | + | + | + | + | + | + | + | + | + | + | + | + | + |
Мелибиозы | - | - | - | - | - | - | - | + | - | - | B <5> | - | - | - | - | - | - | [+] <2> | - | B <5> | - | - | - | - | + |
L-Рамнозы | + <3> | - | + | - | - | - | - | - | + | - | B <5> | - | - | - | - | - | - | + <2> | - | - | - | + | - | + | + |
Раффинозы | - | - | - | - | - | - | - | + | - | - | B <5> | - | - | - | - | - | - | - | - | B <5> | - | - | - | - | + |
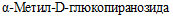 | - | нд | - | - | - | нд | - | нд | - | нд | B <5> | - | - | - | нд | нд | - | - | - | - | - | нд | - | - | нд |
Лактозы | - | - | - | + | [-] | + | [-] | + <2> | B | - | B | [-] | - | - | - <7> | - <7> | + | - | B | B <3> | - | - | [-] | + | - |
L-Сорбозы | - | B | + | + | - | + | B <5> | - | + | + | + | + | + | + | - | - | + | - | [+] | B | - | - | + | + | - |
Мальтозы | [-] | + | + | + | + | + | + | + | + | B | + | + | + | + | + | + | + | + | + | [+] <3> | + | + | + | + | + |
L-Арабинозы | + <2> | + | + | + | + | + | + | - | + | + | + | [+] | + | + | - | + | + | [+] | + <2> | + | - | + | + | + | + |
Целлобиоза | - | + | + | + | + | + | B <5> | + <2> | + | B | + | + | + | + | - <7> | + | + | - | + | + <2> | - | - | + | + | - |
D-Адонитола | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | нд |
Дульцитола | - | нд | - | - | - | нд | - | нд | - | нд | - | - | нд | - | нд | нд | - | - | - | - | - | нд | - | - | - |
D-Маннитола | + | + | + | + | + | + | + | нд | + | + | + | + | + | + | + | + | + | + | + | + | + | нд | + | + | + |
D-Маннозы | + | нд | + | + | + | нд | + | нд | + | + | + | + | нд | + | нд | нд | + | + | + | + | + | нд | + | + | + |
Примечания: "+" - положительная реакция у 90% и более штаммов; "[+]" - положительная реакция у 76 - 89% штаммов; "B" - положительная реакция у 26 - 75% штаммов; "[-]" - положительная реакция у 11 - 25% штаммов; "-" - отрицательная реакция у 90% и более штаммов; нд - нет данных; <1> - данные ограничены, так как в публикациях отсутствует полная информация о биохимической активности штаммов новых видов; | |||||||||||||||||||||||||
к МР 4.2.0292-22
ВИДОВ YERSINIA
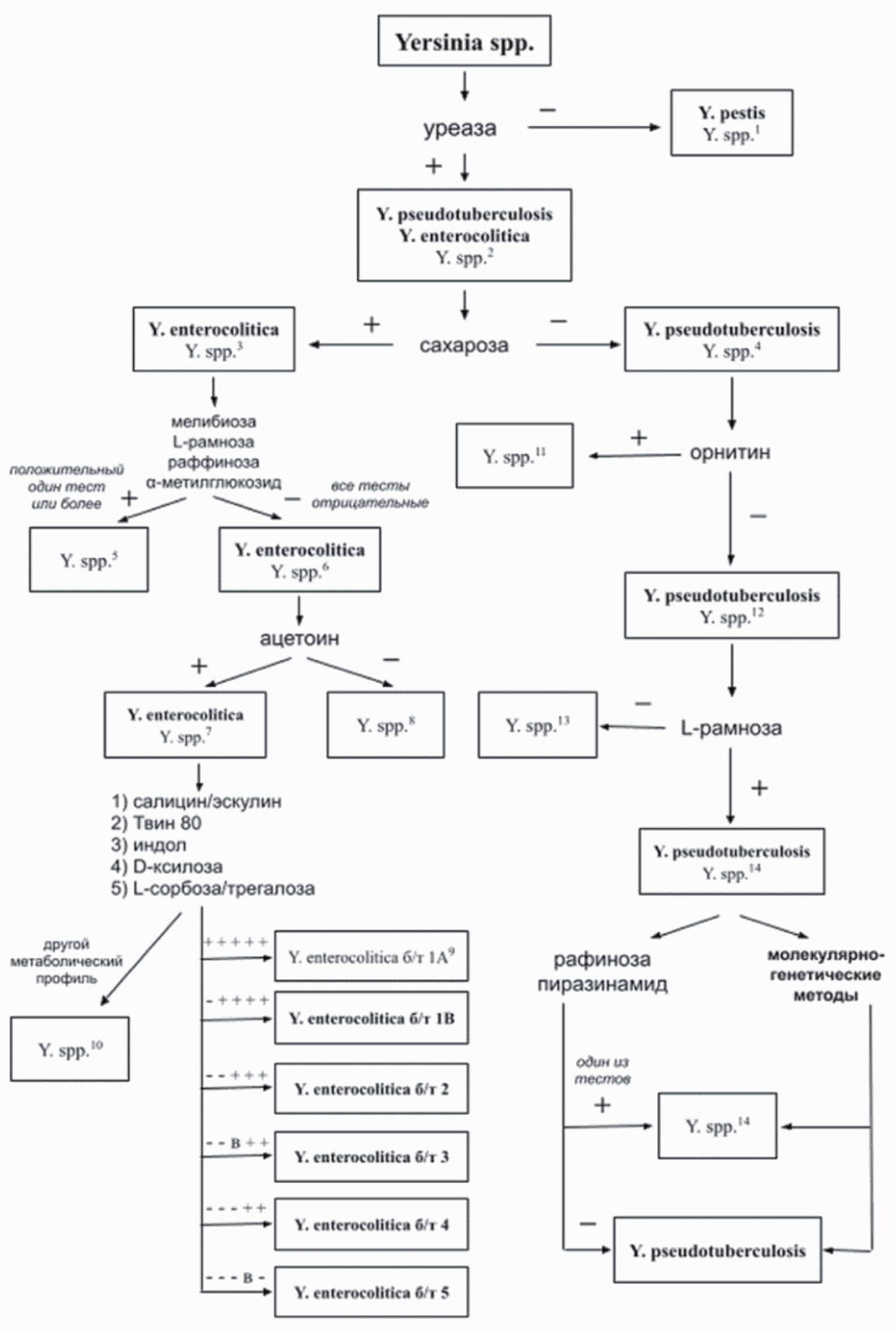
Примечания:
Y. spp. <1> - <14> - виды иерсиний, непатогенные для человека. Виды указаны в соответствии с метаболическими свойствами:
Y. spp. <1> - Y. entomophaga, Y. nurmii, Y. rohdei (уреаза -), Y. ruckeri.
Y. spp. <2> - Y. aldovae, Y. aleksiciae, Y. alsatica, Y. artesiana, Y. bercovieri, Y. canariae, Y. frederiksenii, Y. hibernica, Y. intermedia, Y. kristensenii, Y. massiliensis, Y. mollaretii, Y. pekkanenii, Y. proxima, Y. rochesterensis, Y. rohdei (уреаза +), Y. similis, Y. thracica, Y. vastinensis, Y. wautersii.
Y. spp. <3> - Y. aldovae (сахароза +), Y. alsatica, Y. artesiana, Y. bercovieri, Y. canariae, Y. frederiksenii, Y. intermedia, Y. massiliensis, Y. mollaretii, Y. proxima, Y. rohdei (уреаза +), Y. vastinensis.
Y. spp. <4> - Y. aldovae (сахароза -), Y. aleksiciae, Y. hibernica, Y. kristensenii, Y. pekkanenii, Y. rochesterensis, Y. similis, Y. thracica, Y. wautersii.
Y. spp. <5> - Y. aldovae (сахароза +), Y. alsatica, Y. frederiksenii, Y. intermedia, Y. rohdei (уреаза +, 1 б/т), Y. vastinensis.
Y. spp. <6> - Y. artesiana, Y. bercovieri, Y. canariae, Y. massiliensis, Y. mollaretii, Y. proxima, Y. rohdei (уреаза +; 2 б/т).
Y. spp. <7> - Y. artesiana, Y. massiliensis (ацетоин +), Y. proxima.
Y. spp <8> - Y. bercovieri, Y. canariae, Y. massiliensis, Y. mollaretii, Y. rohdei (уреаза +; 2 б/т).
Y. spp. <9> - Y. enterocolitica б/т 1A и Y. proxima имеют схожий ферментативный профиль и различаются по ферментации L-фукозы [40].
Y. spp. <10> - Y. artesiana, Y. massiliensis (ацетоин +).
Y. spp. <11> Y. aldovae (сахароза -), Y. aleksiciae, Y. hibernica, Y. kristensenii, Y. rochesterensis, Y. thracica (орнитин +).
Y. spp. <12> - Y. pekkanenii, Y. similis, Y. thracica (орнитин -), Y. wautersii.
Y. spp. <13> - Y. pekkanenii, Y. thracica (орнитин -).
Y. spp. <14> - Y. similis, Y. wautersii.
к МР 4.2.0292-22
Пример 1. В тест-систему включены тесты для определения таких признаков, как наличие 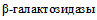 , аргининдигидролазы, лизиндекарбоксилазы, орнитиндекарбоксилазы, уреазы, тринтофандезаминазы, желатиназы, образование сероводорода, индола, ацетоина, утилизации цитрата, D-глюкозы, D-маннитола, инозитола, D-сорбитола, L-рамнозы, сахарозы, мелибиозы, амигдалина, L-арабинозы. Данных тестов недостаточно, чтобы:
, аргининдигидролазы, лизиндекарбоксилазы, орнитиндекарбоксилазы, уреазы, тринтофандезаминазы, желатиназы, образование сероводорода, индола, ацетоина, утилизации цитрата, D-глюкозы, D-маннитола, инозитола, D-сорбитола, L-рамнозы, сахарозы, мелибиозы, амигдалина, L-арабинозы. Данных тестов недостаточно, чтобы:
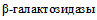 , аргининдигидролазы, лизиндекарбоксилазы, орнитиндекарбоксилазы, уреазы, тринтофандезаминазы, желатиназы, образование сероводорода, индола, ацетоина, утилизации цитрата, D-глюкозы, D-маннитола, инозитола, D-сорбитола, L-рамнозы, сахарозы, мелибиозы, амигдалина, L-арабинозы. Данных тестов недостаточно, чтобы:
, аргининдигидролазы, лизиндекарбоксилазы, орнитиндекарбоксилазы, уреазы, тринтофандезаминазы, желатиназы, образование сероводорода, индола, ацетоина, утилизации цитрата, D-глюкозы, D-маннитола, инозитола, D-сорбитола, L-рамнозы, сахарозы, мелибиозы, амигдалина, L-арабинозы. Данных тестов недостаточно, чтобы:1) установить некоторые биотипы штаммов Y. enterocolitica (1A, 1B, 2); 2) дифференцировать между собой иерсинии видов:
а) Y. enterocolitica и Y. massiliensis;
б) Y. frederiksenii и Y. intermedia (биотип 8, 9, 10);
в) Y. bercovieri и Y. mollaretii;
г) Y. similis, Y. pseudotuberculosis и Y. wautersii;
д) Y. kristensenii/Y. aleksiciae и Y. hibernica.
Для повышения качества видовой идентификации иерсиний такую тест-систему используют с дополнительными отдельными тестами: утилизации салицина/эскулина, раффинозы, L-сорбозы, мальтозы, D-ксилозы, трегалозы, 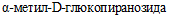 , Твин 80.
, Твин 80.
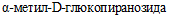 , Твин 80.
, Твин 80.Пример 2. В тест-систему включены тесты для определения следующих признаков: образование сероводорода, наличие лизиндекарбоксилазы, орнитиндекарбоксилазы, уреазы, аргининдигидролазы, 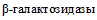 ,
, 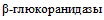 ,
, 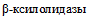 , утилизация цитрата, малоната, ферментация салицина, D-сорбитола, мелибиозы, целлобиозы, лактозы, трегалозы, D-маннитола, дульцитола, D-адонитола, артрата, сахарозы, инозитола, раффинозы, гидролиз эскулина. При использовании такой тест-системы затруднена дифференциация иерсиний многих видов, прежде всего патогенных Y. enterocolitica и непатогенных Y. bercovieri и Y. mollaretii. Тест-система не дифференцирует Y. similis и Y. pseudotuberculosis. По ферментации салицина и гидролизу эскулина устанавливают принадлежность штаммов Y. enterocolitica только к биотипу 1A (непатогенные). Недостаточно тестов для дифференциации Y. enterocolitica биотипа 1A, Y. frederiksenii и Y. intermedia (биотипы 9, 10), Y. massiliensis. В случае применения такой тест-системы следует дополнительно выполнять тесты на образование индола и ацетоина, ферментацию L-рамнозы, L-сорбозы, мальтозы,
, утилизация цитрата, малоната, ферментация салицина, D-сорбитола, мелибиозы, целлобиозы, лактозы, трегалозы, D-маннитола, дульцитола, D-адонитола, артрата, сахарозы, инозитола, раффинозы, гидролиз эскулина. При использовании такой тест-системы затруднена дифференциация иерсиний многих видов, прежде всего патогенных Y. enterocolitica и непатогенных Y. bercovieri и Y. mollaretii. Тест-система не дифференцирует Y. similis и Y. pseudotuberculosis. По ферментации салицина и гидролизу эскулина устанавливают принадлежность штаммов Y. enterocolitica только к биотипу 1A (непатогенные). Недостаточно тестов для дифференциации Y. enterocolitica биотипа 1A, Y. frederiksenii и Y. intermedia (биотипы 9, 10), Y. massiliensis. В случае применения такой тест-системы следует дополнительно выполнять тесты на образование индола и ацетоина, ферментацию L-рамнозы, L-сорбозы, мальтозы, 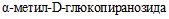 и гидролиз Твин 80.
и гидролиз Твин 80.
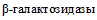 ,
, 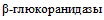 ,
, 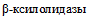 , утилизация цитрата, малоната, ферментация салицина, D-сорбитола, мелибиозы, целлобиозы, лактозы, трегалозы, D-маннитола, дульцитола, D-адонитола, артрата, сахарозы, инозитола, раффинозы, гидролиз эскулина. При использовании такой тест-системы затруднена дифференциация иерсиний многих видов, прежде всего патогенных Y. enterocolitica и непатогенных Y. bercovieri и Y. mollaretii. Тест-система не дифференцирует Y. similis и Y. pseudotuberculosis. По ферментации салицина и гидролизу эскулина устанавливают принадлежность штаммов Y. enterocolitica только к биотипу 1A (непатогенные). Недостаточно тестов для дифференциации Y. enterocolitica биотипа 1A, Y. frederiksenii и Y. intermedia (биотипы 9, 10), Y. massiliensis. В случае применения такой тест-системы следует дополнительно выполнять тесты на образование индола и ацетоина, ферментацию L-рамнозы, L-сорбозы, мальтозы,
, утилизация цитрата, малоната, ферментация салицина, D-сорбитола, мелибиозы, целлобиозы, лактозы, трегалозы, D-маннитола, дульцитола, D-адонитола, артрата, сахарозы, инозитола, раффинозы, гидролиз эскулина. При использовании такой тест-системы затруднена дифференциация иерсиний многих видов, прежде всего патогенных Y. enterocolitica и непатогенных Y. bercovieri и Y. mollaretii. Тест-система не дифференцирует Y. similis и Y. pseudotuberculosis. По ферментации салицина и гидролизу эскулина устанавливают принадлежность штаммов Y. enterocolitica только к биотипу 1A (непатогенные). Недостаточно тестов для дифференциации Y. enterocolitica биотипа 1A, Y. frederiksenii и Y. intermedia (биотипы 9, 10), Y. massiliensis. В случае применения такой тест-системы следует дополнительно выполнять тесты на образование индола и ацетоина, ферментацию L-рамнозы, L-сорбозы, мальтозы, 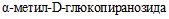 и гидролиз Твин 80.
и гидролиз Твин 80.1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
3. МУ 3.1.1.2438-09 "Эпидемиологический надзор и профилактика псевдотуберкулеза и кишечного иерсиниоза".
4. МУК 4.2.3019-12 "Организация и проведение лабораторных исследований на иерсиниозы на территориальном, региональном и федеральном уровнях".
5. ГОСТ ISO 10273 "Микробиология пищевых продуктов и кормов для животных. Горизонтальный метод выявления условно-патогенной бактерии Yersinia enterocolitica".
6. ГОСТ 24104 Весы лабораторные общего назначения и образцовые. Общие технические условия.
7. ГОСТ 28311 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний.
8. ГОСТ Р ЕН 13060 Стерилизаторы паровые малые.
9. ГОСТ 31598 Стерилизаторы паровые большие. Общие технические требования и методы испытаний.
10. ГОСТ 17206 Агар микробиологический. Технические условия.
11. ГОСТ 23058 Желатин-сырье для медицинской промышленности. Технические условия.
12. ГОСТ 13805 Пептон сухой ферментативный для бактериологических целей. Технические условия.
13. ГОСТ 5833 Реактивы. Сахароза. Технические условия.
14. ГОСТ 5830 Реактивы. Спирт изоамиловый. Технические условия.
15. ГОСТ 5962 Спирт этиловый ректификованный из пищевого сырья. Технические условия.
16. ГОСТ 3771 Реактивы. Аммоний фосфорнокислый однозамещенный. Технические условия.
17. ГОСТ Р 58144 Вода дистиллированная. Технические условия.
18. ГОСТ 4208 Реактивы. Соль закиси железа и аммония двойная сернокислая (соль Мора). Технические условия.
19. ГОСТ 4147 Реактивы. Железо (III) хлорид 6-водный. Технические условия.
20. ГОСТ 24363 Реактивы. Калия гидроокись. Технические условия.
21. ГОСТ 2493 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия.
22. ГОСТ 4198 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия.
23. ГОСТ 450 Кальций хлористый технический. Технические условия.
24. ГОСТ 4523 Реактивы. Магний сернокислый 7-водный. Технические условия.
25. ГОСТ 9803 Реактивы. Кислота малеиновая. Технические условия.
26. ГОСТ 3164 Масло вазелиновое медицинское. Технические условия.
27. ГОСТ 6691 Реактивы. Карбамид. Технические условия.
28. ГОСТ 4328 Реактивы. Натрия гидроокись. Технические условия.
29. ГОСТ 11773 Реактивы. Натрий фосфорно-кислый двузамещенный. Технические условия.
30. ГОСТ 244 Натрия тиосульфат кристаллический. Технические условия.
31. ГОСТ 4233 Реактивы. Натрий хлористый. Технические условия.
32. ГОСТ 22280 Реактивы. Натрий лимоннокислый 5,5-водный. Технические условия.
33. ГОСТ 3118 Реактивы. Кислота соляная. Технические условия.
34. ГОСТ 12026 Бумага фильтровальная лабораторная. Технические условия.
35. ГОСТ 25556 Вата медицинская гигроскопическая. Технические условия.
36. ГОСТ 29227 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
37. ГОСТ 23932 Посуда и оборудование лабораторные стеклянные. Общие технические условия.
38. ГОСТ 9147 Посуда и оборудование лабораторные фарфоровые. Технические условия.
39. ГОСТ 13646 Термометры стеклянные ртутные для точных измерений. Технические условия.
40. ГОСТ 1770 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия. Общие технические условия.
1. Богумильчик, Е.А. Тест-система для дифференциации видов и биотипов бактерий рода Yersinia: патент на изобретение / Е.А. Богумильчик, Г.Я. Ценева, Е.А. Воскресенская. - М., 2014. - Зарегистр. в Гос. реестре изобретений РФ 10.06.2014, RU N 2518 297 С2.
2. Казарникова, А.В. Выделение и характеристика Yersinia ruckeri при гибели карпов в прудах на юге России / А.В. Казарникова [и др.] // Ветеринария. - 2017. - N 8. - С. 19 - 28.
3. Каримова, Т.В. Молекулярно-биологическая характеристика Yersinia enterocolitica, циркулирующих в различных регионах Российской Федерации / Т.В. Каримова [и др.] // Журн. микробиол. эпидемиол., иммунол. - 2012. - N 1. - С. 16 - 21.
4. Кисличкина, А.А. Дифференциация штаммов Yersinia pestis основного, неосновного подвидов и других представителей Yersinia pseudotuberculosis complex / А.А. Кисличкина [и др.] // Молекулярная генетика, микробиология и вирусология. - 2017. - Т. 35, N 2. - С. 43 - 48. doi 10.18821/0208-0613-2017-35-2-43-48.
5. Методические рекомендации по микробиологической диагностике раневых инфекций в лечебно-диагностических учреждениях армии и флота / Добрынин В.М. [и др.] // утв. Нач. Главн. воен.-мед. управл. МО РФ. - СПб.: Савож, 1999. - 75 с.
6. Методы общей бактериологии: Пер. с англ. / Под ред. Ф. Герхардта [и др.], в 3-х т., Т. 3. - М.: Мир, 1984. - 264 с.
7. Микробиологический контроль качества пищевой продукции / Коллективная монография // Под ред. д.м.н., проф. А.Ю. Поповой и акад. РАН И.А. Дятлова. - М.: "Династия", 2020. - с. 255.
8. Руководство по медицинской микробиологии. Общая и санитарная микробиология. Книга I / Колл. авторов // Под ред. Лабинской А.С. - М.: Издательство БИНОМ, 2008. 1080 с.
9. Руководство по медицинской микробиологии. Частная медицинская микробиология и этиологическая диагностика инфекций. Книга II / Колл. Авторов // Под ред. Лабинской А.С., Костюковой Н.Н., Ивановой С.М. - М.: Издательство БИНОМ, 2010. - 1152 с.
10. Справочник биохимика: перев. с англ. / Р. Досон, Д. Эллиот, У. Эллиот, К. Джонс. - М.: Мир, 1991. - 544 с.
11. Справочник по микробиологическим и вирусологическим методам исследования / Под ред. М.О. Биргера. - 3-е изд. перераб. и доп. - М.: Медицина, 1982. - 464 с.
12. Старостина, Н.В. Эпидемиологические и экологические особенности заболеваний, вызываемых Yersinia frederiksenii, Yersinia kristensenii и Yersinia intermedia: автореф. дисс. канд. мед. наук: 14.00.30 / Старостина Наталья Валерьевна. - М., 2000. - 21 с.
13. Фенотипическая идентификация энтеробактерий / Под. ред. И.В. Смирнова. - Рязань: РязГМУ "Макмах", 2001. - 64 с.
14. Храмов, М.В. Дифференциально-диагностическая питательная среда для выделения возбудителей кишечного иерсиниоза и псевдотуберкулеза: патент на изобретение / М.В. Храмов [и др.]. - М., 1997. - Зарегистр. в Гос. реестре изобретений РФ 20.10.1997, RU N 2101342.
15. Ценева, Г.Я. Дифференциально-диагностическая питательная среда для выделения иерсиний: патент на изобретение / Г.Я. Ценева, Ф.Г. Дятлов, В.Г. Мессорош. - М., 1992. - Зарегистр. в Гос. реестре изобретений РФ 30.11.1992, SU N 1778182 A1.
16. Частная медицинская микробиология с техникой микробиологических исследований: учебное пособие / А.С. Лабинская и [др.]; под ред. А.С. Лабинской, Л.П. Блинковой, А.С. Ещиной. - 3-е изд., стер. - СПб: Лань, 2020. - 608 с.
17. Шепелин, А.П. Питательные среды для энтеробактерий / А.П. Шепелин, И.А. Дятлов. - М.: Династия, 2017. - 232 с.
18. Энтеробактерии: руководство для врачей / Под ред. В.И. Покровского. - М.: Медицина, 1985. - 321 с.
19. Adeolu, М. Genome-based phylogeny and taxonomy of the 'Enterobacteriales': proposal for Enterobacterales ord. nov. divided into the families Enterobacteriaceae, Erwiniaceae fam. nov., Pectobacteriaceae fam. nov., Yersiniaceae fam. nov., Hafniaceae fam. nov., Morganellaceae fam. nov., and Budviciaceae fam. nov. / M. Adeolu, S. Alnajar, S. Naushad, S.R. Gupta // Int. J. Syst. Evol. Microbiol. - 2016. - Vol. 66, N 12. - P. 5575 - 5599. doi: 10.1099/ijsem.0.001485.
20. Aleksic, S. Yersinia rohdei sp. nov. isolated from human and dog feces and surface water/S. Aleksic [et al.] // Int. J. Syst. Bacteriol. - 1987. - Vol. 37. - P. 327 - 332.
21. Archer, J.R. Identification of Yersinia spp. with the API 20E / J.R. Archer [et al.] // J. Clin. Microbiol. - 1987. - Vol. 25, N 12. - P. 2398 - 2399.
22. Bercovier, H. Yersinia aldovae (formerly Yersinia enterocolitica-like Group X2): a new species of Enterobacteriaceae isolated from aquatic ecosystems / H. Bercovier [et al.] // Int. J. Syst. Bacteriol. - 1984. - Vol. 34, N 2/ - P. 166 - 172.
23. Bergey's Manual of Systematic Bacteriology. Vol. 2. The Proteobacteria. Part B. The Gammaproteobacteria / D.J. Brenner [et al.] (eds.). - Springer, 2004. - pp. 587 - 608, 838 - 848.
24. Cunningham, S.A. Yersinia kristensenii subsp. rochesterensis subsp. nov., isolated from human feces / S.A. Cunningham, P. Jeraldo, R. Patel // Int. J. Syst. Evol. Microbiol. - 2019. - Vol. 69. - P. 2292 - 2298.
25. Davies, R.L. Morphological and biochemical differences among isolates of Yersinia ruckeri obtained from wide geographical areas / R.L. Davies, G.N. Frerichs // J. Fish Dis. - 1989. - N 12. - P. 357 - 365.
26. Denis, M. A selective chromogenic plate, YECA, for the detection of pathogenic Yersinia enterocolitica: specificity, sensitivity, and capacity to detect pathogenic Y. enterocolitica from pig tonsils / M. Denis [et al.] // J. Pathog. - 2011. - Vol. 2011. - 8 p. doi: 10.4061/2011/296275.
27. Ewing, W.H. Yersinia ruckeri sp. nov., the redmouth (RM) bacterium / W.H. Ewing, A.J. Ross, D.J. Brenner, G.R. Fanning // Int. J. of Syst. Bacteriol. - 1978. - Vol. 28. - P. 37 - 44.
28. Fukushima, H. Geographical heterogeneity between Far Eastern and Western countries in prevalence of the virulence plasmid, the superantigen Yersinia pseudotuberculosis - derived mitogen, and the high-pathogenicity island among Yersinia pseudotuberculosis strains / H. Fukushima [et al.] // J. Clin. Microbiol. - 2001. - Vol. 39, N 10. - P. 3541 - 3547.
29. Fukushima, H. Yersinia enterocolitica and Yersinia pseudotuberculosis detection in foods / H. Fukushima, S. Shimizu, Y. Inatsu // J Pathog. - 2011. - 9 p. doi: 10.4061/2011/735308.
30. Hallanvuo, S. Simplified phenotypic scheme evaluated by 16S rRNA sequencing for differentiation between Yersinia enterocolitica and Y. enterocolitica-like species / S. Hallanvuo, J. Peltola, T. Heiskanen and A. Siitonen // J Clin Microbiol. - 2006. - Vol. 44, N 3. - P. 1077 - 1080.
31. Head, C.B. Comparative study of selective media for recovery of Yersinia enterocolitica / C.B. Head, D.A. Whitty, S. Ratnam // J. Clin. Microbiol. - 1982. - N 16. - P. 615 - 621.
32. Huang, Y. Biochemical and molecular heterogeneity among isolates of Yersinia ruckeri from rainbow trout (Oncorhynchus mykiss, Walbaum) in north west Germany / Y. Huang [et al.] // BMC Veterinary Research. - 2013. - Vol. 9. - N 215. - 9 p. doi: 10.1186/1746-6148-9-215.
33. Hurst, M.R.H. Yersinia entomophaga sp. nov., isolated from the New Zealand grass grub Costelytra zealandica // M.R.H. Hurst [et al.] // Int. J. Syst. Evol. Microbiol. - 2011, - Vol. 61. - P. 844 - 849.
34. Imori, P.F. Virulence-related genes, adhesion and invasion of some Yersinia enterocolitica-like strains suggests its pathogenic potential / P.F. Imori [et al.] // Microb. Pathog. - 2017. - N 104. - P. 72 - 77.
35. Joutsen, S. Yersinia spp. in wild rodents and shrews in Finland / S. Joutsen [et al.] // Vector Born Zoonotic Dis. - 2017. - Vol. 17, N 5. - P. 303 - 311. doi: 10.1089/vbz.2016.2025.
36. Kandolo, K. Pyrazinamidase activity in Yersinia enterocolitica and related organisms / K. Kandolo, G. Wauters // J. Clin. Microbiol. 1985. - Vol. 21, N 6. - P. 980 - 982.
37. Karhukorpi, J. Differentiation of Yersinia enterocolitica biotype 1A from pathogenic Yersinia enterocolitica biotypes by detection of 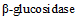 activity: comparison of two chromogenic culture media and Vitek2 / J. Karhukorpi,
activity: comparison of two chromogenic culture media and Vitek2 / J. Karhukorpi,  // J. Med. Microbiol. - 2014. - N 63. - P. 34 - 37. doi: 10.1099/jmm.0.062521-0.
// J. Med. Microbiol. - 2014. - N 63. - P. 34 - 37. doi: 10.1099/jmm.0.062521-0.
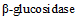 activity: comparison of two chromogenic culture media and Vitek2 / J. Karhukorpi,
activity: comparison of two chromogenic culture media and Vitek2 / J. Karhukorpi,  // J. Med. Microbiol. - 2014. - N 63. - P. 34 - 37. doi: 10.1099/jmm.0.062521-0.
// J. Med. Microbiol. - 2014. - N 63. - P. 34 - 37. doi: 10.1099/jmm.0.062521-0.38. Laukkanen, R. Evaluation of isolation methods for pathogenic Yersinia enterocolitica from pig intestinal content / R. Laukkanen [et al.] // J Appl Microbiol. - 2010. - Vol. 108, N 3. - P. 956 - 964. doi: 10.1111/j.1365-2672.2009.04494.x.
39. Laukkanen-Ninios, R. Population structure of the Yersinia pseudotuberculosis complex according to multilocus sequence typing / R. Laukkanen-Ninios [et al.] // Environ. Microbiol. - 2011. - N 13. - P. 3114 - 3127.
40. Le Guern, A.-S. Yersinia artesiana sp. nov., Yersinia proxima sp. nov., Yersinia alsatica sp. nov., Yersina vastinensis sp. nov., Yersinia thracica sp. nov. and Yersinia occitanica sp. nov., isolated from humans and animals / A.-S. Le Guern [et al.] // Int. J. Syst. Evol. Microbiol. - 2020. - Vol. 70, N 10. - P. 5363 - 5372. doi 10.1099/ijsem.0.004417.
41. Loftus, C.G. Clinical features of patients with novel Yersinia species / C.G. Loftus [et al.] // Dig. Dis. Sci. Microbiol. - 2002. - Vol. 47, N 12. - P. 2805 - 2810.
42. Martin, L. Characterization of atypical isolates of Yersinia intermedia and definition of two new biotypes / L. Martin [et al.] // J. Clin. Microbiol. - 2009. - Vol. 47, N 8. - P. 2376 - 2380.
43. Merhej, V. Yersinia massiliensis sp. nov., isolated from fresh water / V. Merhej [et al.] // Int. J. Syst. Evol. Microbiol. - 2008. - N 58. - P. 779 - 784.
44. Murros-Kontiainen, A. Yersinia pekkanenii sp. nov. / A. Murros-Kontiainen, [et al.] // Int. J. Syst. Evol. Microbiol. - 2011. - N 61. - P. 2363 - 2367.
45. Murros-Kontiainen, A. Yersinia nurmii sp. nov. / A. Murros-Kontiainen [et al.] // Int J Syst Evol Microbiol. - 2011. - N 61. - P. 2368 - 2372.
46. Neubauer, H. A miniaturised semiautomated system for the identification of Yersinia species within the genus Yersinia / H. Neubauer [et al.] // J. Clin. Lab. - 2000. - N 46. - P. 361 - 567.
47. Nguyen, S.V. Yersinia hibernica sp. nov., isolated from pig-production environments / S.V. Nguyen // Int. J. Syst. Evol. Microbiol. - 2019. - N 69. - P. 2023 - 2027.
48. Nguyen, S.V. Yersinia canariae sp. nov., isolated from a human yersiniosis case / S.V. Nguyen [et al.] // Int. J. Syst. Evol. Microbiol. - 2020. - Vol. 70, N 4. - P. 2382 - 2387. doi 10.1099/ijsem.0.004047.
49. Nguyen, S.V. Yersinia occitanica is a later heterotypic synonym of Yersinia kristensenii subsp. rochesterensis and elevation of Yersinia kristensenii subsp. rochesterensis to species status / S.V. Nguyen [et al.] // Int. J. Syst. Evol. Microbiol. - 2021. - Vol. 71, N 2. - 4 p. doi.org/10.1099/ijsem.0.004626.
50. Orozova, P. Diagnostics and antibiotic resistance of Yersinia ruckeri strains isolated from trout fish farms in Bulgaria / P. Orozova, P.V. Chikova, I. Sirakov // Int J Develop Res. - 2015. - Vol. 5, N 1. - P. 3013 - 3019.
51. Petsios, S. Conventional and molecular methods used in the detection and subtyping of Yersinia enterocolitica in food / S. Petsios, M. Fredriksson-Ahomaa, H. Sakkas, C. Papadopoulou // Int. J. Food Microbiol. - 2016. - N 237. - P. 55 - 72.
52. Ramamurthy, T. The novel heat-stable enterotoxin subtype gene (ystB) of Yersinia enterocolitica: nucleotide sequence and distribution of the yst genes // T. Ramamurthy [et al.] // J. Microbial. Pathog. - 1997. - N 304. - P. 189 - 200.
53. Renaud, N. CHROMagar Yersinia, a new chromogenic agar for screening of potentially pathogenic Yersinia enterocolitica isolates in stools / N. Renaud [et al.] // J Clin Microbiol. - 2013. - Vol. 51, N 4. - P. 1184 - 1187.
54. Reuter, S. Parallel independent evolution of pathogenicity within the genus Yersinia / S. Reuter [et al.] // Proc Natl Acad Sci USA. - 2014. - Vol. 111, N 18. - P. 6768 - 6773. doi: 10.1073/pnas.1317161111.
55. Savin, C. The Yersinia pseudotuberculosis complex: characterization and delineation of a new species, Yersinia wautersii / C. Savin [et al.] // Int. J. Med. Microbiol. - 2014. - N 304. - P. 452 - 463.
56. Savin, C. Genus-wide Yersinia core-genome multilocus sequence typing for species identification and strain characterization / C. Savin [et al.] // Microb Genom. 2019. - Vol. 5, N 10. - 4 p. doi: 10.1099/mgen.0.000301.
57. Schiemann, D.A. Synthesis of a selective agar medium for Yersinia enterocolitica / D.A. Schiemann // Can. J. Microbiol. - 1979. - Vol. 25, N 11. - P. 1298 - 1304.
58. Scientific Opinion of the Panel on BIOHAZ on a request from EFSA on monitoring and identification of human enteropathogenic Yersinia spp. // EFSA Journal. - 2007. - Vol. 595, N 1. - 30 p.
59. Sihvonen, L.M. Yersinia enterocolitica and Y. enterocolitica-like species in clinical stool specimens of humans: identification and prevalence of bio/serotypes in Finland / L.M. Sihvonen [et al.] // J. Clin. Mircobiol. Infect. Dis. - 2009. - N 28. - P. 757 - 765.
60. Souza, R.A. Emended description of Yersinia massiliensis / R.A. Souza,  ,
,  // Int. J. Syst. Evol. Microbiol. - 2011. - N 61 - P. 1094 - 1097. doi 10.1099/ijs.0.021840-0.
// Int. J. Syst. Evol. Microbiol. - 2011. - N 61 - P. 1094 - 1097. doi 10.1099/ijs.0.021840-0.
 ,
,  // Int. J. Syst. Evol. Microbiol. - 2011. - N 61 - P. 1094 - 1097. doi 10.1099/ijs.0.021840-0.
// Int. J. Syst. Evol. Microbiol. - 2011. - N 61 - P. 1094 - 1097. doi 10.1099/ijs.0.021840-0.61. Sprague, L.D. Yersinia aleksiciae sp. nov. / L.D. Sprague, H. Neubauer // Int. J. of Syst. and Evol. Microb. - 2005. - N 55. - P. 831 - 835.
62. Sprague, L.D. Yersinia similis sp. nov. / L.D. Sprague [et al.] // Int. J. Syst. Evol. Microbiol. - 2008. - N 58. - P. 952 - 958.
63. Sprague, L.D. Genome sequence of Yersinia similis Y228T, a member of the Yersinia pseudotuberculosis complex / L.D. Sprague, H. Neubauer // Genome Announc. - 2014. - Vol. 2, N 2: doi:10.1128/genomeA.00216-14.
64. Stock, I. Natural antibiotic susceptibility and biochemical profiles of Yersinia enterocolitica-like strains: Y. bercovieri, Y. mollaretii, Y. aldovae and "Y. ruckeri" / I. Stock, B. Henrichfreise, B. Wiedemann // J. Med. Microbiol. - 2002. - Vol. 51, N 1. - P. 56 - 69.
65. Stock, I. Natural antimicrobial susceptibilities and biochemical profiles of Yersinia enterocolitica-like strains: Y. frederiksenii, Y. intermedia, Y. kristensenii and Y. rohdei / I. Stock, B. Wiedemann // FEMS Immunol, and Med. Microbiol. - 2003. - N 38. - P. 139 - 152.
66. Sulakvelidze, A. Yersiniae other than Y. enterocolitica, Y. pseudotuberculosis, and Y. pestis: the ignored species / A. Sulakvelidze // Microbes Infection. - 2000. - N 2. - P. 497 - 513.
67. Tan, L.K. Evaluation of a modified Cefsulodin-Irgasan-Novobiocin agar for isolation of Yersinia / L.K. Tan, P.T. Ooi, E. Carniel, K.L. Thong // PLoS One. - 2014. - Vol. 9, N 8. - 9 p. doi: 10.1371/journal.pone.0106329.
68. The European Union summary report on trends and sources of zoonoses, zoonotic agents and food-borne outbreaks in 2015 // EFSA Journal. - 2016. - Vol. 12, N 14. - 231 p. doi: 10.2903/j.efsa.2016.4634.
69. Thuan, N.K. Evaluation of chromogenic medium for selective isolation of Yersinia / N.K. Thuan // Food Hyg. Saf. Sci. - 2016. - Vol. 57, No. 5. - P. 166 - 168.
70. Tobback, E. Yersinia ruckeri infections in salmonid fish / E. Tobback [et al.] // J Fish Dis. - 2007. - Vol. 30, N 5. - P. 257 - 68.
71. Van Damme, I. Effect of sampling and short isolation methodologies on the recovery of human pathogenic Yersinia enterocolitica from pig tonsils / I. Van Damme, D. Berkvens, L. De Zutter // Foodborn Pathog Dis. - 2012. - Vol. 9, N 7. - P. 600 - 606.
72. Vishnubhatla, A. Rapid 5' nuclease (TaqMan) assay for detection of virulent strains of Yersinia enterocolitica / A. Vishnubhatla [et al.] // Appl. Environ. Microbiol. - 2000. - Vol. 66, N 9. - P. 4131 - 4135.
73. Wauters, G. Yersinia mollaretii sp. nov. and Yersinia bercovieri sp. nov., formerly called Yersinia enterocolitica biogroups 3A and 3B / G. Wauters, M. Janssens, A.G. Steigerwalt, D.J. Brenner // Int. J. Syst. Bacteriol. - 1988. - N 38. - P. 424 - 429.
74. Wauters, G. Somatic and flagellar antigens of Yersinia enterocolitica and related species / G. Wauters, S.  , J. Charlier, G. Schulze // Contrib Microbiol Immunol. - 1991. - N 12. - P. 239 - 43.
, J. Charlier, G. Schulze // Contrib Microbiol Immunol. - 1991. - N 12. - P. 239 - 43.