СПРАВКА
Источник публикации
М.: ИПК Издательство стандартов, 1997
Примечание к документу
Документ утратил силу с 1 января 2020 года в связи с изданием Приказа Росстандарта от 13.11.2018 N 982-ст. Взамен введен в действие ГОСТ 30417-2018.
Документ включен в Перечень стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента Таможенного союза "Технический регламент на масложировую продукцию" (ТР ТС 024/2011) и осуществления оценки соответствия объектов технического регулирования (Решение Комиссии Таможенного союза от 09.12.2011 N 883).
Документ включен в Перечень стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента Таможенного союза "О безопасности пищевой продукции" (ТР ТС 021/2011) и осуществления оценки (подтверждения) соответствия продукции (Решение Комиссии Таможенного союза от 09.12.2011 N 880).
С 1 июля 2003 года до вступления в силу технических регламентов акты федеральных органов исполнительной власти в сфере технического регулирования носят рекомендательный характер и подлежат обязательному исполнению только в части, соответствующей целям, указанным в пункте 1 статьи 46 Федерального закона от 27.12.2002 N 184-ФЗ.
Документ введен в действие с 1 января 1998 года с правом досрочного введения (Постановление Госстандарта России от 12.05.1997 N 158).
Название документа
"ГОСТ 30417-96. Межгосударственный стандарт. Масла растительные. Методы определения массовых долей витаминов A и E"
(введен в действие Постановлением Госстандарта России от 12.05.1997 N 158)
"ГОСТ 30417-96. Межгосударственный стандарт. Масла растительные. Методы определения массовых долей витаминов A и E"
(введен в действие Постановлением Госстандарта России от 12.05.1997 N 158)
Содержание
Постановлением Государственного
комитета Российской Федерации
по стандартизации, метрологии
и сертификации
от 12 мая 1997 г. N 158
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МАСЛА РАСТИТЕЛЬНЫЕ
МЕТОДЫ ОПРЕДЕЛЕНИЯ МАССОВЫХ ДОЛЕЙ ВИТАМИНОВ A И E
Vegetable oils. Methods for determination
of vitamins A and E mass fractions
ГОСТ 30417-96
Группа Н69
ОКС 67.200.10
ОКСТУ 9141,
9142
Дата введения
1 января 1998 года
1. Разработан МТК 238 и Всероссийским научно-исследовательским институтом жиров (ВНИИЖ).
Внесен Госстандартом России.
2. Принят Межгосударственным советом по стандартизации, метрологии и сертификации (Протокол N 10 от 4 октября 1996 г.).
За принятие проголосовали:
Наименование государства | Наименование национального органа по стандартизации |
Азербайджанская Республика | Азгосстандарт |
Республика Армения | Армгосстандарт |
Республика Белоруссия | Госстандарт Белоруссии |
Республика Казахстан | Госстандарт Республики Казахстан |
Киргизская Республика | Киргизстандарт |
Республика Молдова | Молдовастандарт |
Российская Федерация | Госстандарт России |
Республика Таджикистан | Таджикгосстандарт |
Туркменистан | Главная государственная инспекция Туркменистана |
Республика Узбекистан | Узгосстандарт |
Украина | Госстандарт Украины |
3. Постановлением Государственного комитета Российской Федерации по стандартизации, метрологии и сертификации от 12 мая 1997 г. N 158 межгосударственный стандарт ГОСТ 30417-96 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 января 1998 г. с правом досрочного введения.
4. Введен впервые.
Настоящий стандарт распространяется на растительные масла и устанавливает методы определения массовых долей витаминов A и E.
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 1770-74. Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия
ГОСТ 4147-74. Железо (III) хлорид 6-водный. Технические условия
ГОСТ 4166-76. Натрий сернокислый. Технические условия
ГОСТ 4919.1-77. Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
ИС МЕГАНОРМ: примечание. ГОСТ 5471-83 утратил силу на территории Российской Федерации с 1 июня 2004 года в связи с введением в действие ГОСТ Р 52062-2003 (Постановление Госстандарта России от 28.05.2003 N 166-ст). |
ГОСТ 5471-83. Масла растительные. Правила приемки и методы отбора проб
ГОСТ 5815-77. Ангидрид уксусный. Технические условия
ГОСТ 6709-72. Вода дистиллированная. Технические условия
ГОСТ 12026-76. Бумага фильтровальная лабораторная. Технические условия
ГОСТ 14919-83. Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 18300-87. Спирт этиловый ректификованный технический. Технические условия
ГОСТ 20015-88. Хлороформ. Технические условия
ГОСТ 20490-75. Калий марганцевокислый. Технические условия
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-88 с 1 июля 2002 года Постановлением Госстандарта России от 26.10.2001 N 439-ст введен в действие ГОСТ 24104-2001. |
ГОСТ 24104-88. Весы лабораторные общего назначения и образцовые. Общие технические условия
ГОСТ 24363-80. Калия гидроокись. Технические условия
ГОСТ 25336-82. Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91. Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
Отбор проб растительных масел - по ГОСТ 5471.
4.1. Аппаратура, материалы, реактивы
Весы лабораторные - по ГОСТ 24104, 2-го класса точности и наибольшим пределом взвешивания 200 г.
Спектрофотометр СФ-26 или подобный с такой же разрешающей способностью, или спектроколориметр, или фотоколориметр ФЭК-56, или подобный, имеющий светофильтр с эффективной длиной волны 620 нм.
Баня водяная.
Электроплитка - по ГОСТ 14919, закрытого типа.
Колба К-1-250-29/32 по ГОСТ 25336.
Колба мерная 2-100-2-10/19 по ГОСТ 1770.
Пробирки П-4-10-14/23 ХС по ГОСТ 25336.
Цилиндры 1-250 или 3-250 по ГОСТ 1770.
Воронка В-25-38 ХС или В-36-50 ХС по ГОСТ 25336.
Колба Кн-2-250-34 ТХС по ГОСТ 25336.
Воронка ДВ-1-500 по ГОСТ 25336.
Пипетка 2-1-1-1 по ГОСТ 29227.
Ретинола пальмитат [1].
Ретинола ацетат [2].
Испаритель ротационный ИР-1М или установка, состоящая из колбы К-1-100-29/32 ТС по ГОСТ 25336, холодильника ХЛТ-1-400/600/-14/23 по ГОСТ 25336, алонжа АКП-14/23 ТС по ГОСТ 25336, перехода П-10-29/32-14/23 ТС по ГОСТ 25336, колбы К-1-250-14/23 ТС по ГОСТ 25336, насоса водоструйного по ГОСТ 25336.
Бумага фильтровальная по ГОСТ 12026.
Спирт этиловый ректификованный технический по ГОСТ 18300.
Калия гидроокись по ГОСТ 24363, ч., ч.д.а.
Кальций хлористый плавленый [3].
Калий марганцевокислый по ГОСТ 20490, ч., ч.д.а.
Кислота аскорбиновая [4].
Натрий сернокислый по ГОСТ 4166, ч., ч.д.а.
Сурьма треххлористая, ч., ч.д.а., по нормативному документу.
Ангидрид уксусный по ГОСТ 5815.
Фенолфталеин [7], спиртовой раствор с массовой долей индикатора 1%; готовят по ГОСТ 4919.1.
Вода дистиллированная по ГОСТ 6709.
Хлороформ по ГОСТ 20015.
Допускается применение другой аппаратуры или реактивов, по качеству и метрологическим характеристикам не уступающим приведенным выше.
4.2. Условия выполнения измерений
Выполнение измерений оптической плотности продукта колориметрической реакции следует проводить быстро в течение 5 - 6 с.
4.3. Подготовка к проведению измерения
4.3.1. Подготовка растворов и реактивов
4.3.1.1. Приготовление безводного сернокислого натрия
Сернокислый натрий нагревают в фарфоровой чашке при температуре (100 +/- 5) °C до тех пор, пока не образуется рыхлый порошок.
4.3.1.2. Очистка диэтилового эфира
В склянку с корковой пробкой взвешивают (5,0 +/- 1,0) г марганцевокислого калия и (10,0 +/- 1,0) г гидроокиси калия, заливают 1 дм3 диэтилового эфира и оставляют на сутки в темноте. Затем эфир перегоняют при температуре 33 - 35 °C.
4.3.1.3. Приготовление сухого хлороформа
Хлороформ сушат над хлористым кальцием в течение суток, затем перегоняют при температуре 60 - 61 °C и хранят в склянке из темного стекла с притертой пробкой.
4.3.1.4. Приготовление спиртового раствора гидроокиси калия концентрации c (KOH) = 2 моль/дм3
(120 +/- 5) г гидроокиси калия растворяют в 1 дм3 спирта. Спиртовую щелочь хранят в холодильнике не более 1 мес.
В конической колбе взвешивают (20,0 +/- 0,5) г треххлористой сурьмы. Результат взвешивания записывают до второго десятичного знака. Добавляют 100 см3 хлороформа и растворяют, нагревая на водяной бане (температура воды не выше 50 °C), периодически встряхивая. Раствор охлаждают, добавляют 2 - 3 см3 уксусного ангидрида, колбу плотно закрывают и оставляют на ночь для отстаивания. Затем верхнюю прозрачную часть раствора осторожно сливают через бумажный фильтр в темную склянку с притертой пробкой. Раствор годен для работы через сутки.
Перед построением градуировочного графика уточняют концентрацию ретинола ацетата или ретинола пальмитата спектрофотометрическим методом в соответствии с [2] или [1].
В мерной колбе взвешивают (0,10 +/- 0,01) г масляного концентрата витамина A (ретинола пальмитата или ретинола ацетата). Результат взвешивания записывают до четвертого десятичного знака. Растворяют концентрат в хлороформе, доводят хлороформом до метки и хорошо перемешивают.
Массовую долю витамина A в растворе  , м.е. в 1 см3, вычисляют по формуле
, м.е. в 1 см3, вычисляют по формуле
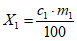 , (1)
, (1)где 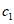 - концентрация витамина A-ацетата (или A-пальмитата), м.е. в 1 г масляного концентрата;
- концентрация витамина A-ацетата (или A-пальмитата), м.е. в 1 г масляного концентрата;
100 - объем хлороформного раствора концентрата витамина A, см3.
Если концентрация витамина A-ацетата (или A-пальмитата) в масляном концентрате выражена в процентах, то концентрацию витамина A 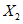 и
и  , м.е. в 1 см3 хлороформного раствора, вычисляют по формулам:
, м.е. в 1 см3 хлороформного раствора, вычисляют по формулам:
(для витамина A-ацетата)
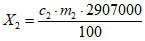 , (2)
, (2)(для витамина A-пальмитата)
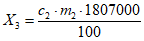 , (3)
, (3)где 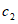 - концентрация витамина A-ацетата (или A-пальмитата) в масляном концентрате, г;
- концентрация витамина A-ацетата (или A-пальмитата) в масляном концентрате, г;
2907000 - активность 1 г витамина A-ацетата с массовой долей 100%, м.е.;
1807000 - активность 1 г витамина A-пальмитата с массовой долей 100%, м.е.
Из хлороформного раствора витамина A готовят в пробирках растворы концентрацией витамина A от (5 +/- 2) до (40 +/- 2) м.е. в 1 см3 с интервалом 5 м.е. Из каждой пробирки отбирают пипеткой по 0,4 см3 раствора в кювету толщиной 1 см, помещают кювету в кюветодержатель фотоэлектроколориметра или спектрофотометра, добавляют 4 см3 раствора треххлористой сурьмы, приготовленного по 4.3.1.5, и быстро измеряют оптическую плотность раствора при длине волны 620 нм. В качестве контроля служит раствор, состоящий из 0,4 см3 хлороформа и 4 см3 раствора треххлористой сурьмы. Для построения градуировочного графика по оси ординат откладывают полученные значения оптической плотности, а по оси абсцисс соответствующую им концентрацию витамина A, м.е. в 1 см3.
Примечания
1. Градуировочный график строится для каждого спектрофотометра или фотоэлектроколориметра и проверяется при смене партий реактивов и приборов путем измерения оптической плотности стандартных растворов двух разных концентраций.
2. В случае длительного хранения масляного концентрата витамина A необходимо один раз в полгода проверять его концентрацию по соответствующему градуировочному графику.
4.4. Проведение измерения
(3 +/- 1) г растительного масла взвешивают в колбе. Результат записывают до четвертого десятичного знака. Добавляют (0,1 +/- 0,01) г аскорбиновой кислоты и 50 см3 спиртового раствора гидроокиси калия концентрации c (KOH) = 2 моль/дм3.
Колбу соединяют с обратным воздушным холодильником и смесь кипятят на водяной бане в течение 30 мин. После этого содержимое колбы охлаждают и количественно переносят в делительную воронку, дважды ополаскивая колбу порциями дистиллированной воды по 50 см3. Неомыляемые вещества экстрагируют тремя порциями этилового эфира по 50 см3.
Объединенный эфирный экстракт переносят в делительную воронку и промывают дистиллированной водой порциями 50 - 100 см3 до нейтральной реакции по фенолфталеину.
Промытую эфирную вытяжку сливают в сухую колбу, добавляют (10 +/- 1) г сернокислого натрия и оставляют на 30 мин в темном месте, периодически взбалтывая. Затем содержимое колбы фильтруют через бумажный фильтр. Сернокислый натрий в колбе и фильтр промывают этиловым эфиром. Эфир собирают в колбе и отгоняют при температуре не выше 30 °C. Остаток в колбе, представляющий неомыляемые вещества, после отгонки растворителя должен быть сухим. Если остаток влажный, его растворяют в 20 см3 этилового эфира, добавляют (2,0 +/- 0,5) г сернокислого натрия, оставляют на 30 мин в темном месте. Затем содержимое колбы фильтруют через бумажный фильтр, тщательно промывая фильтр и сернокислый натрий этиловым эфиром. Эфир отгоняют в вакууме при температуре не выше 30 °C. Остаток неомыляемых веществ растворяют в 10 см3 хлороформа.
Колориметрическую реакцию и измерение проводят, как указано в 4.3.2.
4.5. Обработка результатов
Массовую долю витамина A 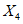 , м.е. в 1 г продукции, вычисляют по формуле
, м.е. в 1 г продукции, вычисляют по формуле
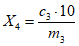 , (4)
, (4)где  - концентрация витамина A в хлороформном растворе, определенная по градуировочному графику, м.е. в см3;
- концентрация витамина A в хлороформном растворе, определенная по градуировочному графику, м.е. в см3;
10 - объем раствора неомыляемых веществ в хлороформе, см3;
Вычисления проводят до первого десятичного знака с последующим округлением результата до целого числа.
За окончательный результат измерения принимают среднее арифметическое результатов двух параллельных измерений.
Метрологические характеристики метода при доверительной вероятности 0,95 приведены в таблице 1.
Таблица 1
ИС МЕГАНОРМ: примечание. Единицы измерения "значения измеряемой величины" даны в соответствии с официальным текстом документа. |
Значение измеряемой величины, и.е. | Предел возможных значений относительной погрешности измерений, % | Относительное расхождение между результатами двух параллельных определений (от их среднего значения), % |
От 10 до 20 включ. | 12 | 17 |
" 20 " 40 " | 9 | 13 |
" 40 " 70 " | 7 | 9 |
Если расхождение между двумя параллельными измерениями превышает указанное в таблице, измерение следует повторить.
МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ
5.1. Аппаратура, реактивы, материалы
Спектрофотометр или фотоэлектроколориметр, позволяющий производить измерения при длине волны  .
.
 .
.ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-88 с 1 июля 2002 года Постановлением Госстандарта России от 26.10.2001 N 439-ст введен в действие ГОСТ 24104-2001. |
Весы лабораторные по ГОСТ 24104, 2-го класса точности с наибольшим пределом взвешивания 200 г или другие весы с таким же классом точности.
Шкаф сушильный лабораторный СЭШ-3М.
Баня водяная.
Колба Кн-1-250-29/32 ТС ГОСТ 25336.
Колба К-1-250-29/32 ТС ГОСТ 25336.
Воронка В-25-38 ХС или В-56-80 ХС ГОСТ 25336.
Воронка ВД-1-250 ХС ГОСТ 25336.
Пробирка П4-25-14/25 ХС ГОСТ 25336.
Холодильник воздушный.
Пипетки 2-1-1-0,5; 1-1-1-1 и 2-1-1-5 ГОСТ 29227.
Цилиндр 1-25 ГОСТ 1770.
Калия гидроокись по ГОСТ 24363, х.ч. или ч.д.а.
Спирт этиловый ректификованный технический по ГОСТ 18300.
Натрий сернокислый по ГОСТ 4166.
Кальций хлористый обезвоженный чистый [3].
Кислота аскорбиновая [4].
Хлороформ по ГОСТ 20015, х.ч.
Калий марганцевокислый по ГОСТ 20490.
Пластинки "Силуфол".
Фенолфталеин [7], спиртовый раствор с массовой долей 1%; готовят по ГОСТ 4919.1.
Бумага фильтровальная по ГОСТ 12026.
Вода дистиллированная по ГОСТ 6709.
Железо хлористое по ГОСТ 4147, спиртовый раствор с массовой долей 0,25%.
 или о-фенантролин, спиртовый раствор с массовой долей 0,1%.
или о-фенантролин, спиртовый раствор с массовой долей 0,1%.Допускается применение другой аппаратуры или реактивов, по качеству и метрологическим характеристикам не уступающих приведенным выше.
5.2. Подготовка к проведению измерения
5.2.1. Подготовка реактивов
Натрий сернокислый сушат в течение 3 - 4 ч при температуре (110 +/- 3) °C.
Этиловый эфир обрабатывают марганцевокислым калием (5 г на 1 дм3) и гидроокисью калия (10 г на 1 дм3) в течение суток, а затем перегоняют.
Хлороформ сушат в течение суток над хлористым кальцием и перегоняют.
Для работы используют только свежеперегнанные растворители.
Реактив Эммери-Энгеля готовят, смешивая равные объемы растворов хлорного железа и  (о-фенантролина).
(о-фенантролина).
 (о-фенантролина).
(о-фенантролина).Все этапы измерения следует проводить по возможности быстро, предохраняя пробы от попадания на них прямого солнечного света.
5.2.2. Подготовка камеры для хроматографирования
Не менее чем за 30 мин до начала хроматографирования в камеру наливают смесь этилового эфира и гексана (1:1) на высоту 0,5 см.
Градуировочный график строят на основании результатов измерения проб с известным содержанием 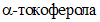 .
.
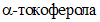 .
. выделяют из препарата
выделяют из препарата  .
.ИС МЕГАНОРМ: примечание. Текст дан в соответствии с официальным текстом документа. |
Для этого отвешивают в колбу (0,05 +/- 0,1) г 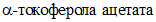 с точностью записи результата до четвертого десятичного знака, проводят омыление и выделяют неомыляемые вещества, как указано в 5.4.1.
с точностью записи результата до четвертого десятичного знака, проводят омыление и выделяют неомыляемые вещества, как указано в 5.4.1.
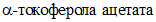 с точностью записи результата до четвертого десятичного знака, проводят омыление и выделяют неомыляемые вещества, как указано в 5.4.1.
с точностью записи результата до четвертого десятичного знака, проводят омыление и выделяют неомыляемые вещества, как указано в 5.4.1.Эфир из объединенного фильтрата отгоняют на кипящей водяной бане до объема 1 - 2 см3. Остаток эфира отгоняют под вакуумом при температуре не выше 30 °C. Остаток немедленно растворяют в этиловом спирте.
Количество  в выделенном остатке M, г, рассчитывают по формуле
в выделенном остатке M, г, рассчитывают по формуле
 в выделенном остатке M, г, рассчитывают по формуле
в выделенном остатке M, г, рассчитывают по формулеM = 0,892m, (5)
где m - масса  , взятая для анализа, г;
, взятая для анализа, г;
 , взятая для анализа, г;
, взятая для анализа, г;0,892 - содержание 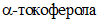 в 1 г
в 1 г  .
.
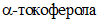 в 1 г
в 1 г  .
.Необходимый объем этилового спирта должен быть таким, чтобы концентрация 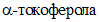 в растворе спирта была 1 мг/см3. (Например, если масса
в растворе спирта была 1 мг/см3. (Например, если масса 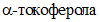 0,053, то объем этилового спирта 53 см3 и т.д.).
0,053, то объем этилового спирта 53 см3 и т.д.).
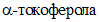 в растворе спирта была 1 мг/см3. (Например, если масса
в растворе спирта была 1 мг/см3. (Например, если масса 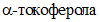 0,053, то объем этилового спирта 53 см3 и т.д.).
0,053, то объем этилового спирта 53 см3 и т.д.).Из полученного раствора готовят серию стандартных растворов в соответствии с таблицей 2.
Номер раствора | Объем основного раствора, см3 | Объем добавляемого этилового спирта, см3 | Концентрация полученного раствора  |
1 | 1,0 | 19,0 | 0,05 |
2 | 0,8 | 19,2 | 0,04 |
3 | 0,6 | 19,4 | 0,03 |
4 | 0,4 | 19,6 | 0,02 |
5 | 0,2 | 19,8 | 0,01 |
6 | 0,1 | 19,9 | 0,005 |
Из каждого раствора в пробирку отбирают пипеткой 1 см3, добавляют 3 см3 этилового спирта, 1 см3 раствора 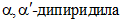 (или о-фенантролина), взбалтывают, добавляют по каплям 1 см3 раствора хлорного железа, снова взбалтывают. Полученный раствор помещают на 3 мин в темное место, после чего наливают в кювету и измеряют его оптическую плотность на спектрофотометре при
(или о-фенантролина), взбалтывают, добавляют по каплям 1 см3 раствора хлорного железа, снова взбалтывают. Полученный раствор помещают на 3 мин в темное место, после чего наливают в кювету и измеряют его оптическую плотность на спектрофотометре при  (или фотоэлектроколориметре с зеленым фильтром). В качестве контрольного раствора используют смесь из 4 см3 этилового спирта, 1 см3 раствора
(или фотоэлектроколориметре с зеленым фильтром). В качестве контрольного раствора используют смесь из 4 см3 этилового спирта, 1 см3 раствора  и 1 см3 раствора хлорного железа, приготовленную в тех же условиях.
и 1 см3 раствора хлорного железа, приготовленную в тех же условиях.
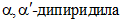 (или о-фенантролина), взбалтывают, добавляют по каплям 1 см3 раствора хлорного железа, снова взбалтывают. Полученный раствор помещают на 3 мин в темное место, после чего наливают в кювету и измеряют его оптическую плотность на спектрофотометре при
(или о-фенантролина), взбалтывают, добавляют по каплям 1 см3 раствора хлорного железа, снова взбалтывают. Полученный раствор помещают на 3 мин в темное место, после чего наливают в кювету и измеряют его оптическую плотность на спектрофотометре при  (или фотоэлектроколориметре с зеленым фильтром). В качестве контрольного раствора используют смесь из 4 см3 этилового спирта, 1 см3 раствора
(или фотоэлектроколориметре с зеленым фильтром). В качестве контрольного раствора используют смесь из 4 см3 этилового спирта, 1 см3 раствора  и 1 см3 раствора хлорного железа, приготовленную в тех же условиях.
и 1 см3 раствора хлорного железа, приготовленную в тех же условиях.Градуировочный график строят в координатах: оптическая плотность (Д) - концентрация  в анализируемом растворе
в анализируемом растворе  , мг/см3, вычисляемая по формуле
, мг/см3, вычисляемая по формуле
 в анализируемом растворе
в анализируемом растворе 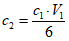 , (6)
, (6)где 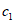 - концентрация
- концентрация  в соответствующем стандартном растворе, мг/см3;
в соответствующем стандартном растворе, мг/см3;
 в соответствующем стандартном растворе, мг/см3;
в соответствующем стандартном растворе, мг/см3;6 - объем анализируемого раствора, см3.
Градуировочный график строится для каждого спектрофотометра (фотоэлектроколориметра) и проверяется при смене партий реактивов путем измерения оптической плотности стандартных растворов двух разных концентраций.
5.4. Проведение измерения
В конической колбе взвешивают (3 +/- 0,2) г растительного масла. Результат записывают до четвертого десятичного знака. Добавляют (0,2 +/- 0,05) г аскорбиновой кислоты и 30 см3 свежеприготовленного спиртового раствора KOH концентрацией c (KOH) = 2 моль/дм3. Смесь нагревают с обратным холодильником на кипящей водяной бане в течение 15 мин, начиная с момента закипания раствора в колбе.
Содержимое колбы охлаждают и количественно переносят в делительную воронку тремя порциями дистиллированной воды общим объемом 100 см3. Неомыленные вещества экстрагируют этиловым эфиром, тремя порциями по 60 см3. Объединенный эфирный экстракт промывают в делительной воронке дистиллированной водой до нейтральной реакции промывных вод по фенолфталеину.
Промытую эфирную вытяжку помещают в сухую колбу, воронку ополаскивают 20 см3 эфира и сливают в ту же колбу. Засыпают 5 - 10 г безводного сернокислого натрия и оставляют в темном месте на 30 мин, периодически взбалтывая. Затем содержимое колбы фильтруют через бумажный фильтр. Колбу и фильтр промывают этиловым эфиром, тремя порциями по 10 см3.
Эфир из объединенного фильтрата отгоняют на кипящей водяной бане до объема 1 - 2 см3. Остаток эфира отгоняют под вакуумом при температуре не выше 30 °C до объема 0,5 - 0,6 см3.
5.4.2. Выделение витамина E с помощью тонкослойных хроматографических пластинок
На пластинки "Силуфол" пипеткой наносят количественно (дважды обмывая колбу порциями эфира по 0,5 см3) весь раствор неомыляемых веществ в виде полосы длиной около 10 см, отстоящей на 2 см от нижнего и боковых краев пластинки. После каждого нанесения полосы следует дать эфиру улетучиться.
ИС МЕГАНОРМ: примечание. Расстояние в см дано в соответствии с официальным текстом документа. |
На одном уровне с пробой на расстоянии см от боковых краев пластинки наносят по капле раствора 1 (см. таблицу 2) концентрацией  0,05 мг/см3 в качестве "свидетеля".
0,05 мг/см3 в качестве "свидетеля".
 0,05 мг/см3 в качестве "свидетеля".
0,05 мг/см3 в качестве "свидетеля".Пластинку "Силуфол" помещают в хроматографическую камеру. В качестве подвижной фазы используют смесь этилового эфира и гексана 1:1. Развитие хроматограммы должно проходить в темноте и заканчиваться при подъеме растворителя до верхнего края пластинки. Пластинку вынимают из камеры, подсушивают на воздухе, затем края пластинки, содержащие "свидетель", опрыскивают реактивом Эммери-Энгеля, предварительно часть пластинки с пробой прикрывая стеклянной пластинкой. Затем пластинку "Силуфол" помещают в темноту на 3 мин, после чего пятна, содержащие  , окрашиваются в розовый цвет. Прочерчивают две линии, выше и ниже окрашенных пятен на 2 мм.
, окрашиваются в розовый цвет. Прочерчивают две линии, выше и ниже окрашенных пятен на 2 мм.
 , окрашиваются в розовый цвет. Прочерчивают две линии, выше и ниже окрашенных пятен на 2 мм.
, окрашиваются в розовый цвет. Прочерчивают две линии, выше и ниже окрашенных пятен на 2 мм.Слой силикагеля, заключенный между линиями, соскабливают в бумажный фильтр диаметром 3 см, помещенный в стеклянную воронку, и элюируют токоферолы в градуированную пробирку, промывая силикагель этиловым спиртом 10 раз порциями по 1 см3. Объем элюата доводят этиловым спиртом до 10 см3.
Для определения приблизительной концентрации токоферола отбирают 1 см3 элюата, добавляют 3 см3 этилового спирта, по 1 см3 растворов  (о-фенантролина) и хлорного железа и измеряют оптическую плотность, как указано в 5.3.
(о-фенантролина) и хлорного железа и измеряют оптическую плотность, как указано в 5.3.
 (о-фенантролина) и хлорного железа и измеряют оптическую плотность, как указано в 5.3.
(о-фенантролина) и хлорного железа и измеряют оптическую плотность, как указано в 5.3.Если измеренная оптическая плотность меньше 0,1, то для основного измерения следует увеличить объем элюата и уменьшить объем этилового спирта так, чтобы сумма этих объемов составляла по-прежнему 4 см3 (например, элюата - 1,3 см3, этилового спирта - 2,7 см3). Если оптическая плотность превышает 0,3, то следует уменьшить объем элюата и соответственно увеличить объем этилового спирта, исходя из такого же расчета (например, элюата - 0,8 см3, этилового спирта - 3,2 см3).
В полученном таким образом растворе проводят колориметрическую реакцию и измеряют оптическую плотность, как указано в 5.3.
Концентрацию 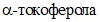 определяют по градуировочному графику.
определяют по градуировочному графику.
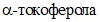 определяют по градуировочному графику.
определяют по градуировочному графику.5.5. Обработка результатов
ИС МЕГАНОРМ: примечание. Единицы измерения даны в соответствии с официальным текстом документа. |
Массовую долю витамина E  , мг на 100 г продукта (мг %), вычисляют по формуле
, мг на 100 г продукта (мг %), вычисляют по формуле
 , (7)
, (7)где c - концентрация  в анализируемом растворе, мг/см3;
в анализируемом растворе, мг/см3;
 в анализируемом растворе, мг/см3;
в анализируемом растворе, мг/см3;6 - общий объем раствора, взятого для колориметрической реакции, см3;
10 - общий объем элюата, см3;
m - масса пробы, г.
Вычисления проводят до второго десятичного знака с последующим округлением результата до первого десятичного знака.
За окончательный результат измерения принимают среднее арифметическое значение результатов двух параллельных измерений.
Метрологические характеристики метода при доверительной вероятности 0,95 приведены в таблице 3.
Таблица 3
Измеряемая величина, мг % | Предел возможных значений абсолютной погрешности измерений, мг % | Абсолютное допустимое расхождение между результатами двух параллельных определений (от их среднего значения), мг % |
От 10,0 до 30,0 включ. | 2,4 | 4,8 |
" 30,0 " 100,0 " | 6,8 | 13,5 |
" 100,0 " 200,0 " | 10,0 | 19,5 |
(информационное)
БИБЛИОГРАФИЯ
ФС 42-2229-84. Ретинола пальмитат | |
Госфармакопея, X изд., ст. 578. Ретинола ацетат | |
ТУ 6-09-4711-81. Кальций хлористый обезвоженный чистый | |
ФС 42-2668-89. Кислота аскорбиновая | |
ОСТ 84-2006-82. Эфир этиловый очищенный | |
Госфармакопея, X изд., ст. 34. Эфир медицинский | |
ТУ 6-09-5360-87. Фенолфталеин | |
ФС 42-2495-87.  | |
ТУ 64-5-68-88. 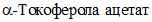 (витамин E). (витамин E). |