СПРАВКА
Источник публикации
М.: ИПК Издательство стандартов, 2000
Примечание к документу
Документ утратил силу с 15 февраля 2015 года в связи с изданием Приказа Росстандарта от 28.06.2013 N 348-ст. Взамен введен в действие ГОСТ 31664-2012.
Документ включен в Перечень национальных стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения Федерального закона "Технический регламент на масложировую продукцию" и осуществления оценки соответствия (Распоряжение Правительства РФ от 27.12.2008 N 2008-р).
Документ включен в Перечень стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента "О безопасности пищевой продукции" (ТР ТС 021/2011) и осуществления оценки (подтверждения) соответствия продукции (Решение Комиссии Таможенного союза от 09.12.2011 N 880).
Документ включен в Перечень национальных стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения Федерального закона "Технический регламент на соковую продукцию из фруктов и овощей" и осуществления оценки соответствия (Распоряжение Правительства РФ от 19.05.2009 N 690-р).
С 1 июля 2003 года до вступления в силу технических регламентов акты федеральных органов исполнительной власти в сфере технического регулирования носят рекомендательный характер и подлежат обязательному исполнению только в части, соответствующей целям, указанным в пункте 1 статьи 46 Федерального закона от 27.12.2002 N 184-ФЗ.
Документ введен в действие с 1 января 2001 года.
Название документа
"ГОСТ Р 51484-99. Государственный стандарт Российской Федерации. Масла растительные и жиры животные. Метод определения состава жирных кислот в положении 2 в молекулах триглицеридов"
(принят и введен в действие Постановлением Госстандарта России от 22.12.1999 N 640-ст)
"ГОСТ Р 51484-99. Государственный стандарт Российской Федерации. Масла растительные и жиры животные. Метод определения состава жирных кислот в положении 2 в молекулах триглицеридов"
(принят и введен в действие Постановлением Госстандарта России от 22.12.1999 N 640-ст)
Содержание
Постановлением Госстандарта России
от 22 декабря 1999 г. N 640-ст
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МАСЛА РАСТИТЕЛЬНЫЕ И ЖИРЫ ЖИВОТНЫЕ
МЕТОД ОПРЕДЕЛЕНИЯ СОСТАВА ЖИРНЫХ КИСЛОТ В ПОЛОЖЕНИИ 2
В МОЛЕКУЛАХ ТРИГЛИЦЕРИДОВ
Vegetable oils and animal fats.
Method for determination of the composition of fatty
acids in the 2-position in the triglyceride molecules
ГОСТ Р 51484-99
Группа Н69
ОКС 67.200.10
ОКСТУ 9109
Дата введения
1 января 2001 года
1. Разработан Временным творческим коллективом, образованным в рамках договора N 9842002 Е 4075 между АФНОР и ВНИЦСМВ с участием членов Технического комитета по стандартизации ТК 238 "Масла растительные и продукты их переработки".
Внесен Техническим комитетом по стандартизации ТК 238 "Масла растительные и продукты их переработки".
2. Принят и введен в действие Постановлением Госстандарта России от 22 декабря 1999 г. N 640-ст.
3. Настоящий стандарт гармонизирован с международным стандартом ИСО 6800:1997 "Масла растительные и жиры животные. Метод определения состава жирных кислот в положении 2 в молекулах триглицеридов".
4. Введен впервые.
Настоящий стандарт распространяется на растительные масла и животные жиры и устанавливает метод определения состава жирных кислот, которые находятся в положении 2 ( или среднем положении) в молекулах триглицеридов в растительных маслах и животных жирах.
или среднем положении) в молекулах триглицеридов в растительных маслах и животных жирах.
В силу природных свойств активности панкреатической липазы метод применим только для жиров температурой плавления ниже 45 °C.
Этот метод не может без ограничений применяться для всех жиров и масел, в частности, содержащих значительные количества:
- жирных кислот с 12 и менее атомами углерода (например кокосовое масло, пальмоядровое масло, молочные жиры, содержащие масляную кислоту);
- жирных кислот с 20 и более атомами углерода и высокой степенью ненасыщенности (более четырех двойных связей) (например рыбные жиры и жиры морских млекопитающих);
- жирных кислот, имеющих вторичные группы, содержащие кислород.
Примечание. Жирные кислоты с двойными связями в положении от  до
до  (например петрозелиновая кислота) лишь в слабой степени подвергаются воздействию панкреатической липазы. Это может привести к искажению результатов.
(например петрозелиновая кислота) лишь в слабой степени подвергаются воздействию панкреатической липазы. Это может привести к искажению результатов.
 до
до  (например петрозелиновая кислота) лишь в слабой степени подвергаются воздействию панкреатической липазы. Это может привести к искажению результатов.
(например петрозелиновая кислота) лишь в слабой степени подвергаются воздействию панкреатической липазы. Это может привести к искажению результатов.В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 61-75 Кислота уксусная
ГОСТ 450-77 Кальций хлористый технический. Технические условия
ГОСТ 2603-79 Ацетон. Технические условия
ГОСТ 3118-77 Кислота соляная. Технические условия
ГОСТ 4328-77 Натрия гидроокись. Технические условия
ИС МЕГАНОРМ: примечание. ГОСТ 5471-83 утратил силу на территории Российской Федерации с 1 июня 2004 года в связи с введением в действие ГОСТ Р 52062-2003 (Постановление Госстандарта России от 28.05.2003 N 166-ст). |
ГОСТ 5471-83 Масла растительные. Правила приемки и методы отбора проб
ГОСТ 5848-73 Кислота муравьиная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Метанол-яд. Технические условия
ГОСТ 8285-91 Жиры животные топленые. Правила приемки и методы испытаний
ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
ГОСТ 9805-84 Спирт изопропиловый. Технические условия
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 20015-88 Хлороформ. Технические условия
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-88 Постановлением Госстандарта России от 26.10.2001 N 439-ст с 1 июля 2002 года введен в действие ГОСТ 24104-2001. |
ГОСТ 24104-88 Весы лабораторные общего назначения и образцовые. Общие технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ Р 51483-99 Масла растительные и жиры животные. Определение методом газовой хроматографии массовой доли метиловых эфиров индивидуальных жирных кислот к их сумме
ГОСТ Р 51486-99 Масла растительные и жиры животные. Получение метиловых эфиров жирных кислот
ИСО 661-89 <*>) Масла и жиры животные и растительные. Подготовка испытуемой пробы
ИСО 5555-91 <*> Масла и жиры животные и растительные. Отбор проб
--------------------------------
<*> Действуют до введения в действие ГОСТ Р, разработанных на основе соответствующих ИСО.
Метод включает нейтрализацию свободных жирных кислот, очистку испытуемой пробы с помощью колоночной хроматографии, частичный энзиматический гидролиз глицеридов, отделение 2-моноглицеридов с помощью тонкослойной хроматографии и определение их жирнокислотного состава с помощью газовой хроматографии.
4.1. Правила приемки и отбор проб:
ИС МЕГАНОРМ: примечание. ГОСТ 5471-83 утратил силу на территории Российской Федерации с 1 июня 2004 года в связи с введением в действие ГОСТ Р 52062-2003 (Постановление Госстандарта России от 28.05.2003 N 166-ст). |
- растительных масел - по ГОСТ 5471;
- животных жиров - по ГОСТ 8285.
При экспортно-импортных поставках - по ИСО 5555.
5.1. Реактивы для очистки испытуемой пробы
5.1.2. Гексан по [1] или эфир легкий петролейный температурой кипения в пределах (30 - 60) °C.
5.1.4. Натрия гидроокись по ГОСТ 4328, раствор молярной концентрации c (NaOH) = 0,5 моль/дм3.
5.1.5. Фенолфталеин по [2], спиртовой раствор массовой долей 1%.
5.1.6. Окись алюминия активированная нейтральная для хроматографии I степени активности, активированная перед использованием в течение 2 ч при 260 °C и хранящаяся в эксикаторе.
5.1.7. Азот по ГОСТ 9293, особой чистоты.
5.2. Реактивы для гидролиза триглицеридов
5.2.1. Эфир диэтиловый по [3], не содержащий перекисей.
5.2.2. Кислота соляная по ГОСТ 3118 концентрации c (HCl) = 6 моль/дм3.
5.2.5. Раствор буферный, 2-амино-2-(гидроксиметил)пропан-1,3-диол <*>) молярной концентрации 1 моль/дм3; раствор доводят соляной кислотой (5.2.2) до pH 8 по pH-метру. Раствор хранят при температуре 0 - 4 °C и используют в течение 14 дней.
--------------------------------
<*> Синонимы: три(гидроксиметил)метиламин, три(гидроксиметил)аминометан.
5.2.6. Липаза панкреатическая активностью 8 - 20 ед/мг. Липазу хранят сухой в холодильнике. Перед употреблением доводят порцию порошка до комнатной температуры.
Примечание. Липаза необходимой активности имеется в продаже. При необходимости она может быть получена и испытана в соответствии с методикой, приведенной в Приложении А.
5.3. Реактивы для отделения 2-моноглицеридов
5.3.1. Спирт этиловый по ГОСТ 18300, 95% (объемная доля).
5.3.2. Гексан по [1] и эфир легкий петролейный, температурой кипения в пределах 30 - 60 °C.
5.3.3. Ацетон по ГОСТ 2603.
Готовят смесь, состоящую из 70 см3 гексана или петролейного эфира (5.3.2), 30 см3 диэтилового эфира и 1 см3 муравьиной кислоты (5.3.7), не менее 98% (объемная доля) или уксусной кислоты (5.3.7).
5.3.6. 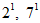 -Дихлорфлуоресцеин, спиртовой раствор индикатора массовой долей 0,2%. Слабощелочная реакция достигается добавлением одной капли гидроокиси натрия молярной концентрации 1 моль/дм3 на 100 см3 раствора.
-Дихлорфлуоресцеин, спиртовой раствор индикатора массовой долей 0,2%. Слабощелочная реакция достигается добавлением одной капли гидроокиси натрия молярной концентрации 1 моль/дм3 на 100 см3 раствора.
5.4 Реактивы для анализа 2-моноглицеридов с помощью газовой хроматографии
Реактивы по ГОСТ Р 51486 и ГОСТ Р 51483.
6.1. Установка для очистки испытуемой пробы
6.1.1. Баня водяная с терморегулятором, обеспечивающая нагрев до 40 °C.
6.1.2. Колонка стеклянная для хроматографии внутренним диаметром 13 мм и длиной 400 мм, снабженная стеклянным пористым фильтром и пробкой.
6.1.4. Трубка для пробулькивания азота.
6.1.5. Воронка делительная ВД-1(3)-500 ХС по ГОСТ 25336.
6.1.6. Колба К-1-100-29/32 ТС по ГОСТ 25336.
6.2. Аппаратура для гидролиза триглицеридов
6.2.1. Центрифуга
6.2.4. Баня водяная с терморегулятором, обеспечивающая температуру (40 +/- 0,5) °C.
6.2.6. Секундомер.
6.3. Аппаратура для отделения 2-моноглицеридов
6.3.1. Камера хроматографическая для тонкослойной хроматографии с притертой стеклянной крышкой, пригодная для размещения стеклянных пластинок размером (200 x 200) мм.
6.3.8. Лампа ультрафиолетовая для определения положения пятен на хроматографических пластинках, например, при длине волны 254 нм.
6.3.9. Колба К-1-25-14/23 ТС по ГОСТ 25336 с воздушным холодильником длиной приблизительно 1 м со шлифом.
6.3.10. Колба Кн-1-250-29/32 ТС по ГОСТ 25336.
6.3.11. Колба Кн-2-50-18(22) ТС по ГОСТ 25336.
6.4. Аппаратура для анализа 2-моноглицеридов с помощью газовой хроматографии:
Аппаратура - по ГОСТ Р 51483-99 и ГОСТ Р 51486.
ИС МЕГАНОРМ: примечание. Взамен ГОСТ 24104-88 Постановлением Госстандарта России от 26.10.2001 N 439-ст с 1 июля 2002 года введен в действие ГОСТ 24104-2001. |
6.5. Весы лабораторные общего назначения по ГОСТ 24104 3-го класса точности с наибольшим пределом взвешивания 500 г.
7.1. Подготовка испытуемой пробы
Готовят испытуемую пробу из лабораторной пробы по ИСО 661.
Если кислотность пробы ниже или равна 3,0%, пробу очищают, пропуская ее через окись алюминия по 8.2.
Если кислотность более 3,0%, вначале нейтрализуют пробу гидроокисью натрия в присутствии растворителя по 8.1, затем очищают ее, пропуская через окись алюминия по 8.2.
Растворяют (10 +/- 1) г испытуемой пробы в 100 см3 гексана или легкого петролейного эфира (5.1.2) и переносят раствор в делительную воронку (6.1.5). Приливают 50 см3 изопропилового или этилового спирта (5.1.1), несколько капель раствора фенолфталеина (5.1.5) и объем гидроокиси натрия (5.1.4), эквивалентный содержанию свободных жирных кислот жира или масла, с избытком 0,5%. Тщательно перемешивают в течение 1 мин и приливают 50 см3 воды, вновь перемешивают и дают отстояться. После разделения слоев сливают нижний слой, содержащий мыло, и промежуточные слои (слизистые и нерастворимые вещества). Промывают раствор нейтрализованного масла в гексане или легком петролейном эфире последовательными порциями по 25 см3 раствора изопропилового или этилового спирта (5.1.3) до тех пор, пока розовый цвет фенолфталеина не исчезнет.
Переносят раствор в колбу ротационного испарителя (6.1.3) и выпаривают большую часть растворителя под вакуумом. Высушивают масло при 30 - 40 °C под вакуумом в токе азота (5.1.7) до тех пор, пока растворитель не будет удален полностью.
Готовят суспензию из 15 г активированной окиси алюминия (5.1.6) в 50 см3 гексана или легкого петролейного эфира (5.1.2) и заполняют ею при постукивании хроматографическую колонку (6.1.2). Убеждаются, что окись алюминия ровно заполнила колонку, оставляют слой растворителя на 1 - 2 мм выше верхнего уровня адсорбента. Осторожно приливают в колонку приготовленный и нейтрализованный (если необходимо) раствор 5 г испытуемой пробы в 25 см3 гексана или легкого петролейного эфира (5.1.2) и собирают весь элюат в круглодонную колбу вместимостью 100 см3 (6.1.6).
Удаляют большую часть растворителя выпариванием в ротационном испарителе под вакуумом, затем высушивают масло при 30 - 40 °C под вакуумом в токе азота (5.1.7) до тех пор, пока растворитель не будет удален полностью.
8.3. Гидролиз триглицеридов
8.3.1. Взвешивают навеску продукта массой (0,1 +/- 0,01) г очищенной испытуемой пробы (8.2) в центрифужную пробирку вместимостью 10 см3 (6.2.2). Если эта навеска не жидкая при комнатной температуре, помещают пробирку в ячейку водяной бани при температуре 60 - 65 °C. Если при этом навеска не расплавится полностью, ее продолжают выдерживать в бане, но не более 10 с.
Вынимают пробирку из водяной бани и продолжают выполнять в быстрой последовательности испытания в соответствии с 8.3.2 - 8.3.5.
8.3.2. Добавляют к жидкой навеске предварительно взвешенные 20 мг липазы (5.2.6) и 2 см3 буферного раствора (5.2.5). Осторожно встряхивают и добавляют последовательно 0,5 см3 раствора холата натрия (5.2.3) и 0,2 см3 раствора хлорида кальция (5.2.4). Закрывают пробирку пробкой, осторожно встряхивают и сразу же помещают пробирку в ячейку водяной бани при 40 °C, выполняя ручное встряхивание в течение (60 +/- 2) с. Все операции до начала ручного встряхивания должны быть выполнены за 30 с.
8.3.3. Извлекают пробирку из водяной бани и интенсивно встряхивают при 40 °C в течение (120 +/- 2) с, используя встряхиватель (6.2.3).
8.3.4. Незамедлительно приливают 1 см3 соляной кислоты (5.2.2) и 1 см3 диэтилового эфира (5.2.1). Закрывают пробкой и интенсивно встряхивают на встряхивателе (6.2.3).
8.3.5. Центрифугируют содержимое центрифужной пробирки и переносят органическую фазу в пробирку для испытания с помощью шприца (6.2.5). Если проба была твердой при комнатной температуре, повторяют экстракцию с еще 1 см3 диэтилового эфира и объединяют экстракты в пробирке для испытания.
8.4. Отделение 2-моноглицеридов
Тщательно очищают стеклянные пластинки (6.3.3) этиловым спиртом (5.3.1), гексаном или легким петролейным эфиром (5.3.2) и ацетоном (5.3.3) до тех пор, пока жировые вещества не будут удалены полностью.
Взвешивают 30 г силикагеля (5.3.4) в коническую колбу вместимостью 250 см3 (6.3.10). Приливают 60 см3 воды. Закрывают пробкой и интенсивно встряхивают в течение 1 мин. Сразу же вносят суспензию в аппликатор (6.3.2). Наносят на очищенные пластинки слой толщиной 0,25 мм. Оставляют пластинки высыхать не менее чем на 1 ч на воздухе.
В любом случае, подготовлены ли пластинки способом, описанным выше, или приобретены готовыми, активируют пластинки в термостате (6.3.7) при 103 °C в течение 1 ч. Перед использованием пластинки охлаждают до комнатной температуры в эксикаторе (6.3.13).
Для уменьшения скорости продвижения кислот пластинки с силикагелем должны быть пропитаны борной кислотой.
Испытуемая смесь должна быть разделена с помощью тонкослойной хроматографии как можно скорее.
В связи с тем что некоторые силикагели содержат органические вещества, которые могут оказывать влияние на результаты в процессе хроматографического анализа, рекомендуется выполнять контрольное определение для того, чтобы убедиться, что силикагели не содержат таких веществ. В противном случае заранее очищают подготовленные пластинки, помещая их в хроматографическую камеру с растворителем (5.3.5) и дают растворителю подняться до верха пластинки.
Допускается применение других хроматографических пластинок, по техническим характеристикам не хуже указанных.
8.4.2. Отделение 2-моноглицеридов
С помощью микрошприца (6.3.4) на подготовленную пластинку (8.4.1) наносят экстракт (8.3.5) каплями в виде сплошной полосы, проходящей на расстоянии 15 мм от нижнего края пластинки.
Устанавливают пластинку в хроматографическую камеру (6.3.1), которая была предварительно насыщена парами разделяющего растворителя (5.3.5). Закрывают камеру крышкой и осуществляют хроматографирование веществ на пластинке до тех пор, пока фронт растворителя не достигнет уровня на расстоянии 10 мм от верхнего края пластинки.
Хроматографическое разделение проводят при температуре 20 °C. Высушивают пластинку на воздухе при температуре 20 °C и опрыскивают ее раствором индикатора (5.3.6), используя приспособление для опрыскивания (6.3.5). Отмечают полосу моноглицеридов ( приблизительно) в ультрафиолетовом свете (6.3.8) и соскребают ее микрошпателем (6.3.6), избегая попадания в нее компонентов с линии старта.
приблизительно) в ультрафиолетовом свете (6.3.8) и соскребают ее микрошпателем (6.3.6), избегая попадания в нее компонентов с линии старта.
 приблизительно) в ультрафиолетовом свете (6.3.8) и соскребают ее микрошпателем (6.3.6), избегая попадания в нее компонентов с линии старта.
приблизительно) в ультрафиолетовом свете (6.3.8) и соскребают ее микрошпателем (6.3.6), избегая попадания в нее компонентов с линии старта.Если очищенные испытуемые пробы (8.2) были жидкими при комнатной температуре, помещают собранный силикагель в колбу для метилирования вместимостью 25 см3 (6.3.9) и выполняют операции, описанные в 8.5.
Если очищенные испытуемые пробы (8.2) были твердыми при комнатной температуре, переносят силикагель в коническую колбу вместимостью 50 см3 (6.3.11), содержащую 15 см3 диэтилового эфира. Интенсивно встряхивают и переносят содержимое на стеклянный пористый фильтр (6.3.12). Промывают фильтр троекратно, используя каждый раз порцию по 15 см3 диэтилового эфира, и собирают фильтрат в колбу для выпаривания. Выпаривают эфирный раствор до объема 4 - 5 см3 и переносят его в предварительно взвешенную круглодонную колбу вместимостью 25 см3 (6.3.9). Затем выпаривают растворитель в токе азота. Взвешивают остаток. Полученное количество моноглицеридов должно колебаться от 10 до 30% от массы испытуемой пробы. Если результат иной, повторяют гидролиз триглицеридов (8.2) или проверяют активность липазы (см. Приложение А).
Готовят метиловые эфиры жирных кислот из моноглицеридов, подвергая собранный силикагель (или экстракт моноглицеридов из силикагеля) процедуре, установленной ГОСТ Р 51486, используя метод, пригодный для нейтральных жиров и масел. Проводят газохроматографический анализ метиловых эфиров по ГОСТ Р 51483.
Рассчитывают отношение массы метилового эфира каждой жирной кислоты в положении 2, выраженное в процентах, к общей массе метиловых эфиров жирных кислот в 2-моноглицеридах.
Результаты записывают с точностью до первого десятичного знака.
Расхождение между результатами двух независимых единичных определений, выполненных при использовании одного метода, на идентичном испытуемом материале, в одной лаборатории, одним аналитиком, на одном оборудовании, в течение короткого промежутка времени, не должно превышать, при доверительной вероятности P = 0,95:
0,2 (абсолютное значение) - при содержании искомых веществ менее 5%;
1 (абсолютное значение) и 3 (по отношению к среднему значению двух результатов) - при содержании искомых веществ, равном или более 5%.
Расхождение между результатами двух единичных определений, выполненных одним методом, на идентичном испытуемом материале, в разных лабораториях, разными аналитиками, на различном оборудовании, не должно превышать, при доверительной вероятности P = 0,95:
0,5 (абсолютное значение) - при содержании искомых веществ менее 5%;
3 (абсолютное значение) и 10 (по отношению к среднему значению двух результатов) - при содержании искомых веществ, равном или более 5%.
(обязательное)
А.1. Приготовление липазы
Охлаждают 5 кг свежей свиной поджелудочной железы до 0 °C. Удаляют твердый жир и соединительную ткань, ее окружающую, и измельчают железу до получения жидкой пасты. Перемешивают эту пасту с 2,5 дм3 безводного ацетона в течение 4 - 6 ч на холоде и затем центрифугируют.
Экстрагируют остаток еще три раза, используя тот же объем ацетона; дважды используют смесь одной объемной доли ацетона и одной объемной доли диэтилового эфира и дважды используют диэтиловый эфир.
Высушивают остаток в течение 48 ч под вакуумом до образования порошка. Порошок хранят в холодильнике.
А.2. Проверка активности липазы
Готовят масляную эмульсию, встряхивая смесь 165 см3 гуммиарабика концентрации 100 г/дм3, 15 г дробленого льда и 20 см3 предварительно нейтрализованного масла в течение 10 мин на пригодном для этой цели миксере.
Наливают последовательно 10 см3 эмульсии, 0,3 см3 раствора хлората натрия (200 г/дм3) и 20 см3 дистиллированной воды в стакан вместимостью 50 см3.
Помещают стакан в водяную баню при 37 °C (см. примечание).
В стакан опускают электроды pH-метра и пропеллерную мешалку и, используя бюретку вместимостью 5 см3, приливают по каплям раствор c (NaOH) = 0,1 моль/дм3 до тех пор, пока не будет достигнуто значение pH 8,5.
Приливают соответствующий (см. примечание) и точно отмеренный объем 0,1%-ной водной суспензии анализируемого порошка липазы. Как только pH достигнет значения 8,3 по шкале pH-метра, включают секундомер и добавляют раствор молярной концентрации c (NaOH) = 0,1 моль/дм3 так, чтобы значение pH 8,3 сохранялось. Записывают объем раствора щелочи, приливаемого каждую минуту в течение 10 мин.
Наносят полученные данные на график, откладывая на оси X время в минутах и на оси Y объем в сантиметрах кубических раствора щелочи, использованного для поддержания постоянного значения pH. Результат должен выражаться в виде прямой линии.
Примечания
1. Когда используют жидкое масло, гидролиз проводят при 37 °C. Однако для испытания устанавливают температуру 40 °C, позволяющую проанализировать жиры, имеющие температуру плавления до 45 °C.
2. Для испытания образцов используют такое количество суспензии липазы, при котором потребляется 1 см3 раствора щелочи за 4 - 5 мин. Такой результат обычно достигается при использовании 2 - 5 см3 суспензии липазы, то есть от 1 до 5 мг порошка.
Единица липазы определяется как количество энзима, которое требуется для высвобождения 1 мкмоль кислоты в минуту при 37 °C и pH 8,3.
Активность A, выраженную в единицах липазы на миллиграмм использованного порошка, определяют по формуле

где V - объем израсходованного раствора гидроокиси натрия, разделенный на время опыта, рассчитанный по графику, см3/мин;
m - масса испытуемой пробы порошка липазы; используемая липаза должна иметь активность от 8 до 20 единиц липазы на миллиграмм;
c - концентрация раствора гидроокиси натрия, ммоль/дм3 - c = 100 ммоль/дм3.
(справочное)
БИБЛИОГРАФИЯ