СПРАВКА
Источник публикации
М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2023
Примечание к документу
Взамен МУК 3.2.988-00.
Название документа
"МУК 3.2.3804-22. 3.2. Профилактика паразитарных болезней. Методы санитарно-паразитологической экспертизы рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки. Методические указания"
(утв. Роспотребнадзором 02.12.2022)
"МУК 3.2.3804-22. 3.2. Профилактика паразитарных болезней. Методы санитарно-паразитологической экспертизы рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки. Методические указания"
(утв. Роспотребнадзором 02.12.2022)
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный врач
Российской Федерации
А.Ю.ПОПОВА
2 декабря 2022 года
3.2. ПРОФИЛАКТИКА ПАРАЗИТАРНЫХ БОЛЕЗНЕЙ
МЕТОДЫ САНИТАРНО-ПАРАЗИТОЛОГИЧЕСКОЙ ЭКСПЕРТИЗЫ РЫБЫ,
МОЛЛЮСКОВ, РАКООБРАЗНЫХ, ЗЕМНОВОДНЫХ, ПРЕСМЫКАЮЩИХСЯ
И ПРОДУКТОВ ИХ ПЕРЕРАБОТКИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
МУК 3.2.3804-22
1. Разработаны ФБУН "Тюменский научно-исследовательский институт краевой инфекционной патологии" Роспотребнадзора (Т.Ф. Степанова, Р.Г. Фаттахов, М.И. Беляева, А.В. Ушаков, К.Б. Степанова, И.В. Бакштановская, Р.В. Кошкарев, Т.Н. Цыбина); Институтом медицинской паразитологии, тропических и трансмиссивных заболеваний им. Е.И. Марциновского ФГАОУ ВО "Первый Московский государственный медицинский университет им. И.М. Сеченова" Минздрава России (О.П. Зеля, В.Д. Завойкин, А.Н. Лукашев); ФБУН "Хабаровский научно-исследовательский институт эпидемиологии и микробиологии" Роспотребнадзора (О.Е. Троценко, А.Г. Драгомерецкая); ФБУН "Ростовский научно-исследовательский институт микробиологии и паразитологии" Роспотребнадзора (Т.И. Твердохлебова, О.С. Думбадзе, С.А. Нагорный, М.П. Черникова, М.А. Калюжина); ФГБОУ ВО "Курский государственный университет" (Н.С. Малышева); ФБУЗ "Центр гигиены и эпидемиологии в городе Москве" (Н.И. Тимошенко, М.В. Касаткина); ФБУЗ "Центр гигиены и эпидемиологии в Самарской области" (М.В. Видманова).
2. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 2 декабря 2022 г.
3. МУК 3.2.3804-22 введены взамен МУК 3.2.988-00 "Методы санитарно-паразитологической экспертизы рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки", утвержденных Главным государственным санитарным врачом Российской Федерации, Первым заместителем министра здравоохранения Российской Федерации 25.10.2000.
1.1. Настоящие методические указания (далее - МУК) устанавливают методы санитарно-паразитологической экспертизы рыбы и нерыбных объектов (моллюсков, ракообразных, земноводных, пресмыкающихся), а также продуктов их переработки на соответствие требованиям безопасности по паразитологическим показателям <1>.
--------------------------------
<1> Федеральный закон Российской Федерации от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения"; Федеральный закон Российской Федерации от 02.01.2000 N 29-ФЗ "О качестве и безопасности пищевых продуктов"; технический регламент Таможенного Союза "О безопасности пищевой продукции" (далее - ТР ТС 021/2011), утвержденный решением Комиссии Таможенного союза от 09.12.2011 N 880; технический регламент Евразийского экономического союза "О безопасности рыбы и рыбной продукции" (далее - ТР ЕАЭС 040/2016), утвержденный решением Совета Евразийской экономической комиссии от 18.10.2016 N 162.
1.2. МУК предназначены для органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также могут быть использованы испытательными лабораториями, осуществляющими контроль качества и безопасности продовольственного сырья и пищевых продуктов и аккредитованными в установленном порядке <2>.
--------------------------------
<2> Федеральный закон от 28.12.2013 N 412-ФЗ "Об аккредитации в национальной системе аккредитации"; ГОСТ ISO/IEC 17025 "Общие требования к компетентности испытательных и калибровочных лабораторий (Переиздание)", утвержденный приказом Росстандарта от 15.07.2019 N 385-ст.
1.3. МУК носят рекомендательный характер.
2.1. К заболеваниям, передающимся через необезвреженную рыбу, ракообразных, моллюсков, земноводных, пресмыкающихся и продуктов их переработки, относятся описторхоз, клонорхоз, метагонимозы, нанофиетоз, псевдамфистомоз, дифиллоботриозы, анизакидозы, которые являются наиболее распространенными. Существует риск заражения личинками Metorchis bilis (albidus), Heterophyes heterophyes, Echinochasmus perfoliatus, Diphyllobothrium balaenopterae, рода Cryptocotyle и других паразитов через необезвреженную рыбную продукцию.
2.2. Предметом санитарно-паразитологических исследований является пищевая рыбная продукция, полученная из уловов водных биологических ресурсов и объектов аквакультуры животного происхождения, в переработанном или непереработанном виде (рыба, моллюски, ракообразные, земноводные, пресмыкающиеся). Среди паразитов, встречающихся в рыбе, водных беспозвоночных и в других водных животных, опасными для здоровья человека являются личинки гельминтов: трематод, цестод, нематод и скребней.
2.3. Опасность заражения для человека представляют живые личинки гельминтов. При паразитологической экспертизе рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки следует определять жизнеспособность выявленных метацеркарий, плероцеркоидов, личинок нематод и скребней.
водных беспозвоночных, других водных животных
и продуктов их переработки
3.1. Отбор проб рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки осуществляется для исследования по паразитологическим показателям.
3.2. Отбор проб в рыбодобывающих, рыбоперерабатывающих организациях, в рыбоводных хозяйствах и от поставщиков производят методом случайной выборки. Вес объединенной пробы не должен превышать 3 кг одноименной продукции. Мелкую рыбу, нерыбные объекты отбирают в количестве 10 - 12 экземпляров из разных мест исследуемой партии (не более 3 кг). Крупную рыбу (при весе 1 экземпляра более 1,5 - 2 кг) и крупные экземпляры нерыбных объектов отбирают в количестве не более 3 экземпляров из разных мест исследуемой партии. Пробы замороженных сырых полуфабрикатов отбирают из трех мест транспортной упаковки по 2 - 3 кусочка или 1 - 2 единицы потребительской упаковки.
3.3. Отбор проб замороженных полуфабрикатов в виде блоков допускается с применением ножа, долота, топора или другого инструмента. Для формирования объединенной пробы (не более 3 кг) откалывают по 2 - 3 куска от 3 разных блоков (мест). Продукты в потребительской упаковке отбирают по одной или две единицы от каждого вскрытого транспортировочного ящика (коробки).
3.4. Отбор проб в организациях торговли и общественного питания производят с учетом объема продукции (кг) методом случайной выборки из 3 - 5 мест транспортной или потребительской упаковки: не менее 1 экземпляра (кусочка, упаковки) одноименной продукции из одной транспортной или потребительской упаковки (не более 1 - 2 кг); при весе 1 экземпляра рыбы не более 2 кг отбирают 2 - 3 экземпляра; от целых экземпляров рыб весом более 2 кг отбирают по 5 - 10 проб в виде кусочков общим весом не менее 0,5 кг в зависимости от цели и вида исследования.
3.5. Отбор средней пробы икры-зерна производят из трех мест обследуемой партии общей массой не более 100 грамм. Отбор проб икры, расфасованной в бочки, проводят щупом из верхнего, среднего и нижнего слоев. Отбор проб икры, расфасованной в металлические и стеклянные банки, проводят по одной единице расфасовки (если в банке меньше 50 г, то отбирают две единицы расфасовки) по каждому виду тары и по ассортименту: икра зернистая развесная - 25 - 50 г из потребительской упаковки; икра зернистая консервированная (баночная) - 1 - 2 банки от партии. Молоки и ястыки отбирают по 2 - 3 кусочка из разных мест общей массой 100 г. Рыбный фарш отбирают из разных мест общей массой около 200 г из 3 - 5 точечных проб. Пресервы и консервы отбирают по 2 банки от партии. Моллюски и раки - по 3 экземпляра из каждой транспортной упаковки или 1 потребительскую упаковку, но не более 1,0 - 1,5 кг.
3.6. Продукцию, не имеющую потребительской упаковки, отбирают в чистую стеклянную посуду или полиэтиленовые мешки с возможностью герметичного закрывания. Каждая проба упаковывается и маркируется для возможности идентификации. Доставка образцов в испытательную лабораторию должна осуществляться в термоконтейнерах или термосумках с использованием охлаждающих элементов для поддержания необходимого температурного режима и предотвращения дефростации замороженных объектов.
3.7. Каждая проба сопровождается актом отбора проб, где указываются: наименование предприятия, организации (заявителя); наименование пробы (образца); объем отбираемой пробы; метод отбора пробы; нормативные документы на оценку объекта испытания; место отбора, адрес изготовителя; дата изготовления; номер партии; объем партии; условия хранения; дополнительные сведения (цель исследований, например, экспертиза, заявка организации).
3.8. В случае возникновения разногласий в оценке качества и безопасности продукции, а также по требованию заинтересованной стороны должен быть произведен отбор удвоенного количества средней пробы, одну часть которой направляют на испытания, а вторую оставляют. Вторая проба должна быть опечатана или опломбирована и должна храниться до получения результатов испытаний в аккредитованной лаборатории, проводящей испытания.
3.9. Поступившую на испытания пробу регистрируют в рабочем журнале (формуляре), указывая следующие данные:
- порядковый номер (лабораторный номер);
- код пробы (образца);
- дату поступления пробы (образца) в лабораторию;
- цель направления пробы (образца);
- определяемые показатели;
- метод исследования.
3.10. Хранить свежую или охлажденную рыбу, водных беспозвоночных, других водных животных и продукты их разделки до исследования следует в холодильнике при температуре плюс 2 - 4 °C. Замороженная рыбная продукция (сырье, полуфабрикаты и готовые изделия) до исследования хранится при температуре и в условиях согласно нормативно-технической документации на нее и до исследования не должна подвергаться дефростации.
3.11. Непосредственно перед исследованием мороженую продукцию размораживают до температуры не ниже 0 °C в толще тела рыбы, моллюсков, ракообразных, земноводных, пресмыкающихся и продуктов их переработки. Живых ракообразных помещают в кипяток или усыпляют для обездвиживания (п. 5.6).
3.12. При исследовании вяленой, соленой и копченой рыбы ее предварительно вымачивают в течение суток до размягчения мышц, меняя воду каждые 4 - 6 ч в течение рабочего дня. На ночь убирают в холодильник (плюс 5 - 6 °C).
3.13. Другие виды рыбной продукции (пресервы, икра, молоки, жареная рыба, фарш и пр.) специальной подготовки не требуют и сохраняются в холодильнике до начала исследования. Рыбный фарш, котлеты из рыбы могут храниться не более 24 ч при температуре плюс 2 - 4 °C, жареная рыба - до 36 ч при температуре плюс 2 - 4 °C.
3.14. Видовую принадлежность исследуемого образца, поступившего в лабораторию, определяют по документам, сопровождающим пробу (акт отбора проб, товаросопроводительная документация).
и реактивы <3>
--------------------------------
<3> Примечание. Допускается использование оборудования, лабораторной посуды, материалов и реактивов с аналогичными или с лучшими характеристиками.
Таблица 1
Наименование оборудования | Обозначение и наименование документов, технические характеристики |
Микроскоп стереоскопический, микроскоп бинокулярный | - |
Микроскоп медицинский, микроскоп биологический | ГОСТ 28489 |
Окуляр-микрометр | Для светового микроскопа |
Окуляр-микрометр | Для бинокулярного микроскопа |
Весы электронные | |
Холодильник бытовой электрический | |
Дозаторы пипеточные одноканальные | С диапазоном измерения 100 - 1000 мкл, погрешность +/- 1,0 - 1,5% |
Термометры жидкостные (не ртутные) | |
Лупа | |
Мясорубка, блендер или другой прибор для измельчения | - |
Нож (долото, топор или другой инструмент) | - |
Лабораторный источник постоянного тока | С диапазонами напряжения 0 - 15 В и силы тока 0 - 3 А |
Компрессорий | Размер ячейки 13 x 11 мм, толщина каждой пластины 6 мм |
Таймер электронный (лабораторный) | - |
Сантиметр или линейка |
Таблица 2
Лабораторная посуда и материалы
Наименование лабораторной посуды и материалов | Обозначение и наименование документов, технические характеристики |
1 | 2 |
Пробирки | |
Цилиндры мерные | 0,5 - 0,25 л ГОСТ 1770 |
Ножницы медицинские | |
Пинцеты медицинские | |
Иглы гистологические препаровальные прямые | - |
Скальпель хирургический | |
Кюветы эмалированные металлические | - |
Бюксы разных размеров | - |
Колбы | Вместимостью 200, 400, 1000, 1600 см3 ГОСТ 1770 |
Банки стеклянные с притертой пробкой для хранения реактивов | 0,1, 0,25, 0,5 л ГОСТ 34037 |
Стекла предметные для микропрепаратов | |
Стекла предметные | 6 - 8 x 12 - 15 см, толщиной 3 - 5 мм |
Стекла покровные для микропрепаратов | |
Стекла часовые | ГОСТ 14183 |
Ситечки | С ячеей 1 x 1 мм |
Чашки биологические Петри | |
Химические стаканы | |
Пипетки стеклянные пастеровские | - |
Пипетки | Вместимостью 1 - 10 см3 ГОСТ 29227 |
Груши резиновые | - |
Спиртовки лабораторные стеклянные | |
Бумага фильтровальная | |
Вата медицинская гигроскопическая | |
Марля медицинская | |
Проволока медная | |
Нить швейная для наложения лигатур | N 10 |
Таблица 3
Наименование реактивов | Обозначение и наименование документов, технические характеристики |
Глицерин | 50% ГОСТ 6259 |
Вода дистиллированная | |
Желчь сухая или желчь нативная сельскохозяйственных животных | - |
Калия гидроокись | |
Калий хлористый | |
Кальций двухлористый | - |
Кислота соляная | 35 - 38% ГОСТ 3118 |
Натрия гидроокись | |
Натрий хлористый | |
Натрий углекислый | |
Нейтральный красный (нейтральрот) | - |
Метиленовый синий | 1,0% |
Молочная кислота | 80% ГОСТ 490 |
Пепсин | - |
Раствор физиологический | 0,9% |
Розоловая кислота (аурин) | - |
Спирт этиловый ректификованный | 96,0% ГОСТ 5962 |
Трипсин | 0,5% |
Формалин | 40%-й раствор формальдегида |
Хлороформ | |
Эфир |
животных в целях оценки ихтиопаразитологического
состояния водоема
5.1. При оценке ихтиопаразитологического состояния рыбохозяйственного водоема (района промысла) исследуют виды рыб, наиболее подверженные заражению. Индикаторами неблагополучия водоема в отношении инвазии личинками Opisthorchis felineus является язь, далее по убывающей - елец, плотва, лещ и т.д.; в отношении Opisthorchis (Clonorchis) sinensis - дальневосточные виды семейства Cyprinidae: горчаки обыкновенный и Лайта, карась серебряный, троегуб, сазан, язь амурский. В отношении Dibothriocephalus latus (Diphyllobothrium latum) - щука и налим. Для исследования на наличие метацеркарий Opisthorchis felineus, Opisthorchis (Clonorchis) sinensis и плероцеркоидов Dibothriocephalus latus (D. latum) целесообразнее отбирать рыб старших возрастов, т.к. число личинок увеличивается с возрастом рыб. Для установления места заражения рыб семейства Cyprinidae личинками возбудителей описторхоза и клонорхоза исследуют сеголеток, так как первое лето своей жизни карповые виды рыб проводят вблизи от места своего рождения. Метацеркарии Metorchis bilis чаще обнаруживаются у сеголеток и рыб младших возрастов, а Echinochasmus perfoliatus - преимущественно у мальков. Индикаторами неблагополучия водоема в отношении инвазии личинками Nanophyetus salmincola schikhobalowi являются ленок острорылый, далее по убывающей - таймень сибирский, ленок тупорылый, сиг амурский, хариус нижнеамурский. Индикаторами неблагополучия водоема в отношении инвазии личинками трематод рода Metagonimus являются конь пятнистый, верхогляд, толстолоб, подуст, горчак амурский, карась, язь амурский, востробрюшка.
5.2. До начала исследования следует определить, какими потенциальными носителями видов гельминтов, опасных для здоровья человека, являются рыбы, моллюски, ракообразные, земноводные и пресмыкающиеся. Один и тот же вид позвоночных или беспозвоночных животных может служить дополнительным или резервуарным (факультативным) хозяином для нескольких видов гельминтов (приложение 1 к настоящим МУК).
5.3. Перед исследованием рыбу (или нерыбный объект промысла) отмывают от слизи, протирают, взвешивают, измеряют длину и делают записи в журнале (бумажном и (или) электронном), касающиеся учета исследований.
5.4. Для определения возраста у рыб с циклоидной чешуей последнюю берут с переднебоковой поверхности выше боковой линии в количестве 15 - 20 крупных чешуек. У рыб с ктеноидной чешуей, а также с голой кожей берут отолиты или колючий шип грудного плавника.
5.5. Для исследования на наличие метацеркарий Metagonimus yokogawai, Metagonimus katsuradai и Metagonimus suifunensis sp. n. отбирают по 20 чешуек из разных частей тела рыбы в спинной области, у карася - вдоль боковой линии. Крупные чешуйки (у сазанов, карасей) перед исследованием просветляют в течение 15 - 20 мин в 50%-м растворе глицерина (приложение 3 к настоящим МУК).
5.6. Перед исследованием живых раков и крабов рекомендуется поместить в кипящую воду на 0,5 - 1,0 мин (в зависимости от размеров ракообразных) до прекращения движения или усыпить их эфиром или хлороформом. Для этого помещают раков и крабов в бюксы или другую стеклянную посуду с хорошо притертой крышкой, под которую кладут тампон, смоченный эфиром или хлороформом.
5.7. На основании комплексных лабораторных исследований (пп. 6.2 - 6.5, 7.2 - 7.6) рыбы, водных беспозвоночных, других водных животных и выявления личинок, опасных для здоровья человека, оценивается ихтиопаразитологическое состояние водоема <4>.
--------------------------------
<4> Глава XLIII СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденных постановлением Главного государственного санитарного врача Российской Федерации от 28.01.2021 N 4 (зарегистрировано Минюстом России 15.02.2021, регистрационный N 62500).
беспозвоночных, других водных животных и продуктов
их переработки
6.1. Выбор метода исследования.
6.1.1. Порядок исследования и необходимость проведения всех или только отдельных его этапов зависит от вида (видов) гельминта (его личинок), встречающегося в исследуемом объекте, типичной локализации личинок в нем и вида продукции (приложения 2 - 6, 12 к настоящим МУК).
6.1.2. При исследовании рыбной продукции используют два основных подхода:
- выявление личинок гельминтов, видимых невооруженным глазом (плероцеркоиды, акантеллы (личинки скребней), личинки нематод размером более 2 мм) путем тщательного осмотра всех органов, полостей и тканей промежуточных (или резервуарных) хозяев (приложения 2, 5, 6 к настоящим МУК);
- выявление личинок гельминтов, плохо видимых или не видимых невооруженным глазом (в основном метацеркарий трематод и мелких нематод), путем исследования органов и тканей (мест наиболее вероятной локализации) с использованием оптических средств. Уточнение видовой принадлежности личинок гельминтов в обоих случаях ведется с применением световых микроскопов (микроскоп бинокулярный стереоскопический, далее - тип МБС; микроскоп стереоскопический панкратический, далее - тип МСП) (приложения 3, 5 к настоящим МУК).
6.1.3. На наличие метацеркарий большинства видов трематод исследуют только верхний слой мышечной ткани и подкожную клетчатку в области спинных мышц. Для обнаружения метацеркарий Metagonimus yokogawai, Metagonimus katsuradai и Metagonimus suifunensis sp. n. в первую очередь исследуют чешую, Echinochasmus perfoliatus - жабры, Apophallus muhlingi и Rossicotrema donicum - ткани плавников, Nanophyetus salmincola schikhohalowi - почки (приложения 3, 7, 9 к настоящим МУК).
6.1.4. Мороженую, соленую, пряную, маринованную, вяленую, сушеную и копченую рыбную продукцию после предварительного вымачивания исследуют по методике неполного гельминтологического вскрытия. При обнаружении личинок гельминтов определяют их жизнеспособность (глава VII).
6.1.5. Продукты переработки рыбы (пресервы, фарш, жареная или заливная рыба) предварительно осматривают, а затем исследуют компрессорным методом или методом переваривания в искусственном желудочном соке (пп. 6.4 - 6.5).
6.1.6. Рыбу потрошеную обезглавленную, разделанную на тушку, спинку, кусок и филе, лапки земноводных, мышечные ткани и мантию двустворчатых моллюсков, а также мантию головоногих в зависимости от целей паразитологической экспертизы (вида гельминта) исследуют по одной из предложенных методик исследования мускулатуры (пп. 6.3 - 6.5).
6.1.7. Икру (гонады), как свежую, так и продукты ее переработки, исследуют в соответствии с методикой неполного гельминтологического исследования рыбы, земноводных и пресмыкающихся (п. 6.2.6). Молоки (семенники) тщательно осматривают снаружи на наличие полостных паразитов. Внутри молок опасные для здоровья человека личинки паразитов отсутствуют.
6.2.1. Рыбу вскрывают в большом эмалированном кювете или на широкой гладкой доске. Проводят наружный осмотр рыбы для выявления личинок, просвечивающих через кожу, извлекают их препаровальной иглой.
6.2.2. Затем вырезают левую стенку полости тела и открывают доступ к последней. Для этого, повернув рыбу брюхом кверху, делают короткий надрез вперед от анального отверстия, куда затем вводят тупой конец ножниц и разрезают рыбу вдоль срединной линии брюшка до угла нижней челюсти. Делают дугообразный надрез, вырезают левую брюшную стенку, отделяют ее. Рыбу кладут на правый бок. При внимательном осмотре полости тела и внутренних органов могут быть обнаружены свободно лежащие или под серозной оболочкой, или в капсулах личинки цестод, нематод, скребней, видимые невооруженным глазом.
6.2.3. Накладывают лигатуры на кишечник близ анального отверстия и на пищевод в его начальном отделе, чтобы содержимое пищеварительного тракта не вышло наружу. Затем извлекают внутренние органы. Вырезают яичники (икру) или семенники (молоки), помещая их в отдельные чашки Петри, и просматривают. Осматривают плавательный пузырь снаружи и внутри. Вырезают и осматривают сердце, а также сердечную полость. Компрессорным методом исследуют содержимое, оставшееся в полости тела (п. 6.4). Полость протирают марлевой салфеткой, соскабливают брюшину.
6.2.4. Проводят препарацию органов пищеварительной системы. Выделяют желчный пузырь, лежащий на поверхности печени, так, чтобы его содержимое (в том числе и паразиты) не залило остальные внутренние органы. Затем выделяют пищеварительный тракт, печень, селезенку, поджелудочную железу. Данные органы отделяют друг от друга и от окружающей их жировой ткани и осматривают. Жировую ткань разрезают на тонкие пластинки толщиной около 3 мм или исследуют компрессорно между стеклами на темном фоне (п. 6.3 - 6.4). Исследуют освобожденный от жировой ткани пищеварительный тракт, отыскивая личинок в капсулах на его поверхности или просвечивающих через серозные покровы (Dibothriocephalus dendriticus (Diphyllobothrium dendriticum), Dibothriocephalus latus, Dioctophyme renale, Eustrongylides exicisus, Corynosoma strumosum, Corynosoma semerse, Bolbosoma caenoforme, личинки семейства Anisakidae). Пилорические придатки (развитые у налимовых, сиговых, лососевых) расправляют и осматривают снаружи (Pyramicocephalus phocarum, личинки семейства Anisakidae). Стенки желудка и пищевода после наружного осмотра вскрывают, соскабливают их содержимое и исследуют под бинокулярным стереоскопическим микроскопом.
6.2.5. При наружном осмотре печени невооруженным глазом можно заметить плероцеркоиды цестод (Dibothriocephalus latus, Pyramicocephalus phocarum, Eustrongylides exicisus) и личинки семейства Anisakidae. Поджелудочную железу, селезенку, печень осматривают снаружи и также разрезают на пластинки толщиной около 3 мм (п. 6.3).
6.2.6. У яичника разрезают оболочку, содержимое соскабливают и компрессируют (могут быть обнаружены плероцеркоиды Dibothriocephalus latus) (п. 6.4). Компрессорным методом просматривают только мелкую икру. При исследовании крупных икринок следует разбирать их препаровальными иглами в чашке Петри с небольшим добавлением воды.
6.2.7. Почки соскабливают и по частям исследуют компрессорным способом, добавляя несколько капель воды (п. 6.4). При исследовании лососеобразных рыб промыслового размера (лососевых, сиговых, хариусовых) на наличие личинок Nanophyetus salmincola schikhobalowi почки исследуют в первую очередь, так как метацеркарии обнаруживаются в них при любой, даже самой низкой, интенсивности инвазии (приложения 7, 9 к настоящим МУК).
6.2.8. Плавники просматривают под микроскопом (типа МБС, МСП) в небольшом количестве воды. Могут быть заметны в виде маленьких черных точек пигментированные цисты Apophallus muhlingi и Rossicotrema donicum, а также метацеркарии Metagonimus yokogawai, Metagonimus katsuradai и Metagonimus suifunensis sp. n. (приложения 3, 7, 9, 11 к настоящим МУК). Мышцы плавников исследуют компрессорным способом (п. 6.4).
6.2.9. Снимают жаберную крышку и ножницами вырезают все жаберные дуги. Их по очереди рассматривают в чашке Петри под микроскопом (типа МБС, МСП), перебирая лепестки препаровальными иглами и одновременно контролируя то, чтобы они были покрыты водой. Затем отрезают от дуги лепестки у их основания и, разбирая препаровальными иглами, выявляют паразитов, оставшихся незамеченными. На жабрах можно обнаружить метацеркарий Echinochasmus perfoliatus, Metagonimus yokogawai, Metagonimus katsuradai, Metagonimus suifunensis sp. n., Nanophyetus salmincola, Opisthorchis felineus.
6.2.10. После просмотра внутренних органов с рыбы снимают кожу в направлении от головы к хвосту, подрезая ее ножницами и оттягивая хирургическим пинцетом или рукой. Осматривают внутреннюю сторону кожи, а часть мышц, отделившихся с кожей, разрезают на пластинки или соскабливают и компрессируют (п. 6.4).
6.2.11. При экспертизе земноводных и пресмыкающихся исследуют полость тела, органы и ткани, включая мускулатуру (пп. 6.2.4 - 6.2.7).
6.2.12. Двустворчатые моллюски. Для раскрытия раковины скальпель вводят между створками и разрезают мускул-замыкатель. Из открытой раковины, надрезав мантию в передней ее части, сливают мантийную жидкость. Между одной из створок и прилегающей к ней мантийной складкой вводится плоская ручка скальпеля. Двигая ее по краю створки вперед и назад, сначала отделяют край мантии, прикрепленный к створке, затем передний и задний мускулы-замыкатели (аддукторы). На следующем этапе отделяют мантию и аддукторы от другой створки, после чего раковина легко удаляется. У гребешков и устриц аддуктор один и находится в середине тела, несколько ближе к заднему краю.
6.2.13. Вынутое из раковины тело моллюска помещают в кювету (или чашку Петри) с водой. Осматривают мантию и просвечивающие в спинной части тела через полупрозрачную кожу внутренние органы: печень, лежащую непосредственно позади переднего аддуктора или на спинной стороне над аддуктором (у гребешков и устриц), перикардий и граничащие с задним аддуктором почки. Обнаруженных личинок нематод извлекают препаровальной иглой.
6.2.14. Мантийные складки отрезают и компрессируют (п. 6.4). Затем отрезают и осматривают жабры.
6.2.15. Препарируют гонады, залегающие в спинной части ноги. Они расчленены и слагаются из многочисленных мелких долек, окружающих петлю кишечника. Гонады исследуют компрессорным способом (п. 6.4). Здесь наиболее вероятно обнаружение личинок Echinochephalus sinensis и Sulcascaris sulcata. Затем выделяют пищеварительную систему и исследуют таким же образом (приложения 5, 10 к настоящим МУК).
6.2.16. Аддукторы и ногу исследуют так же, как мускулатуру у рыб (пп. 6.3 - 6.4). Аддуктор гребешков - место наиболее вероятной локализации Sulcascaris sulcata.
6.2.17. Выявленных личинок помещают в чашку Петри или на часовое стекло с физиологическим раствором для дальнейшего определения вида паразита.
6.2.18. Головоногие моллюски. У кальмаров и каракатиц разрезается мантия на брюшной стороне. Разрез делают ножницами или скальпелем по срединной линии, начиная от края мантии, до основания плавника, не повреждая чернильный мешок. У осьминогов разрезают мускулистую продольную перегородку, открывая доступ в мантийную полость. Отгибают стенки мантии и осматривают внутренности. Последовательно отделяют жабры, гонады, пищеварительную систему. Внутренние органы исследуют компрессорно (п. 6.4). Особое внимание обращают на гонаду, где возможно обнаружение личинок нематод рода Anisakis. Освобожденную от внутренних органов мантию исследуют аналогично мышечной ткани рыб - методом параллельных разрезов (п. 6.3). На внутренней стороне мантии в пленках встречаются личинки нематод родов Anisakis и Contracaecum.
6.2.19. Ракообразные. При экспертизе пресноводных крабов и раков на наличие метацеркарий парагонимид в первую очередь исследуют мышцы грудного отдела и сердце как места наиболее вероятной локализации личинок (до 90% случаев) (приложения 7, 9 к настоящим МУК). Для этого у ракообразных ножницами срезают карапакс (верхний щит панциря) и с помощью скальпеля вырезают мышцы грудного отдела. Из задней части грудного отдела вычленяют сердце, со стороны головогруди срезают жабры и исследуют, используя компрессорный метод (п. 6.4).
6.2.20. Для выделения мяса из абдомена (брюшко) последний отрезают от груди и ножницами разрезают панцирь от верхнего края "шейки" до тельсона (хвостового веера). Конечности (у крабов и раков) разрезают на части (поперек) вблизи кожистых суставов, одновременно разрезая хитиновую пластинку, прикрепленную к суставу. Панцирные трубки разрезают вдоль и извлекают мясо, клешню разбивают. Всю мышечную ткань просматривают компрессорным методом или методом переваривания в искусственном желудочном соке (пп. 6.4 - 6.5).
6.3.1. Метод применяется для обнаружения в мышечной ткани рыб, моллюсков, ракообразных, земноводных и пресмыкающихся личинок гельминтов, видимых без использования увеличительных приборов (цестод, нематод, скребней).
6.3.2. Мышечную ткань острым скальпелем разрезают на пластинки толщиной до 5 мм, которые затем раздвигают и просматривают в падающем свете невооруженным глазом. Разрезы выполняют поперек и вдоль мышечных волокон. Делая разрезы мускулатуры и встречая в ее толще крупных личинок или капсулы с личинками (величиной около 1 см и более), извлекают несколько экземпляров паразитов целиком для определения вида.
6.3.3. Выделенных личинок помещают в чашку Петри или на часовое стекло с физиологическим раствором.
6.3.4. При исследовании тихоокеанских лососей, кунджи и сахалинского тайменя на наличие плероцеркоидов Dibothriocephalus nihonkaiensis (D. luxi, D. klebanovskii) разрезы проводят поперек мышечных волокон всей дорсальной части тела; большинство личинок локализуется между жировым и спинным плавниками (приложение 8 к настоящим МУК).
6.4.1. Метод применяется в основном для выявления метацеркарий трематод. Используют метод при просмотре мышечной ткани и внутренних органов рыб, а также мышечной ткани ракообразных. Возможно его использование при исследовании внутренних органов рыб, водных беспозвоночных и других водных животных на наличие личинок нематод и цестод.
6.4.2. Компрессорному исследованию подвергают органы и участки мышечной ткани наиболее вероятной локализации метацеркарий (приложения 3, 4, 9 к настоящим МУК).
6.4.3. Участок тела наиболее вероятной локализации метацеркарий освобождают от чешуи, затем скальпелем надрезают кожу по средней линии спины и двумя надрезами от первого надреза до боковой линии, выделяют участок средней трети спины. Кожу с вычлененного участка поднимают пинцетом и с помощью скальпеля отделяют ее так, чтобы подкожная клетчатка осталась на поверхности мышц. Острым скальпелем соскабливают или срезают тонкие пластинки поверхностного слоя мышц толщиной не более 2 - 3 мм, размещают их на нижнем стекле компрессория, накрывают другим стеклом и сдавливают их.
6.4.4. Срезы просматривают с помощью микроскопа (типа МБС, МСП). Для уточнения видовой принадлежности метацеркарий трематод кусочки тканей с личинками переносят на предметные стекла, накрывают покровными и исследуют при большем увеличении с помощью биологического микроскопа.
6.4.5. При обнаружении личинок ограничиваются просмотром мышц с одной стороны тела. При отсутствии личинок необходимо просмотреть срез и с другой стороны.
6.4.6. При исследовании молоди рыб длиной до 20 - 25 мм их компрессируют целиком. Более крупных сеголеток распластывают на две половинки и просматривают в компрессории со стороны разреза, не снимая кожи и не освобождая от чешуи.
6.4.7. Подсыхающие срезы, препараты увлажняют водой или физиологическим раствором из пипетки.
6.5.1. Метод используется для выделения метацеркарий трематод, реже личинок нематод (приложения 3 - 5, 8 - 9 к настоящим МУК), из тканей рыб, водных беспозвоночных, других водных животных и продуктов их переработки (соленая, вяленая, копченая, жареная рыба, фарш, пресервы и др.). Метод основан на том, что в кислой среде метацеркарии освобождаются от наружной оболочки, а окружающая их мышечная ткань переваривается в искусственном желудочном соке.
6.5.2. Приготовление искусственного желудочного сока. На 1000 мл дистиллированной воды (при ее отсутствии можно использовать кипяченую остывшую до температуры плюс 37 - 38 °C водопроводную воду) добавляют 7 г пепсина, 9,0 г поваренной соли и 10 мл концентрированной (35 - 38%) соляной кислоты. Искусственный желудочный сок годен для применения в течение 8 часов с момента приготовления. Хранится в холодильнике при температуре плюс 5 - 8 °C.
6.5.3. Для выделения метацеркарий трематод берут подкожную мышечную ткань (до 0,5 см), а мелких личинок нематод - всю мышечную ткань. Ее отделяют от кожи, измельчают ножом или в мясорубке (при выделении личинок Nanophyetus salmincola schikhobalowi используют дополнительно и почки). Затем ее заливают в соотношении 1:10 приготовленным искусственным желудочным соком (1 часть фарша и 10 частей искусственного желудочного сока). Пробу помещают в термостат на 3 ч при температуре плюс 36 - 37 °C, периодически помешивая стеклянной палочкой.
6.5.4. Содержимое фильтруют в стеклянные цилиндры через металлический фильтр с размером ячеек 1 x 1 мм или однослойный бинт. После отстаивания (15 - 20 мин) верхний слой желудочного сока с переваренной мышечной тканью сливают; а осадок переносят в чашку Петри (или глубокое часовое стекло) и микроскопируют.
6.5.5. Для лучшего отделения личинок в чашку Петри наливают физиологический раствор, делают несколько круговых движений, в результате которых метацеркарии концентрируются в центре чашки Петри (часового стекла), а излишки физиологического раствора с остатками мышечной ткани удаляют пипеткой. Процедуру повторяют до полного исчезновения остатков непереваренной мышечной ткани.
6.5.6. Метацеркарии трематод, выделенные этим способом из свежей рыбы, сохраняют свою структуру и жизнеспособность в физиологическом растворе в течение 10 - 24 ч при температуре плюс 20 - 25 °C и 5 - 7 дней при температуре плюс 1 - 4 °C.
7.1. При обнаружении личинок в рыбной продукции, в том числе при оценке эффективности ее обеззараживания, необходимо определить жизнеспособность <5> всех выделенных личинок.
--------------------------------
<5> ГОСТ 34812 "Продукция рыбная пищевая. Методы определения жизнеспособности личинок гельминтов (с Поправкой)", утвержденный приказом Росстандарта от 31.03.2022 N 186-ст.
7.2.1. Личинок цестод, нематод и скребней помещают в чашку Петри или часовое стекло с подогретым физиологическим раствором (плюс 37 - 40 °C) и рассматривают под микроскопом (типа МБС, МСП) при увеличении, соответствующем размеру личинки или ее рассматриваемой части. Инцистированных личинок извлекают из оболочек. Живые личинки могут не проявлять признаков активности. Их движение можно стимулировать с помощью физического раздражения, уколов личинки острой препаровальной иглой. У живой личинки уколы вызывают сокращение тела. Личинок семейства Anisakidae (в физиологическом растворе) помещают на 2 ч в термостат при температуре плюс 37 °C. Изменение цвета, отслоение покровов, другие деструктивные изменения тела указывают на нежизнеспособность личинок. Если видимых изменений нет, но и признаков жизни обнаружить не удается, то применяют метод химического воздействия.
7.2.2. Метацеркарии трематод, выделенные из тканей рыбы (или ракообразных) с помощью препаровальной иглы (или посредством переваривания в искусственном желудочном соке), помещают в каплю теплой воды или физиологического раствора (плюс 37 - 40 °C) на предметное стекло, накрывают покровным стеклом и исследуют на жизнеспособность под малым и большим увеличением микроскопа. Метацеркарии обладают способностью совершать движения, находясь в цисте. Наличие движений личинки свидетельствует о ее жизнеспособности. Отсутствие движения еще не свидетельствует о гибели личинки. Движение стимулируют слабым нажатием препаровальной иглой на покровное стекло с препаратом метацеркарий. Нежизнеспособность метацеркарий устанавливают по деструктивным морфологическим признакам: нарушение целостности оболочек цист, изменение внутреннего строения личинки и распад ее содержимого, разрушение экскреторного пузыря.
7.3. Метод электрического стимулирования (с использованием постоянного электрического тока) используют для определения жизнеспособности личинок нематод, цестод и скребней.
7.3.1. Личинок помещают в чашку Петри на мокрую фильтровальную бумагу, смоченную физиологическим раствором, и воздействуют на них слабым постоянным электрическим током с напряжением в диапазоне 0,5 - 1,5 В (при необходимости допускается ступенчатое повышение напряжения и силы электрического тока от минимальных выходных параметров к максимальным). Для этого два изолированных провода от положительного и отрицательного полюсов прибора (лабораторный источник постоянного тока с диапазонами напряжения 0 - 15 В и силы тока 0 - 3 А) прикрепляют к двум препаровальным иглам так, чтобы зажимы проводов прибора фиксировались на металлической части препаровальной иглы. При наличии в комплектации прибора щупов ток подается непосредственно ими. Проявление сократительных движений личинок контролируют под микроскопом (типа МБС, МСП).
7.4. Метод химического воздействия (с использованием химических раздражителей).
7.4.1. Вызвать движение личинок можно, воздействуя 0,5%-м раствором трипсина. В основном метод применяют для определения жизнеспособности метацеркарий трематод.
7.4.2. На выделенных метацеркарий наносят несколько капель химического реагента так, чтобы полностью покрыть личинки. Для ускорения эксцистирования предметное (или часовое) стекло с личинками можно слегка подогреть над пламенем спиртовки или внести предварительно подогретый до плюс 37 - 40 °C 0,5%-й раствор трипсина, либо поставить в термостат при плюс 37 °C на 10 мин. Через несколько секунд под воздействием химического раздражителя начинается выход личинок из цист и их активное движение, что служит показателем жизнеспособности. Процесс эксцистирования личинок контролируют под микроскопом (типа МБС, МСП). Отсутствие в течение 30 мин всякой двигательной реакции свидетельствует о гибели личинок.
7.4.3. Для определения жизнеспособности личинок нематод из рыбы или моллюсков, подвергнутых ранее замораживанию или холодному копчению, гельминтов инкубируют в термостате при плюс 37 °C в физиологическом растворе или 0,5%-м растворе трипсина. Личинок инкубируют в течение трех дней, ежедневно проверяя их жизнеспособность.
7.5. Метод окрашивания (с использованием красителей).
7.5.1. В зависимости от используемого красителя окрашиваются либо живые, либо мертвые личинки гельминтов.
7.5.2. Личинок нематод, цестод и скребней помещают в чашку Петри (или часовое стекло) с раствором метиленового синего (метиленовый синий - 0,05 г, натрий едкий - 0,5 г, молочная кислота - 15 мл). Мертвые личинки окрашиваются в синий цвет. У них хорошо прокрашиваются нервные волокна и ядра клеток. Живые личинки остаются неокрашенными, так как не пропускают краску через свою оболочку. Живыми считаются только недеформированные личинки, не окрасившиеся в течение 2 ч.
7.5.3. Живые плероцеркоиды окрашиваются водным раствором нейтральрота (0,1 г нейтрального красного разводят в 100 мл дистиллированной воды) в течение 5 - 20 мин, приобретая стойкую розовую окраску. Для контроля личинки извлекают из краски, помещают в чистый физиологический раствор и в нем просматривают степень окрашивания. Мертвые личинки не получают стойкой окраски.
7.5.4. Для определения жизнеспособности метацеркарий трематод используют окрашивание раствором розоловой кислоты (0,3 г розоловой кислоты растворяют в 100 мл 70%-го спирта). Кусочки мышц с личинками освобождают от жира. На ткань наносят 2 капли розоловой кислоты, а через 2 мин - две капли 0,1 N нормального раствора гидроокиси калия, равномерно распределяя его по ткани. Избыток жидкости с препарата снимают фильтровальной бумагой. Накрывают покровным стеклом и микроскопируют. Ткань рыбы окрашивается в розовый цвет, живые личинки не окрашиваются, а мертвые становятся розовыми.
7.6.1. Биологическая проба (заражение лабораторных животных) рекомендуется при специальных исследованиях в учреждениях, имеющих условия (виварий) для содержания лабораторных животных. Метод основан на способности большинства видов гельминтов, паразитирующих у человека, приживаться и у других млекопитающих. Наиболее удобным лабораторным животным для этой цели является золотистый хомяк. В некоторых случаях необходимо использовать других животных (котят, белых мышей и крыс).
7.6.2. Кусочки внутренних органов или мышц дополнительных (или резервуарных) хозяев с личинками скармливают лабораторным животным. Через определенное для каждого вида гельминта время в фекалиях животного обнаруживают яйца паразита. Затем животное усыпляют и вскрывают методом неполного гельминтологического вскрытия. Обнаруженных гельминтов определяют до вида.
7.6.3. Цестоды. Для дифиллоботриид в качестве лабораторных животных можно использовать золотистых хомяков, которым скармливают по 5 - 10 плероцеркоидов. Яйца цестод могут быть обнаружены в фекалиях лабораторных животных через 2 - 3 недели для Dibothriocephalus latus и Dibothriocephalus nihonkaiensis, через 1 - 2 недели - для Dibothriocephalus dendriticus. При заражении золотистых хомяков спарганумами Spirometra erinaceieuropaei они остаются на личиночной стадии и яйца не выделяются.
7.6.4. При вскрытии животных половозрелые лентецы рода Dibothriocephalus могут быть обнаружены в тонком кишечнике, спарганумы спирометры - в полости тела, внутренних органах, подкожной клетчатке, мышцах. Для получения половозрелой спирометры можно заразить собаку или кошку. В этом случае яйца гельминта можно обнаружить через 12 - 15 дней у собак и через 10 - 14 - у кошек.
7.6.5. Трематоды. Opisthorchis felineus, Metorchis bilis, Opisthorchis (Clonorshis) sinensis, Nanophyetus salmincola schikhobalowi приживаются у золотистых хомяков. В сомнительных случаях дифференциальной диагностики между Opisthorchis felineus и Pseudamphistomum truncatum заражают молочных котят, так как Pseudamphistomum truncatum не приживаются у хомяков. Metagonimus yokogawai, Metagonimus kaisuradai, Metagonimus suifunensis sp. n., Rossicotrema donicum, Apophallus muehlingi также развиваются только у котят и щенят собак. Для заражения возбудителями парагонимоза наиболее часто используют лабораторных мышей и крыс.
7.6.6. Нематоды. Лабораторным животным (лучше котятам и щенятам) скармливают (или вводят с помощью пинцета) кусочки рыбы с личинками в количестве 20 - 25 экземпляров. Через 3 - 6 дней животных усыпляют с последующим гельминтологическим обследованием желудка и кишечника на наличие личинок.
7.6.7. Способы заражения животных метацеркариями.
7.6.7.1. Заражение личинками, содержащимися в мышечной ткани рыбы (или ракообразных). Для этого исследуют рыбу компрессорным методом (п. 6.4), замечают местоположение цист и, глядя в микроскоп (типа МБС, МСП; увеличение: окуляр 8x, объектив 2x), верхнее стекло осторожно сдвигают в сторону и препаровальными иглами выбирают кусочки ткани вместе с метацеркариями, стараясь их не повредить; набирают по 30 личинок и скармливают опытным животным (золотистым хомякам массой 40 - 70 г; молочным котятам и щенятам, белым крысам массой 70 - 90 г; белым мышам массой 18 - 25 г).
7.6.7.2. Введение животным через рот личинок, полученных в результате переваривания рыбы (или ракообразных) в искусственном желудочном соке (п. 6.5). Метацеркарии отмывают в физиологическом растворе, подсчитывают и вводят в желудок животным с помощью шприца со специальной канюлей. Метацеркарии Opisthorchidae вводят в количестве 50 личинок на одну особь, а Paragonimidae - в количестве 20 экземпляров на особь.
7.6.7.3. Выделение яиц Opisthorchis felineus, Pseudamphistomum truncatum, Metorchis bilis, Opisthorchis (Clonorshis) sinensis начинается через 20 - 25 суток после заражения. При вскрытии животных через 3 - 5 недель после заражения половозрелых трематод обнаруживают в желчных протоках печени, желчном пузыре и селезенке.
7.6.7.4. Выделение яиц Metagonimus yokogawai, Metagonimus katsuradai, Metagonimus suifunensis sp. n., Nanophyetus salmincola schikhobalowi, Rossicotrema donicum, Apophallus muehlingi начинается на 11 - 16 сутки после заражения. При вскрытии животных гельминтов обнаруживают в тонком кишечнике.
7.6.7.5. Вскрытие животных после заражения метацеркариями Paragonimidae производят через 40 - 60 дней. В первую очередь исследуют легкие. Затем последовательно изучают все органы и ткани, в которых могут быть обнаружены личинки в случае развития ларвального парагонимоза или парагонимоза с атипичной локализацией.
8.1. Для фиксации желательно брать живых личинок гельминтов. Перед фиксацией паразитов следует осторожно отделить от окружающих тканей (метацеркарии трематод и мелких личинок нематод предпочтительнее с помощью метода переваривания в искусственном желудочном соке) (п. 6.5). Перед погружением в фиксирующую жидкость для отделения личинок от крови, слизи и других загрязнений, а также при необходимости их расправления личинок цестод и скребней следует поместить в воду, а личинок трематод и нематод в физиологический раствор или раствор Рингера (хлористый натрий - 0,65 г, хлористый калий - 0,025 г; карбонат натрия - 0,02 г; двухлористый кальций - 0,03 г, бидистиллированная вода - 100 мл. Соли растворяют в указанном порядке) на 15 - 30 мин.
8.2. Объем фиксатора должен превышать объем фиксируемого материала в 20 - 40 раз.
8.3. Личинок цестод, трематод, скребней фиксируют в 70%-м этиловом спирте. Для того чтобы хоботок у скребней и сколекс у цестод оставался в вывернутом состоянии, применяют способ осторожного, но достаточно сильного сдавливания червей между стеклами, подпуская пипеткой 80%-й этиловый спирт. Избыток фиксирующей жидкости оттягивают фильтровальной бумагой со стороны, противоположной пипетке. Выдерживают 15 - 20 мин. Затем стекло осторожно приподнимают и личинку переносят в 70%-й этиловый спирт.
8.4. Личинок круглых червей рекомендуется фиксировать и хранить в жидкости Барбагалло (4%-й раствор формалина в физиологическом растворе). Чтобы тело личинки при фиксации не скручивалось, рекомендуется фиксация горячей (до плюс 70 °C) жидкостью Барбагалло.
9.1. Результаты исследований вносятся в рабочий журнал (формуляр), где отмечаются ход исследования (применяемый метод паразитологического исследования), сведения о наличии или отсутствии личинок паразитов. При обнаружении личинок указывается вид гельминта, жизнеспособность личинок, метод установления жизнеспособности, количество личинок, а также место локализации (органы и ткани). Оформляется протокол результатов исследований (табл. 4 - 5).
Таблица 4
при положительном результате
ПАРАЗИТОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ | ||||
Регистрационный номер, код пробы (образца) | Определяемые показатели | Результаты исследований (вид возбудителя, жизнеспособность, экстенсивность и интенсивность инвазии) | Гигиенический норматив | Номер документа на методы исследования |
1 | Личинки паразитов в живом виде | Обнаружены жизнеспособные личинки Opisthorchis felineus. ИИ - 50 личинок в верхнем участке средней трети спины | Не допускаются личинки паразитов в живом виде | |
ИС МЕГАНОРМ: примечание. Сноска дана в соответствии с официальным текстом документа. |
--------------------------------
<6> МУ 3.2.3463-17 "Профилактика дальневосточных трематодозов", утвержденные Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации 27.03.2017.
Таблица 5
при отрицательном результате
ПАРАЗИТОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ | ||||
Регистрационный номер, код пробы (образца) | Определяемые показатели | Результаты исследований (вид возбудителя, жизнеспособность, экстенсивность и интенсивность инвазии) | Гигиенический норматив <7> | Номер документа на методы исследования |
1 | Личинки паразитов в живом виде | Не обнаружены | Не допускаются личинки паразитов в живом виде | |
--------------------------------
9.2. После проведения исследования необходимого числа экземпляров рыб регистрируются следующие показатели:
- экстенсивность инвазии (ЭИ) - степень зараженности рыб в процентах. Определяется делением числа зараженных экземпляров на число исследованных с последующим умножением на 100 (подсчитывается, когда число исследованных рыб равняется или превышает 15 экземпляров);
- интенсивность инвазии (далее - ИИ) - количество паразитов, обнаруженных у зараженных рыб (мин, макс), а также их среднее значение. Делением общего количества паразитов на число зараженных рыб определяется средняя ИИ.
9.3. Для расчета ИИ у лососеобразных рыб промыслового размера личинками Nanophyetus salmincola schikhobalowi используется формула:
I = 2n,
где I - интенсивность инвазии;
n - число метацеркарий, обнаруженных в почках.
9.4. Расчет ИИ у язей промысловых размеров метацеркариями Opisthorchis felineus проводится по формуле:
I = 10n,
где n - число метацеркарий в верхнем участке средней трети спины.
9.5. При наличии в рыбной продукции видимых невооруженным глазом погибших и не опасных для здоровья человека и животных личинок гельминтов по результатам исследований вычисляют показатели зараженности рыбы данного вида:
- ЭИ;
- ИИ;
- средняя интенсивность инвазии - число личинок, приходящееся в среднем на одну зараженную рыбу;
- индекс обилия - число личинок, приходящееся на одну исследованную (не только зараженную) особь рыбы данного вида;
- амплитуда интенсивности - величины минимальной и максимальной интенсивности, встречаемые в обследованной выборке;
- среднее число паразитов на 1 кг массы - находится делением общего числа паразитов в выборке на общую массу (в кг) выборки.
9.6. Чтобы облегчить подсчет выявленных при исследовании паразитов, цифры зараженности каждой особи (интенсивность) записываются в виде рабочей таблицы (табл. 6).
Таблица 6
Число паразитов в рыбе (куске) | Число рыб (кусков), содержащих соответствующие количества паразитов | Общие количества паразитов в рыбах, зараженных одинаково |
0 | 17 - число незараженных рыб | 0 |
1 | 6 | 6 |
2 | 4 | 8 |
3 | 1 | 3 |
5 | 2 | 10 |
17 | 1 | 17 |
23 | 1 | 23 |
- | Всего обследовано рыб (кусков) - 32 | Общее число паразитов в выборке - 67 |
Цифры правой вертикальной колонки получаются перемножением цифр соответствующего горизонтального ряда двух предшествующих колонок. Записывается также общая масса выборки: для нашего примера примем 30 кг. Из сделанных записей определяются следующие показатели. Экстенсивность инвазии: (15:32 x 100) = 46,9%. Амплитуда интенсивности: от 0 до 23. Индекс обилия: (67:32) = 2,1 паразитов. Среднее число паразитов на 1 кг массы: (67:30) = 2,2. Последний показатель определяют и при обнаружении паразитов, не представляющих опасности для здоровья человека.
к МУК 3.2.3804-22
БИОГЕЛЬМИНТОВ, ОПАСНЫХ ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА
1. Потенциальными носителями личинок возбудителя описторхоза Opisthorchis felineus являются следующие виды рыб семейства карповых: язь Leuciscus idus (Linnaeus, 1758), елец Leuciscus leuciscus (Linnaeus, 1758), плотва обыкновенная (синонимы: вобла, тарань, чебак, сорога) Rutilus rutilus (Linnaeus, 1758), плотва сибирская Rutilus rutilus lacustris (Pallas, 1814), лещ Abramis brama (Linnaeus, 1758), пескарь Gobio gobio (Linnaeus, 1758), уклея Alburnus alburnus (Linnaeus, 1758), верховка Leucaspius delineatus (Heckel, 1843) (для Сибири, Урала, бассейнов рек Оби, Иртыша, Урала, Енисея), голавль Squalius cephalus (Linnaeus, 1758), синец Ballerus ballerus (Linnaeus, 1758), белоглазка Ballerus sapa (Pallas, 1814), чехонь Pelecus cultratus (Linnaeus, 1758), жерех Aspius aspius (Linnaeus, 1758), линь Tinca tinca (Linnaeus, 1758), красноперка Scardinius erythrophthalmus (Linnaeus, 1758), гольян обыкновенный Phoxinus phoxinus (Linnaeus, 1758), гольян озерный Phoxinus percnurus (Pallas, 1811), гольян Чекановского Phoxinus czekanowski (Dybowski, 1869), густера Blicca bjoerkna (Linnaeus, 1758), подуст Chondrostoma nasus (Linnaeus, 1758).
Помимо карповых в качестве потенциальных носителей выступают рыбы семейства вьюновых: щиповка обыкновенная Cobitis taenia (Linnaeus, 1758) (для европейской части Российской Федерации, бассейнов рек Волги, Камы, Дона, Днепра, Северной Двины), а также щиповка сибирская Cobitis melanoleuca (Nichols, 1925).
2. Носителями личинок возбудителя клонорхоза Opisthorchis (Clonorshis) sinensis являются многочисленные виды рыб семейства карповых бассейнов рек Уссури и Амура (среднего и нижнего течения): горчак Лайта Rhodeus lighti (Wu, 1931), горчак обыкновенный Rhodeus sericeus (Pallas, 1776), белый амур Ctenopharyngodon idella (Valenciennes in Cuvier and Valenciennes, 1844), черный амур Mylopharyngodon piceus (Richardson, 1846), золотой карась Carassius carassius (Linnaeus, 1758), серебряный карась Carassius gibelio (Bloch, 1782), сазан Cyprinus carpio (Linnaeus, 1758), уклей (амурская острогрудка) Culter alburnus (Basilewsky, 1855), амурский чебак (амурский язь) Leuciscus waleckii (Dybowski, 1869), гольян Лаговского (амурский гольян) Rhynchocypris lagowskii (Dybowski, 1869), белый толстолобик Hypophthalmichthys molitrix (Valenciennes, 1844), пестрый толстолоб Hypophthalmichthys nobilis (Richardson, 1845), амурский чебачок Pseudorasbora parva (Temminck et Schlegel, 1846), желтощек Elopichthys bambusa (Richardson, 1845), верхогляд Chanodichthys erythropterus (Basilewsky, 1855), сибирский пескарь Gobio gobio (Linnaeus, 1758), длиннохвостый колючий пескарь Saurogobio dabryi (Bleeker, 1872), конь-губарь Hemibarbus labeo (Pallas, 1776), пестрый конь (пятнистый конь) Hemibarbus maculatus (Bleeker, 1871), амурский лжепескарь Abbottina rivularis (Basilewsky, 1855), пескарь-лень Sarcocheilichthys sinensis (Bleeker, 1871), подуст-чернобрюшка (амурский подуст-чернобрюшка) Xenocypris argentea (Basilewsky, 1855).
К потенциальным носителям личинок возбудителя клонорхоза Opisthorchis (Clonorshis) sinensis относятся также представители семейств осетровых: калуга Huso dauricus (Georgi, 1775), амурский осетр Acipenser schrenckii (Brandt, 1869); вьюновых: сибирская щиповка Cobitis melanoleuca (Nichols, 1925), лептобоция манчжурская Parabotia fasciata (Dabry de Thiersant, 1872); головешковых: ротан Perccottus glenii (Dybowski, 1877); косатковых: косатка-скрипун Tachysurus fulvidraco (Richardson, 1846), малая косатка Tachysurus nitidus (Sauvage et Dabry, 1874); корюшковых: корюшка малоротая речная Hypomesus olidus (Pallas, 1811); цихлидовых: рода тиляпия Tilapia (Smith, 1840).
3. Потенциальными носителями личинок возбудителей метагонимоза Metagonimus yokogawa, Metagonimus katsuradai и Metagonimus suifunensis sp. n. являются следующие виды карповых: плотва обыкновенная Rutilus rutilus (Linnaeus, 1758), плотва сибирская Rutilus rutilus lacustris (Pallas, 1814), карась серебряный Carassius gibelio (Bloch, 1782), сазан Cyprinus carpio (Linnaeus, 1758), верхогляд Chanodichthys erythropterus (Basilewsky, 1855), пескарь Gobio gobio (Linnaeus, 1758), толстолобик Hypophthalmichthys molitrix (Valenciennes, 1844), белый амур Ctenopharyngodon idella (Valenciennes in Cuvier and Valenciennes, 1844), черный амур Mylopharyngodon piceus (Richardson, 1846), конь-губарь Hemibarbus labeo (Pallas, 1776), пестрый конь Hemibarbus maculatus (Bleeker, 1871), востробрюшка Hemiculter elongatus (Nguyen and Ngo, 2001), подуст Xenocypris argentea (Basilewsky, 1855).
Метацеркарии Metagonimus yokogawai часто обнаруживаются у сига Coregonus ussuriensis (Berg, 1906), хариуса Thymallus tugarinae (Knizhin, Antonov, Safronov et Weiss, 2006), а также у лососевых: у острорылого ленка Brachymystax lenok (Pallas, 1773), тупорылого ленка Brachymystax tumensis (Mori, 1931) (бассейны рек Уссури и Амура).
4. Потенциальными носителями личинок возбудителя нанофиетоза Nanophyetus salmincola schikhobalowi являются рыбы семейства лососевых: хариус Thymallus tugarinae (Knizhin, Antonov, Safronov et Weiss, 2006), сима Oncorhynchus masou (Brevoort, 1856), ленки Brachymystax (Gunther, 1866), таймень Hucho taimen (Pallas, 1773), кета Oncorhynchus keta (Walbaum, 1792), горбуша Oncorhynchus gorbuscha (Walbaum, 1792) в бассейнах рек нижнего Приамурья, Приуссурья и северного Сахалина. Встречается возбудитель и у представителей семейства карповых: амурский язь (амурский чебак) Leuciscus waleckii (Dybowski, 1869), амурский гольян (гольян Лаговского) Rhynchocypris lagowskii (Dybowski, 1869).
В семействе щуковых Nanophyetus salmincola schikhobalowi встречается у амурской щуки Esox reichertii (Dybowski, 1869) в реках Приамурья и Приморья.
5. Потенциальными носителями личинок возбудителей дифиллоботриозов являются следующие виды рыб:
5.1. Плероцеркоидов Dibothriocephalus latus - представители семейств щуковых: обыкновенная щука Esox lucius (Linnaeus, 1758); тресковые: налим Lota lota (Linnaeus, 1758); окуневых: обыкновенный окунь Perca fluviatilis (Linnaeus, 1758), обыкновенный ерш Gymnocephalus cernuus (Linnaeus, 1758), обыкновенный судак Sander lucioperca (Linnaeus, 1758), волжский судак (берш) Sander volgensis (Gmelin, 1789).
5.2. Плероцеркоидов Dibothriocephalus dendriticus - многочисленные виды рыб семейства лососевых: гольцы рода Salvelinus (Richardson, 1836), лосось Кларка (Salmo clarki), лосось Гарднера Salmo gairdneri, горбуша Oncorhynchus gorbuscha (Walbaum, 1792), семга Salmo salar (Linnaeus, 1758), кумжа Salmo trutta (Linnaeus, 1758), таймень Hucho taimen (Pallas, 1773), сахалинский таймень Parahucho perryi (Brevoort, 1856), кижуч Oncorhynchus kisutch (Walbaum, 1792), острорылый ленок Brachymystax lenok (Pallas, 1773), тупорылый ленок Brachymystax tumensis (Mori, 1931), хариусы рода Thymallus (Cuvier, 1829) и сиги: пелядь Coregonus peled (Gmelin, 1788), омуль Coregonus autumnalis (Pallas, 1776), сибирский сиг (пыжьян) Coregonus lavaretus pidschian (Gmelin, 1788), муксун Coregonus muksun (Pallas, 1814), чир Coregonus nasus (Pallas, 1776), тугун (сосьвинская сельдь) Coregonus tugun (Pallas, 1814), сибирская ряпушка Coregonus sardinella (Vallenciennes, 1848).
Личинками Dibothriocephalus dendriticas могут быть заражены представители семейства колюшковых: колюшка Pungitius bussei (Warpachowski, 1887), колюшка трехиглая Gasterosteus aculeatus (Linnaeus, 1758), колюшка девятииглая Pungitius pungitius (Linnaeus, 1758); из тресковых - налим Lota lota (Linnaeus, 1758); из корюшковых - корюшка малоротая речная Hypomesus olidus (Pallas, 1811).
5.3. Плероцеркоидов Dibothriocephalus nihonkaiensis (D. klebanovskii, D. luxi) - дальневосточных лососевых: кета Oncorhynchus keta (Walbaum, 1792), горбуша Oncorhynchus gorbuscha (Walbaum, 1792), кунджа Salvelinus leucomaenis (Pallas, 1814), сима Oncorhynchus masou (Brevoort, 1856), сахалинский таймень Parahucho perryi (Brevoort, 1856).
6. Потенциальными носителями личинок семейства Anisakidae и других, опасных для человека и животных гельминтов морской фауны (Diphyllobothrium balaenopterae, Pyramicocephalus phocarum, Cryptocotyle lingua, Corynosoma strumosum и др.), являются представители более 20 семейств промысловых морских рыб, ракообразных и моллюсков, в том числе семейства Nototheniidae: большой широколобик Pagothenia borchgrevinki (Boulenger, 1902) и малый широколобик Pagothenia brachysoma (Pappenheim, 1912); семейства сельдевых: сардина обыкновенная Sardina pilchardus (Walbaum, 1792), сардины родов Sardinops (Hubbs, 1929) и Sardinella (Valenciennes, 1847), сельдь тихоокеанская Clupea pallasii (Cuvier, 1817), салака Clupea harengus membras (Linnaeus, 1761); семейства скумбриевых: Scomber scomhrus (Linnaeus, 1758), тунцы рода Thunnus (South, 1845); лососевые: кета Oncorhynchus gorbuscha (Walbaum, 1792), горбуша Oncorhynchus gorbuscha (Walbaum, 1792), гольцы, кунджа Salvelinus leucomaenis (Pallas, 1814), мальма Salvelinus malma (Walbaum, 1792), кижуч Oncorhynchus kisutch (Walbaum, 1792), нерка Oncorhynchus nerka (Walbaum, 1792), чавыча Oncorhynchus tshawytscha (Walbaum, 1792), палия Salvelinus fontinalis (Mitchill, 1814); представители семейства ставридовых: ставрида Trachurus trachurus (Linnaeus, 1758); тресковых: треска Gadus morhua (Linnaeus, 1758), пикша Melanogrammus aeglefinus (Linnaeus, 1758), сколопендровые: морские окуни Sebastes (Cuvier, 1829); камбаловых: камбала Pleuronectes platessa (Linnaeus, 1758); волосохвостые: рыба-сабля Trichiuridae (Rafinesque, 1810); кальмары отряда Teuthida; креветки Caridea (Dana, 1852).
7. Потенциальными носителями личинок возбудителей семейства Paragonimidae являются ракообразные: раки Malacostraca (Latreille, 1802), крабы Brachyura (Linnaeus, 1758), креветки Caridea (Dana, 1852) из пресноводных водоемов Приморского края, бассейна Амура, водоемов КНР, Корейского полуострова, Японии, стран юго-восточной Азии, Шри-Ланки, Центральной Америки, Либерии, Нигерии, Камеруна, Мексики, Перу, Филиппин.
к МУК 3.2.3804-22
DIPHYLLOBOTHRIIDAE, ОПАСНЫХ ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА
N п/п | Вид гельминта | Географическое распространение | Дополнительные хозяева (рыбы, земноводные, пресмыкающиеся) | Локализация в теле хозяина | Наличие или отсутствие капсул | Строение и размеры плероцеркоида |
1 | 2 | 3 | 4 | 5 | 6 | 7 |
1 | Dibothriocephalus latus (Лентец широкий) | Пресные водоемы и опресненные участки морей севера Евразии (Российская Федерация, Латвия, Литва, Эстония, Финляндия, Дания, Швеция, Польша, Швейцария, Северная Италии и Франция); Северной Америки (США, Канада); бассейны Волги, Дуная, Днепра, сибирских рек | Щука, налим, окунь обыкновенный, окунь желтый, ерш, сом, судак обыкновенный, берш, судаки светлоперый и канадский | Полость тела, икра, внутренние органы, мышцы | Обычно без капсул | Личинки беловато-молочного цвета, длиной от нескольких мм до 7 см. На теле и сколексе нет заметных под световым микроскопом ворсинок. Характерно наличие на теле личинки глубоких складок, которые частично сохраняются и после расслабления в воде. Сколекс с двумя щелевидными ботриями обычно втянут |
2 | Dibothriocephalus dendriticus (Лентец чаечный) | Пресные водоемы севера Европы (Российская Федерация, Литва, Латвия, Эстония, Финляндия, Норвегия, Швеция, Польша, Германия, Ирландия, Великобритания); Канада, США; пресные водоемы Сибири (Российская Федерация), Дальнего Востока (Сахалин), оз. Иссык-Куль | Пелядь, омуль, сиг, голец, семга, лососи (Кларка, стальноголовый), муксун, чир, хариусы (сибирский и европейский), тугун, кумжа, таймень, ленок (острорылый и тупорылый), ряпушка сибирская, палия обыкновенная и американская, кижуч, корюшка, османы, налим, широколобки | На стенках и в толще стенок пищевода и желудка, реже на других органах и в мышечной ткани | Обычно в капсулах диаметром 2,2 - 11 мм. При локализации в икре, как правило, без капсул. У некоторых видов (например, сибирская ряпушка), наряду с личинками в капсулах, встречаются и свободно залегающие в полости тела плероцеркоиды | Личинки светлого кремового цвета. Длина 1 - 10 см, иногда до 20 см. После расслабления в воде складчатость слабо выражена. Сколекс четко отграничен от тела. Он обычно втянут или частично вытянут, при этом участки тела вокруг него образуют подобие "плечиков". Края ботридиальных листков выглядят фестончатыми. У расслабленных личинок сколекс приобретает овально-миндалевидную форму, ботридиальные щели раскрываются широко. Тело покрыто ворсинками длиной 7 - 11 мкм, которые на сколексе едва заметны |
3 | Dibothriocephalus nihonkaiensis (D. luxi, D. klebanovskii) (Лентец дальневосточный) | Дальний Восток. Чукотка, моря Тихого океана и бассейны рек, впадающих в них, в границах ареала дополнительных хозяев гельминта, за исключением северной части западного Приохотъя. Ареал D. nihonkaense не пересекается с ареалом D. latum | Тихоокеанские лососи: кета, горбуша, сима, кунджа, сахалинский таймень | Вся дорсальная мускулатура | Овальные капсулы с прозрачными стенками (4 - 6 x 2 - 5 мм). В мускулатуре горбуши раннего хода и симы личинки залегают без капсул или находятся на разных стадиях инкапсуляции | Плероцеркоиды морфологически сходны с личинками D. latum, но в отличие от них обычно инкапсулированы. Поры фронтальных желез располагаются на сколексе и теле личинки |
4 | Dibothriocephalus ditremus (D. ditremum) | Пресные водоемы севера Европы, Азии и Северной Америки (на юг до 40 - 50° с. ш.) | Семга, форель, арктический голец, палия американская, ряпушки (сибирская, европейская), омуль, сиг обыкновенный, пелядь, тугун, хариусы (сибирский, европейский), корюшки (европейская, зубастая), налим, колюшки (трехиглая и девятииглая) | Серозные покровы пищеварительного тракта (пищевод, желудок, пилорические придатки), реже на других внутренних органах | В капсулах | Плероцеркоиды белого цвета, длиной 6 - 12 мм, после расслабления и гибели в воде тело равномерно вытянутое, палочковидное, без складок, сколекс отграничен от тела. Тело и сколекс покрыты ворсинками длиной 0,01 - 0,03 мм. Выживает в воде не более 10 мин |
5 | Diplogonoporus balaenopterae | Северный Ледовитый океан, север Атлантического океана, север Тихого океана, Аляска, Япония, Южная Атлантика, Антарктика | Рыбы семейства камбаловых. Предположительно: анчоусы, японские сардины, полосатый тунец | На внутренних органах рыб, редко - в мускулатуре | В капсулах | Плероцеркоиды белого цвета, длиной 6 - 12 мм, после расслабления и гибели в воде тело равномерно вытянутое, палочковидное, без складок, сколекс отграничен от тела. Тело и сколекс покрыты ворсинками длиной 0,01 - 0,03 мм. Выживает в воде не более 10 мин |
6 | Pyramicocephalus phocarum | Субарктическая и арктическая зоны Мирового океана | Тресковые (треска, минтай, сайка, навага, пикша); скорпеновые (окунь-клювач); рогатковые (рогатка, керчак), пинагоровые (пинагор); камбаловые (камбала-ершоватка, камбала-ерш, камбала морская), палтус | Полость тела и сероза внутренних органов (печень, пилорические придатки желудка); у минтая и наваги встречается в скелетной мускулатуре | Без капсул | Морфологически сходны с личинками рода Dibothriocephalus (Diphyllobothrium). Длина тела 8 - 25 мм, до 40 мм, ширина 1 - 3 мм. Обычно тело в складках. Сколекс относительно массивный, булавовидно-стреловидной формы (размеры сколекса 2 x 1 мм) |
7 | Spirometra erinaceieuropaei | Европа и Азия. В Российской Федерации чаще всего встречается в дельте Волги, Приморье, на Сахалине | Земноводные (лягушка озерная, прудовая); пресмыкающиеся (уж водяной, уж обыкновенный, полозы) | У лягушек - в мышцах (чаще в бедрах), в полости тела, между петлями кишечника, во внутренних органах. У змей в подкожной клетчатке, полости тела, мускулатуре, межмышечной соединительной ткани | Обычно без капсул, у змей иногда в тонких капсулах на кишечнике или подкожно | Личинки молочно-белого цвета. Длина от 5 мм до 30 см и более, в зависимости от возраста и степени сокращения личинки. Выделенный из хозяина плероцеркоид характеризуется присутствием на теле узлов сокращения, чередующихся с расслабленными участками тела. В сокращенных участках тело широкое и плоское, с глубокими поперечными складками; в расслабленных участках - узкое и лишенное складчатости. Передний конец тела обычно сокращен сильнее других участков. Сколекс небольшой, от тела не обособлен, втянут внутрь и обычно повернут в сторону. Ботрии значительно короче, чем у других дифиллоботриид (0,2 - 0,4 мм) |
к МУК 3.2.3804-22
OPISTHORCHIDAE, HETEROPHYIDAE, NANOPHYETIDAE
И ECHINOSTOMATIDAE, ОПАСНЫЕ ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА
N п/п | Вид гельминта | Географическое распространение | Виды рыб - дополнительных хозяев | Локализация в теле рыбы | Размер (в мм) и характеристика цисты | Характеристика экскреторного пузыря | Положение и подвижность личинки | Строение и размеры освобожденной от цисты личинки (в мм) |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
1 | Opisthorchis felineus | Пресные водоемы Европы; бассейны рек Обь, Иртыш, Енисей, реки Казахстана: Уил, Сары-Су, Байконур, Уил-Жиланшик, Иргиз, Тургай, Нура, Шидерты, Кургальджинские озера | Язь, елец, линь, красноперка, плотва, верховка, голавль, лещ, чехонь, синец, гольян обыкновенный, подуст, белоглазка, уклея, густера, пескарь, щиповка, жерех | Верхний слой мышечной ткани (2 - 4 мм) и подкожная клетчатка в области спины, реже в плавниках, на жабрах, в чешуе | 0,17 - 0,34 x 0,23 - 0,43 овальная, реже округлая. Оболочка двуслойная, тонкая, прозрачная. Внутренняя, по всему периметру равномерно прилегает к наружной | Крупный, до 1/3 части тела. В лучах проходящего света в виде большого темного пятна | Метацеркария лежит в цисте в изогнутом положении, которое меняется из-за почти постоянного энергичного движения личинки | 0,44 - 1,36 x 0,15 - 0,30. РП <*> - 0,07 - 0,1; БП <**> - 0,09 - 0,14. Тело личинки не пигментировано, покрыто шипиками до уровня БП. Пищевод длинный (в 2 раза длиннее глотки). Развилка кишечника лежит на равном расстоянии от переднего конца тела и БП. Зачатки семенников лежат наискось один к другому по краям экскреторного пузыря |
2 | Metorchis bilis | Пресные водоемы Западной и Восточной Европы, Западной Сибири, реки Казахстана: Иргиз, Тургай, Шидерты, Уил, Сары-Су, Байконыр | Язь, елец, линь, красноперка, плотва (вобла), верховка, голавль, лещ, чехонь, синец, гольян обыкновенный, подуст, белоглазка, уклея, густера, пескарь, щиповка, жерех | Верхний слой мышечной ткани (2 - 4 мм) и подкожная клетчатка в области спины | 0,19 - 0,22 x 0,12 - 0,16 овальная. Оболочка тонкостенная двухслойная. Наружный слой стенки цисты бесцветный, гиалиновый, в виде прозрачного ободка, внутренний - гомогенный, слабо окрашенный | До 1/4 объема задней части тела черный, округлый | Движения замедленные | 0,27 - 0,33 x 0,05 - 0,1. РП несколько больше БП - 0,05, расположена несколько кзади от середины тела. Тело не пигментировано. Покрыто шипиками треугольной формы до уровня заднего края БП. Пищевод очень короткий |
3 | Pseudamphis Pseudamphistomum truncatum | Пресные водоемы средней полосы России, Поволжья, Казахстана, Западной Сибири, бассейны рек, впадающих в Черное море | Язь, плотва (вобла), густера, лещ, линь, красноперка, синец, белоглазка, уклея, чехонь, жерех | Верхний слой мышечной ткани (2 - 4 мм) и подкожная клетчатка в области спины | 0,43 - 0,63 x 0,37 - 0,56. Овальная, реже шаровидная. Оболочка тонкая прозрачная двуслойная. Слои равномерно прилегают друг к другу | Крупный черный округлый почковидный, занимает не более 1/3 тела. Пузырь заполнен экскретами, сильно преломляющими свет, благодаря чему он кажется темным в проходящем свете и темным в отраженном | Метацеркария сложена в средней части тела в вентральном положении, лежит в цисте свободно. Движения редкие | 1,28 - 1,54 x 0,34 - 0,40. БП, как правило, крупнее РП. Тело покрыто шипиками, немного не доходящими до заднего конца тела. Пищевод короткий, такой же длины, как глотка. Развилка кишечника лежит много выше, чем у Opisthorchis felineus, приближена к РП. Зачатки семенников лежат почти на одном уровне |
4 | Opisthorchis (Opisthorchis (Clonorshis) sinensis) | Пресные водоемы юго-восточных и центральных районов стран Дальнего Востока (Япония, Китай, Корея, Вьетнам). В Российской Федерации бассейны Амура и Уссури | Карповые китайского ихтиокомплекса (более 70 видов); косатковые: косатка-плеть, косатка-скрипун; японская оризия; сом Солдатова, амурский бычок; головешковые: китайский элеотрис, ротан, японская малоротая корюшка, змееголов, риногобиус, тиляпия | Верхний слой мышечной ткани (2 - 4 мм) и подкожная клетчатка в области спины | 0,13 - 0,15 x 0,15 - 0,18 шаровидной формы. Оболочка двуслойная, внутренняя равномерно прилегает к наружной | Черный грушевидный, до 1/4 части тела. Заполнен плотно расположенными гранулами (до 10 мкм) | Слабые движения | 0,3 - 0,4 x 0,12 - 0,14. РП - 0,05, БП - 0,06. Тело желто-коричневой пигментации. Шипики по всему телу, за исключением самой задней части. Пищевод длинный, разветвляется на уровне середины расстояния между глоткой и передним краем БП. Имеется 14 сенсорных папилл по краям тела, 12 вокруг РП, 9 вокруг БП |
5 | Apophallus muehlingi | Дельта Волги, Северный Каспий; широко распространен в Евразии, от западного побережья Атлантики до Приморья и Камчатки | Карповые: плотва (вобла), язь, красноперка, уклея, густера, лещ, белоглазка, синец, чехонь, серебряный карась, сазан, щиповка, голавль; окуневые: судак, берш, окунь, ерш | В лучах плавников и хвоста, на жабрах, в мышцах туловища, обычно вблизи костей | 0,20 - 0,29 x 0,14 - 0,26, эллипсовидной или шаровидной формы. Вокруг цист откладывается черный пигмент, что делает цисту хорошо заметной. При локализации в мышцах пигмент откладывается не всегда | Y-образной формы, задний конец S-образно изогнут | 0,50 - 0,58 x 0,10 - 0,12. Пищевод доходит до половины длины тела. Кутикула покрыта мелкими шипиками-чешуйками. Зачатки семенников лежат один за другим, наискось по сторонам выделительного пузыря | |
6 | Rossicotrema (Apophallus) donicum | Реки, впадающие в Черное море, лиманы Азовского моря, низовье Волги, р. Тиса | Окуневые: окунь, судак, ерш, берш; атериновые, реже карповые: плотва (вобла), густера, лещ, красноперка, белоглазка | Внутри и между лучами плавников, реже в мышцах | 0,26 - 0,34 x 0,20 - 0,23, эллипсовидной формы. Оболочка двуслойная, окружена кольцом черного пигмента | Y-образной формы | 0,49 - 0,53 x 0,13 - 0,15. РП - 0,035 - 0,045. БП меньше РП. Пищевод 0,05 - 0,10 (не более 1/4 длины тела). Зачатки семенников округлые, диаметром 0,04, почти на одном уровне, чуть наискось по бокам выделительного пузыря | |
7 | Metagonimus yokogawai, Metagonimus katsuradai, Metagonimus suifunensis sp. n. | Пресные водоемы стран Дальнего Востока (Японии, Китая, Кореи, Российской Федерации); бассейны рек Средиземного, Черного и Каспийского моря; реки Карпат и Прикарпатья, пруды Дагестана, Азербайджана | Свыше 60 видов рыб 9 семейств: карповые: плотва, серебряный карась, сазан, верхогляд, пескарь, толстолобик, белый амур, черный амур, конь-губарь, пестрый конь, подуст-чернобрюшка; лососевые: острорылый ленок, тупорылый ленок; сиговые: сиг; хариусовые: хариус; плекоглоссовые (аювые): аю; лавраковые, щуковые, сомовые, окуневые | В чешуе, реже на плавниках, жабрах, в подкожной соединительной ткани, мышцах | 0,15 - 0,23. Сферической, овоидной или чечевицеобразной или овальной формы. Оболочка двухслойная | Y-образной формы, черный, гранулы темно-бурые мелкие | Движения активные | 0,32 - 0,40 x 0,09 - 0,1. РП - 0,05, БП - 0,04. Личинка листовидной или языковидной формы. На поверхности передней части тела ясно видны чешуеобразные образования - шипы. Пищевод длинный, 0,18 мм. Половой синус сдвинут в сторону от срединной линии тела |
8 | Cryptocotyle lingua | Бассейны Черного и Азовского морей, Северного Каспия | Бычки: бычок-кругляк, бычок-песочник бычок-ширман, ротан | Мышцы | 0,6 - 0,9 x 0,5 - 0,7, шаровидной или эллипсовидной формы. Оболочка двухслойная. Окружена кольцом черного пигмента | T-образный, его непарный ствол изгибается между семенниками | 0,45 - 0,48. РП - 0,03 x 0,04, субтерминальна. БП слабо выражена, в задней трети тела. Личинка языковидной формы. Кутикула покрыта мелкими шипиками. Половая присоска крупнее РП и БП позади последней в виде 1 сосочка | |
9 | Cryptocotyle sp. | Дальневосточные моря Тихого океана, о. Сахалин, оз. Долгое | Тихоокеанские лососи (горбуша, кета, нерка, кижуч, чавыча) | Подкожная соединительная ткань | 0,3 - 0,4 овальная. Окружена кольцом черного пигмента | V-обрачной формы | БП немного крупнее РП, расположена позади нее. Личинка языковидной формы | |
10 | Heterophyes heterophyes | Моря, омывающие Палестину, Египет, Тунис, Израиль, страны южной Европы, Японию, Индию. Речные эстуарии и пресные водоемы (в т.ч. прудовые хозяйства) Палестины, Египта, Туниса, Израиля, стран южной Европы, Японии, Индии | Кефалевые, ставридовые, цихлидовые, лавраковые | Мускулатура тела | 0,13 - 0,26, беловатой окраски, округлые или слегка овальные. Толстая наружная оболочка (0,004 - 0,012) и тонкая внутренняя мембрана | Сердцевидный, занимает 1/8 часть длины тела | Метацеркария в цисте согнута так, что ее передняя часть налегает на заднюю с брюшной стороны | 0,21 x 0,40. РП - 0,03 - 0,05, БП - 0,03 - 0,04. 3/4 тела густо покрыто чешуеобразными шипиками, передний конец сплющен дорсовентрально, задний округлый. Ветви кишечника тянутся до заднего конца тела, сразу за бифуркацией они шире, чем в задней части |
11 | Nanophyetus salmincola schikhobalowi | Реки, впадающие в северную часть Тихого океана: в Российской Федерации - бассейн среднего и нижнего Амура, побережье Татарского пролива, водоемы севера Сахалина, Командорских островов; США, Канада | Лососевые: таймень, острорылый ленок, тупорылый ленок, горбуша, кета, сима, мальма; сиговые: амурский сиг, сиг-хадары, кунджа; хариусовые: нижнеамурский хариус, амурский хариус; редко: амурские язь, гольян Лаговского, щука, широколобка | Почки, мышцы плавников и тела, жабры, печень, стенки кишечника | 0,156 - 0,179 x 0,145 - 0,156, округлые или овальные с тонкостенной оболочкой | Крупный 0,07 - 0,10 x 0,23 - 0,24, темный, наполнен непрозрачными гранулами | 0,35 - 0,65 x 0,18 - 0,34. РП - 0,07 - 0,12, БП - 0,07 - 0,11, расположена посередине длины метацеркария. Вся кутикула покрыта тонкими, отогнутыми назад шипиками. Зачатки 2 семенников в задней половине тела. Ветви кишечника достигают зачатков семенников | |
12 | Echinochasmus perfoliatus | Пресные водоемы Европы (Венгрии, Румынии, Италии, Германии, Украины, Российской Федерации); юго-восточной Азии (Японии, Китая, Тайваня) | Карповые: белоглазка, линь, сазан, язь, синец, плотва, карась, лещ, уклейка, жерех и др.; щука, окунь, судак, ерш, берш | Жабры (на основании жаберных лепестков) | 0,05 - 0,11 x 0,04 - 0,098, круглой формы. Оболочка очень тонкая, двухслойная, бесцветная, 0,002 - 0,003 | Латеральные коллекторные сосуды, впадающие в экскреторный пузырь, расширяются в средней части в так называемые сифоны, содержащие известковые тельца | Движения слабые | 0,0116 - 0,043. РП = БП = 0,0258 - 0,03. Тело личинки широкоокруглое. РП окружена адоральным диском, ширина его менее ширины тела. Крупные светопреломляющие шипы на нем расположены дорсально, прерванным рядом из 24 шипов |
Примечание: | ||||||||
к МУК 3.2.3804-22
PARAGONIMIDAE, ОПАСНЫХ ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА
N п/п | Вид гельминта | Географическое распространение | Виды пресноводных ракообразных - вторых дополнительных хозяев | Размер и форма цисты (мм) | Строение и размеры освобожденной от цисты личинки (в мм) |
1 | 2 | 3 | 4 | 5 | 6 |
1 | Paragonimus westermani westermani | Индия, Шри-Ланка, Таиланд, Малайзия, Индонезия, Китайская Народная Республика, Япония, Российская Федерация (южные и центральные районы Хабаровского края, Южное Приморье) | Крабы рода Parathelphysa, Candidopotamon, Potamon и др., раки рода Cambaroides | 0,259 - 0,300 сферическая, оболочка трехслойная | 0,8 - 1,1 x 0,27 - 0,38, РП <*> - 0,065 - 0,08 x 0,09 - 0,1, БП <**> - 0,115 - 0,14 x 0,0117 - 0,147 расположена преэкваториально. Поверхность тела густо покрыта шипиками. Кишечные стволы делают три изгиба и тянутся до конца тела |
2 | Paragonimus westermani ichunensis | Китайская Народная Республика, Российская Федерация (южные и центральные районы Хабаровского края, Южное Приморье) | Раки рода Cambaroides schrencki, Cambaroides dauricus | 0,259 - 0,347 сферическая, оболочка трехслойная | 0,4 - 0,86 x 0,22 - 0,15, РП - 0,08 - 0,09, стилет - до 0,017, БП - 0,10 - 0,11. Эксцистированная метацеркария очень подвижна. Вся поверхность густо покрыта одиночными шипами |
3 | Paragonimus pulmonalis | Япония, Тайвань, КНР, Корея, возможно Российская Федерация (Южное Приморье) | Крабы рода Eriocher japonicus, раки Cambaroides similis | 0,389 - 0,450 сферическая, оболочка трехслойная | РП несколько крупнее БП. Тело покрыто редкими шипиками. Кишечные стволы извиваются слабо |
4 | Paragonimus skrjabini | Китайская Народная Республика | Крабы рода Potamon denticulatus, P. yaanensis | 0,427 - 0,436 сферическая, оболочка трехслойная 0,010 - 0,014 | 0,453 - 1,138 x 0,188 - 0,533. Кишечные стволы извилистые |
Примечание: | |||||
к МУК 3.2.3804-22
DIOCTOPHYMIDAE, GNATHOSTOMATIDAE, ANISAKIDAE, ОПАСНЫХ
ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА
N п/п | Вид гельминта | Географическое распространение | Виды животных, наиболее часто играющие роль промежуточных или резервуарных хозяев | Локализация в теле промежуточного или резервуарного хозяина | Строение и размер личинок | Характеристика головного вооружения и нервной системы личинок | Особенности строения пищеварительной и выделительной систем |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
1 | Dioctophyme renale | Бассейны рек Амударьи, Вахш, Аральское и Каспийское моря | Рыбы: аральские лопатоносы, щука, жерех, язь, чехонь, плотва, аральский усач, шемая, быстрянки, сом, сомик карликовый, гамбузия, окунь | У рыб: стенка кишечника и желудка, различные органы и ткани | Тело нитевидное, с суживающимся головным концом и оканчивающимся тупо задним, желтоватое или бледно-розовое. Длина 6,9 - 8,0, ширина 0,11 - 0,20 мм. У личинок обоих полов хвост симметричный. В соединительно-тканных капсулах | На головном конце 12 чувствительных сосочков, расположенных в 2 круга по 6 в каждом (наружные крупнее таковых внутреннего круга). Нервное кольцо сдвинуто к головному концу и удалено от него на 0,05 мм | Ротовое отверстие ведет в узкую ротовую капсулу, переходящую в толстостенный пищевод, длина которого 2,02 - 2,41, ширина 0,18 - 0,19 мм. При переходе пищевода в кишку расположен трехстворчатый клапан. Средняя кишка состоит из одного ряда клеток |
Повсеместно | Земноводные: лягушка озерная | У лягушек: в стенке желудка, в мышцах живота, спины и конечностей | |||||
2 | Eustrongylides excisus | Бассейны Каспийского моря, Дуная, Днестра, Оби | Осетровые (осетр, белуга); сельдь-черноспинка, щука; карповые (жерех, лещ, вобла, красноперка); сом, окунь | Полость тела, мускулатура стенки брюшной полости, реже стенки кишечника, печень, семенники | Тело суживается к обоим концам. Длина тела 8 - 50, ширина 0,11 - 0,19 мм. Головной конец в виде пирамиды, хвостовой асимметричный (у личинок самцов) и симметричный, закругленный (у личинок самок). В капсулах или свободно | На головном конце также 2 круга папилл по 6 в каждом. Сосочки наружного круга короткие, с широким основанием, в виде холмиков с тупыми вершинами. Нервное кольцо в 0,09 - 0,11 мм от головного конца | Длина ротовой полости 0,09, пищевода 2,46 - 4,53, задней кишки 0,13 - 0,56 мм. Пищеводный клапан развит слабо |
3 | Echinochephalus sinensis | Морские тропические и субтропические воды (Гонконг, Южный Китай, Цейлон, западная Австралия) | Двустворчатые моллюски: обыкновенная и гигантская устрицы, пинктада, амусиум | У моллюсков: в просвете гонадукта с поражением ресничного эпителия | Личинки II стадии: самцы - 6,4 +/- 0,8 мм; самки - 7,1 +/- 1,2 мм; III стадии: самцы - 11,6 +/- 1,1 мм; самки - 11,2 +/- 0,8 мм. В соединительно-тканных капсулах | У личинок II стадии конический головной конец с 6 рядами головных шипов, III стадии - бульбусовидный с 7 рядами шипов (первый из 6 маленьких). Нервное кольцо приближено к головному концу | Пищевод из мышечного и железистого отделов. В месте перехода одной части в другую вентрально открывается экскреторная пора |
Пресмыкающиеся: логгерхед (головастая морская черепаха - каретта) | У черепах: в желудке и кишечнике | ||||||
4 | Gnathostoma hispidum | Аральское море; реки Амударья и Вахш; низовья и дельта Волги | Рыбы: карповые; сом, гамбузия, окунь, судак. Земноводные: лягушки. Пресмыкающиеся: пресноводные черепахи, змеи | Мускулатура, реже полость тела и внутренние органы | Личинка III ст., свернута в спираль диаметром 1 мм, в капсуле. Длина тела 1,3 - 2,3, ширина 0,40 мм. Кутикула прозрачная, четко исчерчена, вооружена многочисленными рядами мелких шипиков на всем теле или его передней половине | Округлое головное вздутие вооружено 4 рядами шипов по 30 - 40 в каждом. На его переднем конце трехлопастные губы, каждая с тремя сосочками. Нервное кольцо на границе перехода пищевода в кишечник | Деление пищевода на мышечную и железистую часть выражено слабо. Вдоль пищевода примерно до его середины располагаются 4 пищеводные железы. Экскреторная пора удалена на 0,15 - 0,20 мм от переднего конца тела |
р. Красная (Северный Вьетнам) | Рыбы: змееголовые | ||||||
5 | Gnathostoma spinigerum | Пресные водоемы Дальнего Востока (Япония, Таиланд, Китай, в Российской Федерации - бассейн Амура) | Лососевые; угорь, желтощек, сазан, вьюн, амурский сом, китайский окунь; змееголовые | Мускулатура, реже полость тела и внутренние органы | Личинка III стадии свернута в спираль в капсуле диаметром 1 мм. Тело личинки покрыто поперечными рядами (более 200) простых заостренных шипиков длиной 0,01 мм | Головное вздутие вооружено 4 рядами шипов, число которых в ряду увеличивается по направлению назад (обычно > 40). Нервное кольцо на границе перехода пищевода в кишечник | Пищевод подразделен на два отдела. 4 одноядерные пищеводные железы выражены отчетливо. Экскреторная пора приближена к головному концу |
6 | Anisakis simplex | Все зоогеографические области Мирового океана, пресные водоемы Камчатки, Сахалина, Японии | Морские промысловые рыбы: треска, палтус, камбала, мойва, навага, пикша, сайда, зубатка, морские окуни, хек, сельдь и др. Проходные рыбы: семга, кумжа, кета, горбуша, голец и др. Пресноводные рыбы, связанные с морской акваторией. Головоногие моллюски: осьминоги, кальмары, каракатицы | У рыб - в полости тела, на серозе внутренних органов, под перитонеальной оболочкой, в мышцах (преимущественно брюшной стенки, а у тихоокеанских лососей - скелетных) в капсулах или свободно; у головоногих - в мантии и на внутренних органах | Личинки III стадии светло-кремового или беловатого цвета свернуты в плоскую спираль внутри прозрачной капсулы, реже лежат свободно без капсулы. Длина 7 - 33 мм. Ширина тела у крупных форм составляет 0,5 - 0,7 мм. Сквозь покровы тела хорошо виден желудочек | На головном конце три выраженных губы и хорошо развитый сверлильный зуб, расположенный вентрально от ротового отверстия между латеровентральными губами. Нервное кольцо сдвинуто к переднему концу | Желудочек удлиненной формы. Задняя его часть, примыкающая к кишечнику, скошена так, что вентральная сторона оказывается длиннее, чем дорсальная. Желудочный и кишечный отростки отсутствуют. Экскреторная пора открывается на голове между латеровентральными губами снизу, т.е. снаружи от границы сверлильного зуба вентрально |
7 | Anisakis schupakovi | Каспийское море, дельта Волги | Осетр, шип, стерлядь, белуга, севрюга, пузанок, сельдь-черноспинка, каспийский лосось, щука, вобла, кутум, линь, красноперка, шемая, рыбец, чехонь, сазан, жерех, усач, лещ, белоглазка, густера, синец, уклея, сом, окунь, судак, морской судак, берш | Серозные покровы органов брюшной полости, у долгинской сельди встречается и в мышцах | Личинки III стадии желтого цвета, длиной 6,69 - 15,8, шириной 0,12 - 0,40 мм. Кутикула с поперечной и продольной исчерченностью | На переднем конце хорошо заметны личиночный зуб и 4 сосочка, 2 из которых расположены дорсолатерально и 2 субвентрально. Нервное кольцо удалено от переднего конца тела на 0,16 - 0,29 мм | Пищевод мышечный длиной 0,74 - 1,42 мм, максимальная ширина 0,05 - 0,09 мм. Желудочек вытянутый, 0,20 - 0,46 x 0,06 - 0,18 мм. Отношение длины тела к длине пищевода 8,2 - 11,8:1, длины тела к длине желудочка 23,7 - 27,6:1. Экскреторная пора открывается на головном конце |
8 | Pseudoterrunova decipiens | Все зоогеографические области Мирового океана, пресные водоемы Камчатки, Сахалина, Японии | Морские промысловые рыбы: сельдь, корюшка, треска, палтус, камбала, мойва, навага, пикша, сайда, зубатка, морские окуни, хек и др. Проходные рыбы: тихоокеанские лососи, голец и др. Моллюски: кальмары | У рыб: в мускулатуре свободно, без капсул; в полости тела свободно или покрытые капсулами, прикрепленными к серозным покровам внутренних органов; у кальмаров: в мантии и во внутренних органах | Личинки III стадии 14,0 - 33,0 мм длиной, окрашены в коричневые или красноватые цвета | Головной конец несет 3 достаточно хорошо выраженные губы и небольшой сверлильный зуб, расположенный между латеровентральными губами. Нервное кольцо удалено от переднего конца тела на 0,25 - 0,31 мм | Удлиненный пищевод переходит в округлый, овальный или четырехугольный желудочек. Желудочный отросток отсутствует. Дистальный конец кишечного отростка прикрепляется к стенке тела пучком мышц. Экскреторное отверстие на головном конце между латеровентральными губами внизу |
9 | Contracaecum osculatum | Арктические воды, Атлантика (Балтийское море); озеро Байкал с предустьевыми участками рек; водоемы Камчатки и Сахалина | Рыбы; сельдь, ленок, тихоокеанские лососи, семга, омуль, обыкновенный и байкальский хариусы, корюшка, треска, налим, мерланг, мольва, длиннокрылый и желтокрылый бычки, морской окунь, керчак, рогатка; песчаная, ушканская, жирная и плоская широколобки; голомянка, палтусовидная и морская камбалы, лиманда, черный палтус. Моллюски: кальмары | На серозе внутренних органов (печень, пилорические придатки, мезентерий) | Личинки с плотной кутикулой, 13 - 28 мм длиной и 0,41 - 0,52 мм шириной. Могут быть в капсулах и без них | Зачатки губ на головном конце отчетливые. Личиночный зуб расположен между зачатками латеровентральных губ, еще не разделенных перетяжкой. Нервное кольцо в 0,37 - 0,42 мм от переднего конца тела | Пищевод цилиндрический, с маленьким желудочком. Имеются кишечный и желудочный отростки, направленные в противоположные стороны. Кишечный вырост обычно длиннее половины пищевода. Экскреторная пора открывается на вентральной стороне головного конца у основания субвентральных губ |
10 | Sulcascaris sulcata | Теплые и умеренные воды Мирового океана, включая Красное, Средиземное и Карибское моря; Южную, Среднюю и Западную Атлантику; Австралия, Цейлон | Съедобные двустворчатые моллюски; устрицы, спондилюс, пинктада, пинна, спизулла, мактра; морские гребешки (пектен, аргопектен, хламис, амусиум). Морские черепахи; хелония (зеленая или суповая черепаха), логгерхед (головастая морская черепаха - каретта) | В спизулах - во всех тканях: во внутренних органах - в 60%, в ноге - в 27%, в аддукторе - в 12%, в мантии - в 1%; в гребешках - в мышце-аддукторе гонадах; у черепах - в желудке и кишечнике, прикрепленные к стенке | В моллюсках - личинки IV стадии (8,3 - 45 мм длиной), редко III стадии (4,2 - 4,3 мм); в черепахах - IV стадии (19 - 33 мм) и взрослые. Личинки могут быть в соединительно-тканных капсулах. Мелкие личинки - белые и малозаметные, более крупные от желтого до светло-оранжевого или коричневого цвета. В случае поражения их гаплоспоридиями (гиперпаразитизм) они становятся темно-коричневыми, почти черными | Головной конец личинки IV стадии несет три оформленных губы, края которых характеризуются редкой зазубренностью. Между главными губами помещаются интерлабии. Нервное кольцо отстоит от переднего конца тела личинки на расстоянии 0,25 - 0,67 мм | Пищевод 1,3 - 4,0 мм длиной при ширине 0,08 - 0,23 мм. Желудочек удлиненной формы. Имеется короткий кишечный вырост. Экскреторная пора открывается на головном конце при основании вентральной интерлабии |
к МУК 3.2.3804-22
(АКАНТОЦЕФАЛЫ, КОЛЮЧЕГОЛОВЫЕ)
N п/п | Вид гельминта | Географическое распространение | Второй промежуточный хозяин | Локализация в теле промежуточного хозяина | Строение и размер личинок | Характеристика хоботка личинок |
1 | 2 | 3 | 4 | 5 | 6 | 7 |
1 | Семейство Polymorphidae (род Corynosoma) | Разные районы Мирового океана, во всех морях, омывающих Российскую Федерацию, а также в Каспийском море, Ладожском озере и реках, впадающих в них | Различные морские, проходные, а также пресноводные рыбы, обитающие в нижнем течении рек и в некоторых континентальных водоемах (лососевые, корюшковые, сельдевые, тресковые, мерлузовые, нототениевые, белокровные, терпуговые, камбаловые) и миноги. Обычны акантеллы р. Corynosoma для осетровых Каспийского моря. Наиболее часто заражены придонные рыбы | Полость тела, другие органы (брыжейка, гонады, печень, почки, серозные покровы желудка и кишечника), мышцы | Размер капсул с личинками 2 - 4 мм. Тело личинки грушевидной формы, расширенное к передней части, длиной до 10 мм. Поверхность передней части личинки покрыта шипами: более крупными, расположенными в шахматном порядке, - в первой трети тела и более мелкими, расположенными хаотично, - в остальной части | Хоботок почти цилиндрический, слегка расширяющийся в середине |
У Corynosoma strumosum тело 3,5 - 9 мм длиной, шириной до 1,5 мм | У Corynosoma strumosum на хоботке 18 продольных рядов крючьев по 10 - 12 в каждом ряду. | |||||
Тело Corynosoma semerse длиной до 5 мм | У Corynosoma semerse на хоботке 22 - 24 продольных ряда крючьев | |||||
2 | Семейство Polymorphidae (род Bolbosoma) | Скумбриевые рыбы в Северной Атлантике; мерлузовые, волосохвостые в Южной Атлантике; лососевые, скорпеновые, бериксовые, гемпиловые, скумбриевые в Тихом океане | Скумбриевые рыбы в Северной Атлантике; мерлузовые, волосохвостые в Южной Атлантике; лососевые, скорпеновые, бериксовые, гемпиловые, скумбриевые в Тихом океане | Полость тела, на внутренних органах | У Bolbosoma caenoforme тело личинки обычно цилиндрическое, но в передней части образует бульбусовидное расширение, передняя часть которого вооружена шипами. Акантеллы размером 7 - 12 x 0,9 - 1,2 мм. Живые личинки розовато-красноватого цвета | На цилиндрическом хоботке 18 продольных рядов крючьев, по 6 в каждом ряду |
к МУК 3.2.3804-22
ПРИЗНАКИ ДЛЯ ОПРЕДЕЛЕНИЯ МЕТАЦЕРКАРИЙ ТРЕМАТОД <8>
--------------------------------
<8> Определитель паразитов пресноводных рыб фауны СССР. - Т. 3. Паразитические многоклеточные. - Ленинград: Наука. 1987. - 583 с.
1. Принадлежность метацеркарий трематод к семействам определяется по следующим морфологическим признакам:
1(2) <9> Метацеркарии локализуются в различных тканях ракообразных. Семейство Paragonimidae (п. 6 приложения 7 настоящих МУК).
--------------------------------
<9> Если признак не соответствует указанному в определителе признаку - тезе, то следует перейти к антитезе, обозначенной цифрой в скобках.
2(1) Метацеркарии локализуются в различных тканях рыб.
3(4) Передний конец тела вооружен шипами. Семейство Echinostomatidae (п. 5 приложения 7 настоящих МУК).
4(3) Передний конец тела не несет шипов.
5(8) Ветви кишечника длинные, до конца тела.
6(7) Ветви кишечника прямые. Шипиков вокруг ротового отверстия нет. Брюшная присоска, как правило, крупнее ротовой. Предглотки нет. Выделительный пузырь большой, темный. Семейство Opisthorchidae (п. 2 приложения 7 настоящих МУК).
7(6) Концы ветвей кишечника более или менее загибаются внутрь, к срединной линии тела. Предглотка имеется. Семейство Heterophyidae (п. 3 приложения 7 настоящих МУК).
8(5) Ветви кишечника короткие, не переходят за уровень заднего края зачатков семенников. Семейство Nanophyetidae (п. 4 приложения 7 настоящих МУК).
2. К семейству Opisthorchidae относятся трематоды с удлиненным, сплющенным и всегда заметно суженным кпереди телом. Присоски сравнительно слабо развиты и сближены. Ветви кишечника длинные, пищевод разной длины. Во взрослом состоянии - паразиты желчных протоков печени, желчного пузыря и поджелудочной железы млекопитающих, птиц, рептилий. Метацеркарии семейства Opisthorchidae определяются по следующим морфологическим признакам:
1(2) Циста с толстой оболочкой, сферическая. Metorchis xanthosomus (рисунок 11 к приложению 9 настоящих МУК) <10>.
--------------------------------
2(1) Циста тонкостенная, сферическая или овальная.
3(6) Пищевод длинный, развилок кишечника удален от ротовой присоски.
4(5) Шипики по всему телу. Желто-коричневая пигментация тела. Ротовая присоска меньше брюшной. Opisthorchis (Clonorshis) sinensis (рисунок 8 к приложению 9 настоящих МУК).
5(4) Шипики до заднего края брюшной присоски <11>. Тело не пигментировано. Ротовая присоска несколько меньше по величине брюшной присоски. Opisthorchis felineus (рисунок 7 к приложению 9 настоящих МУК).
--------------------------------
6(3) Пищевод короткий, развилок кишечника приближен к ротовой присоске.
7(8) Тело покрыто шипиками, немного не доходящими до заднего конца тела. Брюшная присоска крупнее ротовой. Pseudamphistomum truncatum (рисунок 10 к приложению 9 настоящих МУК).
8(7) Шипики до уровня заднего края брюшной присоски. Ротовая присоска несколько больше по величине брюшной присоски. Metorchis bilis (рисунок 9 к приложению 9 настоящих МУК).
3. К семейству Heterophyidae относятся мелкие трематоды с телом, покрытым чешуеобразными шипиками, число которых уменьшается к заднему концу. Присоски слабо развиты. У видов, имеющих медицинское значение, ротовая присоска без шипов. Зачатки семенников в заднем конце тела, обычно на одном горизонтальном уровне или слегка наискось. На брюшной стороне имеется более или менее сильно развитая впадина - генитальный синус, в котором бывает скрыта редуцированная брюшная присоска. Имеется половая присоска, которая часто объединяется с брюшной в общий комплекс. Метацеркарии семейства Heterophyidae определяются по следующим морфологическим признакам:
1(2) Экскреторный пузырь сердцевидный. Heterophyes heterophyes (рисунок 13 к приложению 9 настоящих МУК).
2(1) Экскреторный пузырь иной формы (V-образной, Y-образной или мешковидной формы).
3(4) Половой синус сдвинут в сторону. Род Metagonimus (рисунок 12 к приложению 9 настоящих МУК).
4(3) Половой синус расположен медианно.
5(8) Половая присоска представлена двумя более или менее выраженными сосочками впереди брюшной присоски.
6(7) Предглотка длинная, пищевод достигает половины длины тела. Преимущественно у карповых рыб. Apophalus muehlingi (рисунок 16 к приложению 9 настоящих МУК).
7(6) Предглотка короткая, пищевод не более 1/4 тела. Преимущественно у окуневых рыб. Rossicotrema donicum (рисунок 15 к приложению 9 настоящих МУК).
8(5) Половая присоска представлена одним сосочком, расположенным позади брюшной присоски. Род Cryptocotyle (рисунок 14 к приложению 9 настоящих МУК).
4. К семейству Nanophyetidae относятся маленькие грушевидные или удлиненные трематоды. Ротовая присоска субтерминальна, хорошо развита. Глотка имеется. Пищевод очень короткий, кишечник различной длины (ветви не переходят за уровень заднего края зачатков семенников). Брюшная присоска в средней трети тела. Зачатки семенников симметрично находятся в задней части тела. Выделительный пузырь мешковидный. Паразиты кишечника человека, рыбоядных млекопитающих и птиц (Nanophyetus salmincola schikhobalowi) (рисунок 17 к приложению 9 настоящих МУК).
5. У трематод семейства Echinostomatidae передний конец тела образует особый воротничок (адоральный диск), окружающий ротовую присоску и несущий по краю одинарный или двойной ряд крупных шипов, число и расположение которых определенно для отдельных родов и видов. Определение связано с трудностями, так как на первых этапах развития (10 - 12 дней) личинки не имеют адорального диска. Половозрелые черви рода Echinochasmus - паразиты кишечника рыбоядных птиц. Описаны случаи заражения человека Echinochasmus perfoliatus (рисунок 18 к приложению 9 настоящих МУК).
6. Тело эксцистированной метацеркарии семейства Paragonimidae удлиненно-овальной формы. В живом виде метацеркария способна сильно вытягиваться и сокращаться. Тегумент обладает густыми рядами шипиков, величина которых уменьшается к заднему концу. Присоски развиты слабо, одинакового размера, в ротовой почти всегда имеется стилет. Пищевод короткий, ветви кишечника достигают конца тела, все пространство между ними заполняет большой мешковидный черный (в проходящем свете) экскреторный пузырь. Впереди брюшной присоски располагаются разделенные на две группы 14 крупных железистых клеток (рисунок 19 - 20 к приложению 9 настоящих МУК). Дифференциальные признаки метацеркарий трематод семейства Paragonimidae, опасных для здоровья человека приведены в приложении 4 к настоящим МУК. Потенциальное медицинское значение имеют все виды парагонимид: одни вызывают типичный легочный парагонимоз, другие дают больший процент атипичных локализаций, а третьи не развиваются в человеке до стадии мариты, а используют его как резервуарного хозяина.
к МУК 3.2.3804-22
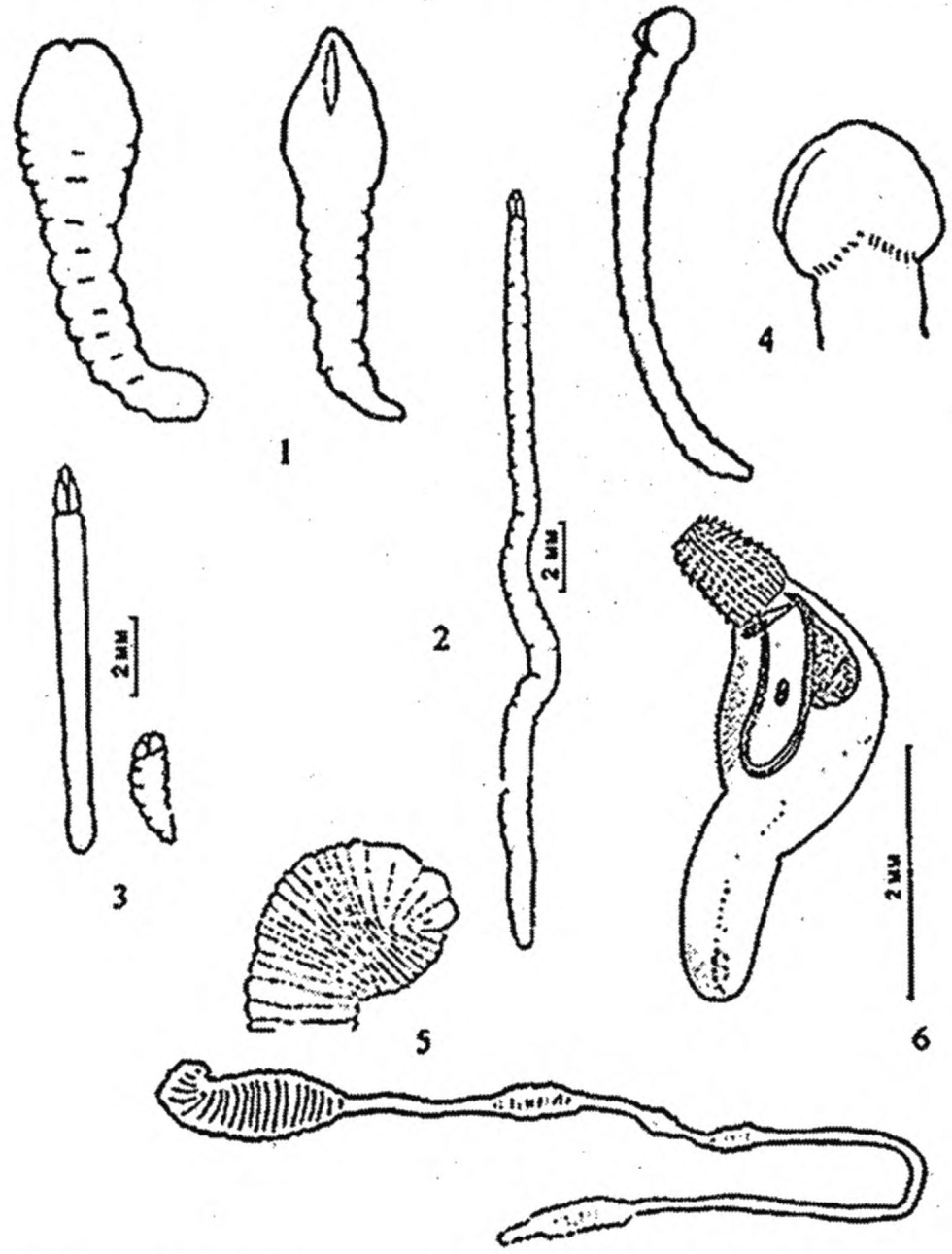
Рисунок 1 - 6. Плероцеркоиды семейства Diphyllobothriidae:
1 - Dibothriocephalus latus (Diphyllobothrium. latum)
с инвагинированным и эвагинированными сколексами);
2 - Dibothriocephalus dendriticus (Diphyllobothrium
dendriticum); 3 - Dibothriocephalus ditremus
(Diphyllobothrium ditremum) (в расслабленном и сокращенном
состоянии); 4 - Pyramicocephalus phocarum (общий вид
и головной конец) (из: Делямуре, Скрябин, Сердюков, 1985);
5 - Spirometra erinaceieuropaei (головной конец и общий
вид); 6 - Corynosoma strumosum (из: Гаевская,
Ковалева, 1991)
к МУК 3.2.3804-22
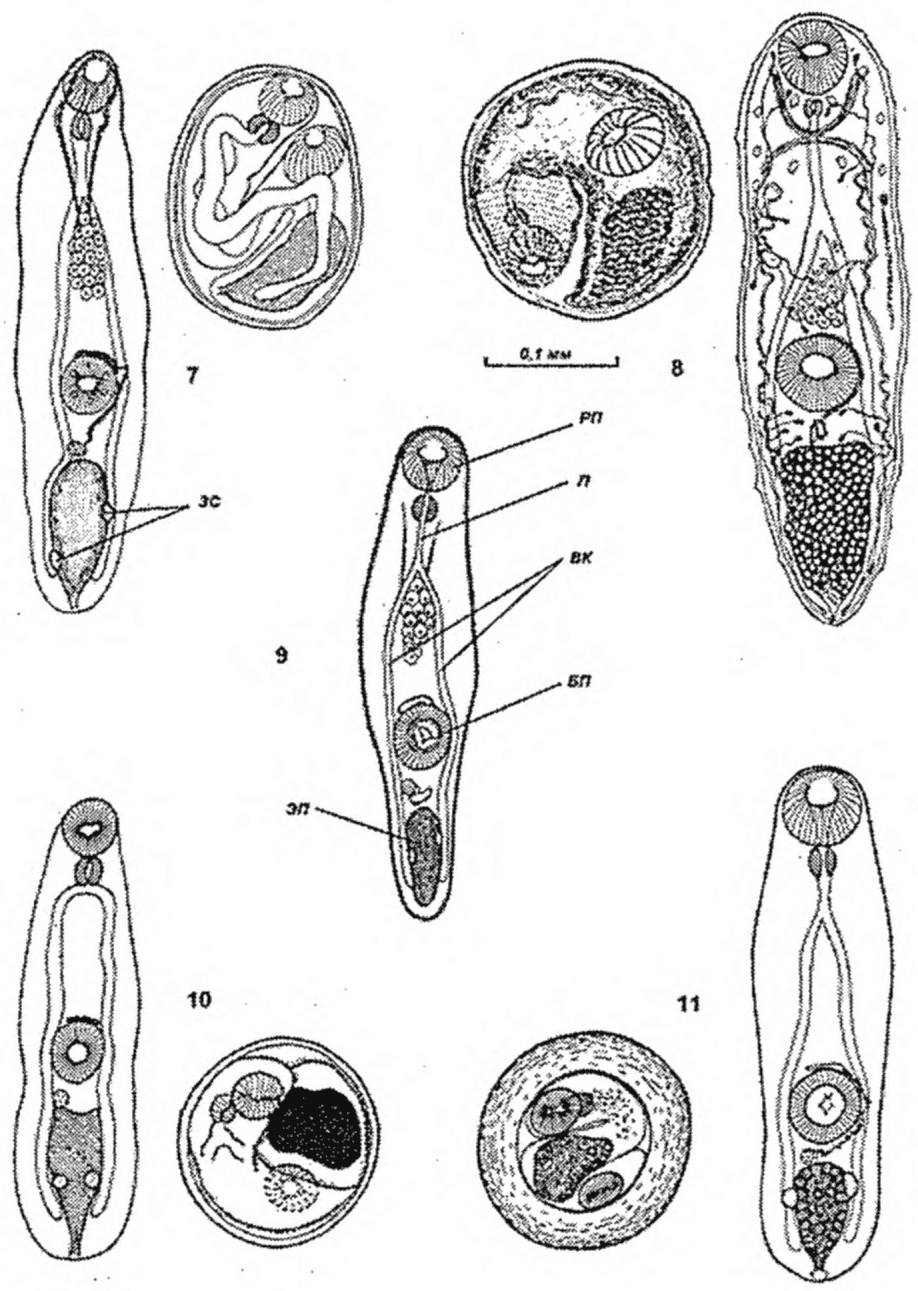
7 - Opisthorchis felineus, личинка вне цисты и в цисте;
8 - Opisthorchis (Clonorshis) sinensis, личинка вне цисты
и в цисте; 9 - Metorchis bilis (M. albidus);
10 - Pseudamphistomum truncatum, личинка вне цисты
и в цисте; 11 - Metorchis xanthosomus, личинка вне цисты
и в цисте (из: Судариков и др., 2002); РП - ротовая
присоска; П - пищевод; ВК - ветви кишечника; БП - брюшная
присоска; ЭП - экскреторный пузырь; ЗС - зачатки семенников
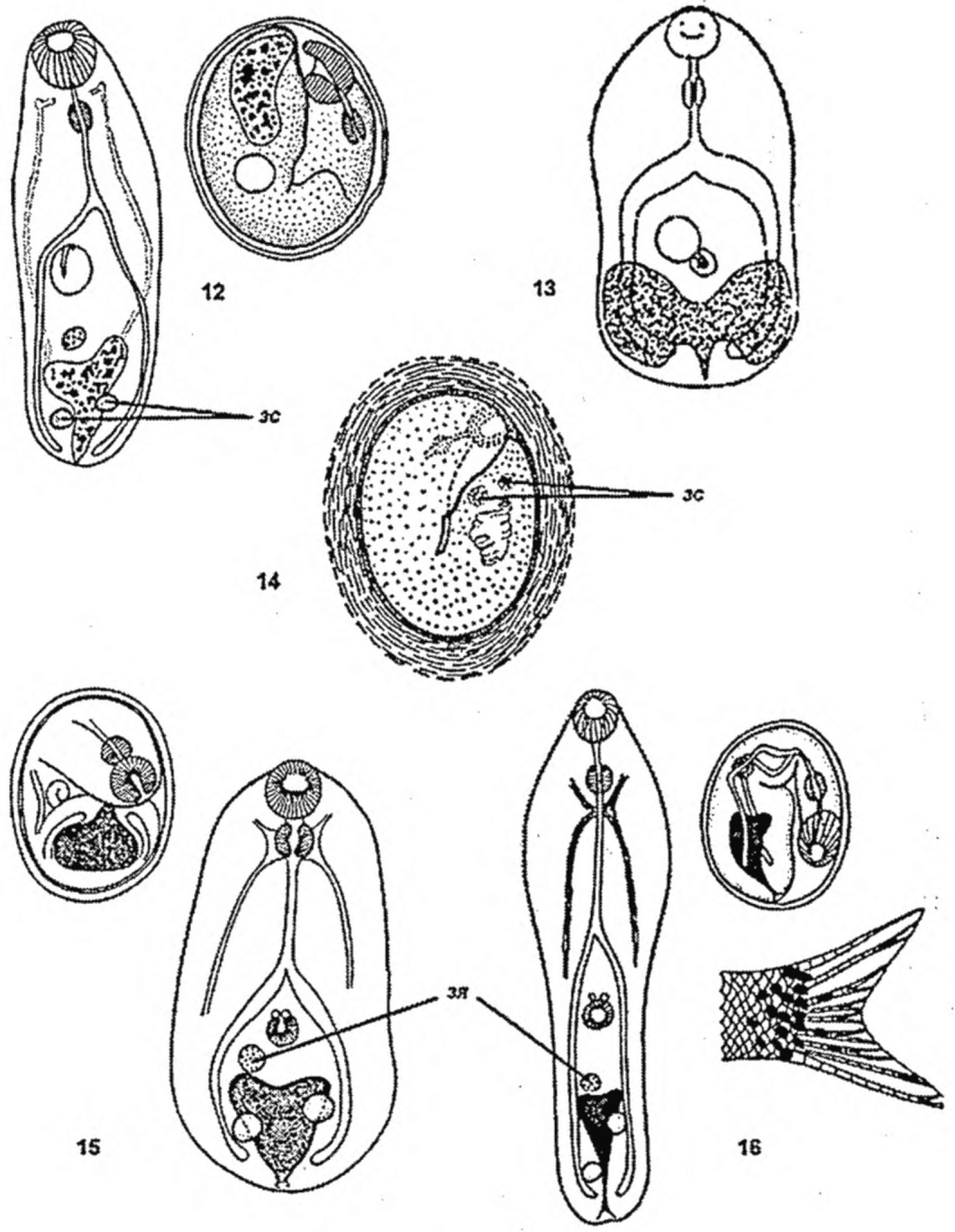
12 - Metagonimus yokogawai, личинка вне цисты и в цисте;
13 - Heterophyes heterophyes; 14 - Cryptocotyle lingua
(из: Определитель паразитов пресноводных рыб, Т. 3, 1987);
15 - Rossicotrema donicum (из: Судариков и др., 2002);
16 - Apophallus muehlingi, личинка вне цисты, в цисте
и хвостовой плавник рыбы с цистами (из: Дубинин, 1952);
ЗС - зачатки семенников, ЗЯ - зачаток яичника
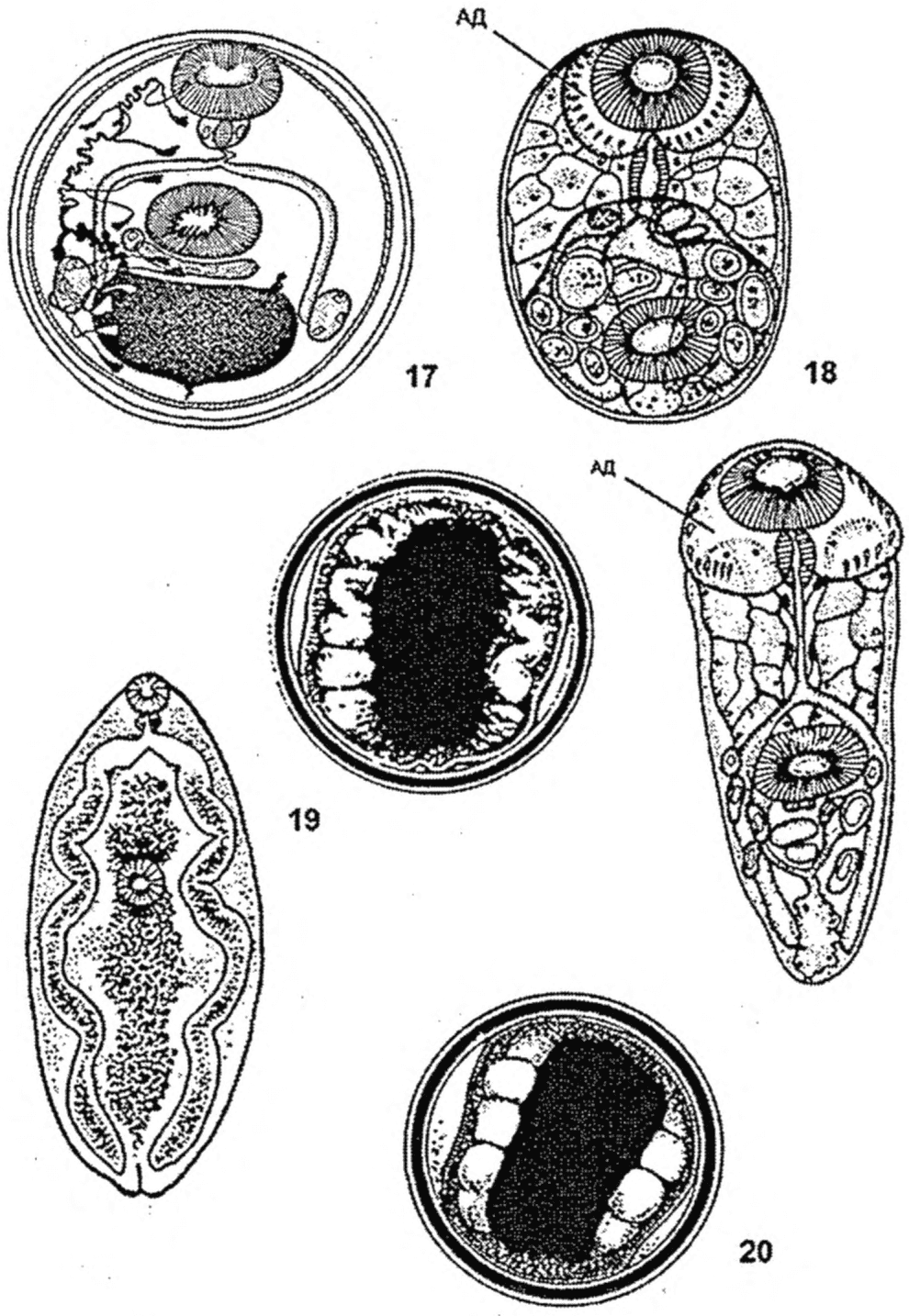
Echinostomatidae, Paragonimidae: 17 - Nanophyetus salmincola
schikhobalowi (из: Филимонова, 1963); 18 - Echinochasmus
perfoliatus (личинка в цисте и вне цисты) (из: Мозговой,
1967); 19 - Paragonimus westermani ichunensis (личинка
вне цисты и в цисте); 20 - Paragonimus westermani westermani
(из: Курочкин, 1987); АД - адоральный диск
к МУК 3.2.3804-22
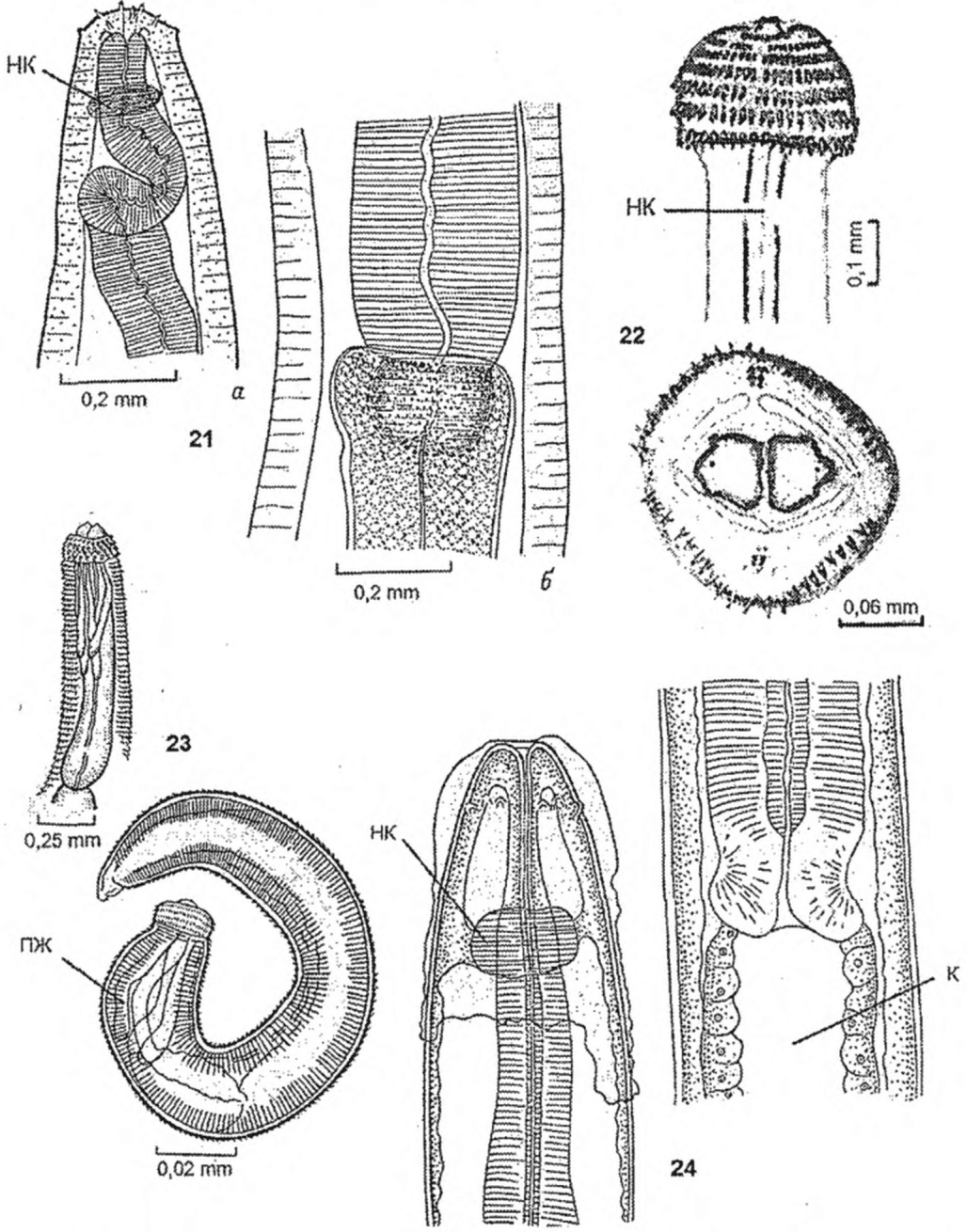
Рисунок 21 - 24. Личинки семейств Dioctophymidae,
Gnathostomatidae: 21 - Eustrongylides excisus, larva
(а - головной конец, б - область перехода пищевода
и кишечника); 22 - Echinochephalus sinensis, larva III
(передний конец - вид сбоку и сверху); 23 - Gnathostoma
hispidum, larva III (головной конец и общий вид);
24 - Dioctophyme renale, larva III (передний конец и область
границы пищевода и кишечника) (из: Определитель паразитов
пресноводных рыб, Т. 3, 1987); НК - нервное кольцо;
П - пищевод; ПЖ - пищеводная железа; К - кишечник
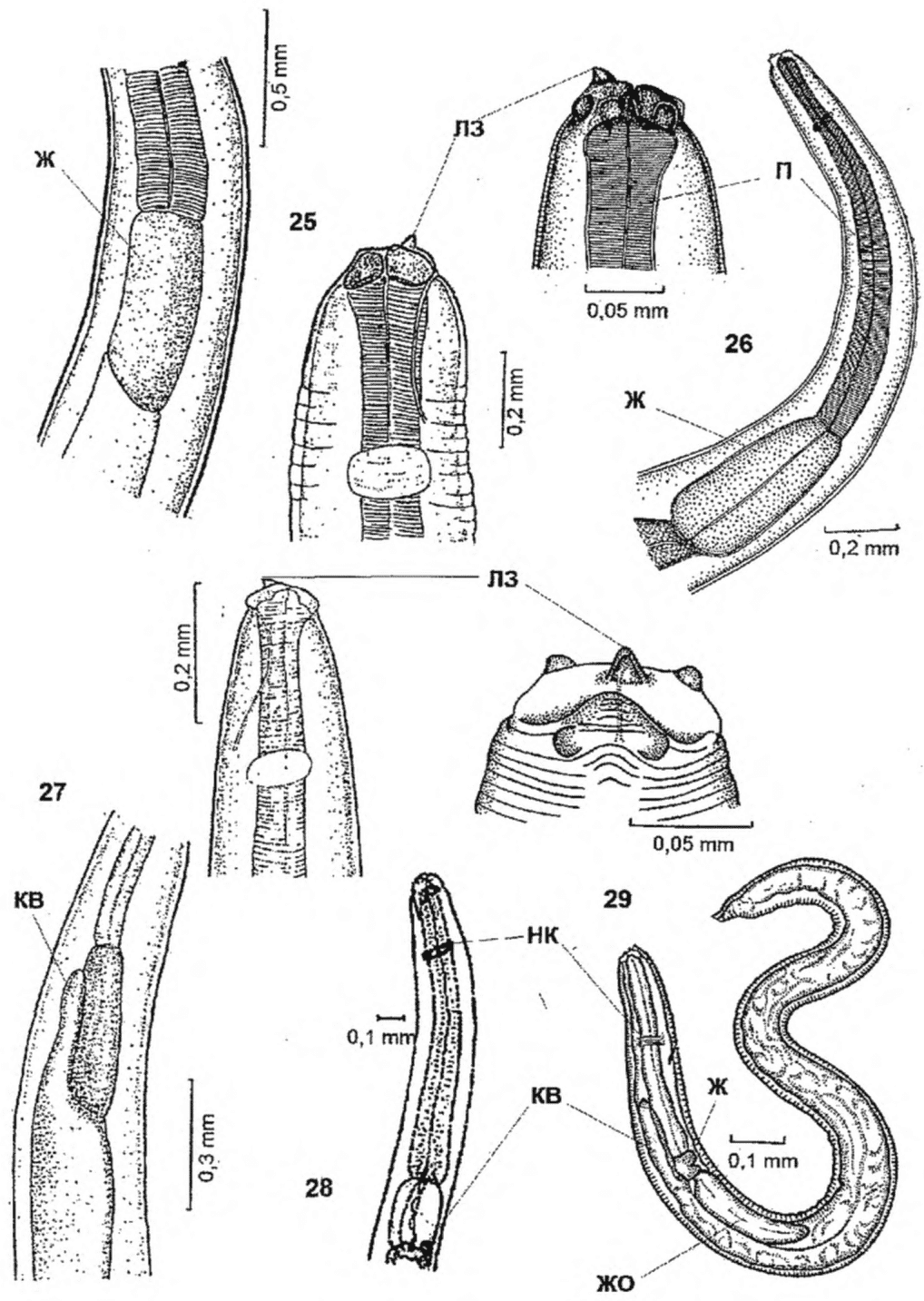
Рисунок 25 - 29. Личинки семейства Anisakidae: 25 - Anisakis
simplex, larva III (головной конец и средняя часть тела)
(из: Гаевская, Ковалева, 1991); 26 - Anisakis schupakovi,
larva III (головной конец и общий вид); (из: Определитель
паразитов пресноводных рыб, Т. 3, 1987);
27 - Pseudoterranova decipiens, larva III (общий вид
и средняя часть тела) (из: Гаевская, Ковалева, 1991);
28 - Sulcascaris sulcata, larva III; 29 - Contracaecum
osculatum, larva III; ЛЗ - личиночный зуб; НК - нервное
кольцо; П - пищевод; Ж - желудочек; ЖО - желудочный
отросток; К - кишечник; КВ - кишечный вырост
к МУК 3.2.3804-22
СЕМЕЙСТВ OPISTHORCHIDAE, NANOPHYETIDAE, HETEROPHYIDAE
(METAGONIMUS), DIPHYLLOBOTHRIIDAE, ANISAKIDAE,
POLYMORPHIDAE (BOLBOSOMA)
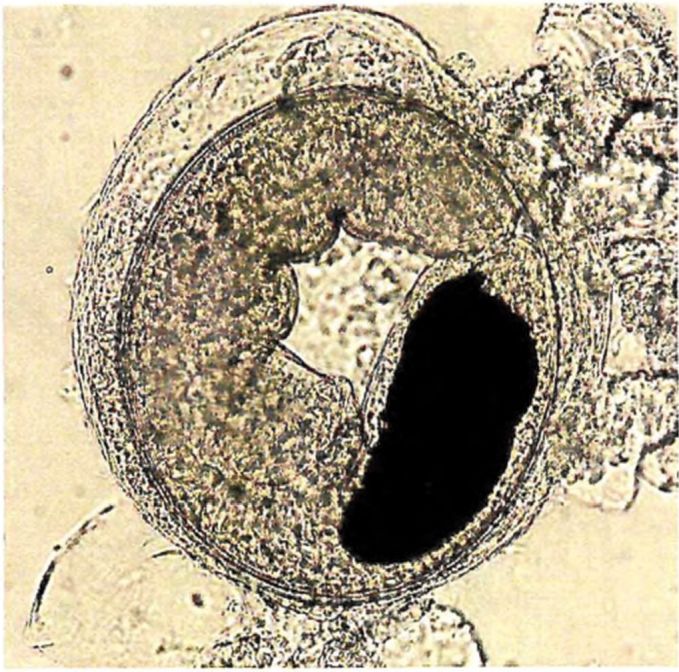
а
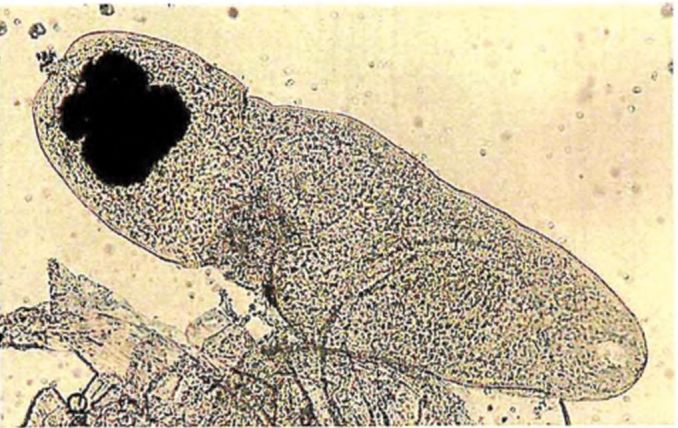
б
Рисунок 30. Личинки Opisthorchis felineus (фото ориг.,
увеличение 400x) а - в цисте, б - вне цисты
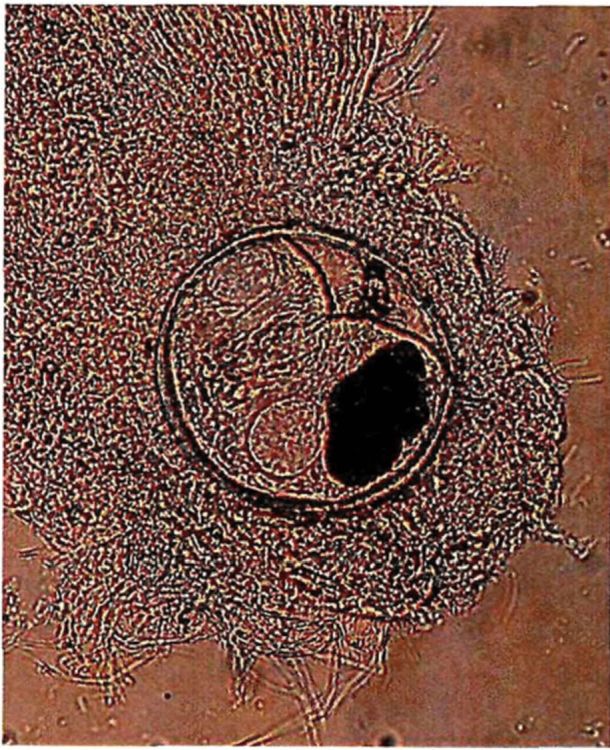 | 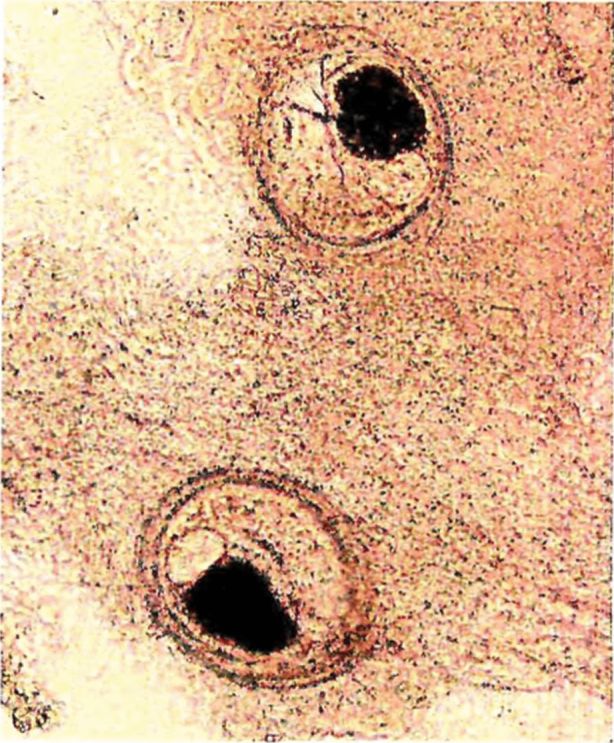 |
а | б |
Рисунок 31. Личинки Opisthorchis (Clonorshis) sinensis
в мышцах рыбы (фото ориг., а - увеличение 200x;
б - увеличение 100x)
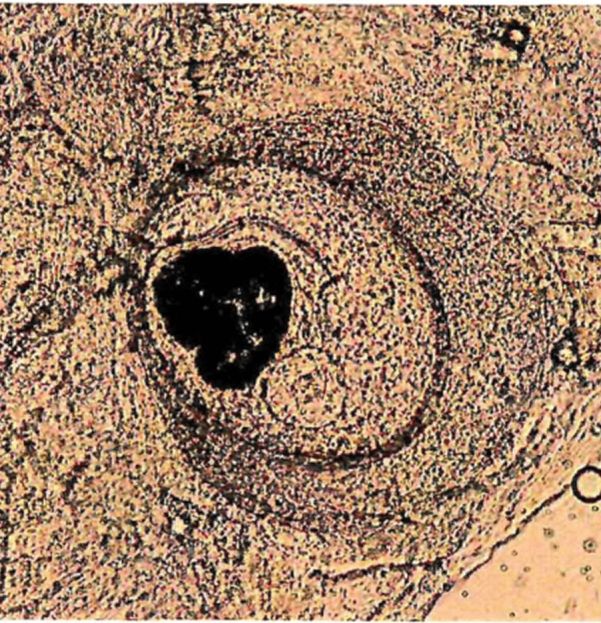 | 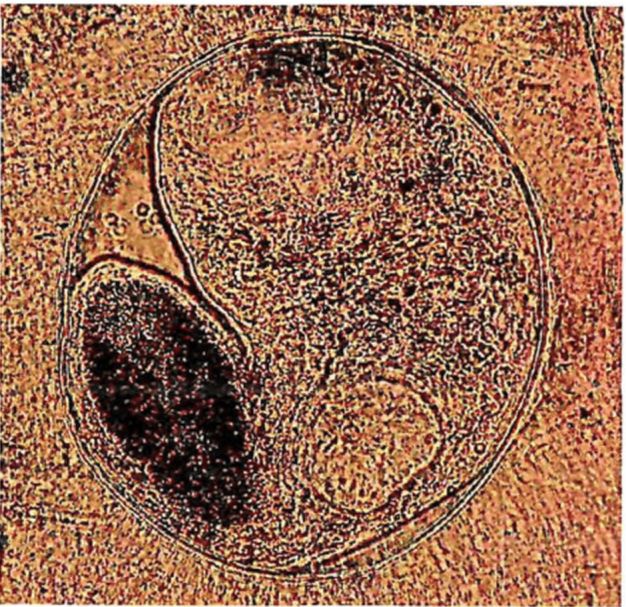 |
а | б |
Рисунок 32. Личинки Metorchis bilis (фото ориг.,
а - увеличение 200x; б - увеличение 400x)
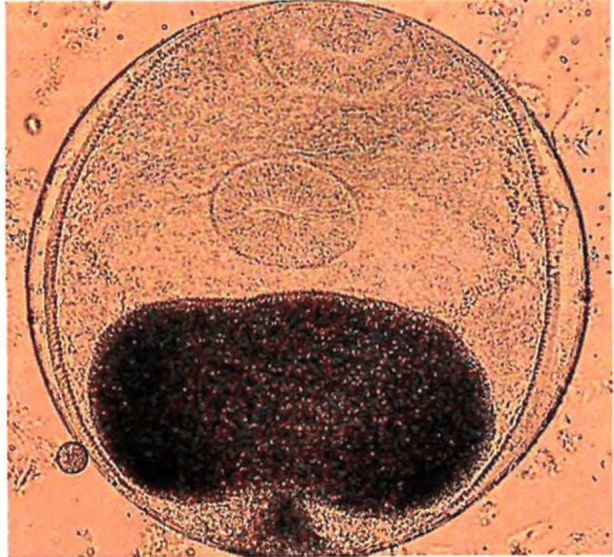
Рисунок 33. Личинка Nanophyetus salmincola schikhobalowi
(фото ориг., увеличение 400x)
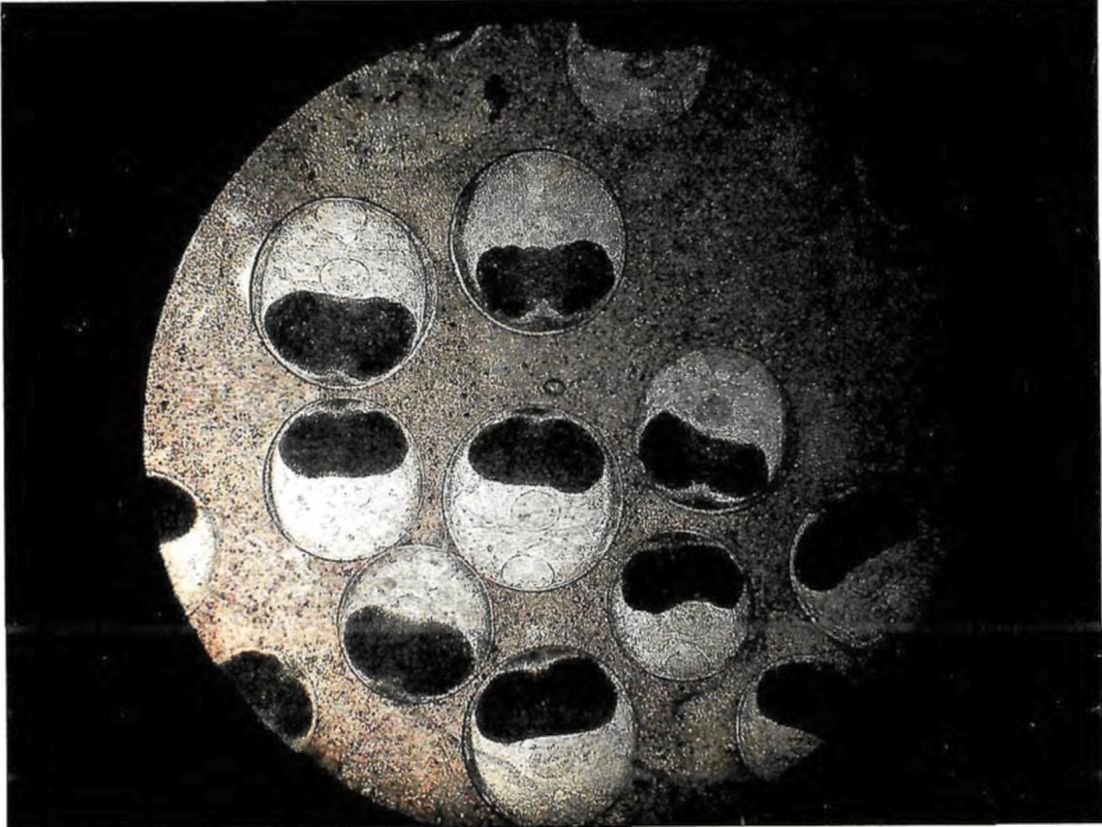
Рисунок 34. Метацеркарии Nanophyetus salmincola
schikhobalowi в почках рыбы (фото ориг., 10 x 10)
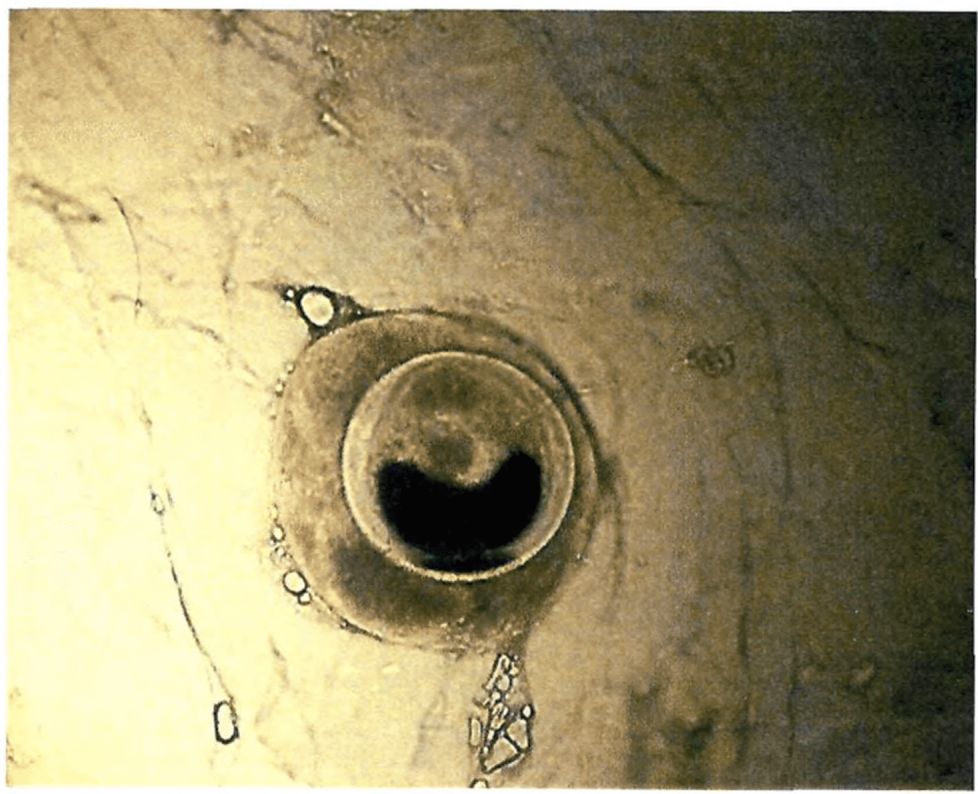
Рисунок 35. Метацеркария Nanophyetus salmincola
schikhobalowi в мышцах рыбы (фото ориг., 10 x 20)
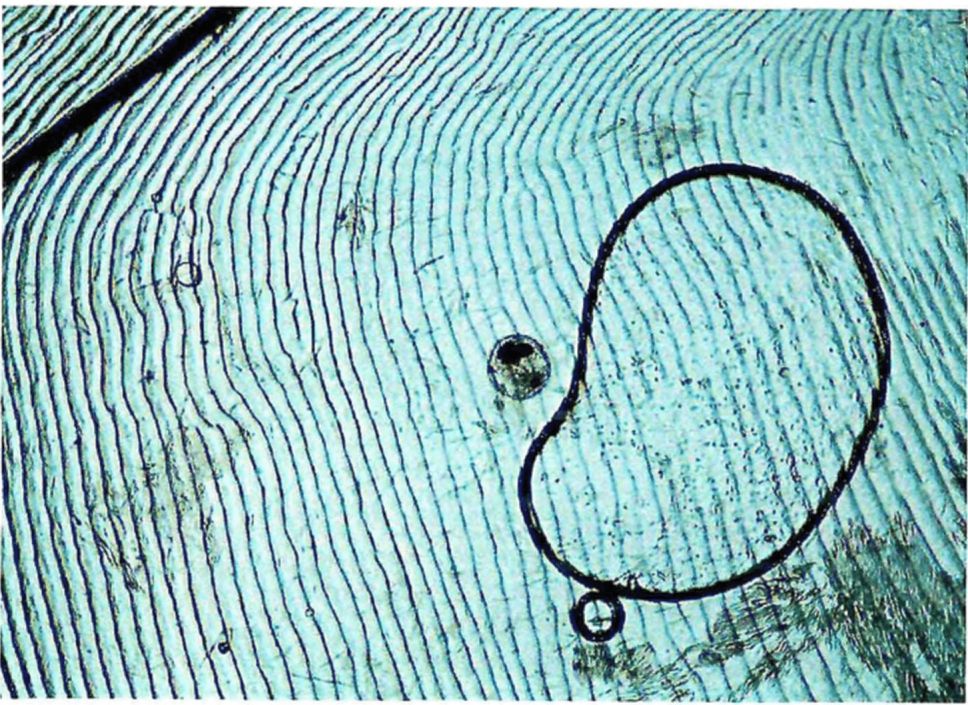
Рисунок 36. Метацеркарии Metagonimus spp. на чешуе
толстолобика белого (фото ориг., увеличение 10 x 10)
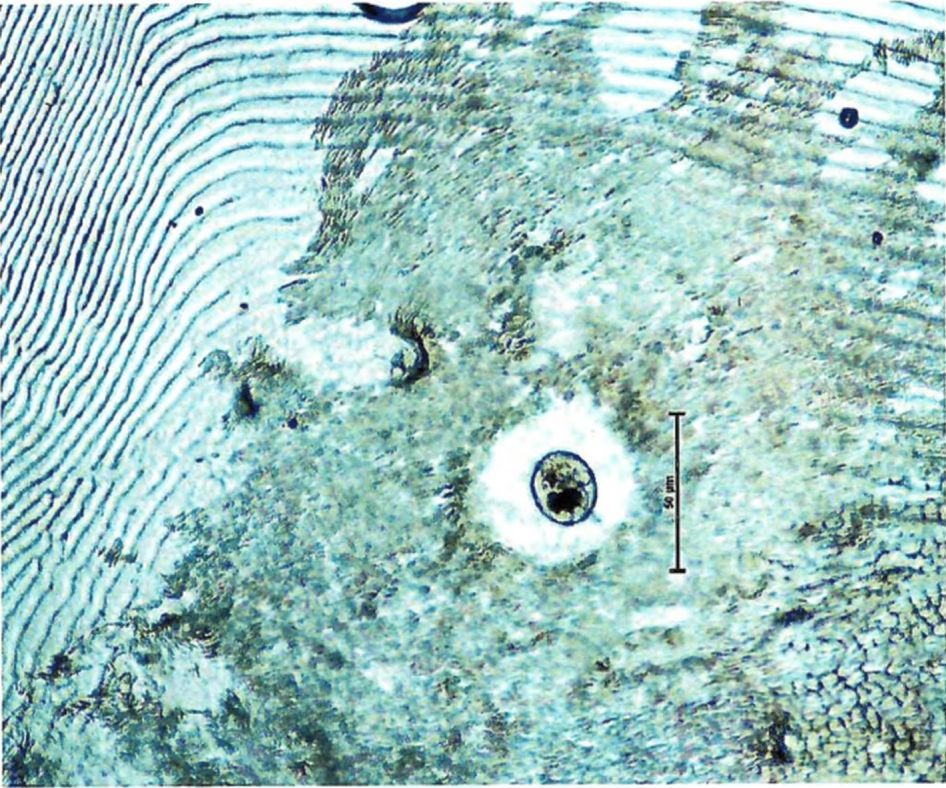
Рисунок 37. Метацеркарии Metagonimus spp. на чешуе
верхогляда (фото ориг., увеличение 10 x 10)
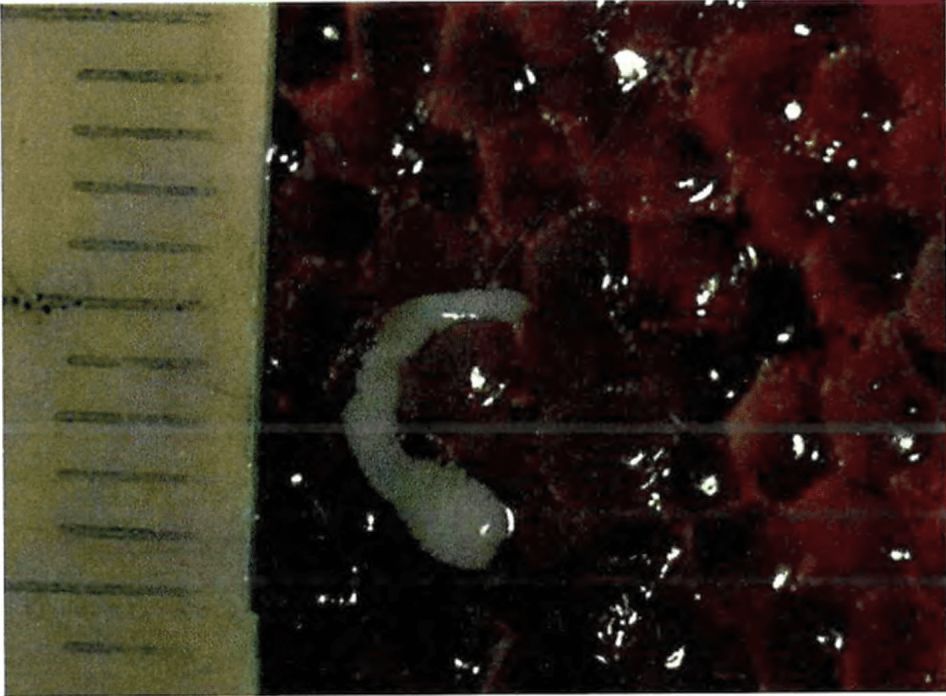
Рисунок 38. Плероцеркоид Dibothriocephalus latus в икре щуки
(фото ориг.)
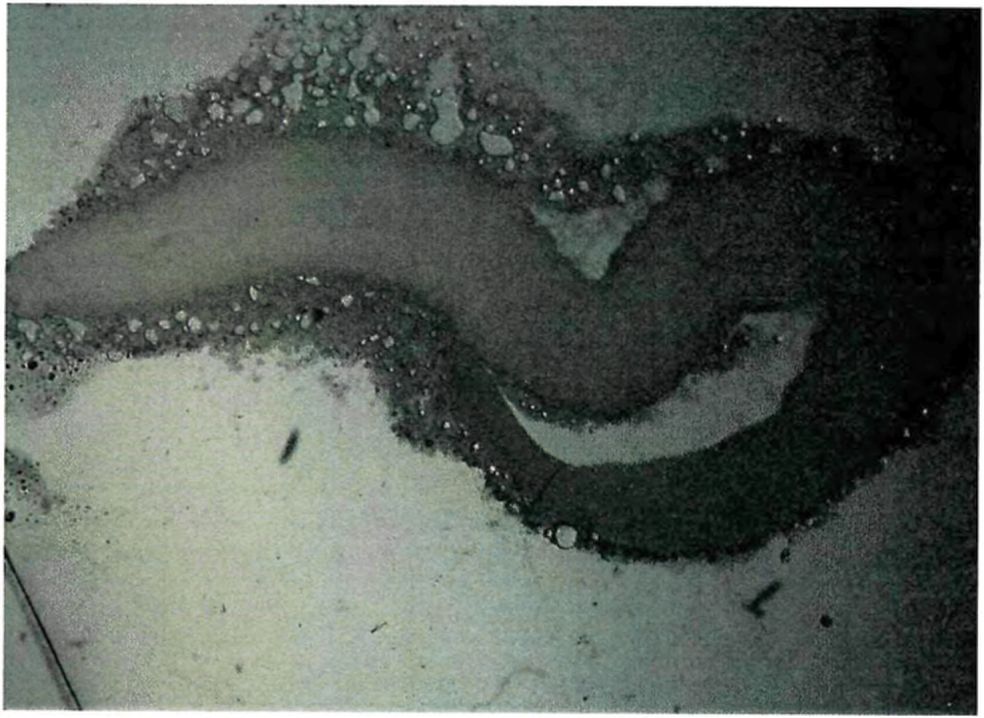
Рисунок 39. Плероцеркоид Dibothriocephalus dendriticus
(свободно лежащий) (фото ориг., увеличение 8x)
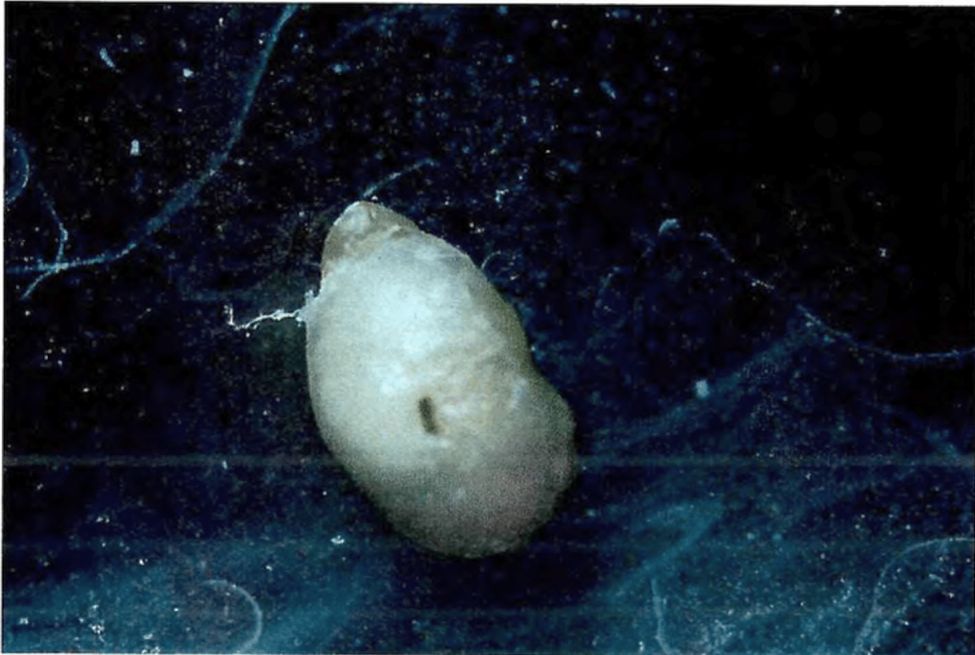
Рисунок 40. Плероцеркоид Dibothriocephalus dendriticus
(инкапсулированный) (фото ориг., увеличение 6,5x)
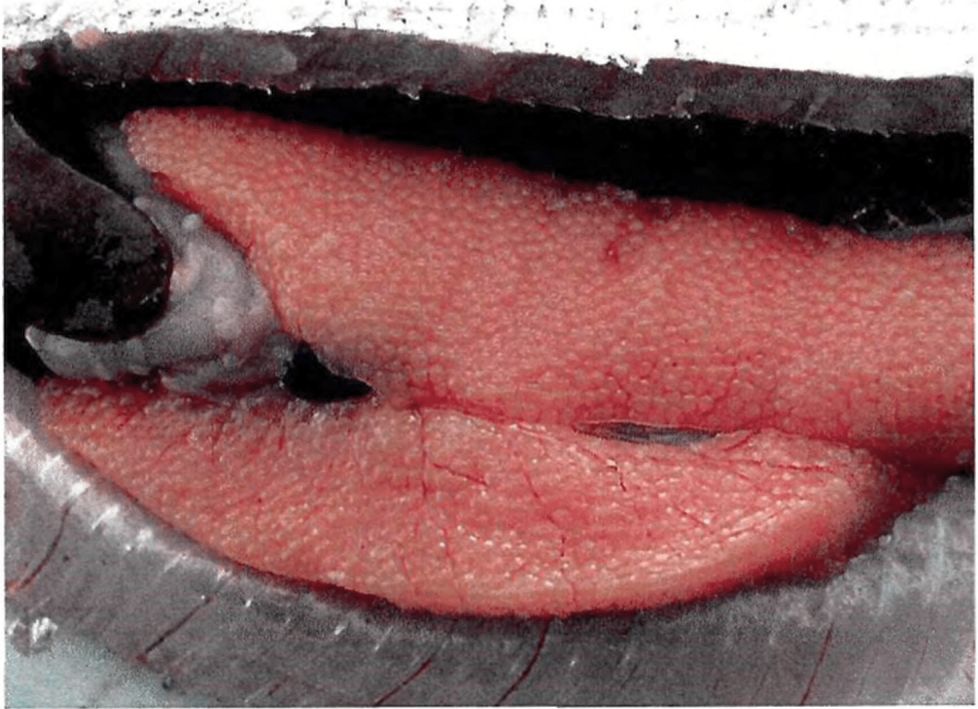
Рисунок 41. Инкапсулированные плероцеркоиды лентеца чаечного
Dibothriocephalus dendriticus в полости тела сибирской
ряпушки (фото ориг., увеличение 16x)
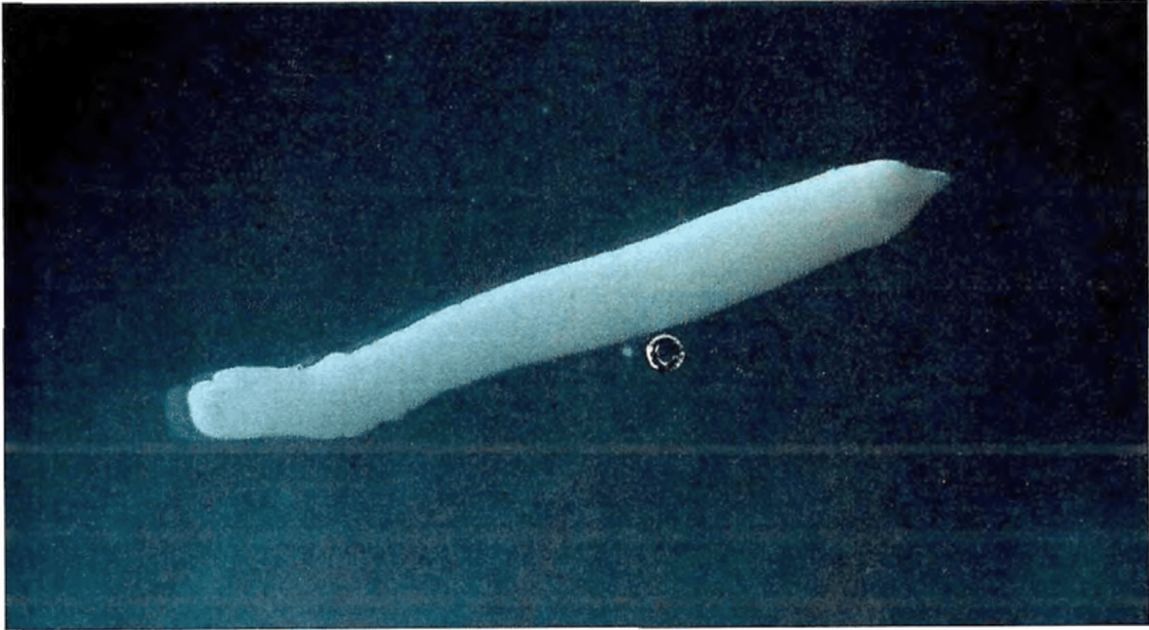
Рисунок 42. Плероцеркоид Dibothriocephalus ditremus
(свободно лежащий) (фото ориг. увеличение 6,5x)
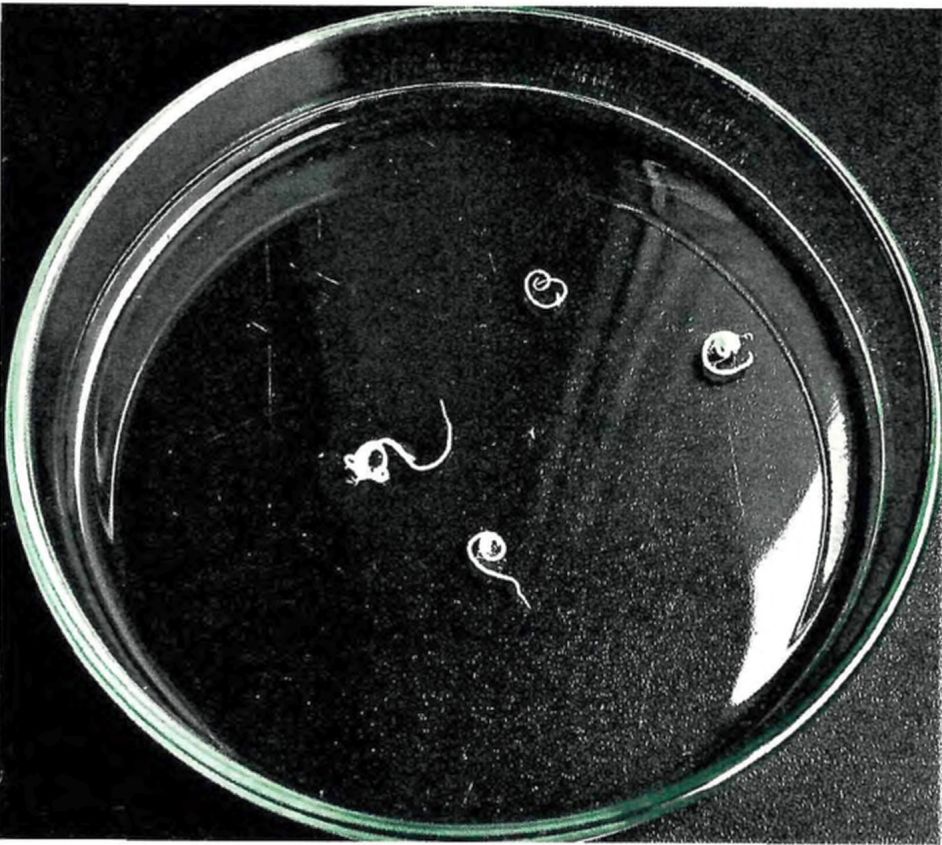
Рисунок 43. Личинка Anisakis simplex (фото ориг.,
увеличение 6,5x)
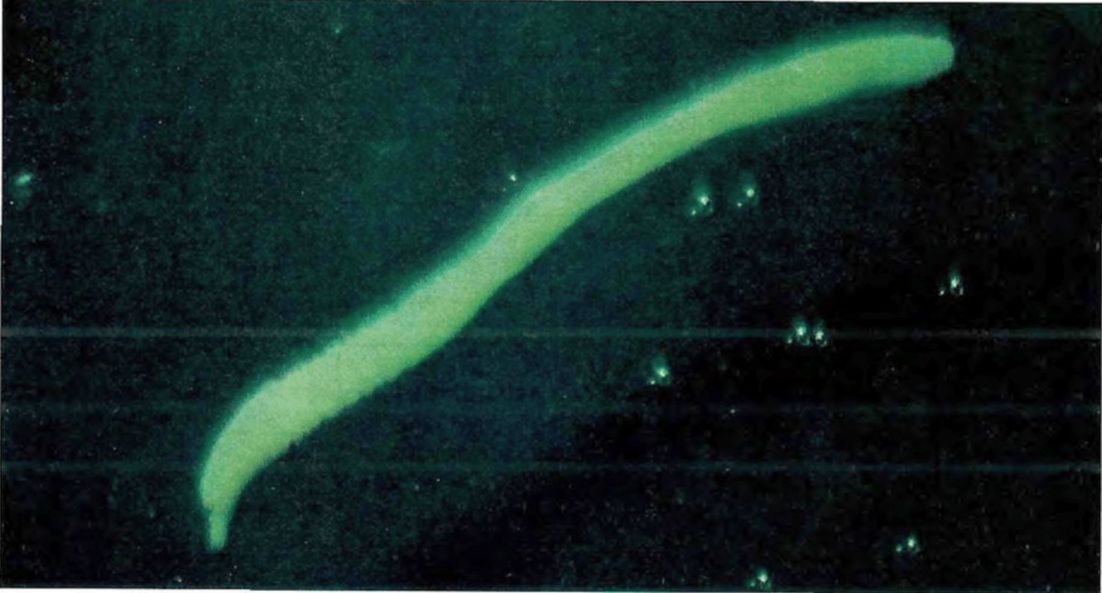
Рисунок 44. Личинка Bolbosoma spp.
(фото ориг., увеличение 10 x 10)
к МУК 3.2.3804-22
Гельминты, скребни | Вид гельминта (латинское, русское название) | Наименования личинок гельминтов <12> |
1 | 2 | 3 |
Cestoidea (Цестоды - ленточные черви) | Dibothriocephalus latus (Лентец широкий) | дифиллоботриумы |
Dibothriocephalus dendriticus (Лентец чаечный) | ||
Dibothriocephalus nihonkaiensis (D. luxi, D. klebanovskii) (Лентец дальневосточный) | ||
Dibothriocephalus ditremus (D. ditremum) | ||
Diplogonoporus balaenopterae | диплогонопорусы | |
Pyramicocephalus phocarum | пирамикоцефалусы | |
Spirometra erinaceieuropaei | спирометры | |
Trematoda (Трематоды - сосальщики) | Opisthorchis felineus | описторхисы |
Metorchis bilis | меторхисы | |
Pseudamphistomum truncatum | псевдамфисты | |
Opisthorchis (Clonorshis) sinensis | клонорхисы | |
Apophallus muehlingi | апофалусы | |
Rossicotrema (Apophallus) donicum | россикотремы | |
Metagonimus yokogawai, Metagonimus katsuradai, Metagonimus suifunensis sp. n. | метагонимусы | |
Cryptocotyle lingua | криптокортилусы | |
Cryptocotyle sp. | ||
Heterophyes heterophyes | гетерофиетусы | |
Nanophyetus salmincola schikhobalowi | нанофиетусы | |
Echinochasmus perfoliatus | эхинохазмусы | |
Paragonimus westermani westermani Paragonimus westermani ichunensis, Paragonimus pulmonalis Paragonimus skrjabini | парагонимусы | |
Nematoda (Нематоды - круглые черви) | Dioctophyme renale | диоктофимы |
Echinochephalus sinensis | эхиноцефалусы | |
Gnathostoma hispidum Gnathostoma spinigerum | гнатостомы | |
Anisakis simplex Anisakis schupakovi | анизакисы | |
Pseudoterranova decipiens | псевдотерраны | |
Contracaecum osculatum | контрацекумы | |
Sulcascaris sulcata | сулькаскарисы | |
Acanthocephala (Скребни - акантоцефалы, колючеголовые) | род Corynosoma | коринозомы |
род Bolbosoma | болбозомы |
--------------------------------
1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. Федеральный закон от 02.01.2000 N 29-ФЗ "О качестве и безопасности пищевых продуктов".
3. Федеральный закон от 28.12.2013 N 412-ФЗ "Об аккредитации в национальной системе аккредитации".
4. Технический регламент Таможенного союза "О безопасности пищевой продукции" (ТР ТС 021/2011).
5. Технический регламент Евразийского экономического союза "О безопасности рыбы и рыбной продукции" (ТР ЕАЭС 040/2016).
6. СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
7. ГОСТ ISO/IEC 17025 "Общие требования к компетентности испытательных и калибровочных лабораторий".
8. ГОСТ 34812-2021 "Продукция рыбная пищевая. Методы определения жизнеспособности личинок гельминтов".
9. МУ 3.2.3463-17 "Профилактика дальневосточных трематодозов".
10. Беэр С.А. Биология возбудителя описторхоза. - Москва: Товарищество научных изданий КМК, 2005. - 336 с.
11. Беэр С.А. Методы изучения промежуточных хозяев возбудителей описторхоза/С.А. Беэр, Ю.В. Белякова, Е.Г. Сидоров. - Алма-Ата: Наука, 1987. - 86 с.
12. Гаевская А.В. Справочник основных болезней и паразитов промысловых рыб Атлантического океана/А.В. Гаевская, А.А. Ковалева; АтлантНИРО. - Калининград: ООО "Книжное издательство", 1991. - 208 с. - ISBN 5-85500-214-4.
13. Делямуре С.Л. Дифиллоботрииды - ленточные гельминты человека, млекопитающих и птиц/С.Л. Делямуре, А.С. Скрябин, А.М. Сердюков//Основы цестодологии. - Т. 11. - Москва: Наука, 1985. - 200 с.
14. Дубинин В.Б. Фауна личинок паразитических червей позвоночных животных дельты Волги//Паразитологический сборник/Отв. ред. Павловский Е.Н. - Т. XIV. - Ленинград, 1952. - С. 213 - 265.
15. Курочкин Ю.В. Трематоды фауны СССР. Парагонимиды/Ю.В. Курочкин - Москва: Наука, 1987. - 152 с.
16. Мозговой А.А. Гельминты домашних и диких животных и вызываемые ими заболевания/А.А. Мозговой. - Москва: Наука, 1967. - 540 с.
17. Определитель паразитов пресноводных рыб фауны СССР. - Т. 3. Паразитические многоклеточные. - Ленинград: Наука, 1987. - 583 с.
18. Судариков В.Е. Метацеркарии трематод - паразиты пресноводных гидробионтов Центральной России/В.Е. Судариков, А.А. Шигин, Ю.В. Курочкин [и др.]. - Москва, Наука, 2002. - 298 с.
19. Филимонова Л.В. Биологический цикл трематоды Nanophyetus schikhobalowi/Л.В. Филимонова//Труды гельминтологической лаборатории/Под ред. К.И. Скрябина. - Т. 13. - Москва: Издательство Академии наук СССР, 1963. - С. 347 - 357.