СПРАВКА
Источник публикации
М.: ИПК Издательство стандартов, 2003
Примечание к документу
С 1 июля 2003 года до вступления в силу технических регламентов акты федеральных органов исполнительной власти в сфере технического регулирования носят рекомендательный характер и подлежат обязательному исполнению только в части, соответствующей целям, указанным в пункте 1 статьи 46 Федерального закона от 27.12.2002 N 184-ФЗ.
Документ введен в действие с 1 января 2001 года.
Название документа
"ГОСТ Р 51416-99 (ИСО 5510-84). Государственный стандарт Российской Федерации. Корма, комбикорма, комбикормовое сырье. Определение массовой доли доступного лизина"
(принят и введен в действие Постановлением Госстандарта России от 22.12.1999 N 571-ст)
"ГОСТ Р 51416-99 (ИСО 5510-84). Государственный стандарт Российской Федерации. Корма, комбикорма, комбикормовое сырье. Определение массовой доли доступного лизина"
(принят и введен в действие Постановлением Госстандарта России от 22.12.1999 N 571-ст)
Содержание
Постановлением Госстандарта России
от 22 декабря 1999 г. N 571-ст
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КОРМА, КОМБИКОРМА, КОМБИКОРМОВОЕ СЫРЬЕ
ОПРЕДЕЛЕНИЕ МАССОВОЙ ДОЛИ ДОСТУПНОГО ЛИЗИНА
Feeds, mixed feeds and raw material. Determination
of available lysine massfraction
ГОСТ Р 51416-99
(ИСО 5510-84)
ОКС 65.120;
ОКСТУ 9209
Дата введения
1 января 2001 года
1. Разработан Временным творческим коллективом, образованным в рамках договора N М98 42 002 Е 4075 между АФНОР и ВНИИЦСМВ с участием членов Технического комитета по стандартизации ТК 4 "Комбикорма, БВД, премиксы".
Внесен Техническим комитетом по стандартизации ТК 4 "Комбикорма, БВД, премиксы".
2. Принят и введен в действие Постановлением Госстандарта России от 22 декабря 1999 г. N 571-ст.
3. Настоящий стандарт за исключением 2, 6.6, 6.7, 6.8 и 7 представляет собой аутентичный текст международного стандарта ИСО 5510-84 "Корма для животных. Определение доступного лизина".
4. Введен впервые.
5. Переиздание. Апрель 2003 г.
Настоящий стандарт устанавливает метод определения доступного лизина в кормах, содержащих белки животного или растительного происхождения.
Лизин кормов считается усвояемым в том случае, если в нем не связана конечная аминогруппа (аминогруппа  ). Определяют эту фракцию лизина, используя способность связанных конечных аминогрупп соединяться с 2,4-динитрофторбензолом.
). Определяют эту фракцию лизина, используя способность связанных конечных аминогрупп соединяться с 2,4-динитрофторбензолом.
Однако данный метод по сравнению с биологическим завышает содержание доступного лизина, поэтому следует быть осторожным при интерпретации полученных результатов.
ГОСТ 13496.0-80 <*>. Комбикорма, сырье. Методы отбора проб
--------------------------------
<*> Действует до введения ГОСТ Р, разработанного на основе ИСО 6497 [1].
ГОСТ Р 51417-99 (ИСО 5983-97). Корма, комбикорма, комбикормовое сырье. Определение массовой доли азота и вычисление массовой доли сырого протеина. Метод Кьельдаля
ГОСТ Р 51419-99 (ИСО 6498-98). Корма, комбикорма, комбикормовое сырье. Подготовка испытуемых проб.
В настоящем стандарте применяют следующий термин с соответствующим определением:
Доступный лизин: масса лизина, представляющая разницу между массами общего и недоступного лизина, определяемыми при условиях, установленных настоящим стандартом. Результат выражают в процентах в испытуемом продукте.
Измельченную навеску пробы гидролизуют хлористоводородной кислотой, общий лизин выделяют при помощи хроматографии на колонке и измеряют его содержание на спектрометре при длине волны 570 нм.
Вторую навеску измельченной пробы обрабатывают спиртовым раствором 2,4-динитрофторбензола в щелочной среде, очищают, гидролизуют хлористоводородной кислотой, выделяют недоступный лизин при помощи хроматографии на колонке и измеряют его содержание на спектрофотометре при 570 нм.
Все реактивы должны быть квалификации х.ч. или ч.д.а. Вода должна быть дистиллированной.
5.1. Диэтиловый эфир, свободный от перекисей.
5.2. Кислый углекислый натрий, раствор массовой концентрации 80 г/дм3.
5.3. Спиртовый раствор 2,4-динитрофторбензола (ДНФБ)
В 12 см3 95%-ного (по объему) этилового спирта растворяют 0,15 см3 ДНФБ.
Раствор готовят перед использованием.
5.4. Раствор хлористоводородной кислоты молярной концентрации 6 моль/дм3
Один объем хлористоводородной кислоты плотностью 1,19 г/см3 смешивают с 1 объемом дистиллированной воды.
Последовательно растворяют в дистиллированной воде 21 г лимонной кислоты; 8 г гидроокиси натрия; 16 см3 хлористоводородной кислоты плотностью 1,19 г/см3; 0,1 см3 октиловой (каприловой) кислоты; 20 см3 тиодигликоля; 3 см3 30%-ного (по объему) водного раствора додецилового эфира полиоксиэтилена с приблизительно 23 молекулами оксиэтилена. Объем раствора доводят до 1000 см3 дистиллированной водой.
Последовательно растворяют в дистиллированной воде 24,5 г одноводной лимонной кислоты; 14 г гидроокиси натрия; 6,8 см3 хлористоводородной кислоты плотностью 1,19 г/см3; 0,1 см3 октиловой (каприловой) кислоты; 3 см3 30%-ного (по объему) водного раствора додецилового эфира полиэтоксила с приблизительно 23 молекулами оксиэтилена. Объем раствора доводят до 1000 см3 дистиллированной водой. Устанавливают pH 5,28 +/- 0,02, используя хлористоводородную кислоту плотностью 1,19 г/см3 или раствор гидроокиси натрия массовой долей 50%.
5.7. Нингидриновый реактив
5.7.1. Пропионовокислый натрий, буферный раствор pH 5,5 +/- 0,1
В приблизительно 400 см3 дистиллированной воды растворяют 168 г гидроокиси натрия. Охлаждают, затем при встряхивании добавляют 498 см3 пропионовой кислоты. Объем раствора доводят до 1000 см3 дистиллированной водой.
5.7.2. Приготовление реактива
Нингидриновый реактив готовят в атмосфере азота и в темноте. В колбу вместимостью 2000 см3 помещают 1000 см3 свободного от перекисей монометилового эфира этиленгликоля, 1000 см3 буферного раствора пропионовокислого натрия и 40 г нингидрина. Встряхивают до полного растворения, затем добавляют 1,33 г 2-водного хлористого олова (II)  . Перемешивают встряхиванием до полного растворения. (См. примечание).
. Перемешивают встряхиванием до полного растворения. (См. примечание).
 . Перемешивают встряхиванием до полного растворения. (См. примечание).
. Перемешивают встряхиванием до полного растворения. (См. примечание).Реактив устойчив в течение 1 мес при хранении при 4 °C под небольшим давлением в атмосфере азота и в темноте.
Примечание. Если наблюдается выпадение осадка хлористого олова (II), его заменяют 7,5 см3 раствора хлористого титана массовой концентрации 150 г/дм3 или 1,5 г гидриндантина на 1 дм3 реактива.
5.8. Лизин, стандартный раствор молярной концентрации c 1 мкмоль/дм3
В 100 см3 раствора хлористоводородной кислоты молярной концентрации c (HCl) = 0,1 моль/дм3 растворяют 182,5 мг моногидрохлорида лизина. Отбирают точно 10 см3 этого раствора и разбавляют его до 100 см3 буферным раствором лимоннокислого натрия pH 2,2 (5.5). 1 см3 этого раствора содержит 1 мкмоль лизина.
Обычная лабораторная аппаратура, а также указанная в 6.1 - 6.8.
6.1. Колбы плоскодонные вместимостью 250 и 1000 см3, короткогорлые с притертым коническим шлифом и обратные холодильники, подходящие к колбам.
6.2. Тигли с фильтрующей пористой стеклянной пластинкой Р16 (размер пор от 10 до 16 мк).
6.3. Масляная баня температурой, обеспечивающей обратную конденсацию (от 120 до 130 °C).
6.4. Ротационный испаритель.
6.5. Автоанализатор аминокислот или система для хроматографии вручную, включающая:
а) хроматографическую колонку длиной около 250 мм и внутренним диаметром 6 мм, термостатируемая при 55 °C при помощи водяной рубашки с циркулирующей водой и заполненная до высоты 200 мм 8%-ной сильнокислой катионобменной смолой с поперечными связями и функциональными сульфогруппами, размер частиц (13 +/- 2) мк;
б) небольшой поршневой насос, обеспечивающий скорость потока 50 см3/ч;
в) коллектор фракций;
г) кипящую водяную баню;
д) спектрометр со спектральной областью, включающей 570 нм, с кюветами толщиной 10 мм.
6.6. Градуировочные пипетки вместимостью 1,5 и 10 см3 с допускаемой относительной погрешностью +/- 1%.
7.1. Отбор проб по ГОСТ 13496.0.
8.1. Подготовка проб по ГОСТ Р 51419.
Две навески, взятые на весах 2-го класса точности, массой, содержащей около 100 мг сырого протеина, помещают в две колбы (6.1). Содержание сырого протеина определяют по ГОСТ Р 51417.
8.3. Общий лизин
В колбу вместимостью 1000 см3 к навеске добавляют 500 см3 хлористоводородной кислоты молярной концентрации c (HCl) = 6 моль/дм3. Закрывают колбу обратным холодильником и помещают в масляную баню, предварительно нагретую до 120 - 130 °C.
После медленного кипячения в течение 24 ч колбу охлаждают и содержимое фильтруют через тигель. Фильтрат выпаривают при температуре не выше 40 °C на ротационном испарителе. К остатку добавляют дистиллированную воду и снова выпаривают. Эту операцию повторяют до тех пор, пока не будет удалена хлористоводородная кислота; для этого обычно достаточно четыре обработки, используя каждый раз по 30 см3 дистиллированной воды. Остаток растворяют в буферном растворе pH 2,2 и количественно переносят в мерную колбу вместимостью 100 см3. Объем раствора доводят до метки буферным раствором pH 2,2. Фильтруют через складчатый бумажный фильтр.
Насос анализатора присоединяют к емкости, содержащей буферный раствор лимоннокислого натрия с pH 5,28 (5.6). Затем его регулируют, чтобы обеспечить скорость потока жидкости 50 см3/ч. Насос присоединяют в колонке со смолой, нагретой предварительно до 55 °C, и в течение 20 мин через колонку пропускают буферный раствор, чтобы установилось равновесие. Насос отсоединяют. Удаляют большую часть жидкости над смолой, следя при этом, чтобы поверхность смолы все время была покрыта жидкостью.
При помощи пипетки 0,5 см3 гидролизата (или 1 см3, если ручная система) наносят на колонку и пропускают его через колонку под небольшим давлением азота. Стенки колонки обмывают 0,5 см3 буферного раствора pH 5,28 и пропускают через колонку. Колонку доверху заполняют буферным раствором и присоединяют к насосу.
Включают анализатор. Прибор градуируют по 8.3.2, используя 0,25 мкмоль лизина (0,25 см3 стандартного раствора лизина) или массу лизина, установленную в инструкции к анализатору.
8.3.3.2. Ручная система
8.3.3.2.1. Локализация лизина
Фракцию элюата, содержащую лизин, определяют, используя раствор лизина известной концентрации, например, 1 мкмоль/см3. Для этого отбрасывают первые 25 - 30 см3 элюата и затем собирают в пробирки фракции по 1 см3 до тех пор, пока не получат 50 фракцию, считая с начала элюирования. К каждой фракции между 30 и 50 фракциями добавляют по 1 см3 нингидринового реактива. Перемешивают, переносят в кипящую водяную баню и оставляют на 15 мин. Охлаждают и разбавляют путем добавления 10 см3 буферного раствора pH 5,28.
Примечание. Исключительно для информации: при описанных условиях лизин обычно элюируется между 39 и 45 фракциями.
Если лизин элюировался между 39 и 45 фракциями, отбрасывают первые 38 см3 элюата, собирают и смешивают фракции (от 39 до 45), соответствующие пику лизина, и высушивают на ротационном испарителе.
Примечание. После получения фракций, содержащих лизин, через колонку пропускают еще около 200 см3 буферного раствора, чтобы удалить нежелательные компоненты, которые могут остаться.
Остаток растворяют в 5 см3 буферного раствора pH 5,28 и добавляют 5 см3 нингидринового реактива. Перемешивают, переносят в кипящую водяную баню и оставляют на 15 мин. Охлаждают и разбавляют буферным раствором pH 5,28, чтобы концентрация лизина в измеряемом растворе составляла приблизительно 0,02 мкмоль/см3. (Пусть  - объем полученного таким образом измеряемого раствора).
- объем полученного таким образом измеряемого раствора).
Измеряют поглощение на спектрометре при 570 нм против жидкости, представляющей смесь одного объема буферного раствора и одного объема нингидринового реактива, которую предварительно помещают на 15 мин в кипящую водяную баню, и после охлаждения разбавляют до объема  .
.
Отбирают точно 5 см3 стандартного раствора лизина, прибавляют 5 см3 нингидринового реактива. Перемешивают, ставят на 15 мин в кипящую водяную баню. Охлаждают и разбавляют до 100 см3 буферным раствором pH 5,28.
Измеряют поглощение на спектрометре при тех же условиях, как в 8.3.3.2.2.
8.4. Недоступный лизин
8.4.1. Реакция динитрофенилирования
В колбу вместимостью 250 см3, где находится вторая навеска испытуемой пробы (см. 8.2), при помощи пипетки переносят 8 см3 раствора кислого углекислого натрия. Оставляют приблизительно на 10 мин, помешивая время от времени. Затем добавляют раствор ДНФБ, колбу закрывают, содержимое перемешивают, следя за тем, чтобы не осталось частичек, прилипших к стенкам колбы. Смесь оставляют на ночь при комнатной температуре в темном месте.
8.4.2. Очистка
Жидкость выпаривают досуха на ротационном испарителе при температуре ниже 40 °C. Затем в колбу добавляют 75 см3 диэтилового эфира, перемешивают и дают отстояться. Выливают большую часть диэтилового эфира с предосторожностями, чтобы не удалить при этом твердые частички. Эту операцию повторяют еще два раза, используя каждый раз по 50 см3 диэтилового эфира. Оставшиеся следы диэтилового эфира удаляют путем нагревания на ротационном испарителе.
8.4.3. Гидролиз хлористоводородной кислотой
В колбу вносят 150 см3 хлористоводородной кислоты и выполняют процедуры по 8.3.1, но гидролизат, растворенный в буферном растворе pH 2,2, количественно переносят в мерную колбу вместимостью 20 см3 (или 10 см3 при использовании ручной системы).
В ручном варианте измерение на спектрофотометре можно проводить после разбавления смеси лизин плюс реактив до 20 см3 буферным раствором pH 5,28. (Пусть  - объем полученного таким образом измеряемого раствора).
- объем полученного таким образом измеряемого раствора).
8.5. Количество определений
Проводят два параллельных определения, используя две разные пары навесок испытуемой пробы.
9.1.1. Определение на автоанализаторе
Массовую долю общего лизина в испытуемой пробе  , %, вычисляют по формуле
, %, вычисляют по формуле
 , (1)
, (1)где 0,25 - объем стандартного раствора лизина, нанесенный на колонку, см3;
0,146 - массовая концентрация стандартного раствора лизина, мг/см3;
100 - объем гидролизата пробы, см3;
100 - коэффициент пересчета в проценты;
 ), см3;
), см3;1000 - коэффициент пересчета мг в г.
9.1.2. Определение вручную
Массовую долю общего лизина в испытуемой пробе  , %, вычисляют по формуле
, %, вычисляют по формуле
 , (2)
, (2)ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: пункт 8.3.2.2 отсутствует. |
где  - оптическая плотность, определяемая по 8.3.2.2;
- оптическая плотность, определяемая по 8.3.2.2;
100 - коэффициент пересчета в проценты;
0,73 - масса лизина в 5 см3 стандартного раствора лизина, мг;
 ), см3;
), см3;1000 - коэффициент пересчета мг в г.
9.2.1. Определение на автоанализаторе
Массовую долю недоступного лизина в испытуемой пробе  , %, вычисляют по формуле
, %, вычисляют по формуле
 , (3)
, (3)где  - площадь пика, соответствующего недоступному лизину, определяемому по 8.4.4, мм2;
- площадь пика, соответствующего недоступному лизину, определяемому по 8.4.4, мм2;
 ), см3.
), см3.9.2.2. Определение вручную
Массовую долю недоступного лизина в испытуемой пробе  , %, вычисляют по формуле
, %, вычисляют по формуле
 , (4)
, (4)где  - оптическая плотность, определяемая по 8.4.4;
- оптическая плотность, определяемая по 8.4.4;
 ), см3;
), см3;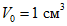 ), см3;
), см3;9.3. Доступный лизин
Массовую долю доступного лизина в испытуемой пробе  , %, вычисляют по формуле
, %, вычисляют по формуле
 , (5)
, (5)где  - массовая доля общего лизина (см. 9.1);
- массовая доля общего лизина (см. 9.1);
Примечание. Массовую долю доступного лизина в общем лизине, %, вычисляют по формуле
 (6)
(6)9.4. Сходимость
Расхождение результатов двух параллельных определений не должно превышать 10% от их среднего арифметического значения.
9.5. Воспроизводимость
Расхождение результатов двух определений, выполненных при различных условиях, не должно превышать 20% от их среднего арифметического значения.
В отчете об испытании должны быть указаны:
- используемый метод;
- полученные результаты;
- любые условия проведения испытаний, не установленные данным стандартом и касающиеся подробностей, которые могли повлиять на результат.
В отчете должны быть все данные, необходимые для полной идентификации пробы.
(справочное)
БИБЛИОГРАФИЯ