Скачать ГОСТ Р ИСО 12417-1-2019 Имплантаты сердечно-сосудистые и экстракорпоральные системы. Сосудистые устройства, включающие лекарственные компоненты. Часть 1. Общие требования
Дата актуализации: 01.01.2021

 ГОСТ Р ИСО 12417-1-2019
ГОСТ Р ИСО 12417-1-2019
Имплантаты сердечно-сосудистые и экстракорпоральные системы. Сосудистые устройства, включающие лекарственные компоненты. Часть 1. Общие требования
| Обозначение: |  ГОСТ Р ИСО 12417-1-2019 ГОСТ Р ИСО 12417-1-2019 |
| Обозначение англ: |  GOST R ISO 12417-1-2019 GOST R ISO 12417-1-2019 |
| Статус: | введен впервые |
| Название рус.: | Имплантаты сердечно-сосудистые и экстракорпоральные системы. Сосудистые устройства, включающие лекарственные компоненты. Часть 1. Общие требования |
| Название англ.: | Cardiovascular implants and extracorporeal systems. Vascular device-drug combination products. Part 1. General requirements |
| Дата добавления в базу: | 01.02.2020 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.05.2020 |
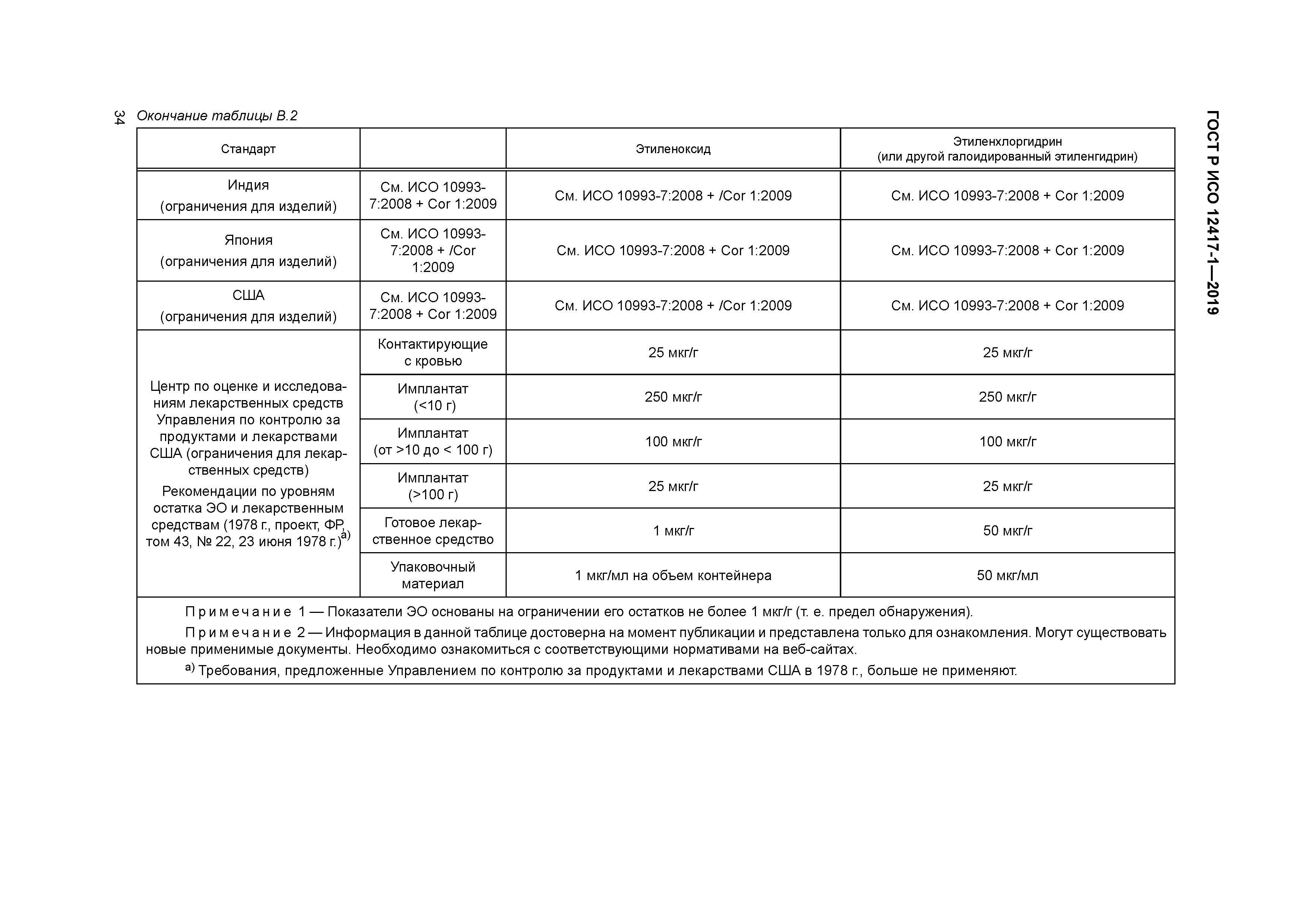
| Область применения: | Стандарт содержит требования к сосудистым устройствам, включающим лекарственные компоненты (СУВЛК) на основе текущих технических и медицинских знаний. СУВЛК — это медицинские изделия с различными клиническими показаниями для использования в кровеносно-сосудистой системе человека. СУВЛК содержит в себе, в качестве неотъемлемой части, вещество(а), которое(ые), если они использует(ют)ся отдельно, может(гут) рассматриваться как лекарственное вещество или средство (лекарственное вещество, лекарственное средство), но действие лекарственного вещества является вспомогательным по отношению к действию лекарственного средства и поддерживает основной способ действия (ОСД) устройства. Относительно вопросов безопасности в стандарте изложены требования к предполагаемому использованию, характеристикам конструкции, материалам, оценке конструкции, производству, стерилизации, упаковке и информации, предоставленной производителем. В отношении имплантатов стандарт следует рассматривать как дополнение к ИСО 14630, в котором указаны общие требования, предъявляемые к характеристикам неактивных хирургических имплантатов. Стандарт следует также рассматривать в качестве дополнения к соответствующим стандартам для определенных устройств, таким как спецификации ИСО 25539, содержащие требования к эндоваскулярным устройствам. Требования, перечисленные в стандарте, также относятся к СУВЛК, которые не являются постоянными имплантатами. Системы позиционирования или части системы позиционирования включены в область применения стандарта, если они являются неотъемлемой частью устройства и если они покрыты лекарственным средством (например, баллонные катетеры с лекарственным покрытием и проводники с лекарственным покрытием). Устройства, чей ОСД должен обеспечивать канал для доставки лекарственного средства, не регулируются стандартом (например, инфузионные катетеры), если они не содержат лекарственный компонент, который предназначен для вспомогательного воздействия на элемент устройства (например, инфузионный катетер с противомикробным покрытием). Процедуры и устройства, используемые до и после введения СУВЛК (например, устройства для баллонной ангиопластики), не регулируются настоящим стандартом, если они не влияют на аспекты устройства, связанные с лекарственным средством. Стандарт не охватывает все аспекты в отношении фармакологической оценки СУВЛК. Информация о требованиях различных национальных и региональных органов приведена в приложении В. Абсорбируемые компоненты СУВЛК (например, покрытия) рассматриваются в стандарте в связи с аспектами устройства, связанными с лекарственным средством. Разрушение и другие, зависящие от времени, аспекты абсорбируемых имплантатов и покрытий не полностью описаны в стандарте. В стандарте не рассматриваются проблемы, связанные с жизнеспособными или нежизнеспособными биологическими материалами, такими как ткани, клетки или белки, и с активными хирургическими имплантатами (т.е. имплантатами, которым необходима энергия, не генерируемая человеческим телом или гравитацией). |
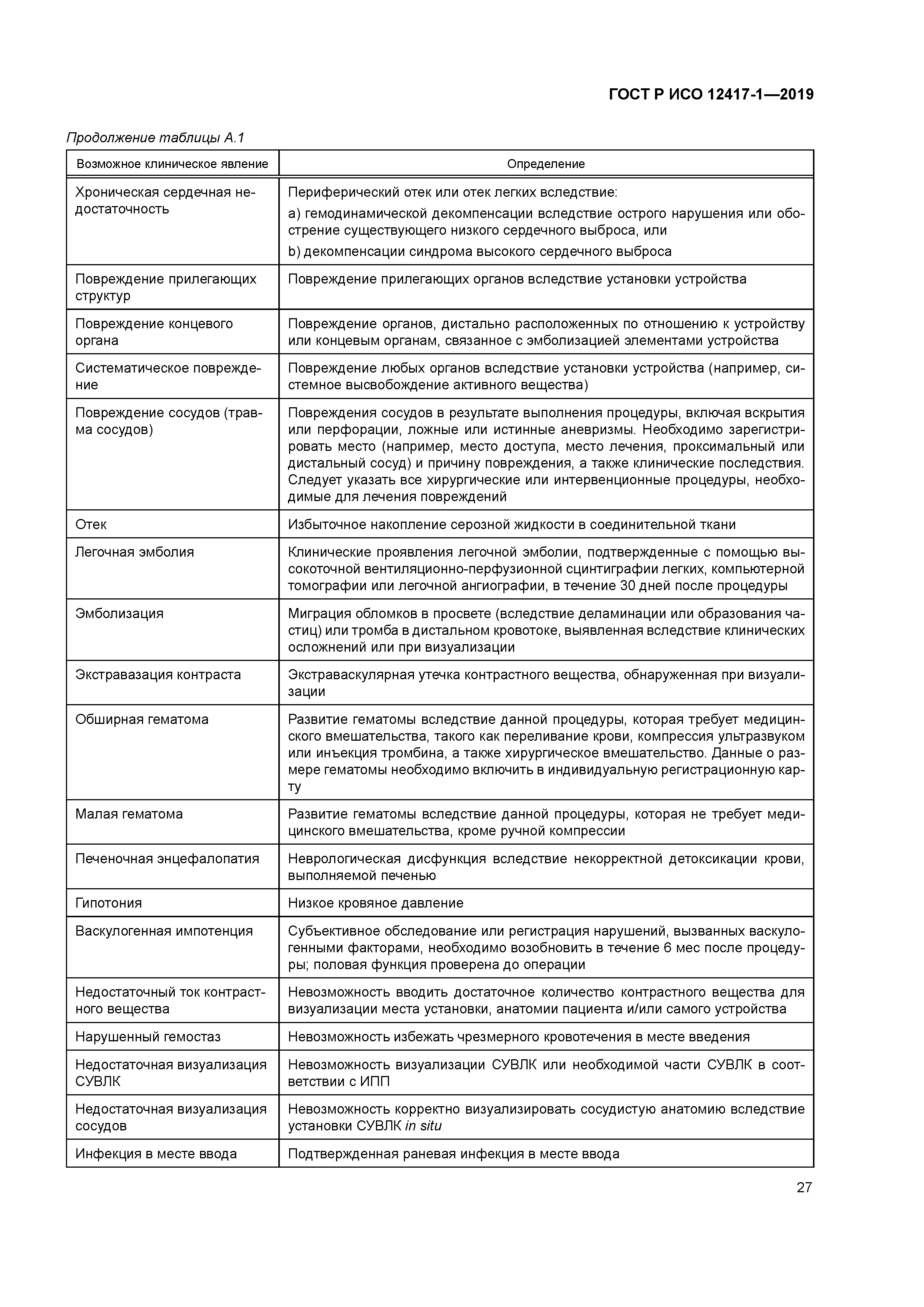
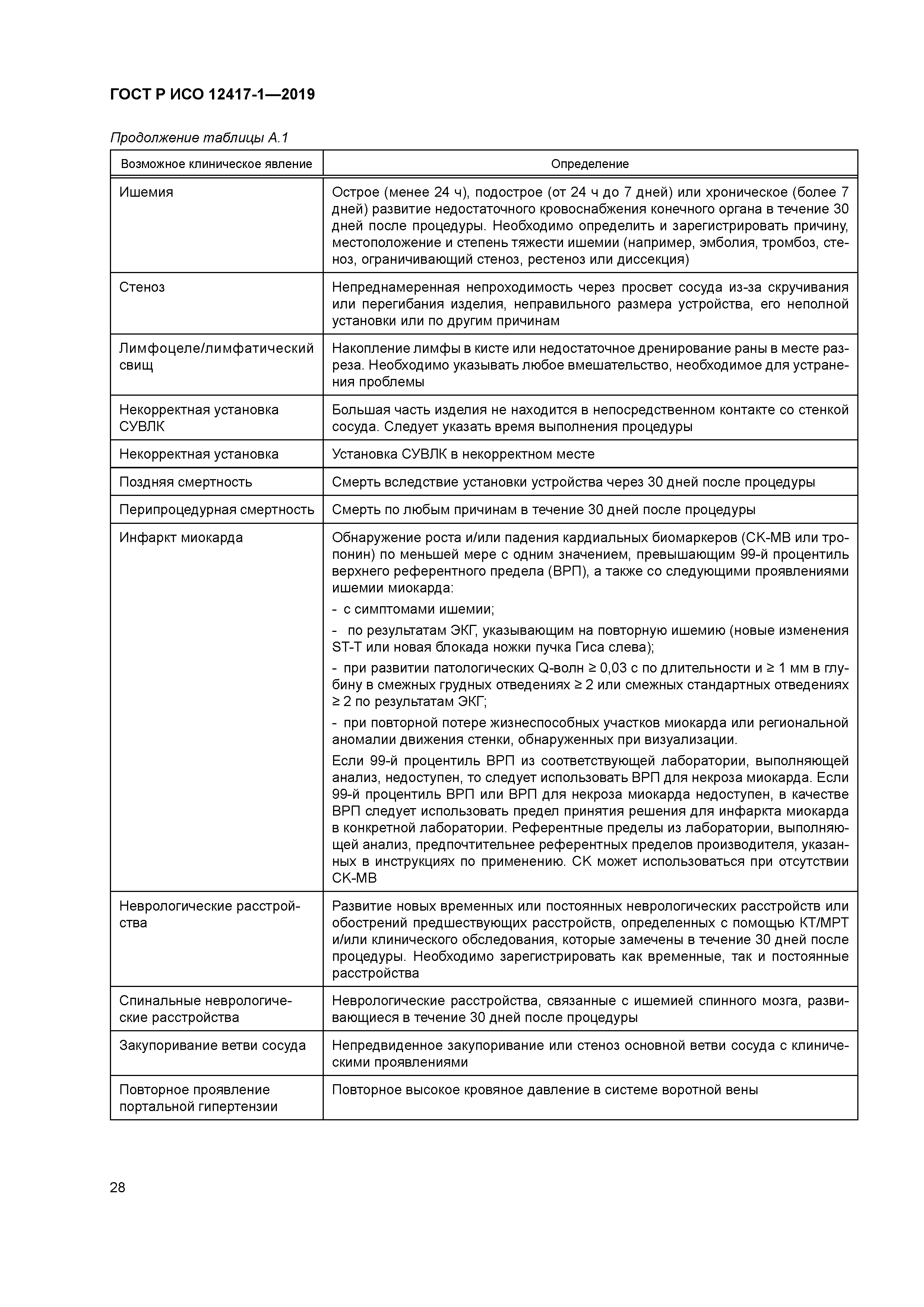
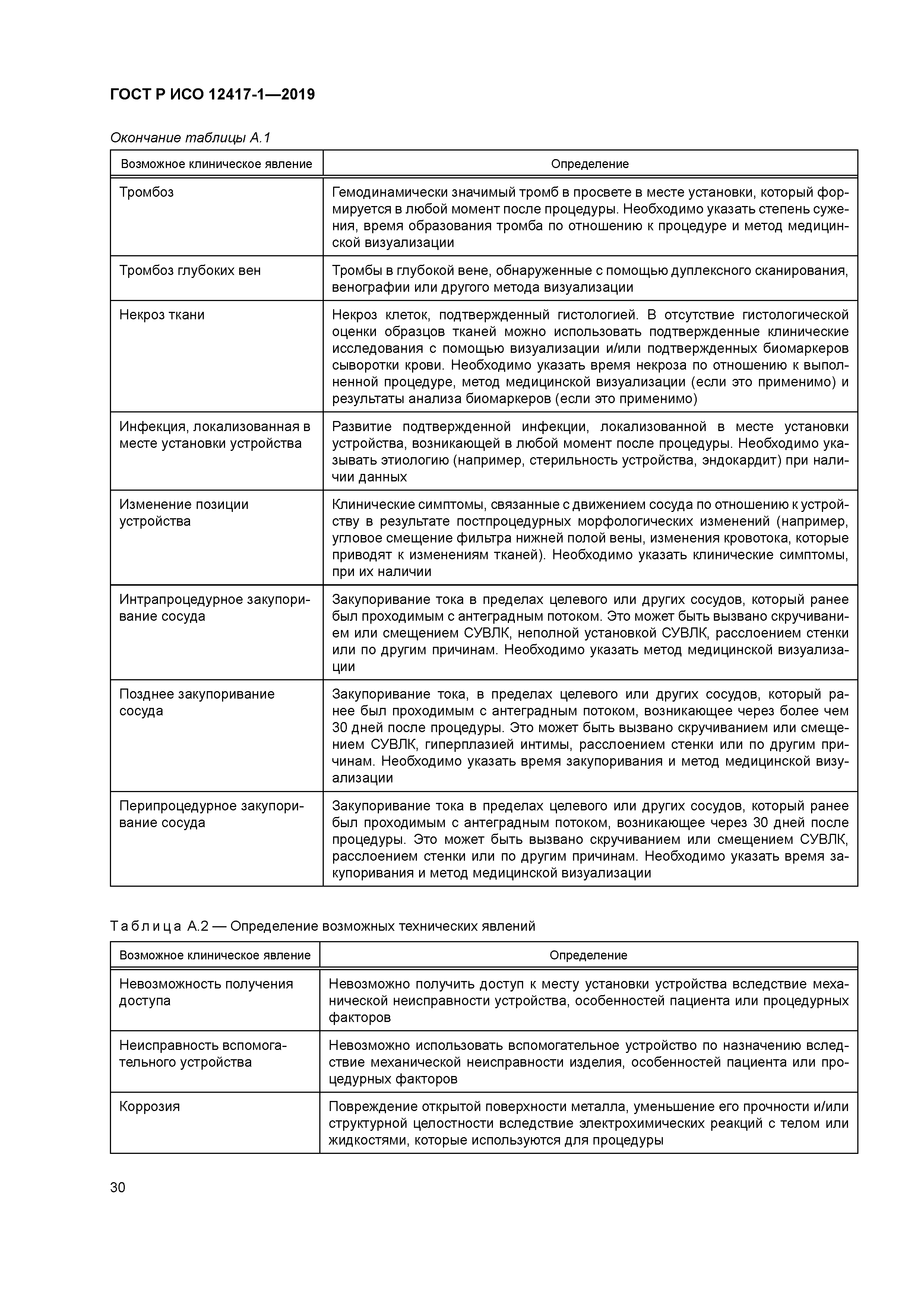
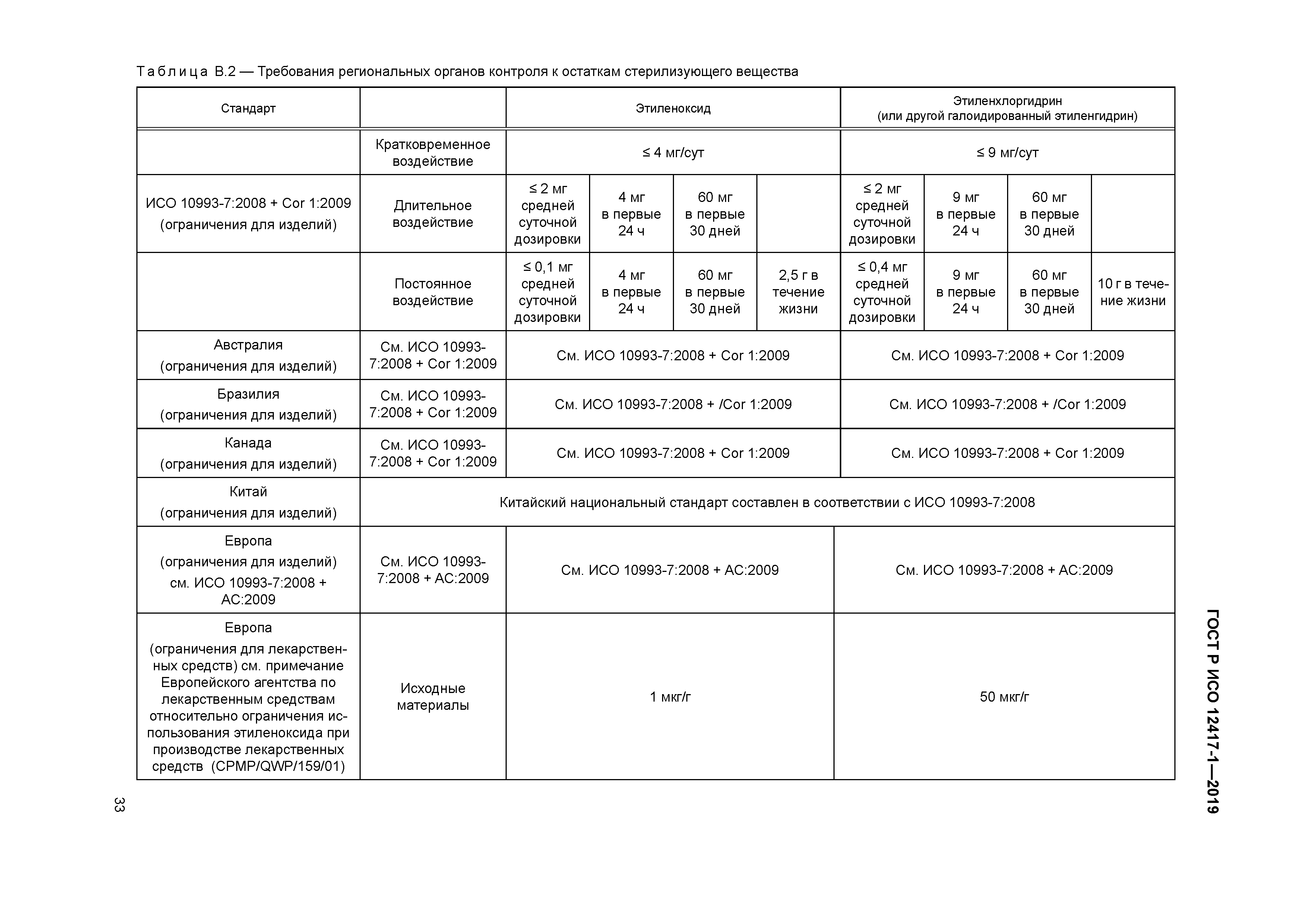
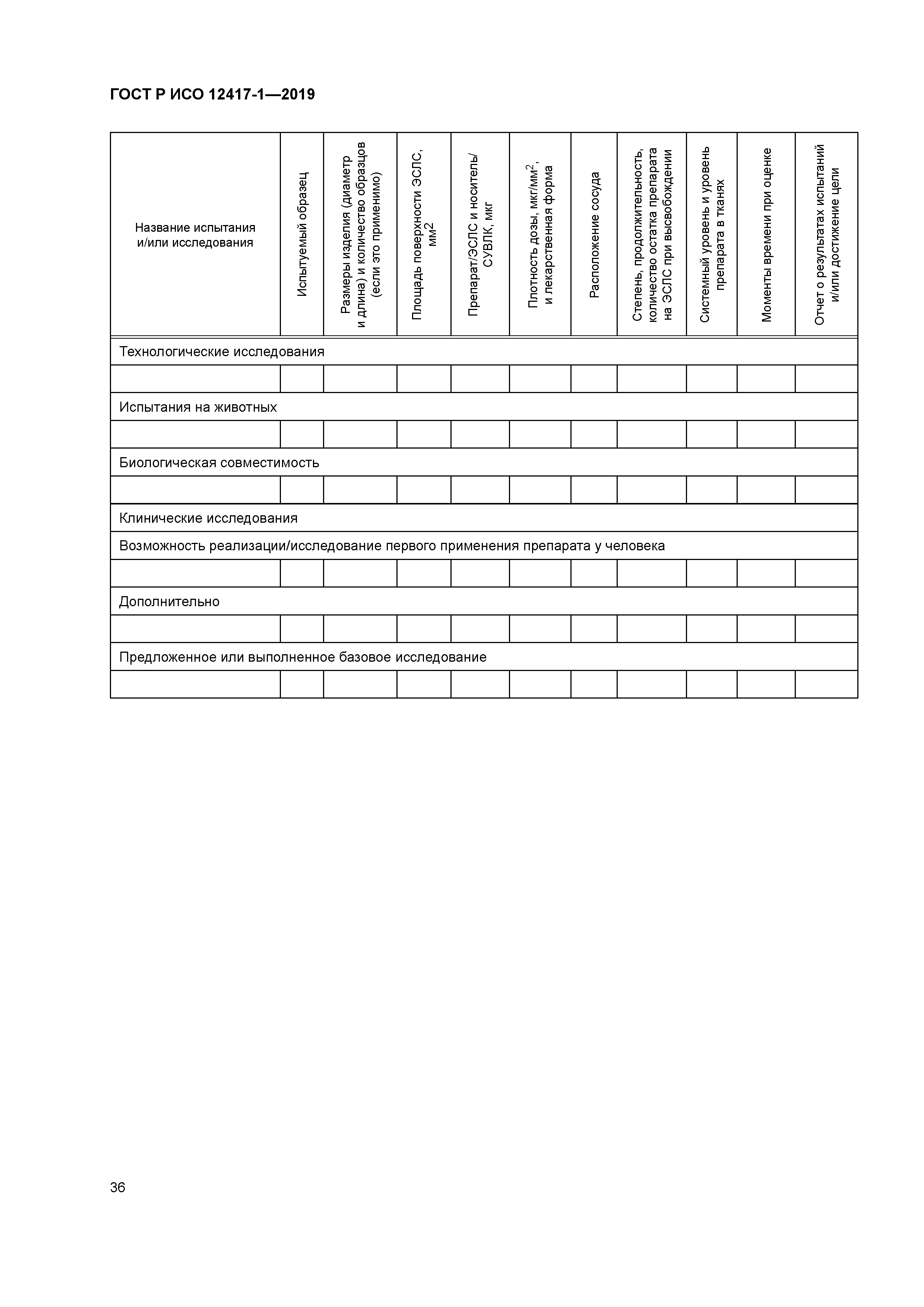
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Предполагаемое использование 4.1 Общая информация 4.2 Классификация 4.3 Предполагаемая клиническая локализация 5 Характеристики конструкции 5.1 Общая информация 5.2 Элемент СУВЛК, содержащий лекарственное средство (ЭСЛС) 6 Материалы 7 Оценка конструкции 7.1 Общая информация 7.2 Доклиническая оценка 7.3 Клиническая оценка 7.4 Послепродажный контроль 8 Производство 8.1 Общая информация 8.2 Представление отчетов о материалах и анализ АФИ 8.3 Анализ материалов и отчеты о вспомогательных веществах 8.4 Испытание выпуска партии СУВЛК 9 Стерилизация 9.1 Продукция, которая поставляется стерильной 9.2 Продукция, которая поставляется нестерильной 9.3 Остатки после стерилизации 10 Упаковка 10.1 Общая информация 10.2 Рекомендации по хранению СУВЛК 10.3 Влияние изменения температуры хранения и транспортирования на СУВЛК 11 Информация, предоставленная производителем 11.1 Общая информация 11.2 Маркировка 11.3 Инструкции по применению (ИПП) Приложение А (справочное) Определение возможных клинических и технических явлений Приложение В (справочное) Информация о местных органах контроля, выполняющих регистрацию СУВЛК Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным и межгосударственным стандартам Библиография |
| Разработан: | ФГУП СТАНДАРТИНФОРМ ООО ЦСД |
| Утверждён: | 08.08.2019 Федеральное агентство по техническому регулированию и метрологии (485-ст) |
| Издан: | Стандартинформ (2019 г. ) |
| Нормативные ссылки: |
|


































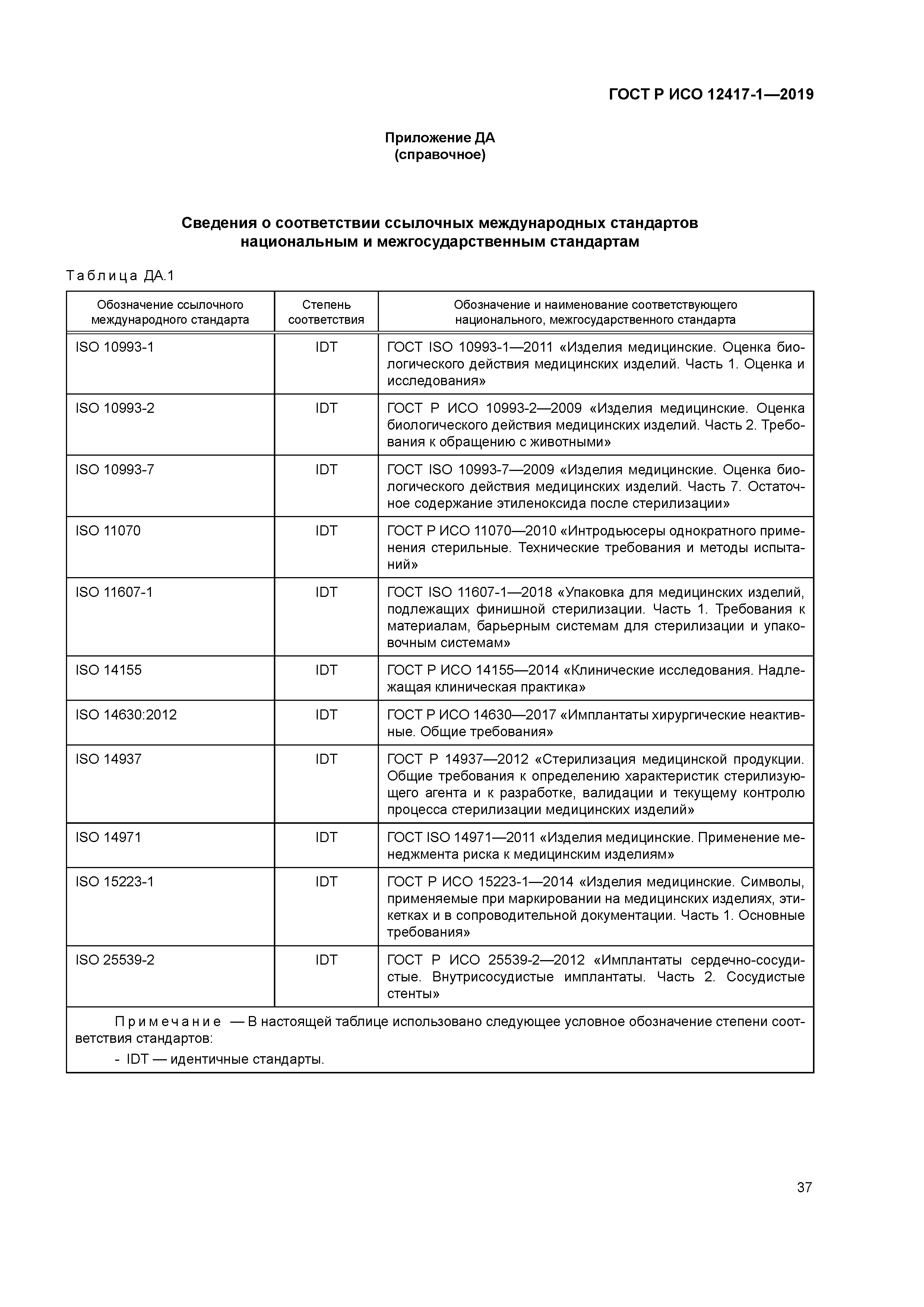








 ГОСТ Р ИСО 10993-2-2009 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 2. Требования к обращению с животными»
ГОСТ Р ИСО 10993-2-2009 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 2. Требования к обращению с животными»