СПРАВКА
Источник публикации
Документ опубликован не был
Примечание к документу
Текст документа приведен в соответствии с публикацией на сайте https://minzdrav.gov.ru/ по состоянию на 23.08.2023.
В соответствии с Приказом Минздрава России от 20.07.2023 N 377 данный документ введен в действие с 01.09.2023.
Название документа
"ФС.2.1.0315. Фармакопейная статья. Цефазолин натрия. Цефазолин"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание")
"ФС.2.1.0315. Фармакопейная статья. Цефазолин натрия. Цефазолин"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание")
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Цефазолин натрия Цефазолин Cefazolinum natricum | ФС |
Вводится впервые |
 | |
C14H13N8NaO4S3 [27164-46-1] | М.м. 476,49 |
(6R,7R)-3-{[(5-Метил-1,3,4-тиадиазол-2-ил)сульфанил]метил}-8-оксо-7-[2-(1H-тетразол-1-ил)ацетамидо]-5-тиа-1-азабицикло[4.2.0]окт-2-ен-2-карбоксилат натрия.
Содержит не менее 95,0% и не более 102,0% цефазолина натрия C14H13N8NaO4S3 в пересчете на безводное и свободное от остаточных органических растворителей вещество.
Полусинтетический антибиотик, производное продукта ферментации.
Описание. Белый или почти белый порошок.
<*> Очень гигроскопичен. Обладает полиморфизмом.
--------------------------------
<*> Приводится для информации.
Растворимость. Легко растворим в воде, очень мало растворим в спирте 96%, практически нерастворим в хлороформе.
1. ИК-спектрометрия (ОФС "Спектрометрия в средней инфракрасной области"). Инфракрасный спектр субстанции в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру фармакопейного стандартного образца цефазолина.
Испытуемый раствор. Растворяют 0,15 г субстанции в 5 мл воды, прибавляют 0,5 мл уксусной кислоты разведенной 12% и выдерживают на ледяной бане в течение 10 мин. Полученный раствор фильтруют и промывают осадок 2 мл воды. Осадок растворяют в смеси вода - ацетон 1:9, выпаривают на водяной бане почти досуха и сушат в сушильном шкафу при температуре 60 °C в течение 30 мин.
2. Качественная реакция. Субстанция должна давать характерную реакцию А на натрий (ОФС "Общие реакции на подлинность").
Удельное вращение. От -15 до -24 в пересчете на безводное вещество (5% раствор субстанции в воде, ОФС "Оптическое вращение").
Удельный показатель поглощения. От 260 до 300 в пересчете на безводное вещество при длине волны 272 нм (ОФС "Спектрофотометрия в ультрафиолетовой и видимой областях").
Испытуемый раствор. В мерную колбу вместимостью 100 мл помещают 0,1 г субстанции, растворяют в воде и доводят объем раствора тем же растворителем до метки. 2,0 мл полученного раствора помещают в мерную колбу вместимостью 100 мл и доводят объем раствора натрия гидрокарбоната раствором 4,2%.
Прозрачность раствора. Раствор 2,5 г субстанции в 25 мл воды, должен быть прозрачным (ОФС "Прозрачность и степень опалесценции (мутности) жидкостей").
Оптическая плотность. Оптическая плотность раствора, полученного в испытании "Прозрачность раствора", измеренная в кювете с толщиной слоя 1 см в максимуме поглощения при длине волны 430 нм, не должна превышать 0,15 (ОФС "Спектрофотометрия в ультрафиолетовой и видимой областях").
pH раствора. От 4,0 до 6,0 (раствор, полученный в испытании "Прозрачность раствора", ОФС "Ионометрия", метод 3).
Родственные примеси. Определение проводят методом ВЭЖХ (ОФС "Высокоэффективная жидкостная хроматография").
Подвижная фаза А (ПФА). Около 14,54 г динатрия гидрофосфата додекагидрата и около 3,53 г калия дигидрофосфата помещают в мерную колбу вместимостью 1000 мл, растворяют в воде и доводят объем раствора водой до метки.
Подвижная фаза Б (ПФБ). Ацетонитрил.
Испытуемый раствор. В мерную колбу вместимостью 20 мл помещают 50 мг субстанции, растворяют в ПФА и доводят объем раствора тем же растворителем до метки.
Раствор сравнения. В мерную колбу вместимостью 100 мл помещают 1,0 мл испытуемого раствора и доводят объем раствора ПФА до метки.
Раствор для проверки пригодности хроматографической системы. В мерную колбу вместимостью 20 мл помещают 20 мг субстанции, растворяют в 10 мл натрия гидроксида растворе 0,05 М и выдерживают в течение 30 мин. В мерную колбу вместимостью 20 мл помещают 1,0 мл полученного раствора и доводят объем раствора ПФА до метки.
Раствор для проверки чувствительности хроматографической системы. В мерную колбу вместимостью 10 мл помещают 0,5 мл раствора сравнения и доводят объем раствора ПФА до метки.
Примечание
Примесь L: (6R,7S)-3-{[(5-метил-1,3,4-тиадиазол-2-ил)сульфанил]метил}-8-оксо-7-[2-(1H-тетразол-1-ил)ацетамидо]-5-тиа-1-азабицикло[4.2.0]окт-2-ен-2-карбоновая кислота.
Хроматографические условия
Колонка | 125 x 4,0 мм, силикагель октадецилсилильный, эндкепированный, для хроматографии, 3 мкм; |
Температура колонки | 45 °C; |
Скорость потока | 1,2 мл/мин; |
Детектор | спектрофотометрический, 254 нм; |
Объем пробы | 5 мкл. |
Режим хроматографирования
Время, мин | ПФА, % | ПФБ, % |
0 - 2 | 98 | 2 |
2 - 4 |  |  |
4 - 10 |  | 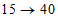 |
10 - 11,5 |  |  |
11,5 - 12 | 35 | 65 |
12 - 15 |  |  |
15 - 21 | 98 | 2 |
Хроматографируют раствор для проверки чувствительности хроматографической системы, раствор для проверки пригодности хроматографической системы, раствор сравнения и испытуемый раствор.
Относительное время удерживания соединений. Цефазолин - 1 (около 6,5 мин), примесь L - около 1,05.
Пригодность хроматографической системы. На хроматограмме раствора для проверки чувствительности хроматографической системы отношение сигнал/шум (S/N) для пика цефазолина должно быть не менее 10.
На хроматограмме раствора для проверки пригодности хроматографической системы:
- разрешение (RS) между пиками цефазолина и примеси L должно быть не менее 2,0;
- фактор асимметрии пика (AS) цефазолина должен быть не более 2,0.
Допустимое содержание примесей. На хроматограмме испытуемого раствора:
- площадь пика любой примеси не должна превышать площадь пика цефазолина на хроматограмме раствора сравнения (не более 1,0%);
- суммарная площадь пиков всех примесей не должна превышать 3,5-кратную площадь пика цефазолина на хроматограмме раствора сравнения (не более 3,5%).
Не учитывают пики, площадь которых менее площади пика цефазолина на хроматограмме раствора для проверки чувствительности хроматографической системы (менее 0,05%).
Вода. Не более 6,0% (ОФС "Определение воды", метод 2). Для определения используют 0,3 г (точная навеска) субстанции.
N,N-Диметиланилин. Не более 0,002%. (ОФС "N,N-Диметиланилин").
Остаточные органические растворители. В соответствии с ОФС "Остаточные органические растворители".
Аномальная токсичность. Субстанция должна быть нетоксичной (ОФС "Аномальная токсичность"). Тест-доза - 40 мг цефазолина в 0,5 мл воды для инъекций на мышь, внутривенно. Срок наблюдения - 48 ч.
Бактериальные эндотоксины. Не более 0,1 ЕЭ на 1 мг цефазолина (ОФС "Бактериальные эндотоксины").
Стерильность. Субстанция должна быть стерильной (ОФС "Стерильность").
Определение проводят методом ВЭЖХ (ОФС "Высокоэффективная жидкостная хроматография").
Раствор А. В мерную колбу вместимостью 1000 мл помещают 2,77 г динатрия гидрофосфата додекагидрата и 1,86 г лимонной кислоты, растворяют в воде и доводят объем раствора водой до метки.
Подвижная фаза (ПФ). Ацетонитрил - раствор А 100:900.
Испытуемый раствор. В мерную колбу вместимостью 50 мл помещают 50 мг (точная навеска) субстанции, растворяют в ПФ и доводят объем раствора тем же растворителем до метки.
Раствор стандартного образца цефазолина. В мерную колбу вместимостью 50 мл помещают 50 мг (точная навеска) фармакопейного стандартного образца цефазолина, растворяют в ПФ и доводят объем раствора тем же растворителем до метки.
Раствор для проверки разделительной способности хроматографической системы. В мерную колбу вместимостью 100 мл помещают около 5 мг фармакопейного стандартного образца цефуроксима натрия, растворяют в 10 мл раствора стандартного образца цефазолина и доводят объем раствора ПФ до метки.
Хроматографические условия
Колонка | 250 x 4,6 мм, силикагель октадецилсилильный, эндкепированный, для хроматографии, 5 мкм; |
Температура колонки | 25 °C; |
Скорость потока | 1,0 мл/мин; |
Детектор | спектрофотометрический, 270 нм; |
Объем пробы | 20 мкл. |
Хроматографируют раствор для проверки разделительной способности хроматографической системы, раствор стандартного образца цефазолина натрия и испытуемый раствор.
Пригодность хроматографической системы. На хроматограмме раствора для проверки разделительной способности хроматографической системы разрешение (RS) между пиками цефазолина и цефуроксима должно быть не менее 2,0.
На хроматограмме раствора стандартного образца цефазолина натрия:
- фактор асимметрии пика (AS) цефазолина должен быть не менее 0,8 и не более 3,0;
- относительное стандартное отклонение площади пика цефазолина должно быть не более 2,0% (6 введений).
Содержание цефазолина натрия C14H13N8NaO4S3 в субстанции в процентах (X) в пересчете на безводное и свободное от остаточных органических растворителей вещество вычисляют по формуле:
 ,
,где S1 - площадь пика цефазолина на хроматограмме испытуемого раствора;
S0 - площадь пика цефазолина на хроматограмме раствора стандартного образца цефазолина;
a1 - навеска субстанции, мг;
a0 - навеска фармакопейного стандартного образца цефазолина, мг;
W - суммарное содержание воды и остаточных органических растворителей в субстанции, %;
P - содержание цефазолина в фармакопейном стандартном образце цефазолина, %;
476,5 - молекулярная масса цефазолина натрия;
454,5 - молекулярная масса цефазолина.
В сухом, защищенном от света месте.