СПРАВКА
Источник публикации
Документ опубликован не был
Примечание к документу
Текст документа приведен в соответствии с публикацией на сайте https://minzdrav.gov.ru/ по состоянию на 15.08.2023.
В соответствии с Приказом Минздрава России от 20.07.2023 N 377 данный документ введен в действие с 01.09.2023.
Взамен ОФС.1.2.1.0004.15.
Название документа
"ОФС.1.2.1.0004. Общая фармакопейная статья. Ионометрия"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание)
"ОФС.1.2.1.0004. Общая фармакопейная статья. Ионометрия"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
Ионометрия | ОФС.1.2.1.0004 |
Взамен ОФС.1.2.1.0004.15 |
Метод ионометрии основан на измерении активности (концентрации) определяемых ионов с помощью ионоселективных (индикаторных) электродов. Ионоселективный электрод обладает избирательной чувствительностью к определенному виду ионов, от содержания которых зависит его потенциал. В основу ионометрии положен принцип потенциометрического анализа, заключающийся в измерении разности потенциалов (электродвижущей силы) индикаторного ионоселективного электрода и электрода сравнения, потенциал которого постоянен.
Зависимость электродвижущей силы электродной системы от активности потенциалопределяющего иона описывается уравнением Нернста:
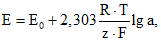 (1)
(1)где E - разность потенциалов между индикаторным ионселективным электродом и электродом сравнения (электродвижущая сила), мВ;
E0 - стандартное значение электродвижущей силы при a = 1, мВ;
R - универсальная газовая постоянная, Дж/(моль·К);
T - абсолютная температура, К;
F - число Фарадея, Кл/моль;
z - заряд определяемого иона;
a - активность или эффективная концентрация свободных ионов в растворе, связанная с концентрацией соотношением.
a = f·C, (2)
где C - молярная концентрация, моль/л;
f - коэффициент активности.
Для очень разбавленных растворов коэффициент активности близок к единице и активность ионов равна концентрации.
Если коэффициент активности поддерживается постоянным, уравнение Нернста принимает вид:
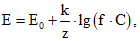 (3)
(3)где 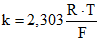 коэффициент, который означает изменение электродвижущей силы на единицу изменения lg a, и может быть рассчитан по формуле при любой температуре:
коэффициент, который означает изменение электродвижущей силы на единицу изменения lg a, и может быть рассчитан по формуле при любой температуре:
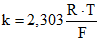 коэффициент, который означает изменение электродвижущей силы на единицу изменения lg a, и может быть рассчитан по формуле при любой температуре:
коэффициент, который означает изменение электродвижущей силы на единицу изменения lg a, и может быть рассчитан по формуле при любой температуре:k = [0,05916 + 0,000198·(t - 25 °C)]. (4)
Значения коэффициента k при различных температурах приведены в табл. 1.
Таблица 1
Температура, °C | k, вольт |
15 | 0,0572 |
20 | 0,0582 |
25 | 0,0592 |
30 | 0,0602 |
35 | 0,0611 |
Коэффициент активности f считается постоянным, если при измерениях во всех анализируемых и калибровочных растворах поддерживается одинаковая ионная сила. Для создания постоянной ионной силы к раствору прибавляют раствор индифферентного электролита (фоновый раствор) с концентрацией в 10 - 100 раз больше, чем суммарная концентрация других ионов в растворе, с тем, чтобы различные количества анализируемого иона не влияли на ионную силу раствора и коэффициент активности определяемого иона оставался постоянным.
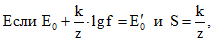
где S - крутизна электродной функции, то
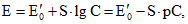 (5)
(5)где pC = -lg C.
Таким образом, при постоянной ионной силе раствора и постоянной температуре наблюдается линейная зависимость электродвижущей силы электродной системы от концентрации определяемого иона.
Измерение активности и концентрации ионов
Ионометрические измерения осуществляют с использованием иономера (высокоомного потенциометра с входным сопротивлением по крайней мере в 100 раз большим, чем сопротивление используемых электродов), который включает в себя электродную систему и измерительный преобразователь.
В качестве ионоселективных электродов используют различные электроды: с жидкой (пластифицированные электроды) или с твердой мембраной (монокристаллические, поликристаллические или стеклянные электроды); электроды с заряженными (положительно или отрицательно) или нейтральными подвижными носителями; сенсибилизированные электроды (электроды с ферментативной подложкой, газ-индикаторные электроды). Электродом сравнения служит, главным образом, хлорсеребряный электрод или каломельный электрод с соответствующими индифферентными соединительными жидкостями.
Показания прибора снимают в милливольтах или в единицах pX. Подготовка иономера к работе и проведение измерений проводят согласно инструкциям, прилагаемым к прибору. Измерения выполняют при постоянной температуре +/- 0,5 °C и постоянной ионной силе раствора.
Помещают электроды в испытуемый раствор и снимают установившееся показание при медленном и постоянном перемешивании.
При частых измерениях периодически проверяют стабильность отклика и линейность градуировочного графика в диапазоне концентраций испытуемого раствора. В противном случае проверку проводят перед каждым измерением.
Метод градуировочного графика заключается в построении графика зависимости электродвижущей силы электродной системы от логарифма концентрации стандартных растворов и последующем нахождении концентрации испытуемого раствора по измеренному в нем значению электродвижущей силы электродной системы. Градуировочный (калибровочный) график строится микропроцессором измерительного преобразователя автоматически на основе введенных в него значений электродвижущей силы электродной системы и соответствующих им значений pX при калибровке иономера в стандартных растворах (двух и более). Подбор концентраций стандартных растворов должен соответствовать диапазону концентраций испытуемых растворов: крайние значения концентраций испытуемых растворов должны находиться внутри линейной области калибровочного графика. Значение pX в испытуемом растворе находится автоматически с использованием градуировочного графика по измеренному значению электродвижущей силы электродной системы (E) - рис. 1.
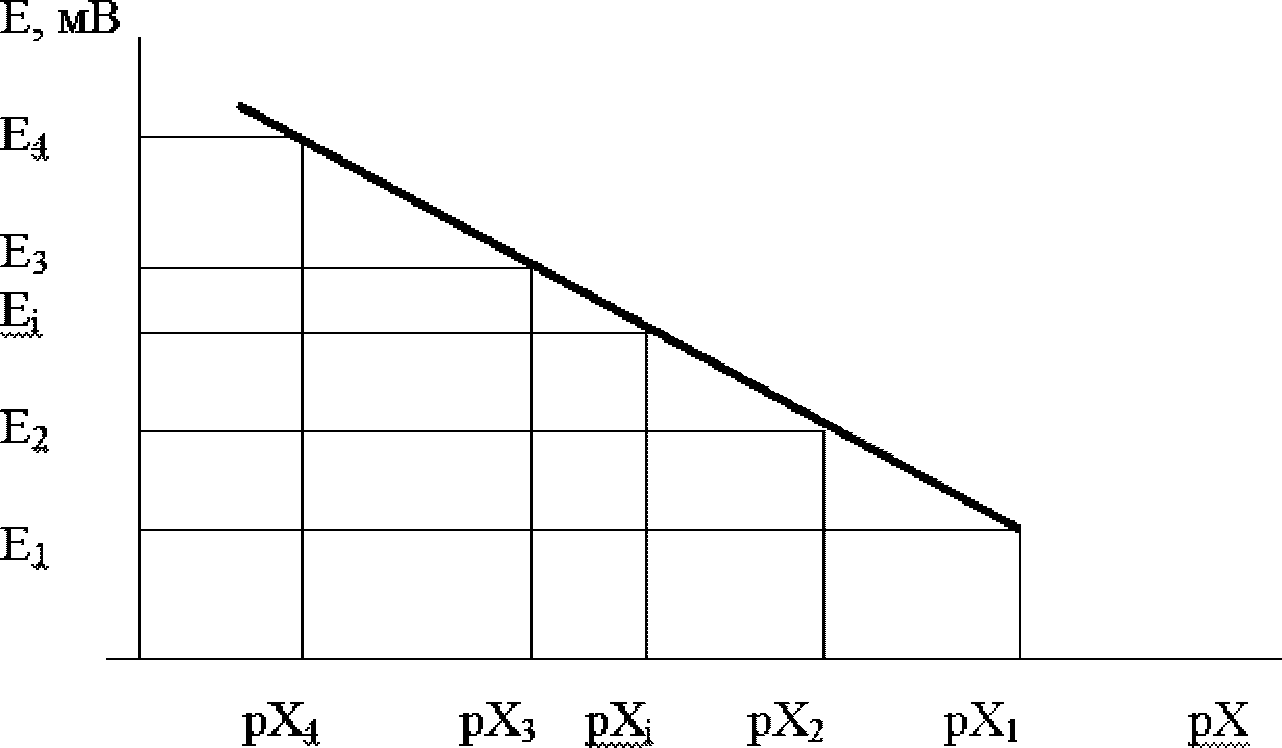
электродвижущей силы электродной системы от концентрации
потенциалопределяющего иона
Поскольку в разбавленных растворах pX = -lg C, значение молярной концентрации (моль/л) вычисляют по уравнению:
C = 10-pX. (6)
Значение массовой концентрации иона (г/л) рассчитывают исходя из уравнения:
C = M·10-pX, (7)
где M - молярная масса иона, г/моль.
При наличии влияния других компонентов испытуемого раствора на потенциал ионоселективного электрода используют метод стандартных добавок.
Метод применим в линейных областях калибровочной кривой.
В испытуемый раствор объемом V, приготовленный как указано в фармакопейной статье, вводят несколько (не менее трех) порций объемом V0 (V0 <= 0,01V) раствора с известной концентрацией определяемого иона, соблюдая условие неизменной ионной силы в растворе. Измеряют потенциал до и после каждой добавки, и вычисляют разность 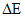 между потенциалом, измеренным после прибавления раствора с известной концентрацией, и исходным потенциалом испытуемого раствора. Полученная величина связана с концентрацией определяемого иона уравнением:
между потенциалом, измеренным после прибавления раствора с известной концентрацией, и исходным потенциалом испытуемого раствора. Полученная величина связана с концентрацией определяемого иона уравнением:
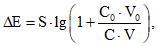 (8)
(8)или
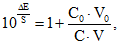 (9)
(9)где V - объем испытуемого раствора, л;
C - молярная концентрация определяемого иона в испытуемом растворе, моль/л;
V0 - добавленный объем стандартного раствора, л;
C0 - концентрация определяемого иона в стандартном растворе, моль/л;
S - крутизна электродной функции, определяемая экспериментально при постоянной температуре измерением разности потенциалов двух стандартных растворов, концентрации которых отличаются в 10 раз и соответствуют линейной области калибровочной кривой, мВ.
Строят график зависимости 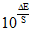 от объема добавки V0 и экстраполируют полученную прямую до пересечения с осью абсцисс. В точке пересечения концентрация испытуемого раствора определяемого иона выражается уравнением:
от объема добавки V0 и экстраполируют полученную прямую до пересечения с осью абсцисс. В точке пересечения концентрация испытуемого раствора определяемого иона выражается уравнением:
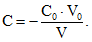 (10)
(10)К объему V испытуемого раствора, приготовленного как описано в фармакопейной статье, прибавляют объем V0 стандартного раствора с концентрацией C0. Контрольный раствор готовят в тех же условиях. Измеряют потенциалы испытуемого и контрольного раствора до и после прибавления стандартного раствора. Вычисляют концентрацию С анализируемого иона, используя следующее уравнение и делая необходимые поправки на контрольный раствор:
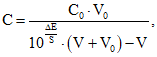 (11)
(11)где V - объем испытуемого или контрольного раствора, л;
C - концентрация определяемого иона в испытуемом растворе, моль/л;
V0 - добавленный объем стандартного раствора, л;
C0 - концентрация определяемого иона в стандартном растворе, моль/л;
S - крутизна электродной функции, определяемая экспериментально при постоянной температуре измерением разности потенциалов двух стандартных растворов, концентрации которых отличаются в 10 раз и соответствуют линейной области калибровочной кривой, мВ;
Водородным показателем pH, характеризующим концентрацию ионов водорода в водных растворах, называют отрицательный десятичный логарифм активности ионов водорода
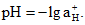 (12)
(12)Потенциометрическое определение pH заключается в измерении электродвижущей силы электродной системы, где в качестве ионоселективного электрода используют чувствительный к ионам водорода электрод (обычно стеклянный), в качестве электрода сравнения - стандартный электрод с известной величиной потенциала (насыщенный каломельный или хлорсеребряный электроды). На практике для измерения pH применяют метод градуировочного графика. pH испытуемого раствора связан с pH стандартного раствора следующим уравнением:
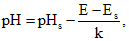 (13)
(13)где E - потенциал электрода в испытуемом растворе, мВ;
Es - потенциал того же электрода в растворе с известным значением pH (стандартном растворе), мВ;
k - коэффициент, который означает изменения электродвижущей силы на единицу изменения pH, мВ;
pHs - pH стандартного раствора.
Оборудование. В качестве прибора для потенциометрического определения pH используют иономеры или pH-метры с чувствительностью не менее 0,05 единиц pH или 3 мВ. Калибровку приборов проводят по стандартным буферным растворам.
Методика. Все измерения проводят при одной и той же температуре в интервале от 20 до 25 °C, если нет других указаний в фармакопейной статье. В табл. 2 приведена зависимость значений pH от температуры для различных стандартных буферных растворов, используемых для калибровки прибора. Для приготовления указанных растворов могут быть использованы стандарт-титры для приготовления буферных растворов - рабочих эталонов pH промышленного производства.
Таблица 2
Температура, °C | 15 | 20 | 25 | 30 | 35 | |
0,05 М раствор калия тетраоксалата | 1,67 | 1,68 | 1,68 | 1,68 | 1,69 | 0,001 |
Насыщенный при 25 °C раствор калия гидротартрата | 3,56 | 3,55 | 3,55 | -0,0014 | ||
0,05 М раствор калия дигидроцитрата | 3,80 | 3,79 | 3,78 | 3,77 | 3,76 | -0,0022 |
0,05 М раствор калия гидрофталата | 4,00 | 4,00 | 4,01 | 4,02 | 4,02 | 0,0012 |
0,025 М раствор калия фосфата и однозамещенного 0,025 М раствор динатрия гидрофосфата безводного | 6,90 | 6,88 | 6,87 | 6,85 | 6,84 | -0,0028 |
0,0087 М раствор калия фосфата однозамещенного и 0,0303 М раствор динатрия гидрофосфата безводного | 7,45 | 7,43 | 7,41 | 7,40 | 7,39 | -0,0028 |
0,01 М раствор натрия тетрабората | 9,28 | 9,23 | 9,18 | 9,14 | 9,10 | -0,0082 |
0,025 М раствор натрия карбоната и 0,025 М раствор натрия гидрокарбоната | 10,12 | 10,06 | 10,01 | 9,97 | 9,93 | -0,0096 |
Насыщенный при 25 °C раствор кальция гидроксида | 12,81 | 12,63 | 12,45 | 12,29 | 12,29 | -0,034 |
Прибор калибруют при помощи буферного раствора калия гидрофталата (первичный стандарт) и одного из буферных растворов с другим значением pH (табл. 2). Показания прибора для третьего буферного раствора с промежуточным значением pH не должны отличаться больше, чем на 0,05 единиц pH от табличного значения pH этого раствора. Электроды прибора погружают в испытуемый раствор и измеряют pH в тех же условиях, что и для буферных растворов.
Все испытуемые растворы и стандартные буферные растворы должны быть приготовлены на воде очищенной, не содержащей углерода диоксид, для чего перед употреблением ее необходимо прокипятить. Вода, не содержащая углерода диоксид, должна иметь pH 5,8 - 7,0.
Приготовление стандартных буферных растворов
0,05 М раствор калия тетраоксалата. 12,61 г KC4H3O8·2H2O растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл.
Насыщенный при 25 °C раствор калия гидротартрата. Избыток KC4H5O6 энергично встряхивают с водой при температуре 25 °C в течение 30 мин. Фильтруют или декантируют. Раствор используют свежеприготовленным.
0,05 М раствор калия дигидроцитрата. 11,41 г KC6H7O7 растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл. Раствор используют свежеприготовленным.
0,05 М раствор калия гидрофталата. 10,13 г KC8H5O4, предварительно высушенного при температуре от 110 до 135 °C до постоянной массы, растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл.
0,025 М раствор калия фосфата однозамещенного и 0,025 М раствор динатрия гидрофосфата безводного. 3,39 г KH2PO4 и 3,53 г NaHPO4, предварительно высушенных в течение двух часов при температуре от 110 до 130 °C до постоянной массы, растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл.
0,0087 М раствор калия фосфата однозамещенного и 0,0303 М раствор динатрия гидрофосфата безводного. 1,18 г KH2PO4 и 4,30 г NaHPO4, предварительно высушенных при температуре от 110 до 130 °C, растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл.
0,01 М раствор натрия тетрабората. 3,80 г Na2B4O7·10H2O растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл. Хранят, защищая от углерода диоксида.
0,025 М раствор натрия карбоната и 0,025 М раствор натрия гидрокарбоната. 2,64 г Na2CO3 и 2,09 г NaHCO3 растворяют в воде и доводят объем раствора тем же растворителем до 1000,0 мл.
При измерении pH в неводных и смешанных растворителях, а также в некоторых коллоидных системах, следует иметь в виду, что полученные значения pH являются условными.
Примечание - Буферные растворы хранят в хорошо закрытых флаконах нейтрального стекла в течение 3 мес. При образовании осадков и видимых изменений буферные растворы не подлежат использованию.