СПРАВКА
Источник публикации
М.: ИПК Издательство стандартов, 1998
Примечание к документу
Документ утратил силу с 1 июля 2019 года в связи с изданием Приказа Росстандарта от 27.06.2018 N 366-ст. Взамен введен в действие ГОСТ 34410-2018.
Документ включен в Перечень стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента Таможенного союза "Технический регламент на соковую продукцию из фруктов и овощей" (ТР ТС 023/2011) и осуществления оценки (подтверждения) соответствия продукции (Решение Комиссии Таможенного союза от 09.12.2011 N 882).
Документ включен в Перечень национальных стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения Федерального закона "Технический регламент на соковую продукцию из фруктов и овощей" и осуществления оценки соответствия (Распоряжение Правительства РФ от 19.05.2009 N 690-р).
С 1 июля 2003 года до вступления в силу технических регламентов акты федеральных органов исполнительной власти в сфере технического регулирования носят рекомендательный характер и подлежат обязательному исполнению только в части, соответствующей целям, указанным в пункте 1 статьи 46 Федерального закона от 27.12.2002 N 184-ФЗ.
Документ введен в действие с 1 июля 1998 года.
Название документа
"ГОСТ Р 51128-98. Государственный стандарт Российской Федерации. Соки фруктовые и овощные. Метод определения D-изолимонной кислоты"
(принят и введен в действие Постановлением Госстандарта России от 19.01.1998 N 6)
"ГОСТ Р 51128-98. Государственный стандарт Российской Федерации. Соки фруктовые и овощные. Метод определения D-изолимонной кислоты"
(принят и введен в действие Постановлением Госстандарта России от 19.01.1998 N 6)
Содержание
Постановлением Госстандарта России
от 19 января 1998 г. N 6
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
СОКИ ФРУКТОВЫЕ И ОВОЩНЫЕ
МЕТОД ОПРЕДЕЛЕНИЯ D-ИЗОЛИМОННОЙ КИСЛОТЫ
Fruit and vegetable juices. Method for determination
of D-isocitric acid
ГОСТ Р 51128-98
Группа Н59
ОКС 67.080;
ОКСТУ 9109
Дата введения
1 июля 1998 года
1. Разработан Московской государственной академией пищевых производств, Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности.
Внесен Техническим комитетом ТК 335 "Методы испытаний агропромышленной продукции на безопасность".
2. Принят и введен в действие Постановлением Госстандарта России от 19 января 1998 г. N 6.
3. Разделы настоящего стандарта за исключением 2; 5; 6; 8.2; 9 представляют собой аутентичный текст европейского стандарта ЕН 1139-94 "Фруктовые и овощные соки. Ферментативное определение содержания D-изолимонной кислоты. Спектрофотометрическое определение никотинамида-дениндинуклеотидфосфата (НАДФH)".
4. Введен впервые.
Настоящий стандарт распространяется на фруктовые и овощные соки, нектары и сокосодержащие напитки и устанавливает метод определения D-изолимонной кислоты в виде свободной кислоты или ее соли, включая эфиры и лактоны.
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 1770-74. Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия
ГОСТ 2603-79. Ацетон. Технические условия
ГОСТ 3118-77. Кислота соляная. Технические условия
ГОСТ 3760-79. Аммиак водный. Технические условия
ГОСТ 4108-72. Барий хлорид 2-водный. Технические условия
ГОСТ 4166-76. Натрий сернокислый. Технические условия
ГОСТ 4328-77. Натрий гидроокись. Технические условия
ГОСТ 6259-75. Глицерин. Технические условия
ГОСТ 6709-72. Вода дистиллированная. Технические условия
ГОСТ 10652-77. Этилендиаминтетрауксусной кислоты динатриевая соль. Технические условия
ГОСТ 12026-76. Бумага фильтровальная лабораторная. Технические условия
ГОСТ 26313-84. Продукты переработки плодов и овощей. Правила приемки, методы отбора проб
ГОСТ 26671-85. Продукты переработки плодов и овощей, консервы мясные и мясорастительные. Подготовка проб для лабораторных анализов
ГОСТ 29227-91. Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
3.1. В настоящем стандарте применяют следующие термины с соответствующими определениями:
Массовая концентрация D-изолимонной кислоты во фруктовых и овощных соках, нектарах и сокосодержащих напитках: массовая концентрация D-изолимонной кислоты, определенная в соответствии с методикой, установленной настоящим стандартом, выраженная в мг/дм3.
3.2. В настоящем стандарте применяют следующие сокращения:
ИЦДГ - изоцитратдегидрогеназа, ЕС 1.1.1.42 [1];
НАДФ - никотинамидадениндинуклеотидфосфат, окисленная форма;
НАДФH - никотинамидадениндинуклеотидфосфат, восстановленная форма;
E - стандартная единица, определяет количество (активность) фермента, которое служит катализатором при 25 °C для превращения 1 мкмоля вещества в минуту.
Метод основан на осаждении D-изолимонной кислоты в виде соли бария, перерастворении соли, ферментативном декарбоксилировании иона цитрата под действием НАДФ в присутствии ИЦДГ, фотометрическом измерении количества образовавшегося НАДФH, эквивалентного количеству D-изолимонной кислоты.
В ходе анализа протекают следующие ферментативные реакции:
 . (1)
. (1)РЕАКТИВЫ И МАТЕРИАЛЫ
Спектрофотометр, позволяющий проводить исследования при длине волны 340 нм, или фотометр фотоэлектрический шириной спектральной полосы не более 10 нм и допустимой абсолютной погрешностью измерений коэффициента пропускания не более 1%, или спектрофотометр на ртутной лампе, позволяющий проводить измерения при длинах волн 365 или 334 нм.
Кюветы из оптического стекла или полистироловые рабочей длиной 10 мм.
Иономер или pH-метр с погрешностью измерения не более 0,05 pH.
Электрод для измерения pH стеклянный.
Электрод сравнения (каломельный).
Пипетки по ГОСТ 29227 типа 3, исполнения 1, 1-го класса точности, вместимостью 1 и 10 см3.
Дозаторы пипеточные объемами 1, 0,2 и 0,02 см3 относительной погрешностью дозирования +/- 1% [2].
Колба мерная по ГОСТ 1770, исполнения 2, вместимостью 50 см3.
Центрифуга лабораторная, обеспечивающая увеличение ускорения свободного падения при центрифугировании в 3000 раз.
Стаканы для центрифугирования вместимостью 100 см3.
Фильтры бумажные обеззоленные марки ФОМ по ГОСТ 12026.
Баня водяная [3].
Кислота D-изолимонная по НД [4], раствор массовой концентрации  .
.
 .
.Кислота соляная по ГОСТ 3118, х.ч., раствор молярной концентрации c (HCl) = 4 моль/дм3.
Аммиак водный по ГОСТ 3760, ч.д.а.
Ацетон по ГОСТ 2603, ч.д.а.
Барий хлористый 2-водный по ГОСТ 4108, х.ч., раствор массовой концентрации  .
.
 .
.Натрия гидроокись по ГОСТ 4328, ч.д.а., раствор молярной концентрации c (NaOH) = 4 моль/дм3.
Натрий сернокислый по ГОСТ 4166, ч.д.а., раствор массовой концентрации  .
.
 .
.Марганец (II) сернокислый [5], раствор массовой концентрации  .
.
 .
.Этилендиаминтетрауксусной кислоты динатриевая соль 2-водная по ГОСТ 10652, ч.д.а.
Трис(гидроксиметил)аминометан [6], х.ч.
Глицерин по ГОСТ 6259.
НАДФ (динатриевая соль) по [4].
ИЦДГ [4].
Вода дистиллированная по ГОСТ 6709.
Допускается применять другие средства измерений с метрологическими характеристиками, вспомогательные устройства с техническими характеристиками, а также реактивы по качеству не ниже перечисленных.
Отбор проб - по ГОСТ 26313, подготовка их к испытанию - по ГОСТ 26671.
6.1. Выделение D-изолимонной кислоты из фруктового и овощного сока, нектаров и сокосодержащих напитков
В стакане для центрифугирования 10 см3 исследуемого образца смешивают с 5 см3 раствора гидроокиси натрия. Раствор выдерживают в течение 10 мин при температуре от 20 до 25 °C. После добавления 5 см3 соляной кислоты объем раствора доводят водой до 25 см3. Последовательно приливают 2 см3 раствора аммиака, 3 см3 раствора хлористого бария и 20 см3 ацетона и хорошо перемешивают стеклянной палочкой. Раствор выдерживают в течение 10 мин, затем в течение 5 мин центрифугируют. Надосадочную жидкость осторожно декантируют, осадок в стакане для центрифугирования растворяют в 20 см3 раствора сернокислого натрия, помешивая стеклянной палочкой. Для ускорения растворения осадка стакан помещают на кипящую водяную баню и выдерживают в течение 10 мин при неоднократном перемешивании. После охлаждения до температуры от 20 до 25 °C раствор количественно переносят в мерную колбу вместимостью 50 см3 и доводят буферным раствором до метки. Из мерной колбы раствор переносят в колбу Эрленмейера, содержащую 1 г активированного угля, выдерживают в течение 5 мин и фильтруют через складчатый бумажный фильтр. Прозрачный, бесцветный фильтрат используют для ферментативного определения D-изолимонной кислоты.
6.2. Выделение D-изолимонной кислоты из концентратов фруктовых и овощных соков, нектаров и сокосодержащих напитков
Перед выделением D-изолимонной кислоты концентрат разводят водой до содержания сухих веществ по рецептуре натурального сока, нектара или сокосодержащего напитка. Далее выделение D-изолимонной кислоты проводят по 6.1.
7.1. Приготовление буферного раствора активной кислотностью 7,0 pH
2,42 г трис(гидроксиметил)аминометана и 35 мг динатриевой соли этилендиаминтетрауксусной кислоты (дигидрата) растворяют в 80 см3 воды, значение pH раствора доводят с помощью соляной кислоты до 7,0 и объем доводят до 100 см3. Буферный раствор устойчив при температуре 4 °C в течение 1 г.
7.2. Приготовление буферного раствора активной кислотностью 7,4 pH
2,42 г трис(гидроксиметил)аминометана и 35 мг динатриевой соли этилендиаминтетрауксусной кислоты (дигидрата) растворяют в 80 см3 воды, значение pH раствора доводят с помощью соляной кислоты до 7,4, затем объем раствора доводят дистиллированной водой до 100 см3. Буферный раствор устойчив при температуре 4 °C в течение 1 г.
7.3. Приготовление раствора НАДФ
50 мг динатриевой соли НАДФ растворяют в 5 см3 воды. Раствор устойчив при температуре 4 °C в течение четырех недель.
7.4. Приготовление раствора ИЦДГ
10,0 мг лиофилизата ИЦДГ из свиного сердца растворяют в 1 см3 (20 E/см3) глицерина. Раствор устойчив при температуре 4 °C в течение 6 мес.
Анализ проводят при температуре от 20 до 25 °C.
При проведении испытания количество реактивов задают в см3, а результаты пересчитывают на 1 дм3 пробы.
Для дозирования исследуемой пробы и растворов используют пипетки с делениями или пипеточные дозаторы.
Растворы ферментов, коферментов и буфера вносят соответствующими пипеточными дозаторами.
Ферментативное определение D-изолимонной кислоты может быть проведено также с использованием имеющихся в продаже специальных наборов реактивов.
В кювету спектрофотометра вносят 2,0 см3 буферного раствора активной кислотностью 7,4 pH, 0,1 см3 раствора сульфата марганца, 0,1 см3 раствора НАДФ и 1,00 см3 исследуемого раствора пробы, подготовленного по разделу 6. Смесь перемешивают, выдерживают в течение 3 мин и измеряют оптическую плотность раствора -  относительно воздуха.
относительно воздуха.
 относительно воздуха.
относительно воздуха.К подготовленному в кювете по 8.1 раствору добавляют 0,01 см3 раствора ИЦДГ. Раствор перемешивают. Через 10 мин (окончание реакции) измеряют оптическую плотность  раствора относительно воздуха.
раствора относительно воздуха.
 раствора относительно воздуха.
раствора относительно воздуха.Через 5 мин проводят контрольное измерение. Если оптическая плотность меняется, измерения проводят каждые следующие 5 мин до тех пор, пока не будет достигнута постоянная величина ее приращения. В этом случае оптическую плотность раствора  определяют экстраполяцией на момент внесения раствора ИЦДГ.
определяют экстраполяцией на момент внесения раствора ИЦДГ.
 определяют экстраполяцией на момент внесения раствора ИЦДГ.
определяют экстраполяцией на момент внесения раствора ИЦДГ.8.3. Контрольное испытание
Контрольное испытание проводят параллельно с основным. В кювету спектрофотометра вносят 3,0 см3 буферного раствора активной кислотностью 7,4 pH и 0,1 см3 раствора НАДФ. Смесь перемешивают, выдерживают в течение 3 мин и измеряют оптическую плотность  относительно воздуха.
относительно воздуха.
 относительно воздуха.
относительно воздуха.К подготовленному в кювете раствору добавляют 0,01 см3 раствора ИЦДГ, перемешивают и через 10 мин измеряют оптическую плотность раствора  , как в 8.2.
, как в 8.2.
 , как в 8.2.
, как в 8.2.Основой данного метода является линейная зависимость между образующимся количеством НАДФH и количеством D-изолимонной кислоты.
Разность измеренных оптических плотностей  вычисляют по формуле
вычисляют по формуле
 . (2)
. (2)Массовую концентрацию D-изолимонной кислоты в пробе X, мг/дм3, вычисляют по формуле
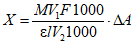 , (3)
, (3)где M - молярная масса D-изолимонной кислоты, M = 192,1 г/моль;
F - фактор разведения пробы в процессе выделения D-изолимонной кислоты, рассчитываемый как отношение объема разведенной пробы к объему, взятому для разведения;
при 340 нм -  ,
,
 ,
,при 365 нм -  (ртутная лампа),
(ртутная лампа),
 (ртутная лампа),
(ртутная лампа),при 334 нм -  (ртутная лампа);
(ртутная лампа);
 (ртутная лампа);
(ртутная лампа);l - рабочая длина кюветы, см;
Для указанных в прописи объемов растворов массовую концентрацию D-изолимонной кислоты в пробе X, мг/дм3, вычисляют по формуле
 . (4)
. (4)При использовании имеющихся в продаже наборов реактивов численный коэффициент (3083) в формуле (4) может быть иным из-за изменения суммарного объема раствора в кювете  .
.
При анализе концентратов соков, продуктов с высокой вязкостью и/или очень большим содержанием мякоти результаты испытаний могут быть выражены как массовая доля D-изолимонной кислоты в пробе  ,
,  , по формуле
, по формуле
 , (5)
, (5)где V - объем разведенного концентрата сока, продукта с высокой вязкостью и/или очень большим содержанием мякоти, см3;
m - масса концентрата сока, продукта с высокой вязкостью и/или очень большим содержанием мякоти, взятых для разведения, г.
За окончательный результат испытания принимают среднее арифметическое значение результатов двух параллельных определений, округленное до целого значения.
Абсолютное расхождение между результатами двух параллельных определений, выполненных в одной лаборатории, не должно превышать более чем в 5% случаев значения показателя сходимости d = 2,5 мг/дм3.
Абсолютное расхождение между результатами двух измерений, выполненных в двух лабораториях, не должно превышать более чем в 5% случаев значение показателя воспроизводимости D = 4,4 мг/дм3.
Достоверность получаемых результатов рекомендуется контролировать с помощью стандартного раствора D-изолимонной кислоты массовой концентрации не более 500 мг/дм3, который испытывают по 8.1 - 8.2 без предварительного разведения.
Если массовая концентрация D-изолимонной кислоты, определенная в результате испытания, составляет менее 95% концентрации стандартного раствора, то испытание повторяют со свежеприготовленными растворами реактивов.
В отчете об испытании должны быть указаны:
- обозначение настоящего стандарта;
- дата и способ отбора проб (если это возможно);
- дата доставки образца;
- дата проведения анализа;
- результаты исследования;
- обнаруженные в ходе исследования особенности;
- все рабочие условия, не установленные данным стандартом или касающиеся как необязательных, так и любых других подробностей, которые могут повлиять на конечный результат.
В отчете должны быть указаны все детали, необходимые для полной идентификации пробы.
(информационное)
БИБЛИОГРАФИЯ
союза по номенклатуре и классификации ферментов, а также единицам
ферментов и символам кинетики ферментативных реакций. М. 1979
или с огневым подогревом
und Lebensmitteleanalytik mit Tesl-Combinationen