СПРАВКА
Источник публикации
М.: ФГБУ "Институт стандартизации", 2025
Примечание к документу
Документ вводится в действие с 01.09.2025.
Взамен ГОСТ Р ИСО 22442-1-2011.
Название документа
"ГОСТ Р ИСО 22442-1-2025. Национальный стандарт Российской Федерации. Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Применение менеджмента риска"
(утв. и введен в действие Приказом Росстандарта от 17.04.2025 N 310-ст)
"ГОСТ Р ИСО 22442-1-2025. Национальный стандарт Российской Федерации. Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Применение менеджмента риска"
(утв. и введен в действие Приказом Росстандарта от 17.04.2025 N 310-ст)
Содержание
Приказом Федерального
агентства по техническому
регулированию и метрологии
от 17 апреля 2025 г. N 310-ст
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ, ИСПОЛЬЗУЮЩИЕ ТКАНИ И ИХ ПРОИЗВОДНЫЕ
ЖИВОТНОГО ПРОИСХОЖДЕНИЯ
ЧАСТЬ 1
ПРИМЕНЕНИЕ МЕНЕДЖМЕНТА РИСКА
Medical devices utilizing animal tissues and their
derivatives. Part 1. Application of risk management
(ISO 22442-1:2020, IDT)
ГОСТ Р ИСО 22442-1-2025
ОКС 11.100.20
Дата введения
1 сентября 2025 года
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией "Институт медико-биологических исследований и технологий" (АНО "ИМБИИТ") на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 422 "Оценка биологического действия медицинских изделий"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 17 апреля 2025 г. N 310-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 22442-1:2020 "Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Применение менеджмента риска" (ISO 22442-1:2020 "Medical devices utilizing animal tissues and their derivatives - Part 1: Application of risk management", IDT).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные и межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА.
Дополнительная сноска в тексте стандарта, выделенная курсивом, приведена для пояснения текста оригинала
5 ВЗАМЕН ГОСТ Р ИСО 22442-1-2011
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. N 162-ФЗ "О стандартизации в Российской Федерации". Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.rst.gov.ru)
ИСО (Международная организация стандартизации) является всемирной федерацией органов национальных стандартов (организации - члены ИСО). Работа по подготовке международных стандартов, как правило, осуществляется техническими комитетами ИСО. Каждая организация-член, заинтересованная в предмете, для которого создавался технический комитет, имеет право быть представленной в этом комитете. Международные правительственные и неправительственные организации также принимают участие в работе во взаимодействии с ИСО. ИСО тесно сотрудничает с Международной электротехнической комиссией (МЭК) по всем вопросам электротехнической стандартизации.
Процедуры, примененные при разработке данного стандарта, а также процедуры, предназначенные для его дальнейшей поддержки, описаны в Директивах ИСО/МЭК, часть 1. В частности, нужно отметить необходимость различных критериев утверждения для различных типов документов ИСО. Данный документ был составлен в соответствии с редакционными правилами Директив ИСО/МЭК, часть 2 (см. www.iso.org/directives).
Необходимо обратить внимание на возможность того, что некоторые элементы данного стандарта могут подвергаться патентным правам. ИСО снимает с себя ответственность за обозначение каких-либо патентных прав. Детали каких-либо патентных прав, обозначенных при разработке стандарта, будут содержаться во введении и/или в перечне полученных патентных деклараций ИСО (см. www.iso.org/patents).
Любая торговая марка, указанная в стандарте, является информацией, приведенной для удобства пользователей, и не является рекламой.
Для разъяснения добровольного характера стандартов, значений конкретных терминов ИСО и выражений, связанных с оценкой соответствия, а также информации о приверженности ИСО принципам ВТО по техническим барьерам в торговле (ТВТ) см. следующий URL: www.iso.org/iso/foreword.html.
Настоящий стандарт был подготовлен Техническим комитетом ИСО/ТК 194 "Биологическая и клиническая оценка медицинских изделий", подкомитет ПК 1 "Безопасность тканевых продуктов", в сотрудничестве с Европейским комитетом по стандартизации (CEN), Технический комитет CEN/TC 206 "Оценка биологического и клинического действия медицинских изделий" в соответствии с соглашением о техническом сотрудничестве между ИСО и CEN (Венское соглашение).
Третье издание межгосударственного стандарта отменяет и заменяет второе издание (ИСО 22442-1:2015).
По сравнению с предыдущим изданием основными изменениями являются:
- обновлен пункт 4.4.2;
- обновлены интернет-ссылки в C.2, пункт маркированного перечня 1, C.3.3 и C.4.4;
- обновлена интернет-ссылка в D.3.3;
- добавлен пункт C.10;
- обновлена библиография.
Перечень всех частей серии ИСО 22442 размещен на сайте ИСО.
Любые отзывы или вопросы по данному документу должны направляться в органы национальных стандартов пользователя. Их полный перечень размещен по адресу www.iso.org/members.html.
Некоторые медицинские изделия используют материалы животного происхождения.
Ткани животных и их производные применяют в разработке и производстве медицинских изделий для обеспечения эксплуатационных качеств, выбранных из-за их преимуществ по сравнению с материалами неживотного происхождения. Диапазон и количество материалов животного происхождения в медицинских изделиях может различаться. Такие материалы являются значительной частью изделия (например, бычьи/свиные сердечные клапаны, костные заместители для стоматологического или ортопедического применения, гемостатические изделия), могут быть внешним слоем изделия или его пропиткой (например, коллаген, желатин, гепарин) либо использоваться в процессе производства материала (например, жировые производные, такие как олеаты и стеараты, эмбриональная телячья сыворотка, ферменты, культуральная среда).
ИСО 14971 является общим стандартом, устанавливающим процесс для изготовителя путем идентификации опасностей и опасных ситуаций, связанных с медицинскими изделиями, включая медицинские изделия in vitro, для определения и оценивания рисков, связанных с данными опасностями, управления этими рисками и мониторинга результативности такого управления на протяжении всего жизненного цикла. Данный документ приводит дополнительные требования и руководство для оценки медицинских изделий, изготовленных с использованием тканей животного происхождения или их производных, которые не являются жизнеспособными или были приведены в такое состояние.
Настоящий стандарт охватывает медицинские изделия, включая активные имплантируемые медицинские изделия, такие как имплантируемые инфузионные насосы.
Настоящий стандарт неприменим к диагностическим изделиям in vitro.
Настоящий стандарт может применяться только в сочетании с ИСО 14971 и не является отдельно применяемым стандартом.
Примечание - Соответствие настоящему стандарту демонстрируется выполнением его обозначенных требований. Руководство, приводимое в примечаниях и справочных приложениях, не является нормативным и не предоставляется в качестве контрольного листа для аудиторов.
Настоящий стандарт распространяется на медицинские изделия (МИ), за исключением диагностических МИ in vitro, изготовленных с использованием материалов животного происхождения, являющихся нежизнеспособными или приведенными в нежизнеспособное состояние. Настоящий стандарт в сочетании с ИСО 14971 определяет процедуру идентификации опасностей и опасных ситуаций, связанных с такими изделиями, для определения и оценивания возникающих рисков, управления этими рисками и мониторинга результативности такого управления. Настоящий стандарт устанавливает процесс принятия решения о допустимости остаточного риска, с учетом баланса остаточного риска, как установлено в ИСО 14971, и ожидаемой медицинской пользы по сравнению с существующими альтернативами. В настоящем стандарте установлены требования и приведены рекомендации по применению менеджмента риска, связанного с опасностями, характерными для МИ, произведенных с использованием тканей или их производных животного происхождения, такими как:
a) контаминация бактериями, плесневыми или дрожжевыми грибами;
b) контаминация вирусами;
c) контаминация агентами, вызывающими инфекционные губчатые энцефалопатии (TSE);
d) материал, вызывающий нежелательные (неблагоприятные) пирогенные, иммунологические или токсикологические реакции.
Аналогичные требования и рекомендации могут быть применимы для паразитов и других неклассифицированных патогенных единиц.
Настоящий стандарт не устанавливает допустимые уровни приемлемости, так как таковые определяются множеством факторов и не могут быть зафиксированы в настоящем стандарте, за исключением некоторых отдельных производных тканей, представленных в приложении C. В приложении C установлены допустимые уровни риска TSE для производных жира, костяного угля, молока и производных молока, производных шерсти и аминокислот.
Настоящий стандарт не определяет систему менеджмента качества для контроля всех этапов производства МИ.
Настоящий стандарт не распространяется на МИ, изготовленные с использованием материалов человеческого происхождения.
Примечание 1 - Наличие полной системы менеджмента качества в процессе производства МИ не является требованием настоящего стандарта. Однако следует обратить внимание на международные стандарты систем менеджмента качества (см. ИСО 13485), которые управляют всеми этапами производства или переработки МИ.
Примечание 2 - Рекомендации по применению настоящего стандарта приведены в приложении A.
В настоящем стандарте использованы нормативные ссылки на следующие стандарты [для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных - последнее издание (включая все изменения)]:
ISO 10993-1, Biological evaluation of medical devices - Part 1: Evaluation and testing within a risk management process (Оценка биологического действия. Часть 1. Оценка и исследования в процессе менеджмента риска)
ISO 14971, Medical devices - Application of risk management to medical devices (Изделия медицинские. Применение менеджмента риска к медицинским изделиям)
ISO 22442-2, Medical devices utilizing animal tissues and their derivatives - Part 2: Controls on sourcing, collection and handling (Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 2. Контроль отбора, сбора и обработки)
ISO 22442-3, Medical devices utilizing animal tissues and their derivatives - Part 3: Validation of the elimination and/or inactivation of viruses and transmissible spongiform encephalopathy (TSE) agents [Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 3. Валидация уничтожения и/или инактивации вирусов и агентов инфекционной губчатой энцефалопатии (TSE)]
В настоящем стандарте применены термины по ИСО 14971, а также следующие термины с соответствующими определениями.
ИСО и МЭК ведут терминологические базы данных для использования в стандартизации по следующим адресам:
- Электропедия МЭК: доступна на http://www.electropedia.org/;
- платформа онлайн-просмотра ИСО: доступна на http://www.iso.org/obp.
3.1 животное (animal): Любое позвоночное или беспозвоночное [включая земноводных, членистоногих (например, ракообразных), птиц, кораллы, рыб, рептилий, моллюсков и млекопитающих], за исключением человека (Homo sapiens).
3.2 клетка (cell): Наименьшая организованная единица любой живой формы, способная к независимому существованию и к возмещению собственного вещества в подходящей среде.
3.3 производная (derivative): Вещество, полученное на основе животного (3.1) материала, непосредственно задействованного в изготовлении МИ или являющееся частью готового МИ.
Пример - гиалуроновая кислота, коллаген, желатин, моноклональные антитела, хитозан, альбумин.
3.4 удаление (elimination, removal): Процесс удаления, путем которого сокращается число передающихся агентов.
Примечание 1 - Эффективность процесса для удаления вирусов и агентов TSE должна быть выражена математически посредством коэффициента сокращения (см. C.2 и ИСО 22442-3:2007, приложение F).
Примечание 2 - Целью удаления является предотвращение инфекции или патогенной реакции, вызванной инфекционными агентами.
3.5 дезактивация (inactivation): Процесс, посредством которого сокращена способность инфекционного агента вызывать инфекцию или патогенную реакцию.
Примечание 1 - Эффективность процесса для дезактивации вирусов и агентов TSE должна быть выражена математически посредством коэффициента сокращения (см. ИСО 22442-3:2007, приложение F).
Примечание 2 - Целью дезактивации является предотвращение заражения инфекционными агентами и их размножения.
3.6 медицинское изделие (medical device): Любой инструмент, аппарат, приспособление, механизм, прибор, имплантат, реагент для применения in vitro, программное обеспечение, материал или другое похожее или родственное изделие, предназначенное изготовителем для применения либо изолированно, либо в комбинации, на человеке, в таких одной или нескольких конкретных медицинских целях, как:
- диагностика, профилактика, наблюдение, лечение или облегчение болезни;
- диагностика, наблюдение, лечение, облегчение или компенсация повреждения органов или физического недостатка;
- исследование, замена, модификация или поддержка анатомии или физиологического процесса;
- поддержание или обеспечение жизнедеятельности;
- контрацепция;
- дезинфекция МИ;
- предоставление информации путем исследования in vitro образцов, полученных от человека и которое не является фармакологическим, иммунологическим или метаболическим средством в применении на человеке, но может быть дополнено такими средствами.
Примечание 1 - Изделия, которые относят к МИ в отдельных случаях:
- дезинфицирующие средства;
- вспомогательные средства для лиц с ограниченными возможностями;
- изделия, включающие ткани животного (3.1) и/или человеческого происхождения;
- изделия для оплодотворения in vitro или репродуктивных технологий.
[ISO 13485:2003, 3.7]
3.7 нежизнеспособный (non-viable): Не имеющий потенциала к метаболизму или размножению.
3.8 техническое соглашение (technical agreement): Обязательственный договор между двумя или более сторонами, распределяющий ответственность за выполнение технических требований.
3.9 ткань (tissue): Тканевая организация клеток (3.2) и/или внеклеточных составляющих.
3.10 инфекционные агенты (transmissible agents): Бактерии, плесневые и дрожжевые грибы, паразиты, вирусы, агенты TSE и неклассифицированные патогенные единицы.
Применимы требования ИСО 14971. Соответствие данным требованиям должно быть подтверждено проверкой соответствующей документации по менеджменту риска.
Изготовитель МИ должен обосновать использование материала животного происхождения (включая выбор видов животных и тканей), опираясь на приемлемость остаточного риска, учитывая баланс остаточного риска и ожидаемой медицинской пользы по сравнению с существующими альтернативами.
Примечание - Дальнейшее обсуждение медицинской пользы и анализ соотношения риск-выгода приведены в ИСО 14971.
4.2.1 Установление качественных и количественных характеристик, связанных с безопасностью МИ
4.2.1.1 Контактирует изделие с пациентом или другими людьми?
Количество материала, площадь контактной поверхности и тип материала, контактирующего с тканями тела или жидкостями, а также тип ткани организма или жидкости, с которыми происходит контакт, должны быть предусмотрены в анализе риска. Рекомендации для TSE приведены в D.3.7.
Примечание 1 - МИ, такие как ортопедическая обувь, или компоненты, такие как кожаные ремни, которые контактируют только с неповрежденными кожными покровами, представляют низкий инфекционный риск.
Примечание 2 - Количество контактирующего материала является одним из факторов при создании биологических эффектов [см. ИСО 10993 (все части) для оценки таких эффектов].
Примечание 3 - Структура обрабатываемых тканей животных может оказать влияние на дезактивацию и/или удаление инфекционных агентов, а на потенциал к сохранению жизнеспособных клеток может повлиять структура обрабатываемых тканей животных и их производных.
4.2.1.2 Какие материалы и/или компоненты включены в МИ либо используются или контактируют с ним?
Необходимо предусмотреть следующие факторы, если применимо:
a) подтверждение, что готовое МИ не содержит какого-либо жизнеспособного материала животного происхождения, если в его производстве используются жизнеспособные материалы животного происхождения;
b) предназначенное использование любой животной ткани или ее производных животного происхождения;
c) географический источник, вид, возраст и корм (включая использование белка животного происхождения) животных;
d) ветеринарный контроль, условия, при которых материалы животного происхождения были собраны, потенциал к перекрестной контаминации;
e) тип и анатомический источник ткани;
f) производственный процесс, особенно если в нем использованы материалы, собранные от более чем одного животного;
g) характер материала, используемого в МИ (например, неповрежденная ткань, высокоочищенный производный материал);
h) метод использования или включения в МИ.
В случае МИ, использующих несколько рассматриваемых составляющих (например, различных видов, происхождения или тканей) или несколько схожих типов составляющих, произведенных с использованием разных методов, каждая отдельная составляющая должна быть проанализирована отдельно.
4.2.1.3 Поставляется ли изделие в стерильном виде или предназначено для стерилизации пользователем, либо применимы другие методы микробиологического контроля?
Учитывая биологический характер тканей и их производных животного происхождения, необходимо оценить уровень их бионагрузки микроорганизмами.
Примечание - См. ИСО 11737-1, ИСО 14160.
4.2.1.4 Появляются ли нежелательные вещества?
Возможное наличие остаточного количества токсичных веществ, связанного с применяемым производственным процессом или деградацией побочных продуктов, должно быть предусмотрено, принимая во внимание физические характеристики (например, пористость, гетерогенность) и химический состав тканей животного происхождения или их производных.
Примечание - См. ИСО 10993-1, ИСО 10993-9, ИСО 10993-17, ИСО 10993-18 и ISO/TS 10993-19.
4.2.2 Идентификация опасности и опасных ситуаций
Возможные факторы опасности, связанные с тканями или их производными животного происхождения, должны быть идентифицированы и отражены документально.
Особое внимание необходимо уделить возможным опасностям, исходящим от тканей животного происхождения или их производными в случае:
- потенциальной контаминации инфекционными агентами и их чувствительности к уничтожению и/или дезактивации в процессе обработки;
- потенциала к контаминантам на готовом материале, который может вызвать нежелательную пирогенную, иммунологическую или токсикологическую реакции;
- потенциала самого готового материала вызывать нежелательную пирогенную, иммунологическую или токсикологическую реакции.
В соответствии с ИСО 14971 должны быть оценены все идентифицированные риски. Биологическая безопасность должна быть оценена в соответствии с ИСО 10993-1. Оценивание риска инфекционных агентов должно быть осуществлено посредством раздельного рассмотрения рисков, связанных с различными категориями инфекционных агентов. В приложении B определены основные категории риска, необходимые к рассмотрению.
Соответствие риска TSE требованиям, изложенным в приложении C для отдельных материалов животного происхождения, может означать допустимость риска.
Примечание - В приложении C учтены элементы оценивания риска и управления риском.
4.4.1 Общая часть
Варианты управления риском должны быть обоснованы и отражены документально.
На блок-схеме в приложении B представлен процесс менеджмента риска. Если при использовании настоящего стандарта выявлены дополнительные риски, то изготовитель МИ может принять решение соответствовать любому другому применимому стандарту или подходу. Решение должно быть обосновано и отражено документально.
4.4.2 Управление риском для вирусов и агентов TSE
Управление риском должно осуществляться путем раздельного рассмотрения рисков, связанных с различными категориями вирусов и агентов TSE. После определения характеристик продукта изготовитель МИ должен соблюдать требования ИСО 22442-2 и ИСО 22442-3. Если делают исключения из установленных требований, то таковые исключения должны быть обоснованы и отражены документально.
Производные жира, костяной уголь и аминокислоты, приемлемые с точки зрения риска развития TSE, как рассмотрено в приложении C, по причине их обработки, а не источника, также должны быть отнесены к имеющим приемлемый (минимальный) риск, связанный с вирусами.
В отношении риска TSE, меры управления риском, приведенные в приложении C для определенных материалов животного происхождения, должны быть приняты, если применимо. Если изготовитель считает любое требование неприменимым, то причина и обоснование должны быть отражены документально.
Для МИ, в которых процесс дезактивации вызывает неприемлемую деградацию, изготовители могут применять ИСО 22442-2 для соответствия требованиям настоящего стандарта.
Если вид животных таков, что изготовители не могут предоставить информацию об источнике происхождения животного для полного соответствия требованиям ИСО 22442-2, то они должны показать, что уровень дезактивации передающихся агентов в валидированном производственном процессе достаточен для достижения приемлемого уровня риска согласно требованиям ИСО 22442-3.
Примечание - Критерии и принципы, относящиеся к менеджменту риска TSE, описаны в приложении D. В приложении D приведена информация по соответствующим мерам управления риском.
4.4.3 Управление риском для других опасностей
Управление риском, связанным с бактериями, плесневыми и дрожжевыми грибами, а также нежелательными пирогенными, иммунологическими и токсикологическими реакциями, следует внедрять согласно существующим стандартам.
Производные жира, костяной уголь и аминокислоты, приемлемые с точки зрения риска развития TSE, как рассмотрено в приложении C по причине их обработки, а не источника, также должны быть отнесены к имеющим приемлемый риск, связанный с бактериями, а также плесневыми и дрожжевыми грибами, учитывая выполнение надлежащих условий хранения.
Изготовитель должен проводить периодические микробиологические исследования для установления и количественного определения исходной бионагрузки поступающего материала животного происхождения для производства МИ.
Примечание - Международными стандартами, которые могут быть применимыми, являются:
a) ИСО 11135, ИСО 11137 (все части), ИСО 11737-1, ИСО 13408 (все части), ИСО 14160, ИСО 14937, ИСО 17664 и ИСО 17665-1, которые могут иметь отношение к бактериям, а также плесневым и дрожжевым грибам;
b) ИСО 10993-2, ИСО 10993-3, ИСО 10993-4, ИСО 10993-5, ИСО 10993-6, ИСО 10993-7, ИСО 10993-9, ИСО 10993-10, ИСО 10993-11, ИСО 10993-12, ИСО 10993-13, ИСО 10993-14, ИСО 10993-15, ИСО 10993-16, ИСО 10993-17, ИСО 10993-18, ISO/TS 10993-19 и ISO/TS 10993-20, которые могут применяться в процессе менеджмента риска, связанного с нежелательными пирогенными, иммунологическими или токсикологическими реакциями.
Применение этих международных стандартов разъяснено в приложении B.
4.4.4 Оценивание остаточного риска
4.4.4.1 Общие положения
Для каждого риска должна быть проведена оценка остаточного риска.
4.4.4.2 Риск TSE
Риск TSE может быть признан допустимым при соответствии всем приведенным ниже критериям с учетом наличия альтернативных материалов:
a) значение остаточного риска показывает, что риск TSE подвергся управлению до допустимого уровня;
b) считается, что медицинская польза, получаемая от применения изделия по назначению, превышает значение остаточного риска.
Примечание - Рекомендации по применению менеджмента риска к агентам TSE приведены в приложении D. Приемлемость может быть основана на соответствии особым требованиям для некоторых материалов животного происхождения, приведенным в приложении C, или требованиям, касающимся источников, сбора и обращения с материалами от крупного рогатого скота, приведенным в приложении A ИСО 22442-2:2020.
Особые соображения приведены в приложении C в отношении остаточного риска TSE. Некоторые производные, такие как производные жира, костяной уголь, производные молока, шерсти и аминокислоты, выработанные в соответствии с условиями, указанными в приложении C, считаются представляющими приемлемый риск TSE.
В случаях, когда риск TSE не управлялся на приемлемом уровне для пользователей и получателей, совокупный риск может быть признан приемлемым только в том случае, если он сбалансирован по соображениям исключительной пользы и выполнимости.
4.5.1 Общие положения
При оценивании приемлемости совокупного остаточного риска следует учитывать баланс между остаточным риском после внедрения всех мер управления риском и ожидаемой медицинской пользой по сравнению с существующими альтернативами. Там, где существуют остаточные риски, связанные с контаминацией передаваемыми агентами, в ходе оценивания следует специально рассмотреть риски и пользу:
- при использовании альтернативных материалов, не представляющих риска контаминации данными передающимися агентами, такими как синтетические материалы, материалы от других видов животных или материалы человеческого происхождения, и
- применении альтернатив изделию в целом для тех же предполагаемых целей.
В случаях, когда риск не управлялся на приемлемом уровне для пользователей и пациентов, совокупный риск может быть признан приемлемым только в том случае, если он сбалансирован соображениями исключительной пользы и выполнимости.
4.5.2 Документация
Обоснование приемлемости риска должно быть отражено в документации по менеджменту риска.
Изготовители должны обеспечить, чтобы система идентифицировала изменения в зоонозном статусе выбранного источника материалов животного происхождения. Любое изменение зоонозного статуса исходного материала должно быть учтено при оценивании в рамках менеджмента риска.
(справочное)
A.1 Общие положения
В ситуациях, обозначенных в настоящем стандарте как "подлежит рассмотрению", необходимо либо принять меры по управлению риском, либо обосновать в отчете по менеджменту риска, почему этого не было сделано.
A.2 Применение материалов животного происхождения
Настоящий стандарт применим к таким материалам, как:
- сердечные клапаны свиньи, бычьи кости, связки крупного рогатого скота и бычий перикард;
- производные тканей животных, такие как хондроитина сульфат, полученный из акул, и коллаген, произведенный из шкур, а также крови и сыворотки животных;
- материалы, произведенные in vivo соответствующими животными, например антитела, используемые в производственном процессе;
- исходные материалы, такие как альбумин бычьей сыворотки, ферменты, культуральная среда, включая используемые для приготовления рабочих культур клеток, маточных культур клеток или маточной затравки для таких продуктов, как гиалуроновая кислота.
A.3 Применение материалов, поставленных третьими лицами
Настоящий стандарт может быть применен, когда материалы, используемые изготовителями МИ, были приготовлены из материалов животного происхождения третьими лицами или субподрядчиками. Примером является желатин, полученный из шкур или костей животных. При рассмотрении риска, связанного с использованием этих продуктов, изготовители МИ должны запросить у своих поставщиков доказательства того, что при оценке пригодности животного материала были применены соответствующие требования настоящего стандарта либо были использованы альтернативные подходы. Полученная информация должна быть по применимости включена в отчет менеджмента риска, связанного с МИ, но может нуждаться в дополнении информацией, полученной от третьих лиц или субподрядчиков.
(справочное)
ДЛЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ, ИСПОЛЬЗУЮЩИХ МАТЕРИАЛЫ
ЖИВОТНОГО ПРОИСХОЖДЕНИЯ
Графическое представление части процесса менеджмента риска для МИ, использующих животный материал, приведено на рисунке B.1. Данная схема иллюстрирует часть процесса менеджмента риска в соответствии с ИСО 14971 и настоящим стандартом. В процессе менеджмента риска должны быть рассмотрены все риски, показанные на данной схеме.
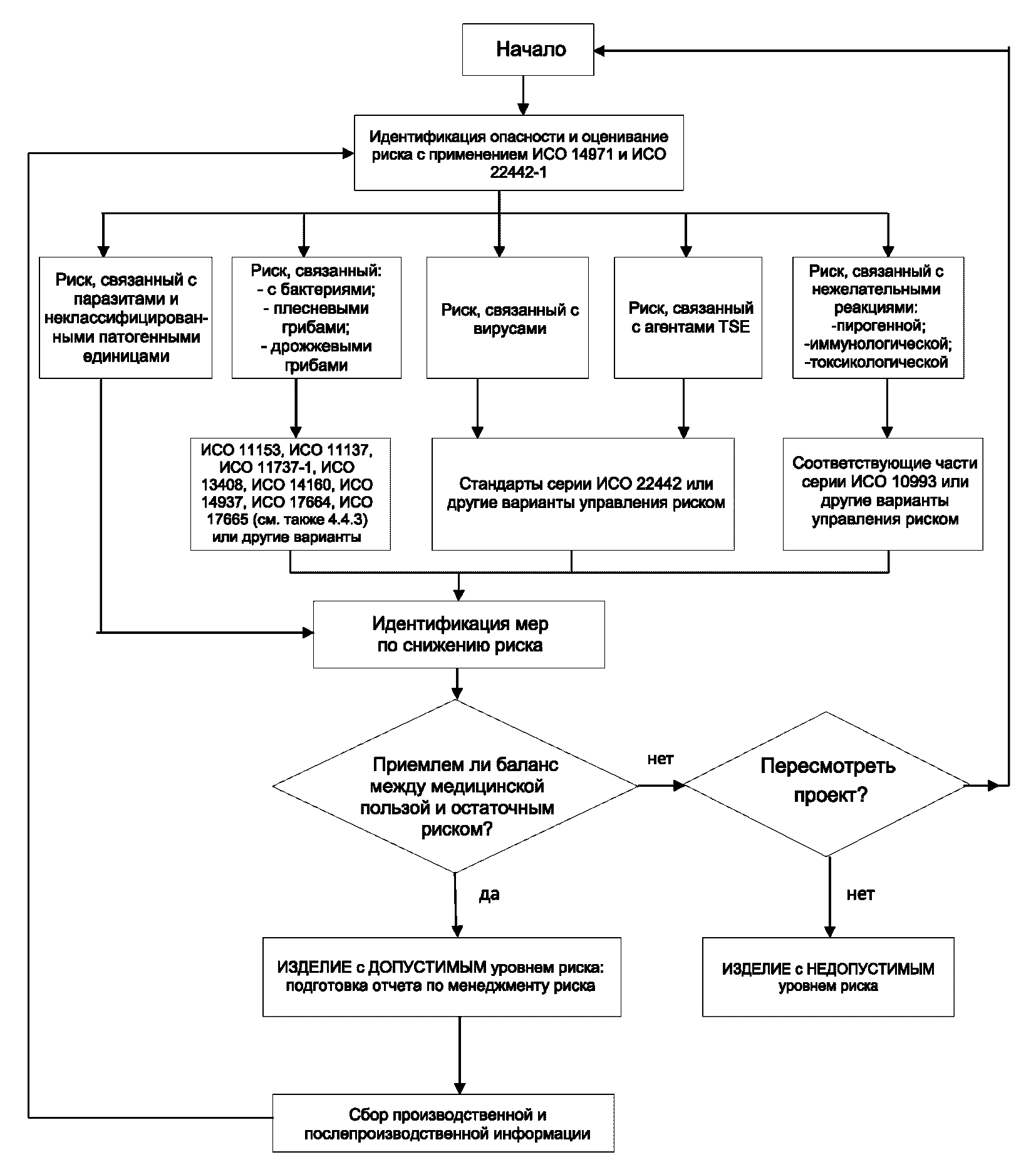
процесса менеджмента риска
(обязательное)
ПРОИСХОЖДЕНИЯ С УЧЕТОМ МЕНЕДЖМЕНТА РИСКА К АГЕНТАМ TSE
C.1 Общие положения
Требования данного приложения не отменяют необходимость проведения оценки риска TSE, включая требования, изложенные в разделе 4 в качестве части процесса оценки менеджмента риска, описанного в ИСО 14971.
В менеджменте риска может быть рассмотрена переработка, закупка или сочетание того и другого. Производные жира, костяной уголь и аминокислоты приемлемы с точки зрения риска TSE из-за их переработки, а не из-за их источника происхождения.
Приложение A ИСО 22442-2:2020 содержит дополнительные требования, относящиеся к применению настоящего стандарта к материалам, полученным от крупного рогатого скота.
Для демонстрации соответствия требованиям настоящего стандарта необходимо привести в исполнение техническое соглашение между изготовителем МИ и поставщиком материала/производной животного происхождения (см. ИСО 22442-2:2020, раздел 6).
Дальнейшая информация по менеджменту риска TSE изложена в приложении D.
Коллаген является белковым волокнистым компонентом соединительной ткани млекопитающих.
Для коллагена необходимо предоставить документацию для демонстрации соответствия настоящему стандарту, учитывая соответствующие требования настоящего приложения.
При выполнении процедур менеджмента риска, которые предусмотрены настоящим стандартом, необходимо учитывать следующее:
- для коллагена, получаемого из костей, кость должна быть из стран с минимальной подверженностью губчатой энцефалопатии крупного рогатого скота (BSE). Страны с ограниченной подверженностью BSE как источники кости должны быть обоснованы посредством ссылки на другие применимые меры управления риском (см. приложение A, ИСО 22442-2:2020). Недопустима кость происхождением из стран, где инфицирование агентом BSE не определено (см. классификацию OIE <*>), если источником не является стадо с низким уровнем риска, как определено в ИСО 22442-2;
- для коллагена, получаемого из костей, применимы условия производства, указанные для желатина (см. C.3);
- коллаген, полученный из шкур и кожи, как правило, не представляет значительного риска TSE, при условии, что во время их заготовки не допускается перекрестная контаминация потенциально инфицированными материалами, например тканями центральной нервной системы. Для демонстрации соответствия требованиям настоящего стандарта необходимо ввести меры по предотвращению перекрестной контаминации (см. ИСО 22442-2) и отразить документально меры, принятые согласно техническому соглашению между поставщиком коллагена и изготовителем МИ для предотвращения такой перекрестной контаминации.
--------------------------------
<*> OIE - Всемирная организация по охране здоровья животных. Организация OIE в 2022 году преобразована в WOAH (Всемирная организация охраны здоровья животных).
Коллаген должен быть получен от животных, признанных годными для употребления в пищу человеком (см. ИСО 22442-2).
Страны-источники с "минимальной подверженностью BSE" должны быть интерпретированы как страны с незначительным риском BSE <1>, или страны в списке Службы инспекции состояния животных и растений (APHIS) <2>, или от стада с низким уровнем риска, как определено в ИСО 22442-2.
Страны-источники с "ограниченной подверженностью BSE" должны быть интерпретированы, как и страны с контролируемым риском BSE как приводится в сноске <2>.
--------------------------------
<1> Европейский союз опубликовал документы по географическому риску BSE для ряда стран, доступные на веб-сайте Научного руководящего комитета Комиссии Европейского союза: https://ec.europa.eu/food/safety/biosafety/food_borne_diseases/tse_bse_en.
<2> Разрешенный список, публикуемый Службой инспекции состояния животных и растений, находится на https://www.aphis.usda.gov/aphis/ourfocus/animalhealth/animal-and-animal-product-import-information/animal-health-status-of-regions.
C.3.1 Общие положения
Желатин является желирующим или нежелирующим растворимым белком, получаемым путем частичного гидролиза коллагена из костей, шкур и кож, жил и сухожилий животных.
Для желатина необходимо предоставить документацию, демонстрирующую соответствие настоящему стандарту, учитывая применимые требования, приведенные в настоящем приложении.
Желатин должен быть получен от животных, признанных годными для употребления в пищу человеком.
При выполнении оценивания и управления риском, требуемыми настоящим стандартом, необходимо принять во внимание положения C.3.2 - C.3.4.
Основываясь на существующем опыте, шкуры, используемые для получения желатина, представляют более безопасный исходный материал по сравнению с костями.
Желатин, полученный из шкур, как правило, не представляет значительного риска TSE, при условии, что во время их заготовки не допускается перекрестная контаминация потенциально инфицированными материалами, например тканями центральной нервной системы. Для демонстрации соответствия требованиям настоящего стандарта необходимо ввести меры по предотвращению перекрестной контаминации (см. ИСО 22442-2) и отразить документально меры, принятые согласно техническому соглашению между поставщиком желатина и изготовителем МИ для предотвращения такой перекрестной контаминации.
C.3.3 Кости в качестве исходного материала
При использовании костей для получения желатина качество исходных материалов является основным параметром, обеспечивающим безопасность готового изделия. Таким образом, необходимо применить следующее:
- кости должны быть получены из стран с минимальным или ограниченным риском BSE. Кости не должны поступать из стран, где инфицирование агентом BSE классифицируется OIE как неопределенное, если источником не является стадо низкого риска, как определено в ИСО 22442-2.
Примечание - Применяется национальное законодательство;
- кости черепа и спинной мозг должны быть удалены из собранных костей (сырье/исходный материал) крупного рогатого скота определенного возраста.
Примечание - Данный процесс определяется национальным законодательством;
- дополнительно, из сырья/исходных материалов, полученных от крупного рогатого скота всех возрастов из стран с ограниченной подверженностью BSE, должны быть удалены позвонки.
Для желатина, получаемого из шкур, не требуется никаких специальных условий обработки, при условии, что будут применены средства управления, позволяющие избежать перекрестной контаминации, как при закупке шкур, так и в процессе производства (см. C.3.2).
В тех случаях, когда в качестве исходного материала используются кости, информация о материале изготовления приводится ниже.
Хотя способ щелочной экстракции (перед завершающими этапами) показал немного более высокую способность к дезактивации/удалению по сравнению с процессом с применением кислоты, однако как кислотный, так и щелочной методы производства конечного желатина показали в целом схожую степень дезактивации/удаления инфицированности желатина TSE в валидационных испытаниях. Исследования продемонстрировали, что дополнительная щелочная обработка (pH 13, не менее 1 ч) костей/оссеина повышает способность кислотного производственного процесса к дезактивации/удалению TSE. Изготовитель должен рассмотреть возможность поиска поставщиков в странах с незначительным риском TSE.
При обычном щелочном способе производства кости мелко измельчают, обезжиривают горячей водой и деминерализуют разбавленной соляной кислотой (концентрацией не менее 4% и pH менее 1,5) в течение как минимум двух дней для получения оссеина. Далее проводится щелочная обработка насыщенным раствором извести (pH не менее 12,5) в течение не менее 20 дней. Желатин экстрагируют, промывают, фильтруют и концентрируют. Затем проводится мгновенная термообработка при температуре от 138 °C до 140 °C в течение 4 с. Бычьи кости также могут быть обработаны с использованием кислоты. Этап известкования в таком случае заменяют предварительной обработкой кислотой, при которой оссеин вымачивают в течение одной ночи при pH менее 4. В процессе термообработки высушенные, обезжиренные, измельченные кости обрабатываются в автоклаве насыщенным паром при давлении более 3 бар и минимальной температуре 133 °C в течение не менее 20 мин, после чего белок экстрагируется горячей водой. Завершающие этапы как кислотного способа, так и термического процесса под давлением аналогичны щелочному способу.
C.4 Производные крови крупного рогатого скота
C.4.1 Общие положения
Эмбриональная телячья сыворотка, как правило, используется для культивирования клеток. Эмбриональная телячья сыворотка должна быть получена от зародышей, забранных на бойне от здоровых самок (коров), пригодных для употребления в пищу человеком, при этом матка должна быть полностью удалена. Кровь плода следует забирать в специально отведенном месте или участке путем пункции сердца, в закрытую систему сбора с использованием асептических методов.
Сыворотку новорожденного теленка получают от телят возрастом до 20 дней либо от животных возрастом менее 12 мес. В случае донорской бычьей сыворотки, при условии, что она может быть получена от животных возрастом менее 36 мес, статус BSE донорского стада должен быть четко определен и отражен документально. Во всех случаях сыворотку должны забирать сотрудники, подготовленные к таким процедурам, следуя обозначенным протоколам и мерам предосторожности, необходимым для исключения перекрестной контаминации с тканями более высокого риска.
Для производных крови крупного рогатого скота необходимо предоставить документацию, демонстрирующую соответствие настоящему стандарту с учетом требований данного приложения. При выполнении установленных настоящим стандартом требований по менеджменту риска необходимо рассмотреть C.4.2 - C.4.4.
Для каждой партии сыворотки или плазмы должна быть обеспечена прослеживаемость до скотобойни. Скотобойни должны иметь в своем распоряжении списки ферм, откуда поступают животные.
Если сыворотка производится от живых животных, то для каждой партии сыворотки должны быть доступны записи, чтобы обеспечить прослеживаемость до ферм и конкретного животного. Если прослеживаемость до конкретного животного невозможна, то это должно быть обосновано в файле менеджмента рисками.
C.4.3 Географические источники происхождения
Бычья кровь должна быть получена из стран с минимальным риском BSE, если иное не обосновано и не разрешено.
Если кровь получена от забитых животных, то метод забоя является важным для обеспечения безопасности материала. Было доказано, что оглушение электрошоком определенного разряда с прокалыванием или без, а также пневматическим оглушителем, особенно если таковой впускает воздух, может разрушить мозг и распространить мозговой материал по системе кровообращения. Существуют данные, что непроникающее оглушение может вызывать эмболию центральной нервной системы (ЦНС). Методы забоя должны быть описаны для процесса сбора бычьей крови, кроме случаев, когда материал был получен из страны с незначительным географическим риском BSE (см. ИСО 22442-2:2020, A.3.1).
Когда источником крови являются страны с ограниченным риском BSE, для забоя животных возрастом более 12 мес необходимо использовать непроникающий оглушитель или электронаркоз. Применение непроникающего оглушения должно быть обосновано применением оценки риска распространения частиц мозга в крови.
Примечание - Дополнительная информация по методам оглушения находится в документах Научного совета по планированию (SSC) по методам оглушения и риску BSE (Риск распространения частиц мозга в крови и туше при применении некоторых методов оглушения), принятых на совещании от 10 - 11 января 2002 г. (https://ec.europa.eu/food/sites/food/files/safety/docs/sci-com_ssc_out245_en.pdf) и документах Рабочей группы Европейского управления безопасности пищевых продуктов (EFSA) по риску BSE от распространения частиц мозга в крови и туше, Вопрос номер EFSA-Q-2003-122, принятых 21 октября 2004 г. (http://www.efsa.europa.eu/en/efsajournal/pub/123).
C.5 Производные жира
Жиром называют жир, получаемый из тканей, включая подкожные, брюшные и межмышечные области и кости.
Считается, что производные жира, такие как глицерин и жирные кислоты, полученные из жира, используя технологические процессы с жесткими параметрами, имеют малую вероятность инфицированности. По этой причине такие материалы, выработанные при условиях, по меньшей мере, таких же жестких, как приведенные ниже, должны рассматриваться как представляющие приемлемый риск TSE, вне зависимости от географического источника и характера тканей, из которых получены производные жира. Примерами технологических процессов с жесткими параметрами являются:
a) переэтерификация или гидролиз при температуре не менее чем 200 °C в течение не меньше чем 20 мин под давлением (производство глицерина, жирных кислот и эфиров жирных кислот);
b) сапонификация раствором гидроксида натрия при концентрации в 12 моль/л (производство глицерина и мыла):
1) периодический процесс: при температуре не менее чем 95 °C в течение не менее чем 3 ч;
2) непрерывный процесс: при температуре не менее чем 140 °C, под давлением в течение не менее чем 8 мин или аналогичные условия;
c) дистилляция при температуре 200 °C.
C.6 Костяной уголь
Костяной уголь получают карбонизацией тканей животного происхождения, таких как кости, при температуре 800 °C и выше.
Вне зависимости от географического источника и характера тканей, животный уголь, полученный при этих условиях, должен рассматриваться как представляющий приемлемый риск TSE.
Определенные материалы, включая лактозу, экстрагируют из молочной сыворотки, жидкости, отработанной при производстве сыра после коагуляции. Коагуляция может включать в себя использование сычужного фермента теленка, экстракт сычугов или сычужный фермент, полученный от других жвачных. Была проведена оценка риска для лактозы и других производных молочной сыворотки, полученных с использованием сычужного фермента теленка <3>, а также было сделано заключение о том, что риск TSE незначителен, если сычужный фермент теленка выработан в соответствии с процессом, описанным в отчете оценки риска Комитета по запатентованным лекарственным препаратам (CPMP) [44].
--------------------------------
<3> Комитет по запатентованным лекарственным препаратам и Рабочая группа по биотехнологиям провели оценку риска и нормативов лактозы, приготовленной с использованием сычужного фермента теленка. Оценка риска включала источник животных, отделение сычугов и наличие четко определенных процедур гарантии качества. Качество любых заменителей молока, используемых для корма животного, от которого получены сычуги, является особенно важным.
Производные молока, выработанные согласно условиям, приведенным ниже, считаются представляющими приемлемый риск TSE:
- молоко получено от здоровых животных при тех же условиях, что и молоко, получаемое для употребления в пищу человеком;
- никакие другие материалы, полученные от жвачных, за исключением сычужного фермента теленка, не использовались в приготовлении таких производных (например, перевары казеина панкреатическими ферментами).
Примечание - Может применяться национальное законодательство.
C.8 Шерсть и ее производные
Шерсть и ее производные, такие как ланолин и спирты, должны отвечать требованиям настоящего стандарта при условии, что шерсть получена от живых здоровых животных.
Производные шерсти, полученные от забитых животных, признанных "годными для употребления в пищу человеком", считаются представляющими приемлемый риск TSE, если процесс производства отвечает, по меньшей мере, одному из условий обработки, приведенных ниже, касательно pH, температуры и продолжительности обработки:
- обработка при pH, больше или равном 13 (начальная; соответствует концентрациям гидроксида натрия, больше или равным 0,1 моль/л), при температуре, больше или равной 60 °C, в течение по меньшей мере 1 ч; это, как правило, происходит во время отжима на стадии органически-щелочной обработки;
- молекулярная дистилляция при температуре, больше или равной 220 °C, при пониженном давлении.
C.9 Аминокислоты
Аминокислоты могут быть получены гидролизом материалов животного происхождения из различных источников.
Аминокислоты, приготовленные с использованием следующих условий обработки, считаются представляющими приемлемый риск TSE:
- аминокислоты, полученные из шкур и кож способом, включающим воздействие на материал pH от 1 до 2, последующим pH более 11, последующей тепловой обработкой при температуре 140 °C в течение 30 мин при давлении 3 бар;
- полученные аминокислоты или пептиды должны быть отфильтрованы;
- необходимо провести анализ, используя валидированный и чувствительный методы для контроля каких-либо остаточных неповрежденных макромолекул с установленным обоснованным пределом.
C.10 Пептоны
Пептоны являются продуктами частичного гидролиза белков молока или мяса животных, получаемыми путем ферментативного или кислотного расщепления. Они используются в микробиологических культуральных средах для питания микроорганизмов или ферментации в промышленных масштабах при производстве медицинских продуктов для человека и ветеринарии, включая вакцины.
Существует значительный интерес к применению растительного белка в качестве альтернативы белку животного происхождения. Однако:
- если в качестве источника белка используется желатин, см. ссылку в C.3;
- если в качестве источника белка используется казеин, см. ссылку в C.7;
- в тех случаях, когда источником белка являются ткани животных, соответствующих TSE, эти ткани должны быть получены от животных, пригодных для употребления в пищу (см. D.3.2), максимальный возраст которых составляет 30 мес для крупного рогатого скота из стран с контролируемым риском BSE (категория B). Возраст животных имеет минимальное значение забота о животных из стран с незначительным риском BSE (категория A).
(справочное)
D.1 Общие положения
К естественным TSE, встречающимся в природе, относятся почесуха (у овец и коз), хроническая изнуряющая болезнь (у чернохвостых оленей и лосей), губчатая энцефалопатия крупного рогатого скота (BSE), а также болезнь Куру и болезнь Крейтцфельдта-Якоба (CJD) у людей. Агентов, вызывающих эти заболевания, трудно обнаружить in vivo. После многолетних латентных периодов агенты вызывают заболевание и приводят к летальному исходу. Средства лечения неизвестны.
Существующая информация о характеристиках возбудителей ограничена. Они чрезвычайно устойчивы к большинству химических и физических процедур, дезактивирующих обычные вирусы. Они не вызывают обнаруживаемого иммунного ответа. Существуют естественные барьеры, ограничивающие межвидовое распространение передающегося агента, но при соответствующих условиях они могут быть преодолены. Это, как правило, зависит от штамма, дозы, способа воздействия и видового барьера. Испытания на лабораторных животных показали, что внутрицеребральная инокуляция является наиболее эффективным путем передачи.
D.2 Риск для человека
Существуют значительные косвенные доказательства, что вариантная форма человеческого CJD (vCJD) проистекает от BSE, и разумно утверждать, что агент BSE может передаваться человеку. Таким образом, настоящий стандарт содержит ряд требований, обеспечивающих контроль факторов риска при использовании биологических материалов от видов, подверженных TSE, для производства МИ. В настоящем приложении приведены рекомендации, которые необходимо соблюдать для сведения к минимуму риска контаминации. В нем определено, когда применимы требования, указанные в настоящем стандарте, и когда уместна информация из других источников. Все изделия следует рассматривать в индивидуальном порядке.
D.3 Менеджмент риска агентов TSE
D.3.1 Принцип
Безопасность МИ с точки зрения его потенциала передачи агента TSE зависит от ряда факторов, восемь наиболее важных из которых приведены ниже и должны быть проанализированы, оценены и урегулированы:
- используемые виды животных (см. D.3.2);
- географические источники (см. D.3.3);
- природа исходной ткани (см. D.3.4);
- контроль забоя и обработки для предотвращения перекрестной контаминации (см. D.3.5);
- методы, используемые для дезактивации или удаления агентов TSE (см. D.3.6);
- количество исходного материала животного происхождения, требуемого для выработки одной единицы МИ (см. D.3.7.1);
- количество материала животного происхождения, контактирующего с пациентами и пользователями (см. D.3.7.2);
- способ введения (см. D.3.7.3).
При наличии выбора у изготовителей предпочтительно использование материалов от видов животных, не имеющих отношения к TSE, или материалов неживотного происхождения.
Риск заражения TSE зависит от источника происхождения, штамма и природы исходной ткани. Так как накапливание инфицированности TSE происходит в течение инкубационного периода в несколько лет, забор от молодых здоровых животных считается фактором снижения риска. Использование животных постарше может повысить риск. Использование в качестве источников животных в возрасте до 6 мес понижает уровень риска. Использование павших животных, животных, забитых в аварийно-защитных целях, а также животных с подозрением на TSE может значительно повысить риск и должно быть исключено. Факторы риска такого характера предусматриваются путем демонстрации соответствия требованиям в ИСО 22442-2:2020, приложение A.
Определенные географические факторы влияют на риск BSE, связанный с использованием сырьевых тканей или производных из отдельных стран. Они применимы конкретно к BSE, но могут также быть использованы для определения риска TSE для других видов животных.
Изготовители должны учитывать опубликованные экспертные оценки, касающиеся риска BSE, связанного с определенными странами. Например, МЭБ опубликовал документы по статусу BSE для ряда стран (Наземный Кодекс МЭБ доступен на http://www.oie.int/international-standard-setting/terrestrial-code/). Департамент сельского хозяйства США опубликовал перечень разрешенных и несанкционированных стран-источников [см. приложение C, сноску 3]. Министерство здоровья, труда и благосостояния Японии также опубликовало список разрешенных и несанкционированных стран-источников (см. [47]).
Изготовитель должен учитывать классификацию опасностей, связанных с различными типами исходной ткани. По возможности, соответственно местным обычаям и практикам, источники животной ткани должны подвергаться контролю и индивидуальной инспекции ветеринаром, а туша животного должна быть сертифицирована как годная для употребления в пищу человеком. Изготовитель не должен использовать в качестве источника животную ткань, классифицированную как имеющую потенциально высокую инфективность TSE. Единственным исключением являются случаи отсутствия альтернативной исходной ткани и значительной медицинской пользы для пациента.
Классификация опасностей, связанных с различными типами исходного животного материала, была установлена и утверждена Всемирной организацией здравоохранения (ВОЗ) [42]. Таблицы D.1 - D.3 основаны на классификации тканей ВОЗ в 2006 году, а таблицы ВОЗ по распределению инфективности ткани для TSE были обновлены в 2010 году [43]. Оценка риска должна быть пересмотрена в свете более современной информации по мере ее поступления и должна учитывать уровень неопределенности, свойственный существующим данным.
"+" - наличие инфективности или PrPTSE <4>;
"-" - отсутствие выявляемой инфективности PrPTSE;
NT - не испытывалось;
NA - неприменимо;
? - спорные или неопределенные результаты;
() - ограниченные или предварительные данные.
[] - инфективность или данные PrPTSE, основанные исключительно на биопробах трансгенных мышей (Tg), сверхэкспрессирующих кодирующий ген PrP, или методах амплификации PrPTSE.
--------------------------------
Таблица D.1
Ткани ЦНС, которые приобретают титр инфективности в поздних стадиях всех TSE, и некоторые ткани, анатомически связанные с ЦНС | ||||||||
Ткани | Человек | Крупный рогатый скот | Овцы и козы | |||||
vCJD | Другие TSE | BSE | Почесуха | |||||
инфективность <a> | PrPTSE | инфективность <a> | PrPTSE | инфективность <a> | PrPTSE | инфективность <a> | PrPTSE | |
Головной мозг | + | + | + | + | + | + | + | + |
Спинной мозг | + | + | + | + | + | + | + | + |
Сетчатка глаза | NT | + | + | + | + | NT | NT | + |
Зрительный нерв <b> | NT | + | NT | + | + | NT | NT | + |
Спинно-мозговые узлы | + | + | NT | + | + | NT | + | + |
Тройничные узлы | + | + | NT | + | + | + | NT | + |
Гипофиз <c> | NT | + | + | + | - | + | + | + |
Твердая мозговая оболочка | NT | (+) | + | - | NT | NT | NT | NT |
<a> Биопробы инфективности тканей человека проводились на приматах либо на мышах (либо на обеих группах); биопробы тканей скота проводились на скоте либо на мышах (либо на обеих группах); большинство биопроб тканей овец и/или коз проводилось только на мышах. Касательно овец и коз не все результаты последовательны для обоих видов; например, две козы (но ни одной овцы) заразились BSE естественным путем. <b> В опытных моделях TSE было показано, что зрительный нерв является путем нейровторжения и содержит высокие титры инфективности. <c> По инфективности гипофиза или твердой мозговой оболочки человека нет опытных данных, но аллографтные вставки из трупной твердой мозговой оболочки и гормон роста, полученный из трупных гипофизов, передали заболевание сотням человек и, таким образом, должны быть включены в категорию тканей высокого риска. | ||||||||
Таблица D.2
Периферические ткани с положительным результатом на инфективность и/или PrPTSE по меньшей мере в одной форме TSE | ||||||||
Ткани | Человек | Крупный рогатый скот | Овцы и козы | |||||
vCJD | Другие TSE | BSE | Почесуха | |||||
инфективность | PrPTSE | инфективность | PrPTSE | инфективность | PrPTSE | инфективность | PrPTSE | |
Периферическая нервная система | ||||||||
Периферические нервы | + | + | (-) | + | [+] | + | + | + |
Автономные ганглии <a> | NT | + | NT | (-) | NT | + | NT | + |
Лимфоретикулярные ткани | ||||||||
Селезенка | + | + | + | + | - | - | + | + |
Лимфоузлы | + | + | + | - | - | - | + | + |
Миндалина | + | + | NT | - | + | - | + | + |
Мигательная перепонка | NA | NA | NA | NA | + | - | [+] | + |
Вилочковая железа | NT | + | NT | - | - | NT | + | + |
Пищеварительный тракт <b> | ||||||||
Пищевод | NT | - | NT | - | - | NT | [+] | + |
Передний отдел желудка <c> (только для жвачных) | NA | NA | NA | NA | - | NT | [+] | + |
Желудок/сычуг | NT | - | NT | NT | - | NT | [+] | + |
Двенадцатиперстная кишка | NT | - | NT | - | - | - | [+] | + |
Тонкая кишка <d> | NT | + | NT | - | - | + | [+] | + |
Подвздошная кишка | NT | + | NT | - | + | + | + | + |
Аппендикс | (-) | + | NT | - | NA | NA | NA | NA |
Толстый кишечник/слепая кишка <d> | NT | + | NT | - | - | - | + | + |
Прямая кишка | [+] | + | NT | NT | NT | NT | NT | + |
Репродуктивные ткани | ||||||||
Плацента <e> | NT | - | (+) | - | - | NT | + | + |
Яичник <f> | NT | - (+) | NT | - | - | NT | - | - |
Матка <f> | NT | - (+) | NT | - | - | NT | - | - |
Другие ткани | ||||||||
NT | - | NT | - | - | NT | - | + | |
NT | - (+) | NT | - | - | NT | - | + | |
Жировая ткань | NT | - | (-) | - | - | NT | NT | NT |
Сердце/перикард | NT | - | - | - | - | NT | - | NT |
Легкое | NT | - | + | - | - | NT | - | - |
Печень <f> | NT | - (+) | + | - | - | NT | + | - |
NT | - (+) | + | - | - | - | [+] | + | |
Надпочечник | NT | + | - | - | [+] | + | + | - |
Поджелудочная железа <f> | NT | - (+) | NT | - | - | NT | + | NT |
Костный мозг <j> | - | - | (-) | - | (+) | NT | + | NT |
Скелетные мышцы <k> | NT | + | (-) | + | (+) | NT | + | + |
Язык <l> | NT | - | NT | - | - | NT | [+] | + |
Кровеносные сосуды | NT | + | NT | + | - | NT | NT | + |
NT | NT | NT | + | - | NT | + | + | |
Слюнная железа | NT | - | NT | - | - | NT | + | NT |
Роговица <n> | NT | - | + | - | NT | NT | NT | NT |
Биологические жидкости | ||||||||
ЦСЖ | - | - | + | - | - | NT | + | - |
Кровь <o> | + | ? | - | ? | - | ? | + | ? |
Слюна | NT | - | - | NT | NT | NT | - | NT |
Молоко <p> | NT | NT | (-) | NT | - | - | + | [+] |
Моча <q> | NT | - | - | - | - | NT | - | - |
Кал <q> | NT | NT | - | NT | - | NT | - | NT |
<a> У крупного рогатого скота PrPTSE периодически присутствуют в кишечных сплетениях дистального отдела подвздошной кишки, но иммуногистохимическое исследование тканей от единственного случая BSE в Японии показало (хотя неоднозначно) вовлечение внутренних сплетений в толстом и тонком кишечнике. <b> При vCJD, PrPTSE ограничивается кишечной лимфоидной и нервной тканью (слизистая, мускульная и серозная показывают отрицательный результат). <c> Передние отделы желудков жвачных (сетка, рубец и книжка) широко употребляются в пищу, так же как и истинный желудок (сычуг). Сычуг крупного рогатого скота (и иногда овец) также является источником сычужного фермента. <d> При применении большой пероральной дозы BSE для экспериментального инфицирования крупного рогатого скота инфективность была обнаружена в тонком кишечнике и соединении подвздошной и слепой кишки в мышах Tg, сверхэкспрессирующих PrP. PrPTSE был обнаружен с низкой частотой в лимфоидной ткани подвздошной кишки и с еще более низкой частотой в лимфоидной ткани тонкого кишечника скота, также инфицированного перорально. <e> Единственный отчет о передаче спорадической инфективности CJD человеческой плацентой не был подтвержден и считается недоказуемым. <f> PrPTSE был обнаружен методом иммуноблотирования в твердой мозговой оболочке пациентки с vCJD, которая скончалась в США после необычайно длительного инкубационного периода (другие ткани с позитивным результатом включали кожу, почку, печень, поджелудочную железу, яичники и матку). Необходимо отметить, что в более ранних исследованиях многочисленных случаев в Великобритании результат для всех этих тканей был отрицательным. <g> PrPTSE был обнаружен у овец с хроническим маститом, инфицированных почесухой, но не у инфицированных овец без мастита. <h> Исследования хомяков, перорально инфицированных почесухой, показали, что PrPTSE в коже в основном локализуется в мелких нервных волокнах. <j> При многократных попытках передачи инфекции от крупного рогатого скота, которому перорально вводили зараженный BSE мозг, инфицирование костного мозга получено в единственном случае. <k> Мышечные гомогенаты не передавали заболевание приматам от людей с sCJD или скоту от скота с BSE. Тем не менее внутрицеребральная инокуляция гомогената полусухожильной мышцы (включая нервные и лимфатические элементы) от единственной коровы с BSE передала заболевание трансгенным мышам, сверхэкспрессирующим PrP, в степени, свидетельствующей только об остаточных уровнях инфективности. Также в недавних опубликованных и неопубликованных исследованиях сообщалось о наличии PrPTSE в скелетных мышцах у грызунов в опытных моделях почесухи и vCJD, при опытных и природных инфекциях овец и коз, у овец, перорально инфицированных BSE, и у людей с sCJD, iCJD и vCJD. В настоящее время проводятся биопробы для определения, связан ли PrPTSE с возможностью передачи этих экспериментальных или естественных инфекций. <l> У крупного рогатого скота биопроба инфективности была отрицательной, но наличие PrPTSE в небной миндалине привело к опасениям возможной инфективности в язычной тонзиллярной ткани у основания языка, которая может не удаляться при забое. Среди овец, инфицированных почесухой естественным образом, у 7 из 10 животных обнаруживалась PrPTSE в языке. <n> Так как только один или два случая CJD были достоверно соотнесены с роговичными трансплантатами из сотен тысяч реципиентов, роговица относится к категории тканей более низкого риска; другие ткани передней камеры (хрусталик, водянистая влага, радужка, конъюнктива) при анализах показали отрицательный результат как на vCJD, так и на другие TSE человека, и нет эпидемиологических доказательств, что они были связаны с передачей ятрогенного заболевания. <o> Обширные данные, полученные в результате исследований инфекционности крови на экспериментальных моделях TSE на грызунах, были дополнены недавними исследованиями, подтвердившими инфективность крови овец, зараженных естественным путем, и овец, которым перелили кровь крупного рогатого скота, инфицированного BSE; и (по данным эпидемиологических наблюдений) фракции эритроцитов (которая включает значительное количество как плазмы, так и лейкоцитов) четырех доноров крови на доклинической стадии инфекции vCJD). Введение фактора плазмы VIII также было потенциально связано с этим субклиническим случаем с vCJD у пациента с гемофилией. Не было доказано, что заболевание передается через кровь человека с какой-либо формой "классической" TSE или от крупного рогатого скота с BSE (включая кровь плода). Ряд лабораторий, используя новые высокочувствительные методы обнаружения PrPTSE, объявляют об успешных исследованиях на животных и человеке. Тем не менее, некоторые из них столкнулись с трудностями получения воспроизводимых результатов в плазме крови, и пока не ясно, означают ли положительные результаты потенциальную возможность передачи заболевания либо из-за ложноположительных результатов или "истинно" положительных результатов, которые обусловлены концентрациями PrPTSE, не допускающими передачи инфекции. Исходя из этих соображений (при том, что пока нет данных о слепом тестировании образцов, взятых от инфицированных естественным путем человека или животных), экспертная группа ВОЗ посчитала, что с достаточной уверенностью оценивать пригодность этих испытаний для достижения отрицательного или положительного заключения пока еще рано. <p> Доказательства, что инфективность отсутствует в молоке крупного рогатого скота, зараженного BSE, включают временно-пространственные эпидемиологические наблюдения, не обнаружившие передачу от матери к телятам, вскармливаемым долгое время; клинические наблюдения более сотни телят, вскормленных инфицированными коровами, у которых BSE не появилась, и опытные наблюдения, что молоко инфицированных коров, выращенных до возраста, превышающего минимальный инкубационный период, не передавало заболевание при внутрицеребральном или пероральном введении мышам. Также, PrPTSE не обнаруживался в молоке крупного рогатого скота, инкубирующего BSE после опытной пероральной проверки иммунности. Тем не менее, низкие уровни ( <q> Недавние биопробы на мышах Tg показали, что болезнь передается как с мочой, так и с экскрементами. Кроме того, у мышей Tg с лимфоцитарным нефритом, которые были экспериментально инфицированы почесухой, обнаружены как PrPTSE, так и инфективные свойства мочи. Также очень низкие уровни инфективности мочи (при гистологически нормальных почках) были обнаружены у хомяков, экспериментально инфицированных почесухой. Наконец, в экспериментальной модели почесухи на хомяках пероральное введение привело к инфицированию экскрементов при биопробе у мышей Tg с избыточной экспрессией PrP. | ||||||||
Таблица D.3
Ткани | Человек | Крупный рогатый скот | Овцы и козы | |||||
vCJD | Другие TSE | BSE | Почесуха | |||||
инфективность | PrPTSE | инфективность | PrPTSE | инфективность | PrPTSE | инфективность | PrPTSE | |
Репродуктивные ткани | ||||||||
Семенник | NT | - | (-) | - | - | NT | - | - |
Простата/эпидидимис/семенной пузырек | NT | - | (-) | - | - | NT | - | - |
Семенная жидкость | NT | - | (-) | - | - | NT | - | - |
Плацентные жидкости | NT | NT | (-) | (-) | - | NT | NT | NT |
Плод <a> | NT | NT | NT | NT | - | NT | - | - |
Эмбрионы <a> | NT | NT | NT | NT | - | NT | ? | NT |
Скелетно-мышечные ткани | ||||||||
Кость | NT | NT | NT | - | - | NT | NT | NT |
Сухожилия | NT | NT | NT | - | - | NT | NT | NT |
Другие ткани | ||||||||
Гингивальная ткань | NT | - | - | - | NT | NT | NT | NT |
Пульпа зуба | NT | - | NT | - | NT | NT | NT | NT |
Трахея | NT | - | NT | - | - | NT | NT | NT |
Щитовидная железа | NT | - | (-) | - | NT | NT | - | NT |
Биологические жидкости, секреции и выделения | ||||||||
Колострум <b> | NT | (-) | (-) | NT | (-) | - | (?) | NT |
Пуповинная кровь <b> | NT | (-) | (-) | NT | - | NT | NT | NT |
Пот | NT | - | - | NT | NT | NT | NT | NT |
Слезы | NT | - | - | NT | NT | NT | NT | NT |
Носовая слизь | NT | - | - | NT | NT | NT | NT | NT |
Желчь | NT | NT | NT | NT | NT | NT | NT | NT |
<a> Эмбрионы крупного рогатого скота, пораженного BSE, не передавали заболевание мышам, но никаких определений инфективности тканей плода теленка, кроме крови, не проводилось (отрицательная биопроба на мышах). Телята, рожденные от самок, получивших эмбрионы от крупного рогатого скота, пораженного BSE, выживали в течение периодов наблюдения до семи лет, и анализ мозга как непораженных самок, так и их потомства не показал какой-либо губчатой энцефалопатии или PrPTSE. <b> Ранние сообщения о передаче спорадической инфективности CJD через пуповинную кровь и колострум человека не подтвердились и считаются маловероятными. Биопроба от коровы с BSE на трансгенных мышах, сверхэкспрессирующих PrP крупного рогатого скота, дала отрицательный результат, а также PrPTSE не был обнаружен в колоструме крупного рогатого скота, инкубировавшего BSE после экспериментального перорального введения. | ||||||||
Отнесение данной ткани к той или иной категории может зависеть от конкретного заболевания и может быть пересмотрено по мере поступления новых данных в результате все более чувствительных анализов. В сущности, возможно представить, что обнаружение инфективности с использованием трансгенных мышей, которые сверхэкспрессируют гены, кодирующие различные прионовые белки, или обнаружение PrPTSE с использованием некоторых недавно разработанных методов амплификации могут оказаться более чувствительными, чем исследования передачи в биопробах диких животных и, таким образом, могут не соотноситься с передачей заболевания в природе.
Также важно осознавать разницу между категориями инфективности и категориями риска, что требует учета не только уровня инфективности в ткани, но и количества ткани, контактирующей с человеком или животным, а также пути передачи инфекции. Например, несмотря на то, что уровень инфективности ткани является наиболее важным фактором при оценке риска передачи перекрестной контаминацией инструментов во время хирургических процедур (например, нейрохирургия по сравнению с общей хирургией), это только одна определяющая риска передачи путем переливания крови, при котором большое количество материала с низкой инфективностью вводится внутривенно, или риска передачи через пищу, который вне зависимости от высокой или низкой инфективности, включает относительно неэффективный пероральный путь инфицирования.
Изготовитель должен принять все необходимые меры для сведения к минимуму риска перекрестной контаминации во время забоя и обработки.
Для изделий, которые не могут выдержать процесс дезактивации/удаления без неприемлемой деградации, изготовитель должен полагаться в основном на контроль источников (см. ИСО 22442-2).
Для других изделий в случае заявлений изготовителя о способности производственных процессов удалить или дезактивировать агенты TSE, таковые должны быть подкреплены соответствующей документацией. Уместная информация из соответствующего обзора научной литературы может быть использована для поддержки факторов дезактивации/уничтожения в случаях, когда определенные процессы, представленные в литературе, сопоставимы с используемыми для изделия.
В случае если обзор литературы не может обосновать заявления, то изготовитель должен провести специальное исследование дезактивации и/или уничтожения, которое должно предусмотреть следующее:
- установление опасности, связанной с тканью;
- установление соответствующих модельных агентов TSE;
- рациональную основу выбора конкретных комбинаций модельных агентов TSE;
- установление стадии, избранной для уничтожения и/или дезактивации агентов TSE;
- вычисление коэффициентов сокращения.
Заключительный отчет должен определить производственные параметры и пределы, критические для эффективности процесса дезактивации или уничтожения.
Необходимо применить надлежащие процедуры, отраженные документально, для обеспечения использования утвержденных параметров обработки во время обычного производства.
D.3.7.1 Количество исходного материала животного происхождения, необходимого для производства одной единицы МИ.
Изготовитель должен оценить количество необработанных тканей или производных животного происхождения, необходимых для производства одной единицы МИ. Изготовитель должен оценить, имеет ли производственный процесс потенциал к концентрации уровней агентов TSE, присутствующих в исходных животных тканях или производных.
Изготовители должны учитывать максимальное количество материала животного происхождения, который может контактировать с пациентами и пользователями (включая какую-либо абсорбцию и/или деградацию). Необходимо учитывать количество МИ, которое может быть использовано в данной процедуре, и число процедур.
Необходимо учитывать способ введения, рекомендованный в информации об изделии. От наивысшего риска до самого низкого, перечень состоит из:
a) изделий, контактирующих с центральной нервной системой (включая внутриглазной путь введения);
b) изделий, контактирующих с центральной системой кровообращения или вводимых парентерально, или инвазивных устройств, или приспособлений используемых на открытых ранах, включая препараты для лечения язв;
c) изделий, требующих введения на неповрежденные слизистые мембраны, например конъюнктивные, внутриносовые, бронхиальные, ректальные, вагинальные, мочевого пузыря; изделий, которые должны оставаться в ротовой полости (ротовые, подъязычные) или быть проглоченными;
d) продуктов, предназначенных для нанесения на неповрежденные кожные покровы.
D.3.7.4 Определение риска для времени воздействия
Следует оценить влияние времени воздействия на риск TSE и определить степень этого влияния на совокупный риск TSE.
(справочное)
НАЦИОНАЛЬНЫМ И МЕЖГОСУДАРСТВЕННЫМ СТАНДАРТАМ
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование национального, межгосударственного стандарта |
ИСО 10993-1 | IDT | ГОСТ ISO 10993-1-2021 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования в процессе менеджмента риска" |
ИСО 14971 | IDT | ГОСТ ISO 14971-2021 "Изделия медицинские. Применение менеджмента риска к медицинским изделиям" |
ИСО 22442-2 | IDT | ГОСТ Р ИСО 22442-2-2025 "Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 2. Контроль отбора, сбора и обработки" |
ИСО 22442-3 | IDT | ГОСТ Р ИСО 22442-3-2011 "Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 3. Валидация уничтожения и/или дезактивации вирусов и агентов инфекционной губчатой энцефалопатии" |
Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов: - IDT - идентичные стандарты. | ||
[1] | ISO 10993-2, Biological evaluation of medical devices - Part 2: Animal welfare requirements (Оценка биологического действия медицинских изделий. Часть 2. Требования к обращению с животными) |
[2] | ISO 10993-3, Biological evaluation of medical devices - Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity (Оценка биологического действия медицинских изделий. Часть 3. Исследование генотоксичности, канцерогенности и токсического действие на репродуктивную функцию) |
[3] | ISO 10993-4, Biological evaluation of medical devices - Part 4: Selection of tests for interactions with blood (Оценка биологического действия медицинских изделий. Часть 4. Исследование изделий, взаимодействующих с кровью) |
[4] | ISO 10993-5, Biological evaluation of medical devices - Part 5: Tests for in vitro cytotoxicity (Биологическая оценка медицинских изделий. Часть 5. Испытания на цитотоксичность in vitro) |
[5] | ISO 10993-6, Biological evaluation of medical devices - Part 6: Tests for local effects after implantation (Оценка биологического действия. Часть 6. Исследования местного действия после имплантации) |
[6] | ISO 10993-7, Biological evaluation of medical devices - Part 7: Ethylene oxide sterilization residuals (Оценка биологического действия медицинских изделий. Часть 7. Остаточное содержание этиленоксида после стерилизации) |
[7] | ISO 10993-9, Biological evaluation of medical devices - Part 9: Framework for identification and quantification of potential degradation products (Оценка биологического действия медицинских изделий. Часть 9. Основные принципы идентификации и количественного определения потенциальных продуктов деградации) |
[8] | ISO 10993-10, Biological evaluation of medical devices - Part 10: Tests for skin sensitization (Оценка биологического действия медицинских изделий. Часть 10. Исследования на кожную сенсибилизацию) |
[9] | ISO 10993-11, Biological evaluation of medical devices - Part 11: Tests for systemic toxicity (Изделия медицинские. Оценка биологического действия. Часть 11. Исследования общетоксического действия) |
[10] | ISO 10993-12, Biological evaluation of medical devices - Part 12: Sample preparation and reference materials (Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы) |
[11] | ISO 10993-13, Biological evaluation of medical devices - Part 13: Identification and quantification of degradation products from polymeric medical devices (Оценка биологическая медицинских изделий. Часть 13. Идентификация и количественная оценка продуктов разложения в полимерных медицинских устройствах) |
[12] | ISO 10993-14, Biological evaluation of medical devices - Part 14: Identification and quantification of degradation products from ceramics (Оценка биологического действия медицинских изделий. Часть 14. Идентификация и количественная оценка продуктов деградации керамики) |
[13] | ISO 10993-15, Biological evaluation of medical devices - Part 15: Identification and quantification of degradation products from metals and alloys (Оценка биологического действия медицинских изделий. Часть 15. Идентификация и количественное определение продуктов деградации из металлов и сплавов) |
[14] | ISO 10993-16, Biological evaluation of medical devices - Part 16: Toxicokinetic study design for degradation products and leachables (Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов разложения и выщелачиваемых веществ) |
[15] | ISO 10993-17, Biological evaluation of medical devices - Part 17: Toxicological risk assessment of medical device constituents (Оценка биологического действия медицинских изделий. Часть 17. Оценка токсикологического риска компонентов медицинских изделий) |
[16] | ISO 10993-18, Biological evaluation of medical devices - Part 18: Chemical characterization of medical device materials within a risk management process (Оценка биологического действия медицинских изделий. Часть 18. Исследование химических свойств материалов в рамках процесса менеджмента риска) |
[17] | ISO/TS 10993-19, Biological evaluation of medical devices - Part 19: Physico-chemical, morphological and topographical characterization of materials (Оценка биологического действия медицинских изделий. Часть 19. Исследования физико-химических, морфологических и топографических свойств материалов) |
[18] | ISO/TS 10993-20, Biological evaluation of medical devices - Part 20: Principles and methods for immunotoxicology testing of medical devices (Оценка биологическая медицинских изделий. Часть 20. Принципы и методы иммунотоксикологических испытаний медицинских изделий) |
[19] | ISO 11135 (все части), Sterilization of health-care products - Ethylene oxide - Requirements for the development, validation and routine control of a sterilization process for medical devices (Стерилизация медицинских изделий. Требования к разработке, валидации и регулярному контролю процесса стерилизации медицинских изделий) |
[20] | ISO 11137 (все части), Sterilization of health care products - Radiation (Стерилизация медицинской продукции. Радиационная стерилизация) |
[21] | ISO 11737 (все части), Sterilization of health care products - Microbiological methods (Стерилизация медицинских изделий. Микробиологические методы) |
[22] | ISO 13408-1, Aseptic processing of health care products - Part 1: General requirements (Асептическое производство медицинской продукции. Часть 1. Общие требования) |
[23] | ISO 13408-2, Aseptic processing of health care products - Part 2: Sterilizing filtration (Асептическое производство медицинской продукции. Часть 2. Стерилизующая фильтрация) |
[24] | ISO 13408-3, Aseptic processing of health care products - Part 3: Lyophilization (Асептическое производство медицинской продукции. Часть 3. Лиофилизация) |
[25] | ISO 13408-4, Aseptic processing of health care products - Part 4: Clean-in-place technologies (Асептическое производство медицинской продукции. Часть 4. Методики очистки на месте) |
[26] | ISO 13408-5, Aseptic processing of health care products - Part 5: Sterilization in place (Асептическое производство медицинской продукции. Часть 5. Стерилизация на месте) |
[27] | ISO 13408-6, Aseptic processing of health care products - Part 6: Isolator systems (Асептическое производство медицинской продукции. Часть 6. Изолирующие системы) |
[28] | ISO 13408-7, Aseptic processing of health care products - Part 7: Alternative processes for medical devices and combination products (Асептическое производство медицинской продукции. Часть 7. Альтернативные технологии для нестандартных медицинских изделий и комбинаций продуктов) |
[29] | ISO 13485, Medical devices - Quality management systems - Requirements for regulatory purposes (Изделия медицинские. Системы менеджмента качества. Требования для целей регулирования) |
[30] | ISO 14160, Sterilization of health care products - Liquid chemical sterilizing agents for single-use medical devices utilizing animal tissues and their derivatives - Requirements for characterization, development, validation and routine control of a sterilization process for medical devices (Стерилизация медицинской продукции. Жидкие стерилизующие средства для одноразовых медицинских изделий, содержащих ткани животных и их производные. Требования к определению характеристик, разработке, валидации и текущему контролю процесса стерилизации медицинских изделий) |
[31] | ISO 14937, Sterilization of health care products - General requirements for characterization of a sterilizing agent and the development, validation and routine control of a sterilization process for medical devices (Стерилизация медицинской продукции. Общие требования к определению характеристик стерилизующего средства и разработке, валидации и текущему контролю процесса стерилизации медицинских изделий) |
[32] | ISO 17664, Processing of health care products - Information to be provided by the medical device manufacturer for the processing of medical devices (Обработка медицинской продукции. Информация, предоставляемая изготовителем медицинских изделий для их обработки) |
[33] | ISO 17665-1, Sterilization of health care products - Moist heat - Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices (Стерилизация медицинской продукции. Стерилизация паром. Часть 1. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий) |
[34] | European Pharmacopoeia, 2.6.8 Pyrogens |
[35] | European Pharmacopoeia, 2.6.14 Bacterial endotoxins |
[36] | European Pharmacopoeia, 5.2.8 Minimizing the risk of transmitting animal spongiform - encephalopathy agents via human and veterinary medicinal products |
[37] | US Pharmacopeia, 85> Bacterial Endotoxins Test |
[38] | US Pharmacopeia, 151> Pyrogen Test |
[39] | Supplement 1, Japanese Pharmacopoeia XIV, 17. Basic Requirements for Viral Safety of Biotechnological/Biological Products, listed in Japanese pharmacopoeia, pp. 1618 - 1631, 2003 |
[40] | Global Harmonization Task Force (GHTF) - Study Group 1 (SG1) Document No. N029R13, Stage PD dated December 2003 (http://www.ghtf.org) |
[41] | WHO Guidelines on Transmissible Spongiform Encephalopathies in relation to Biological and Pharmaceutical Products, 2003 (https://www.who.int/bloodproducts/publications/en/WHO_TSE_2003_.pdf) |
WHO Guidelines on Tissue Infectivity Distribution in Transmissible Spongiform Encephalopathies, 2006 (https:// www.who.int/bloodproducts/TSEPUBLISHEDREPORT.pdf) | |
WHO Tables on Tissue Infectivity Distribution in Transmissible Spongiform Encephalopathies, Updated 2010 (https://www.who.int/bloodproducts/_tablestissueinfectivity.pdf) | |
EMEA/410/01 Rev.3 - June 2011, Note for guidance on minimising the risk of transmitting animal spongiform encephalopathy agents via human and veterinary medicinal products adopted by the Committee for Proprietary Medicinal Products (CPMP) and by the Committee for Veterinary Medicinal Products (CVMP) - Official Journal of the European Union 5.3.2011 | |
[45] | EMEA/CPMP/571/02 - February 2002, Public statement on Lactose prepared using calf rennet of the European Agency for the Evaluation of Medicinal Products |
[46] | Terrestrial Animal Health Code from OIE - Office International des Epizooties/World Organisation for Animal Health https://www.oie.int/ |
No N. 177 of the Ministry of Health, Labour and Welfare on the standard for biological ingredients, 31 March 2005 on Standards for Raw Materials Originating from Living Organisms (in Japanese) | |
[48] | Assessment of Risk of Bovine Spongiform Encephalopathy in Pharmaceutical Products, Part 1, Pharmaceutical Research and Manufacturers of America (PhRMA) BSE Committee, BioPharm., 11, Number 1, pp. 20 - 31, 56, January, 1998 |
[49] | Assessment of Risk of Bovine Spongiform Encephalopathy in Pharmaceutical Products, Part 2, Example Risk Assessment for a Hypothetical Product, Pharmaceutical Research and Manufacturers of America (PhRMA) BSE Committee, BioPharm., 11, Number 3, pp. 18 - 30, March, 1998 |
УДК 615.46:002:006.354 | ОКС 11.100.20 |
Ключевые слова: изделие медицинское; ткани животных и их производные; менеджмент риска | |