СПРАВКА
Источник публикации
Директива на русском языке подготовлена для публикации в системах ИС МЕГАНОРМ.
Директива на английском языке опубликована не была.
Примечание к документу
Данная редакция документа вступила в силу 5 декабря 2011 года (официальный сайт законодательства Европейского Союза http://eur-lex.europa.eu/ по состоянию на 14.04.2017). Россия не участвует.
Первоначальная редакция данного документа вступила в силу 12 июля 2002 года (официальный сайт законодательства Европейского Союза http://eur-lex.europa.eu/ по состоянию на 14.04.2017). Россия не участвует.
Название документа
Директива N 2002/46/ЕС Европейского парламента и Совета Европейского Союза
"О сближении законодательства государств-членов ЕС в отношении пищевых добавок" [рус., англ.]
(Вместе с <Витаминами, минералами и минеральными веществами, разрешенными к использованию при производстве пищевых добавок>)
(Принята в г. Люксембурге 10.06.2002)
(с изм. и доп. от 14.11.2011)
Договаривающиеся стороны
Директива N 2002/46/ЕС Европейского парламента и Совета Европейского Союза
"О сближении законодательства государств-членов ЕС в отношении пищевых добавок" [рус., англ.]
(Вместе с <Витаминами, минералами и минеральными веществами, разрешенными к использованию при производстве пищевых добавок>)
(Принята в г. Люксембурге 10.06.2002)
(с изм. и доп. от 14.11.2011)
Содержание
[неофициальный перевод] <1>
ЕВРОПЕЙСКИЙ СОЮЗ
ДИРЕКТИВА N 2002/46/ЕС
ЕВРОПЕЙСКОГО ПАРЛАМЕНТА И СОВЕТА ЕС
О СБЛИЖЕНИИ ЗАКОНОДАТЕЛЬСТВА ГОСУДАРСТВ-ЧЛЕНОВ ЕС
В ОТНОШЕНИИ ПИЩЕВЫХ ДОБАВОК <2>
(Люксембург, 10 июня 2002 года)
(действие Директивы распространяется
на Европейское экономическое пространство)
(текст в редакции Директивы 2006/37/ЕС
Европейской комиссии от 30 марта 2006 г. <3>,
Регламента (ЕС) 1137/2008 Европейского парламента
и Совета ЕС от 22 октября 2008 г. <4>, Регламента (ЕС)
1170/2009 Европейской комиссии от 30 ноября 2009 г. <5>,
Регламента (ЕС) 1161/2011 Европейской комиссии
от 14 ноября 2011 г. <6>)
--------------------------------
<2> Directive 2002/46/EC of the European Parliament and of the Council of 10 June 2002 on the approximation of the laws of the Member States relating to food supplements (Text with EEA relevance). Опубликована в Официальном журнале (далее - ОЖ) N L 183, 12.07.2002, стр. 51.
Европейский парламент и Совет Европейского Союза,
ИС МЕГАНОРМ: примечание. В информационный банк включен Договор, учреждающий Европейское сообщество, от 25.03.1957 с изм. и доп. от 26.02.2001. |
принимая во внимание Договор об учреждении Европейского сообщества, и, в частности, статью 95 Договора,
принимая во внимание предложение Европейской комиссии <*>,
--------------------------------
принимая во внимание Заключение Европейского комитета по экономическим и социальным вопросам <*>,
--------------------------------
действуя в соответствии с процедурой, установленной в статье 251 Договора <*>,
--------------------------------
<*> Заключение Европейского парламента от 14 февраля 2001 г. (ОЖ N C 276, 01.10.2001, стр. 126), Общая позиция Совета ЕС от 3 декабря 2001 г. (ОЖ N C 90 E, 16.04.2002, стр. 1) и Решение Европейского парламента от 13 марта 2002 г. Решение Совета ЕС от 30 мая 2002 г.
принимая во внимание следующие обстоятельства:
1) Увеличивается количество поступающих на рынок Сообщества продуктов, содержащих концентрированные источники питательных веществ и представленных для дополнения приема этих питательных веществ в обычном рационе.
2) Отношения, связанные с такими продуктами, регулируются в государствах-членах ЕС различными национальными нормами, что может ограничить свободное обращение таких продуктов, создать неравные условия конкуренции и таким образом оказать прямое воздействие на функционирование внутреннего рынка. Следовательно, необходимо принять нормы Сообщества о таких продуктах, поступающих на рынок в качестве пищевых.
3) Полноценное и разнообразное питание должно при нормальных условиях содержать все питательные вещества, необходимые для нормального развития и поддержания здоровой жизни, в количествах, определенных и рекомендуемых на основе общепризнанных научных данных. Однако, как показывают исследования, такая идеальная ситуация существует далеко не со всеми питательными веществами и группами населения в Сообществе.
4) Потребители вследствие особенностей образа жизни или по другим причинам могут решить дополнить потребление отдельных питательных веществ за счет пищевых добавок.
5) Для того чтобы обеспечить высокий уровень защиты потребителей и облегчить их выбор, поступающие на рынок продукты должны быть безопасными и иметь маркировку, содержащую достаточную и соответствующую информацию.
6) Существует большое количество питательных веществ и других ингредиентов, которые могут присутствовать в пищевых добавках, включая витамины, минералы, аминокислоты, незаменимые жирные кислоты, волокна, различные растения и экстракты трав, но не ограничиваясь ими.
7) Прежде всего настоящая Директива должна установить специальные нормы для витаминов и минералов, используемых в качестве ингредиентов пищевых добавок. Пищевые добавки, содержащие витамины, минералы и другие ингредиенты, должны также соответствовать специальным нормам о витаминах и минералах, установленным настоящей Директивой.
8) Специальные нормы, касающиеся питательных веществ, помимо витаминов и минералов, или других веществ с питательным или физиологическим действием, используемых в качестве ингредиентов пищевых добавок, должны быть установлены позже, при появлении достаточных и соответствующих научных данных об этих веществах. До принятия таких специальных норм Сообщества и без ущерба действию положений Договора могут применяться национальные нормы, касающиеся питательных веществ или других веществ с питательным или физиологическим действием, используемых в качестве ингредиентов пищевых добавок, для которых не приняты специальные нормы Сообщества.
9) Только витамины и минералы, которые обычно содержатся в рационе и потребляются в качестве его части, следует разрешить использовать в пищевых добавках. Однако это не означает, что их присутствие в пищевых добавках обязательно. Следует избежать возможных споров о видах таких питательных веществ. В связи с этим целесообразно составить позитивный список таких витаминов и минералов.
10) На рынке государств-членов ЕС имеется широкий спектр используемых при производстве добавок к пище витаминных препаратов и минеральных веществ, которые не проходили оценку Научного комитета по пищевым продуктам, вследствие чего не были включены в данные позитивные списки. Как только заинтересованные стороны представят соответствующие досье, они должны быть представлены для немедленной оценки в Европейский орган по безопасности пищевых продуктов.
11) Химические вещества, используемые в качестве источников витаминов и минералов при производстве пищевых добавок, должны быть безопасными, а также должны усваиваться организмом. Это еще одна причина для составления позитивного списка этих веществ. Такие вещества, которые одобрены Научным комитетом по пищевым продуктам на основе вышеперечисленных критериев для использования при производстве продуктов для младенцев и детей раннего возраста от 1 года до 3 лет и при производстве других продуктов для специального питания, также могут использоваться при производстве пищевых добавок.
12) Важно при необходимости своевременно пересматривать вышеуказанные списки с учетом научно-технического прогресса. Такие пересмотры представляют собой имплементационные меры технического характера, правом на их принятие следует наделить Европейскую комиссию, чтобы упростить и ускорить эту процедуру.
13) Чрезмерное потребление витаминов и минералов может привести к неблагоприятному воздействию на организм человека. В связи с этим необходимо установить их максимальные количества в пищевых добавках в зависимости от ситуации. Эти количества должны гарантировать, что обычное использование такого продукта согласно инструкции по применению от производителя будет безопасным для потребителя.
14) По этой причине такие максимальные количества следует устанавливать с учетом верхних безопасных уровней витаминов и минералов, определенных при научной оценке факторов риска на основе общепризнанных научных данных и с учетом возможного потребления этих питательных веществ с обычным рационом. Кроме того, необходимо учитывать рекомендуемое потребление населением с пищей витаминов и минералов.
15) Потребители приобретают пищевые добавки с целью дополнения того, что потребляется с рационом. Для достижения этой цели необходимо, чтобы витамины и минералы, если они указаны на маркировке пищевых добавок, присутствовали в продукте в значительном количестве.
16) Принятие на основании критериев, установленных настоящей Директивой, и на основании соответствующих научных рекомендаций специальных значений максимальных и минимальных количеств присутствующих в пищевых добавках витаминов и минералов представляет собой имплементационные меры, правом на их принятие следует наделить Европейскую комиссию.
17) Общие правила маркировки и основные определения содержатся в Директиве 2000/13/ЕС Европейского парламента и Совета ЕС от 20 марта 2000 г. о сближении законодательства государств-членов ЕС в отношении маркировки, представления и рекламы пищевых продуктов <*> и не требуют повторения. В связи с этим настоящая Директива должна ограничиваться только внесением необходимых дополнительных норм.
--------------------------------
18) Директива 90/496/ЕЭС Совета ЕС от 24 сентября 1990 г. о маркировке продуктов питания с указанием их питательной ценности <*> не применяется к пищевым добавкам. Информация, касающаяся содержания в пищевых добавках питательных веществ, важна для осуществления потребителями, которые их приобретают, осознанного выбора, а также для правильного и безопасного их использования. Такая информация, с учетом свойств этих продуктов, должна обязательно присутствовать и ограничиваться фактически содержащимися в продукте питательными веществами.
--------------------------------
19) Принимая во внимание особые свойства пищевых добавок, помимо мер, которые обычно имеются в распоряжении контролирующих органов, должны применяться дополнительные меры, чтобы упростить процедуру эффективного мониторинга таких продуктов.
20) Меры, необходимые для имплементации настоящей Директивы, должны быть приняты в соответствии с Решением 1999/468/ЕС Совета ЕС от 28 июня 1999 г., устанавливающим процедуру осуществления полномочий, которыми наделена Европейская комиссия <*>,
--------------------------------
приняли настоящую Директиву:
1. Настоящая Директива касается пищевых добавок, поступающих на рынок в качестве пищевых продуктов и представляемых как таковых. Эти продукты должны поступать конечному потребителю только в предварительно упакованном виде.
2. Настоящая Директива не применяется к лекарственным препаратам, определение которым дано в Директиве 2001/83/ЕС Европейского парламента и Совета ЕС от 6 ноября 2001 г. о Кодексе Сообщества в отношении лекарственных средств для использования человеком <*>.
--------------------------------
1. Для целей настоящей Директивы:
a) "пищевые добавки" означает пищевые продукты, предназначенные для дополнения обычного рациона и представляющие собой концентрированные источники питательных веществ или других веществ с питательным или физиологическим действием, в отдельности или в сочетании с другими веществами, поступающие на рынок в дозированной форме, а именно в виде капсул, пастилок, таблеток, пилюль и других подобных форм, порошков в пакетиках, жидкостей в ампулах, капель в пузырьках с дозатором и других подобных формах, предназначенных для приема жидкостей или порошков в дозированных небольших количествах;
b) "питательные вещества" означает следующие вещества:
i) витамины;
ii) минералы.
Государства-члены ЕС должны обеспечить поступление на рынок Сообщества только пищевых добавок, соответствующих правилам, изложенным в настоящей Директиве.
1. Только витамины и минералы, перечисленные в Приложении I, в формах, перечисленных в Приложении II, могут использоваться при производстве пищевых добавок с соблюдением положений параграфа 6.
2. Критерии чистоты веществ, перечисленных в Приложении II к настоящей Директиве, должны устанавливаться Европейской комиссией, за исключением случаев их применения в соответствии с параграфом 3. Такие меры, разработанные в целях внесения изменений в несущественные элементы настоящей Директивы путем ее дополнения, должны быть приняты с соблюдением регулятивной процедуры, предусмотренной статьей 13 (3).
3. При производстве продуктов для целей, не подпадающих под действие настоящей Директивы, применяются критерии чистоты веществ, перечисленных в Приложении II, установленные законодательством Сообщества.
4. К таким веществам, перечисленным в Приложении II, для которых критерии чистоты не установлены законодательством Сообщества, и до принятия соответствующих положений применяются общепринятые критерии чистоты, рекомендованные международными органами. Национальные нормы, устанавливающие более строгие критерии чистоты, могут сохранять свое действие.
5. Поправки в списки, указанные в параграфе 1, разработанные в целях внесения изменений в несущественные элементы настоящей Директивы путем ее дополнения, должны быть приняты с соблюдением регулятивной процедуры, предусмотренной статьей 13 (3). В случае срочности Европейская комиссия вправе прибегнуть к срочной процедуре, предусмотренной статьей 13 (4), чтобы убрать витамин или минерал из списка, указанного в параграфе 1 настоящей статьи.
6. Посредством частичного отступления от параграфа 1 и до 31 декабря 2009 г. государства-члены ЕС вправе разрешить использование на их территории витаминов и минералов, не перечисленных в Приложении I, или в формах, не перечисленных в Приложении II, при условии, что:
a) на момент вступления в силу настоящей Директивы соответствующее вещество используется в одной или более пищевых добавках, поступивших на рынок Сообщества;
b) Европейский орган по безопасности пищевых продуктов по вопросу использования такого вещества или по вопросу его использования в такой форме при производстве пищевых добавок не выдал неблагоприятное заключение на основании досье, подтверждающего представление государством-членом ЕС вопроса об использовании такого вещества на рассмотрение Европейской комиссии не позднее 12 июля 2005 г.
7. Несмотря на параграф 6, государства-члены ЕС вправе с соблюдением положений Договора продолжить применять существующие национальные ограничения или запреты на торговлю пищевыми добавками, содержащими витамины и минералы, не включенные в список Приложения I, или содержащими их в формах, не перечисленных в Приложении II.
8. Европейская комиссия не позднее 12 июля 2007 г. должна представить в Европейский парламент и Совет ЕС отчет о целесообразности принятия специальных норм (включая при необходимости позитивные списки), касающихся категорий питательных веществ или веществ с питательным или физиологическим действием, помимо указанных в параграфе 1, с приложением любых предложений о внесении изменений в настоящую Директиву, которые Европейская комиссия сочтет необходимыми.
1. Максимальные количества витаминов и минералов, содержащиеся в суточной дозировке пищевой добавки, рекомендуемой производителем, должны устанавливаться с учетом:
a) верхних безопасных уровней витаминов и минералов, определенных при научной оценке факторов риска на основе общепризнанных научных данных, с учетом при необходимости различий в уровне восприимчивости у разных групп потребителей;
b) потребления витаминов и минералов из других источников питания.
2. При установлении максимальных количеств, указанных в параграфе 1, необходимо также уделить должное внимание рекомендуемому потреблению населением витаминов и минералов.
3. Для того чтобы гарантировать содержание значительных количеств витаминов и минералов в пищевых добавках, при необходимости должна быть установлена рекомендуемая изготовителем минимальная суточная дозировка потребления.
4. Максимальные и минимальные количества витаминов и минералов, указанные в параграфах 1, 2 и 3, должны устанавливаться Европейской комиссией. Такие меры, разработанные в целях внесения изменений в несущественные элементы настоящей Директивы путем ее дополнения, должны быть приняты с соблюдением регулятивной процедуры, предусмотренной статьей 13 (3).
1. В соответствии со статьей 5 (1) Директивы 2000/13/ЕС продукты, подпадающие под действие настоящей Директивы, должны продаваться под наименованием "пищевая добавка".
2. Маркировка, представление и реклама не должны приписывать пищевым добавкам профилактические или лечебные свойства, а также указывать на наличие у них таких свойств.
3. Без ущерба действию Директивы 2000/13/ЕС маркировка должна содержать следующую информацию:
a) наименование категорий питательных или других веществ, характеризующих продукт, или указание на происхождение данных питательных или других веществ;
b) дозировка продукта, рекомендуемая для суточного потребления;
c) предупреждение не превышать установленную рекомендуемую суточную дозировку;
d) заявление о том, что пищевые добавки не должны использоваться в качестве замены разнообразного питания;
e) заявление о том, что продукт необходимо хранить в недоступном для детей месте.
Маркировка, представление и реклама пищевых добавок не должны содержать утверждений или намеков о том, что сбалансированное и разнообразное питание не может в целом обеспечить поступление питательных веществ в нужных количествах.
Правила имплементации настоящей статьи могут быть определены в соответствии с процедурой, предусмотренной статьей 13 (2).
1. Количество питательных веществ или веществ с питательным или физиологическим действием, содержащихся в продукте, должно быть указано на маркировке в числовой форме. Единицы измерения, применяемые для витаминов и минералов, определены в Приложении I.
Правила имплементации настоящего параграфа могут быть определены в соответствии с процедурой, предусмотренной статьей 13 (2).
2. Количество заявленных питательных или других веществ должно быть приведено в расчете на рекомендуемую суточную дозировку продукта, указанную на маркировке.
3. Информация о витаминах и минералах должна быть также выражена в процентном отношении к значениям рекомендуемого потребления, приведенным в приложении к Директиве 90/496/ЕЭС.
1. Заявленные значения, указанные в статье 8 (1) и (2), должны представлять собой средние значения, основанные на анализе продукта его производителем.
Последующие правила имплементации настоящего параграфа, в частности, в отношении различий между заявленными значениями и значениями, установленными в ходе проведения официальных проверок, должны устанавливаться в соответствии с процедурой, предусмотренной статьей 13 (2).
2. Процентное отношение к значениям рекомендуемого потребления витаминов и минералов, указанное в статье 8 (3), также может быть представлено в графической форме.
Правила имплементации настоящего параграфа могут быть приняты в соответствии с процедурой, предусмотренной статьей 13 (2).
Для упрощения процесса эффективного мониторинга пищевых добавок государства-члены ЕС вправе требовать, чтобы производитель или лицо, размещающее такие продукты на рынке на их территории, уведомляли компетентный орган о таком размещении на рынке, предоставляя образец маркировки, используемой для продукта.
1. Без ущерба действию статьи 4 (7) государства-члены ЕС не должны по причинам, связанным с составом, производственными спецификациями, представлением или маркировкой, запрещать или ограничивать торговлю продуктами, указанными в статье 1, которые соответствуют требованиям настоящей Директивы и при необходимости требованиям актов Сообщества, принятых для имплементации настоящей Директивы.
2. Без ущерба действию Договора, в частности, статей 28 и 30, параграф 1 не должен оказывать влияние на национальные нормы, применяемые при отсутствии актов Сообщества, принятых согласно настоящей Директиве.
1. В случае если у государства-члена ЕС ввиду получения новой или переоценки существующей информации после принятия одной из специальных Директив или одного из имплементационных актов Сообщества есть полные основания утверждать, что продукт, указанный в статье 1, угрожает здоровью населения, хотя и соответствует требованиям соответствующей директивы или соответствующих актов, это государство-член ЕС вправе временно приостановить или ограничить применение на своей территории спорных норм. Оно должно незамедлительно сообщить об этом другим государствам-членам ЕС и Европейской комиссии, а также обосновать причины своего решения.
2. Европейская комиссия должна в кратчайшие сроки изучить основания, представленные соответствующим государством-членом ЕС, проконсультироваться с государствами-членами ЕС в рамках Постоянного комитета по пищевой цепи и здоровью животных, затем безотлагательно огласить свое заключение и принять соответствующие меры.
3. Для преодоления трудностей, упомянутых в параграфе 1, и для обеспечения защиты здоровья населения Европейская комиссия должна внести изменения в настоящую Директиву или ее имплементационные меры. Такие меры, разработанные в целях внесения изменений в несущественные элементы настоящей Директивы, inter alia, путем ее дополнения, должны быть приняты с соблюдением регулятивной процедуры, предусмотренной статьей 13 (3). В случае срочности Европейская комиссия вправе прибегнуть к срочной процедуре, предусмотренной статьей 13 (4), для принятия таких изменений. Государство-член ЕС, которое приняло меры предосторожности, вправе в таком случае сохранять их в силе до внесения соответствующих изменений.
1. Постоянный комитет по пищевой цепи и здоровью животных, учрежденный согласно Регламенту (ЕС) 178/2002 Европейского парламента и Совета ЕС <*>, должен оказывать содействие Европейской комиссии.
--------------------------------
2. При ссылке на настоящий параграф применяются статьи 5 и 7 Решения 1999/468/ЕС с учетом положений статьи 8 указанного Решения.
Срок, установленный в статье 5 (6) Решения 1999/468/ЕС, считается равным трем месяцам.
3. При ссылке на настоящий параграф применяются статья 5a (1) - (4) и статья 7 Решения 1999/468/ЕС с учетом положений статьи 8 указанного Решения.
4. При ссылке на настоящий параграф применяются статья 5a (1), (2), (4) и (6) и статья 7 Решения 1999/468/ЕС с учетом положений статьи 8 указанного Решения.
Нормы, которые могут оказать воздействие на здоровье населения, должны приниматься только после консультации с Европейским органом по безопасности пищевых продуктов.
Государства-члены ЕС к 31 июля 2003 г. должны ввести в действие законодательные, регламентарные и административные положения, необходимые для соответствия требованиям настоящей Директивы. Они должны незамедлительно проинформировать об этом Европейскую комиссию.
Эти законодательные, регламентарные и административные положения должны применяться таким образом, чтобы:
a) не позднее 1 августа 2003 г. разрешить торговлю продуктами, соответствующими требованиям настоящей Директивы;
b) не позднее 1 августа 2005 г. запретить торговлю продуктами, не соответствующими требованиям настоящей Директивы.
Меры, принимаемые государствами-членами ЕС, должны содержать ссылку на настоящую Директиву или сопровождаться такой ссылкой при их официальном опубликовании. Способы указания такой ссылки должны устанавливаться государствами-членами ЕС.
Настоящая Директива вступает в силу в день ее опубликования в Официальном журнале Европейских сообществ.
Настоящая Директива адресована государствам-членам ЕС.
Совершено в Люксембурге 10 июня 2002 г.
(Подписи)
ПРИ ПРОИЗВОДСТВЕ ПИЩЕВЫХ ДОБАВОК
Витамин A (мкг RE)
Витамин D (мкг)
Витамин E (мг a-TE)
Витамин K (мкг)
Витамин B1 (мг)
Витамин B2 (мг)
Ниацин (мг NE)
Пантотеновая кислота (мг)
Витамин B6 (мг)
Фолиевая кислота (мкг) <*>
--------------------------------
<*> Фолиевая кислота - это термин, включенный в приложение I к Директиве 2008/100/ЕС Европейской комиссии от 28 октября 2008 г., изменяющей Директиву 90/496/ЕЭС Совета ЕС о маркировке продуктов питания с указанием их питательной ценности в части рекомендованного ежедневного потребления, факторов преобразования энергии и определений, используемых для маркировки питательной ценности; включает в себя все формы фолатов.
Витамин B12 (мкг)
Биотин (мкг)
Витамин C (мг)
Кальций (мг)
Магний (мг)
Железо (мг)
Медь (мкг)
Йод (мкг)
Цинк (мг)
Марганец (мг)
Натрий (мг)
Калий (мг)
Селен (мкг)
Хром (мкг)
Молибден (мкг)
Фтор (мг)
Хлор (мг)
Фосфор (мг)
Бор (мг)
Кремний (мг)
К ИСПОЛЬЗОВАНИЮ ПРИ ПРОИЗВОДСТВЕ ПИЩЕВЫХ ДОБАВОК
a) ретинол
b) ретинил ацетат
c) ретинил пальмитат
d) бета-каротин
a) холекальциферол
b) эргокальциферол
a) D-альфа-токоферол
b) DL-альфа-токоферол
c) D-альфа-токоферил ацетат
d) DL-альфа-токоферил ацетат
e) D-альфа-токофериловой кислоты сукцинат
f) смешанные токоферолы <*>
--------------------------------
<*> Альфа-токоферол < 20%, бета-токоферол < 10%, гамма-токоферол 50 - 70% и дельта-токоферол 10-30%.
g) токотриенол токоферол <*>
--------------------------------
- 115 мг/г альфа-токоферол (минимум 101 мг/г);
- 5 мг/г бета-токоферол (минимум < 1 мг/г);
- 45 мг/г гамма-токоферол (минимум 25 мг/г);
- 12 мг/г дельта-токоферол (минимум 3 мг/г);
- 67 мг/г альфа-токотриенол (минимум 30 мг/г);
- < 1 мг/г бета-токотриенол (минимум < 1 мг/г);
- 82 мг/г гамма-токотриенол (минимум 45 мг/г);
- 5 мг/г дельта-токотриенол (минимум < 1 мг/г).
a) филлохинон (фитоменадион)
b) менахинон <*>
--------------------------------
<*> Менахинон встречается, главным образом, в форме менахинона-7 и в меньшей степени в форме менахинона-6.
a) тиамина гидрохлорид
b) тиамина мононитрат
c) тиамина монофосфат хлорид
d) тиамина пирофосфат хлорид
a) рибофлавин
b) рибофлавин 5'-фосфат натрия
a) никотиновая кислота
b) никотинамид
c) инозитола гексаникотинат (инозитола гексаниацинат)
a) D-пантотенат кальция
b) D-пантотенат натрия
c) декспантенол
d) пантетин
a) пиридоксина гидрохлорид
b) пиридоксин 5'-фосфат
c) пиридоксаль 5'-фосфат
a) птероилмоноглютаминовая кислота
b) кальция L-метилфолат
a) цианокобаламин
b) гидроксокобаламин
c) 5'-дезоксиаденозилкобаламин
d) метилкобаламин
a) D-биотин
a) L-аскорбиновая кислота
b) натрия L-аскорбат
c) кальция L-аскорбат <*>
--------------------------------
d) калия L-аскорбат
e) L-аскорбил 6-пальмитат
f) магния L-аскорбат
g) цинка L-аскорбат
кальция ацетат
кальция L-аскорбат
кальция бисглицинат
кальция карбонат
кальция хлорид
кальция цитрат малат
кальциевые соли лимонной кислоты
кальция глюконат
кальция глицерофосфат
кальция лактат
кальция пируват
кальциевые соли ортофосфорной кислоты
кальция сукцинат
кальция гидроксид
кальция L-лизинат
кальция малат
кальция оксид
кальция L-пидолат
кальция L-треонат
кальция сульфат
магния ацетат
магния L-аскорбат
магния бисглицинат
магния карбонат
магния хлорид
магниевые соли лимонной кислоты
магния глюконат
магния глицерофосфат
магниевые соли ортофосфорной кислоты
магния лактат
магния L-лизинат
магния гидроксид
магния малат
магния оксид
магния L-пидолат
магния-калия цитрат
магния пируват
магния сукцинат
магния сульфат
магния таурат
магния ацетил таурат
железа карбонат
железа цитрат
железо-аммонийный цитрат
железа глюконат
железа фумарат
натрий-железа дифосфат
железа лактат
железа сульфат
железа дифосфат (железа пирофосфат)
железа сахарат
элементарное железо (карбонильное + электролитическое + водородное восстановление)
железа бисглицинат
железа L-пидолат
железа фосфат
железо-аммоний фосфат
железа натриевая соль ЭДТА
железа (II) таурат
меди карбонат
меди цитрат
меди глюконат
меди сульфат
меди L-аспартат
меди бисглицинат
меди лизиновый комплекс
меди (II) оксид
натрия йодид
натрия йодат
калия йодид
калия йодат
цинка ацетат
цинка L-аскорбат
цинка L-аспартат
цинка бисглицинат
цинка хлорид
цинка цитрат
цинка глюконат
цинка лактат
цинка L-лизинат
цинка малат
цинка моно-L-метионин сульфат
цинка оксид
цинка карбонат
цинка L-пидолат
цинка пиколинат
цинка сульфат
марганца аскорбат
марганца L-аспартат
марганца бисглицинат
марганца карбонат
марганца хлорид
марганца цитрат
марганца глюконат
марганца глицерофосфат
марганца пидолат
марганца сульфат
натрия бикарбонат
натрия карбонат
натрия хлорид
натрия цитрат
натрия глюконат
натрия лактат
натрия гидроксид
натриевые соли ортофосфорной кислоты
натрия сульфат
калия сульфат
калия бикарбонат
калия карбонат
калия хлорид
калия цитрат
калия глюконат
калия глицерофосфат
калия лактат
калия гидроксид
калия L-пидолат
калия малат
калийные соли ортофосфорной кислоты
L-селенометионин
обогащенные селеном дрожжи <*>
--------------------------------
<*> Обогащенные селеном дрожжи искусственно производятся с использованием натрия селенита в качестве источника селена и содержат в 1 г сухого продукта при продаже не более 2,5 мг Se. Преобладающей органической формой селена в дрожжах является селенометионин (от 60 до 85% всего экстрагированного селена в продукте). Содержание других органических соединений селена, включая селеноцистеин, не должно превышать 10% всего экстрагированного селена. Количество неорганического селена в нормальных условиях не должно превышать 1% всего экстрагированного селена.
селенистая кислота
натрия селенат
натрия гидроселенит
натрия селенит
хрома (III) хлорид
хрома (III) лактат тригидрат
хрома нитрат
хрома пиколинат
хрома (III) сульфат
аммония молибдат (молибден (VI))
калия молибдат (молибден (VI))
натрия молибдат (молибден (VI))
кальция фторид
калия фторид
натрия фторид
натрия монофторфосфат
борная кислота
натрия борат
ортокремниевая кислота, стабилизированная холином
кремния диоксид
кремниевая кислота <*>
--------------------------------
OF THE EUROPEAN PARLIAMENT AND OF THE COUNCIL
ON THE APPROXIMATION OF THE LAWS OF THE MEMBER
STATES RELATING TO FOOD SUPPLEMENTS
(Luxembourg, 10.VI.2002)
(Text with EEA relevance)
(Amended by Commission Directive 2006/37/EC
of 30 March 2006, Regulation (EC) No 1137/2008
of the European Parliament and of the Council
of 22 October 2008, Commission Regulation (EC)
No 1170/2009 of 30 November 2009, Commission
Regulation (EU) No 1161/2011 of 14 November 2011)
The European Parliament and the Council of the European Union,
Having regard to the Treaty establishing the European Community, and in particular Article 95 thereof,
Having regard to the proposal from the Commission <*>,
--------------------------------
<*> OJ C 311 E, 31.10.2000, p. 207 and
OJ C 180 E, 26.6.2001, p. 248.
Having regard to the opinion of the Economic and Social Committee <*>,
--------------------------------
<*> OJ C 14, 16.1.2001, p. 42.
Acting in accordance with the procedure laid down in Article 251 of the Treaty <*>,
--------------------------------
<*> Opinion of the European Parliament of 14 February 2001 (OJ C 276, 1.10.2001, p. 126), Council Common Position of 3 December 2001 (OJ C 90 E, 16.4.2002, p. 1) and Decision of the European Parliament of 13 March 2002. Council Decision of 30 May 2002.
Whereas:
(1) There is an increasing number of products marketed in the Community as foods containing concentrated sources of nutrients and presented for supplementing the intake of those nutrients from the normal diet.
(2) Those products are regulated in Member States by differing national rules that may impede their free movement, create unequal conditions of competition, and thus have a direct impact on the functioning of the internal market. It is therefore necessary to adopt Community rules on those products marketed as foodstuffs.
(3) An adequate and varied diet could, under normal circumstances, provide all necessary nutrients for normal development and maintenance of a healthy life in quantities which meet those established and recommended by generally acceptable scientific data. However, surveys show that this ideal situation is not being achieved for all nutrients and by all groups of the population across the Community.
(4) Consumers, because of their particular lifestyles or for other reasons, may choose to supplement their intake of some nutrients through food supplements.
(5) In order to ensure a high level of protection for consumers and facilitate their choice, the products that will be put on to the market must be safe and bear adequate and appropriate labelling.
(6) There is a wide range of nutrients and other ingredients that might be present in food supplements including, but not limited to, vitamins, minerals, amino acids, essential fatty acids, fibre and various plants and herbal extracts.
(7) As a first stage, this Directive should lay down specific rules for vitamins and minerals used as ingredients of food supplements. Food supplements containing vitamins or minerals as well as other ingredients should also be in conformity with the specific rules on vitamins and minerals laid down in this Directive.
(8) Specific rules concerning nutrients, other than vitamins and minerals, or other substances with a nutritional or physiological effect used as ingredients of food supplements should be laid down at a later stage, provided that adequate and appropriate scientific data about them become available. Until such specific Community rules are adopted and without prejudice to the provisions of the Treaty, national rules concerning nutrients or other substances with nutritional or physiological effect used as ingredients of food supplements, for which no Community specific rules have been adopted, may be applicable.
(9) Only vitamins and minerals normally found in, and consumed as part of, the diet should be allowed to be present in food supplements although this does not mean that their presence therein is necessary. Controversy as to the identity of those nutrients that could potentially arise should be avoided. Therefore, it is appropriate to establish a positive list of those vitamins and minerals.
(10) There is a wide range of vitamin preparations and mineral substances used in the manufacture of food supplements currently marketed in some Member States that have not been evaluated by the Scientific Committee on Food and consequently are not included in the positive lists. These should be submitted to the European Food Safety Authority for urgent evaluation, as soon as appropriate files are presented by the interested parties.
(11) The chemical substances used as sources of vitamins and minerals in the manufacture of food supplements should be safe and also be available to be used by the body. For this reason, a positive list of those substances should also be established. Such substances as have been approved by the Scientific Committee on Food, on the basis of the said criteria, for use in the manufacture of foods intended for infants and young children and other foods for particular nutritional uses can also be used in the manufacture of food supplements.
(12) In order to keep up with scientific and technological developments it is important to revise the lists promptly, when necessary. Such revisions would be implementing measures of a technical nature and their adoption should be entrusted to the Commission in order to simplify and expedite the procedure.
(13) Excessive intake of vitamins and minerals may result in adverse effects and therefore necessitate the setting of maximum safe levels for them in food supplements, as appropriate. Those levels must ensure that the normal use of the products under the instructions of use provided by the manufacturer will be safe for the consumer.
(14) When maximum levels are set, therefore, account should be taken of the upper safe levels of the vitamins and minerals, as established by scientific risk assessment based on generally acceptable scientific data, and of intakes of those nutrients from the normal diet. Due account should also be taken of reference intake amounts when setting maximum levels.
(15) Food supplements are purchased by consumers for supplementing intakes from the diet. In order to ensure that this aim is achieved, if vitamins and minerals are declared on the label of food supplements, they should be present in the product in a significant amount.
(16) The adoption of the specific values for maximum and minimum levels for vitamins and minerals present in food supplements, based on the criteria set out in this Directive and appropriate scientific advice, would be an implementing measure and should be entrusted to the Commission.
(17) General labelling provisions and definitions are contained in Directive 2000/13/EC of the European Parliament and of the Council of 20 March 2000 on the approximation of the laws of the Member States relating to the labelling, presentation and advertising of foodstuffs <*>, and do not need to be repeated. This Directive should therefore be confined to the necessary additional provisions.
--------------------------------
<*> OJ L 109, 6.5.2000, p. 29.
(18) Council Directive 90/496/EEC of 24 September 1990 on nutrition labelling for foodstuffs <*> does not apply to food supplements. Information relating to nutrient content in food supplements is essential for allowing the consumer who purchases them to make an informed choice and use them properly and safely. That information should, in view of the nature of those products, be confined to the nutrients actually present and be compulsory.
--------------------------------
<*> OJ L 276, 6.10.1990, p. 40.
(19) Given the particular nature of food supplements, additional means to those usually available to monitoring bodies should be available in order to facilitate efficient monitoring of those products.
(20) The measures necessary for the implementation of this Directive should be adopted in accordance with Council Decision 1999/468/EC of 28 June 1999 laying down the procedures for the exercise of implementing powers conferred on the Commission <*>,
--------------------------------
<*> OJ L 184, 17.7.1999, p. 23.
Have adopted this Directive:
1. This Directive concerns food supplements marketed as foodstuffs and presented as such. These products shall be delivered to the ultimate consumer only in a pre-packaged form.
2. This Directive shall not apply to medicinal products as defined by Directive 2001/83/EC of the European Parliament and of the Council of 6 November 2001 on the Community code relating to medicinal products for human use <*>.
--------------------------------
<*> OJ L 311, 28.11.2001, p. 67.
For the purposes of this Directive:
(a) "food supplements" means foodstuffs the purpose of which is to supplement the normal diet and which are concentrated sources of nutrients or other substances with a nutritional or physiological effect, alone or in combination, marketed in dose form, namely forms such as capsules, pastilles, tablets, pills and other similar forms, sachets of powder, ampoules of liquids, drop dispensing bottles, and other similar forms of liquids and powders designed to be taken in measured small unit quantities;
(b) "nutrients" means the following substances:
(i) vitamins,
(ii) minerals.
Member States shall ensure that food supplements may be marketed within the Community only if they comply with the rules laid down in this Directive.
1. Only vitamins and minerals listed in Annex I, in the forms listed in Annex II, may be used for the manufacture of food supplements, subject to paragraph 6.
2. The purity criteria for substances listed in Annex II to this Directive shall be adopted by the Commission, except where such criteria apply pursuant to paragraph 3. Those measures, designed to amend non-essential elements of this Directive by supplementing it, shall be adopted in accordance with the regulatory procedure with scrutiny referred to in Article 13(3).
3. Purity criteria for substances listed in Annex II, specified by Community legislation for their use in the manufacture of foodstuffs for purposes other than those covered by this Directive, shall apply.
4. For those substances listed in Annex II for which purity criteria are not specified by Community legislation, and until such specifications are adopted, generally acceptable purity criteria recommended by international bodies shall be applicable and national rules setting stricter purity criteria may be maintained.
5. Modifications to the lists referred to in paragraph 1, designed to amend non-essential elements of this Directive, shall be adopted in accordance with the regulatory procedure with scrutiny referred to in Article 13(3). On imperative grounds of urgency, the Commission may have recourse to the urgency procedure referred to in Article 13(4) in order to remove a vitamin or a mineral from the list referred to in paragraph 1 of this Article.
6. By way of derogation from paragraph 1 and until 31 December 2009, Member States may allow in their territory the use of vitamins and minerals not listed in Annex I, or in forms not listed in Annex II, provided that:
(a) the substance in question is used in one or more food supplements marketed in the Community on the date of entry into force of this Directive,
(b) the European Food Safety Authority has not given an unfavourable opinion in respect of the use of that substance, or its use in that form, in the manufacture of food supplements, on the basis of a dossier supporting use of the substance in question to be submitted to the Commission by the Member State not later than 12 July 2005.
7. Notwithstanding paragraph 6, Member States may, in compliance with the rules of the Treaty, continue to apply existing national restrictions or bans on trade in food supplements containing vitamins and minerals not included in the list in Annex I or in the forms not listed in Annex II.
8. Not later than 12 July 2007, the Commission shall submit to the European Parliament and the Council a report on the advisability of establishing specific rules, including, where appropriate, positive lists, on categories of nutrients or of substances with a nutritional or physiological effect other than those referred to in paragraph 1, accompanied by any proposals for amendment to this Directive which the Commission deems necessary.
1. Maximum amounts of vitamins and minerals present in food supplements per daily portion of consumption as recommended by the manufacturer shall be set, taking the following into account:
(a) upper safe levels of vitamins and minerals established by scientific risk assessment based on generally accepted scientific data, taking into account, as appropriate, the varying degrees of sensitivity of different consumer groups;
(b) intake of vitamins and minerals from other dietary sources.
2. When the maximum levels referred to in paragraph 1 are set, due account should also be taken of reference intakes of vitamins and minerals for the population.
3. To ensure that significant amounts of vitamins and minerals are present in food supplements, minimum amounts per daily portion of consumption as recommended by the manufacturer shall be set, as appropriate.
4. The maximum and minimum amounts of vitamins and minerals referred to in paragraphs 1, 2 and 3 shall be adopted by the Commission. Those measures, designed to amend non-essential elements of this Directive by supplementing it, shall be adopted in accordance with the regulatory procedure with scrutiny referred to in Article 13(3).
1. For the purposes of Article 5(1) of Directive 2000/13/EC, the name under which products covered by this Directive are sold shall be "food supplement".
2. The labelling, presentation and advertising must not attribute to food supplements the property of preventing, treating or curing a human disease, or refer to such properties.
3. Without prejudice to Directive 2000/13/EC, the labelling shall bear the following particulars:
(a) the names of the categories of nutrients or substances that characterise the product or an indication of the nature of those nutrients or substances;
(b) the portion of the product recommended for daily consumption;
(c) a warning not to exceed the stated recommended daily dose;
(d) a statement to the effect that food supplements should not be used as a substitute for a varied diet;
(e) a statement to the effect that the products should be stored out of the reach of young children.
The labelling, presentation and advertising of food supplements shall not include any mention stating or implying that a balanced and varied diet cannot provide appropriate quantities of nutrients in general.
Rules for implementing this Article may be specified in accordance with the procedure referred to in Article 13(2).
1. The amount of the nutrients or substances with a nutritional or physiological effect present in the product shall be declared on the labelling in numerical form. The units to be used for vitamins and minerals shall be those specified in Annex I.
Rules for implementing this paragraph may be specified in accordance with the procedure referred to in Article 13(2).
2. The amounts of the nutrients or other substances declared shall be those per portion of the product as recommended for daily consumption on the labelling.
3. Information on vitamins and minerals shall also be expressed as a percentage of the reference values mentioned, as the case may be, in the Annex to Directive 90/496/EEC.
1. The declared values mentioned in Article 8(1) and (2) shall be average values based on the manufacturer's analysis of the product.
Further rules for implementing this paragraph with regard in particular to the differences between the declared values and those established in the course of official checks shall be decided upon in accordance with the procedure referred to in Article 13(2).
2. The percentage of the reference values for vitamins and minerals mentioned in Article 8(3) may also be given in graphical form.
Rules for implementing this paragraph may be adopted in accordance with the procedure referred to in Article 13(2).
To facilitate efficient monitoring of food supplements, Member States may require the manufacturer or the person placing the product on the market in their territory to notify the competent authority of that placing on the market by forwarding it a model of the label used for the product.
1. Without prejudice to Article 4(7), Member States shall not, for reasons related to their composition, manufacturing specifications, presentation or labelling, prohibit or restrict trade in products referred to in Article 1 which comply with this Directive and, where appropriate, with Community acts adopted in implementation of this Directive.
2. Without prejudice to the Treaty, in particular Articles 28 and 30 thereof, paragraph 1 shall not affect national provisions which are applicable in the absence of Community acts adopted under this Directive.
1. Where a Member State, as a result of new information or of a reassessment of existing information made since this Directive or one of the implementing Community acts was adopted, has detailed grounds for establishing that a product referred to in Article 1 endangers human health though it complies with the said Directive or said acts, that Member State may temporarily suspend or restrict application of the provisions in question within its territory. It shall immediately inform the other Member States and the Commission thereof and give reasons for its decision.
2. The Commission shall examine as soon as possible the grounds adduced by the Member State concerned and shall consult the Member States within the Standing Committee on the Food Chain and Animal Health, and shall then deliver its opinion without delay and take appropriate measures.
3. In order to remedy the difficulties described in paragraph 1 and to ensure the protection of human health, adaptations of this Directive or of its implementing measures shall be adopted by the Commission. Those measures, designed to amend non-essential elements of this Directive, inter alia, by supplementing it, shall be adopted in accordance with the regulatory procedure with scrutiny referred to in Article 13(3). On imperative grounds of urgency, the Commission may have recourse to the urgency procedure referred to in Article 13(4) in order to adopt those adaptations. The Member State that has adopted safeguard measures may in that event retain such measures until the adoption of the adaptations.
1. The Commission shall be assisted by the Standing Committee on the Food Chain and Animal Health instituted by Regulation (EC) No 178/2002 of the European Parliament and of the Council <*>
--------------------------------
<*> OJ L 31, 1.2.2002, p. 1.
2. Where reference is made to this paragraph, Articles 5 and 7 of Decision 1999/468/EC shall apply, having regard to the provisions of Article 8 thereof.
The period provided for in Article 5(6) of Decision 1999/468/EC shall be set at three months.
3. Where reference is made to this paragraph, Article 5a(1) to (4) and Article 7 of Decision 1999/468/EC shall apply, having regard to the provisions of Article 8 thereof.
4. Where reference is made to this paragraph, Article 5a(1), (2), (4) and (6) and Article 7 of Decision 1999/468/EC shall apply, having regard to the provisions of Article 8 thereof.
Provisions that may have an effect upon public health shall be adopted after consultation with the European Food Safety Authority.
Member States shall bring into force the laws, regulations and administrative provisions necessary to comply with this Directive by 31 July 2003. They shall forthwith inform the Commission thereof.
Those laws, regulations and administrative provisions shall be applied in such a way as to:
(a) permit trade in products complying with this Directive, from 1 August 2003 at the latest;
(b) prohibit trade in products which do not comply with the Directive, from 1 August 2005 at the latest.
When Member States adopt these measures, they shall contain a reference to this Directive or be accompanied by such a reference on the occasion of their official publication. The methods of making such reference shall be adopted by the Member States.
This Directive shall enter into force on the day of its publication in the Official Journal of the European Communities.
This Directive is addressed to the Member States.
VITAMINS AND MINERALS WHICH MAY BE USED
IN THE MANUFACTURE OF FOOD SUPPLEMENTS
Vitamin A (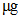 RE)
RE)
Vitamin D 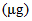
Vitamin E (mg a-TE)
Vitamin K 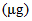
Vitamin B1 (mg)
Vitamin B2 (mg)
Niacin (mg NE)
Pantothenic acid (mg)
Vitamin B6 (mg)
Folic acid 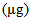 <*>
<*>
--------------------------------
<*> Folic acid is the term included in Annex I of Commission Directive 2008/100/EC of 28 October 2008 amending Council Directive 90/496/EEC on nutrition labelling for foodstuffs as regards recommended daily allowances, energy conversion factors and definitions for nutrition labelling purposes and covers all forms of folates.
Vitamin B12 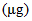
Biotin 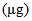
Vitamin C (mg)
Calcium (mg)
Magnesium (mg)
Iron (mg)
Copper 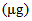
Iodine 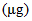
Zinc (mg)
Manganese (mg)
Sodium (mg)
Potassium (mg)
Selenium 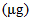
Chromium 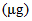
Molybdenum 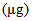
Fluoride (mg)
Chloride (mg)
Phosphorus (mg)
Boron (mg)
Silicon (mg)
VITAMIN AND MINERAL SUBSTANCES WHICH MAY BE USED
IN THE MANUFACTURE OF FOOD SUPPLEMENTS
(a) retinol
(b) retinyl acetate
(c) retinyl palmitate
(d) beta-carotene
(a) cholecalciferol
(b) ergocalciferol
(a) D-alpha-tocopherol
(b) DL-alpha-tocopherol
(c) D-alpha-tocopheryl acetate
(d) DL-alpha-tocopheryl acetate
(e) D-alpha-tocopheryl acid succinate
(f) mixed tocopherols <*>
--------------------------------
<*> alpha-tocopherol < 20%, beta-tocopherol < 10%, gamma-tocopherol 50 - 70% and delta-tocopherol 10 - 30%
(g) tocotrienol tocopherol <*>
--------------------------------
<*> Typical levels of individual tocopherols and tocotrienols:
- 115 mg/g alpha-tocopherol (101 mg/g minimum),
- 5 mg/g beta-tocopherol (< 1 mg/g minimum),
- 45 mg/g gamma-tocopherol (25 mg/g minimum),
- 12 mg/g delta-tocopherol (3 mg/g minimum),
- 67 mg/g alpha-tocotrienol (30 mg/g minimum),
- < 1 mg/g beta-tocotrienol (< 1 mg/g minimum),
- 82 mg/g gamma-tocotrienol (45 mg/g minimum),
- 5 mg/g delta-tocotrienol (< 1 mg/g minimum),
(a) phylloquinone (phytomenadione)
(b) menaquinone <*>
--------------------------------
<*> Menaquinone occurring principally as menaquinone-7 and, to a minor extent, mena-quinone-6.
(a) thiamin hydrochloride
(b) thiamin mononitrate
(c) thiamine monophosphate chloride
(d) thiamine pyrophosphate chloride
(a) riboflavin
(b) riboflavin 5'-phosphate, sodium
(a) nicotinic acid
(b) nicotinamide
(c) inositol hexanicotinate (inositol hexaniacinate)
(a) D-pantothenate, calcium
(b) D-pantothenate, sodium
(c) dexpanthenol
(d) pantethine
(a) pyridoxine hydrochloride
(b) pyridoxine 5'-phosphate
(c) pyridoxal 5'-phosphate
(a) pteroylmonoglutamic acid
(b) calcium-L-methylfolate
(a) cyanocobalamin
(b) hydroxocobalamin
(c) 5'-deoxyadenosylcobalamin
(d) methylcobalamin
(a) D-biotin
(a) L-ascorbic acid
(b) sodium-L-ascorbate
(c) calcium-L-ascorbate <*>
--------------------------------
<*> May contain up to 2% of threonate.
(d) potassium-L-ascorbate
(e) L-ascorbyl 6-palmitate
(f) magnesium L-ascorbate
(g) zinc L-ascorbate
calcium acetate
calcium L-ascorbate
calcium bisglycinate
calcium carbonate
calcium chloride
calcium citrate malate
calcium salts of citric acid
calcium gluconate
calcium glycerophosphate
calcium lactate
calcium pyruvate
calcium salts of orthophosphoric acid
calcium succinate
calcium hydroxide
calcium L-lysinate
calcium malate
calcium oxide
calcium L-pidolate
calcium L-threonate
calcium sulphate
magnesium acetate
magnesium L-ascorbate
magnesium bisglycinate
magnesium carbonate
magnesium chloride
magnesium salts of citric acid
magnesium gluconate
magnesium glycerophosphate
magnesium salts of orthophosphoric acid
magnesium lactate
magnesium L-lysinate
magnesium hydroxide
magnesium malate
magnesium oxide
magnesium L-pidolate
magnesium potassium citrate
magnesium pyruvate
magnesium succinate
magnesium sulphate
magnesium taurate
magnesium acetyl taurate
ferrous carbonate
ferrous citrate
ferric ammonium citrate
ferrous gluconate
ferrous fumarate
ferric sodium diphosphate
ferrous lactate
ferrous sulphate
ferric diphosphate (ferric pyrophosphate)
ferric saccharate
elemental iron (carbonyl + electrolytic + hydrogen reduced)
ferrous bisglycinate
ferrous L-pidolate
ferrous phosphate
ferrous ammonium phosphate
ferric sodium EDTA
iron (II) taurate
cupric carbonate
cupric citrate
cupric gluconate
cupric sulphate
copper L-aspartate
copper bisglycinate
copper lysine complex
copper (II) oxide
sodium iodide
sodium iodate
potassium iodide
potassium iodate
zinc acetate
zinc L-ascorbate
zinc L-aspartate
zinc bisglycinate
zinc chloride
zinc citrate
zinc gluconate
zinc lactate
zinc L-lysinate
zinc malate
zinc mono-L-methionine sulphate
zinc oxide
zinc carbonate
zinc L-pidolate
zinc picolinate
zinc sulphate
manganese ascorbate
manganese L-aspartate
manganese bisglycinate
manganese carbonate
manganese chloride
manganese citrate
manganese gluconate
manganese glycerophosphate
manganese pidolate
manganese sulphate
sodium bicarbonate
sodium carbonate
sodium chloride
sodium citrate
sodium gluconate
sodium lactate
sodium hydroxide
sodium salts of orthophosphoric acid
sodium sulphate
potassium sulphate
potassium bicarbonate
potassium carbonate
potassium chloride
potassium citrate
potassium gluconate
potassium glycerophosphate
potassium lactate
potassium hydroxide
potassium L-pidolate
potassium malate
potassium salts of orthophosphoric acid
L-selenomethionine
selenium enriched yeast <*>
--------------------------------
<*> Selenium-enriched yeasts produced by culture in the presence of sodium selenite as selenium source and containing, in the dried form as marketed, not more than 2,5 mg Se/g. The predominant organic selenium species present in the yeast is selenomethionine (between 60 and 85% of the total extracted selenium in the product). The content of other organic selenium compounds including selenocysteine shall not exceed 10% of total extracted selenium. Levels of inorganic selenium normally shall not exceed 1% of total extracted selenium.
selenious acid
sodium selenate
sodium hydrogen selenite
sodium selenite
chromium (III) chloride
chromium (III) lactate trihydrate
chromium nitrate
chromium picolinate
chromium (III) sulphate
ammonium molybdate (molybdenum (VI))
potassium molybdate (molybdenum (VI))
sodium molybdate (molybdenum (VI))
calcium fluoride
potassium fluoride
sodium fluoride
sodium monofluorophosphate
boric acid
sodium borate
choline-stabilised orthosilicic acid
silicon dioxide
silicic acid <*>
--------------------------------
<*> In the form of gel.