Скачать ГОСТ Р ИСО 20857-2016 Стерилизация медицинской продукции. Горячий воздух. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий
Дата актуализации: 01.01.2021

 ГОСТ Р ИСО 20857-2016
ГОСТ Р ИСО 20857-2016
Стерилизация медицинской продукции. Горячий воздух. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий
| Обозначение: |  ГОСТ Р ИСО 20857-2016 ГОСТ Р ИСО 20857-2016 |
| Обозначение англ: |  GOST R ISO 20857-2016 GOST R ISO 20857-2016 |
| Статус: | введен впервые |
| Название рус.: | Стерилизация медицинской продукции. Горячий воздух. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий |
| Название англ.: | Sterilization of medical devices. Dry heat. Requirements for development, validation and routine control of a sterilization process for medical devices |
| Дата добавления в базу: | 01.02.2017 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.03.2017 |
| Область применения: | Стандарт определяет требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий горячим воздухом. Несмотря на то, что область применения стандарта ограничивается медицинскими изделиями, описанные в нем требования и приведенные рекомендации могут применяться к иной медицинской продукции. Несмотря на то, что в стандарте речь идет, прежде всего, о стерилизации горячим воздухом, в нем также приведены требования и руководство в отношении процессов депирогенизации с применением горячего воздуха. |
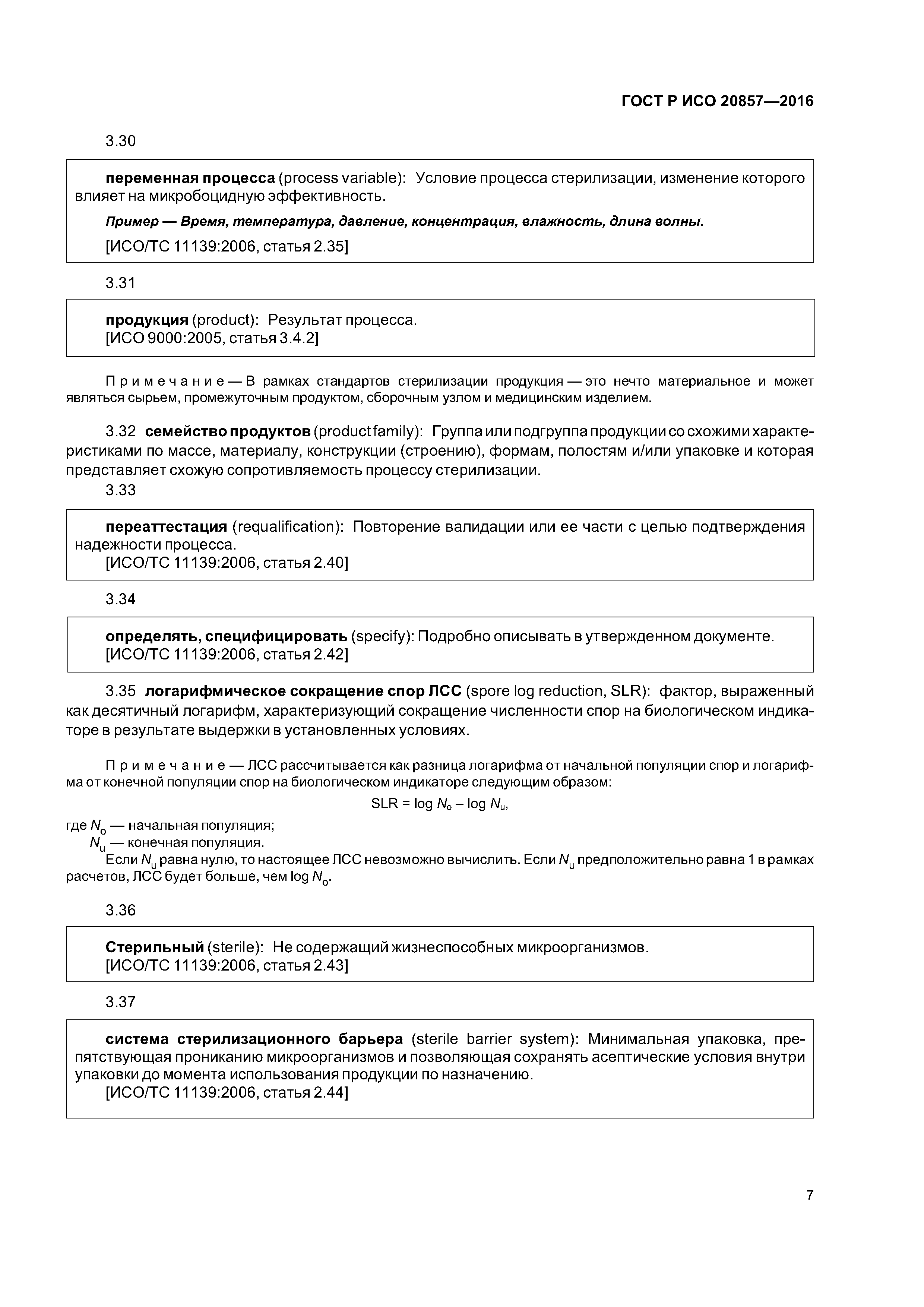
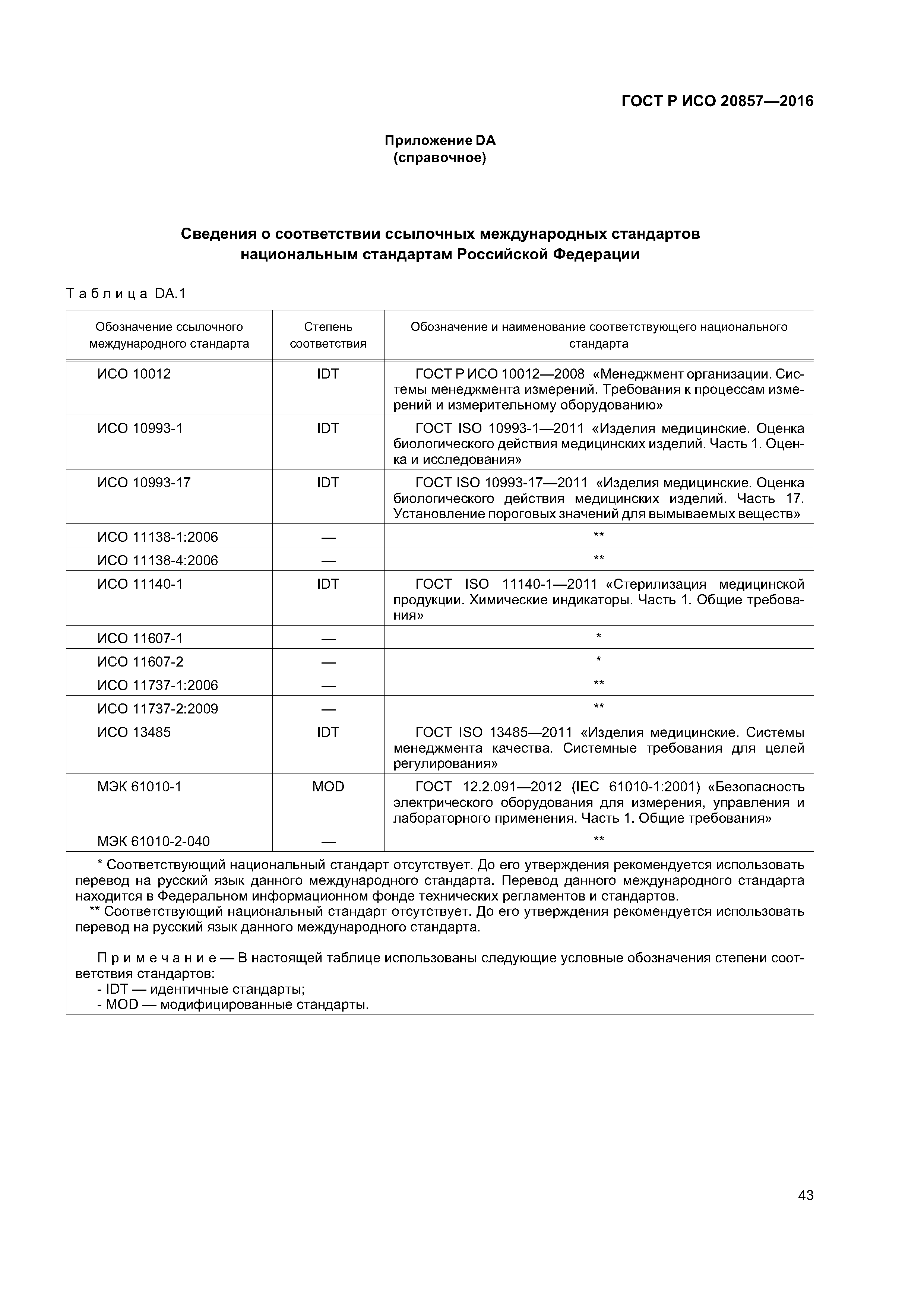
| Оглавление: | 1 Область применения 1.1 Включения 1.2 Исключения 2 Нормативные ссылки 3 Термины и определения 4 Элементы системы менеджмента качества 4.1 Документирование 4.2 Ответственность руководства 4.3 Реализация продукции 4.4 Измерения, анализ и улучшение - Контроль несоответствующей продукции 5 Описание стерилизующего агента 5.1 Стерилизующий агент 5.2 Микробоцидная эффективность 5.3 Воздействие на материалы 5.4 Воздействие на окружающую среду 6 Описание процесса и оборудования 6.1 Описание процесса 6.2 Описание оборудования 7 Определение продукта 7.1 Общая информация 7.2 Безопасность и рабочие характеристики продукта 7.3 Требования к упаковке 7.4 Микробиологическое качество 7.5 Семейство продуктов 7.6 Биологическая безопасность 8 Определение процесса 9 Валидация 9.1 Общая информация 9.2 Аттестация монтажа 9.3 Аттестация функционирования 9.4 Аттестация эксплуатируемого оборудования 9.5 Дополнительные стерилизационные системы 9.6 Анализ и утверждение валидации 10 Текущий мониторинг и контроль 10.1 Текущий контроль 10.2 Текущий мониторинг 10.3 Точки мониторинга процесса 11 Выпуск продукта после стерилизации/депирогенизации 12 Поддержание эффективности процесса 12.1 Общая информация 12.2 Повторная калибровка 12.3 Обслуживание оборудования 12.4 Переаттестация 12.5 Оценка изменений Приложение А (справочное) Руководство по применению настоящего стандарта Приложение В (справочное) Определение процесса, основанное на инактивации микробной популяции в ее естественном состоянии (метод/подход, основанный на бионагрузке) Приложение С (нормативное) Определение процесса, основанное на инактивации контрольных микроорганизмов и знании бионагрузки (комбинированный метод бионагрузки/биологического индикатора) Приложение D (справочное) Консервативное определение процесса, основанное на инактивации контрольных микроорганизмов (метод полной гибели) Приложение Е (справочное) Разработка процесса Приложение DA (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации Библиография |
| Разработан: | ООО ФАРМСТЕР ООО НПФ Винар |
| Утверждён: | 17.03.2016 Федеральное агентство по техническому регулированию и метрологии (161-ст) |
| Издан: | Стандартинформ (2016 г. ) |
| Список изменений: |
|
| Нормативные ссылки: |
|




















































 Текстовое изменение Поправка от 13.09.2016
Текстовое изменение Поправка от 13.09.2016


 ГОСТ Р ИСО 10012-2008 «Менеджмент организации. Системы менеджмента измерений. Требования к процессам измерений и измерительному оборудованию»
ГОСТ Р ИСО 10012-2008 «Менеджмент организации. Системы менеджмента измерений. Требования к процессам измерений и измерительному оборудованию»