СПРАВКА
Источник публикации
М.: Бюро НДТ, 2025
Примечание к документу
Документ вводится в действие с 01.09.2026.
Текст документа приведен в соответствии с публикацией на сайте https://www.rst.gov.ru/portal/gost по состоянию на 23.12.2025.
Взамен ИТС 24-2020.
Название документа
"ИТС 24-2025. Информационно-технический справочник по наилучшим доступным технологиям. Производство редких и редкоземельных металлов"
(утв. Приказом Росстандарта от 15.12.2025 N 2763)
"ИТС 24-2025. Информационно-технический справочник по наилучшим доступным технологиям. Производство редких и редкоземельных металлов"
(утв. Приказом Росстандарта от 15.12.2025 N 2763)
Содержание
Приказом Росстандарта
от 15 декабря 2025 г. N 2763
ИНФОРМАЦИОННО-ТЕХНИЧЕСКИЙ СПРАВОЧНИК
ПО НАИЛУЧШИМ ДОСТУПНЫМ ТЕХНОЛОГИЯМ
ПРОИЗВОДСТВО РЕДКИХ И РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
Manufacture of rare and rare-earth metals
ИТС 24-2025
Дата введения
1 сентября 2026 года
Настоящий справочник НДТ представляет собой документ по стандартизации, разработанный в результате анализа технологических, технических и управленческих решений, применяемых при производстве редких металлов (включая редкоземельные).
Справочник НДТ разработан взамен справочника НДТ ИТС 24-2020 "Производство редких и редкоземельных металлов" в соответствии с распоряжением Правительства Российской Федерации от 10 июня 2022 г. N 1537-р "Об утверждении поэтапного графика актуализации информационно-технических справочников по наилучшим доступным технологиям".
Термин "наилучшие доступные технологии" определен в статье 1 Федерального закона N 7-ФЗ "Об охране окружающей среды", согласно которому НДТ - это технология производства продукции (товаров), выполнения работ, оказания услуг, определяемая на основе современных достижений науки и техники и наилучшего сочетания критериев достижения охраны окружающей среды при условии наличия технической возможности ее применения [1].
Структура настоящего справочника НДТ соответствует ГОСТ Р 113.00.03-2019 [2], формат описания технологий - ГОСТ Р 113.00.04-2024 [3], термины приведены в соответствии с ГОСТ Р 113.00.12-2023 [4].
Введение. Во введении приводятся краткое содержание справочника НДТ и обзор законодательных документов, использованных при его разработке.
Предисловие. Указана цель разработки справочника НДТ, его статус, законодательный контекст, краткое описание процедуры создания в соответствии с установленным порядком, а также взаимосвязь с аналогичными международными документами.
Область применения. Описаны основные и дополнительные виды деятельности, на которые распространяется действие справочника НДТ, а также приводится информация о взаимосвязанных видах деятельности, смежных с определенными в ИТС НДТ, и соответствующие виды деятельности ИТС НДТ.
В разделе 1 представлена информация о состоянии и уровне развития в Российской Федерации производства редких и щелочноземельных (магний и кальций) металлов по основным переделам. Также в разделе 1 приведен краткий обзор экологических аспектов производства.
В разделе 2 представлены сведения о технологических процессах, применяемых при производстве:
- легких редких металлов;
- рассеянных редких металлов;
- тугоплавких редких металлов;
- редкоземельных металлов;
- щелочноземельных металлов (магний и кальций);
- вспомогательных производственных процессов.
Для каждой стадии указывают входные и выходные материальные потоки, основные энергетические потоки, условия проведения процесса или основные операции, основные эмиссии.
Рассмотрены вопросы, касающиеся оценки затрат промышленных предприятий по производству редких металлов на реализацию отдельных природоохранных мероприятий, в том числе на приобретение, монтаж, наладку и эксплуатацию оборудования, которое обеспечивает сокращение эмиссий загрязняющих веществ в окружающую среду.
В разделе 3 дана оценка текущих уровней потребления сырья, материалов, энергетических ресурсов и эмиссий, маркерных веществ, характерных для производства редких металлов в Российской Федерации.
Также приведено описание особенностей производственного экологического контроля, в том числе особенностей измерения, включая измерения системами автоматического контроля.
Раздел подготовлен на основе данных, представленных предприятиями Российской Федерации в рамках разработки справочника НДТ, а также различных литературных источников.
В разделе 4 описаны особенности подходов, примененных при разработке данного справочника НДТ и в целом соответствующих Правилам определения технологии в качестве наилучшей доступной технологии, а также разработки, актуализации и опубликования информационно-технических справочников по наилучшим доступным технологиям (утверждены постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458) и Методическим рекомендациям по определению технологии в качестве наилучшей доступной технологии.
В разделе 5 приведено краткое описание НДТ для производства редких металлов, включая:
- системы экологического и энергетического менеджмента, контроля и мониторинга технологических процессов;
- технические и технологические решения для повышения энергоэффективности, ресурсосбережения, снижения эмиссий загрязняющих веществ, методы обращения с отходами и побочными продуктами производства.
В разделе 6 приведены сведения о перспективных технологиях переработки сырьевых источников и получения чистых металлов.
Заключительные положения и рекомендации. Приведены сведения о членах технической рабочей группы, принимавших участие в разработке справочника НДТ. Рекомендации предприятиям по дальнейшим исследованиям экологических аспектов их деятельности.
Приложения. Приведен перечень маркерных загрязняющих веществ, перечень технологических показателей, перечень НДТ, сведения о ресурсной (в том числе, энергетической) эффективности, а также "Заключение по наилучшим доступным технологиям" для рассматриваемой отрасли промышленности.
"Заключение по наилучшим доступным технологиям" включает части ИТС НДТ, содержащие:
- область применения;
- описание НДТ, уровни эмиссий, соответствующие НДТ (технологические показатели), а также информацию, позволяющую оценить их применимость;
- методы производственного экологического контроля.
"Заключение по наилучшим доступным технологиям" сформировано для использования заинтересованными лицами, в том числе промышленными предприятиями, при формировании заявок на комплексные экологические разрешения, а также надзорными органами при выдаче комплексных экологических разрешений и является кратким описанием основных положений ИТС НДТ, включая описание наилучших доступных технологий, информации, позволяющей оценить их применимость, уровни эмиссий и потребления ресурсов, методы производственного экологического контроля.
Библиография. Приведен перечень источников информации, использованных при разработке настоящего справочника НДТ.
Цели, основные принципы и порядок разработки информационно-технического справочника по наилучшим доступным технологиям установлены постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458. Перечень областей применения наилучших доступных технологий определен распоряжением Правительства Российской Федерации от 24 декабря 2014 г. N 2674-р.
1 Статус документа
Настоящий информационно-технический справочник по наилучшим доступным технологиям (далее - справочник НДТ) является документом по стандартизации.
2 Разработчик
Справочник НДТ разработан технической рабочей группой N 24 (ТРГ 24) "Производство редких и редкоземельных металлов", состав которой утвержден приказом Минпромторга России от 07 марта 2025 г. N 1125.
Перечень организаций и их представителей, принимавших участие в разработке настоящего справочника НДТ, приведен в разделе "Заключительные положения и рекомендации".
3 Краткая характеристика
Настоящий справочник НДТ содержит описание применяемых при производстве редких и щелочноземельных металлов технологических процессов, оборудования, технических способов, методов, в том числе позволяющих снизить негативное воздействие на окружающую природную среду, водопотребление, повысить энергоэффективность, обеспечить экономию ресурсов на предприятиях, относящихся к областям применения НДТ, определенным распоряжением Правительства РФ от 24 декабря 2014 г. N 2674-р. Из числа описанных технологических процессов, технических способов, методов выделены решения, отнесенные к наилучшим доступным технологиям (НДТ), установлены технологические показатели.
Разработка (актуализация) справочника НДТ проводилась в соответствии с порядком, утвержденным постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458 "О порядке определения технологии в качестве наилучшей доступной технологии, а также разработки, актуализации и опубликования информационно-технических справочников по наилучшим доступным технологиям".
4 Сбор данных
Информация о технологических процессах, оборудовании, технических способах, методах, применяемых при производстве редких и редкоземельных металлов в Российской Федерации, собрана в соответствии с Порядком сбора данных, необходимых для разработки информационно-технического справочника по наилучшим доступным технологиям, утвержденным приказом Минпромторга России от 18 декабря 2019 г. N 4841.
5 Взаимосвязь с другими справочниками НДТ
Взаимосвязь настоящего справочника НДТ с другими справочниками НДТ, разрабатываемыми (актуализируемыми) в соответствии с распоряжением Правительства Российской Федерации от 10 июня 2022 г. N 1537-р "Об утверждении поэтапного графика актуализации информационно-технических справочников по наилучшим доступным технологиям", приведена в разделе "Область применения".
6 Информация об утверждении опубликовании и введении в действие
Настоящий справочник НДТ утвержден приказом Росстандарта от 15 декабря 2025 г. N 2763.
Настоящий справочник НДТ введен в действие с 01 сентября 2026 г., официально опубликован в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru).
Настоящий справочник НДТ распространяется на следующие основные виды деятельности:
- процессы производства легких редких металлов;
- процессы производства рассеянных редких металлов;
- процессы производства тугоплавких редких металлов;
- процессы производства редкоземельных металлов;
- процессы производства щелочноземельных металлов (магний и кальций).
Ни один редкий металл не получают непосредственным восстановлением из сырья. Первоначальное сырье обогащают или вскрывают (выщелачивание, спекание), а полученные черновые концентраты и промпродукты перерабатывают в химические соединения. Помимо рудного сырья, источником получения редких металлов являются промышленные отходы цветной и черной металлургии, химических производств.
Справочник НДТ также распространяется на процессы, связанные с основными видами деятельности, которые могут оказать влияние на объемы негативного воздействия и (или) масштабы загрязнения окружающей среды:
- хранение и подготовка сырья;
- хранение и подготовка топлива;
- производственные процессы (химические, пирометаллургические, гидрометаллургические и электролитические);
- методы предотвращения и сокращения выбросов и образования отходов;
- хранение и подготовка продукции
Справочник НДТ не распространяется на:
- добычу и обогащение руд и продуктов, содержащих редкие металлы
- процессы производства радиоактивных металлов;
- вопросы, которые касаются исключительно обеспечения промышленной безопасности или охраны труда.
Вопросы обеспечения промышленной безопасности и охраны труда частично рассматриваются только в тех случаях, когда оказывают влияние на виды деятельности, включенные в область применения настоящего справочника НДТ.
Дополнительные виды деятельности при производстве редких металлов и соответствующие им справочники НДТ (названия справочников НДТ даны в редакции распоряжения Правительства Российской Федерации от 31 октября 2014 г. N 2178-р) приведены в таблице ниже.
Таблица 1
металлов и соответствующие им справочники НДТ
Вид деятельности | Соответствующий справочник НДТ |
Методы очистки сточных вод, направленные на сокращение сбросов металлов в водные объекты | ИТС НДТ 8 "Очистка сточных вод при производстве продукции (товаров), выполнении работ и оказании услуг на крупных предприятиях" |
Обращение с отходами | ИТС НДТ 15 "Утилизация и обезвреживание отходов (кроме обезвреживания термическим способом (сжигание отходов))" |
Промышленные системы охлаждения, например, градирни, пластинчатые теплообменники | ИТС НДТ 20 "Промышленные системы охлаждения" |
Производство оксида магния, гидроксида магния, хлорида магния | ИТС НДТ 21 "Производство оксида магния, гидроксида магния, хлорида магния" |
Методы очистки выбросов загрязняющих веществ в атмосферный воздух | ИТС НДТ 22 "Очистка выбросов вредных (загрязняющих) веществ в атмосферный воздух при производстве продукции (товаров), а также при проведении работ и оказании услуг на крупных предприятиях" |
Общие принципы производственного экологического контроля | ИТС НДТ 22.1 "Общие принципы производственного экологического контроля и его метрологического обеспечения" |
Хранение и обработка материалов | ИТС НДТ 46 "Сокращение выбросов загрязняющих веществ, сбросов загрязняющих веществ при хранении и складировании товаров (грузов)" |
Повышение энергетической эффективности | ИТС НДТ 48 "Повышение энергетической эффективности при осуществлении хозяйственной и (или) иной деятельности" |
Таблица 2
Сфера распространения ИТС НДТ
Наименование продукции по ОК 034-2014 (ОКПД) | Наименование вида деятельности по ОКВЭД 2 | ||||||
Вольфрам и изделия из него, сплавы на основе вольфрама, порошки | Производство вольфрама | ||||||
Вольфрам необработанный, включая прутки, изготовленные простым спеканием | |||||||
Молибден и изделия из него, сплавы на основе молибдена, порошки | Производство молибдена | ||||||
Молибден необработанный, включая прутки, изготовленные простым спеканием | |||||||
Магний и изделия из него, сплавы на основе магния, порошки | Производство магния | ||||||
Титан и изделия из него, сплавы на основе титана, порошки | Производство титана | ||||||
Титан необработанный | |||||||
Проволока, прутки, профили титановые | |||||||
Плиты, листы, полосы и ленты титановые | |||||||
Трубы и трубки титановые | |||||||
Поковки, штамповки, кольца титановые | |||||||
Ванадий и изделия из него, порошок | Производство редких (тантал, ниобий, галлий, германий, иридий) металлов | ||||||
Ванадий необработанный | |||||||
Цирконий и изделия из него, сплавы на основе циркония, порошки | |||||||
Цирконий необработанный | |||||||
Ниобий и изделия из него, сплавы на основе ниобия, порошки | |||||||
Ниобий необработанный | |||||||
Тантал и изделия из него, сплавы на основе тантала, порошки | |||||||
Тантал необработанный, включая прутки, изготовленные простым спеканием | |||||||
Бериллий и изделия из него, сплавы на основе бериллия, порошки | Производство редких (тантал, ниобий, галлий, германий, иридий) и редкоземельных металлов | ||||||
Бериллий необработанный | |||||||
Германий и изделия из него, порошки | |||||||
Германий необработанный | |||||||
Галлий и изделия из него, сплавы на основе галлия, порошки | |||||||
Галлий необработанный | |||||||
Индий и изделия из него, порошки | |||||||
Индий необработанный | |||||||
Рений и изделия из него, порошки | |||||||
Рений необработанный | |||||||
Таллий и изделия из него, порошки | |||||||
Таллий необработанный | |||||||
Гафний и изделия из него, порошки | |||||||
Гафний необработанный | |||||||
| |||||||
Вещества химические неорганические основные прочие | Производство прочих основных неорганических химических веществ | ||||||
Теллур | |||||||
Селен | |||||||
Металлы редкоземельные в чистом виде, в смесях, сплавах | |||||||
Иттрий | |||||||
Гадолиний | |||||||
Тербий | |||||||
Диспрозий | |||||||
Гольмий | |||||||
Эрбий | |||||||
Тулий | |||||||
Иттербий | |||||||
Лютеций | |||||||
Скандий | |||||||
Лантан металлический | |||||||
Церий металлический | |||||||
Празеодим металлический | |||||||
Неодим металлический и неодим в лигатуре | |||||||
Самарий | |||||||
Европий | |||||||
Сплавы церийсодержащие | |||||||
Сплавы и лигатуры на основе редкоземельных металлов прочие | |||||||
Кальций | |||||||
Соединения редкоземельных металлов, иттрия или скандия | |||||||
Соединения редкоземельных металлов, иттрия или скандия | |||||||
Соединения иттрия | |||||||
Соединения скандия | |||||||
Соединения церия | |||||||
Соединения редкоземельных металлов прочие, не включенные в другие группировки | |||||||
Редкие металлы - исторически сложившееся название большой группы элементов периодической системы Д.И. Менделеева, которые располагаются почти во всех группах и периодах и, соответственно, обладают разными свойствами. По этой причине, ни по их расположению, ни по физико-химическим свойствам эти элементы в единую группу объединить нельзя.
Содержание большинства элементов в земной коре не превышает 0,01 - 0,0001%. Такие элементы принято называть редкими. Если редкие элементы обладают слабой способностью к концентрации, то они именуются редкими рассеянными.
Важнейшие обобщающие характеристики проявляются только в названиях подгрупп в промышленной классификации.
Общепризнанный в настоящее время термин "редкие металлы" возник в начале XX в., когда данные металлы только начали использоваться, т.е. применялись редко. И до настоящего времени этот термин в определенной степени отражает ряд их особенностей:
- сравнительно небольшие масштабы производства и потребления (один из наиболее известных редких металлов рубидий производится в количествах, примерно в 130 раз меньших по сравнению с алюминием);
- малая распространенность в природе, их кларки не превышают 1 x 10-9%; (наиболее распространенный редкий металл рубидий содержится в земной коре в количестве 0,015%);
- большинство редких металлов не образуют в природе самостоятельных минералов и находятся в рассеянном состоянии в кристаллических решетках других минералов, многие из них являются природными спутниками тяжелых и легких цветных металлов;
- очень низкое содержание в рудах и крайне сложный состав рудного сырья;
- помимо рудного сырья, источником получения редких цветных металлов являются промышленные отходы цветной и черной металлургии, химических производств.
Редкими металлами (РМ) в современной технике условно называют некоторые химические элементы, в большинстве, по своим свойствам металлы, области возможного использования, природные ресурсы и технология производства которых уже достаточно определены, но которые еще редко и в относительно малых количествах применяются в промышленности, поскольку при достигнутом ранее уровне техники еще можно было обойтись без их широкого использования. Использование редких металлов началось в конце XIX века. Первым из их числа получил признание вольфрам, за ним - молибден (в настоящее время в ряде документов выведенные из классификации РМ), ниобий, тантал, а затем - постепенно и остальные.
Редкие металлы, согласно промышленной классификации, подразделяют на пять подгрупп в зависимости от физико-химических свойств, совместного нахождения в рудном сырье и сходства методов извлечения из сырья. Важнейшие обобщающие характеристики этих металлов заключены в названиях выделенных подгрупп: легкие, рассеянные, тугоплавкие, редкоземельные и радиоактивные.
Легкие редкие металлы - в данную подгруппу входят редкие металлы I и II групп периодической системы Д.И. Менделеева: бериллий, литий, рубидий и цезий. Их отличают малая плотность (меньше 2 г/см3) и высокая химическая активность. Легкие редкие металлы, как и основные легкие, получают электролизом расплавов солей или металлотермическим способом.
Рассеянные редкие металлы - рений, галлий, индий, таллий, германий, гафний, селен и теллур. Эти металлы присутствуют в малых концентрациях в виде примеси в кристаллических решетках минералов. Рассеянные элементы извлекают попутно при комплексной переработке руд, а также отходов основного производства. Например, рений извлекают при переработке молибденита (молибденсодержащий минерал) и медного сульфидного сырья; галлий содержится в алюминиевых минералах; индий, таллий и германий встречаются в сфалерите и других сульфидных минералах; германий - в каменных углях; рений, селен и теллур - в медном сульфидном сырье.
Тугоплавкие редкие металлы - элементы IV, V и VI групп периодической системы Д.И. Менделеева: титан, цирконий, гафний, ванадий, ниобий, тантал, молибден, вольфрам, рений. Данные элементы характеризуются достройкой электронного d-уровня, который определяет особенности физических и химических свойств рассматриваемой подгруппы металлов: высокую температуру плавления, прочность, коррозионную стойкость, а также переменную валентность, многообразие химических соединений. Все металлы данной группы образуют тугоплавкие и твердые карбиды, бориды и силициды, а также их объединяют области применения.
Редкоземельные элементы (РЗЭ). К ним относятся 17 элементов - это элементы III группы Периодической системы Д.И. Менделеева: скандий, иттрий, а также лантаноиды, объединенные сходством физико-химических свойств: лантан, церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий, лютеций, имеющие одинаковое строения внешних электронных оболочек 6s2 (при переходе от одного элемента к другому происходит заполнение глубоколежащего 4fn-уровня, где n меняется от 0 до 14). В природе РЗЭ всегда встречаются вместе в различных пропорциях, и обладают схожими свойствами. Поэтому получение индивидуальных РЗЭ достаточно сложный многостадийный процесс, требующий соответствующего оборудования. Несмотря на близость свойств РЗМ, каждый из них обладает уникальной особенностью и может быть применен в изделии в виде индивидуального элемента либо в определенной смеси с другими. В настоящее время практически ни одно современное техническое изделие не обходится без присутствия РЗМ - это сплавы металлов, магниты, стекло, катализаторы, сцинтилляторы, экраны гаджетов, медицинские препараты и оборудование, т.д. Непрекращающийся промышленный интерес к индивидуальным РЗЭ и расширение областей их применения, ведет к постоянному росту объемов их потребления и производства. В 2015 г. объем добычи и потребления РЗЭ составлял 124000 т (U.S. Geological Survey (USGS), Mineral Commodity Summarries, January 2011), в 2020 г. практически удвоился до 240000 т (U.S. Geological Survey (USGS), Mineral Commodity Summaries, January 2021), в 2024 г. составил 390000 т (U.S. Geological Survey (USGS), Mineral Commodity Summaries, January 2025). Основными мировыми источниками РЗМ являются бастнезит, монацит, ксенотим. Россия обладает большими запасами РЗМ, различными по составу, и входит в пятерку мировых лидеров, но, несмотря на мировой спрос и применение РЗЭ, в настоящее время промышленное производство индивидуальных РЗМ в стране отсутствует.
Радиоактивные редкие металлы. К ним относятся естественные радиоактивные металлы: радий, полоний, актиний, торий, протактиний, уран, и искусственно полученные остальные актиноиды.
В настоящем справочнике рассматриваются характеристики производства четырех подгрупп редких металлов: легких, рассеянных, тугоплавких и редкоземельных.
В справочник по редким металлам дополнительно включены кальций и магний, которые относятся к группе щелочноземельных металлов. Это обусловлено их использованием при металлотермическом восстановлении редких металлов, а также тем, что они производятся на предприятиях, специализирующихся на выпуске редких металлов. Ввиду чего было принято решение о нецелесообразности создания отдельного справочника для кальция и магния, учитывая их роль и применение в контексте технологий получения и обработки редких металлов.
Группа редких металлов не остается неизменной, из данной группы выбывают химические элементы, получившие широкое применение в промышленности, каковыми являются вольфрам, молибден и титан, еще недавно относившиеся к редким. Однако, учитывая их высокую важность для промышленности и то, что они не нашли своего места в выпущенных ранее справочниках, они представлены в данном справочнике условно как редкие металлы.
Ряд редких металлов, наличие сырьевой базы которых имеет высокую экономическую значимость для России, относятся к стратегическим - это галлий, германий, индий, литий, молибден, ниобий, рений, тантал, титан, вольфрам, цирконий, ванадий, скандий, иттрий, лантан и 14 лантаноидов [41].
В 2024 г. правительством России утверждена стратегия развития минерально-сырьевой базы Российской Федерации до 2050 года, которая определяет приоритеты, цели и задачи минерально-сырьевого комплекса, направленные на устойчивое долгосрочное обеспечение национальной экономики минеральным сырьем [42].
Критически важными редкометалльными сырьевыми материалами для России являются металлы и материалы, которые используются в ключевых технологиях, необходимых для обеспечения перехода на "зеленую экономику" с преимущественным использованием возобновляемых источников энергии, цифровизации, космической промышленности и оборонного потенциала. К ним относится минеральное сырье, содержащее цирконий, гафний, редкоземельные элементы, бериллий, индий, тантал, ванадий, вольфрам, молибден, кобальт, ниобий, литий, галлий, титан, германий и др.
Минерально-сырьевая база редких металлов в России, согласно принятой Стратегии на период до 2050 года [42], делится на 3 группы. К первой группе относятся добываемые полезные ископаемые, запасы которых удовлетворяют потребности до 2035 года - из редких металлов это ванадий, германий, рубидий, цезий, индий, галлий, скандий. Ко второй группе относятся полезные ископаемые, достигнутый уровень добычи которых недостаточно обеспечен запасами на период до 2035 г., но редких металлов среди них нет. Третью группу составляют импортозависимые дефицитные виды полезных ископаемых, внутреннее потребление которых обеспечивается импортом - из числа редких металлов это уран, титан, молибден, вольфрам, литий, бериллий, цирконий, ниобий, тантал, рений, редкоземельные элементы.
Для решения проблемы сырья последней группы металлов планируется интенсификация геолого-разведочных работ в России с использованием последних достижений науки и техники в этой области (рения), строительство новых горнодобывающих предприятий на базе разведанных и предварительно оцененных месторождений (лития), попутное получение минерального сырья (титана, циркония, бериллия, лития, цезия, рубидия, ниобия, тантала), организация международных проектов по добыче сырья, утилизация различных техногенных образований и другие методы. Важное значение приобретает рециклинг редких металлов (литий, рений, скандий, РЗМ и др.), включающий переработку техногенного и вторичного сырья.
Разрабатываемых природных источников ренийсодержащего сырья Россия практически не имеет. Сырьевой базой ниобия и тантала является комплексное Ловозерское лопаритовое месторождение (Мурманская область). Это также единственный действующий на сегодняшний день источник производства коллективных карбонатов РЗМ.
Россия располагает достаточно крупной сырьевой базой молибдена, основу которой составляют штокверковые месторождения собственно молибденовых руд, тогда как в мире ключевую роль играют объекты медно-порфирового семейства, в рудах которых молибден присутствует как попутный компонент. Производство молибденовой сырьевой продукции в стране ведется в количестве, недостаточном для удовлетворения внутреннего спроса, что во многом определяется высокой зависимостью от рыночной стоимости продукции, доминированием на мировом рынке попутного молибдена, получаемого совместно с медью и отличающегося сравнительно низкой себестоимостью. В настоящее время выпускаемый в стране молибденовый концентрат в полном объеме перерабатывается в ферромолибден на единственном в стране производственном комплексе, объединяющем обогатительное и ферросплавное производство - Сорском ферросплавном заводе в Республике Хакасия. Его конечная продукция до 2022 г. в основном поставлялась на экспорт, а в последующий период была перенаправлена на внутренний рынок. Остальные потребители молибденовых концентратов вынуждены их импортировать, а также использовать вторичное сырье
Общие запасы бериллиевых руд (BeO) в РФ составляют 49,8% мировых запасов. Балансовые запасы бериллия учтены в 27 месторождениях и превышают мировые подтвержденные запасы, составляя от них 120,6%. Балансовые запасы бериллия России распределены в четырех федеральных округах: Северо-Западном (13,9%), Уральском (22,4%), Сибирском (46,5%), Дальневосточном (17,1%). Источником бериллиевого сырья в России являются Завитинское и Ермаковское (Республика Бурятия) месторождения, которые разрабатывались Забайкальским ГОКом. В настоящее время Завитинское месторождение не эксплуатируется. Ермаковское месторождение содержит 80% запасов бериллия России и является одним из лучших в мире по содержанию бериллия в руде (среднее содержание BeO - 1,19%) и флюорита (среднее содержание CaF2 - 20%). К тому же в рудах отсутствует уран (руды нерадиоактивны). В настоящее время месторождение законсервировано, однако в недрах еще сохранилось около 40% разведанных запасов. В случае возобновления добычи на Ермаковском месторождении производственная мощность предприятия может составить 25 тыс. тонн руды и 130 тонн гидроксида бериллия в год.
По объему запасов лития Россия занимает одно из ведущих мест в мире. В структуре балансовых запасов ведущую роль играют пегматитовые месторождения (75%), тогда как в мире 76% запасов приходится на рапу соляных озер. Прогнозные ресурсы оцениваются в 260 тыс. т. лития, а запасы определены в количестве сотен тысяч тонн. Основным производителем литиевой продукции на российском рынке является НЗХК, который поставляет литий отечественным потребителям и за рубеж.
Россия располагает крупной сырьевой базой циркония, достаточной для обеспечения внутренних потребностей страны. При этом отечественные месторождения в основном комплексные, цирконий в них присутствует в качестве попутного компонента. Это ставит развитие его добычи в зависимость от заинтересованности инвесторов в полезном ископаемом, являющемся в рудах того или иного цирконийсодержащего месторождения основным. Кроме того, извлечение попутных компонентов в товарную продукцию в значительной степени осложняет процесс первичной переработки руд. Выпускаемый в России бадделеитовый концентрат является уникальным высококачественным циркониевым сырьем и до 2022 г. практически полностью экспортировался. При этом для производства металлического циркония (в т.ч. ядерной чистоты), его сплавов и изделий из них отечественными предприятиями использовался импортный цирконовый концентрат. В 2022 - 2023 гг. для производства металлического циркония и гафния стал использоваться бадделеитовый концентрат. В производстве керамики, огнеупорных изделий и абразивов по-прежнему применяется импортный цирконовый концентрат. Реализация проекта по развитию производства на базе Туганского россыпного месторождения в Томской области создает условия для принципиального сокращения, а в перспективе - полного отказа от импорта в Россию циркониевого сырья.
В качестве альтернативного перспективного сырьевого источника циркония и гафния для обеспечения производства единственного российского производителя АО "Чепецкий механический завод" рассматривается эвдиалит. Эвдиалит является уникальным сырьем товарных продуктов на основе Zr/Hf, Nb/Ta, средней и среднетяжелой группы РЗМ, которые так востребованы текущей отечественной промышленностью. Комплекс эвдиалитовых луявритов участка Аллуайв в Ловозерском массиве находится в непосредственной близости от лопаритовых месторождений Умбозеро и Карнасурт. В начале 1990-х годов месторождение было изучено на стадии предварительной разведки. Для начала его промышленного освоения требуется разработка эффективной технологии переработки, включающая получение товарных циркония, гафния, ниобия, тантала и индивидуальных РЗМ средней и среднетяжелой группы (Y, Nd, Dy, Sm и др.), а также постановка запасов на Государственный баланс.
Промышленные запасы германия в России расположены в трех районах нашей страны: на Сахалине (Новиковское месторождение), в Приморском крае (Павловское месторождение, расположенное находящееся в поселке Новошахтинский рядом с Уссурийском) и на Тарбагатайском месторождении в Бурятии. Все они представлены каустобиолитами, в основном бурым углем и углистыми глинами с низкой теплотворной способностью, но с повышенным содержанием германия. Новиковское месторождение на Сахалине сейчас практически выработано, поэтому наиболее важную роль для нашего государства приобретает Павловское буроугольное месторождение в Приморском крае. По некоторым данным, в настоящее время и оно находится в состоянии консервации из-за того, что российские производители германия пользуются большей частью вторичным сырьем. Вторичное сырье, конечно, существенно удешевляет себестоимость производимой продукции на основе германия, но ни в коей мере не может обеспечивать стратегической стабильности нашего государства. В современной России производством германия занимаются два предприятия. АО "Германий", расположенное в Красноярске и созданное при участии специалистов "ГИРЕДМЕТ", с советских времен является крупнейшим отечественным производителем продукции на основе этого элемента. В настоящее время оно входит в состав концерна Швабе и обеспечивает до 90% российского рынка германия. Производственной мощности АО "Германий" достаточно для производства до 30 тонн германиевой продукции в год. причем по всей технологической цепочке. Второе производство, ООО "Германий и приложения", расположено в городе Новомосковске Тульской области. Это частное предприятие было основано в 2006 году. На нем долгое время перерабатывали германийсодержащие зольные уносы, в первую очередь Павловского разреза, что обеспечивало сырьем производство германиевой продукции объемом до 10 тонн в год. На нем также производят монокристаллический германий и пластины из него, диоксид и тетрахлорид германия, заготовки для ИК-оптики. Кроме двух названных выше предприятий с полным технологическим циклом по германию, следует отметить также АО "ОКБ "Астрон", выпускающее тепловизоры и микроболометры. Начиная с 2017 года оно производит монокристаллический германий для собственных нужд [48].
Минерально-сырьевая база редкоземельных элементов характеризуется достаточно высокими количественными показателями. РЗЭ в сырье присутствуют суммарно в различных соотношениях, в основном в форме оксидных соединений - оксидов, карбонатов, фосфатов, силикатов. При этом 95% мировых запасов РЗЭ, представленных в виде минералов бастнезита, монацита, ксенотима. По объему запасов Россия входит в пятерку ведущих стран в мире и обладает разнообразным по составу сырьем РЗЭ. Однако в настоящее время, основным промышленным источником РЗЭ в РФ является лопарит - сложный оксид состава (Na, Ca, Ln)2(Ti, Nb)2O6 с преимущественным содержанием цериевой группы 31 - 34%. Концентрат РЗЭ - лантаноидов и иттрия, получают в виде карбоната на Соликамском магниевом заводе. Производительность предприятия составляет до 3600 т/год. Промышленное получение индивидуальных РЗЭ в стране отсутствует [45].
Относительно скандия - известно, что единственным скандиевым минералом являются тортвейтит. Однако значительных скоплений минералов не обнаружено. В России запасы скандия достаточно велики и сосредоточены в шести месторождениях. Наиболее перспективными являются титановые концентраты Туганского месторождения и руды Томтора [40]. Промышленное производство в стране отсутствует, но в ГК Росатом реализовано опытное производство по извлечению скандия из урановых растворов скважинного подземного выщелачивания в АО "Далур", и в 2023 году - на объектах АО "Хиагда" с производительность не менее 1 т/год фторида и оксида скандия.
Сведения об использовании редких металлов приведены в таблицах 1.1 - 1.4.
Легкие редкие металлы | Сфера распространения, что из них производят, как они используются |
Бериллий Be | Легирование сплавов, детали из металлического бериллия, рентгенотехника, лазерные материалы, аэрокосмическая техника, ракетное топливо, огнеупорные материалы, акустика, компоненты солевых композиций жидкосолевых реакторов. |
Литий Li | Основные области: литий-ионные аккумуляторы (83%) и твердотельные литиевые батареи (15%). Остальное - керамика и стекла, атомная техника и электроника, металлургия, реактивная авиация и ракетная техника, химическая промышленность, медицина, оборонная промышленность, дефектоскопия, текстильная, пищевая и косметическая промышленности. |
Рубидий Rb | Рубидий и его соединения применяются в биомедицинских исследованиях, электронике, пиротехнике и производстве специального стекла. Производство специального стекла является ведущим рынком для рубидия; карбонат рубидия может использоваться для снижения электропроводности, что повышает стабильность и долговечность волоконно-оптических телекоммуникационных сетей. Биомедицинские приложения включают применение солей рубидия в противошоковых средствах, а также в лечении эпилепсии и заболеваний щитовидной железы; рубидий-82, радиоактивный изотоп, - в качестве индикатора кровотока в позитронно-эмиссионной томографии; хлорид рубидия - в качестве антидепрессанта. Атомы рубидия используются в разработке вычислительных устройств на основе квантовой механики - перспективного направления с потенциалом относительно высокого потребления рубидия. В области квантовых вычислений ультрахолодные атомы рубидия используются в различных приложениях. Фотоэмиссионные свойства рубидия делают его полезным для генераторов электрических сигналов в датчиках движения, приборах ночного видения, фотоэлементах (солнечных панелях) и фотоумножителях. Рубидий используется в качестве атомного резонансного генератора опорной частоты для синхронизации телекоммуникационных сетей, играя важную роль в системах глобального позиционирования, богатые рубидием полевые шпаты - в керамических изделиях для свечей зажигания и электрических изоляторов благодаря своей высокой диэлектрической проницаемости, гидроксид рубидия - в фейерверках для получения фиолетовых оттенков. |
Цезий Cs | Электроника, радио-, электро-, рентгенотехника, химическая промышленность, оптика, медицина, ядерная энергетика. Металлический цезий может использоваться в производстве соединений цезия и фотоэлементов, бромид цезия - в инфракрасных детекторах, оптике, фотоэлементах, сцинтилляционных счетчиках и спектрофотометрах, карбонат цезия - в топливных элементах, магнитогидродинамических генераторах и полимерных солнечных батареях. Хлорид цезия применяют в высокотемпературных припоях, в производстве цезия, в изопикническом центрифугировании, как радиоизотоп (цезий-137) в ядерной медицине, как средство от насекомых в сельском хозяйстве и в производстве специального стекла. Гидроксид цезия - в качестве электролита в щелочных аккумуляторных батареях. Иодид цезия используют в рентгеноскопическом оборудовании, в инфракрасных Фурье-спектрометрах в качестве входного люминофора рентгеновских усилителей изображения и в сцинтилляторах. Нитрат цезия может использоваться как краситель и окислитель в пиротехнике, при крекинге нефти, в сцинтилляционных счетчиках и в рентгеновских фосфорах. Сульфаты цезия часто могут применяться в системах очистки воды, топливных элементах и для улучшения оптических свойств научных приборов. |
Таблица 1.2
Рассеянные редкие металлы | Сфера распространения, что из них производят, как они используются |
Рений Re | Жаропрочные никелевые суперсплавы (80% объема производства), платинорениевые катализаторы (15%), в виде сплавов в электрических контактах, электромагнитах, электронных трубках, нагревательных элементах, полупроводниках, температурных контроллерах и др. |
Галлий Ga | Галлий и его эвтектический сплав с индием используют как теплоноситель в контурах реакторов. Галлий применяют как смазочный материал, как покрытие зеркал специального назначения. GaAs применяют для производства полупроводниковых пластин, используемых в интегральных схемах (ИС) и оптоэлектронных устройствах, которые включают лазерные диоды, светодиоды (СИД), фотодетекторы и солнечные элементы. Нитрид галлия (GaN) - для производства ИС и оптоэлектронных устройств. Около 79% галлия, потребляемого в Соединенных Штатах, приходилось на пластины GaAs, GaN и фосфида галлия. Металлический галлий, триэтилгаллий и триметилгаллий, используемые в процессе эпитаксиального наслаивания для изготовления эпипластин для производства ИС и светодиодов, составляли большую часть оставшейся части. Оптоэлектронные устройства использовались в аэрокосмической промышленности, потребительских товарах, промышленном оборудовании, медицинском оборудовании и телекоммуникационном оборудовании. Использования ИС включают оборонные приложения, высокопроизводительные компьютеры и телекоммуникационное оборудование. |
Индий In | Широко применяется в производстве жидкокристаллических экранов, в микроэлектронике. Является компонентом для легкоплавких припоев и сплавов. Производство оксида индия и олова (ITO) составляет большую часть мирового потребления индия. Тонкопленочные покрытия ITO в основном используют в качестве электропроводящих материалов в плоских дисплеях, чаще всего в жидкокристаллических (ЖК) дисплеях. Применяется в производстве сплавов и припоев, соединений, электрических компонентов и полупроводников AIIIBV. |
Таллий Tl | Амальгама таллия применяется для заполнения низкотемпературных термометров и в качестве теплоносителя. Соединения таллия применяются для регистрации ионизирующих излучений. Основные области применения включают: радиоизотоп таллий-201, используемый в медицинских целях для визуализации сердечно-сосудистой системы; таллий - активатор (кристаллы иодида натрия, легированные таллием) в оборудовании для обнаружения гамма-излучения; высокотемпературные сверхпроводники на основе таллия, бария, кальция и меди; таллий, используемый в линзах, призмах и окнах для инфракрасного оборудования обнаружения и передачи; кристаллические фильтры на основе таллия, мышьяка и селена для дифракции света в акустооптических измерительных приборах; и таллий в ртутных сплавах для низкотемпературных измерений. Другие области применения - добавка к стеклу для увеличения его показателя преломления и плотности, катализатор для синтеза органических соединений, компонент высокоплотных жидкостей для гравитационного разделения минералов и компонент износостойких нанопокрытий. |
Германий Ge | Волоконная оптика, тепловизорная оптика, химические катализаторы, полупроводниковая и микроэлектроника, металлургия. |
Гафний Hf | Металлический гафний применяется для производства сплавов для аэрокосмической техники, атомной промышленности, специальной оптике |
Селен Se | Применяется при производстве электролитического марганца в Китае, стекла, химикатов и пигментов, в сельском хозяйстве, электронике, и др. |
Теллур Te | Применяется при производстве кабелей, свинцово-кислотных аккумуляторов, детекторов рентгеновского и гамма-излучения, полупроводниковых материалов. Преимущественно используется в производстве теллурида кадмия (CdTe) для тонкопленочных солнечных батарей, теллурида висмута (BiTe) для термоэлектрических устройств охлаждения и генерации энергии. В металлургии - в качестве легирующей добавки к стали для улучшения характеристик механической обработки и медным сплавам для улучшения обрабатываемости без снижения электропроводности, в свинцовые сплавы для повышения вибростойкости и усталостной стойкости. В химической промышленности - вулканизирующий агент при обработке резины, а также компонент катализаторов для производства синтетических волокон. Другие применения включают в себя использование в фоторецепторных и термоэлектрических устройствах, капсюлях-детонаторах, а также в качестве пигмента для получения различных цветов в стекле и керамике. |
Таблица 1.3
Редкоземельные металлы | Сфера распространения, что из них производят, как они используются |
Скандий Sc | Главное применение - алюминиево-скандиевые сплавы в авиа- и ракетостроении и в производстве твердотопливных элементов. |
Иттрий Y | Основными сферами применения являются катализаторы, керамика, электроника, лазеры, металлургия и производство фосфора. В керамических изделиях соединения иттрия используют в абразивах, подшипниках и уплотнениях, высокотемпературных огнеупорах для сопел непрерывной разливки, покрытиях реактивных двигателей, кислородных датчиках в автомобильных двигателях, а также в износостойких и коррозионностойких режущих инструментах. В электронике железо-иттриевые гранаты используются в микроволновых радарах для управления высокочастотными сигналами. Важный компонент лазерных кристаллов иттрий-алюминиевого граната, используемых в медицинских хирургических процедурах, цифровой связи, дистанционном и температурном измерении, промышленной резке и сварке, нелинейной оптике, фотохимии и фотолюминесценции. В металлургии - добавка для измельчения зерна и раскислитель. Иттрий используют в сплавах для нагревательных элементов, высокотемпературных сверхпроводниках и суперсплавах, а также в фосфорных соединениях для плоских дисплеев и различных осветительных приборов. |
Лантан и лантаноиды | Основная сфера применения индивидуальных РЗЭ в России - катализаторы для нефтехимии и синтеза каучука. Значительное количество используется в составе постоянных магнитов, встроенных в готовые изделия. Другими конечными областями применения являются производство керамики и стекла, металлургические изделия и сплавы, а также полировальные смеси, электроника, лазеры, медицина и др. |
Тугоплавкие редкие металлы | Сфера распространения, что из них производят, как они используются |
Ванадий V | Основное использование - легирующая добавка для чугуна и стали. Главное неметаллургическое применение - катализаторы для производства малеинового ангидрида и серной кислоты. |
Ниобий Nb | Легирующая добавка к стали для повышения прочностных и износостойких характеристик в ракетостроении, авиационной и космической технике, радиотехнике, электронике, химическом аппаратостроении, атомной энергетике. |
Тантал Ta | Жаропрочные и коррозионностойкие сплавы для химической промышленности, теплообменники для ядерно-энергетических систем. Металлический тантал используется для производства танталовых конденсаторов, танталовая проволока применяется для изготовления сеток электронных ламп. |
Цирконий Zr | Основными сферами применения циркона являются керамика, формовочный песок, глушители и огнеупоры, а также абразивы, химикаты, металлические сплавы и покрытия для сварочных электродов. Металлический цирконий востребован в химической промышленности и атомной энергетике. |
Титан Ti | Большую часть металлического титана используют в аэрокосмической промышленности, остальную часть - в производстве брони, морском оборудовании, медицинских имплантах. Основными сферами применения пигмента TiO2 (в порядке убывания) являются краски (включая лаки и глазури), пластмассы и бумага. Пигмент TiO2 также используют в катализаторах, керамике, тканях с покрытием и текстильных изделиях, напольных покрытиях, типографской краске и кровельных гранулах. |
Вольфрам W | Основное использование - производство деталей из твердого сплава, предназначенных для резки и износостойких деталей, в основном в строительстве, металлообработке, горнодобывающей промышленности, а также в нефтегазодобывающей промышленности. Остальной объем - изготовление электродов, нитей накаливания, проволоки и других компонентов для электротехники, электроники, систем отопления, освещения и сварки, а также химикатов для различных применений. Основа тяжелых сплавов в военной технике. |
Молибден Mo | Используется в основном в качестве легирующей добавки в чугуне, стали и суперсплавах, а также в многочисленных химических применениях, включая катализаторы, смазочные материалы и пигменты. |
С 1991 г. за пределами границ России остались как эксплуатируемые месторождения редкометалльного сырья, так и химико-металлургические предприятия, которые перерабатывали различные минеральные концентраты с извлечением редкометалльной продукции - Li, Be, Nb, отдельных РЗЭ, а также рения, индия и других рассеянных редких металлов (РРМ). С ними преимущественно связаны перспективы организации и создания редкометалльного производства, необходимого для развития ОПК и гражданских высокотехнологичных отраслей промышленного производства России.
Уровень производства и потребления редких элементов в настоящее время является индикатором экономической и национальной безопасности стран. За последние 5 лет мировое потребление Li увеличилось в 3,1 раза, Ta - 1,2 раза, Nb и V - в 1,4 раза, и наиболее дефицитных, стратегически важных рассеянных металлов - Re в 1,3 раза, In - в 1,4 раза, РЗЭ - в 1,9 раза, скандия - в 2 раза. Это обусловлено ростом их использования как в традиционных отраслях промышленного производства (металлургия, создание керамических и композиционных материалов, электротехника и электроника, ядерная энергетика), так и в новых высокотехнологичных областях (инфракрасная, микроволновая и СВЧ-техника, телекоммуникационная и волоконно-оптическая связь, новые сплавы, топливные элементы и источники энергии, сверхпроводимость и т.д.).
1.3.1.1 Бериллий - самый легкий из конструкционных материалов.
Бериллий благодаря оптимальному сочетанию физических, химических и механических свойств оценивается в современном мире как космический металл: один из самых легких, прочных, тугоплавких, коррозионно устойчивых и сохраняющих размерность при температурных колебаниях. В АРКТ используются облегченные конструкции из бериллиевых материалов ("Шаттл"). Наиболее заметно расширяется использование бериллиевых сплавов - от традиционного производства наиболее известных бериллиевых бронз - Cu-Be (от 0,2 - 0,7% до 2% Be) и Al-Be-x (до 68% Be) до создания уникального сплава Alloy 390TM для мобильных телефонов. Металлический бериллий был получен восстановлением его хлорида. Производство соединений бериллия металла и его сплавов возникло в 20 - 30 годах прошлого столетия.
По данным Геологической службы США (USGS), годовой объем производства бериллия в мире (в пересчете на металл) в 2025 г. составил 360 тонн; до 40% объема производства сплавов бериллия в США получают из скрапа. Ведущие производители бериллиевой продукции - США (50%), Бразилия и Китай [43].
В России эксплуатируется месторождение бериллиевого сырья Изумрудные копи, которое представлено флогопит-маргарит-берилловыми рудами плагиоклазитов. Их разработка осуществляется Малышевским РУ, для извлечения драгоценного кристаллосырья - изумрудов с сопутствующим александритом. Попутно ранее выпускался бериллиевый концентрат при содержании в исходной руде 0,14% BeO. АО "Мариинский прииск" является оператором Малышевского изумрудно-бериллиевого месторождения. Разведанные запасы составляют ~ 11 млн т изумрудно-бериллиевой и бериллиевой руды, суммарно содержащей ~ 55 т изумрудного сырья и ~ 15,6 тыс. т оксида бериллия. Для интенсификации добычи изумрудов и выхода на рынок бериллия планируется модернизация шахты, что обеспечит рост годового объема добычи руды до 400 тыс. т к 2030 г., постройка новой обогатительной фабрики в п. Малышева и металлургического производства в г. Краснотурьинск. Планируется поставка продукции на внутренний и внешний рынок. На постсоветском пространстве основной и единственный производитель бериллия и его соединений - АО "Ульбинский металлургический завод" Республика Казахстан, г. Усть-Каменогорск.
Берилл (с танталоколумбитом) извлекался из пегматитов соседних месторождений (Квартальное, Липовый Лог), характеризующихся тантал-ниобий-бериллиевой специализацией. Попутные берилловые концентраты выпускались также Забайкальским ГОКом, специализированным на производстве профилирующей литиевой (сподумен) продукции, и Белогорским ГОКом (Казахстан), специализированным на выпуске танталовых концентратов. Балансовые запасы бериллия учтены в 27 месторождениях. Балансовые запасы бериллия России распределены в четырех федеральных округах: Северо-Западном (13,9%), Уральском (22,4%), Сибирском (46,5%), Дальневосточном (17,1%). В настоящее время в качестве базы для организации производства бериллия, лития, тантала и ниобия в РФ рассматривается Забайкальский регион. Резервными объектами освоения являются крупнейшие редкометалльно-флюоритовые месторождения - Вознесенское и Пограничное в Приморском крае.
Ермаковское месторождение содержит 80% запасов бериллия России и является одним из лучших в мире по содержанию бериллия в руде (среднее содержание BeO - 1,19%) и флюорита (среднее содержание CaF2 - 20%); в рудах отсутствует уран. Значительная часть его запасов отработана в 1979 - 1989 годах - сохранилось около 40% разведанных запасов. После прекращения добычи в 1989 году на балансе Ермаковского месторождения в государственной комиссии по запасам полезных ископаемых сохраняется 1,4 миллиона тонн руды по категориям C1+C2. В 2025 году в Бурятии начнется разработка Ермаковского месторождения - крупнейшей в стране сырьевой базы бериллия. В Кижингинском районе будет построен новый горно-обогатительный комбинат с общим объемом инвестиций 6,4 млрд. рублей. Проект рассчитан до 2034 года.
Сложнее будет решаться задача глубокой химико-металлургической переработки различного бериллиевого сырья, которая в СССР осуществлялась на Ульбинском химико-металлургическом заводе в г. Усть-Каменогорске. Тем более что ее решение предусматривалось нереализованной Федеральной программой "ЛИБТОН" "Росатома" (1996 г.). Предпринимаемые в настоящее время попытки ее реанимировать на базе приостановленных, дезинтегрированных и частично утраченных мощностей бывшего Забайкальского ГОКа в пос. Первомайском с использованием остаточных руд и техногенных ресурсов с недопустимо низкими содержаниями редких металлов, нерешенными технологическими задачами их извлечения и потребительского спроса по-прежнему представляются нереальными.
Бериллий относится к категории редких металлов. Согласно официальным данным Минпромторга, сейчас доля его импорта составляет порядка 85%. В связи с этим правительством поставлена задача развивать собственную сырьевую базу и высокотехнологическую отрасль потребления, а также оказывать меры поддержки, для того чтобы к 2025 году этот показатель снизился до 60%, а к 2035-му - до 40%.
1.3.1.2 Литий за последние десятилетия приобрел исключительно важное значение в современной технике и является, безусловно, необходимым для ее дальнейшего развития.
Без учета производства в США, мировая добыча лития в 2024 году увеличилась на 18% до примерно 240 000 тонн по сравнению с 204 000 тоннами в 2023 году. Это произошло в ответ на высокий спрос на литий-ионные батареи, высокие цены на литий в период с 2021 по начало 2023 года и увеличение мировых производственных мощностей лития. Мировое потребление лития в 2024 году оценивается в 220 000 тонн, что на 29% больше пересмотренного потребления в 2023 году в 170 000 тонн.
Россия располагает одной из крупнейших сырьевых баз лития в мире. Промышленными минералами являются сподумен, петалит, лепидолит, амблигонит. Сподуменовый концентрат (5,5 - 7,9% Li2O) преимущественно используется в производстве гидроксида, карбоната батарейного сорта, хлорида, фторида и других солей лития, петалитовый (3,4 - 5,5% Li2O) и амблигонитовый (7,9% Li2O) концентраты - в специальных стекольных и керамических производствах. Руды всех российских месторождений являются комплексными. В зависимости от геолого-промышленного типа помимо лития они содержат тантал, ниобий, бериллий, цезий и другие металлы. Около трех четвертей ресурсов содержится в гидроминеральных источниках сырья - литийсодержащей рапе соляных озер, где литий присутствует в виде различных соединений (в основном сульфатов и хлоридов [45].
Ресурсы лития существенно возросли в результате разведки во всем мире и в 2025 г. составляют около 115 миллионов тонн Li. Измеренные и предполагаемые ресурсы лития в Соединенных Штатах составляют 19 миллионов тонн. Ресурсы лития в других странах пересмотрены до 96 миллионов тонн. Ресурсы распределяются следующим образом, млн т: Аргентина, 23, Боливия 23, Чили 11, Австралия 8,9, Китай 6,8, в России - 1 миллион тонн [43]. Дополнительно запасами лития в количестве 161 тыс. т Li2O располагает Донецкая Народная Республика. В полном объеме они заключены в недрах Шевченковского месторождения в редкометалльных пегматитах со сподуменом. ГБЗ РФ по состоянию на 01.01.2024 эти запасы не учитываются [45].
Ближайшие перспективы развития литиевой промышленности в России связаны с использованием собственной сырьевой базы. В России организуется промышленное производство соединений лития из сподуменовой руды Колмозерского месторождения (ООО "Полярный литий") мощностью до 45 тыс. т литиевой продукции в пересчете на карбонат лития, Полмостундровского месторождений (АО "Арктический литий", производительность 12 тыс. т оксида лития в год), а также из рассолов Ковыктинского месторождения (Газпром) и ряда других. Месторождения Колмозерское и Полмостундровское представлены серией пегматитовых жил протяженностью от первых десятков метров до 1600 м и мощностью от 0,5 до 60 м. Содержание оксида лития - 0,3 - 2,22%. Выход предприятий на проектную мощность ожидается не ранее 2030 года. Планируется промышленное извлечение лития из гидроминерального сырья Ковыктинского газоконденсатного месторождения в Иркутской области. Реализации этих проектов будет способствовать выполнение мероприятий, предусмотренных дорожной картой развития высокотехнологичной области "Технологии новых материалов и веществ" (продуктовое направление "Редкие и редкоземельные металлы") на период до 2030 года, утвержденной Правительством Российской Федерации 24.04.2020.
Переработка литиевых продуктов возможна на предприятии ПАО "Химико-металлургический завод" (ПАО "ХМЗ", г. Красноярск), который является единственным в России производителем гидроксида лития марки ЛГО-3. Ее основными потребителями (в качестве регулятора процесса горения топлива) являются нефтеперерабатывающие заводы и производители электролитов. Часть полученного гидроксида лития предприятие перерабатывает в металл.
Другим переработчиком может стать ООО "ТД "Халмек" (Тульская обл.), который выпускает широкий ассортимент товарных продуктов гидроксида лития: батарейный и технический сорта, высокочистый сорт, гидроксид марки ЛГО-3, а также непылящий сорт. В 2020 году компания "Халмек литиум" запустила инвестиционный проект по строительству своего второго гидрометаллургического завода на территории особой экономической зоны "Узловая" в Тульской области (200 км от Москвы, Россия) мощностью 20 000 т моногидрата гидроксида лития аккумуляторного качества в год. Сырьем для этого предприятия будет сподуменовый концентрат АО "Арктический литий". В настоящее время проект находится в стадии строительства.
Предприятие ПАО "Новосибирский завод химконцентратов" (ПАО "НЗХК"), выпускающий широкий ассортимент литиевой продукции: литий металлический (катализаторный и батарейный сорта, с повышенным содержанием алюминия, сорт ЛЭ), литий-7, хлорид лития, планирует использовать литий Колмозерского месторождения.
Передовым способом добычи лития из гидроминерального сырья в мире является технология DLE (Direct Lithium Extraction). Промышленные компании, внедрившие данную технологию в производство, работают в Аргентине и Китае. В России АО "Аксион - Редкие и Драгоценные Металлы" (АО "АРДМ") разработало собственную запатентованную технологию получения соединений лития (карбонат лития, гидроксид лития, раствор хлорида лития) из гидроминеральных ресурсов (таких как природные рассолы, геотермальные и пластовые, подтоварные воды нефтедобычи) с высокой эффективностью и минимальными капитальными и операционными затратами. Разработанная сорбционная технология DLE абсолютна экологична (не предполагает выщелачивания кислотами, для десорбции лития используется вода) и экономически эффективна даже при низких содержаниях лития. DLE технология производства лития из гидроминерального сырья эффективнее традиционной галургической и экстракционной.
Технология DLE промышленного производства соединений лития (карбонат лития, гидроксид лития, хлорид лития) из природных и технологических рассолов включает сорбцию лития литий-селективным сорбентом, десорбцию лития водой, концентрирование литийсодержащих элюатов, очистку литиевых концентратов от примесей, электролиз водного раствора хлорида лития или осаждение карбоната лития. Данная технология основана на использовании сорбента  Li-sorb, обладающего высокими селективными и емкостными показателями, системы рецикловых потоков, снижающих себестоимость готового продукта, и энергоэффективных методов.
Li-sorb, обладающего высокими селективными и емкостными показателями, системы рецикловых потоков, снижающих себестоимость готового продукта, и энергоэффективных методов.
 Li-sorb, обладающего высокими селективными и емкостными показателями, системы рецикловых потоков, снижающих себестоимость готового продукта, и энергоэффективных методов.
Li-sorb, обладающего высокими селективными и емкостными показателями, системы рецикловых потоков, снижающих себестоимость готового продукта, и энергоэффективных методов.Дополнительным источником лития в ближайшее время могут стать отработанные литий ионные аккумуляторы (ЛИА) с содержанием до 7, 10 и 20% лития, никеля и кобальта, соответственно, которые являются ценным вторичным сырьем.
В АО "Гиредмет" разработана гидрометаллургическая технология переработки отработанных ЛИА с получением солей лития, кобальта и никеля батарейного класса. Планируется проведение опытно-промышленных испытаний технологии.
1.3.1.3 Рубидий. Минерал карналлит KCl·MgCl2·6H2O - сложное химическое соединение, образованное хлоридами калия и магния с водой. Рубидий дает соль аналогичного состава RbCl·MgCl2·6H2O, причем обе соли - калиевая и рубидиевая - имеют одинаковую структуру и образуют непрерывный ряд твердых растворов, кристаллизуясь совместно. Карналлит хорошо растворим в воде, поэтому вскрытие минерала не составляет большого труда. Сейчас разработаны и описаны в литературе рациональные и экономичные методы извлечения рубидия из карналлита попутно с другими элементами.
Общие запасы рубидия в Австралии, Канаде, Китае и Намибии составляют менее 200000 тонн. Значительные залежи рубидийсодержащих пегматитов обнаружены в Афганистане, Австралии, Канаде, Китае, Дании, Германии, Японии, Казахстане, Намибии, Перу, России, Великобритании, США и Замбии. Небольшие количества рубидия имеются в рассолах на севере Чили и Китая, а также в эвапоритах в США (Нью-Мексико и Юта), Франции и Германии. Мировые коммерческие запасы рубидиевой руды, за исключением запасов в Китае, могут быть исчерпаны в ближайшем будущем [43].
Основными мировыми производителями, включая очищенные соединения рубидия являются Китай, Германия и Россия.
Для цезия и рубидия пегматиты и сейчас остаются единственным сырьевым источником, имеющим промышленное значение. В поллуцитовых рудах месторождение Васин-Мыльк, расположенного в Ловозерском районе, содержатся крупные запасы рубидия и цезия. Важнейшим и крупнейшим источником рубидия, цезия, стронция и редких земель являются хибинские апатито-нефелиновые руды.
Госбалансом учитывается Верхнекамское месторождение калийно-магниевых солей, в котором рубидий является попутным полезным ископаемым. В солях рубидий связан с карналлитовой толщей. Содержание оксида рубидия в рудах колеблется от 0 до 120 г/т, среднее - 90 г/т. Массовая доля рубидия в руде и обогащенном карналлите составляет соответственно 0,0104% и 0,013%. Балансовые запасы оксида рубидия (Rb2O) ВКМКС учитываются по Палашерскому, забалансовые - по Усть-Яйвинскому участку.
1.3.1.4 Цезий в природе находится в минерале поллуците. Содержание его в земной коре составляет 3,7·10-4%. В виде примесей цезий входит в ряд алюмосиликатов: лепидолит, флогопит, биотит, амазонит, петалит, берилл, циннвальдит, лейцит, карналлит. Также содержится в редком минерале авогадрите. Из числа собственно цезиевых минералов наиболее распространены поллуцит (Cs, Na) [AlSi2O6]·nH2O (22 - 36% CS2O), цезиевый берилл (морганит) Be2CsAl2(Si6O18) и авогадрит (KCs)BF4. Последние два минерала содержат до 7,5% оксида цезия. В качестве промышленного сырья используются поллуцит и лепидолит. В Китае, по оценкам, имеются богатые цезием месторождения гейзерита с самыми высокими концентрациями в Ичуне, провинция Цзянси.
По добыче цезиевой руды (поллуцита) лидирует Канада - в месторождении Танко сосредоточено около 70% мировых запасов цезия. Добыча цезия в Намибии прекратилась в начале 2000-х годов. Рудник Бикита в Зимбабве истощил запасы поллуцитовой руды в 2018 году. Рудник Синклер в Австралии завершил добычу и отправку всей экономически рентабельной поллуцитовой руды в 2019 году.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: один и тот же текст приведен дважды. |
Добыча цезия в Намибии прекратилась в начале 2000-х годов. Рудник Бикита в Зимбабве истощил запасы поллуцитовой руды в 2018 году. Рудник Синклер в Австралии завершил добычу и отправку всей экономически рентабельной поллуцитовой руды в 2019 году.
В России месторождения поллуцита есть на Кольском полуострове, в Восточном Саяне и Забайкалье. Месторождения поллуцита также имеются в Казахстане, Монголии и Италии (о. Эльба), но они обладают малыми запасами и не имеют важного экономического значения. Наблюдается некоторое увеличение содержания цезия от ультраосновных пород (0,1 г/т) к кислым (5 г/т). Основная его масса в природе находится в рассеянной форме, и лишь незначительная часть заключена в собственных минералах. Постоянно повышенные количества цезия наблюдаются в морганите (1 - 4%), родиците (около 5%), авогадрите и лепидолите (0,85%). По кристаллохимическим свойствам цезий наиболее близок к рубидию, калию и таллию. В повышенных количествах цезий находится в калиевых минералах.
Цезий, как и рубидий, имеет тенденцию накапливаться на поздних стадиях магматических процессов, и в пегматитах его концентрации достигают наивысших значений. Среднее содержание цезия в гранитных пегматитах около 0,01%, а в отдельных пегматитовых жилах, содержащих поллуцит, даже достигает 0,4%, что примерно в 40 раз выше, чем в гранитах. Наиболее высокие концентрации цезия наблюдаются в редкометалльно-замещенных микроклин-альбитовых пегматитах со сподуменом. При пневматолито-гидротермальном процессе повышенные количества цезия связаны с массивами грейзенезированных аляскитов и гранитов с кварц-берилл-вольфрамитовыми жилами, где он присутствует главным образом в мусковитах и полевых шпатах. В зоне гипергенеза (в поверхностных условиях) цезий в небольшом количестве накапливается в глинах, глинистых породах и почвах, содержащих глинистые минералы.
Повышенные концентрации цезия встречаются в рассолах Чили и Китая, а также в геотермальных системах Китая, Германии и Индии.
Мировой рынок цезиевой химической продукции, исключая формиат цезия, оценивается в 2200 тонн в год. На Китай приходится, по оценкам, 1000 тонн в год этого рынка. По оценкам, в составе буровых растворов использовалось около 11 000 тонн формиата цезия. Основные импортеры цезия - Канада (руда), Китай и Германия. Мировые резервы цезия оцениваются в 200 тыс. т [43].
Группа рассеянных редких металлов, извлекаемых попутно в процессах химико-металлургических переделов различного минерального сырья, продуктов и отходов его обогащения, а также глубокой переработки отходов металлургических производств, включает Re, Ga, In, Tl, Ge, Hf, Se, Te. Извлечение рассеянных элементов проводится при комплексной переработке руд: молибдена (рений), алюминия (галлий), олова (индий) и т.д.
1.3.2.1 Рений - редкий рассеянный и наименее распространенный элемент. Среднее содержание его в земной коре очень низкое - 7·10-8% по массе [46].
Общие мировые запасы рения составляют около 13 000 т, в том числе 3 500 т в молибденовом сырье и 9 500 т - в медном. В общем балансе производства рения в мире на них приходится более 80%. Остальное в основном приходится на вторичное сырье [43]. При перспективном уровне потребления рения в количестве 40 - 50 т в год человечеству этого металла может хватить еще на 250 - 300 лет.
Основными импортерами металлического порошка рения в период с 2020 по 2023 год являются:
Чили - 62%;
Германия - 15%;
Канада - 12%;
Польша - 7%;
другие страны - 4%.
Основные сырьевые источники получения рения - молибденовые концентраты (0,01 - 0,04% Re), медные концентраты (0,002 - 0,003% Re). Отходы от переработки медистых сланцев (0,04% Re), отходящие газы обжига молибденовых концентратов и конвертирования медных штейнов, а также сбросные воды гидрометаллургической переработки бедных молибденовых концентратов (10 - 50 мг/л Re). При переработке концентратов для получения парамолибдата аммония попутно извлекают рений.
При обжиге концентратов на воздухе сульфид рения (ReS2) окисляется с образованием высшего оксида - гептаоксида (Re2O7), который возгоняется, уносится отходящими газами и концентрируется в растворе промывной серной кислоты. После сорбционного концентрирования рения из раствора получают перренат аммония.
Рений встречается в виде редкого минерала джезказганита (CuReS4), найденного вблизи казахстанского города Джезказган. Кроме того, в качестве примеси рений входит в колумбит, колчедан, а также в циркон и минералы редкоземельных элементов [21]. Месторождение в кальдере на вершине вулкана представлено фумарольным полем размерами ~ 50x20 м с постоянно действующими источниками высокотемпературных глубинных флюидов - фумаролами. Это означает, что месторождение активно формируется по сегодняшний день: по разным оценкам, с газами в атмосферу уходит от 10 до 37 т рения в год.
Запасы рения в России скудны, его относят к группе дефицитных металлов. Тем не менее можно говорить о запасах рения по категории A+B+C1 в 9,5 т, по категории C2 - в 176,8 т. Эти запасы связаны с наличием рения в месторождениях молибденовых руд (Сорском, Агаскырском, Мало-Ойногорском), медно-порфировых руд (Михеевском, Аг-Сукском), вольфрамо-молибденовых руд (Коклановском), урановых руд в песчаниках (Брикетно-Желтухинском), фумарольных газов вулкана Кудрявый (о. Итуруп). При этом активные запасы отсутствуют. При прогнозируемой потребности в 25 т (2032 год) и 35 т (2062 год) степень обеспечения потребности добычей составляет 20% и 0% соответственно. Необходим поиск новых сырьевых источников, переоценка осваиваемых и вовлекаемых месторождений.
Производство рения в России отсутствует. При прогнозируемой потребности в 25 т (2032 год) и 35 т (2062 год) степень обеспечения ресурсами недостаточна. Лидерами по экспорту рения являются Чили, Канада и Германия, по экспорту перрената аммония лидирует Казахстан.
Необходима организация рециклинга рения при переработке ренийсодержащего скрапа суперсплавов и отработанных катализаторов гидроочистки нефтепродуктов.
1.3.2.2 Галлий - типичный рассеянный элемент. Среднее содержание галлия в земной коре - 1,9·10-3%. Ввиду близости его кристаллохимических свойств с главными породообразующими элементами (Al, Fe и др.) и широкой возможности изоморфизма с ними галлий не образует больших скоплений, несмотря на значительную величину кларка. Выделяются следующие минералы с повышенным содержанием галлия: сфалерит (0 - 0,1%), магнетит (0 - 0,003%), касситерит (0 - 0,005%), гранат (0 - 0,003%), берилл (0 - 0,003%), турмалин (0 - 0,01%), сподумен (0,001 - 0,07%), флогопит (0,001 - 0,005%), биотит (0 - 0,1%), мусковит (0 - 0,01%), серицит (0 - 0,005%), лепидолит (0,001 - 0,03%), хлорит (0 - 0,001%), полевые шпаты (0 - 0,01%), нефелин (0 - 0,1%), гекманит (0,01 - 0,07%), натролит (0 - 0,1%). Концентрация галлия в морской воде - 3·10-5 мг/л. Месторождения галлия известны в Юго-Западной Африке, России, странах СНГ [46].
Главными промышленными источниками галлия являются бокситовые и нефелиновые руды и, в меньшей степени, сульфидные цинковые. За рубежом запасы галлия, связанные с бокситами, оцениваются в 424 тыс. т при среднем содержании галлия ~ 50 г/т. Общие ресурсы, по данным Горного Бюро США, - 3 - 4 млн т. Цены на галлий и его соединения подвержены сильным колебаниям в зависимости от спроса и совершенствования технологии. Сейчас около трети галлия производится из вторичного сырья, а галлий, который добывается из природного сырья, на 90% выделяется из алюминиевых руд.
В России запасы галлия в бокситах 150 тыс. т при среднем содержании его 53 г/т. Основные же запасы галлия (> 60%) и более 70% его добычи приурочены к апатит-нефелиновым рудам со средним содержанием 23,6 г/т. Нефелиновые концентраты перерабатываются на Волховском и Пикалевском глиноземных заводах.
Лидером по производству галлия является Китай (750 т в 2024 г.). Россия занимает второе место по производству галлия (6 т в 2024 г.); объем продукции галлия в мире составил 760 т [3].
1.3.2.3 Индий - рассеянный редкий металл, среднее содержание индия в земной коре - 2,5·10-5%, и его соединения с уникальными свойствами получили промышленное признание в высокотехнологичных отраслях производства в 1970 - 1990 гг. прошлого столетия. Он является естественным спутником Zn, Cu, Pb и Sn, т.е. особо ценным компонентом различных видов сульфидного сырья с содержанием 20 г/т индия и получаемых из них минеральных концентратов: цинковых (2 - 800 г/т), медных (до 100 г/т), свинцовых (1 - 10 г/т) и оловянных (10 - 124 г/т).
Основные зарубежные производства индия преимущественно базируются на импорте его концентратов из Китая. Собственным производством индия страны-потребители обеспечены примерно на 30%. Однако в ближайшие 20 лет прогнозируется истощение зарубежных запасов цинковых руд как основного источника индия.
Россия обладает достаточными природными и техногенными ресурсами этого металла. Запасы индия в России учитываются в 59 месторождениях Cu-Zn колчеданных и полиметаллических, свинцово-цинковых жильных и скарновых, оловянно-сульфидных руд, из которых 17 эксплуатируются без извлечения индия с запасами в них до 30% от учтенных. В нераспределенном фонде 32 месторождения с запасами индия более 50% от учтенных. С медно-колчеданными месторождениями Урала связано 60% запасов индия, который ассоциирует с Sb, Ge, Ga, Se, Te, возможно, с Re, благородными металлами, а также с Cd, As, Tl.
Мировое производство индия составило в 2024 г. 1080 т. Лидером является Китай (выпущено 760 т в 2024 г., экспорт составил 347 т). Россия импортирует как индийсодержащие цинковые концентраты, в небольших объемах металл высокой чистоты. Производство в России составило в 2024 г. 10 т [3].
Технологии пятого поколения (5G) продолжают увеличивать спрос на индий. Ожидается, что искусственный интеллект увеличит спрос на специализированные материалы, изготовленные из InP, которые позволяют выполнять более сложные вычисления.
1.3.2.4 Таллий - рассеянный элемент, его содержание в земной коре 1·10-4%. Содержится в обманках и колчеданах цинка, меди и железа, в калийных солях и слюдах. Таллий - тяжелый металл. Известно лишь семь минералов таллия (круксит (Cu, Tl, Ag)2Se, лорандит TlAsS2, врбаит Tl4Hg3Sb2As8S20, гутчинсонит (Pb, Tl)S·Ag2S·5As2S5, авиценнит Tl2O3), все они крайне редкие. Главная масса таллия связана с сульфидами и прежде всего с дисульфидами железа. В пирите он установлен в 25% проанализированных образцов. Его содержание в дисульфидах железа нередко составляет 0,1 - 0,2%, а иногда достигает 0,5%. В галените содержание таллия колеблется от 0,003% до 0,1% и редко более. Высокие концентрации таллия в дисульфидах и галенитах характерны для низкотемпературных свинцово-цинковых месторождений в известняках. Содержание таллия, достигающее 0,5%, отмечается в некоторых сульфосолях. Небольшое количество таллия встречается во многих других сульфидах, например, в сфалеритах и халькопиритах некоторых медноколчеданных месторождений, содержание колеблется от 25 до 50 г/т. Наибольшее геохимическое сходство таллий имеет с K, Rb, Cs, а также с Pb, Ag, Cu, Bi. Таллий легко мигрирует в биосфере. Из природных вод он сорбируется углями, глинами, гидроксидами марганца, накапливается при испарении воды (например, в озере Сиваш - до 5·10-8 г/л). Содержится в калиевых минералах (слюде, полевых шпатах), сульфидных рудах: галените, сфалерите, марказите (до 0,5%), киновари. Как примесь присутствует в природных оксидах марганца и железа [9].
Природный таллий состоит из двух стабильных изотопов: 205Tl (содержание 70,5% по массе) и 203Tl (29,5%). В ничтожных количествах встречаются радиоактивные изотопы таллия: 201Tl, 204Tl (T1/2 = 3,56 года), 206Tl (T1/2 = 4,19 мин), 207Tl (T1/2 = 4,78 мин), 208Tl (T1/2 = 3,1 мин) и 210Tl (T1/2 = 1,32 мин), являющиеся промежуточными членами рядов распада урана, тория и нептуния.
Таллий входит (в большинстве случаев в качестве изоморфной примеси и очень редко в виде включений собственных минералов) в состав сульфидных минералов Pb, Zn, Cu, Fe. Руды этих металлов имеют промышленное значение для получения таллия. В ряде случаев при их переработке получают и другие рассеянные элементы (Ge, Ga, In). Как правило, руды этих цветных металлов являются полиметаллическими и обогащением разделяются на соответствующие концентраты. При обогащении большая часть таллия (до 70%), содержащаяся в минералах горных пород, теряется с отвальными хвостами. Так, при обогащении полиметаллических руд некоторых месторождений Алтая 7% таллия переходит в свинцовый концентрат и 12% - в пиритный. При обогащении уральских медно-цинковых руд 11% таллия переходит в медно-цинковый концентрат, а 89% - в пиритный. Только небольшая часть таллия переходит в сульфидные концентраты цветных металлов, из которых он, как правило, и извлекается.
Таллий производится в промышленных масштабах лишь в нескольких странах и является побочным продуктом, получаемым из колошниковой пыли при обжиге медных, свинцовых и цинковых руд. При этом большинство производителей не раскрывают данные о его производстве, поэтому информация о мировых объемах выпуска ограничена. По имеющимся данным, в 2023 году (последний год, по которому есть сведения) мировое производство таллия оценивалось примерно в 10 000 килограммов. Китай, Казахстан и Россия, по оценкам, являются ведущими производителями первичного таллия. Значительные месторождения, богатые таллием, обнаружены в Бразилии, Китае, Северной Македонии и России. Предыдущие оценки запасов основывались на содержании таллия в цинковых рудах. Основным источником извлекаемого таллия являются следовые количества, обнаруженные в сульфидных рудах меди, свинца, цинка и других металлов. Мировых ресурсов таллия достаточно для удовлетворения мировых потребностей [3].
В Казахстане таллий производится на свинцовом заводе Усть-Каменогорского металлургического комплекса, где его извлекают как сопутствующий продукт при переработке свинцовых и медных пылей [38].
1.3.2.5 Германий - общее содержание в земной коре 1,4·10-4% по массе, т.е. больше, чем, например, сурьмы, серебра, висмута. Германий вследствие незначительного содержания в земной коре и геохимического сродства с некоторыми широко распространенными элементами обнаруживает ограниченную способность к образованию собственных минералов, внедряясь в кристаллические решетки других минералов. Поэтому собственные минералы германия встречаются исключительно редко. Почти все они представляют собой сульфосоли: германит Cu2(Cu, Fe, Ge, Zn)2 (S, As)4 (6 - 10% Ge), аргиродит Ag8GeS6 (3,6 - 7% Ge), конфильдит Ag8(Sn, Ge) S6 (до 2% Ge) и другие редкие минералы (ультрабазит, ранерит, франкеит). Основная масса германия рассеяна в земной коре в большом числе горных пород и минералов. Так, например, в некоторых сфалеритах содержание германия достигает в энаргитах до 5 кг/т, в пираргирите до 10 кг/т, в сульваните и франкеите 1 кг/т, в других сульфидах и силикатах - сотни и десятки г/т. Германий концентрируется в месторождениях многих металлов - в сульфидных рудах цветных металлов, в железных рудах, в некоторых окисных минералах (хромите, магнетите, рутиле и др.), в гранитах, диабазах и базальтах. Кроме того, германий присутствует почти во всех силикатах, в некоторых месторождениях каменного угля и нефти. Концентрация германия в морской воде 6·10-5 мг/л [14].
Германий встречается в виде примеси к полиметаллическим, никелевым, вольфрамовым рудам, а также в силикатах. В результате сложных и трудоемких операций по обогащению руды и ее концентрированию германий выделяют в виде оксида GeO2.
Ежегодное производство германия в основном в виде изделий из монокристаллического германия в России находится на уровне 5 - 8 тонн/год.
В России месторождение германиеносных лигнитов есть в Енисейском районе Красноярского края, оно выявлено в бассейне рек Кас и Сым. В 2012 году ООО "Кас" было согласовано проведение работ по изучению Касовского месторождения для добычи германия. Запасы месторождения по категории C2 превышают 13 тыс. кг, прогнозные ресурсы по категории P1 - более 180 тонн, P2 - более 2,3 тыс. тонн.
Для получения германия в России используются германиеносные угли следующих месторождений: Павловское (Михайловский район Приморского края), Новиковское (Корсаковский городской округ Сахалинской области), Тарбагатайское (Петровск-Забайкальский район Забайкальского края). Германиеносные угли этих месторождений в среднем содержат 200 граммов германия на тонну.
Павловское буроугольное месторождение - крупнейшее в мире по запасам германия. Его эксплуатация рассчитана на несколько десятилетий. В среднем, эксплуатируемый разрез способен обеспечить производство до 21 тонны германия в год, но в связи со сложностью извлечения и обогащения, производители германия в РФ в основном используют привозное сырье из Китая.
В 2020 - 2023 гг. основными экспортерами металла являлись Китай (51%), Бельгия (27%), Германия (15%); 5% германия поставила Россия. Поставки диоксида германия осуществляли Бельгия (53%), Канада (41%). Значительное внимание в мире уделялось переработке лома с германием - оптики, пластин солнечных элементов, оптических волокон [43].
1.3.2.6 Гафний - общее содержание в земной коре 1,0·10-4%. Как спутник циркония в основном извлекается из цирконовых (ZrSiO4) концентратов, добываемых из прибрежно-морских россыпных месторождений (Австралия, ЮАР, в меньшей степени США, Бразилия, Индия, Украина). Однако его извлечение осуществляется из 3 - 5% цирконовых концентратов, перерабатываемых в целях получения циркония для ядерных реакторов; преобладающее количество циркона используется в производствах огнеупоров, стекол и керамики. Соотношение гафния с цирконием в цирконах варьируется от 1:50 до 1:100.
Россия обладает различными технологиями производства металлического (электролиз хлоридов и фторидов) и особо чистого гафния (йодидное рафинирование или рафинирование электронно-лучевой плавкой). Разработана кальциетермическая технология восстановления тетрафторида гафния с использованием индукционных печей и получением слитков до 400 кг, которая, однако, не позволяет получать гафний, соответствующий требованиям атомной энергетики. Применение на АО "Чепецкий механический завод" (АО "ЧМЗ") в г. Глазове (Удмуртия) технологии, основанной на различной растворимости в воде фторидов циркония и гафния, обусловило накопление складских запасов 6 - 8% гафниевых концентратов при дефиците реакторного гафния.
Сырьевые ресурсы гафния в нашей стране представлены разведанными запасами циркония в месторождениях Ti-Zr-x россыпных месторождений европейской части (Центральное, Лукояновское, Бешпагирское и др.) и юга Сибири (Туганское, Тарское). Все они легкодоступны, но различаются содержанием таких сопутствующих высоколиквидных компонентов как к.п.ш., глауконит, монацит и др., а также и лимитируемых (хром, торий, уран), и мощностями пород вскрыши. Наиболее ценное циркон-рутил-ильменитовое сырье сосредоточено в двух лицензированных месторождениях: Лукояновском (Нижегородская обл.) и Туганском (Томская обл.). Это позволяет рассчитывать на решение в ближайшей перспективе проблемы обеспечения российской промышленности и прежде всего производств госкорпорации "Росатом" как собственным цирконием, так и сопутствующим ему гафнием.
Продукция действующего ОАО "Ковдорский ГОК" представлена уникальным бадделеитовым концентратом, который нигде в мире, кроме Ковдора, не выпускается. В бадделеитах Ковдора, кроме естественных радионуклидов, выявлено стабильно высокое содержание гафния (13 - 15 кг/т) как изоморфного спутника циркония, а также скандия (200 г/т), оксидов тантала (1 - 1,5 кг/т) и ниобия (1,8 - 4,7 кг/т), суммы оксидов редких земель (130 - 150 г/т). Содержание этих редких металлов определяет повышенную извлекаемую ценность ковдорского бадделеита, что ориентирует на увеличение стоимости товарных бадделеитовых концентратов не только как природного диоксида циркония, но и как высококомплексного редкометалльного продукта, не имеющего аналогов за рубежом. Соотношение гафния с цирконием в бадделеитовых концентратах Ковдора 1:6 значительно выше, чем в цирконах. В 2018 году на производственных площадках ЧМЗ был создан первый в России промышленный участок получения йодидного гафния. На предприятии создан полный цикл изготовления оксида гафния.
В связи с организацией промышленного освоения лопарит-эвдиалитовых руд Ловозера в качестве крупного и стабильного источника иттриевоземельных среднетяжелых РЗМ с сопутствующим цирконием представляется целесообразным оценить и перспективы извлечения гафния из эвдиалитовых концентратов. Содержание в них 1,6 - 1,8 кг/т гафния ниже, чем в цирконовом сырье, примерно в 10 раз, в то время как соотношение гафния с цирконием примерно сопоставимо. Однако эвдиалитовое сырье выгодно отличается практически неограниченными запасами, доступностью, локализацией в пределах инфраструктуры действующего Ловозерского ГОКа, комплексностью и высокой ликвидностью содержащихся в нем редких металлов, отсутствием радиоактивности, легкой растворимостью и легкоплавкостью, а также наличием разработанных технологических схем как обогащения, так и переделов.
1.3.2.7 Селен - содержание в земной коре 5·10-6%. Основные черты геохимии селена в земной коре определяются близостью его ионного радиуса к ионному радиусу серы. Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит FeSe, клаусталит PbSe, тиманнит HgSe, гуанахуатит Bi2(Se, S)3, хастит CoSe2, платинит PbBi2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом. Изредка встречается самородный селен. Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Концентрация селена в морской воде 4·10-4 мг/л [7]. На территории Кавказских Минеральных Вод встречаются источники с содержанием Se от 50 мкг/дм3. Значительные количества селена получают из шлама медно-электролитных производств, в котором селен присутствует в виде селенида серебра. Применяют несколько способов получения: окислительный обжиг с возгонкой SeO2; нагревание шлама с концентрированной серной кислотой, окисление соединений селена до SeO2 с его последующей возгонкой; окислительное спекание с содой, конверсия полученной смеси соединений селена до соединений Se(IV) и их восстановление до элементарного селена действием SO2.
Объем производство селена в мире в 2024 г. составил 3700 т, лидерами по его производству являются Китай (1800 т) и Япония (710 т); в России произведено 340 т. Запасы и резервы селена оценены с учетом выявленных месторождений меди и среднем содержании селена. Другие потенциальные источники селена включают свинцовые, никелевые и цинковые руды. Резервы селена в мире оценены в 92 тыс. т, Россия лидирует с 26 тыс. т [43].
1.3.2.8 Теллур - содержание в земной коре 1·10-7% по массе. Известно около 100 минералов теллура. Наиболее часты теллуриды меди, свинца, цинка, серебра и золота. Изоморфная примесь теллура наблюдается во многих сульфидах, однако изоморфизм Te-S выражен хуже, чем в ряду Se-S, и в сульфиды входит ограниченная примесь теллура. Среди минералов теллура особое значение имеют алтаит (PbTe), сильванит (AgAuTe4), калаверит (AuTe2), гессит (Ag2Te), креннерит [(Au, Ag)Te], петцит (Ag3AuTe2), мутманнит [(Au, Ag)Te], монбрейит (Au2Te3), нагиагит ([Pb5Au(Te, Sb)]4S5), тетрадимит (Bi2Te2S). Встречаются кислородные соединения теллура, например, TeO2 - теллуровая охра. Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0,17% Te и 0,06% Se). Большая часть упомянутых минералов развита в низкотемпературных золотосеребряных месторождениях, где они обычно выделяются после основной массы сульфидов совместно с самородным золотом, сульфосолями серебра, свинца, а также с минералами висмута. Промышленное значение имеют сульфидные минералы. В частности, теллур входит в состав халькопирита медно-никелевых месторождений магматического происхождения, а также халькопирита в медноколчеданных гидротермальных месторождениях. Теллур находится также в составе пирита, халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, связанных со скарнами, сульфидно-кобальтовых, сурьмяно-ртутных и некоторых других. Содержание теллура в молибдените колеблется в пределах 8 - 53 г/т, в халькопирите - 9 - 31 г/т, в пирите - до 70 г/т. Основной источник - шламы электролитического рафинирования меди и свинца.
Более 90% всего производимого теллура получают из анодных шламов как побочный продукт при электролитическом рафинировании меди. Остальная часть добывается из отходов свинцовых заводов, а также из дымовых пылей и газов, образующихся при плавке висмутсодержащих, медных и свинцово-цинковых руд.
Более 90% теллура в мире получают из анодных шламов электролитического рафинирования меди; остальная часть была получена из шламов на свинцовых заводах, а также из колошниковой пыли и газов, образующихся при плавке висмутовых, медных и свинцово-цинковых руд.
Россия производит более 10 - 12% рафинированного теллура в мире: 70 т в 2024 г. (2 место вместе с Японией после Китая). Общий объем мирового производства составил в 2024 г. 980 т. Запасы и резервы теллура основаны на выявленных месторождениях меди и среднем содержании теллура. Другие потенциальные источники теллура включают висмутовые теллуридные и золототеллуридные руды. Резервы России по теллуру оцениваются в 5800 т, в мире - 35 тыс. т [43].
Редкоземельные металлы (РЗМ) - это группа из 17 элементов, включающая: скандий, иттрий и лантаноиды (лантан, церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий, лютеций), производство и потребление которых в мире ежегодно увеличивается.
РЗМ входят в перечень стратегических видов сырья. В 2024 году объем редкоземельного производства составил ~ 390000 т РЗЭ (U.S. Geological Survey (USGS), Mineral Commodity Summarries, January 2025). Основная часть мировой минеральной сырьевой базы РЗМ распределена среди четырех стран: Китай (31%), Россия (26%), Бразилия (15,5%), Вьетнам (15,5%). 95% производства концентратов РЗМ сосредоточено в Китае, который и определяет динамику мировых цен на редкоземельную продукцию. Основным сырьевым источником являются бастнезитовые карбонатиты.
В России существует промышленная добыча РЗЭ - на Соликамском магниевом заводе осуществляется попутное производство суммарного концентрата в объеме ~ до 3600 тонн/год в виде карбоната, но отсутствует промышленное получение индивидуальных РЗЭ [45].
Сырьевая база редкоземельных металлов России может удовлетворить потребность в них, даже в случае значительных темпов ее роста. Однако освоение отечественных месторождений сдерживается низким спросом на РЗМ из-за слабого развития в России высокотехнологичных производств и сложностью конкурирования с основным мировым поставщиком Китаем, диктующим цены на продукцию.
Ведущими потребителями РЗМ в России являются Государственная корпорация "Ростех" в лице ее предприятий АО "Росэлектроника", АО "Объединенная двигательная корпорация", холдинг "Швабе", и Государственная корпорация "Росатом". Относительно крупные закупки (более сотни тонн РЗМ в год) осуществляют нефтеперерабатывающие компании.
1.3.3.1 Скандий является рассеянным элементом и входит в состав многих минералов. Собственно, скандиевых минералов известно 2: тортвейтит (Sc, Y)2 Si2O7 (Sc2O3 до 53,5%) и стерреттит (кольбекит Sc[PO4]·2H2O (Sc2O3 до 39,2%). Основные минералы-носители скандия: флюорит (до 1% Sc2O3), касситерит (0,005 - 0,2%), вольфрамит (0 - 0,4%), ильменорутил (0,0015 - 0,3%), торианит (0,46% Sc2O3), самарскит (0,45%), виикит (1,17%), ксенотим (0,0015 - 1,5%), берилл (0,2%), баццит (скандиевый берилл, 3 - 14,44%). Исключением является тортвейтит - (Sc, Y)2Si2O7 - собственный минерал скандия. Самые значительные месторождения тортвейтита (минерала, наиболее богатого скандием) расположены на Мадагаскаре и в Норвегии.
По данным ФГУП "ИМГРЭ", тортвейтит обнаружен в хвостах обогащения флюоритового сырья в России (Кумир в Алтайском крае), где содержащие его грейзены обогащены иттрием (191 г/т) и скандием (50 - 150 г/т). Однако в качестве основных и потенциальных промышленных источников скандия как типичного элемента попутной добычи рассматриваются месторождения урановых руд, титанового сырья (ильменита, рутила, титаномагнетита), фосфатов, бокситов, вольфрамита, касситерита, РЗМ и циркона.
Мировые запасы скандия значительны и составляют, по мнению различных авторов, от 0,5 до 3 млн. т, из которых около 80% сосредоточены в бокситах [U.S. Geological Survey, Reston, Virginia: 2024]. Наиболее перспективными для извлечения скандия считаются никелевые латериты (так, содержание Sc в руде никелевых руд New South Wales, Австралия составляет 130 - 370 ppm, запасы 37 000 т Sc2O3), и красные шламы отхода производства глинозема (содержание в российском сырье 80 - 120 ppm скандия; ежегодно в мире образуется более 200 млн. т таких отходов).
Месторождения скандия обнаружены в следующих странах: Австралия, Канада, Китай, Финляндия, Гвинея, Казахстан, Мадагаскар, Норвегия, Филиппины, Россия, Южная Африка, Украина, США.
Месторождения скандия в России имеют весьма значительные прогнозные ресурсы. Предварительно оценено, что технологически скандий может производиться из титановых концентратов Туганского месторождения и руд Томторского месторождения. Разведанное в нашей стране скандийсодержащее сырье представлено титаново-цирконовой россыпью (с рутилом и ильменитом) Туганского месторождения в Томской области (108 г/т). Наиболее предпочтительными объектами для организации ускоренного производства скандиевой продукции представляются отходы или возобновляемые техногенные ресурсы действующих производств:
1) Красные шламы бокситов.
2) Силикатные (пироксеновые) текущие и лежалые хвосты обогащения титаножелезорудного сырья ОАО "Качканарский ГОК" со средним содержанием 100 - 150 г/т Sc, обнаруженным Л.Ф. Борисенко (ФГУП "ИМГРЭ") еще в середине прошлого века. Этих хвостов накоплено свыше 1 млрд т. Хвостохранилище занимает площадь более 40 га и ежегодно пополняется примерно на 35 млн т свежих отходов. Хвосты обогащения на 90% состоят из пироксена, на 10% из амфибола, оливина, титаномагнетита и ильменита. Концентрация скандия в хвостах примерно соответствует его содержанию в минералах-носителях и составляет 0,01 - 0,02%. Запасы скандия превышают 120 - 150 тыс. т.
3) Бадделеитсодержащие силикатные хвосты обогащения редкометалльно-фосфатно-железорудного сырья ОАО "Ковдорский ГОК" холдинга "Еврохим", содержащие 690 г/т Sc2O3 в отходах ММС и 580 г/т в пылях доводки при содержании в бадделеитовых концентратах от 250 до 770 г/т. Эти данные являются дополнительными аргументами в пользу рекомендуемой с начала 1990-х гг. техногеохимической ревизии производства Ковдорского ГОКа на широкий перечень дефицитных редких металлов (Ta, Hf, Sc и др.), включая вовлекаемые в добычу и обогащение новые виды сырья - апатитовые и штаффелитовые руды, а также все хвосты обогащения и промпродукты.
4) Сернокислые возвратные растворы выщелачивания урана, "АО Далур" (Курганская обл.) с содержанием скандия около 1 мг/л.
Руда Томторского месторождения содержит до 300 ppm скандия, от 1,12 до 13,3% ниобия, 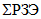 - от 5,33 до 28,27%. Месторождение расположено в Якутии.
- от 5,33 до 28,27%. Месторождение расположено в Якутии.
В России имеются готовые технологические решения по извлечению скандия из большинства перечисленных промышленных скандийсодержащих отходов, большой практический опыт по использованию продукции их переработки (фторида скандия) в сырье для получения алюминиево-скандиевой лигатуры, а также опыт применения в авиастроении целого ряда промышленных скандийсодержащих алюминиевых сплавов.
В 2024 году мировое потребление оксида скандия оценивалось примерно в 30 - 40 тонн в год при общей производственной мощности около 80 тонн в год. По оценкам отрасли, глобальное производство составило 40 тонн. Скандий извлекался из технологических отходов производства кобальта, никеля, титана и циркония. Лидером по производству является Китай.
В последние годы производство лигатуры Al - 2% Sc и оксида скандия в мире выросло с 15 - 20 до 30 - 40 т/год, т.е. в 2 раза за счет использования скандия в твердотопливных элементах [43]. Основным производителем оксида скандия (переработка руд титана и РЗЭ) является Китай; в провинции Hebei строится завод по производству 20 т/год высокочистого оксида скандия из сырья Папуа Новая Гвинея. Канада производит от 3 до 12 т/год Sc2O3 при переработке отходов. Компания Platina Scandium Project в New South Wales (Австралия) планирует производство из никелевых латеритов мощностью до 40 т/год Sc2O3. Компания ScaVanger project производит 21 тонну Sc2O3 в год попутно при производстве диоксида титана. На Филиппинах объем производства составляет от 7 до 8 т/год оксида скандия.
1.3.3.2 Иттрий почти всегда содержится вместе с лантаноидами в минеральном сырье. Несмотря на неограниченный изоморфизм, в группе редких земель в определенных геологических условиях возможна раздельная концентрация редких земель иттриевой и цериевой подгрупп. Например, со щелочными породами и связанными с ними постмагматическими продуктами преимущественное развитие получает цериевая подгруппа, а с постмагматическими продуктами гранитоидов с повышенной щелочностью - иттриевая. Большинство фторкарбонатов обогащено элементами цериевой подгруппы. Многие тантало-ниобаты содержат иттриевую подгруппу, а титанаты и титано-тантало-ниобаты - цериевую. Главнейшие минералы иттрия - ксенотим YPO4, гадолинит Y2FeBe2Si2O10.
Мировая добыча иттрия в эквиваленте Y2O3, содержащегося в концентратах РЗЭ, оценивается в 15 000 - 20 000 тонн. Большая часть этой добычи приходилась в 2024 г. на Китай и Бирму [43]. В 2024 г. Китай производил большую часть иттрия из концентрата РЗЭ глинистых рудных месторождений в южных провинциях - в основном в Фуцзяне, Гуандуне и Цзянси - и, в меньшей степени, из месторождений в Гуанси и Хунани. Иттрий также добывался из аналогичных глин в Бирме. Министерство промышленности и информационных технологий Китая увеличило квоты на добычу и разделение РЗЭ в 2024 году до 270 000 тонн в эквиваленте оксида редкоземельного металла. Содержание иттрия в квоте на добычу не уточнялось. Квоты на добычу полезных ископаемых составили 250 850 тонн легких редкоземельных металлов и 19 150 тонн ионно-адсорбционных глин. В 2024 году Китай экспортировал, по оценкам, 3100 тонн иттрия (в эквиваленте Y2O3) соединений и металлического иттрия. Ведущими странами-поставщиками экспорта (в порядке убывания) являются Япония, США, Нидерланды и Республика Корея [43].
Ведущими странами по общим запасам оксидов редкоземельных металлов являются Австралия, Бразилия, Китай, Индия, Россия и Вьетнам. Мировых запасов достаточно для удовлетворения текущего спроса. В России иттрий входит в состав коллективного концентрата карбонатов РЗЭ, производимого Соликамским магниевым заводом.
1.3.3.3 Лантаноиды входят в перечень стратегических видов сырья. Основная часть минеральной сырьевой базы РЗМ мира распределена среди четырех стран: Китай (31%), Россия (26%), Бразилия (15,5%), Вьетнам (15,5%). 95% производства концентратов РЗМ сосредоточено в Китае. Крупнейшим в мире является комплексное ниобий-редкоземельно-железорудное месторождение Байюнь-Обо (Внутренняя Монголия, Китай) с жилообразными телами карбонатитов, обогащенными редкоземельными элементами. Оруденение представлено бастнезитовыми рудами с гематитом, магнетитом, монацитом, пирохлором, эшинитом. Запасы РЗМ месторождения оценены в 48 млн т, что составляет около 81,7% запасов РЗМ Китая. Кроме того, запасы железа на месторождении составляют 470 млн т, ниобия - более 1 млн т. В южных провинциях Китая сосредоточены месторождения так называемых "ионных руд", представленных ионно-адсорбционными рудами в глинах кор выветривания по редкометалльным субщелочным лейкогранитам. Руды содержат невысокие концентрации (0,03 - 0,15%) РЗМ, в которых содержания РЗЭ иттриевой группы составляют около 70%. Благодаря наличию мощной минерально-сырьевой базы РЗМ Китай производит более 270 тыс. т РЗМ, что составляет более 80% их общемирового производства [7].
Крупнейшим продуцентом РЗМ также является австралийская компания Lynas Corporation Ltd, которая в 2012 г. начала разработку австралийского месторождения кор выветривания бастнезитовых карбонатитов Маунтин-Уэлд. В небольшом объеме разрабатываются монацитовые россыпи в Индии (~ 1,7 тыс. т TR2O3) и в Бразилии, где ведется разработка объектов кор выветривания карбонатитов.
За рубежом разрабатываемые на РЗМ месторождения сложены в основном мономинеральными легкообогатимыми рудами со средним содержанием до 10% 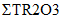 . Это бастнезитовые карбонатиты Китая и США, богатые россыпи с монацитом и ксенотимом в Индии, Австралии, Бразилии, коры выветривания щелочных гранитов и алюмосиликатных пород в Китае и Бразилии.
. Это бастнезитовые карбонатиты Китая и США, богатые россыпи с монацитом и ксенотимом в Индии, Австралии, Бразилии, коры выветривания щелочных гранитов и алюмосиликатных пород в Китае и Бразилии.
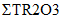 . Это бастнезитовые карбонатиты Китая и США, богатые россыпи с монацитом и ксенотимом в Индии, Австралии, Бразилии, коры выветривания щелочных гранитов и алюмосиликатных пород в Китае и Бразилии.
. Это бастнезитовые карбонатиты Китая и США, богатые россыпи с монацитом и ксенотимом в Индии, Австралии, Бразилии, коры выветривания щелочных гранитов и алюмосиликатных пород в Китае и Бразилии.Сырьевая база РЗМ Российской Федерации является одной из крупнейших в мире. Государственным балансом запасов полезных ископаемых учитываются запасы в количестве 28,53 млн т  , что позволяет стране занимать второе место в мире, уступая только Китаю. Доля распределенного фонда составляет 34,1%. Ресурсный потенциал существенно меньше, хотя и отличается высокой степенью изученности: прогнозные ресурсы категории P1 оценены почти в 8 млн т, категории P2 - в 0,435 млн т. Все они находятся в нераспределенном фонде недр. Российская сырьевая база РЗМ базируется на месторождениях апатит-нефелиновых и лопаритовых руд, причем главной ее особенностью является то, что РЗМ в основном являются попутными компонентами, содержание
, что позволяет стране занимать второе место в мире, уступая только Китаю. Доля распределенного фонда составляет 34,1%. Ресурсный потенциал существенно меньше, хотя и отличается высокой степенью изученности: прогнозные ресурсы категории P1 оценены почти в 8 млн т, категории P2 - в 0,435 млн т. Все они находятся в нераспределенном фонде недр. Российская сырьевая база РЗМ базируется на месторождениях апатит-нефелиновых и лопаритовых руд, причем главной ее особенностью является то, что РЗМ в основном являются попутными компонентами, содержание 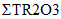 в которых редко превышает 1%. На сегодняшний день в отработку вовлечено почти 28% отечественных запасов РЗМ, при этом на долю руд, из которых они извлекаются, приходится всего 2% запасов страны.
в которых редко превышает 1%. На сегодняшний день в отработку вовлечено почти 28% отечественных запасов РЗМ, при этом на долю руд, из которых они извлекаются, приходится всего 2% запасов страны.
 , что позволяет стране занимать второе место в мире, уступая только Китаю. Доля распределенного фонда составляет 34,1%. Ресурсный потенциал существенно меньше, хотя и отличается высокой степенью изученности: прогнозные ресурсы категории P1 оценены почти в 8 млн т, категории P2 - в 0,435 млн т. Все они находятся в нераспределенном фонде недр. Российская сырьевая база РЗМ базируется на месторождениях апатит-нефелиновых и лопаритовых руд, причем главной ее особенностью является то, что РЗМ в основном являются попутными компонентами, содержание
, что позволяет стране занимать второе место в мире, уступая только Китаю. Доля распределенного фонда составляет 34,1%. Ресурсный потенциал существенно меньше, хотя и отличается высокой степенью изученности: прогнозные ресурсы категории P1 оценены почти в 8 млн т, категории P2 - в 0,435 млн т. Все они находятся в нераспределенном фонде недр. Российская сырьевая база РЗМ базируется на месторождениях апатит-нефелиновых и лопаритовых руд, причем главной ее особенностью является то, что РЗМ в основном являются попутными компонентами, содержание 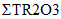 в которых редко превышает 1%. На сегодняшний день в отработку вовлечено почти 28% отечественных запасов РЗМ, при этом на долю руд, из которых они извлекаются, приходится всего 2% запасов страны.
в которых редко превышает 1%. На сегодняшний день в отработку вовлечено почти 28% отечественных запасов РЗМ, при этом на долю руд, из которых они извлекаются, приходится всего 2% запасов страны.Большая часть запасов РЗМ учитывается в апатит-нефелиновых месторождениях, где их содержание невелико, а извлечение, как правило, нерентабельно даже при условии разработки этих месторождений на другие виды сырья. Имеющиеся в России крупные объекты с уникально богатыми рудами часто размещены в отдаленных районах со слабо развитой инфраструктурой, а руды их труднообогатимы.
Распределение запасов и прогнозных ресурсов по территории страны неравномерно. Более 90% запасов РЗМ категорий A+B+C1+C2 сосредоточено в двух регионах - Мурманской области и Республике Саха (Якутия).
Сырьевая база редкоземельных металлов Российской Федерации локализована в небольшом числе регионов - половина запасов сосредоточена в объектах Мурманской области, из них около 40% - в лопаритовых рудах Ловозерского месторождения, еще примерно 60% - в апатит-нефелиновых объектах Хибинской группы. Более 43% отечественных запасов заключено в объектах Сибири и Дальнего Востока, где выявлены крупные месторождения, связанные с карбонатитами и корами выветривания по ним (Томторское в Республике Саха (Якутия), Чуктуконское в Красноярском крае и Белозиминское в Иркутской обл.), крупное Селигдарское месторождение апатит-карбонатных метасоматитов в Республике Саха (Якутия) и мелкие комплексные редкометалльные объекты в щелочных гранитах (Улуг-Танзекское в Республике Тыва и Зашихинское в Иркутской обл.) и метасоматитах (Катугинское в Забайкальском крае). Около 3% запасов РЗМ содержится в нефтеносных лейкоксеновых песчаниках Ярегского месторождения в Республике Коми. Кроме того, незначительные запасы подсчитаны в Республике Калмыкия в мелком Шаргадыкском месторождении редкоземельно-фосфор-урановых руд, где основные концентрации урана и редкоземельных элементов связаны с фоссилизированным костным детритом.
Государственным балансом запасов полезных ископаемых Российской Федерации учтено 17 коренных месторождений с запасами РЗМ. В девяти апатит-нефелиновых месторождениях Хибинской группы в Мурманской области заключено около 11 млн т РЗМ, или 55% российских запасов категорий A+B+C1+C2. Основным компонентом их руд является фосфор, РЗМ играют роль попутных при низких их концентрациях: среднее содержание составляет 0,34% 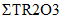 .
.
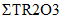 .
.Еще около 16% запасов редкоземельных металлов, преимущественно цериевой группы, сосредоточено в лопаритовых рудах титан-ниобий-тантал-редкоземельного Ловозерского месторождения. Это единственный объект в России, где ведется извлечение попутных РЗМ в концентраты для их дальнейшей переработки в индивидуальные оксиды и соединения РЗМ. Содержание в рудах отрабатываемых участков Карнасурт и Кедыквырпахк - 1,39% 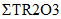 . Месторождения, подобные Ловозерскому, нигде более в мире на РЗМ не разрабатываются.
. Месторождения, подобные Ловозерскому, нигде более в мире на РЗМ не разрабатываются.
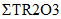 . Месторождения, подобные Ловозерскому, нигде более в мире на РЗМ не разрабатываются.
. Месторождения, подобные Ловозерскому, нигде более в мире на РЗМ не разрабатываются.Прогнозные ресурсы РЗМ категории P1 в Мурманской области не локализованы, здесь оценены прогнозные ресурсы категории P2 в перовскит-магнетитовых рудах месторождения Африканда (836 тыс. т). Республика Саха (Якутия) обладает значительным редкоземельным сырьевым потенциалом, и на ее территории в последние годы активно велись геологоразведочные работы на перспективных объектах как за счет средств федерального бюджета, так и собственных средств недропользователей. Запасы категорий ABC1+C2 составляют 4 529,7 тыс. т TR2O3 и учитываются на трех месторождениях: крупном апатитовом Селигдарском, участке Буранный редкометалльного Томторского и техногенной россыпи бассейна р. Уралсаах Центральная-Нижняя. Селигдарское месторождение заключает в себе 25,7% разведанных запасов РЗМ Российской Федерации (TR2O3 категории ABC1 4410,4 тыс. т) и находится в нераспределенном фонде недр. Подготавливается к эксплуатации месторождение Томторское участок Буранный.
Томторское месторождение имеет значительные разведанные запасы, и является одним из крупнейших в мире. Месторождение также характеризуется значительными запасами ниобия и скандия. Основное количество запасов редких металлов Томторского месторождения разведано в пределах Буранного участка; балансовые запасы категорий B+C1 составляют: 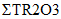 - 2640,4 тыс. т; по категории C2
- 2640,4 тыс. т; по категории C2 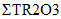 - 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6%
- 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6% 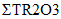 , имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
, имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
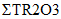 - 2640,4 тыс. т; по категории C2
- 2640,4 тыс. т; по категории C2 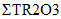 - 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6%
- 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6% 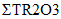 , имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
, имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.На участках Северный и Южный Томторского редкометалльного месторождения оценено 1487,8 тыс. т запасов категории C1+C2.
В рамках реализации подпрограммы 4 "Развитие производства традиционных и новых материалов" государственной программы "Развитие промышленности и повышение ее конкурентоспособности" в 2018 г. прошли государственную экспертизу и поставлены на Государственный баланс запасы категорий C1+C2 комплексных месторождений:
- Чуктуконское (Красноярский край) - 2 376 тыс. т 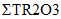 ; 3,4 тыс. т оксида скандия;
; 3,4 тыс. т оксида скандия;
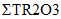 ; 3,4 тыс. т оксида скандия;
; 3,4 тыс. т оксида скандия;- Томторское (Республика Саха (Якутия)): по участку Буранный - 3 232,9 тыс. т 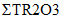 ; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т
; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т 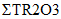 ; 2,2 тыс. т оксида скандия, запасы ниобия;
; 2,2 тыс. т оксида скандия, запасы ниобия;
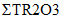 ; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т
; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т 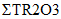 ; 2,2 тыс. т оксида скандия, запасы ниобия;
; 2,2 тыс. т оксида скандия, запасы ниобия;В результате доразведки редкометалльного месторождения Томторское участок Буранный, запасы редкоземельных металлов месторождения категорий B1+C1+C2 увеличились на 3,1 млн т.
Ближайшие перспективы развития редкоземельной промышленности в России связаны с реализацией дорожной карты Госкорпорации (ГК) "Росатом" развития высокотехнологичной области "Технологии новых материалов и веществ" на период до 2030 г., утвержденной Правительством Российской Федерации 27 апреля 2020 г. Предметом ее направления "Редкие и редкоземельные металлы" является, среди прочего, развитие производства РЗМ и полный отказ от их импорта к 2030 г. На развитие редкоземельной отрасли страны также нацелен национальный проект по обеспечению технологического лидерства "Новые материалы и химия". Его реализация будет осуществляться в период с 2025 по 2030 гг.
Добыча редкоземельных металлов в России составляет порядка 84 - 120 тыс. т оксидов в год, причем извлекается в концентраты и поступает на дальнейшую переработку 2 - 3% от этого количества. Добыча РЗМ сосредоточена в Мурманской области. Из добываемых апатит-нефелиновых руд вырабатываются апатитовый и нефелиновый концентраты. Содержащиеся в апатитовых концентратах РЗЭ в настоящее время в промышленном масштабе не извлекаются. Получаемый при переработке апатитового концентрата фосфогипс содержит около 0,5% суммы РЗЭ; разработан ряд технологий по извлечению РЗЭ из этого вида отходов [33, 60 - 66]. В настоящее время ГК "Скайград" реализует проект по комплексной переработке текущего фосфогипса Воскресенского завода минеральных удобрений с получением группового концентрата РЗЭ и 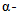 и
и 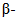 гипса. Производительность первой линии производства - 75 тыс. т. фосфогипса [66].
гипса. Производительность первой линии производства - 75 тыс. т. фосфогипса [66].
ООО "Ловозерский ГОК" в Мурманской области ведет добычу лопаритовых руд, содержащих соединения РЗМ, тантала, ниобия и титана. Получаемый лопаритовый концентрат содержит 95 - 97% минерала. На дальнейшую переработку лопаритовый концентрат направляется на ОАО "Соликамский магниевый завод", редкоземельной продукцией которого являются суммарные карбонаты La, Ce, Pr, Nd, Sm, Eu, Gd, дидима (смесь оксидов Pr+Nd). Содержание суммы оксидов РЗМ 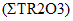 в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
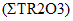 в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].Активно проводятся работы по разработке и внедрению промышленных технологий получения индивидуальных РЗМ (АО "ГК "Русредмет", ОАО СМЗ, АО "ЧМЗ"), из фосфогипса и экстракционной фосфорной кислоты (ОАО "ФосАгро-Череповец", ПАО "Акрон", АО "Росатом Недра"). На сегодняшний день ООО "ЛИТ" имеет производство по разделению группового концентрата РЗЭ производительностью 150 - 180 т с получением оксидов (карбонатов) церия, лантана, неодима, празеодима, концентрата среднетяжелых РЗЭ, продукции второго передела-азотнокислого раствора лантана для катализаторов нефтехимии, неодеканоата неодима и хлоридов неодима и празеодима - компонентов катализатора синтеза каучука, полирующих порошков на основе оксидов церия и др. [34 - 36, 73, 77].
Необходимое количество индивидуальных РЗЭ в Россию поступает по импорту. Мировое производство РЗЭ в 2024 г. составило 390 тыс. т, из которых 270 тыс. т произвел Китай. Мировые прогнозные ресурсы РЗЭ превышают 90 млн. т., из которых у России более 8 млн т. оксидов РЗЭ [3, 5]. прогнозные ресурсы категории P3 в бокситоносных корах выветривания на Боровско-Светлинском участке (43 тыс. т).
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: один и тот же текст приведен дважды. |
Республика Саха (Якутия) обладает значительным редкоземельным сырьевым потенциалом, и на ее территории в последние годы активно велись геологоразведочные работы на перспективных объектах как за счет средств федерального бюджета, так и собственных средств недропользователей. Запасы категорий ABC1+C2 составляют 4 529,7 тыс. т TR2O3 и учитываются на трех месторождениях: крупном апатитовом Селигдарском, участке Буранный редкометалльного Томторского и техногенной россыпи бассейна р. Уралсаах Центральная-Нижняя. Селигдарское месторождение заключает в себе 25,7% разведанных запасов РЗМ Российской Федерации (TR2O3 категории ABC1 4410,4 тыс. т) и находится в нераспределенном фонде недр. Подготавливается к эксплуатации месторождение Томторское участок Буранный.
Томторское месторождение имеет значительные разведанные запасы, и является одним из крупнейших в мире. Месторождение также характеризуется значительными запасами ниобия и скандия. Основное количество запасов редких металлов Томторского месторождения разведано в пределах Буранного участка; балансовые запасы категорий B+C1 составляют: 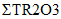 - 2640,4 тыс. т; по категории C2
- 2640,4 тыс. т; по категории C2 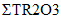 - 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6%
- 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6% 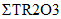 , имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
, имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
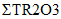 - 2640,4 тыс. т; по категории C2
- 2640,4 тыс. т; по категории C2 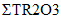 - 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6%
- 592,5 тыс. т. Комплексные редкометалльные руды содержат 10,6% 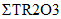 , имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.
, имеют сложный состав, по набору минералов не имеющий аналогов в мире, характеризуются тонкодисперсными выделениями рудных минералов, их тесными взаимопрорастаниями и весьма сложны для переработки. Месторождение находится в районе с суровыми климатическими условиями и неразвитой инфраструктурой.На участках Северный и Южный Томторского редкометалльного месторождения оценено 1487,8 тыс. т запасов категории C1+C2.
В рамках реализации подпрограммы 4 "Развитие производства традиционных и новых материалов" государственной программы "Развитие промышленности и повышение ее конкурентоспособности" в 2018 г. прошли государственную экспертизу и поставлены на Государственный баланс запасы категорий C1+C2 комплексных месторождений:
- Чуктуконское (Красноярский край) - 2 376 тыс. т 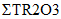 ; 3,4 тыс. т оксида скандия;
; 3,4 тыс. т оксида скандия;
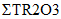 ; 3,4 тыс. т оксида скандия;
; 3,4 тыс. т оксида скандия;- Томторское (Республика Саха (Якутия)): по участку Буранный - 3 232,9 тыс. т 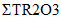 ; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т
; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т 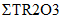 ; 2,2 тыс. т оксида скандия, запасы ниобия;
; 2,2 тыс. т оксида скандия, запасы ниобия;
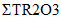 ; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т
; 11,5 тыс. т оксида скандия, запасы ниобия; по участкам Северный и Южный - 905 тыс. т 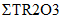 ; 2,2 тыс. т оксида скандия, запасы ниобия;
; 2,2 тыс. т оксида скандия, запасы ниобия;В результате доразведки редкометалльного месторождения Томторское участок Буранный, запасы редкоземельных металлов месторождения категорий B1+C1+C2 увеличились на 3,1 млн т.
Ближайшие перспективы развития редкоземельной промышленности в России связаны с реализацией дорожной карты Госкорпорации (ГК) "Росатом" развития высокотехнологичной области "Технологии новых материалов и веществ" на период до 2030 г., утвержденной Правительством Российской Федерации 27 апреля 2020 г. Предметом ее направления "Редкие и редкоземельные металлы" является, среди прочего, развитие производства РЗМ и полный отказ от их импорта к 2030 г. На развитие редкоземельной отрасли страны также нацелен национальный проект по обеспечению технологического лидерства "Новые материалы и химия". Его реализация будет осуществляться в период с 2025 по 2030 гг.
Добыча редкоземельных металлов в России составляет порядка 84 - 120 тыс. т оксидов в год, причем извлекается в концентраты и поступает на дальнейшую переработку 2 - 3% от этого количества. Добыча РЗМ сосредоточена в Мурманской области. Из добываемых апатит-нефелиновых руд вырабатываются апатитовый и нефелиновый концентраты. Содержащиеся в апатитовых концентратах РЗЭ в настоящее время в промышленном масштабе не извлекаются. Получаемый при переработке апатитового концентрата фосфогипс содержит около 0,5% суммы РЗЭ; разработан ряд технологий по извлечению РЗЭ из этого вида отходов [33, 60 - 66]. В настоящее время ГК "Скайград" реализует проект по комплексной переработке текущего фосфогипса Воскресенского завода минеральных удобрений с получением группового концентрата РЗЭ и 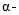 и
и 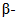 гипса. Производительность первой линии производства - 75 тыс. т. фосфогипса [66].
гипса. Производительность первой линии производства - 75 тыс. т. фосфогипса [66].
ООО "Ловозерский ГОК" в Мурманской области ведет добычу лопаритовых руд, содержащих соединения РЗМ, тантала, ниобия и титана. Получаемый лопаритовый концентрат содержит 95 - 97% минерала. На дальнейшую переработку лопаритовый концентрат направляется на ОАО "Соликамский магниевый завод", редкоземельной продукцией которого являются суммарные карбонаты La, Ce, Pr, Nd, Sm, Eu, Gd, дидима (смесь оксидов Pr+Nd). Содержание суммы оксидов РЗМ 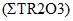 в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
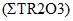 в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].
в карбонатах превышает 40%. Основная масса карбонатов РЗМ производства Соликамского магниевого завода поставляется компании NPM Silmet в Эстонию и Китай. Производство карбонатов РЗЭ в виде суммарного концентрата составило в 2024 г. 2500 т/год [3].Активно проводятся работы по разработке и внедрению промышленных технологий получения индивидуальных РЗМ (АО "ГК "Русредмет", ОАО СМЗ, АО "ЧМЗ"), из фосфогипса и экстракционной фосфорной кислоты (ОАО "ФосАгро-Череповец", ПАО "Акрон", АО "Росатом Недра"). На сегодняшний день ООО "ЛИТ" имеет производство по разделению группового концентрата РЗЭ производительностью 150 - 180 т с получением оксидов (карбонатов) церия, лантана, неодима, празеодима, концентрата среднетяжелых РЗЭ, продукции второго передела-азотнокислого раствора лантана для катализаторов нефтехимии, неодеканоата неодима и хлоридов неодима и празеодима - компонентов катализатора синтеза каучука, полирующих порошков на основе оксидов церия и др. [34 - 36, 73, 77].
Необходимое количество индивидуальных РЗЭ поступает по импорту. Мировое производство РЗЭ в 2024 г. составило 390 тыс. т, из которых 270 тыс. т произвел Китай. Мировые прогнозные ресурсы РЗЭ превышают 90 млн. т., из которых у России более 8 млн т. оксидов РЗЭ [3, 5].
1.3.4.1 Ванадий относится к рассеянным элементам и в природе в свободном виде не встречается. Содержание ванадия в земной коре - 9,0·10-3% по массе. Наиболее высокое среднее содержание ванадия в магматических породах отмечается в габбро и базальтах (230 - 290 г/т). В осадочных породах значительное накопление ванадия происходит в биолитах (асфальтитах, углях, битуминозных фосфатах), битуминозных сланцах, бокситах, а также в оолитовых и кремнистых железных рудах. Близость ионных радиусов ванадия и широко распространенных в магматических породах железа и титана приводит к тому, что ванадий в гипогенных процессах целиком находится в рассеянном состоянии и не образует собственных минералов. Его носителями являются многочисленные минералы титана (титаномагнетит, сфен, рутил, ильменит), слюды, пироксены и гранаты, обладающие повышенной изоморфной емкостью по отношению к ванадию. Важнейшие минералы: патронит V(S2)2, ванадинит Pb5(VO4)3Cl и некоторые другие. Основной источник получения ванадия - железные руды, содержащие ванадий как примесь. Известны месторождения в Перу, США, ЮАР, Финляндии, Австралии, Армении, России, Турции, Англии [12]. Заметную роль играет рециклинг ванадия из отработанных катализаторов.
В России основные учтенные запасы ванадия сосредоточены в низкотитанистых титаномагнетитовых рудах магматических месторождений (Гусевогорское, Первоуральское, Волковское).
Качканарский горно-обогатительный комбинат (ЕВРАЗ КГОК) входит в пятерку крупнейших горнорудных предприятий страны, более того, это единственный производитель ванадийсодержащей железной руды в России. Комбинат разрабатывает Гусевогорское месторождение титаномагнетитовых железных руд, содержащих примеси ванадия. Из бедных титаномагнетитовых руд получают высококачественные железованадиевые концентраты для агломерации и окомкования с массовой долей железа 60 и 63% соответственно и пятиокиси ванадия 0,55 - 0,6%. Почти весь пентаоксид ванадия в России производится на двух предприятиях: "Евраз Ванадий Тула" и ОАО "Чусовской металлургический завод".
К 2024 году потребление ванадия в мире в виде алюминиево-ванадиевой лигатуры, феррованадия, руды, концентрата и соединений достигло 100 тыс. тонн. Россия стабильно входит в тройку крупнейших экспортеров оксидов и гидроксидов ванадия; производство ванадия в 2024 г. в России составило 21 тыс. тонн [3]. Ожидаемый рост потребления ванадия связывают с повышением объема производства ванадиевых проточных аккумуляторных батарей (VRFB) и натрий-ионных аккумуляторов.
По оценкам Геологической службы США (USGS), мировые прогнозные ресурсы ванадия в фосфатных рудах, титаномагнетите, урансодержащих песчаниках и алевритах, бокситах и углеродсодержащих материалах, таких как уголь, сырая нефть, горючие сланцы и битуминозные пески, составляют более 63 млн тонн [3].
1.3.4.2 Ниобий входит в перечень основных видов стратегического минерального сырья. Запасы в России на 01.01.2024 составляют 8527 тыс. т Nb2O5, доля распределенного фонда - 11,2%, прогнозные ресурсы - 1540 тыс. т пентаоксида ниобия [5]. Прогнозные ресурсы ниобия учтены всего на девяти объектах, расположенных в Северо-Западном, Сибирском и Дальневосточном округах. Подавляющая часть российских прогнозных ресурсов категории P1 (81,4%) находится в пределах Чуктуконского рудного поля в Красноярском крае и связана с корой выветривания карбонатитового массива, где ниобий учитывается как попутный компонент. Россия располагает крупной сырьевой базой ниобия, достаточной для обеспечения внутренних потребностей в металле на длительную перспективу, однако степень ее освоенности низкая.
Промышленные минералы ниобия: колумбит-танталит (Fe, Mn) (Nb, Ta)2O6, пирохлор (Na, Ca, TR, U)2(Nb, Ta, Ti)2O6(OH, F) (Nb2O5 30 - 63%), лопарит (Na, Ca, Ce) (Ti, Nb)O3 ((Nb, Ta)2O5 8 - 10%). Иногда используются эвксенит, торолит, ильменорутил, а также минералы, содержащие ниобий в виде примесей (ильменит, касситерит, вольфрамит). Содержание ниобия в сырье увеличивается от ультраосновных (0,2 г/т Nb) к кислым породам (24 г/т Nb). Ниобию всегда сопутствует тантал. Близкие химические свойства ниобия и тантала обусловливают совместное их нахождение в одних и тех же минералах и участие в общих геологических процессах. Ниобий способен замещать титан в ряде титансодержащих минералов (сфен, ортит, перовскит, биотит). Форма нахождения ниобия в природе может быть разной: рассеянной (в породообразующих и акцессорных минералах магматических пород) и минеральной. В щелочных ультраосновных породах ниобий рассеивается в минералах типа перовскита и в эвдиалите. В экзогенных процессах минералы ниобия и тантала, являясь устойчивыми, могут накапливаться в делювиально-аллювиальных россыпях (колумбитовые россыпи), иногда - в бокситах коры выветривания. Месторождения ниобия расположены в США, Японии, России, Бразилии, Канаде [3]. Качество российской минерально-сырьевой базы ниобия в целом низкое. Богатые руды (> 1% Nb2O5) выявлены только в коре выветривания Томторского месторождения пирохлор-монацит-крандаллитовых руд. В среднем по месторождению содержание Nb2O5 составляет 4,2%, варьируя от 1,6 до 4,5% в зависимости от участка и конкретного типа руды. Среднее содержание в рудах остальных месторождений - 0,34% Nb2O5.
Производство соединений ниобия в России (тантал-ниобиевый химконцентрат, пентахлориды и пентаоксиды ниобия и тантала) осуществляется лишь в объеме около 600 т на Соликамском магниевом заводе (СМЗ) из лопарита, добываемого на Ловозерском месторождении. При этом потребность в них составляет 3 - 4 тыс. т в пересчете на Nb2O5.
Производство ниобия в 2024 г. в мире составило 110 тыс. т, из них 110 тыс. т - Бразилией, и 350 т. произведено в России. Мировые резервы ниобия оцениваются в более чем 19 млн. т., из которых 18 млн. т - в Бразилии [3].
В перспективе при переработке 150 тыс. т комплексных руд Томторского месторождения наряду с РЗМ и Sc возможно получать большой объем Nb2O5 (порядка 8 - 9 тыс. т в год), что полностью удовлетворит внутренние потребности. Также, в зависимости от размещения будущих перерабатывающих производств, перечня наиболее востребованных попутных компонентов, логистики и других факторов могут быть приняты решения о начале освоения других месторождений - Белозиминского, Большетагнинского, Катугинского и т.д. [7].
В ближайшие годы дефицит ниобия на российском рынке сохранится, и потребности российских предприятий, скорее всего, будут удовлетворяться за счет импорта феррониобия из Бразилии или других стран.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: п. [15] Библиографии отсутствует. |
1.3.4.3 Тантал. Тантал входит в перечень основных видов стратегического минерального сырья. В земной коре на его долю приходится 2,5·10-4%. В природе встречается в виде двух изотопов: стабильного 181Ta (99,9877%) и радиоактивного (вероятно) с периодом полураспада более 1015 лет 180mTa (0,0123%). Последний является чрезвычайно стабильным изомером (возбужденным состоянием) изотопа 180Ta, период полураспада которого всего чуть более 8 ч [15]. Известно около 20 собственных минералов тантала - серия колумбит-танталит, воджинит, лопарит, манганотанталит и др., а также более 60 минералов, содержащих тантал. Все они связаны с эндогенным минералообразованием. В минералах тантал всегда находится совместно с ниобием вследствие сходства их физических и химических свойств. Тантал - типично рассеянный элемент, так как изоморфен со многими химическими элементами. Месторождения тантала приурочены к гранитным пегматитам, карбонатитам и щелочным расслоенным интрузиям. В составе руд тантал всегда ассоциирует с ниобием, причем их количественные соотношения в зависимости от генетических условий варьируют в широких пределах, при обычном преобладании ниобия. В соответствии с этим выделяют руды собственно танталовые (отношение Nb/Ta от 0,2 до 4, ниобий не играет заметной роли в стоимости получаемой продукции), танталониобиевые (отношение Nb/Ta от 5 до 20 с преобладающим, но сопоставимым в денежном выражении объемом получаемой ниобиевой продукции) и ниобиевые (отношение Nb/Ta > 20, извлечение тантала экономически нецелесообразно, поэтому он совместно с ниобием поступает в коллективный продукт, а при геолого-экономической оценке суммируется с ним). В танталовых и ниобий-танталовых рудах в промышленных концентрациях могут содержаться другие полезные компоненты. В танталовых рудах это обычно литий, цезий, рубидий, бериллий, иногда олово. В ниобий-танталовых рудах часто содержатся РЗМ, цирконий, гафний, торий, иногда уран, титан, литий, рубидий, флюорит, криолит и др. В зависимости от характера танталониобиевой минерализации в редкометалльных месторождениях России выделяются следующие основные типы руд: лопаритовый, пирохлоровый, пирохлор-колумбитовый, гатчеттолитовый, танталитовый, колумбитовый, танталит-колумбитовый и микролитовый. Качество российской минерально-сырьевой базы тантала в целом низкое. Богатые руды с содержанием Ta2O5 более 0,025% выделены только в пределах отдельных горизонтов и участков уникального Ловозерского месторождения.
Самые крупные месторождения танталовых руд находятся во Франции, Египте, Таиланде, Китае. Месторождения танталовых руд имеются также в Мозамбике, Австралии, Нигерии, Канаде, Бразилии, СНГ, ДРК, Малайзии. Крупнейшее мировое месторождение танталовых руд Гринбушес расположено в Австралии в штате Западная Австралия в 250 км к югу от Перта [12].
У России процент потребления тантала довольно низок - примерно 2%, так же невелика и добыча. В России значительная доля запасов приходится на ниобиевые и титановые месторождения, которым сопутствует тантал.
По состоянию на 01.01.2024 балансовые запасы тантала, учтенные в рудах 24 месторождений, составили 427 тыс. т Ta2O5, в рудах еще восьми месторождений учитываются только забалансовые запасы. Забалансовые запасы тантала в целом по стране составляют 126,5 тыс. т Ta2O5. В распределенном фонде недр находится всего 8,8% его запасов.
Зашихинское тантал-ниобиевое месторождение, расположенное в Нижнеудинском районе Иркутской области, характеризуется самым высоким среди российских месторождений содержанием оксида тантала в руде (около 0,03%). Освоение Зашихинского месторождения позволит снять зависимость страны от импорта танталовой продукции и значительно снизить зависимость от импортной ниобиевой продукции (прежде всего феррониобия).
Разведаны следующие ниобий-танталовые месторождения: Катугинское (Читинская обл.) - 0,019% Ta2O5, Среднезиминское (Восточный Саян) - 0,024% Ta2O5, Ковдорское (Мурманская обл.) - 0,012% Ta2O5, Вуориярвинское (участок Тухта-Вара) - 0,013% Ta2O5, Себльяврское (Мурманская обл.) - менее 0,012% Ta2O5, Гулинское (Западное Прианабарье).
Поставщиками на рынок металлургического тантала являются H.C. Starck (Германия), GAM (Австралия - США), китайские производители, АО "Ульбинский металлургический завод" (Казахстан), Mitsui Mining & Smelting (Япония), AMG (Бразилия), ОАО "Соликамский магниевый завод" и AS Silmet (Эстония).
В 2024 г. в мире произведено 2040 т тантала, лидером среди производителей является Конго (Киншаса), где объем производства составил 880 т; в России произведено 29 т тантала. Основные мировые ресурсы тантала находятся в Австралии, Бразилии, Канаде и Китае [43].
1.3.4.4 Цирконий. Мировой минерально-сырьевой потенциал циркония огромен и составляет более 100 млн т оксида металла, сосредоточенных главным образом в прибрежно-морских россыпях. Странами-лидерами по запасам сырья и производству цирконового концентрата являются Австралия - 14 млн т ZrO2 и 600 тыс. т производства концентрата, ЮАР - 7,2 млн т и 350 тыс. т, Индия - 9 млн т и 110 тыс. т. Запасы диоксида циркония России составляют около 12 млн т при производстве концентрата 8 тыс. т в год [45]. При этом из них в разрабатываемых и осваиваемых объектах заключено 3,1 млн т запасов диоксида циркония категорий A+B+C1+C2; по величине этих активных запасов страна занимает четвертое место в мире. Российская Федерация располагает значительной, но слабо освоенной сырьевой базой циркония.
В отличие от основных стран-продуцентов циркониевых концентратов, в российской минерально-сырьевой базе преобладают коренные магматогенные месторождения - в них находится почти 70% запасов диоксида циркония, в россыпных объектах - всего 30%. Половина российских запасов диоксида циркония заключена в двух крупных коренных месторождениях, приуроченных к массивам редкометалльных гранитов - циркон-пирохлоркриолитовом Катугинском (3,09 млн т) в Забайкальском крае и циркон-пирохлор-колумбитовом Улуг-Танзекском (2,9 млн т) в Республике Тыва. Комплексные труднообогатимые руды с танталом, ниобием, редкоземельными элементами и ураном содержат 1,58% ZrO2 в подготавливаемом к освоению Катугинском и 0,4% ZrO2 - в не переданном в освоение Улуг-Танзекском месторождении. Нигде в мире месторождения подобного типа не разрабатываются. В Катугинском рудном районе локализованы незначительные прогнозные ресурсы диоксида циркония категории P1 (11,5 тыс. т) в циркон-пирохлор-криолитовых россыпях.
В Мурманской области Государственным балансом запасов полезных ископаемых учитываются также гигантские забалансовые запасы коренных эвдиалитовых руд участка Аллуайв Ловозерского редкометалльного месторождения - 7,275 млн т диоксида циркония. В рудах цирконий находится в составе минерала эвдиалита - сложного силиката циркония и редких земель иттриевой группы; руды содержат в среднем 1,83% ZrO2, но на отдельных участках содержание ZrO2 достигает 5 - 9%.
В Западно-Сибирской россыпной провинции на территории Томской, Омской, Новосибирской областей и Ханты-Мансийского автономного округа сосредоточено 15,5% отечественных запасов диоксида циркония в россыпях, большей частью - в крупном Туганском и среднем Георгиевском циркон-рутил-ильменитовых месторождениях Томской области. Руды осваиваемого Туганского месторождения залегают на глубине 10 - 98 м, руды нелицензированного Георгиевского месторождения на глубине 120 - 180 м.
В Нижегородской области находится самое богатое из российских по содержанию ZrO2 Лукояновское циркон-рутил-ильменитовое месторождение среднего масштаба; в его наиболее крупной Итмановской россыпи, залегающей на глубине 40 - 80 м, заключено 389 тыс. т запасов диоксида циркония [45].
Россия - единственная страна, выпускающая бадделеитовый концентрат из руд коренного месторождения - Ковдорского бадделеит-апатит-магнетитового в Мурманской области. В месторождении сконцентрировано 2,29 млн т, или около 20% запасов диоксида циркония России. Цирконий, как и фосфор, является попутным компонентом в его рудах; основной компонент - железо. Содержание диоксида циркония в рудах невысокое - 0,15%, но минералом циркония является бадделеит - природный диоксид циркония (ZrO2), более редкий и ценный, чем содержащийся в россыпях силикат циркония - циркон (ZrSiO4). Ковдорское техногенное месторождение, представленное отходами обогащения бадделеит-апатит-магнетитовых руд, содержит 37,7 тыс. т запасов диоксида циркония категорий A+B+C1. Объем производимого концентрата составляет около 7 - 8 тыс. т в год и практически полностью экспортируется. [45]
АО "Туганский горно-обогатительный комбинат "Ильменит", запуск которого состоялся в конце 2021 г., добывает и перерабатывает рудные пески, из которых производит ильменитовый, рутил-лейкоксеновый и цирконовый концентраты.
В 2024 г. в мире выпуск циркониевой продукции (диоксида циркония) составил 1,5 млн. т., из которых 0,5 млн. т составило производство в Австралии. Мировые резервы оцениваются в более 70 млн. т [43].
1.3.4.5 Титан находится на 9-м месте по распространенности в природе. Содержание в земной коре - 0,6% по массе [46]. В ультраосновных породах присутствует 300 г/т, в основных - 9 кг/т, в кислых - 2,3 кг/т, в глинах и сланцах - 4,5 кг/т. В земной коре титан почти всегда четырехвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках. Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30% TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях [8], [10].
Российская Федерация располагает одной из крупнейших в мире сырьевой базой титана, однако освоена она крайне слабо, в связи с чем титановая промышленность страны работает на импортном сырье. В отработку вовлечено лишь 7,2% запасов диоксида титана страны, причем только из 0,1% добываемого из недр сырья металл извлекается в концентраты, остальное уходит в отвалы. Тем не менее в России действует крупное производство металлического титана на базе привозного сырья, что позволяет России входить в тройку крупнейших мировых продуцентов губчатого титана, уступая только Китаю и Японии.
Балансовые запасы диоксида титана России ~ 600,45 млн т. Запасы категорий A+B+C1 составляют немногим менее половины балансовых запасов - 261,4 млн т, при этом лишь 45% от этого количества находится в разрабатываемых, осваиваемых и разведываемых месторождениях [45]; по величине этой активной части запасов Россия находится на третьем месте в мире с долей 13%. Прогнозные ресурсы диоксида титана России огромны, причем более трети из них имеет высокую степень достоверности.
Российская минерально-сырьевая база титана характеризуется большим разнообразием с преобладанием коренных месторождений, в которых заключено 97% запасов диоксида титана страны: 46% запасов находится в погребенных литифицированных россыпях Ярегского нефте-титанового месторождения, 37% - в магматогенных месторождениях в габброидах, 14% - в магматогенных месторождениях в щелочных породах. В погребенных прибрежно-морских россыпях Восточно-Европейской и Западно-Сибирской россыпных провинций заключено только 3% запасов диоксида титана РФ.
Большая часть запасов российских магматогенных месторождений в габброидах (18% российских) представлена ильменит-титано-магнетитовыми рудами, одно месторождение (Кручининское) содержит апатит-ильменит-титаномагнетитовые руды (8%), остальные (11%) - титаномагнетитовые; все руды комплексные с железом, ванадием, иногда фосфором и другими элементами. Наиболее перспективны месторождения с высокой долей диоксида титана, содержащегося в ильмените: ильменит-титаномагнетитовые, апатит-ильменит-титаномагнетитовые и ильменит-магнетитовые, поскольку извлекать диоксид титана из титаномагнетита пока не удается [45].
Почти половина (46%) отечественных запасов титана сосредоточена в Тимано-Печорской титановой провинции в Республике Коми в Ярегском нефтетитановом месторождении. Оно представляет собой древнюю многопластовую литифицированную россыпь, залегающую на глубине 150 - 280 м. Руды месторождения - нефтеносные кварцевые песчаники с лейкоксеном, содержащие 10,4% диоксида титана, являются одними из самых богатых в России. Однако извлечение диоксида титана из лейкоксена представляет большую сложность из-за высокого содержания в нем кремнезема. За рубежом из подобного типа битуминозных песчаников района Атабаска в Канаде диоксид титана также до сих пор не извлекается. На флангах Ярегского месторождения и в Пижемском рудопроявлении подобного типа локализовано по 15% российских прогнозных ресурсов диоксида титана категорий P1 и P2.
В Карело-Кольской титановой провинции в Мурманской области заключено более пятой части российских запасов диоксида титана. Большая их часть находится в магматогенных месторождениях с бедными рудами в щелочных породах - около 12% в семи апатит-нефелиновых месторождениях Хибинской группы (0,3 - 3,5% TiO2) и 1% в мелком редкометалльном Ловозерском месторождении лопаритовых руд (1,29% TiO2). Титан является попутным компонентом и извлекается лишь из руд Ловозерского месторождения. Еще 8% российских запасов диоксида титана находится в крупном магматогенном месторождении в габброидных породах Юго-Восточная Гремяха. Его руды имеют достаточно высокое содержание TiO2 - 8,6%. В апатит-титаномагнетит-ильменитовом проявлении Гремяха-Вырмес с небогатыми рудами, содержащими 6,8% TiO2 локализовано 12,2 млн т, или около 4% российских прогнозных ресурсов категории P1; еще 2,6 млн т ресурсов категории P1 и 3,1 млн т категории P2 выявлено в Палалахтинском рудопроявлении с достаточно богатыми ильменит-магнетитовыми рудами, содержащими 10% TiO2.
В Олекмо-Становой титановой провинции в Забайкальском крае разведано 18% российских запасов диоксида титана. Они заключены в двух крупных месторождениях: апатит-ильменит-титаномагнетитовом Кручининском и титаномагнетитовом Чинейском. Руды Кручининского месторождения содержат 8,4% TiO2, Чинейского - только 6,5% TiO2, но они богаче по содержанию железа (33,5%) и пентаоксида ванадия - 0,53% (в Кручининском - 18% и 0,1% соответственно). Освоение месторождений сдерживается плохой обогатимостью руд и отсутствием технологии получения кондиционной титановой продукции. На флангах Чинейского месторождения локализованы значительные прогнозные ресурсы диоксида титана в рудах с содержанием 6,8% TiO2 - 34 млн т категории P1 (9% российских).
Также в Олекмо-Становой провинции на территории Хабаровского края в апатит-ильменит-титаномагнетитовых рудах (Геранский рудный район), содержащих 5,5 - 8,9% TiO2, оценены прогнозные ресурсы диоксида титана категории P1 в количестве 34 млн т (9% российских). В Республике Бурятия в Витимконском рудном поле локализована почти треть прогнозных ресурсов категории P2 в титаномагнетит-ильменитовых рудах с содержанием 7,6% TiO2.
В Уральской титановой провинции в Челябинской области находится Медведевское ильменит-титаномагнетитовое месторождение, в котором сконцентрировано 5% российских запасов диоксида титана. Его руды, содержащие 7% TiO2, труднообогатимы из-за тонкого прорастания слагающих их минералов. На флангах месторождения и в россыпных проявлениях локализованы незначительные ресурсы диоксида титана категории P1 - 4 млн т и столько же категории P2.
Производителем титановых концентратов из собственного сырья в России является Ловозерский ГОК, ведущий добычу на одноименном месторождении с выпуском лопаритового концентрата, содержащего 38 - 44% TiO2 для дальнейшей переработки на Соликамском магниевом заводе с получением тетрахлорида титана и губчатого титана по хлоридной технологии. Предприятиями компании АО "Апатит" на месторождениях Хибинской группы из хвостов флотации апатит-нефелиновых руд при получении апатитового концентрата дополнительно извлекают незначительное количество титансодержащего сфенового концентрата (28% TiO2), который перерабатывается на титано-кальциевый пигмент, используемый в производстве масляных красок и эмалей. Подавляющая часть сфена и титаномагнетита остаются в отходах обогащения, которые складируются в хвостохранилища в связи с отсутствием эффективной промышленной технологии извлечения из них диоксида титана. Обеспеченность добывающих компаний сырьем значительна и достигает 50 лет [45].
АО "Туганский горно-обогатительный комбинат "Ильменит", запуск которого состоялся в конце 2021 г., добывает и перерабатывает рудные пески, из которых производит ильменитовый, рутил-лейкоксеновый и цирконовый концентраты.
В Амурской области добывается ильменитовый концентрат с содержанием диоксида титана 48 - 50% на Куранахском ильменит-титаномагнетитовом месторождении, разрабатываемом на железо и не учитываемом Государственным балансом запасов титана.
Более 95% производства губчатого титана обеспечивает ПАО "Корпорация "ВСМПО-АВИСМА". Пигментный диоксид титана производит только одна компания - АФ ООО "Титановые инвестиции" на заводе в г. Армянске, Республика Крым.
В мире россыпные месторождения обеспечивают около 70% производства диоксида титана в титановых концентратах и шлаках. Остальные 30% получают из руд коренных магматогенных месторождений в габброидах, разрабатываемых в Канаде - месторождение Лак-Тио с рудами, содержащими 34% TiO2, в Норвегии - месторождение Теллнес (18% TiO2), в Китае - месторождения группы Паньчжихуа (6 - 12% TiO2) и в России - Куранахское месторождение (9,8% TiO2).
В 2024 г. мировое производство металла и диоксида титана составило 320 тыс. т и 9800 тыс. т, в России - 20 тыс. т. и 55 тыс. т, соответственно. Мировые ресурсы анатаза, ильменита и рутила оценивается более 2 млрд. тонн [43].
1.3.4.6 Вольфрам. Вольфрам входит в перечень основных видов стратегического минерального сырья [41], а также в перечень дефицитных видов твердых полезных ископаемых [42]. По степени обеспеченности потребностей национальной экономики и необходимого экспорта запасами минерального сырья вольфрам относится к третьей группе полезных ископаемых, куда входят импортозависимые дефицитные виды.
Россия занимает третье место в мире как по размерам сырьевой базы вольфрама (после Китая и Казахстана), так и по объемам его добычи (после Китая и Вьетнама). В настоящее время в отработку вовлечено менее 6% балансовых запасов вольфрама страны.
Учитываемые Государственным балансом запасы полезных ископаемых запасы вольфрама значительны и составляют на 01.01.2024 категории A+B+C1 945,4 тыс. т, категории C2 370,2 тыс. т в пересчете на WO3. Прогнозные ресурсы категории P1 оцениваются в 199,5 тыс. т, P2 - 879,1 тыс. т, P3 - 5163,2 тыс. т WO3 [45].
По своей структуре российская сырьевая база вольфрама в целом соответствует мировой. Основу и той, и другой составляют месторождения двух типов: штокверкового (в том числе с вольфрам-молибденовыми рудами) и скарнового. В то же время в России роль жильных месторождений принципиально меньше, чем за рубежом, что в значительной степени связано с их исчерпанием в результате отработки. Среди объектов, отнесенных к прочим, преобладают грейзеновые и оловорудные с попутным вольфрамом; в их число также входят россыпи.
По данным Минприроды, на 2025 год в России зарегистрировано порядка 95 месторождений вольфрамовых руд.
Существенно вольфрамовые месторождения относятся к трем типам: скарновому, штокверковому и жильному. Скарновые объекты сложены шеелитовыми рудами неоднородного качества, и имеющими комплексный состав (возможные попутные компоненты Mo, Cu, Bi, Au, Ag и др.). В их числе эксплуатируемое, но практически отработанное Восток 2 в Приморском крае и самое крупное в России и одно из крупнейших в мире Тырныаузское в Кабардино-Балкарской Республике. Штокверковые месторождения содержат руды с вольфрамитовой (крупное Инкурское в Республике Бурятия и среднее Спокойнинское в Забайкальском крае), и с шеелитовой (крупное Кти-Тебердинское в Карачаево-Черкесской Республике) минерализацией. Жильные объекты сложены вольфрамитовыми рудами, но практически все месторождения по запасам относятся к мелким. Среди объектов, отнесенных к прочим, преобладают грейзеновые и оловорудные с попутным вольфрамом; в их число также входят россыпи. Особенностью вещественного состава вольфрамовых руд является разнообразие минералов вольфрама (шеелит, вольфрамит, гюбнерит, тунгстит, молибдошеелит и др.).
В 2023 г. добычу вольфрамовых руд вели АО "Приморский ГОК", АО "Закаменск", ООО "Правоурмийское" и АО "Оловянная рудная компания"; отработку существенно вольфрамовых руд проводил только АО "Приморский ГОК" на месторождении Восток 2 в Приморском крае подземным способом. На остальных месторождениях, имеющих статус "разрабатываемые" - Спокойнинское в Забайкальском крае (ЗАО "Новоорловский ГОК"), Лермонтовское в Приморском крае (ООО "Лермонтовский ГОК") и Бом-Горхонское в Забайкальском крае (ООО "Забайкальский вольфрам") добыча из недр не велась. В Республике Бурятия АО "Закаменск" вело добычу рудных песков Барун-Нарынского техногенного месторождения и россыпи руч. Инкур, где вольфрам также является основным полезным компонентом [45].
В качестве попутного компонента вольфрам добывался и извлекался в товарный концентрат на оловорудных месторождениях Правоурмийское (ООО "Правоурмийское") и Фестивальное (АО "Оловянная рудная компания") в Хабаровском крае (обе компании контролирует ПАО "Русолово" - оловодобывающий дивизион ПАО "Селигдар").
По расчетам Минприроды, к 2030 году все проектные мощности по добыче вольфрама в России заработают, а объем производства составит 18 тыс. тонн оксида вольфрама. Такие объемы позволят не только обеспечить потребности отечественной экономики, но и нарастить поставки на мировые рынки.
Мировые поставки вольфрама в основном обеспечивались за счет производства и экспорта Китая.
Производство вольфрамового концентрата за пределами Китая, по оценкам, увеличилось в 2024 году, но осталось на уровне около 20% от общего мирового производства. Отчасти это произошло благодаря запуску двух новых предприятий в Австралии. Проект в Республике Корея приближался к стадии производства; дополнительные проекты за пределами Китая ожидали финансирования для дальнейшего развития.
Лом продолжал оставаться важным источником сырья для вольфрамовой промышленности. На потребление вольфрама сильно влияют экономические условия и промышленная активность. Китай продолжал оставаться ведущим мировым потребителем вольфрама.
В 2024 г. мировое производство вольфрама составило 81 тыс. т, из них Китай произвел 67 тыс. т, Россия - 2 тыс. т. Мировые запасы вольфрама оценивается более 4,6 млн. тонн [43], ресурсы превышают 22 млн. т [44]. Мировые поставки вольфрама были обусловлены преимущественно экспортом из Китая. Производство вольфрамового концентрата за пределами Китая, по оценкам, увеличилось в 2024 году благодаря добавлению двух новых предприятий в Австралии. Металлолом продолжает оставаться важным источником сырья для вольфрамовой промышленности [43].
1.3.4.7 Молибден. Молибден входит в перечень основных видов стратегического минерального сырья, Российская Федерация располагает значительной сырьевой базой молибдена: запасы металла, учитываемые Государственным балансом запасов, превышают 2,1 млн т. Прогнозные ресурсы категории P1 составляют 294,7 тыс. т, категории P2 - 870,9 тыс. т, категории P3 - 2475 тыс. т [45].
В число крупных продуцентов металла Россия не входит, обеспечивая лишь около 1% мирового производства. Наиболее развита его добыча в КНР, Чили, США и Перу, на долю которых приходится 88% производства металла в мире.
По состоянию на 01.01.2024 балансовые запасы молибдена, заключенные в рудах 30 коренных месторождений, составили 2 201,7 тыс. т; еще на пяти месторождениях учтены только забалансовые запасы. Забалансовые запасы в целом по стране составили 881,2 тыс. т. [45]. Российская сырьевая база молибдена отличается высокой степенью концентрации: более 70% запасов металла заключено в месторождениях, локализованных на юге Сибири, прежде всего - в Забайкальском крае, а также в республиках Хакасия и Бурятия. Основу сырьевой базы молибдена России составляют месторождения собственно молибденовых руд.
На юге Забайкальского края, в пределах Монголо-Охотской металлогенической провинции расположено уникальное по масштабу запасов Бугдаинское месторождение штокверкового (молибден-порфирового) типа, заключающее почти 600 тыс. т молибдена или 28% запасов страны. Руды его характеризуются рядовым качеством (0,08% Mo) и, помимо молибдена, содержат золото, серебро и свинец. Месторождение имеет некоторые перспективы прироста запасов - прогнозные ресурсы категории P1 на одном из его участков оценены в 10 тыс. т.
На севере края находится среднее по масштабу Жирекенское месторождение того же типа, но с богатыми рудами (0,105% Mo). Месторождение приурочено к Байкало-Витимской металлогенической провинции, на продолжении которой, в недрах Республики Бурятия разведаны еще три объекта штокверкового собственно молибденового типа: крупные Орекитканское и Мало-Ойногорское, а также среднее Жарчихинское. Качество руд Орекитканского и Жарчихинского месторождений сравнительно высокое, в среднем 0,099% и 0,086% Mo соответственно. Руды Мало-Ойногорского месторождения значительно беднее (0,051% Mo), но в качестве попутного компонента содержат вольфрам. Прогнозные ресурсы, локализованные в пределах республики, относятся к наименее достоверной категории P3.
В Республике Хакасия, в пределах Алтае-Саянской металлогенической провинции, расположены штокверковые месторождения Сорское и Агаскырское, суммарно заключающие 12% запасов молибдена страны, с рудами среднего качества (0,06% и 0,05% Mo соответственно). В республике также разведано Ипчульское место рождение штокверковых собственно молибденовых руд сопоставимого качества (0,061% Mo), запасы которого в количестве 144,5 тыс. т отнесены к забалансовым.
Алтае-Саянская провинция обладает значительными перспективами наращивания сырьевой базы молибдена: на территории Красноярского края в ее пределах расположено Джетское рудопроявление с прогнозными ресурсами P1, оцененными в 150,9 тыс. т молибдена.
В Курганской области разведано новое Коклановское штокверковое собственно молибденовое месторождение, запасы которого превышают 155 тыс. т при среднем содержании молибдена в рудах 0,082%; подсчитаны также запасы попутного вольфрама. Возможности прироста запасов металла в регионе не определены.
В Республике Тыва разведано молибден-медно-порфировое Ак-Сугское месторождение, заключающее 78 тыс. т металла со средним содержанием в руде 0,015% Mo. Запасы молибдена категории P1 в количестве 150,9 тыс. т, локализованы на Джетском штокверковом рудопроявлении в Красноярском крае.
В Свердловской области, в пределах Уральской металлогенической провинции, расположено среднемасштабное Южно-Шамейское месторождение штокверковых руд среднего качества (0,07% Mo). Запасы объекта составляют немногим более 60 тыс. т молибдена, однако на его флангах локализованы прогнозные ресурсы P1 в количестве 40 тыс. т, а в расположенном неподалеку рудопроявлении Партизанское - еще 20 тыс. т.
В Республике Карелия (Карело-Кольская металлогеническая провинция) разведано штокверковое месторождение Лобаш, заключающее около 6% запасов молибдена страны (128,6 тыс. т). Месторождение характеризуется средним качеством руд (0,069% Mo). В республике локализованы прогнозные ресурсы только категории P3.
На территории Кабардино-Балкарской Республики (Северо-Кавказская металлогеническая провинция) находятся скарновые месторождения вольфрама с попутным молибденом: Тырныаузское (0,077% Mo) и Гитче-Тырныауз (0,065% Mo). Суммарные запасы молибдена в рудах двух объектов республики составляют всего 62,5 тыс. т. Прогнозные ресурсы молибдена в республике не оценены.
Незначительный прирост запасов A+B+C1 получен также на разрабатываемых месторождениях Михеевское в Челябинской области (584 т) и Сорское в Республике Хакасия (388 т).
В результате переоценки значительно сократились оставшиеся в недрах после отработки запасы Тырныаузского месторождения в Кабардино-Балкарской Республике: запасы категорий A+B+C1 уменьшились на 94,3 тыс. т (72,5%), составив 35,8 тыс. т, категории C2 - на 12,8 тыс. т (94%), до 0,8 тыс. т; при этом его забалансовые запасы увеличились в 200 раз, до 101,6 тыс. т.
В нераспределенном фонде недр по состоянию на 01.01.2024 оставалось 30,1% запасов молибдена, подавляющая часть которых сосредоточена в трех штокверковых месторождениях: Орекитканском (Республика Бурятия) и Лобаш (Республика Карелия) собственно молибденовых руд, Мало-Ойногорском (Республика Бурятия) вольфрам-молибденовых руд.
Добыча молибдена в 2023 г. велась на трех месторождениях: Сорском (ООО "Сорский ГОК", входит в структуру АО "УК "Союзметаллресурс" - непрофильного актива En+ Group), Михеевском (АО "Михеевский ГОК", структура АО "Русская медная компания") и Мало-Тулукуевском (ПАО "Приаргунское ПГХО")
Россия располагает достаточно мощной сырьевой базой молибдена. Однако из-за преобладания в ее составе месторождений собственно молибденовых руд она в условиях современного рынка мало востребована. Хотя доля запасов, находящихся в распределенном фонде недр, значительна, реальные перспективы вовлечения в эксплуатацию есть только у запасов попутного молибдена, заключенных в медно-порфировых объектах. Но на сегодняшний день их доля в структуре запасов невелика.
Отечественная сырьевая база молибдена сформирована месторождениями, сопоставимыми с зарубежными по качеству руд и масштабам оруденения, которые в большинстве своем находятся в районах с развитой инфраструктурой и в целом являются инвестиционно привлекательными. Однако перспективы их освоения напрямую зависят от ситуации на мировом рынке молибдена. Падение цен спровоцировало сворачивание работ по освоению собственно молибденовых месторождений и, частично, по производству металла. Осенью 2013 г. остановлена работа Жирекенского ГОКа, в период с конца 2014 г. по 2016 г. приостановлены либо прекращены работы по подготовке к эксплуатации всех осваиваемых отечественных собственно молибденовых месторождений: Бугдаинского, Орекитканского, Жарчихинского и Агаскырского.
В настоящее время выпускаемый в стране молибденовый концентрат в полном объеме перерабатывается в ферромолибден на единственном в стране производственном комплексе, объединяющем обогатительное и ферросплавное производство - Сорском ферросплавном заводе, далее СФМЗ в Республике Хакасия. Его конечная продукция до 2022 г. в основном поставлялась на экспорт, а в последующий период была перенаправлена на внутренний рынок. Кроме ООО "СФМЗ" ферромолибден выпускают еще несколько российских предприятий, работающих на импортном сырье. Крупнейшим из них является ООО "Молирен" (Московская обл.). Остальные потребители молибденовых концентратов вынуждены их импортировать, а также использовать вторичное сырье [45].
В 2024 г. выпуск молибденовой продукции в мире составил 260 тыс. т, в Китае - 110 тыс. т, в России - 1700 т. Мировые запасы молибдена составляют 15 млн т. Прогнозные ресурсы оцениваются в 20 млн т [43]. Рециклинг молибдена достигает 30%.
1.3.5.1 Магний - один из наиболее распространенных металлов в земной коре. Благодаря своим уникальным свойствам, таким как легкость, высокая прочность и хорошая коррозионная стойкость, магний широко используется в различных отраслях промышленности: авиационная, космическая и автомобильная промышленность, электроника, медицина, металлургия.
Мировое производство магния сосредоточено в нескольких странах, среди которых лидируют Китай, Турция, Бразилия, Россия, Австралия. По данным за 2023 год, объем мирового производства магния составляет: соединений - 21,2 млн тонн, металла - 0,94 млн тонн. Лидером по добыче и производству является Китай, который обеспечивает более 80% мирового объема [84].
Запасы доломита, серпентина и содержащих магний эвапоритовых минералов огромны. По оценкам, рассолы, содержащие магний, представляют собой ресурс в миллиарды тонн, а магний можно извлекать из морской воды вдоль побережий всего мира. Установленные мировые запасы магнезита и брусита составляют 13 миллиардов тонн и несколько миллионов тонн соответственно. Запасы доломита, форстерита, содержащих магний эвапоритовых минералов и содержащих магнезию рассолов, по оценкам, составляют миллиарды тонн.
В России магний производится преимущественно из двух видов сырья: карналлита и бишофита.
Верхнекамское (Пермский край) - крупнейшее в России месторождение карналлита (KCl·MgCl2·6H2O), разработку которого осуществляет компания "Уралкалий". Полученный карналлитовый концентрат перерабатываться в ОАО "Соликамский магниевый завод" и в ООО "АВИСМА" (дочернем хозяйственном обществе ПАО "Корпорация ВСМПО-АВИСМА") с получением металлического магния и его соединений.
Крупнейшие запасы бишофита (MgCl2·6H2O) в России находятся в Волгоградской области (Городищенское, Светлоярское и Наримановское месторождения). Добыча и переработка с получением хлористого магния ведется компаниями ООО "Волгоградский магниевый завод" и АО "Каустик".
Другими потенциальными источниками являются: серпентинит и доломит. Проект "Русский магний" предполагал переработку серпентинита из отвалов "Ураласбеста" (Свердловская область), но был приостановлен из-за финансовых трудностей. В Свердловской области есть значительные запасы доломита (около 80 млн тонн), который потенциально может использоваться для получения магния.
1.3.5.2 Кальций - один из наиболее распространенных металлов в земной коре. Ввиду уникальных свойств имеет очень широкое применение во многих отраслях (металлургия, машиностроение, строительство, химическая промышленность, сельское хозяйство и др.) В металлургии металлический кальций выступает важным восстановителем при получении редких металлов, как титан, цирконий, ванадий, гафний, рубидий и цезий, а также применяется для раскисления и десульфурации сталей и сплавов - очистки расплавов от кислорода, серы и азота. Металлический кальций высокой чистоты служит восстановителем при получении металлического урана из его соединений - прежде всего из тетрафторида урана.
Мировое производство металлического кальция оценивается экспертами в 40 - 45 тыс. тонн в год. Крупнейшим производителем является Китай, на долю которого приходится около 70 - 80% мирового выпуска. Оставшиеся объемы приходятся на Россию, США и другие страны.
АО "Чепецкий механический завод" (АО "ЧМЗ") - один из крупнейших мировых производителей кальция и единственный в России и Европе. Поэтапное расширение производственных мощностей позволило увеличить номенклатуру кальциевой продукции предприятия, усовершенствовать технологию, повысить безотходность и безопасность производства. Завод производит металлический кальций в виде слитков, кусков, стружки, крупки и гранул. На предприятии разработаны технологии получения сплавов кальция с магнием, алюминием и никелем. Освоено производство кальциевой инжекционной проволоки.
Характеризуя ситуацию в России с добычей из недр конкретных видов минерального сырья, следует отметить, что в 2023 г. по сравнению с уровнем 2022 г. выросла добыча циркония (+7,5%), вольфрама (+1,7%), производство титана в концентратах (+30,8%). В то же время сократилась добыча молибдена (-15,4%), производство вольфрама в концентратах (-17,1%), молибдена в концентратах (-10,6%), циркония в концентратах (-1,7%). Для решения стоящих перед Россией задач достижения технологического и минерально-сырьевого суверенитета требуется радикальное изменение объемов добычи и переработки целого ряда видов минерального сырья.
В 2022 г. в России определен перечень стратегических металлов, имеющих важное значение для экономики и обороноспособности страны. Также правительством Российской Федерации распоряжением от 16.04.2024 N 939-р утвержден Перечень критических видов сырья, в 3 группу которого (импортозависимые дефицитные виды) из редких металлов включены титан, молибден, вольфрам, литий, бериллий, редкоземельные металлы (иттрий, лантан, церий, празеодим, неодим, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий, лютеций), цирконий, ниобий, тантал и рений.
Работа по снижению импортных поставок минерального сырья в Россию ведется: выданы лицензии на право пользования недрами литиевых месторождений Колмозерское и Полмостундровское в Мурманской области и Тастыгское в Республике Тыва, редкометалльного Большетагнинского месторождения в Иркутской области, вольфрамовых месторождений Агылкинское в Республике Саха (Якутия), Рудный Лог и Иультин Гора в Чукотском АО, Гитче-Тырныауз в Кабардино-Балкарской Республике [45]. Разработка новых месторождений требует создания новых отечественных технологий получения концентратов и их переработки с получением востребованной продукции - нужны оснащенные лаборатории и грамотные специалисты - обогатители, аналитики, технологи.
РМ в значительных концентрациях присутствуют в техногенном и вторичном сырье, поэтому расширение масштабов их переработки позволит осуществлять рециклинг целого ряда редких стратегических металлов - рения, скандия, РЗЭ, тантала, лития и др. К такому сырью относятся красные шламы производства глинозема (с содержанием РЗЭ около 1%), фосфогипс (с содержанием суммы оксидов РЗЭ 0,35 - 0,65%), отходы производства магнитов и магниты из отработанной техники (содержащие 25 - 30% дефицитных РЗМ: неодима, самария, тербия и диспрозия), отработанные аккумуляторы (содержат 2 - 3% лития), скрап ренийсодержащих суперсплавов, отработанные катализаторы и многие другие.
Переработка скрапа также позволит заметно уменьшить отрицательное воздействие отходов на окружающую среду.
Организация редкометалльного импортозамещения имеет свою специфику и поэтому должна проводиться системно, с учетом мировых тенденций, возможностей и перспектив создания эффективных производств редких металлов полного технологического цикла (горная добыча - обогащение - химико-металлургические переделы - промышленное использование - рециклинг) с применением взвешенных мер государственной поддержки.
Раздел 2. Технологические, технические решения и системы менеджмента, используемые в настоящее время в рассматриваемой отрасли промышленности
Технологии получения всех редких металлов высокой чистоты включают три основные последовательные стадии: разложение рудных концентратов, получение чистых химических соединений (оксидов или солей), выделение металла из его соединения. В большинстве случаев металлургической переработке рудного сырья предшествует его обогащение.
На первой стадии из коллективного концентрата отделяют извлекаемый металл от сопутствующих примесей, концентрируя его в растворе, осадке или пыли пирометаллургическим способом (обжигом, сплавлением, дистилляцией) или выщелачиванием растворами кислот, гидроксидов щелочных металлов или солей.
На второй стадии выделяют и очищают химическое соединение гидрометаллургическими (осаждением из растворов, кристаллизацией, сорбцией, экстракцией и др.) или пирометаллургическими (дистилляцией или ректификацией) способами.
Третья стадия - цементация или электролиз - завершается получением чистых редких металлов (из водных растворов), восстановлением оксидов водородом, оксидом углерода или углеродом при повышенных температурах, а также их восстановлением металлотермическим способом или электролизом расплавленных солей.
Технологии получения соединений бериллия
Из черновых бериллиевых концентратов получают оксид и гидроксид бериллия, из которых затем получают фторид или хлорид бериллия - исходные соли для производства металлического бериллия.
В промышленной практике преимущественно применяют сульфатный способ переработки концентратов для получения оксида и гидроксида бериллия.
Сульфатный способ основан на переводе бериллия вместе с алюминием и железом в сернокислый раствор с оставлением основной массы диоксида кремния в нерастворимом остатке. Поскольку берилл медленно реагирует с концентрированной серной кислотой даже при температуре 200 - 250 °C, проводят подготовительные операции: сплавления концентрата с известью или термическое активирование берилла.
С известью концентрат плавят в электродуговых печах при температуре 1500 - 1600 °C. Ориентировочно протекающий процесс описывается реакциями:
Be3Al2(Si6O18) + 7CaO = 3CaBeSiO4 + CaOAl2O3 + 3CaSiO3 (2.1)
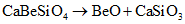 (2.2)
(2.2)Расплав гранулируют в воде, и гранулы измельчают. Образующиеся в результате плавки соединения хорошо разлагаются концентрированной серной кислотой.
При термическом активировании берилла концентрат плавят при температуре 1700 °C в дуговой печи с последующим быстрым охлаждением плава (закалкой) и грануляцией в холодной проточной воде. Преимущество термического активирования перед плавкой с известью - меньший расход серной кислоты, которую в этом случае не приходится расходовать на взаимодействие с соединениями кальция.
Сульфатизация и выщелачивание
Для перевода бериллия и других компонентов в сульфаты измельченный гранулированный материал обрабатывают концентрированной серной кислотой при температуре 150 - 200 °C в стальных реакторах. Затем полусухую массу выщелачивают водой при нагревании. В раствор переходят сульфаты бериллия, алюминия, железа, магния.
Из очищенного раствора выделяют гидроксид бериллия Be(OH)2 двумя способами:
1 Прямое осаждение гидроксида бериллия добавлением гидроксида натрия или пропусканием аммиака. При pH 7,5 и нагревании раствора до температуры 95 - 98 °C выделяются хорошо фильтруемые осадки гидроксида бериллия 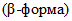 .
.
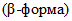 .
.2 Гидролитическое разложение бериллата натрия, полученного при добавлении в раствор сульфата избытка гидроксида натрия:
BeSO4 + 4NaOH = Na2BeO2 + Na2SO4 + 2H2O (2.3)
Na2BeO2 + 2H2O = Be(OH)2 + 2NaOH (2.4)
Полученный технический гидроксид бериллия служит исходным материалом для получения чистого оксида бериллия и его солей. Из него также получают прокаливанием при температуре 700 - 800 °C и технический оксид бериллия.
Для получения оксида бериллия высокой чистоты, применяемого в ядерной энергетике и производстве огнеупорных изделий, технический гидроксид очищают, используя различные способы.
Карбонатно-аммонийный способ очистки основан на растворении гидроксида бериллия в насыщенном растворе карбоната аммония, тогда как гидроксид алюминия и железа нерастворимы в нем.
Дополнительная очистка от следов тяжелых металлов достигается осаждением сульфидов. При кипячении раствора комплексный карбонат (NH4)2[Be(CO3)2] разлагается с выделением основного карбоната бериллия. Прокаливанием последнего получают оксид бериллия.
Эффективен ацетатный способ очистки, который заключается в возгонке оксиацетата бериллия Be4O(CH3COO)6 при температуре 360 - 400 °C. Иногда чистый оксид бериллия получают через кристаллогидрат сульфата бериллия BeSO4·4H2O, который кристаллизуют выпариванием из сульфатного раствора.
Металлургия бериллия
Для металлотермического восстановления бериллия используют его фторид, который обладает высокими температурами плавления (800 °C) и кипения (1327 °C). Это позволяет проводить восстановление при атмосферном давлении с подъемом температуры выше плавления бериллия (1284 °C), в результате чего легко отделить металл от расплава солей. В качестве восстановителя используют магний, не образующий с бериллием соединений и твердых растворов:
BeF2 + Mg = Be + MgF2 (2.5)
DG1000K = -118 кДж, H298K = -150 кДж.
Восстановление ведут в графитовых тиглях, нагреваемых в индукционных печах.
При охлаждении тигля бериллий затвердевает раньше шлака, что позволяет извлечь слиток бериллия из расплава солей щипцами.
Промышленный способ электролитического получения бериллия основан на использовании хлоридного электролита, содержащего хлориды в соотношении BeCl2:NaCl = 1:1 (по массе). Это соотношение близко к составу эвтектики (58,7% BeCl2 + 41,3% NaCl), плавящейся при 215 °C, что позволяет проводить электролиз при низкой температуре (350 °C).
Напряжение разложения хлорида бериллия в расплаве эвтектического состава при температуре 420 °C равно 2,08 В. Электролиз ведут в электролизерах из никеля. Анодом служит графитовый стержень, катодом - никелевые сменные перфорированные тигли (рисунок 2.1).
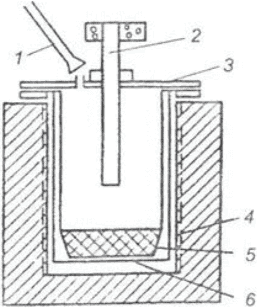
1 - труба для отсоса газов; 2 - графитовый анод; 3 - крышка;
4 - электропечь; 5 - сменный никелевый катод;
6 - ванная из никеля
для получения бериллия
Катод с осадком бериллия извлекают из ванны в горячем состоянии. После охлаждения катодный продукт для отделения электролита от металла промывают водой, раствором гидроксида натрия, разбавленного азотной кислотой, снова водой, центрифугируют и сушат.
Чешуйчатый бериллий прессуют в брикеты на гидравлическом прессе. Брикеты переплавляют в вакуумной печи в тиглях из оксида бериллия. Содержание примесей в электролитическом бериллии после вакуумной переплавки, %: Fe - 0,007; Al - 0,003; Si - 0,02 - 0,003; Ni - 0,003; Cl - 0,002; Ca - 0,003.
Литой бериллий обычно имеет крупнокристаллическую структуру, что в связи с большой анизотропией свойств кристаллов бериллия затрудняет его обработку давлением. Поэтому большую часть компактных бериллиевых заготовок и изделий получают методами порошковой металлургии.
Исходные порошки бериллия приготовляют измельчением бериллиевой стружки, полученной резанием на станке бериллиевых слитков вакуумной переплавки. Стружку измельчают в водоохлаждаемом дисковом истирателе, футерованном бериллием, в среде сухого инертного газа.
Прессование заготовок из порошка требует высокого давления - 1 - 1,5 ГПа, так как частицы бериллия малопластичны. Спекание проводят в вакууме при температуре 1200 °C, после чего дополнительно прессуют на холоде под давлением 1 - 1,5 ГПа. Цилиндрические заготовки прессуют при температуре 1120 - 1180 °C и давлении 3 - 7 МПа.
Технология получения лития
Термическое обогащение (декрипитацию) применяют при обогащении сподуменовых руд. Способ основан на переходе a-сподумена в 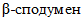 при нагревании руды до температуры 1000 - 1100 °C. Превращение сопровождается изменением объема, что приводит к разрушению вмещающей сподумен породы с выделением
при нагревании руды до температуры 1000 - 1100 °C. Превращение сопровождается изменением объема, что приводит к разрушению вмещающей сподумен породы с выделением 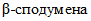 в виде измельченной фракции, отделяемой грохочением или воздушной сепарацией. Извлечение лития в концентрат составляет 60 - 80%. Также указанный способ применяют для обработки сподуменовых концентратов с целью перевода a-сподумена в реакционно активный
в виде измельченной фракции, отделяемой грохочением или воздушной сепарацией. Извлечение лития в концентрат составляет 60 - 80%. Также указанный способ применяют для обработки сподуменовых концентратов с целью перевода a-сподумена в реакционно активный 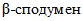 для последующего химического разложения концентратов.
для последующего химического разложения концентратов.
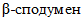 при нагревании руды до температуры 1000 - 1100 °C. Превращение сопровождается изменением объема, что приводит к разрушению вмещающей сподумен породы с выделением
при нагревании руды до температуры 1000 - 1100 °C. Превращение сопровождается изменением объема, что приводит к разрушению вмещающей сподумен породы с выделением 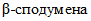 в виде измельченной фракции, отделяемой грохочением или воздушной сепарацией. Извлечение лития в концентрат составляет 60 - 80%. Также указанный способ применяют для обработки сподуменовых концентратов с целью перевода a-сподумена в реакционно активный
в виде измельченной фракции, отделяемой грохочением или воздушной сепарацией. Извлечение лития в концентрат составляет 60 - 80%. Также указанный способ применяют для обработки сподуменовых концентратов с целью перевода a-сподумена в реакционно активный 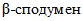 для последующего химического разложения концентратов.
для последующего химического разложения концентратов.Метод гравитационного обогащения литиевых руд в тяжелых средах (тяжелосредная сепарация) используется для разделения крупных классов литиевой руды, например, сподумена с относительно крупным размером кристаллов. Этот метод применяется в комбинированных схемах обогащения, сочетая гравитацию с другими методами (флотацией, магнитной сепарацией и др.)
Флотацию сподумена осуществляют с применением анионных собирателей (жирных кислот и их мыл) с выделением в пенный продукт литиевых минералов (прямая флотация) или с использованием катионных собирателей при выделении в пенный продукт минералов пустой породы, тогда как литиевые минералы остаются в хвостах (обратная флотация).
Для флотации лепидолита используют преимущественно обратную флотацию с катионными собирателями
Продуктами переработки литиевых концентратов являются соли лития (карбонат, сульфат, хлорид) и гидроксид. Наиболее распространенный конечный продукт - карбонат лития. Он служит исходным материалом для получения других соединений, в частности, хлорида лития, из которого получают металлический литий.
В промышленной практике применяют преимущественно три способа разложения литиевых концентратов: сернокислотный, сульфатный (спекание с K2SO4) и известковый. Кроме того, иногда используют известково-хлоридный способ.
Сернокислотный способ применяют для литиевых концентратов всех типов: сподуменовых, лепидолитовых и амблигонитовых. В результате разложения концентрированной серной кислотой при температуре 200 - 250 °C и последующего выщелачивания продукта водой получают растворы, содержащие сульфат лития, из которых осаждают карбонат лития.
Переработка сподумена. Для эффективного разложения сподумена серной кислотой необходима первоначальная термическая обработка. Серная кислота практически не разлагает 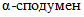 . Обжиг проводят в барабанной печи. Особенность взаимодействия серной кислоты с
. Обжиг проводят в барабанной печи. Особенность взаимодействия серной кислоты с 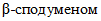 состоит в замещении катионов лития протонами кислоты при сохранении - структуры
состоит в замещении катионов лития протонами кислоты при сохранении - структуры 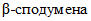 .
.
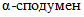 . Обжиг проводят в барабанной печи. Особенность взаимодействия серной кислоты с
. Обжиг проводят в барабанной печи. Особенность взаимодействия серной кислоты с 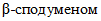 состоит в замещении катионов лития протонами кислоты при сохранении - структуры
состоит в замещении катионов лития протонами кислоты при сохранении - структуры 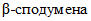 .
.Сульфатизированный материал выщелачивают водой, подавая в реактор мел для нейтрализации избытка серной кислоты (до pH 6 - 6,5). Отфильтрованный раствор очищают от магния нейтрализацией известью (pH 12 - 14), а затем от кальция осаждением карбоната кальция CaCO3 содой.
После отделения осадка фильтрацией из раствора осаждают карбонат лития насыщенным раствором соды. Промытые осадки содержат 96 - 97% Li2CO3. Извлечение в карбонат лития из сподуменового концентрата 85 - 90%.
Переработку лепидолита осуществляют непосредственно серной кислотой при температуре 320 - 330 °C. Для ускорения процесса иногда применяют предварительное плавление лепидолита при температуре 1090 °C, превращая его в стеклообразную массу, которую после измельчения сульфатизируют.
Получаемые при переработке лепидолита сернокислые растворы содержат сульфаты: Li2SO4, K2SO4, Na2SO4, Al2(SO4)3. Из отфильтрованного раствора осаждают карбонат лития.
Сульфатный способ основан на спекании литиевых концентратов с сульфатом калия с последующим выщелачиванием спека водой:
Так как реакция (2.6) обратима, требуется большой избыток сульфата калия (до 150%) для обеспечения высокой степени превращения.
Спекание проводят в барабанных печах при температуре 1100 - 1150 °C в течение 1 - 2 ч. Выщелачивание ведут на холоде в барабанных мельницах (растворимость сульфата лития Li2SO4 понижается с повышением температуры).
Сульфатный способ применяют также для переработки лепидолита и циннвальдита. Различие состоит лишь в дозировке сульфата калия в шихте и более низкой температуре спекания (850 - 950 °C).
Преимущество сульфатного способа переработки литиевого сырья - его универсальность и высокая степень вскрытия концентратов, недостаток - высокий расход сульфата калия. При известковом способе литиевые концентраты (сподумен или лепидолит) спекают с известью или мелом. При последующем выщелачивании спека водой получают раствор, содержащий гидроксид лития, который кристаллизуется в результате выпаривания раствора в составе моногидрата LiOH·H2O.
Известковый способ применяют также при переработке лепидолитовых концентратов. В отличие от сподумена, спекание лепидолита с известью (или мелом) проводят при более низкой температуре (900 - 950 °C).
Преимущества известкового способа - применимость к любым типам литиевых концентратов, возможность прямого получения гидроксида лития.
В последние годы интенсивно разрабатываются способы получения литиевых солей из нетрадиционных видов сырья. Литий производится из природных рассолов в США и Чили. В Чили на базе подземных рассолов месторождения в пустыне Атакама построен комбинат. Состав различных рассолов литийгидроминерального сырья (ЛГМС) приведен в табл. 2.1.
Таблица 2.1
N п/п | Страна (месторождение) | Концентрация, г/л | ||||||
Li+ | Na+ | K+ | Mg2+ | Ca2+ | Cl-I | SO42- | ||
1 | США, Невада (оз. Силвер-Пик) | 0,44 | 88,0 | 11,0 | 0,7 | 0,6 | 128,5 | Нет данных |
2 | Чили (Атакама) | 0,5 - 0,2 | 113,4 | 32,1 | 11,4 | 0,5 | 210,6 | 17,2 |
3 | Боливия (Де-Уюни) | 0,8 - 2,0 | 105,2 | 24,2 | 16,6 | 0,5 | 190,5 | 9,1 |
4 | Россия (Тарумовское) | 0,2 | 67,0 | 3,8 | 0,8 | 10,1 | 127,3 | Нет данных |
5 | Китай, Цинхай (Дунтай) | 0,49 | 68,6 | 17,7 | 29,3 | - | 190,4 | 23,1 |
6 | Китай, Цинхай (Илипин) | 0,96 | 1,4 | 1,1 | 107,8 | 4,3 | 326,0 | 0,1 |
7 | Россия, Республика Саха (Удачнинский комплекс) | 0,41 n | 35,6 | 20,3 | 11,2 | 65,5 | 220 | - |
8 | Россия, Красноярский край (Сухотунгусское) | 0,22 | 46,8 | 23,1 | 9,5 | 58,8 | 233,9 | - |
9 | Россия, Эвенкия (Верхнекостинское) | 0,45 | 50,2 | 19,7 | 11,2 | 81,7 | 271,8 | - |
10 | Россия, Иркутская область (Знаменское) | 0,48 | 2,4 | 4,3 | 28,5 | 134,3 | 322,5 | - |
11 | Россия, Иркутская область (Ковыктинское) | 0,39 | 1,9 | 11,7 | 29,0 | 154,0 | 338,9 | - |
При стадийном солнечном упаривании происходит последовательное осаждение галита, сильвинита, а также двойной соли Li2SO4·K2SO4. Полученный таким образом литиевый концентрат транспортируется по железной дороге на завод, где рассол очищают от магния известковым молоком, от кальция содой и далее также содой осаждают из него в стандартных условиях карбонат лития. Осадок промывают, сушат и гранулируют. Для выделения лития меньшую часть рассола, полученного после первой стадии испарения и отделения сильвинита (15% от потока лития), направляют на вторую стадию испарения, а большую часть этого рассола (85% от потока лития) закачивают обратно в пласт.
На второй стадии испарения при температуре рассола выше 18 °C в процессе его концентрирования литий испаряется в испарительных картах вместе с оставшимся калием в виде двойной соли Li2SO4·K2SO4, которую отделяют от рассола и перевозят на литиевые заводы. Из рассола на второй стадии испарения может быть выделено в виде двойной соли только 50% лития от его общего содержания. Степень извлечения лития повышают до 70%, используя рассол, прошедший вторую стадию концентрирования и выпадения двойной соли.
Двойную литиевую соль, осажденную при температуре 25 °C и концентрации лития в рассоле не менее 10%, затем растворяют в насыщенном растворе хлорида калия, высаливая K2SO4, который является ликвидным товарным продуктом:
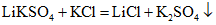 (2.7)
(2.7)Маточный раствор после осаждения K2SO4, представляющий собой практически насыщенный раствор хлорида лития, направляют на осаждение карбоната лития содой по реакции:
2LiCl + Na2CO3 = Li2CO3 (2.8)
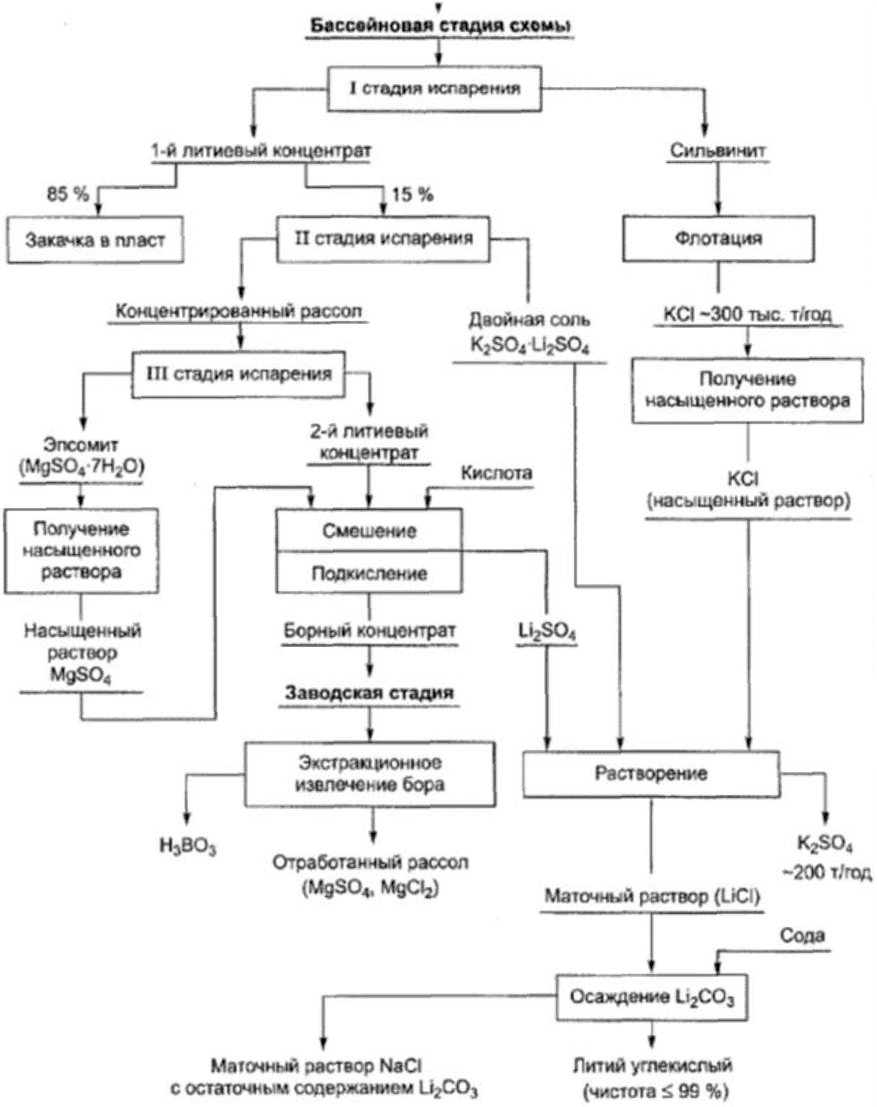
Рисунок 2.2 - Схема переработки литиевых рассолов
Технология AXIONIT DLE промышленного производства соединений лития (карбонат лития, гидроксид лития, хлорид лития) из природных и технологических рассолов включает очистку рассолов от органики, сорбцию лития литийселективным сорбентом, десорбцию лития водой, концентрирование литийсодержащих элюатов, очистку литиевых концентратов от примесей и получение гидроксида лития путем электролиза литиевого концентрата или осаждение карбоната лития из литиевого концентрата. Технология позволяет извлекать до 90% лития из природных и технологических рассолов с получением соединений лития (карбонат лития, гидроксид лития, хлорид лития) высокого качества с долей основного вещества от 99.5% до 99.8%.
Технологическая схема производства в общем виде приведена на рисунке 2.3.
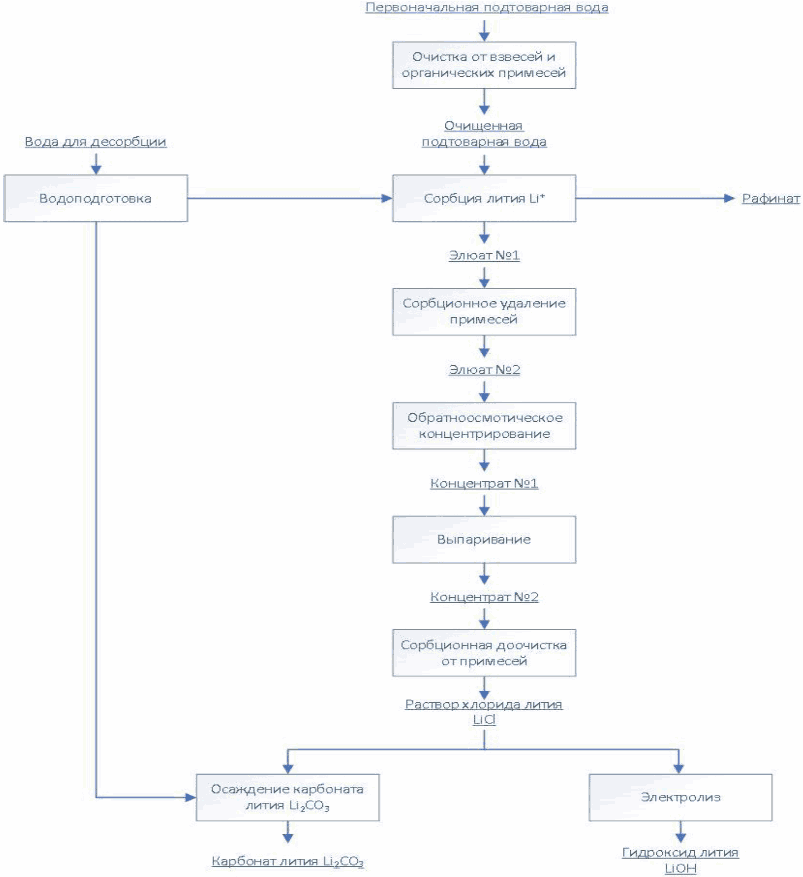
Безводный хлорид лития, служащий исходным материалом для производства металлического лития, обычно получают из карбоната лития. По техническим условиям в хлориде лития допускается следующее содержание примесей, %, не более: Na - 0,12; Ca - 0,03; Al - 0,05; Fe - 0,005; SO2- - 0,1; SiO- - 0,05; PO- - 0,005.
Для получения хлорида лития указанной чистоты обычно требуется предварительная очистка карбоната лития от примесей. Очистку осуществляют методом перекристаллизации через хорошо растворимый бикарбонат лития (способ Труста).
Электролиз хлорида лития - наиболее экономичный способ производства металла технической чистоты. Его проводят в диафрагменных или бездиафрагменных электролизерах особой конструкции (рисунок 2.4).
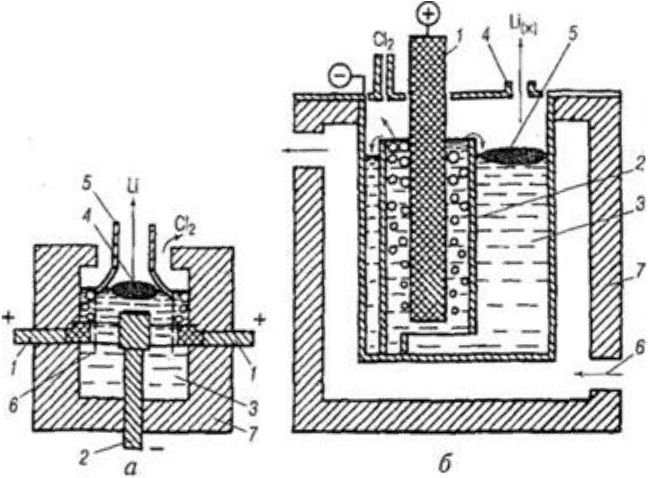
а - диафрагменный электролизер:
1 - кольцевой графитовый анод; 2 - стальной катод;
3 - расплав С-КС; 4 - жидкий литий; 5 - сборник;
6 - стальная сетчатая диафрагма; 7 - теплоизоляция;
б - бездиафрагменный электролизер:
1 - графитовый анод; 2 - стальной трубчатый катод;
3 - расплав С-КС; 4 - люк для выборки лития; 5 - литий;
6 - топочные газы; 7 - теплоизоляция
из расплава LiCl
В диафрагменном электролизере (рис. 2.4а) стальной катод введен в днище в центре ванны. На уровне верхнего торца катода расположен кольцевой угольный анод с боковым токоподводом через стенки электролизера. В межэлектродном пространстве установлена сетчатая стальная диафрагма. Исходный хлорид лития погружается заливкой расплава через люк в крышке. Литий при электролизе всплывает на поверхность электролита и удаляется из ванны вручную дырчатой ложкой. Большое поверхностное натяжение лития и плохая смачиваемость сетки удерживают металл в съемной ложке, а электролит легко стекает обратно в ванну через отверстия в сетке.
Рабочей ванной в бездиафрагменном электролизере является катодно-поляризованный стальной тигель, в котором электролит расплавляется за счет теплоты топочных газов (газовая горелка). Графитовый анод вводится сверху. Получаемый при электролизе технический литий содержит 97 - 98% Li.
Для получения металла, пригодного для ядерной технологии, чистота лития повышается его рафинированием.
Эффективен метод рафинирования лития дистилляцией в вакууме. Сначала при температуре 450 °C отгоняют основное количество примесей щелочных металлов (калия, натрия). Затем для более полной очистки литий испаряют при температуре 600 - 800 °C под давлением 1,3·10-3 Па, поддерживая температуру в конденсаторе 340 - 420 °C. При извлечении лития в конденсат, равном 85 - 90%, содержание примесей в нем снижается до тысячных долей процента.
Литий выпускают в виде слитков, гранул, прутков, проволоки. Хранят его в герметичной железной таре под слоем пастообразной массы из парафина и минерального масла либо под газолином или петролейным эфиром, заполняющим тару доверху. Перед применением лития минеральное масло смывают петролейным эфиром или бензолом, который затем испаряют в вакууме.
Технология получения рубидия
Большую часть добываемого рубидия получают как побочный продукт при производстве лития из лепидолита. После выделения лития в виде карбоната или гидроксида рубидий осаждают из маточных растворов в виде смеси алюморубидиевых, алюмокалиевых и алюмоцезиевых квасцов RbAl(SO4)2·12H2O, KAl(SO4)2·12H2O, CsAl(SO4)2·12H2O. Смесь разделяют многократной перекристаллизацией.
Рубидий также выделяют и из отработанного электролита, получающегося при получении магния из карналлита. Из него рубидий выделяют сорбцией на осадках ферроцианидов железа или никеля. Затем ферроцианиды прокаливают и получают карбонат рубидия с примесями калия и цезия. При получении цезия из поллуцита рубидий извлекают из маточных растворов после осаждения Cs3[Sb2Cl9]. Можно извлекать рубидий и из технологических растворов, образующихся при получении глинозема из нефелина.
Для извлечения рубидия используют методы экстракции и ионообменной хроматографии. Соединения рубидия высокой чистоты получают с использованием полигалогенидов.
Значительную часть производимого рубидия выделяют в ходе получения лития, поэтому появление большого интереса к литию для использования его в термоядерных процессах в 1950-х привело к увеличению добычи лития, а, следовательно, и рубидия. Именно поэтому соединения рубидия стали более доступными.
Технология получения цезия
При промышленном получении цезий в виде соединений извлекается из минерала поллуцита. Это делается хлоридным или сульфатным вскрытием. Хлоридное вскрытие включает обработку исходного минерала подогретой соляной кислотой, добавление хлорида сурьмы SbCl3 для осаждения соединения Cs3[Sb2Cl9] и промывку горячей водой или раствором аммиака с образованием хлорида цезия CsCl. При сульфатном вскрытии минерал обрабатывается подогретой серной кислотой с образованием алюмоцезиевых квасцов CsAl(SO4)2 12H2O.
Для получения цезия достаточной степени чистоты требуется многократная ректификация в вакууме, очистка от механических примесей на металлокерамических фильтрах, нагревание с геттерами для удаления следов водорода, азота, кислорода и многократная ступенчатая кристаллизация.
Сложности получения цезия обусловливают постоянный поиск его минералов: извлечение этого металла из руд неполное, в процессе эксплуатации материала он рассеивается и потому безвозвратно теряется. Промышленность нуждается именно в очень чистом материале (на уровне 99,9 - 99,999%), и это является одной из труднейших задач в металлургии редких элементов.
В России переработка и извлечение солей цезия из поллуцита ведется в Новосибирске на ЗАО "Завод редких металлов".
Существует несколько лабораторных методов получения цезия [12]. Он может быть получен:
- нагревом в вакууме смеси хромата или дихромата цезия с цирконием;
- разложением азида цезия в вакууме;
- нагревом смеси хлорида цезия и специально подготовленного кальция.
Все методы являются трудоемкими. Второй позволяет получить высокочистый металл, однако является взрывоопасным и требует на реализацию несколько суток.
Технология получения рения
При переработке молибденитовых концентратов, кроме сернокислых растворов мокрых систем пылеулавливания, источниками получения рения могут служить растворы после гидрометаллургической переработки огарков и азотно-сернокислые растворы от разложения молибденита азотной кислотой.
Переработка медно-молибденовых ренийсодержащих промпродуктов в настоящее время осуществляется по схеме окислительного обжига с возгонкой рения, содового выщелачивания обожженного продукта с последующим выделением из растворов молибдата кальция. Возогнанный рений улавливается в мокрой системе очистки газов и затем извлекается по сорбционной схеме в товарный перренат аммония. Окислительно-автоклавное выщелачивание растворами соды и едкого натра обеспечивает извлечение в раствор молибдена и рения до 98%. Экстракционные методы извлечения молибдена и рения с последующим получением парамолибдата и перрената аммония обеспечивают извлечение из исходного сырья 96% молибдена и около 90% рения.
Для выбора способа переработки вовлекаемого в производство сырья необходимо учитывать качество исходного материала, наличие примесей, лимитирующих выбор конечной продукции, а также имеющиеся производственные мощности.
Основными способами переработки ренийсодержащих производственных растворов в настоящее время являются сорбция на высокоосновных анионитах (ионообменных смолах) и жидкостная экстракция.
Газообразные продукты, получающиеся при обжиге молибденитовых концентратов или при плавках медных концентратов, охлаждают, фильтруют и растворяют в серной кислоте с последующим выделением перренатов калия или аммония (KReO4 или NH4ReO4) ионообменной сорбцией на активированном угле или ионообменных углях, а также жидкостной экстракцией три-бутилфосфатом или аминами.
Металлургия рения
Дальнейшая переработка перренатов калия и аммония направлена на получение порошкообразного и компактного рения.
Для получения рениевого порошка перренат аммония (или калия) восстанавливают водородом в трубчатых печах с использованием лодочек из молибдена.
Полученный водородным восстановлением перрената калия порошкообразный рений содержит ряд легколетучих примесей, которые не позволяют применять его в жаропрочных сплавах и в электронных приборах, работающих в глубоком вакууме. Особенно вредны примеси свинца, олова, кадмия, висмута и сурьмы. Содержание их в металлическом рении не должно превышать 1*10-4% каждой.
Достаточно полно указанные примеси могут быть удалены вакуумной дистилляцией при нагревании рения до высоких температур при остаточном давлении 1*10-4 мм рт. ст. В этих условиях при 2000 °C наблюдается заметное спекание порошкообразного материала, а при 2300 - 2500 °C происходит интенсивная очистка рения от большинства присутствующих в нем примесей. Чистота металла, за вычетом тринадцати примесей (Fe, Al, Mo, K, Na, Ca, Ni, Cu, Pb, Sn, Bi, Cd, Sb), составляет 99,988%. Больше всего в рении калия (0,0035 - 0,0030%) и кальция (0,0023 - 0,050%). Интенсивное удаление железа и никеля начинается при 2200 °C, а калия и кальция - выше 2300 °C. Содержание алюминия остается практически неизменным.
При исходном содержании в рении 0,003% Pb, 0,0006% Sn, 0,0007% Cd, 0,0003% Bi и 0,0004% Sb и после выдерживания металла в течение 2 часов при остаточном давлении 1*10-4 мм рт. ст. содержание этих примесей в металле снижается менее чем до 0,0001% каждой. Этого же эффекта можно достигнуть, если увеличить продолжительность нагрева до 4 - 6 ч при 2050 °C.
Снизить содержание кислорода в рении можно также с помощью небольших добавок редкоземельных металлов, особенно лантана, раскисляющих рений. Так, при введении в рений 0,01% (по массе) лантана содержание кислорода в раскисленном таким путем рении составит 0,008% (по массе) против 0,015% (по массе) в исходном литом рении, что позволит снизить твердость и повысить пластические свойства рения.
Глубокую очистку рения от примесей возможно также осуществить через его оксихлориды. Наиболее удобно для этой цели применить монооксихлорид ReOCl4, который плавится при 30 °C и кипит при 228 °C. Это соединение легко очищается ректификацией. Вначале технический рений подвергают хлорированию газообразным хлором, получая пентахлорид рения ReCl5; далее пентахлорид окислением кислородом при 160 - 180 °C превращают в монооксихлорид, который и очищают ректификацией. Наконец, чистый ReOCl4 переводят в перренат аммония, который затем восстанавливают до металла.
Спеченный порошок рения может быть подвергнут процессу рафинирования переплавкой в вакуумных электронно-лучевых печах.
Полученный металл характеризуется высокой чистотой.
Технология получения галлия
Основным источником получения галлия служат растворы глиноземного производства при переработке боксита (обычно содержащие незначительные его примеси (до 0,1%)) и нефелина. Галлий также можно получить с помощью переработки полиметаллических руд и зол от сжигания угля. Значительно  его количества (до 1,5%) были обнаружены в золе некоторых каменных углей. Извлекается он электролизом щелочных растворов, являющихся промежуточным продуктом переработки природных бокситов на технический глинозем. Концентрация галлия в щелочном алюминатном растворе после разложения в процессе Байера: 100 - 150 мг/л, по способу спекания: 50 - 65 мг/л. По этим способам галлий отделяют от большей части алюминия карбонизацией, концентрируя в последней фракции осадка. Затем обогащенный осадок обрабатывают известью, галлий переходит в раствор, откуда черновой металл выделяется электролизом.
его количества (до 1,5%) были обнаружены в золе некоторых каменных углей. Извлекается он электролизом щелочных растворов, являющихся промежуточным продуктом переработки природных бокситов на технический глинозем. Концентрация галлия в щелочном алюминатном растворе после разложения в процессе Байера: 100 - 150 мг/л, по способу спекания: 50 - 65 мг/л. По этим способам галлий отделяют от большей части алюминия карбонизацией, концентрируя в последней фракции осадка. Затем обогащенный осадок обрабатывают известью, галлий переходит в раствор, откуда черновой металл выделяется электролизом.
 его количества (до 1,5%) были обнаружены в золе некоторых каменных углей. Извлекается он электролизом щелочных растворов, являющихся промежуточным продуктом переработки природных бокситов на технический глинозем. Концентрация галлия в щелочном алюминатном растворе после разложения в процессе Байера: 100 - 150 мг/л, по способу спекания: 50 - 65 мг/л. По этим способам галлий отделяют от большей части алюминия карбонизацией, концентрируя в последней фракции осадка. Затем обогащенный осадок обрабатывают известью, галлий переходит в раствор, откуда черновой металл выделяется электролизом.
его количества (до 1,5%) были обнаружены в золе некоторых каменных углей. Извлекается он электролизом щелочных растворов, являющихся промежуточным продуктом переработки природных бокситов на технический глинозем. Концентрация галлия в щелочном алюминатном растворе после разложения в процессе Байера: 100 - 150 мг/л, по способу спекания: 50 - 65 мг/л. По этим способам галлий отделяют от большей части алюминия карбонизацией, концентрируя в последней фракции осадка. Затем обогащенный осадок обрабатывают известью, галлий переходит в раствор, откуда черновой металл выделяется электролизом.Загрязненный галлий промывают водой, после этого фильтруют через пористые пластины и нагревают в вакууме для того, чтобы удалить летучие примеси. Для получения галлия высокой чистоты используют процессы перекристаллизации из водных растворов солей галлия, с последующим электролизом, электролитическое рафинирование, методы очистки направленной кристаллизацией и вакуумной дистилляции, доводя содержание основного вещества до уровня 99,9999%.
Вторым источником получения галлия являются сульфатные растворы цинкового производства, получаемые от выщелачивания вельц-оксидов. При извлечении цинка из сфалеритовых концентратов пирометаллургическим способом галлий практически полностью остается в огарке. В процессе выщелачивания полученного огарка отработанным цинковым электролитом галлий из растворов переходит в осадок вместе с железом и другими примесями в виде цинкового кека. Переработка кеков методом вельцевания позволяет концентрировать часть галлия в возгонах ("вельц-окислах"), при переработке которых образуются растворы с содержанием галлия до 50 мг/л пригодные для экстракционного извлечения фосфорорганическими кислотами в разбавителях и/или сорбционного метода четвертичными аминами. В результате реэкстракции или десорбции получают реэкстрагенты и элюаты, которые направляют на извлечение галлия электролизом или цементацией на галламе.
Металлургия галлия
Около 97% мирового производства галлия идет на синтез различных полупроводниковых соединений. Галлий имеет ряд сплавов жидких при комнатной температуре (так называемых галлам) с температурами плавления вплоть до минус 19 °C. По отношению к алюминию и его сплавам галлий понизитель прочности. Галлий и его эвтектический сплав с индием используются как теплоноситель в контурах ядерных реакторов.
Металлическим галлием заполняют кварцевые термометры (вместо ртути) для измерения высоких температур.
Технология получения индия
Индий не имеет собственных месторождений и способ отработки месторождений различных технологических типов руд, содержащих индий, определяется по основному металлу (меди, цинку, свинцу, олову и т.д.) и не зависит от содержания в них индия (как и прочих попутных металлов).
В промышленном производстве индия можно выделить три основные стадии:
- получение индиевого концентрата с содержанием индия не менее 1 - 2%;
- получение чернового индия;
- рафинирование чернового индия.
Цинковые концентраты - основной источник индия в мировой практике и единственный в настоящее время для России.
При переработке цинковых концентратов образуются цинковые кеки. В мировой практике распространены три основных метода их переработки с целью извлечения находящихся в них ценных компонентов. Это вельц-процесс или вельцевание - разрушение ферритов цинка углеродистыми восстановителями C и CO; разложение ферритов сернистым ангидридом или концентрированной серной кислотой (сульфатизация) и непосредственное растворение кеков в серной кислоте при повышенной температуре и кислотности (методы автоклавные: ярозит-процесс и гетит-процесс).
В России используется вельцевание (возгонка из твердой шихты) цинковых кеков. При переработке цинковых кеков в вельц-печах индий в основном концентрируется в вельц-возгонах. Переход индия в возгоны объясняется увлечением его в газовую фазу парами возгоняющегося цинка с последующей конденсацией. Выщелачивание вельц-возгонов проводят в несколько стадий: нейтральное выщелачивание для извлечения цинка, выщелачивание гидратно-свинцового кека с получением индийсодержащего раствора; высокотемпературное довыщелачивание свинцового кека проводится для доизвлечения цинка и индия из упорных соединений. Раствор после выщелачивания свинцового кека направляют на стадию выщелачивания гидратно-свинцового кека. Раствор, содержащий индий обрабатывают для перевода железа в двухвалентную форму медным кеком или железным порошком. Подготовленный раствор с содержанием индия до 300 мг/л направляется для экстракционного извлечения фосфорорганическими кислотами в разбавителях в присутствии 2-этилгексилового спирта. Реэкстракция проводится раствором серной кислоты с концентрацией 400 г/л с добавлением хлорид-ионов. Реэкстракты с содержанием индия 25 - 45 г/л проходят очистку сероводородом от мышьяка и сурьмы.
Для выделения индия из предварительно очищенных растворов и получения чернового индия используется метод цементации из сульфатных растворов на цинковых или алюминиевых листах, их хлоридных растворов - цинковой пылью.
Конечной товарной продукцией является металлический индий. Индий поставляется в соответствии с марками ИН-00, ИН-0, ИН-1, ИН-2. Содержание индия в двух первых марках не менее 99,999% и 99,998%, а десяти контролируемых примесей по 0,0001 - 0,00001% каждой. Особо чистый индий (более 99,9999%) содержит примесей на порядок меньше, чем в обычных марках этого металла.
Для отделения индия от сопутствующих металлов и концентрирования растворов используют экстракцию, например, раствором ди-2-этилгексилфосфорной кислоты в керосине, или ионный обмен, например, на фосфорнокислых катионитах. Выделяют индий из растворов электролизом либо цементацией на металлическом Al (т.е. вытеснением индия из раствора по реакции: In3+ + Al0 = In0 + Al3+) с последующей переплавкой под слоем щелочи. Для очистки индия используют чаще всего электролитическое рафинирование, вакуумную обработку для удаления летучих примесей, зонную плавку или вытягивание кристаллов из расплава. Предложен также ряд методов очистки индия с промежуточным образованием его соединений, в частности, хлоридов.
Вельцевание является наиболее эффективным методом переработки индийсодержащих продуктов, в том числе цинковых кеков.
В АО "ЧЦЗ" на основании изучения влияния на извлечение индия, оксида и хлорида кальция разработан способ подачи хлорсодержащих материалов и флюсующих добавок через разгрузочное отверстие вельц-печей. Технология внедрена на крупногабаритной вельц-печи (L = 60 м, D = 4,0 м). Внедрение позволило увеличить извлечение индия в вельц-окись на 10%.
Другим направлением совершенствования производства индия явилась модернизация экстракционной установки, которая позволила:
- стабилизировать процесс экстракции индия с высоким содержанием кремнезема из сернокислых растворов, получающихся при выщелачивании вельц-окиси;
- снизить расходы на приготовление аппаратов в 10 раз;
- упростить обслуживание и ремонт экстракционной установки.
Технология получения таллия
В настоящее время источником получения таллия являются сульфидные руды. При обогащении таких руд таллий переходит в медные, цинковые и особенно свинцовые концентраты. Таллий изоморфно входит в состав, как сульфидных руд, так и силикатных минералов, поэтому степень извлечения таллия в концентраты колеблется от 10% до 80%. Содержание таллия в обогащенных продуктах составляет около 10-3%, поэтому такие концентраты не могут служить непосредственным сырьем для промышленного получения таллия. Источником таллия являются отходы медного, цинкового, свинцового и сернокислотного производства - колошниковая пыль, образующаяся при обжиге сульфидных руд, и шлаки, собираемые при выплавке металлов.
В связи с тем, что таллий из перерабатываемых продуктов извлекается обычно в комплексе с рядом других элементов, действующие схемы комплексной переработки металлических руд включают в себя большое количество пиро- и гидрометаллургических операций, являются достаточно сложными и постоянно видоизменяются на предприятиях в зависимости от изменения состава перерабатываемого сырья.
Для получения богатых таллием концентратов пользуются методом возгонки. Таллий может улетучиваться при обжиге как в окислительной, так и в восстановительной атмосфере. Это дает возможность сочетать получение обогащенных таллием возгонов с процессами извлечения других ценных элементов. Особенно высокое обогащение таллием получается при применении хлорирующего обжига - с добавкой хлористого натрия или сильвинита. Равновесие обменной реакции 2NaCl + Tl2SO4 = 2TlCl + Na2SO4 сдвинуто в сторону образования хлорида таллия, который при температуре свыше 600 °C обладает хорошей летучестью и почти полностью возгоняется. При окислительном обжиге концентратов, кроме хлорида, возгоняется оксид таллия Tl2O и механически захватывается потоком газа пылевидные частицы сульфата, сульфида и силиката таллия. В пыли и возгонах, получаемых при восстановительных процессах, часть таллия может находиться в виде металла.
Следующей стадией выделения таллия является цикличное выщелачивание возгонов водой, которое нужно проводить при нагревании, так как растворимость таллия сильно зависит от температуры. Иногда вместо водного выщелачивания применяют выщелачивание слабыми содовыми растворами. Это предотвращает переход в раствор хлоридов других металлов, например, кадмия. Если основная часть таллия присутствует в виде труднорастворимых соединений, то применяется выщелачивание разбавленной серной кислотой.
Из водных растворов от выщелачивания таллий по разным технологическим схемам выделяют в виде хлорида, сульфида, иодида, хромата, гидроксида трехвалентного таллия или в виде металлического таллия цементацией - осаждением цинковой пылью или амальгамой.
При осаждении таллия в виде сульфида (горячим раствором сульфида натрия) достигается полное извлечение металла из раствора, но этот способ осаждения не является селективным, так как все металлы-спутники таллия также образуют нерастворимые сульфиды, поэтому этот способ применяют только к растворам с низким содержанием примесей. Сульфидный таллиевый концентрат выщелачивают раствором сульфата цинка, при этом в раствор переходит сульфат таллия: Tl2S + ZnSO4 = Tl2SO4 + ZnS. Из полученного раствора металлический таллий выделяют цементацией.
В настоящее время для очистки таллия используют его экстракцию из сульфатсодержащих растворов раствором иода в смеси 50% трибутилфосфата и 50% керосина. После этого таллий экстрагируют из органической фазы серной кислотой (300 г/л) с добавкой перекиси водорода.
Технически чистый таллий очищают от других элементов, содержащихся в колошниковой пыли (Ni, Zn, Cd, In, Ge, Pb, As, Se, Te), растворением в теплой разбавленной кислоте с последующим осаждением нерастворимого сульфата свинца и добавлением HCl для осаждения хлорида таллия (TlCl). Дальнейшая очистка достигается электролизом сульфата таллия в разбавленной серной кислоте с использованием проволоки из платины с последующим плавлением выделившегося таллия в атмосфере водорода при 350 - 400 °C.
Технология получения германия
Германий извлекается из продуктов металлургической переработки сульфидного сырья, в котором он находится в виде изоморфной примеси в минералах меди, цинка, свинца. Помимо перечисленных, источниками германия могут быть некоторые железные руды и каменные и бурые угли, преимущественно малометаморфизированные.
В зависимости от состава исходного сырья применяют различные способы их первичной обработки для получения более богатых германием продуктов - германиевых концентратов.
Выщелачивание серной кислотой. При большом содержании в исходном материале сульфидов, выщелачиванию предшествует окислительный обжиг. При выщелачивании материала 10 - 15%-ной серной кислотой германий (вместе с кадмием, цинком, мышьяком, частью железа) извлекается в раствор.
Сульфатизирующий обжиг. Для перевода германия и других составляющих исходного сырья в сульфаты нагревают исходный материал с серной кислотой при температуре 450 - 500 °C и затем выщелачивают продукт сульфатизации разбавленной серной кислотой.
Возгонка GeS в восстановительной среде, основанная на летучести, применяется для извлечения германия из рудных концентратов, пылей и других видов сырья. Материал нагревают в присутствии сульфатизирующего агента (пирита или серы) при температуре 800 - 900 °C в среде генераторного газа. Таким образом происходит извлечение германия из углей при работе котельных. А также для вторичного рудотермического обогащения первичных возгонов.
Восстановительная плавка в присутствии меди применяется для относительно богатого исходного материала. При этом получают сплав меди с германием. Полученный сплав меди с германием, содержащий 3 - 4% Ge растворяют в соляной кислоте. Из раствора дистиллируют тетрахлорид германия GeCl4.
Методы экстракции и сорбции применяют для получения германия из бедных растворов (0,01 - 0,1 г/дм3 Ge).
Экстракция. Из солянокислых растворов высокой концентрации (9 - 11 н. HCl), в которых содержатся недиссоциированные молекулы тетрахлорида германия GeCl4, германий избирательно экстрагируют смесями углеводородов, в частности, керосином. Из органической фазы германий реэкстрагируют водой, получая реэкстракты со степенью концентрирования 100 и более раз.
Сорбционные методы. Германий сорбирует из слабощелочных растворов; на анионитах, а из слабокислых растворов - на катионитах. Ионообменная сорбция германия менее избирательна, чем экстракция, и мало используется в промышленной практике.
Из полученных в результате экстракций или ионного обмена растворов с повышенной концентрацией германия осаждают германиевый концентрат. Германиевые концентраты выделяют из сернокислых растворов, осаждая, малорастворимые соединения или используя метод цементации.
Осаждение танниносодержащими веществами. Из бедных растворов (например, надсмольных вод) германий полно осаждается таннином (или содержащим таннин дубовым экстрактом).
Осаждение германата магния. При содержании в растворах 1 - 2 г/дм3 Ge можно из раствора добавлением оксида магния выделить германат магния Mg2GeO4.
Соосаждение с гидроксидом железа применяют для бедных растворов с концентрацией германия 0,01 - 0,02 г/дм3.
Цементация. Нормальный потенциал германия - 0,15 В. Это позволяет выделить германий из растворов цементацией на цинковой пыли.
Общепринятая технология получения диоксида германия высокой чистоты включает три стадии: получение технического тетрахлорида германия из германиевых концентратов (а также отходов германия); очистку тетрахлорида германия и получение диоксида германия из очищенного тетрахлорида.
В современных производствах проводят очистку технического тетрахлорида германия экстракцией примесей химически чистой соляной кислотой с последующей очисткой ректификацией.
Полученный тетрахлорид германия, с содержанием примесей на уровне 10-6% масс. Может быть дополнительно очищен до уровня тетрахлорида германия, применяемого при производстве оптического волокна, либо направляется на гидролиз и получение диоксида германия. Восстановление диоксида германия водородом - наиболее распространенный в промышленной практике способ получения германия. Процесс протекает с выходом до 98% и без потери качества материала.
Металлургия германия
Германий, полученный восстановлением высокочистого диоксида водородом, непригоден для применения в полупроводниковой электронике и требует процесса доочистки. Необходимая степень очистки достигается применением зонной плавки. Из очищенного этими методами германия затем получают монокристаллы. Применение монокристаллов позволяет обеспечить стабильность и однородность электрических и оптических свойств германия.
Для получения монокристалла германия применяют способ вытягивания из расплава методом Чохральского. В РФ имеются модификации данного метода, позволяющие получать монокристаллы до 250 мм в диаметре с приемлемой структурой.
Для оценки качества получаемых монокристаллов германия обычно определяют без разрушения слитка тип проводимости, удельное сопротивление, время жизни неравновесных носителей заряда, а также кристаллографические методы контроля структуры кристалла.
Технология получения гафния
Ввиду отсутствия у гафния собственных минералов и постоянного сопутствия его цирконию, его получают путем переработки циркониевых руд, где он содержится в количестве 2,5% от веса циркония (циркон содержит 4% HfO2, бадделеит - 4 - 6% HfO2). В мире в год в среднем добывается около 70 т гафния, и объемы его добычи пропорциональны объемам добычи циркония.
Металлический гафний в настоящее время получают восстановлением. Полной аналогии в свойствах продуктов плазменно-фторидной и экстракционно-фторидной технологий производства циркония нет, поскольку в экстракционно-фторидной технологии цирконий и гафний разделяют на гидрохимической стадии с помощью экстракции. В случае использования плазменно-фторидной технологии переработки циркона при сублимационной очистке циркония от примесей гафний в основном следует за цирконием. Гафниевую фракцию для очистки от обычных примесей (Fe, Al и др.) фильтруют через слой фосфатной катионнообменной смолы РФ, причем гафний целиком поглощается сорбентом. Вымывание гафния со смолы осуществляют раствором оксалата аммония. Таким образом, был получен концентрат гафния 99%. В технологии чистых соединений циркония применяют в основном перекристаллизационные, осадительные и экстракционные методы очистки. Метод ионного обмена применим к гафнию, поскольку масштабы производства существенно меньше.
Интересна особенность скандиевого минерала - тортвейтита: в нем содержится гафния в процентном отношении гораздо больше, чем циркония, и это обстоятельство очень важно при переработке тортвейтита на скандий и концентрировании гафния из него
Технология получения селена и теллура
Основным источником селена и теллура в современной металлургической практике являются полуфабрикаты переработки анодных шламов электролитического рафинирования меди. Селен и теллур извлекают из растворов и пылей газоочистки обжиговых и/или плавильных печей шламового производства. Теллур также извлекают из теллурового цементата, который образуется на стадии удаления меди из шлама автоклавным или аэрационным способом.
Селен из пылей шламового производства извлекают посредством окислительного обжига в электропечах при жидкостном улавливании газовой фазы с образованием раствора селенистой кислоты, из которого селен осаждают (восстанавливают) газообразным диоксидом серы или растворами сульфитов и/или гидросульфитов щелочных металлов. Аналогичным способом извлекают селен из растворов улавливания газов от обжига обезмеженного медеэлектролитного шлама. Для получения из технологических растворов марочного товарного селена применяют их предварительную очистку от тяжелых металлов на анионитах и от теллура посредством нейтрализации, при которой теллур осаждается в виде гидроксида. Для дополнительной очистки селена применяют щелочное кондиционирование в 1М растворе гидроксида натрия, а также окислительную плавку и вакуумную дистилляцию.
Технологические схемы извлечения селена и теллура из шламов медеэлектролитных заводов весьма сложны и многообразны. Выбор такой схемы зависит в основном от соотношения содержания этих двух элементов и благородных металлов, а также от масштабов производства.
Состав анодных шламов медного производства колеблется в пределах, %: 10 - 45 Cu; 0,05 - 5 Au; 5 - 45 Ag; 2 - 18 Se; 0,3 - 10 Te; 2 - 40 Pb; 0,5 - 16 Sb; 0,5 - 9 As.
Комплексную переработку анодных шламов обычно начинают с обезмеживания (перевода меди из шлама в раствор). Процесс осуществляют в реакторах при аэрации суспензии шлама в растворах серной кислоты воздухом:
Cu + H2SO4 + 0,5O2 = CuSO4 + H2O (2.9)
Для обезмеживания шламов на ряде производств используются автоклавы, где процесс ведут при повышенном давлении кислорода.
По окончании процесса обезмеживания пульпу фильтруют и кек направляют на извлечение селена и теллура. Извлечение селена в раствор при переработке шлама осуществляют посредством обжига: окислительного или сульфатизирующего с переводом селена в газообразный диоксид и его улавливанием в кислые или щелочные растворы. Вариантом извлечения селена из шламов может служить способ спекания с содой.
Применяемый ранее на предприятиях сульфатизирующий обжиг шлама, так же как и технология спекания с содой, отличаются низкой эффективностью и высокой экологической опасностью, в настоящее время практически не используются.
Сегодня на большинстве медерафинировочных производств мира применяют окислительный обжиг. Основной процесс - окисление с использованием воздуха, КВС (кислородо-воздушной смеси) или технического кислорода. В течение процесса проходит взаимодействие с кислородом присутствующих в шламе селенидов и теллуридов металлов - меди, серебра, свинца, палладия и ряда других. Например:
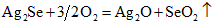 (2.10)
(2.10)Cu2Te + 2O2 = CuTeO3 + CuO (2.11)
Процессы окисления проходят в диапазоне температур 300 - 700 °C. В отличие от теллура, образующего нелетучие теллуриты меди, свинца, серебра и золота, селен переходит в газообразный диоксид. В газовую фазу также переходят образующиеся в процессе окисления сульфидов диоксид серы SO2, а также оксид мышьяка (III) As2O3.
Операцию обжига селена проводят в печах с обеспечением периодического или непрерывного процесса. На рисунке 2.5 представлена схема установки по обжигу шлама, находящегося в печи на противнях, в стационарном режиме с дальнейшим переводом селена в газовую фазу, восстановлением и итоговом получении продукта на фильтр-прессе. В печь загружается обычно от 1,5 до 3 тонн шлама с влажностью 15 - 20%. Обжиг такой партии шлама производится при температуре 600 - 650 °C в течение 20 - 24 часов.
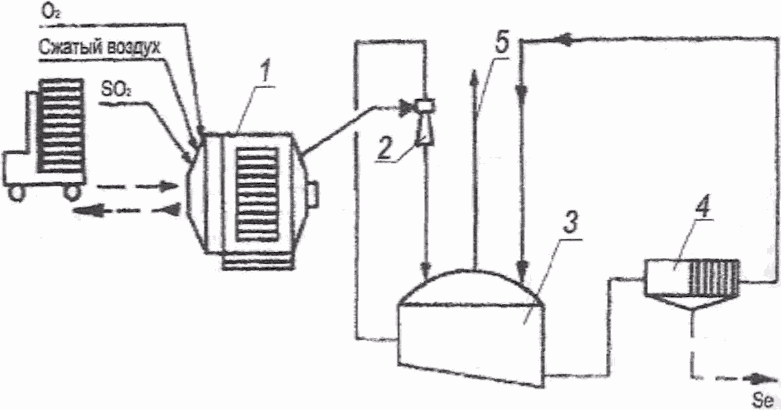
1 - печь обжига селена; 2 - эжектор; 3 - циркуляционная
емкость; 4 - фильтр-пресс; 5 - очищенный от диоксида
селена газ
На большинстве производств при обжиге шламов диоксид селена улавливают кислыми растворами с получением селенистой кислоты. Восстановление селена из растворов в этом случае производят газообразным диоксидом серы (в том числе присутствующим в газах обжига) или сульфитом (бисульфитом) натрия с получением технического селена:
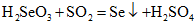 (2.12)
(2.12)Этот способ выделения селена основан на различии в величинах окислительно-восстановительных потенциалов системы, а именно:
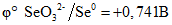 ,
,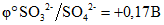 .
.Горным институтом (Санкт-Петербург) и институтом "Гинцветмет" была разработана и на ряде производств применяется технология извлечения селена из шламов, согласно которой обезмеженный шлам смешивают с добавками, гранулируют и обжигают при температуре 700 - 800 °C в печах шахтного типа с пропусканием через слой гранул горячего воздуха (рисунок 2.6). Производительность печи - 3 тонны шлама в сутки.
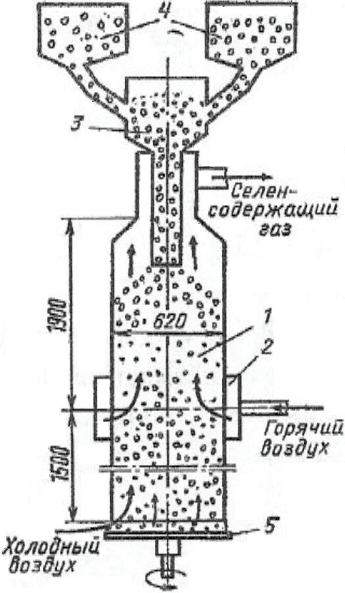
1 - шахта печи; 2 - фурменный пояс; 3 - загрузочная воронка;
4 - емкость (кюбель) с гранулированным шламом;
5 - тарельчатый питатель для разгрузки огарка
непрерывного действия
Во время обжига селен из селенидов металлов окисляется и возгоняется в виде диоксида SeO2, который поглощается оборотным щелочным раствором с образованием селенита натрия Na2SeO3. Полученный селенитный раствор восстанавливают алюминиевым порошком до полиселенида натрия Na2Sen. По окончании восстановления и фильтрации селенидный раствор поступает на очистку от примесей и последующую аэрацию для осаждения селена. При этом регенерируется гидроксид натрия:
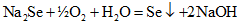 (2.13)
(2.13)Данный процесс отличается замкнутым циклом по растворам. Его технологическая схема приведена на рисунке 2.7.
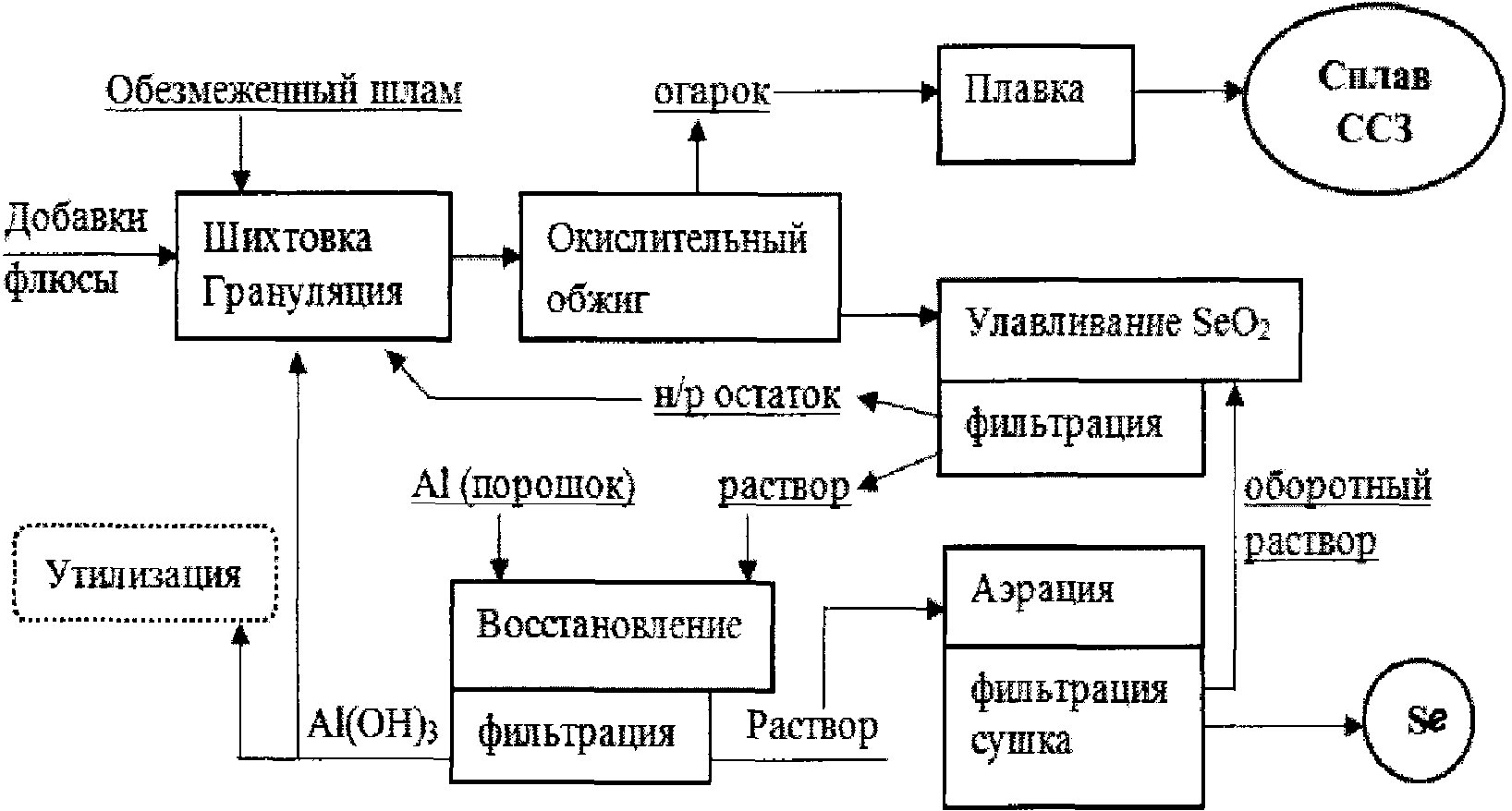
Технический селен, выпускаемый по отмеченным методам, содержит от 93 до 96% основного вещества. Его подсушивают, производят рассев и поставляют потребителям по ГОСТ 10298-79 в виде порошка или слитков после переплавки.
Огарок после обжига шламов плавят на получение сплава серебряно-золотого (ССЗ - сплава Доре). Теллур при этом извлекается в специально наводимые содистые шлаки в виде теллурита натрия Na2TeO3. Содержание теллура в шлаках доходит до 40 - 45%. Содистый шлак подвергается водному выщелачиванию; полученный раствор очищается от сопутствующих компонентов введением реагентов: сульфида натрия и оксида кальция. Очищенный раствор подвергается электроэкстракции с получением чернового теллура чистотой 95 - 97%. Катодный черновой теллур содержит 2 - 5% примесей. Последующая теллуридная перечистка заключается в следующем: порошкообразный металл растворяют в щелочи в присутствии восстановителя - алюминиевого порошка, получая раствор теллурида:
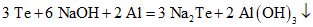 (2.14)
(2.14)Из полученного раствора при аэрации осаждают теллур технических марок:
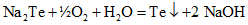 (2.15)
(2.15)Схема этого процесса приведена на рисунке 2.8.
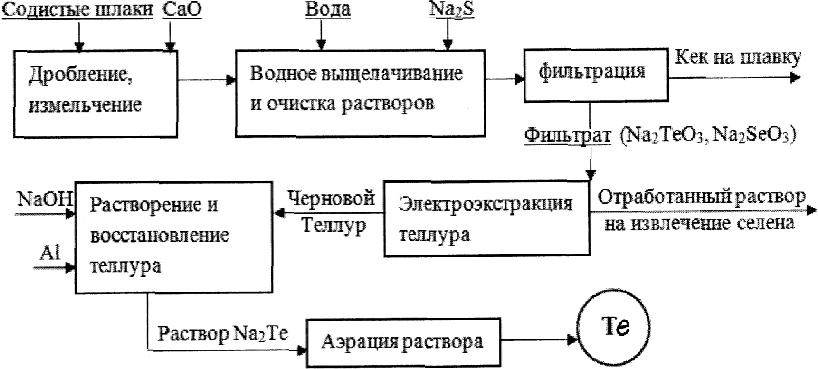
Получаемые по приведенным схемам технические селен и теллур не отличаются высокой чистотой. Они содержат от 2 - 3 до 6 - 7% примесей, сопутствующих этим элементам как в рудном сырье, так и приобретенные при его переработке (мышьяк, медь, свинец, сурьма, алюминий, теллур в селене, селен в теллуре и др.).
По ГОСТ 10298-79 в странах СНГ выпускают селен двух марок: СТ-0 (99,8%), СТ1 (99,0%). Для очистки от примесей селена в настоящее время применяют плавку с аммиачной селитрой и дистилляцию. Плавка с селитрой предусматривает окисление примесей и перевод их в шлак. Так, теллур удаляют в шлак по реакции:
Te + 2NH4NO3 = TeO2 + 2N2 + 4H2O (2.16)
Процесс проводят в котлах - аппаратах из нержавеющей стали с наружным обогревом при температуре 250 - 280 °C (селен плавится при температуре 217 °C). Разложение селитры и окисление примесей начинается при температуре 190 °C. Рафинированный селен разливают в изложницы из нержавеющей стали. По этому способу получают селен чистотой до 99,4%.
Вакуумная дистилляция основана на разной летучести селена и металлов примесей, основная масса которых остается в нелетучем остатке.
Дистилляцию селена проводят при температуре 650 - 680 °C и атмосферном давлении или при температуре 310 - 420 °C и разряжении 27 - 800 Па. Пары селена конденсируют при температуре 250 - 100 °C. Дистилляцию осуществляют в ретортах или емкостях, изготовленных из коррозионностойкой стали. Жидкий селен после дистилляции разливают на слитки или гранулы. Слитки селена медленно охлаждают для получения селена "серой" полиморфной модификации. После двукратной дистилляции селен достигает чистоты 99,99%.
По ГОСТ 17614-80 в странах СНГ выпускают теллур трех марок: Т0 (99,93%), Т1 (99,3%), Т2 (96,5%)
Для получения теллура чистотой до 99,999% также применяют вакуумную дистилляцию. Эту операцию проводят при остаточном давлении ~ 1 Па в аппаратах с электронагревом и использованием диффузионных насосов для создания глубокого вакуума. При дистилляции примеси с меньшей, чем у теллура упругостью паров, остаются в кубовом остатке, а примеси селена, натрия, калия, магния, упругость паров которых выше или равна упругости паров теллура, переходят в дистиллят и конденсируются в разных температурных зонах. В качестве варианта для предварительной переплавки и очистки теллур подвергают фильтрации расплава. При этой операции оксиды части металлов, образующих определенные конгломераты в расплаве теллура, отфильтровываются на огнеупорной фильтрующей перегородке с размером отверстий 0,1 - 0,15 мм.
Способ дистилляции с предварительными операциями дополнительной очистки обеспечивает получение теллура чистотой 99,99 - 99,999% и выше. Для удаления примесей из очищенного теллура, в зависимости от требуемой чистоты металла, помимо вакуумной дистилляции, применяют способы теллуридного рафинирования, зейгерования и зонной плавки.
Селен и его соединения применяется в электронике (фотоэлементы, полупроводниковые материалы, термосплавы), в химической, стекольной промышленности (включая пигменты), при изготовлении керамики, лекарственных средств, в качестве кормовых добавок.
Теллур технический используется в производстве прецизионных сплавов, в стекольной и химической промышленности, особочистый теллур применяется в электронной промышленности для изготовления полупроводников, термосплавов, лазеров, солнечных батарей.
Технология получения ванадия
Несмотря на относительно высокое содержание ванадия в земной коре, превышающее содержание в ней цинка, меди и свинца, он практически не образует самостоятельных месторождений и рассеян в разных минералах и горных породах.
Основной источник получения ванадия - ванадийсодержащие железные руды. При доменной плавке железных руд 80 - 90% ванадия переходит в чугун. При последующем переделе ванадийсодержащего чугуна на сталь получаются шлаки, обогащенные ванадием. Из шлаков ванадий извлекают химическими методами в виде соединений, которые являются исходным продуктом для выплавки феррованадия.
Ванадий также получают из различных ванадийсодержащих руд и концентратов.
При извлечении ванадия из патронитовых руд их подвергают окислительному обжигу с получением богатого огарка, направляемого на алюмотермическое восстановление в электропечах с получением феррованадия, или концентрата. Последний обжигают, и ванадий выщелачивают гидроксидом натрия или калия, а также кислотами с последующим осаждением из раствора пентаоксида ванадия.
Из богатых роскоэлитовых руд ванадий выщелачивают также гидроксидом натрия или калия, кислотами. Затем из растворов осаждают пентаоксид ванадия.
По обеим технологиям извлечение ванадия в феррованадат составляет 95%.
Перспективный способ получения ванадия - восстановление его оксидов углеродом в вакууме при температуре 1250 - 1700 °C.
Эффективный способ рафинирования ванадия - вакуумная электронно-лучевая зонная плавка. Очистка металла в этом случае происходит за счет зонного рафинирования и испарения примесей.
Технология получения ниобия и тантала
Ниобий и тантал входят в состав более 130 минералов, представляющих сложные комплексные соли Nb-Ti-Nb-Ta-кислоты. В состав этих минералов входят также катионы железа, марганца, щелочных и щелочноземельных металлов, редкоземельных элементов, торий, уран и др. Среди известных минералов ниобия и тантала только три имеют промышленное значение. К ним относятся танталит-колумбит, пирохлор и лопарит.
Переработка ниобий- и танталсодержащих концентратов и промпродуктов обогащения включает растворение (вскрытие) их с получением продукта, содержащего оба элемента, либо их хлорирование газообразным хлором в присутствии восстановителя. В качестве восстановителя могут выступать материалы на основе углерода или серы [85].
Технологии переработки танталсодержащего сырья до получения компактного металла и ниобийсодержащего сырья аналогичны, кроме способов получения порошкообразного металлического тантала из его соединений, которые имеют некоторые особенности.
Основной минерал ниобия - колумбит, химически прочный, неразлагаемый минеральными кислотами за исключением фтористоводородной кислоты. Поэтому для вскрытия колумбитовых концентратов применяют сплавление с гидроксидом натрия (калия) или разложение фтористоводородной кислотой.
Гидратированные пентаоксиды ниобия и тантала являются источником получения металлических тантала и ниобия, а также их солей.
Для переработки лопаритовых концентратов применяют два способа: хлорирование и сернокислотное выщелачивание.
При хлорировании компоненты лопаритового концентрата взаимодействуют с газообразным хлором при температуре 750 - 800 °C в присутствии угля. Разделение ценных компонентов в этом процессе обусловлено разной летучестью образующихся хлоридов.
Сернокислотный способ разложения лопаритового концентрата основан на различии в растворимости получаемых двойных сульфатов титана, ниобия, тантала и РЗЭ.
Переработка пирохлоровых концентратов осуществляется выщелачиванием (фтористоводородной, соляной или серной кислотами) или хлорированием.
Порошкообразный ниобий получали при переработке пирохлоровых концентратов и методом хлорирования из лопаритового концентрата, техническую пятиокись ниобия - гидролизом технических хлоридов.
Для выделения ниобия и тантала технический гидроксид ниобия подвергали дробной кристаллизации фтористых солей, что позволяло получить чистые соединения ниобия и тантала.
Гидратированные пентаоксиды ниобия и тантала являются источником получения металлических тантала и ниобия, а также их солей.
Для выделения ниобия и тантала технический гидроксид ниобия подвергали дробной кристаллизации фтористых солей, что позволяло получить чистые соединения ниобия и тантала.
В настоящее время для выделения и разделения тантала и ниобия применяют жидкостную экстракцию органическими растворителями, а также ректификацию хлоридов.
Разделение тантала и ниобия экстракцией проводят из растворов фтористых соединений тантала и ниобия, полученных при растворении концентратов в плавиковой кислоте или смеси серной и плавиковой кислот. В качестве экстрагентов используются ТБФ, метилизобутилкетон, алифатические спирты. При экстракции достигается очистка ниобия и тантала от различных примесей (титана, железа, фосфора и т.д.).
Разделение тантала и ниобия ректификацией хлоридов используют при переработке рудных концентратов (например, лопаритовых) методом хлорирования с получением смеси пентахлоридов металлов.
Технологическая схема разделения смеси пентахлоридов включает предварительную ректификацию для отделения хлоридов тантала и ниобия от сопутствующих примесей титана, кремния, алюминия и др.; основную ректификацию для получения чистого пентахлорида ниобия и концентрата пентахлорида тантала; ректификацию танталовой фракции (получение чистого пентахлорида тантала).
Метод ректификации отличается высокой производительностью и эффективностью разделения металлов. Полученные чистые пентахлориды ниобия и тантала используют для получения тантала и ниобия.
Металлические тантал и ниобий получают восстановлением из ряда их соединений высокой чистоты - оксидов, комплексных фторидов и хлоридов.
В промышленной практике для восстановления этих двух металлов используют различные методы.
В связи с высокими температурами плавления ниобий и тантал получают в основном в порошкообразном состоянии или в виде спекшейся губки.
Натрийтермическое восстановление из комплексных фторидов K2TaF7 и K2NbF7 - старейший способ получения порошков тантала и ниобия. Его применяют до настоящего времени.
Карботермический способ получения ниобия и тантала из их пентаоксидов был вначале разработан для производства ниобия. В настоящее время его используют также при получении тантала и его сплавов с ниобием.
Алюмотермическое получение ниобия и тантала из высших оксидов отличается высокими технико-экономическими показателями, простотой технологии и аппаратурного оформления.
Восстановление тантала и ниобия из хлоридов водородом наиболее перспективно по сравнению с восстановлением магнием или натрием. Водородное восстановление предусматривает получение прутков компактных металлов на нагретых подложках.
Этим способом можно получать также прутки ниобия.
Электролитическое получение тантала возможно только из расплавленных сред. Электролитом служит расплав K2TaF7 и KF - KCl, в котором растворен пентаоксид тантала (Ta2O5).
Длительное время единственным способом получения компактных заготовок ниобия и тантала была порошковая металлургия, сохранившая практическое значение до наших дней. Мелкозернистые порошки тантала прессуют под давлением 300 - 500 МПа, а ниобия - 100 - 150 МПа.
Танталовые и ниобиевые заготовки (штабики) спекают в сварочных аппаратах, применяемых при производстве вольфрама и молибдена, отличающихся наличием вакуумного герметичного колпака. Крупные заготовки и изделия сложной формы из ниобия и тантала спекают при их косвенном нагреве в вакуумных индукционных печах.
Для производства тантала и ниобия особой чистоты представляет интерес бестигельная зонная плавка с электронно-лучевым обогревом.
Для выбора способа переработки вовлекаемого в производство сырья необходимо учитывать качество исходного материала, наличие примесей, лимитирующих выбор конечной продукции, а также имеющиеся производственные мощности.
Технология получения циркония
Обогащение циркониевых руд.
Промышленное получение циркония осуществляется из руд, содержащих два основных минерала: циркон ZrSiO4 и бадделеит ZrO2.
Измельченная руда подвергается магнитной сепарации в слабом поле для получения магнетитового концентрата. Хвосты магнитного обогащения обесшламливаются в гидроциклонах, зернистая фракция +44 мкм подвергается апатитовой флотации с получением апатитового концентрата. Хвосты флотации разделяются на концентрационных столах. Тяжелая фракция, содержащая бадделеит, подвергается обжигу при температуре 400 °C и затем электромагнитной сепарации. Немагнитная фракция подвергается обжигу при температуре 900 °C последующей магнитной сепарацией в слабом поле. Немагнитная фракция представляет собой бадделеитовый концентрат - более 96% ZrO2. Аналогичная схема используется при переработке руд Ковдорского месторождения (Россия).
Разработанные гравитационно-магнитоэлектростатические схемы обогащения могут использоваться для переработки погребенных прибрежно-морских россыпей России (отдельные участки Туганского, Лукояновского и других месторождений). Обогащение комплексных редкометалльных месторождений (Улуч-Танзел) затруднено сложностью минерального состава сырья, наличием радиоактивных примесей.
В производстве циркония принято несколько технологий переработки цирконовых концентратов. Гидрометаллургические способы предусматривают вскрытие цирконовых концентратов предварительным спеканием. По одной технологической схеме спекание осуществляется со щелочами и карбонатами щелочных и щелочноземельных металлов. После выщелачивания, перевода циркония в раствор и выделения из раствора получаются гидратированные соли циркония и после прокалки - технический диоксид циркония. Технический диоксид циркония может являться товарным продуктом для лакокрасочной и керамической промышленности.
По другой технологии спекание происходит с комплексными фторидами щелочных металлов. После выщелачивания и перевода циркония в раствор при охлаждении кристаллизуют фторцирконат калия. Способ получения фторцирконата калия наиболее целесообразен для последующей технологии очистки от гафния.
Бадделеитовые концентраты перерабатывают по гидрометаллургической схеме вскрытием концентрированной серной кислотой с получением фторцирконатов.
Из растворов K2(Zr,Hf)F6 получают цирконий экстракционным разделением при помощи трибутилфосфата. Циркониевые продукты получаются с содержанием гафния до 0,01%. Экстракционный метод пригоден для непрерывных процессов, которые легко контролировать и автоматизировать; позволяет получить довольно чистые продукты; имеет высокую производительность. Этот метод наиболее широко распространен в промышленности.
Кроме того, технология получения фторцирконатов удобна, так как из фторцирконата калия путем его восстановления натрием получают порошки технического циркония.
Порошок немного большей крупности может быть получен кальцийтермическим методом восстановления диоксида циркония.
Переработка циркона с получением фторцирконата калия удобна при использовании ряда технологий получения металлического циркония и соединений циркония и, самое главное, для очистки циркония и его соединений, от гафния.
Основным способом, принятым в промышленности для переработки циркониевых концентратов, в настоящее время является хлорирование для получения цирконовой губки. Хлорирование осуществляют в шахтных электропечах. Процесс хлорирования непрерывный. Кроме того, цирконийсодержащие материалы могут быть прохлорированы в присутствии серы и ее хлоридов [86].
Более перспективен процесс хлорирования карбида и карбонитрида циркония. Полученный в результате хлорирования тетрахлорид циркония является товарным продуктом и исходным компонентом для получения товарного диоксида циркония и металлического циркония.
Очищенный возгонкой тетрахлорид циркония является исходным материалом для получения губчатого циркония. Измельченная губка является материалом для получения компактного металла методом вакуумной дуговой или аргонно-дуговой плавки. Наиболее распространен метод вакуумной дуговой плавки, позволяющей получать компактные слитки до 2 т.
За рубежом практикуется технология восстановления тетрафторида циркония щелочными металлами с получением металлического циркония.
В небольших количествах образцы особо чистого циркония получаются иодидным методом.
Практикуемый в настоящее время в промышленности процесс металлотермического восстановления тетрахлорида циркония периодический. Разработан новый непрерывный процесс получения металлического циркония из его тетрахлорида - процесс аэрозольного восстановления. В качестве восстановителя используются магний или натрий.
Производство губчатого титана во всем мире основано главным образом на процессе Кролла, в котором тетрахлорид титана (TiCl4) получают методом хлорирования диоксида титана (TiO2). Полученный сырец TiCl4 очищается, а затем восстанавливается расплавленным металлическим магнием до металлического титана (Ti) с образованием хлорида магния (MgCl2). Хлорид магния перерабатывается в металлический магний и газообразный хлор методом электролиза его расплава. Металлический Mg возвращается на восстановление тетрахлорида титана, а выделяющийся газообразный хлор направляется на стадию хлорировании TiO2. Существует три основных технологических стадии в производстве губчатого титана по процессу Кролла: хлорирование обогащенного сырья TiO2; восстановление TiCl4 расплавленным Mg и регенерация Mg методом электролиза расплава MgCl2.
Тетрахлорид титана (хлорид титана (IV), четыреххлористый титан) - бинарное соединение титана с хлором с формулой TiCl4.
Тетрахлорид титана был открыт в 1825 году Э.С. Джорджем при пропускании хлора через карбонитрид титана в нагретой стеклянной трубке. Годом позже первый патент на получение TiCl4 был выдан Л.Э. Бартону, который хлорировал карбонизированную смесь угля и TiO2 при 650 °C.
Прорыв в промышленной металлургии титана произошел в конце 1930-х годов благодаря работам У.Дж. Кролла, продемонстрировавшего возможность получения титана путем реакции TiCl4 с расплавленным металлическим магнием при повышенных температурах. За этим последовали интенсивные исследования, проведенные Горным бюро США, где после Второй мировой войны были получены первые тонны металлической титановой губки. В 1948 году процесс Кролла был освоен в промышленных масштабах, когда компания E.I. DuPont de Nemours & Co. построила первый завод по производству титановой губки в Ньюпорте, штат Делавэр.
Разработка процесса получения пигментного TiO2, в котором в качестве промежуточного соединения также используется TiCl4, внесла значительный вклад в развитие технологий производства TiCl4. До 1945 года карбохлорирование руд TiO2 осуществлялось путем пропускания хлора через неподвижный слой горячих брикетов кокса и рутила. Этот метод постепенно был заменен реакторами с псевдоожиженным (кипящим) слоем, которые обеспечивали более высокую производительность.
Хлорирование в кипящем слое было внедрено западными и японскими производителями титановой губки. На заводах по производству титановой губки, построенных в Советском Союзе, была выбрана другая технология производства TiCl4, а именно хлорирование в расплаве солей. В Китае в промышленности применяют обе технологии: хлорирование в кипящем слое и в расплаве солей.
По состоянию на 2017 год титановую губку производили семь стран, а суммарная мировая мощность составила 277 000 тонн в год (таблица 2.2) [52].
Таблица 2.2
хлорирования
Страна | Мощность производства, т | Технология хлорирования |
Китай | 110 000 | Расплавное хлорирование и кипящий слой |
Япония | 68 800 | Кипящий слой |
Россия | 46 500 | Расплавное хлорирование |
Казахстан | 26 000 | Расплавное хлорирование |
США | 13 100 | Кипящий слой |
Украина | 12 000 | Расплавное хлорирование |
Индия | 500 | Кипящий слой |
2.15.3.1 Хлорирование в кипящем слое
Хлорирование в кипящем слое - это непрерывный процесс, в котором исходное сырье TiO2 (такое как природный рутил, синтетический рутил, титановые шлаки или обогащенный титановый шлак (UGS) и кокс) хлорируется в псевдоожиженном слое газообразным хлором.
Несмотря на то, что карбохлорирование исходного TiO2 является хорошо зарекомендовавшей себя коммерческой технологией, оно освоено относительно небольшим числом фирм, в основном производителями пигментов и некоторыми производителями титановой губки. Поскольку эти фирмы считают оптимальные условия проведения технологического процесса коммерческой тайной, то информация об этих производствах в открытой печати крайне ограничена.
При получении тетрахлорида титана протекают следующие реакции:
Реакцию (2.17) можно выразить как комбинацию реакции Будуара:
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: п. [18] Библиографии отсутствует. |
и хлорирование с помощью оксида углерода [18]:
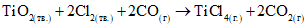 (2.20)
(2.20)Реакции хлорирования являются экзотермическими, и процесс, как правило, осуществляется в автотермическом режиме (хотя при необходимости для сжигания кокса и получения большего количества тепла может добавляться воздух). Хлорирование обычно ведется при 900 - 1100 °C. Реакция (2.18) термодинамически выгодна в этом температурном диапазоне. Равновесное молярное соотношение CO/CO2, предсказанное по реакции Будуара (Реакция 2.19), превышает 10 при температуре выше 900 °C. Однако на практике при хлорировании TiO2 в присутствии углерода молярное соотношениях CO/CO2 составляет около единицы или ниже.
Реакция хлорирования очень быстрая. Обычно, в реакторах кипящего слоя достигается практически полная конверсия хлора.
Эффективная работа хлоратора достигается за счет подбора и поддержания оптимальных условий псевдоожижения. Система подачи газа (трубчатые инжекторы или форсунки) должна обеспечивать достаточный перепад давления для равномерного распределения хлора по всему сечению реактора. Линейная скорость газа должна быть выше минимальной скорости псевдоожижения твердой фазы слоя, которая зависит от характеристик (размера частиц, плотности) исходного TiO2 и кокса. Верхний предел скорости ограничен выносом твердой фазы, что обуславливает чистую потерю TiO2 и кокса.
В промышленности производители пигментной окиси титана применяют реактора кипящего слоя диаметром от 1 до 3 м.
В настоящее время размер реактора с псевдоожиженным слоем может быть масштабирован до диаметра 6 ~ 7 м, что позволяет производить 500 000 т/г TiCl4. Проверенная технология, применяемая в Японии, - это реактор диаметром 3 м с производительностью 140 т/д TiCl4. В Китае компании Zunbao Titanium (филиал Zunyi Titanium) и Luoyang Shuangrui Wanji приобрели в 2008 году технологию хлорирования с псевдоожиженным слоем, разработанную в США. Специализированная технология использует диаметр реактора 2,4 м, что соответствует производству титановой губки мощностью 10 000 т/г. Производительность одной печи достигает 100 т/д. Расход сырья составляет 0,5 т-рутила/т-TiCl4 и 0,9 т-Cl2/т-TiCl4. Содержание хлора в отходящем газе составляет менее 0,1 мг/м3.
Большинство примесей, содержащихся в исходном сырье TiO2, реагируют с хлором и образуют хлориды металлов, некоторые из которых могут оказывать существенное влияние на работу хлоратора. При хлорировании примесей образуется большое количество хлоридов металлов, которые являются отходами основного производства. Кроме того, некоторые хлориды металлов откладываются в газоходах, что может привести к их зарастанию и даже забивке.
По этой причине производители губки в качестве исходного сырья используют, синтетический рутил, хлоридные шлаки и обогащенные титановый шлак (UGS). В целом, высокое содержание TiO2 (> 92% масс.) является предпочтительным ввиду простоты проведения операции его хлорирования. Так большинство компаний по производству металлического титана в Японии используют исходный TiO2 чистотой более 95% (во всем мире используется TiO2 чистотой более 90%). В последние годы высокая стоимость высококачественного исходного TiO2 привела к тому, что некоторые компании в Японии начали использовать сравнительно недорогой исходный TiO2 чистотой более 90%. Однако такое использование ограничено из-за увеличения потерь хлора, засорения труб и повреждения огнеупорных материалов в хлораторе.
Хлорид кальция (CaCl2) и хлорид магния (MgCl2) имеют низкое давление паров в диапазоне рабочих температур хлоратора и поэтому могут накапливаться в жидкой форме в реакционном слое. При относительно высокой концентрации эти расплавленные хлориды могут вызывать слипание слоя и, в конечном итоге приводить к спеканию слоя и остановке процесса. По этой причине титановое сырье, пригодное для хлорирования в реакторе кипящего слоя, должно содержать не более 0,2% CaO и не более 0,8% MgO.
Отложение хлоридов металлов в газоходе хлоратора, которое может в конечном итоге привести к его забивке, является еще одной распространенной проблемой в хлораторах. Наиболее вероятными хлоридами металлов, вызывающими эти проблемы, являются хлорид железа (FeCl2) и хлорид марганца (MnCl2). Требуется быстрое охлаждение газохода хлоратора, чтобы при конденсации хлориды металлов образовывали мелкодисперсные частицы, которые могли бы уноситься с отходящими газами.
В отличие от других примесей, значительная доля диоксида кремния (SiO2) и диоксида циркония (ZrO2), присутствующих в исходном TiO2, не реагирует с хлором. Эти оксиды часто называют "инертными". В зависимости от размера частиц, инертные оксиды могут накапливаться в слое хлоратора и достигать очень высоких концентраций. В определенный момент, для поддержания высокой скорости хлорирования, слой необходимо обновлять.
В природном и синтетическом рутиле SiO2 и ZrO2 в основном присутствуют в виде дискретных частиц. В основном это зерна кварца (SiO2) и/или циркона (ZrSiO4), которые не были полностью удалены в процессе переработки ильменитовой руды. Относительно крупный размер этих зерен препятствует их выносу с отходящими газами, и они имеют тенденцию накапливаться в слое. С другой стороны, SiO2 и ZrO2 в шлаках TiO2 и UGS присутствуют в виде очень мелких силикатных включений, диспергированных в основной фазе TiO2. При хлорировании фазы TiO2 эти включения высвобождаются, и из-за их очень малого размера большая их часть уносится из реактора. В результате скорость накопления инертных веществ в хлораторе значительно ниже при использовании шлаков или UGS. Слой достаточно долго сохраняет свою реакционную способность и не требует частого обновления.
Физические свойства, а точнее размер частиц и пористость, исходного сырья оказывают большое влияние на унос TiO2 из хлоратора. Шлаки TiO2 намеренно производятся с относительно крупным размером частиц (d50 около 300 - 350 мкм) и низкой пористостью. Такие характеристики хорошо подходят для минимизации уноса частиц. Природный рутил плотный, но обычно имеет довольно мелкие размеры (d50 около 125 - 175 мкм), что может привести к более высоким потерям TiO2. Помимо более мелкого размера, синтетический рутил также очень пористый из-за природы процесса обогащения. Это способствует еще более высоким потерям TiO2, поскольку пористые частицы быстрее теряют свою массу в процессе хлорирования и уносятся с пылью. По этой причине конверсия TiO2 не является полной, и небольшая его доля теряется из-за уноса.
Благодаря низкой зольности и низкому содержанию водорода, прокаленный нефтяной кокс является предпочтительным источником углерода для хлорирования в псевдоожиженном слое. Расход кокса на единицу TiCl4 варьируется в зависимости от состава исходного TiO2 (количества и природы примесей), рабочей температуры (учитывая ее влияние на соотношение CO/CO2) и физических потерь из-за уноса. Следует подчеркнуть, что содержание кокса в слое хлоратора не зависит от его использования. У производственников есть свои предпочтения: кокс обычно составляет 20% - 40% от материала слоя. Чтобы обеспечить надлежащее псевдоожижение и минимизировать потери за счет пылеуноса, размер частиц кокса должен быть от 0,25 до 5 мм.
2.15.3.2 Хлорирование в расплаве солей
После окончания Второй мировой войны в СССР был разработан промышленный процесс хлорирования карналлита, калий-магниевого минерала типа KCl·MgCl2·6H2O, в ваннах с расплавленными хлоридами. На основе этого опыта в 1954 году технология хлорирования в расплаве солей была внедрена для переработки титанового шлака. Отработанный электролит, полученный из магниевых электролизеров, использовался в качестве расплава для хлорирования. В этом процессе измельченный титановый шлак и прокаленный пековый кокс суспензируются в расплаве хлоридов металлов (KCl 72 - 76%, NaCl 16%, MgCl2 4 - 6% и CaCl2). Затем в солевой расплав вводится газообразный хлор, который реагирует с титановым шлаком с образованием TiCl4. Эта технология позволяет использовать для переработки титановый шлак с содержанием CaO + MgO около 6%.
Как и при хлорировании в псевдоожиженном слое, в процессе хлорирования в расплавах солей в качестве восстановителя используется кокс или антрацит. Однако реакция протекает при более низких температурах, обычно в диапазоне 700 - 800 °C. В результате преобладает реакция (2.17) и образуется преимущественно CO2, что позволяет минимизировать расход углерода.
Процесс протекает в круглых или прямоугольных хлораторах. Хлор вводится в нижнюю часть реактора через фурмы. Высота расплава составляет 2 - 3 м. Восходящий поток газов создает интенсивную циркуляцию в расплаве, предотвращая оседание исходного TiO2 на дне хлоратора и всплывание частиц угля на поверхность зеркала расплава.
В промышленных хлораторах, использующих процесс хлорирования в расплаве солей (хлоридов), основным компонентом (70 - 80 мас.%) свежего расплава является KCl, а остальное составляют NaCl, CaCl2 и MgCl2. По мере протекания хлорирования примеси, содержащиеся в исходном TiO2, накапливаются в расплаве либо в виде хлоридов (FeCl2, MnCl2 и т.д.), либо в виде оксидов (SiO2). Для поддержания необходимого состава расплава в хлоратор загружают шихту, состоящую из титанового шлака, углерода и поваренной соли (NaCl) Большое количество образующихся при этом отходов (около 250 кг/т TiCl4) является основным недостатком этой технологии.
Основным преимуществом хлорирования в расплаве солей является возможность перерабатывать исходное сырье с высоким содержанием кальция и магния. В отличие от хлораторов с псевдоожиженным слоем, где слой может слипнуться, в процессе хлорирования в расплаве солей жидкие хлориды кальция и магния становятся частью расплава.
Это объясняет, почему данная технология была принята в СССР и Китае, регионах, где местные запасы TiO2 богаты CaO и MgO. Еще одним преимуществом хлорирования в расплаве является возможность использования мелкозернистого сырья. Титановый шлак, измельченный до фракции 80 - 130 мкм, и кокс фракцией 130 - 200 мкм подходят для хлорирования в расплаве солей, что для процесса в кипящем слое не допустимо из-за слишком мелких размеров зерен сырья.
Хлорирование в расплаве солей широко применяется в России. Производительность реакторов хлорирования достигает 120 - 150 т/сут TiCl4, а извлечение титана из шлака составляет около 96%. В Китае компании Pan Steel Titanium и Yunnan Xinli импортировали технологию хлорирования расплавленными солями из Запорожского института титана и магния. Диаметр реактора составляет 3,3 м, а суточная производительность достигает 120 т/сут TiCl4. Компания Pan Steel Titanium недавно объявила, что ее хлоратор успешно переработал титановый шлак с концентрацией TiO2 всего 72%, а суточная производительность достигла 140 т.
Компания Jinzhou Titanium самостоятельно разработала процесс хлорирования в расплаве солей. В своей основе процесс аналогичен технологии Запорожского института титана и магния, но используется более высокая температура хлорирования. Температура хлорирования составляет около 780 °C вместо 720 °C. Суточная производительность в Цзиньчжоу также достигает 130 тонн. Однако более высокая рабочая температура требует более эффективной очистки отходящих газов, поскольку газ TiCl4 увлекает больше пыли и легко засоряет систему очистки отходящих газов.
Главным преимуществом метода хлорирования в расплаве солей является его пригодность для переработки титанового шлака с высоким содержанием CaO+MgO. Менее строгие требования к концентрации газообразного хлора и более широкий диапазон гранулометрического состава исходного сырья делают его предпочтительным для некоторых производителей титана. Однако сложность технологического процесса и суровые условия эксплуатации, особенно большой объем образующихся отходов расплавленных хлоридов, препятствуют развитию этого метода в мире. Чтобы обеспечить непрерывный ход производственного процесса, необходимо регулярно сливать отработанный расплав и добавлять новую соль для поддержания производительности реактора. Это приводит к увеличению производственных затрат и увеличению выбросов твердых отходов. Согласно статистике, в титановой промышленности на каждую тонну произведенного товарного губчатого титана процесс хлорирования в расплаве солей произведет 1,17 тонн отходов - хлоридов и оксидов металлов. В действующих технологиях отработанный расплав размывается водой. Нерастворимый остаток вывозится на полигон, а раствор нейтрализуется известковым молоком и после отстаивания примесей сливается. Однако эффективность метода удаление примесей из раствора довольно низкая.
2.15.3.3 Хлорирование в кипящем слое фурменного типа
Применение реакторов кипящего слоя с перфорированными распределительными решетками для переработки титанового сырья с высоким содержанием CaO+MgO невозможно. Большое количество отходов расплавленных солей и сложная технология делают хлорирование расплавленных солей менее привлекательным. Поэтому в СССР была разработана промышленная технология хлорирования титановых шлаков. Разработчиком технологии и конструкции аппарата хлорирования выступал Всесоюзный научно-исследовательский и проектный институт алюминиевой, магниевой и электродной промышленности (ВАМИ). Испытания опытного образца аппарата хлорирования с фурменной подачей хлора проводились в 1973 году при участии специалистов Запорожского института титана и магния. Несмотря на перспективность этой технологии, она так и не была внедрена на титаномагниевых комбинатах СССР.
Китайские металлурги разработали способ переработки сырья с высоким содержанием CaO+MgO в реакторе кипящего слоя, внеся следующие изменения:
1. Заменили газораспределительную решетку в кипящем слое на фурмы.
2. Увеличили температуру хлорирования до 900 - 1100 °C, что позволило большему количеству CaCl2 и MgCl2 перейти в паровую фазу.
3. Увеличили долю добавляемого углерода с 30 - 35% до 35 - 40%, что обеспечило более высокую температуру реакции (избыточный углерод поглощает CaCl2 и MgCl2, создавая благоприятные условия для хлорирования).
4. Периодически удаляют обогащенный CaCl2 и MgCl2 шлак из нижней части кипящего слоя.
Типичная конфигурация днища фурменного реактора с кипящим слоем показана на рисунке 2.9 ниже.
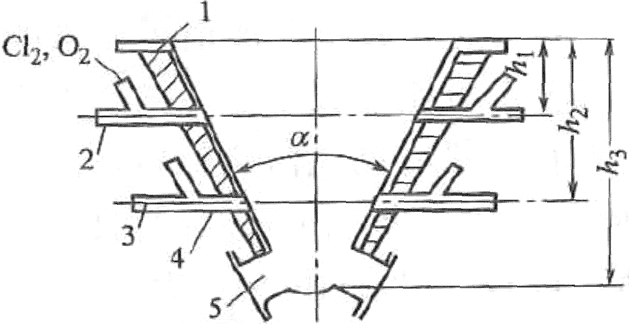
1 - Корпус печи; 2 - Очистное отверстие; 3 - Резиновая
заглушка; 4 - Сопло; 5 - Отверстие для выпуска шлака
с кипящим слоем
После успешного проведения пилотных испытаний эта технология получила широкое применение в Китае. Практически все производители TiCl4 в Китае, за исключением компании Jinzhou Titanium, внедрили эту технологию. Диаметр самого большого реактора кипящего слоя, использующего фурменную технологию, составляет 2,56 м. Однако, разработанная технология имеет некоторые недостатки.
1. Сложно добиться непрерывной работы. Реактор приходится периодически останавливать для удаления шлака.
2. В модернизированной технологии используется некальцинированный нефтяной кокс. Сопутствующие примеси в некальцинированном нефтяном коксе переходят в TiCl4 в виде субхлоридов, которые загрязняют конечный продукт - титановую губку. Расход газообразного хлора также выше, чем при традиционном хлорировании в кипящем слое и хлорировании расплавленными солями из-за использования некальцинированного нефтяного кокса и низкокачественного титанового шлака.
3. Тяжелые условия эксплуатации. Операция по удалению шлака трудоемка и связана с тяжелыми условиями труда.
Недостаточное внимание было уделено исследованиям и разработкам этой усовершенствованной технологии, что ограничивает дальнейшее масштабирование оборудования и производства. Вспомогательные процессы, включая очистку отходящих газов, конденсацию и рециркуляцию шлама, также остаются неоптимизированными. Для совершенствования технологии необходимо продолжение НИОКР.
В таблице 2.3 представлены характеристики аппаратов хлорирования титанового сырья [53]
Таблица 2.3
Россия, Украина, Казахстан | Китай | Япония | США | |
Сырье | Шлак с высоким содержанием CaO+MgO | Титановый шлак, рутил | Рутил | Рутил, титановый шлак |
Технология | Расплавное хлорирование | Кипящий слой, Расплавное хлорирование | Кипящий слой | Кипящий слой |
Размер аппарата | Круглый: 5 м Квадратный: 4,5x3,5x8,5 7x4x13 | Кипящий слой: 1 ~ 2,56 м Расплавное хлорирование: 5 м | 3 м 1,9 м | 3,05 м |
Производительность тонн TiCl4/день | 150 ~ 160 | 25 ~ 120 | 140 | 150 |
Температура хлорирования, °C | 700 ~ 750 | 800 ~ 1000 | 950 ~ 1050 | 950 ~ 1050 |
Расходные коэффициенты по титановому сырью, т/т TiCl4 | 0,49 | 0,5 ~ 0,55 | неизвестна | 0,49 |
Расходные коэффициенты по хлору, т/т TiCl4 | 0,87 ~ 0,9 | 0,9 ~ 1,2 | 0,9 | 0,9 |
Помимо TiCl4, отходящий газ хлоратора содержит хлориды других металлов (в виде паров или твердых частиц), твердые частицы, уносимые слоем, и неконденсирующиеся газы (CO/CO2), которые необходимо отделить перед использованием TiCl4 для получения металлического титана. Поведение примесей в процессе очистки в основном определяется различиями в летучести и температуре плавления.
Первая стадия очистки обычно заключается в конденсации высококипящих хлоридов металлов (например, FeCl2 и MnCl2), которые затем удаляются в сепараторе типа газ-твердое (циклоне или аналогичном оборудовании) вместе с большей частью уносимых твердых частиц (TiO2, кокс, SiO2). На этой стадии температура поддерживается выше точки кипения TiCl4, чтобы он оставался в парообразном состоянии.
Следующий этап - конденсация TiCl4 и отделение неконденсирующихся газов. Обычно это достигается двухступенчатым процессом, включающим конденсаторы с водяным и рассольным охлаждением. На этом этапе процесса получается неочищенный жидкий сырец тетрахлорида титана. Затем используются методы разделения жидкости и твердой фазы для дальнейшего удаления нерастворимых хлоридов металлов и других оставшихся твердых веществ.
Для удаления AlCl3 и VOCl3 требуются специальные методы обработки, поскольку их температуры кипения и растворимость в TiCl4 не позволяют эффективно удалять эти примеси дистилляцией. Хлористый алюминий преобразуется в нерастворимую форму путем добавления небольшого количества воды в газообразный TiCl4. Для обработки ванадия используются химические методы очистки. Недорогие органические материалы, такие как минеральные и растительные масла, являются предпочтительными вариантами, если TiCl4 предназначен для производства пигментов. Однако, на некоторых заводах по производству титановой губки, для очистки применяют медь и сероводород.
Растворенные газы (например, Cl2 и COCl2), низкокипящие хлориды (например, SiCl4 и SnCl4) и оставшиеся примеси с более высокими температурами кипения (например, FeCl3, AlCl3 и TiOCl2) окончательно удаляются методом ректификации. Таким образом, получают очищенный TiCl4 (99,99% масс.), пригодный для производства высококачественной титановой губки. В таблице 2.4 приведены характеристики основных примесей в TiCl4 различных производителей [54].
Таблица 2.4
Производитель | Максимальное содержание (ppm) | |||
Fe | Si | Sn | V | |
Oregon Metallurgical Corp. | 25 | 10 | 50 | 25 |
ПАО Корпорация "ВСМПО-АВИСМА" (марка OTT-0) | - | 2 | - | 2 |
TOHO Titanium Co., Ltd (Grade TLT-1) | 10 | 5 | 30 | 10 |
OSAKA Titanium Technologies Co., Ltd | 10 | 10 | - | 1 |
Titanium Dioxide Manufacturers Association <*> | 10 | 40 | 450 | 10 |
--------------------------------
В процессе восстановления - дистилляции получают металлический титан. Очищенный TiCl4 помещают в реактор, заполненный инертным газом (обычно аргоном), уже содержащим металлический Mg, и нагревают до 800 - 850 °C для проведения реакции восстановления TiCl4. Продуктами реакции являются MgCl2 и Ti, причем Ti образует твердую пористую структуру, называемую губкой, а MgCl2 - жидкость. Губка опускается на дно реторты, а расплавленный магний плавает на поверхности. Конечный продукт - металлический титан - представляет собой смесь чистого металла, металлического Mg и MgCl2. Для удаления металлического Mg и MgCl2 путем испарения применяется вакуумная дистилляция. Испаренный металлический Mg после конденсации, может быть, либо повторно использован непосредственно в процессе восстановления, либо отправлен в печь для очистки магния на заводе по восстановлению магния, а MgCl2 после конденсации направляется в электролизеры для восстановления металлического Mg и газообразного Cl2.
Существует два типа интегрированных реакторов восстановления-дистилляции: I-типа и U-типа с обратным расположением.
2.15.5.1 Полукомбинированный реактор I-типа
Реактор I-типа был разработан в Советском Союзе в 1971 году, рисунок 2.10. Для его эксплуатации требуется установка конденсатора и охлаждающей рубашки на восстановительный реактор после демонтажа трубопровода подачи TiCl4 по завершении реакции восстановления. Дистилляцию нельзя начать до завершения сборки конденсатора. Перед извлечением блока губчатого титана необходимо одновременно поднять и перевернуть как восстановительный сосуд, так и конденсатор. Для этого требуется очень большой кран и большое свободное пространство в здании завода. Производительность реактора I-типа существенно меньше по сравнению с реакторами U-типа. Как правило производительность аппарата составляет 4 - 5 т/партию. Эксплуатация технологии I-типа требует большого количества трудоемких ручных операций. Преимущество технологии I-типа заключается в простоте конструкции.
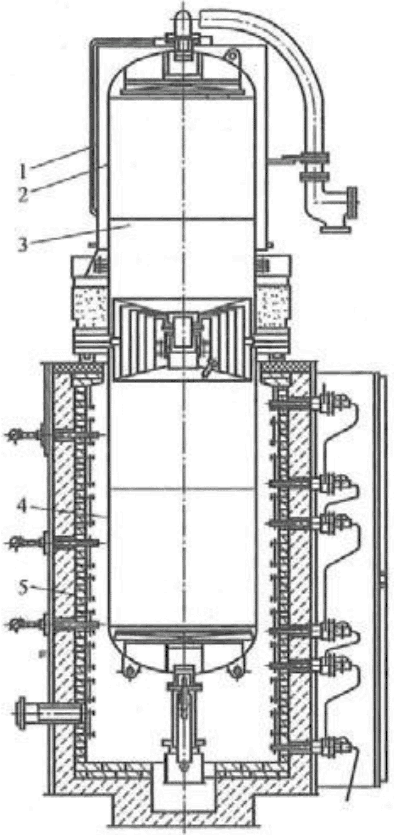
1 - Охлаждающая рубашка; 2 - Конденсатор; 3 - Сепаратор;
4 - Дистилляционный сосуд; 5 - Печь
с нижним выпуском
Технология I-типа применяется на заводах в России в ООО "АВИСМА" (дочернем хозяйственном обществе ПАО "Корпорация ВСМПО-АВИСМА") и ОАО "Соликамский магниевый завод", на Украине на Запорожском титаномагниевом комбинате, в Казахстане на Усть-Каменогорском титаномагниевом комбинате, а также в Китае на Pan Steel Titanium, Chaoyang Jinda и Jinzhou Titanium. Производительность реакторов на китайских фирмах соответственно составляет 7,5, 5 и 3 т за операцию. Реактор I-типа Pan Steel Titanium производительностью 7,5 т/партию, импортированный Запорожским институтом титана и магния в 2012 году, является самым передовым реактором I-типа в Китае.
2.15.5.2 Реактор обратного U-типа
Восстановительный сосуд и конденсатор расположены параллельно и на одном уровне в технологии обратного U-типа, а восстановительный сосуд соединен с конденсатором с помощью переходной трубы. Восстановительный сосуд может перейти к фазе дистилляции непосредственно путем открытия переходной трубы. Технология обратного U-типа более энергоэффективна и производительна по сравнению с технологией I-типа: выход высококачественной титановой губки выше. Самый большой на сегодняшний день реактор U-типа имеет производительность 12 тонн за операцию. Большая производительность, а также менее строгие требования к крану и компоновке оборудования, а также высокая производительность, низкие эксплуатационные расходы и лучшее качество продукта делают эту технологию более предпочтительной для производства губки. Губка высшего качества в основном производится по технологии обратного U-типа. На рисунке 2.11 ниже принципиальная схема восстановительно-дистилляционного реактора обратного U-типа.
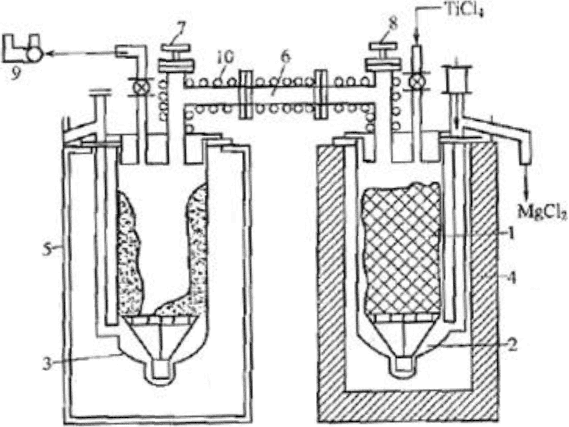
1 - Продукт восстановления; 2 - Сосуд восстановления
и дистилляции; 3 - Конденсатор; 4 - Нагреватель;
5 - Охладитель; 6 - Транспортная трубка; 7, 8 - Клапаны;
9 - Вакуумный насос; 10 - Трубчатый нагревательный элемент
типа "обратная U"
Реакторы обратного U-типа успешно применяются в Японии и США, их производительность достигает 10 тонн/партию, а конечный продукт обладает хорошей пористостью и превосходными химическими свойствами. Два завода в Японии и два в США являются производителями продукции высочайшего качества в мире и, пожалуй, самыми производительными. Китайские компании Zunyi Titanium и Luoyang Shuangrui Wanji разработали собственную технологию обратного U-типа с реакторами производительностью в основном 5, 8 и 10 тонн. В таблице 2.5 представлены рабочие параметры восстановительно-дистилляционных установок в разных странах [55].
Таблица 2.5
Россия | Китай | Япония, США | |
Тип реактора | I-типа | I-типа и U-типа | U-типа |
Производительность, т/операция | 4 ~ 5 | I-типа: 3, 5, 7.5; U-типа: 5, 8, 10, 12 | 10 |
Потребление электроэнергии кВт·ч/т Ti | 6000 | 5000 ~ 5500 | 2500 ~ 3000 |
Цикл производства, ч | 215 | 180 ~ 300 | 240 |
Выход марки A, % | 70 | 40 ~ 60 | 70 |
MgCl2, полученный на установке восстановительной дистилляции, затем направляется в электролизеры для получения металлического магния и газообразного хлора с использованием технологии электролиза расплавленных солей. Рециркуляция между производством титановой губки и электролизом магния снижает общие эксплуатационные расходы завода по производству титановой губки. Контроль качества магния производителем губки также максимально повышает его качественный потенциал, положительно влияя на чистоту получаемой титановой губки. Для электролиза хлорида магния применяются следующие типы ячеек электролизеров: монополярные ячейки на 62,5 кА, монополярные ячейки на 105 кА, монополярные ячейки на 120 кА и многополярные ячейки. Существующие ячейки для производства титановой губки включают монополярные ячейки на 110 кА, проточные ячейки на 200 кА и многополярные ячейки.
2.15.6.1 Монополярный электролизер 110 кА
Монополярный электролизер 110 кА создан на основе бывшего советского монополярного электролизера 105 кА, модернизированного китайским проектным институтом. Он был установлен на заводе Zunyi Titanium для обеспечения соответствия требованиям первой фазы производства титановой губки. Эта технология применяется на заводе Zunyi Titanium с 2001 года. Преимуществами электролиза являются простота эксплуатации, менее строгие требования к исходному сырью MgCl2 и возможность использования местных огнеупоров. Однако в 2013 году из-за спада на рынке титановой губки Zunyi Titanium пришлось закрыть и демонтировать производство первой фазы электролиза магния. С тех пор монополярные электролизер 110 кА в Китае не использовались.
2.15.6.2 Проточный электролизер 220 кА
Проточный электролизный цех состоит из 15 - 30 электролизных ванн. Целью является обеспечение централизованной загрузки сырья и выпуска металлического магния с использованием высокоэффективного оборудования и автоматизации. Ожидается повышение производительности на 150%, снижение энергопотребления до 13 500 кВт·ч/т магния и повышение эффективности по току до 80%.
Компании Pan Steel Titanium и Jinchuan Titanium приобрели у Запорожского института титана и магния технологию проточного электролиза, однако ни одна из них не смогла успешно запустить электролизную установку. Jinchuan Titanium решила отказаться от использования многополярных ячеек, а Pan Steel Titanium в настоящее время испытывает трудности с вводом их в эксплуатацию.
2.15.6.3 Многополярный электролизер 90 - 165 кА
Многополярный электролизер был разработан компанией Alcan для снижения энергопотребления при электролизе магния. Он широко используется в Японии и Америке для производства титановой губки. Многополярные электролизеры, также известные как биполярные электролизеры, по сути, аналогичны традиционным монополярным электролизерам, но между анодом и катодом вставлен проводник. Это значительно повышает производительность и энергоэффективность электролизера.
Первый многополярный электролизер в Китае был создан в 2008 году компаниями Zunbao Titanium (филиал Zunyi Titanium) и Luoyang Shuangrui Wangji. Сейчас эта технология становится самой популярной в Китае. Большинство производителей титановой губки, имеющих мощности по электролизу магния, выбирают многополярные электролизер.
Преимущества многополярного электролизера включают: отсутствие отходящих газов со стороны катода, меньшее окисление металлического магния благодаря защите аргоном; более высокую концентрацию газообразного хлора (более 95%); и небольшое количество шлама, образующегося в процессе эксплуатации, благодаря превосходным уплотнениям и защитному газу. В этом случае процесс удаления шлама минимизируется, а производительность почти в три раза выше, чем у традиционного монополярного электролизера.
Однако высокие инвестиции в многополярные ячейки создают дополнительную нагрузку на производителей титановой губки. Строительство одной многополярной ячейки оценивается от 3 000 000 до 3 500 000 юаней. Многополярные ячейки приходится перестраивать каждые 24 месяца из-за накопления шлама, на долю которого приходится 10 - 12% эксплуатационных расходов на тонну металлического магния. Однако, жизненный цикл многополярных ячеек в других странах мира обычно составляет 36 - 48 месяцев.
Таблица 2.6
Технология электролиза магния в разных странах [56]
Россия | Китай | Япония, США | |
Технология | Моно-полярный | Моно-полярный, мульти-полярный | Мульти-полярный |
Сила тока, А | 175 | Моно-полярный: 105 ~ 120 Мульти-полярный: 129 | 165 |
Производительность по Mg, т/д | 1,525 | Моно-полярный: 1,05 Мульти-полярный: 3,4 | 3,65 |
Производительность по хлору т/т Mg | 2,8 | Моно-полярный: 2,75 Мульти-полярный: 2,9 | 2,9 |
Потребление электроэнергии кВт·ч/т Mg | 12700 | Моно-полярный: 15230 ~ 16350 Мульти-полярный: 11000 ~ 12000 | 10500 |
Выход по току, % | 78 ~ 80 | Моно-полярный: 60 ~ 70 Мульти-полярный: 75 ~ 80 | 80 |
Концентрация хлора, % | 89 | Моно-полярный: 60 ~ 70 Мульти-полярный: 95 | 95 |
Жизненный цикл, мес. | 24 | Моно-полярный: 28 Мульти-полярный: 24 | 36 ~ 48 |
Около 40% мирового выпуска титановой губки осуществляет Китай, что делает его лидером по производству титана. Большая часть мощностей по производству губки в Китае используется при изготовлении промышленной продукции, и только 10% титана соответствует спецификациям для применения в аэрокосмической отрасли. Существенным недостатком, связанным с быстрым ростом производства, является то, что более 70% производителей губки в Китае работают по так называемому "полуфабрикату", то есть завод по производству титановой губки был построен без хлорирования и электролиза магния с целью минимизации инвестиций. Однако качество магния, а также тетрахлорида титана, оказывает существенное влияние на качество губки. Кроме того, объемы сбыта MgCl2 ограничены, и получаемый в результате процесса MgCl2 в основном отправляется на свалки, что делает процесс производства губки очень дорогим. Китай стремится занять значительную долю на международном рынке высококачественного титана для аэрокосмической промышленности, вытеснив с него других производителей. По прогнозам Airline Monitor в период с 2013 по 2035 год будет размещено 45 300 заказов на новые самолеты Боинг и Эйрбас. Поэтому Китай прикладывает все возможные усилия для повышения качества титановой губки.
С целью сохранения позиции России на международном рынке титана отечественным производителям необходимо осуществить модернизацию производств и за счет этого понизить производственные затраты. Используемые технологии отечественных производителей титана были разработаны в 60-х годах прошлого века. Вопросам экологии в то время уделялось недостаточное внимание, главной задачей являлось в кратчайшие сроки нарастить объемы производства титана.
Благодаря внедрению нового способа хлорирование титанового шлака в среде расплава хлористых солей была решена задача по увеличению объемов и удешевлению производства титана, что позволило обеспечить потребности в этом металле развивающихся химической, машиностроительной, атомной, авиационной и др. отраслей промышленностей. Построенные в советское время титаномагниевые комбинаты продолжают свою работу и по сегодняшний день. При этом за прошедшие с момента запуска производств годы серьезных модернизаций технологии выпуска металлического титана не происходило. С точки зрения воздействия на окружающую среду отечественная технология производства титана является устаревшей и не соответствует современным требованиям в этой области. В результате сбросов очистных сооружений периодически фиксируются случаи загрязнения водоемов и почв солевыми стоками титанового производства, которые по своим масштабам квалифицируются как экологическая катастрофа.
Кроме того, в процессе производства образуется значительное количество твердых отходов - нерастворимых остатков отработанного расплава титановых хлораторов (НО ОРТХ). Ежегодно в России на полигонах захоранивается около 10 тыс. тонн НО ОРТХ. Безусловно данный вид отходов представляет опасность для окружающей среды, поскольку, НО ОРТХ содержит соли тяжелых металлов. Попадая в почву и грунтовые воды по пищевой цепочке тяжелые металлы концентрируются в продуктах питания местного производства.
Другим видом загрязнений титановых производств являются выбросы парниковых газов. Сырьем для производства металлического титана являются ильменитовые концентраты, которые подвергаются восстановительной рудотермической плавке для получения титанового шлака. В результате восстановления оксидов металлов углеродом выделяется диоксид углерода, который сбрасывается в атмосферу. Кроме того, образование углекислого газа наблюдается и в процессе приготовления известкового молока. Последнее применяется на производстве для нейтрализации кислых стоков и очистки сбрасываемых сточных вод от растворенных примесей металлов. В качестве сырья для приготовления известкового молока на производстве применяют известняк. В результате обжига известняка происходит его разложение, протекающее с выделением диоксида углерода. Для проведения обжига используют тепло, полученное в результате сгорания природного газа. Совокупный объем выбросов диоксида углерода от сгорания метана, разложения известняка, а также процесса получения титанового шлака составляет около 100 тыс. тонн в год.
Кроме проблемы загрязнения окружающей среды перед производителями титана в последнее время встал вопрос сырьевого обеспечения предприятий. Отечественная технология производства титана была рассчитана на использование в качестве сырья ильменитовых концентратов Иршанского и Вольногорского горно-обогатительных комбинатов. После распада СССР эти предприятия оказались на территории современной Украины. Ни одно из отечественных месторождений титановых руд в промышленном масштабе до настоящего момента времени освоено не было. В результате Российская титановая отрасль все эти годы была вынуждена работать на импортном титановом сырье. В июле 2021 г. Украина ввела санкции на поставку титановых концентратов в нашу страну, в результате поставки сырья были полностью остановлены.
В сложившейся ситуации восполнить дефицит титанового сырья за счет импорта является сложной задачей. При поддержке правительства китайский производитель пигментного диоксида титана Lommon Billions поставил перед собой задачу занять первое место по количеству выпускаемого пигментного диоксида титана в мире. Китай не обладает требуемыми для достижения поставленной цели мощностями по добыче и обогащению титановых руд. В результате практически все доступное на мировом рынке титановое сырье скупается китайскими предприятиями. В результате в России возник дефицит титанового сырья в размере 240 - 260 тыс. тонн в год. Надежным решением сложившейся ситуации является заместить импорт титанового сырья и в кратчайшие сроки освоить собственную минерально-сырьевую базу титана.
Проблема модернизации технологии производства титана по методу магниетермического восстановления тетрахлорида титана во многом связана с усовершенствованием способа получения последнего. Как известно, получение тетрахлорида титана из титановых шлаков является одним из наиболее наукоемких и сложных переделов в производстве титана.
Из-за токсичности твердых хлоридных отходов производство титана не соответствует современным требованиям экологически чистых производств. Решение проблемы возможно осуществить по двум взаимодополняющим направлениям. Основное - это снижение содержания примесей в исходном титановом сырье. Данное направление является основным при промышленном производстве тетрахлорида титана за рубежом. Применение титанового сырья с низким содержанием примесей в отечественной технологии производства металлического титана позволит:
- отказаться от энергоемкой рудотермической плавки и за счет этого существенно повысить энергоресурсоэффективность технологии, а также устранить выбросы углекислого газа, связанные с проведением этой стадии;
- уменьшить углеродный след стадии хлорирования, а также сократить потери хлора и углерода, связанные протеканием побочных реакций хлорирования примесей титанового шлака;
- существенно сократить объем образующихся твердых отходов и жидких стоков за счет уменьшения кратности обновления расплава титановых хлораторов, а также уменьшить выброс углекислого газа образующегося в процессе обжига извести, используемой для очистки солевых стоков;
- повысить выход технического тетрахлорида титана и уменьшить расходный коэффициент по углероду, за счет снижения потерь сырья при выпуске отработанного расплава.
Таким образом переработка титанового сырья с минимальным содержанием примесей способствует не только сокращению образования хлоридных отходов производства и уменьшению углеродного следа, но также повышает энергосбережение и эффективность использования ресурсов.
Предварительные расчеты показали, что переработка сырья, содержащего 93 - 95% TiO2 позволит сократить выбросы диоксида углерода в окружающую среду более чем в два раза. Таким образом, становится понятным, что для достижения целей устойчивого развития РФ отечественная титановая отрасль должна перейти на использование высококачественного титанового сырья, характеризуемого минимальным содержанием примесей. Данное обстоятельство следует учитывать при выборе первоочередного для освоения отечественного месторождения титановой руды для обеспечения потребностей предприятий титановой отрасли. Ильменитовые концентраты отечественных месторождений характеризуются относительно низким содержанием диоксида титана (45 - 55%) и высоким содержанием примесей таких как оксиды железа, хрома, марганца и магния. Для сравнения ильменитовые концентраты украинского производства, до недавнего времени применявшиеся отечественными предприятиями, имеют содержание диоксида титана на уровне 63 - 65%. Для поддержания проектных мощностей по выпуску титана, в случае использования бедных концентратов, производителям придется построить и ввести в эксплуатацию дополнительные печи рудотермической плавки для получения требуемых объемов титанового шлака. Это неизбежно приведет к увеличению выбросов диоксида углерода в окружающую среду. С другой стороны, из низкокачественных ильменитовых концентратов будет получаться титановый шлак с высоким содержанием примесей и относительно низким содержанием диоксида титана. В результате хлорирования подобного шлака возрастет объем выбросов углекислого газа, а также жидких и твердых отходов в окружающую среду. Таким образом становится понятным, что при выборе первоочередного для освоения месторождения следует ориентироваться не только на изученность месторождения, развитую инфраструктуру и логистическую доступность до основных потребителей титанового сырья, но и высокое качество титанового концентрата.
Полностью обеспечить потребность России в высококачественном титановом сырье возможно за счет вовлечения в промышленную разработку Ярегского нефтетитанового месторождения (республика Коми). Месторождение обладает колоссальные запасами титановой руды в количестве 2300 млн тонн, что составляет около 50% балансовых запасов России. В них 640 млн тонн по самой высокой, доказанной категории A+B+C1, обеспечивающих промышленное освоение месторождения и полное обеспечение потребности России в титановом сырье более чем на сто лет вперед.
В состав лейкоксен-кварцевых нефтеносных песчаников входит 6 - 9% тяжелой нефти, 10 - 12% TiO2 и около 80% SiO2. Минеральный состав представлен лейкоксеном, кварцем, гидроксидами железа, сидеритом, слюдистыми минералами. Главным носителем титана является лейкоксен - минерал своеобразного состава. Он представляет собой минеральную структуру тонкого срастания рутила и кварца, в которой рутил образует тонкую игольчатую сетку толщиной 1 - 5 микрон.
Технология выделения нефти из лейкоксен-кварцевых нефтеносных песчаников включает в себя стадию флотационного обогащения, которая обеспечивает получение коллективного нефтетитанового концентрата. На следующей стадии производится экстракция нефти с последующим выделением товарной обезвоженной нефти методом ректификации. Образующийся при этом кварц-лейкоксеновый концентрат содержит 53,2% TiO2, 41,3% SiO2, 2,9% Al2O3, 1,6% Fe2O3 и 1% прочих примесей. Дальнейшее обогащение концентрата возможно осуществить гидрометаллургическим способом путем выщелачивания примесей оксидов кремния и алюминия концентрированными растворами гидроксида натрия. Процесс растворения примесей проводится при температуре 180 - 200 °C в реакторах под давлением (автоклавах), в результате образуется раствор метасиликата натрия и автоклавный концентрат. Обогащенный продукт состоит из 94,5% TiO2, 2,0% SiO2, 1,3% Al2O3, 1,8% Fe2O3 и 0,4% прочих примесей. Минеральный состав концентрата представлен рутилом, кварцем и измененными в процессе выщелачивания алюмосиликатами железа и магния.
Автоклавный концентрат обладает целым рядом технологических преимуществ перед традиционным для титановой отрасли титановым шлаком. Автоклавный концентрат содержит практически в три раза меньшее количество примесей и пригоден для переработки методом хлорирования без проведения каких-либо дополнительных операций. Кроме того, автоклавный концентрат имеет более простой состав примесных соединений. В концентрате содержатся всего четыре основных компонента против семи соединений, составляющих титановый шлак. В концентрате полностью отсутствуют примеси оксидов марганца, хрома, а содержание оксида ванадия (V2O5) составляет всего 0,07%. Для сравнения, в титановом шлаке концентрация оксида ванадия составляет 0,32%, т.е. выше более чем 4,5 раза. Данное обстоятельство имеет критическое значение для технологии хлорирования.
В существующем процессе хлорирования титанового шлака и последующей утилизации расплава создаются условия, при которых возможно образование шестивалентного хрома Cr (VI). Предельно допустимая концентрация шестивалентного хрома в водоемах составляет всего 0,001 мг/л и относится к категории чрезвычайно опасных веществ. Поэтому наличие хрома в титановом сырье обуславливает необходимость производить дорогостоящую очистку сточных вод от этого соединения. Автоклавный концентрат не содержит хром, что существенно упрощает задачу по регенерации отработанного расплава для его повторного использования.
Образующийся в результате хлорирования титанового сырья, оксихлорид ванадия (VOCl3) выделяется совместно с сырцом тетрахлорида титана. Разница температур кипения оксихлорида ванадия и тетрахлорида титана составляет менее 10 °C. По этой причине рафинирование TiCl4 не может быть осуществлена методами ректификационной-дистилляционной очистки. Поэтому предварительно проводят очистку от соединений ванадия химическим способом. Для этого сырец тетрахлорида титана при нагревании обрабатывают активным медным порошком. Это существенно усложняет и удорожает процесс очистки тетрахлорида титана. Сырец тетрахлорида титана, произведенный из автоклавного концентрата, будет иметь содержание оксида ванадия на порядок меньше своего аналога, полученного из титанового шлака, что существенно упрощает схему рафинирования тетрахлорида титана.
Таким образом использование автоклавного концентрата в качестве сырья для получения металлического титана позволит произвести импортозамещение титанового сырья и устранит выбросы углекислого газа, а также твердых отходов и солевых стоков в окружающую среду, а также повысить энергосбережение и эффективность использования ресурсов.
Технологии получения вольфрама
Непосредственная первичная переработка вольфрамовых и молибденовых концентратов, за исключением случаев выплавки ферросплавов, проводится с целью получения из них соответствующих триоксидов, которые используются при производстве металлических вольфрама и молибдена, и их карбидов.
Выбор метода переработки концентратов зависит, в первую очередь, от их вида и минералогического состава. Вольфраму и молибдену свойственны максимальная степень окисления +6 и ее устойчивость для большинства химических соединений при малой вероятности существования простых катионов. Более низкие степени окисления наблюдаются преимущественно в условиях стабилизации комплексообразования. Кроме того, при выборе метода учитываются масштабы производства, технические требования к чистоте и физическим качествам получаемых триоксидов и некоторые технико-экономические показатели процессов.
Вольфрам - светло-серый металл, по виду очень похожий на сталь. По тугоплавкости он уступает только углероду и является самым прочным металлом. Прочность он сохраняет и при высоких температурах. Вольфрам практически нелетуч. Вольфрам отличается высокой химической стойкостью при нормальных условиях. На воздухе при обычной температуре он не взаимодействует с соляной, серной, азотной и фтористоводородной кислотами, устойчив к действию гидроксидов щелочных металлов растворяется только в смеси азотной и фтористоводородной кислот.
С кислородом воздуха вольфрам начинает взаимодействовать при нагреве до температуры 400 - 500 °C с образованием триоксида вольфрама (WO3).
В промышленной практике используют различные технологические схемы переработки концентратов с содержанием 30 - 50% WO3 и промпродуктов - 10 - 20% WO3. Промпродукты, выведенные из цикла обогащения труднообогатимых руд, перерабатываются на искусственный шеелит гидрометаллургией. Комбинированные схемы обеспечивают высокое извлечение вольфрама из таких руд. Полученный триоксид вольфрама служит исходным материалом для производства вольфрама, карбида вольфрама или других продуктов.
Выбор схемы зависит от типа и состава концентратов, масштаба производства, требований к чистоте и физическим характеристикам триоксида вольфрама.
Главным в технологической схеме является способ разложения концентрата. Известные способы разделяются на группы по виду полученных в результате разложения растворов:
- для получения растворов вольфрамата натрия используют способы с применением соды, щелочей, нейтральных солей (NaF, NaNO3 и др.). Из растворов после очистки от примесей выделяют малорастворимые соединения вольфрама или извлекают вольфрам методом экстракции или ионного обмена (сорбции);
- для получения осадков технической вольфрамовой кислоты применяют способы разложения кислотами (HCl, HNO3). Полученную техническую вольфрамовую кислоту растворяют в аммиачной воде и выделяют из раствора паравольфрамат аммония или вольфрамовую кислоту;
- при хлорировании вольфрамового сырья хлором или его соединениями возгоняют летучие хлориды и оксохлориды вольфрама. Гидролитическим разложением конденсата хлоридов и оксохлоридов получают вольфрамовую кислоту.
Самый распространенный в промышленной практике и универсальный способ разложения вольфрамитовых и шеелитовых концентратов - спекание с содой. Процесс ведется при температуре 800 - 900 °C во вращающихся трубчатых печах. Шихта составляется с избытком соды на 10 - 20% для вольфрамитовых концентратов и с избытком 80 - 100% от стехиометрического для шеелитовых, а также кварцевого песка. Степень разложения при этом составляет более 99%. Данная технология применялась на Скопинском ГМЗ.
Электротермический способ разложения шеелитовых концентратов - плавка шихты при 1400 - 1500 °C в электропечи - обеспечивает степень вскрытия 98%, высокую производительность, меньший расход реагентов (соды и кремнезема), меньший объем пульпы. Однако требует высокого расхода электроэнергии 1100 кВт·ч на 1 т концентрата и ведет к потерям вольфрама со шлаком.
Автоклавно-содовый способ разложения широко используется на отечественных заводах, а также в США, Японии, Великобритании, Германии, Австрии. Преимущества автоклавно-содового способа разложения вольфрамового сырья перед спеканием состоят в исключении печного процесса, предшествующего выщелачиванию, и меньшем содержании примесей в вольфраматных растворах. Кроме того, способ применим к вскрытию не только стандартных концентратов, но и низкосортных промпродуктов и хвостов обогащения, содержащих 4 - 5% WO3.
При разложении шеелитовых концентратов степень извлечения вольфрама в раствор достигает 98,6 - 99,5%, содержание вольфрама в отвальных хвостах не превышает 1%. Для вольфрамитовых концентратов показатели несколько ниже.
В отечественной практике автоклавно-содовая схема применяется на Нальчикском ГМЗ.
При переработке низкокачественного сырья за рубежом отдается предпочтение автоклавно-содовой схеме, а для высококачественных концентратов используется кислотное вскрытие, являющееся в этом случае более экономичным из-за короткого производственного цикла.
Переработка растворов вольфрамата натрия, содержащих 60 - 150 г/л WO3, с получением триоксида вольфрама требуемой чистоты, по традиционной технологии включает; очистку от примесей кремния, фтора, фосфора, мышьяка, железа, молибдена; осаждение искусственного шеелита, разложение его кислотами с получением осадка технической вольфрамовой кислоты; растворение вольфрамовой кислоты в аммиачной воде и выделение из растворов паравольфрамата аммония методом выпарки (термическим разложением получают триоксид вольфрама).
Существенное упрощение многостадийной схемы переработки растворов вольфрамата натрия достигается при извлечении вольфрама методом экстракции с последующей реэкстракцией растворами аммиака и выделением из аммиачных растворов паравольфрамата аммония. Экстракционная технология используется на предприятиях США и освоена в России. Для экстракции используются третичные амины и четвертичные аммониевые основания.
Применение ионообменных смол - конкурирующее с экстракцией направление совершенствования схемы переработки вольфраматных растворов. К преимуществам применения смол следует отнести отсутствие сбросных растворов, содержащих органические примеси, пожаробезопасность, нетоксичность смол.
Основной промышленный способ получения порошков вольфрама - восстановление триоксида металла водородом. Высокотемпературное восстановление водородом проводят в горизонтальных многотрубных печах, имеющих несколько зон нагрева, температура в которых регулируется автоматически. Эти печи могут быть проходными или садочными.
Технология получения вольфрама из вторичного сырья
Поскольку первичных ресурсов вольфрама недостаточно для удовлетворения спроса при производстве современных материалов, все большее значение для промышленности приобретает его извлечение из вторичных ресурсов, таких как отработанные катализаторы гидрокрекинга тяжелых нефтяных дистиллятов и гидроочистки дизельных фракций с повышенным содержанием полиароматических соединений, состава NiMoW и NiWS, шлифотходы и лом вольфрамовых сплавов.
Вольфрамовые сплавы подразделяются на тяжелые сплавы и твердые. К тяжелым относятся сплавы на основе W-Ni-Fe и W-Ni-Cu (ВК, ТК и ТТК), применяемые для изготовления боеприпасов, контейнеров для хранения радиоактивных изотопов, роторов гироскопов, в элитном спортинвентаре и др.
Твердые сплавы на основе карбида вольфрама WC применяются для изготовления режущих инструментов. К ним относятся сплавы ВНЖ, ВНМ, ВД и ВМ.
Основой метода получения высокочистого оксида вольфрама из техногенных отходов является процесс жидкостной экстракции из растворов содового выщелачивания, который позволил существенно сократить расход материалов и основные стадии технологии. Раствор вольфрамата натрия подвергали экстракционной очистке, который после кристаллизации подвергали сушке.
На данный момент технология прошла испытания, получены опытные образцы продукции - паравольфрамата аммония. Содержание основного вещества W составило 99,9%. Этот продукт также является высококачественным сырьем для производства металлического вольфрама, используемого в микроэлектронике и электротехнике.
Технологии получения молибдена
По механической прочности молибден уступает только вольфраму, но легче его поддается обработке давлением.
При переработке молибденовых концентратов первичная цель - получение триоксида. Основным и практически единственным промышленным способом первоначальной обработки молибденитовых концентратов является окислительный обжиг, в результате которого происходит окисление молибденита с образованием огарка, загрязненного примесями.
Для получения чистого оксида молибдена применяют либо метод возгонки триоксида молибдена, либо химическую переработку огарка.
Основной промышленный способ получения порошков молибдена - восстановление триоксида металла водородом.
В производстве металлического молибдена используется металлургическое оборудование, аналогичное оборудованию в производстве металлического вольфрама.
Основной, широко применяемый в промышленной практике способ разложения молибденитовых концентратов - окислительный обжиг. Продукт обжига - огарок, содержащий триоксид молибдена и примеси в заданных пределах, поступает на выплавку ферромолибдена или служит исходным материалом для производства химических соединений, наиболее чистое по примесям, из которых - триоксид молибдена. Переработка огарка может проводиться способом возгонки, однако наиболее распространены гидрометаллургические схемы переработки огарка.
В заводской практике обжиг молебденитовых концентратов проводят в печах "кипящего слоя" (КС). Обжиг в КС позволяет получать огарки с высоким содержанием выщелачиваемого в растворах аммиака молибдена, поддерживать строго определенный интервал температур 560 - 580 °C, не допуская спекания материала и взаимного контакта материала, предотвращая образование молибдатов.
Организация обжига концентратов с целью получения огарков, кондиционных по сере и пригодных для выплавки ферромолибдена, требует создания установки двухступенчатого обжига. Вторая стадия обжига обеспечивает дожигание серы во вращающихся трубчатых печах до содержания менее 0,2%. Эта технология разработана институтом "Гинцветмет" и прошла опытно-промышленные испытания.
Получение чистого триоксида молибдена из огарков ведется гидрометаллургическим аммиачным способом. Огарок выщелачивают раствором аммиака, из аммиачного раствора после очистки от примесей выделяют молибден в форме парамолибдата или полимолибдатов. Триоксид молибдена получают термическим разложением парамолибдата аммония.
В производственной практике термическое разложение парамолибдата аммония проводят при температуре 450 - 500 °C в трубчатых печах непрерывного действия с электрообогревом с получением чистого триоксида молибдена.
В промышленную практику внедрен гидрометаллургический способ разложения азотной кислотой. Пульпа, состоящая из концентрата и 30 - 35%-ной азотной кислоты, проходит выщелачивание в последовательно установленных пачуках при перемешивании сжатым воздухом и нагреве острым паром до температуры 90 - 100 °C.
Молибден извлекают из кислых маточных растворов, используя различные способы сорбции или экстракции.
За рубежом применяется автоклавный способ окисления молибденита кислородом. Процесс ведется в автоклаве при температуре 120 - 160 °C и давлении кислорода 0,1 - 0,14 МПа (10 - 14 ат). Прямое извлечение молибдена в триоксид по этому способу 90%, в кислых пульпах содержание серной кислоты составляет 75%, в циркулирующем растворе повышается концентрация рения. Переработка медно-молибденовых ренийсодержащих промпродуктов в настоящее время осуществляется по схеме окислительного обжига с возгонкой рения, содового выщелачивания обожженного продукта с последующим выделением из растворов молибдата кальция. Возогнанный рений улавливается в мокрой системе очистки газов и затем извлекается по сорбционной схеме в товарный перренат аммония. Окислительно-автоклавное выщелачивание растворами соды и едкого натра при температуре 160 - 180 °C, парциальном давлении кислорода 1 - 2 ат, отношении Ж:Т = 1:8 и продолжительности 14 - 17 ч обеспечивает извлечение в раствор молибдена и рения до 98%. Экстракционные методы извлечения молибдена и рения с последующим получением парамолибдата и перрената аммония обеспечивают извлечение из исходного сырья 96% молибдена и около 90% рения.
Для выбора способа переработки вовлекаемого в производство сырья необходимо учитывать качество исходного материала, наличие примесей, лимитирующих выбор конечной продукции, а также имеющиеся производственные мощности.
Технология получения молибдена из вторичного сырья
Для производства дизельного топлива Евро-5 на российских нефтеперерабатывающих предприятиях широко используют катализаторы глубокой очистки, произведенные на базе соединений молибдена, кобальта и никеля. В 2020 году в России общий объем потребления катализаторов крекинга, гидроочистки и гидрокрекинга составил более 17,5 тыс. т. Срок службы таких катализаторов, в зависимости от многих факторов, варьирует от полугода до трех лет. Они являются опасными отходами II - III класса и не подлежат захоронению в грунт. Отработанные катализаторы содержат до 10 - 25% молибдена и 2 - 5% кобальта и никеля. В России ежегодно отправляются на складирование около 4,0 - 4,5 тыс. т отработанных катализаторов гидроочистки. Это порядка 700 т оксида молибдена.
ООО "ЛИТ" (ГК "Скайград") разработало технологию переработки отработанных катализаторов гидроочистки с получением оксида молибдена (MoO3 - 99,9%). В основе метода получения высокочистого оксида молибдена из техногенного отхода и очистки от примесей лежит процесс жидкостной экстракции из растворов содового выщелачивания, который позволил существенно сократить расход материалов и основные стадии технологии. Перед выщелачиванием отработанный катализатор гидроочистки отжигали в трубчатой печи с доступом воздуха при температуре 450 - 500 °C до остаточного содержания серы <= 0,8%, углерода <= 0,5%. Полученный раствор молибдата натрия подвергали экстракционной очистке с использованием смеси третичного амина (ТАА) с трибутилфосфатом (ТБФ) в углеводородном разбавителе с образованием в реэкстракте парамолибдата аммония, который после кристаллизации обжигали в печи с получением оксида молибдена (VI) [14]. На данный момент технология переработки использованных катализаторов Mo-Co марки KF-780 1,3Q прошла испытания на пилотной установке, включающей каскад центробежных экстракторов модели ЭЦ-10ФА производства ГК "Скайград", получены опытные образцы продукции - оксида молибдена (VI). Содержание основного вещества (MoO3) составило >= 99,9%. Образцы прошли предварительные испытания у основного Заказчика - ООО "Газпромнефть - Каталитические системы". Технология готовится к запуску в производство.
Этот продукт также является высококачественным сырьем для производства металлического молибдена, используемого в микроэлектронике и электротехнике.
Технология получения иттрия
Соединения иттрия получают из смесей с другими редкоземельными металлами экстракцией и ионным обменом. Металлический иттрий получают восстановлением безводных галогенидов иттрия литием или кальцием с последующей отгонкой примесей. Элементы иттриевой группы получают комбинированием способов дробного осаждения с ионообменной технологией, так как для такого элемента, как иттрий, продукция которого значительна, методы функционального осаждения все еще необходимы. Наряду с ионообменной технологией применяют способы дробного осаждения и кристаллизации и экстракции.
Чистый оксид иттрия можно получить ионным обменом, когда применяются 90 - 99%-ные концентраты иттрия, получаемые в результате отделения его в виде основных нитратов или другими методами.
Технология получения соединений скандия
Наиболее простые и эффективные схемы извлечения скандия связаны с комплексной переработкой различных руд и использованием технологических растворов - возвратных производственных растворов после извлечения урана [74, 75], технологического раствора фильтрации основного сульфата циркония при переработке циркона, где концентрация элемента составляет около 1,0 мг/л, но объемы растворов достигают нескольких десятков тысяч кубометров/сутки (вскрытие сырья не требуется). Концентрирование скандия с попутным отделением макроэлементов и получением чернового концентрата скандия проводят экстракцией либо сорбцией [49, 71, 75]. После проведения очистных операций возможно получение фторида или оксида скандия с содержанием основного вещества не ниже 99%.
Раствор гидролизной титановой кислоты производства пигментного диоксида титана (около 20 мг/л скандия) - сырьевой источник скандия ряда промышленных установок в мире по производству оксида скандия.
Переработка твердых сложных по составу скандийсодержащих промпродуктов и комплексных руд требует проведения выщелачивания, поэтому разработанные технологические схемы включают получение дополнительной продукции (железные пигменты и концентрат РЗЭ при переработке красных шламов [50].
Извлечение скандия при переработке комплексной руды New South Wales, Австралия (содержит гематит, лимонит, сапролит), включает получение соединений никеля и кобальта. С учетом большой мощности месторождения по скандию, разработана и реализуется в промышленном масштабе сложная технологическая схема переработки этой руды, запасы которой составляют 37 000 тонн по оксиду скандия. Технология включает предварительный обжиг руды, автоклавное сернокислотное выщелачивание, экстракцию, осаждение оксалата скандия и его прокаливание до оксида скандия.
Получение лигатуры Al - 2% Sc
Скандий - эффективный модификатор и лучший антирекристаллизатор алюминия и его сплавов. Положительное действие добавки скандия объясняется почти полным размерноструктурным соответствием структурной решетки алюминия и высокодисперсных интерметаллидов Al3Sc, которые оказывают не только модифицирующее и антирекристаллизационное воздействие на структуру, но и обеспечивают упрочнение сплава. Изготовление таких сплавов ведут с использованием лигатуры Al - 2% Sc.
Для получения алюминиево-скандиевой лигатуры в промышленности используют ряд методов. Метод алюминотермического восстановления фторида скандия разработан в АО ВНИИХТ Маширевым В.П. и освоен на Прикаспийском горно-металлургическом комбинате (г. Шевченко, Казахстан) в 1989 году [43]. Получение фторида скандия из его оксида осуществляли фторированием в никелевом фтораторе газообразным фтороводородом.
Другой метод, разработанный в НИТУ МИСиС под руководством проф. В.И. Москвитина, заключается в алюминотермическом восстановлении оксида скандия квалификации ОС-99,0 под слоем фторирующего флюса, т.е. исходным соединением также является фторид скандия [51]. Этот метод использован в России для получения лигатуры Al - 2% Sc в течение последних 20 лет.
Технические показатели на лигатуру скандия согласно ТУ 11-01-01-2001 представлены в таблице 2.7.
Таблица 2.7
ТУ 11-01-01-2001
Примесь | Содержание, %, не более |
Сумма примесей | 0,15 |
Fe | 0,05 |
Si | 0,05 |
Cu | 0,01 |
Mn | 0,01 |
Mg | 0,01 |
Сумма РЗЭ | 0,01 |
F | 0,01 |
В небольших количествах получают металлический скандий марки СКМ-1 и СКМ-2 и дистиллированный скандий высокой чистоты. При этом применяют кальциетермическое восстановление фторида скандия в танталовом тигле в индукционной печи и инертной атмосфере при температуре 1550 - 1600 °C, натриетермическое восстановление в вакууме хлорида скандия и литиетермию.
Нормы содержания примесей в металлическом скандии по ТУ 48-4-483-87 представлены в таблице 2.8.
Таблица 2.8
по ТУ 48-4-483-87
Примесь, в пересчете на оксид | Содержание примеси, % | |
СКМ-1 | СКМ-2 | |
Fe | 0,03 | 0,06 |
Al | 0,01 | 0,01 |
Ca | 0,03 | 0,06 |
Cu | 0,01 | 0,01 |
Si | 0,02 | 0,05 |
Mg | 0,01 | 0,02 |
Y | 0,01 | 0,01 |
Yb | 0,01 | 0,01 |
Zr | 0,01 | 0,01 |
Ti | 0,01 | 0,02 |
Предпочтение часто отдается восстановлению фторида скандия благодаря отсутствию у него гигроскопичности, т.к. ScCl3 образует кристаллогидраты и гидролизуется в собственной кристаллизационной воде.
2.20.1 Получение групповых концентратов РЗЭ из различного типа минерального сырья
Соединения РЗЭ получают из концентратов, выделенных из минерального сырья. Известно более 100 редкоземельных минералов, образованных оксидами, фосфатами, карбонатами, силикатами, фторидами РЗЭ. В настоящее время промышленное значение имеют только некоторые из РЗЭ минералов. Это прежде всего фосфаты - монацит (CePO4), ксенотим (YPO4), фтор-карбонаты - бастнезит (CeCO3F), иттросинхизит (YCa(CeCO3)2F), сложный оксид - лопарит (NaCeTi2O6). Промышленным источником РЗЭ являются также минералы коры выветривания гранитов, в которых РЗЭ в ионной форме адсорбированы на поверхности частиц.
Потенциальным промышленным минеральным сырьем, подлежащим переработке для выделения суммы РЗЭ, является гадолинит, содержащий до 50 масс. % суммы оксидов Ln2O3, гагаринит (до 40), иттрофлюорит (до 40), эвдиалит (2), апатит (до 10) и некоторые другие. Для каждого вида минерального сырья различается не только общее содержание суммы РЗЭ, но и состав или содержание каждого индивидуального РЗЭ.
При переработке перечисленных видов сырья получают концентраты РЗЭ, причем состав каждого такого концентрата соответствует составу РЗЭ в минералах (при условии количественного выделения РЗЭ). Эти концентраты (как правило, РЗЭ в них находятся в виде оксидов или карбонатов) используют как основное исходное сырье для разделения на промежуточные концентраты или на индивидуальные элементы. Содержание отдельных РЗЭ в исходном концентрате будет определять в значительной степени стратегию разделения и выбор соответствующей экстракционной системы. В таблицах 2.9 - 2.10 представлены составы РЗК основных промышленно перерабатываемых руд, добываемых в Российской Федерации, и для сравнения в Китае - основном производителе редкоземельных соединений для промышленного производства изделий из РЗЭ.
Таблица 2.9
РЗЭ | La | Ce | Pr | Nd | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Y |
Лопарит, Ловозерское месторождение | |||||||||||||||
Содержание, % вес. | 25 | 54 | 5 | 14 | 0,9 | 0,08 | 0,56 | 0,37 | 0,12 | 0,08 | 0,016 | 0,003 | 0,008 | 0,002 | 0,008 |
Апатит | |||||||||||||||
Содержание, % вес. | 26,3 | 44,5 | 4,3 | 15,4 | 2,4 | 0,48 | 1,8 | 0,21 | 0,74 | 0,16 | 0,21 | 0,01 | 0,1 | 0,02 | 3,3 |
Красноуфимские монацитовые концентраты, в пересчете на оксиды | |||||||||||||||
Содержание, % вес. | 24,6 | 43,0 | 5,5 | 20,5 | 2,0 | 0,2 | 1,1 | 0,7 | 0,3 | 0,1 | 0,3 | 0,1 | 0,05 | 0,1 | 1,4 |
Eu - монацит | |||||||||||||||
Содержание, % вес. | 19,7 | 45,6 | 4,7 | 21,7 | 3,7 | 0,88 | 2,17 | - | 0,14 | 0,31 | 0,16 | - | 0,5 | - | 0,38 |
Гагаринит, Катугинское месторождение | |||||||||||||||
Содержание, % вес. | 2,6 | 9,5 | 1,7 | 7,9 | 3,3 | 0,2 | 7,1 | 1,1 | 9,3 | 1,4 | 5,2 | 1,0 | 3,8 | 0,7 | 45,2 |
Иттрофлюорит, Катугинское месторождение | |||||||||||||||
Содержание, % вес. | 4,7 | 12,1 | 1,7 | 6,5 | 2,6 | 0,2 | 4,7 | 0,4 | 6,9 | 0,9 | 5,2 | 1,1 | 5,6 | 1,2 | 46,2 |
Эвдиалит | |||||||||||||||
Содержание, % вес. | 13,5 | 29,1 | 3,1 | 13,1 | 4,3 | 1,6 | 3,5 | 0,6 | 4,2 | 0,9 | 2,1 | 0,3 | 2,4 | 0,3 | 21,0 |
Таблица 2.10
Компонент | La | Ce | Pr | Nd | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Y |
Бастнезит из Внутренней Монголии | |||||||||||||||
Содержание, % вес. | 25,0 | 49,5 | 5,0 | 15,5 | 1,5 | 0,2 | 0,5 | < 0,1 | 0,1 | < 0,1 | 0,2 | ||||
Монацит из Гуандунга | |||||||||||||||
Содержание, % вес. | 21,0 | 48,0 | 5,5 | 16,5 | 2,5 | 0,08 | 1,8 | 0,26 | 1,36 | 3,0 | |||||
Ионные руды с низким содержанием иттрия (Синву, Пингвин в Гуандуне) | |||||||||||||||
Содержание, % вес. | 31,1 | 3,4 | 8,7 | 28,1 | 5,3 | 0,6 | 4,5 | 0,5 | 1,2 | 0,8 | 0,3 | 0,1 | 0,5 | < 0,1 | 15,4 |
Ионные руды со средним содержанием иттрия (Синфенг в Цзянси) | |||||||||||||||
Содержание, % вес. | 26,5 | 2,4 | 6,0 | 20,0 | 4,0 | 0,8 | 4,0 | 0,6 | 4,0 | 0,8 | 1,8 | 0,3 | 1,2 | 0,1 | 27,5 |
Ионные руды с высоким содержанием иттрия (Лонгнан в Цзянси) | |||||||||||||||
Содержание, % вес. | 1,8 | 0,2 | 0,9 | 3,8 | 2,8 | 0,02 | 5,7 | 1,2 | 8,4 | 1,8 | 5,1 | 0,8 | 4,6 | 0,6 | 62,5 |
В ряде способов переработки РЗЭ-содержащего минерального сырья извлечение отдельных элементов осуществляют методами осаждения. В результате такой переработки, полученные для дальнейшего экстракционного разделения исходные концентраты РЗЭ, могут изменять свой исходный состав.
2.20.2 Получение группового редкоземельного концентрата из лопарита
Способ хлорирования. Все ценные составляющие лопарита наиболее просто можно извлечь способом хлорирования. Сущность его состоит в том, что компоненты рудного концентрата взаимодействуют с газообразным хлором при температуре 750 - 850 °C в присутствии угля или кокса. Различия в летучести образующихся хлоридов позволяют разделить основные ценные составляющие концентрата. Ниже в таблице 2.11 приведены температуры плавления и кипения некоторых хлоридов:
Таблица 2.11
Хлорид | NbCl5 | NbOCl3 | AlCl3 | TaCl5 | TaCl4 | |
t пл, C | 204,7 | - | - | 216,5 | -23 | |
t кип, °C | 248,3 | ~ 400 (субл.) | 180 (субл.) | 234 | 136 | |
Хлорид | FeCl3 | SiCl4 | CeCl3 | LaCl3 | CaCl2 | NaCl |
t пл, °C | 304 | -67 | 800 | 850 | 782 | 800 |
t кип, °C | 319 | 58 | 1730 | 1750 | 2027 | 1465 |
Хлориды ниобия, тантала и титана, имеющие сравнительно низкие точки кипения, в процессе хлорирования уносятся с газами и улавливаются в конденсационных устройствах; высококипящие хлориды редкоземельных металлов, натрия и кальция остаются в хлораторе в форме плава хлоридов.
Ниже приведены реакции хлорирования основных ценных составляющих лопарита:
Nb2O5 + 3Cl2 + 1,5C = 2NbOCl3 + 1,5 CO2 (2.21)
Nb2O5 + 5Cl2 + 2,5C = 2NbCl5 + 2,5 CO2 (2.22)
Ta2O5 + 2Cl2 + 2,5C = 2TaCl5 + 2,5 CO2 (2.23)
TiO2 + 2Cl2 + C = TiCl4 + CO2 (2.24)
(Ln)2O3 + 3Cl2 + 1,5C = 2(Ln)Cl3 + 1,5CO2 (2.25)
Одновременно CO2 реагирует с углеродом с образованием CO:
 (2.26)
(2.26)Хлорирование оксидов происходит также с участием оксида углерода, например, по реакциям:
Nb2O5 + 3CO + 3Cl2 = 2NbOCl3 + 3CO2 (2.27)
TiO2 + 2CO + 2Cl2 = TiCl4 + 2CO2 (2.28)
Одновременно при хлорировании образуются хлориды CaCl2, NaCl, AlCl3, FeCl3, SiCl4.
Реакции хлорирования протекают со значительной убылью энергии Гиббса и практически необратимы. Роль углерода состоит не только в связывании кислорода в CO2, но также в активировании процесса хлорирования.
Ниже на рисунке 2.12 представлен хлоратор для хлорирования лопаритового концентрата в солевом расплаве, включающий: 1 - бункеры для концентрата и кокса; 2 - шнековый питатель; 3 - хлоратор, футерованный шамотным кирпичом; 4 - фурмы; 5 - расплав; 6 - копильник; 7 - летка; 8 - охлаждаемый газоход; 9 - патрубок вывода ПГС в систему конденсации.
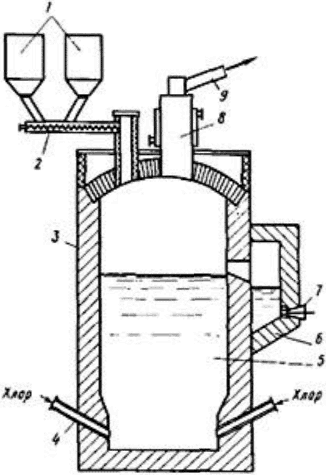
концентрата в солевом расплаве
Хлорирование лопаритового концентрата можно проводить в хлораторах шахтного типа с брикетированной шихтой или в хлораторах с солевым расплавом. Последние имеют существенные преимущества: исключаются трудоемкие операции приготовления брикетов и их прокаливания; благодаря эффективному массо- и теплообмену в перемешиваемом барботирующим хлором расплаве обеспечивается высокая скорость процесса и, соответственно, высокая удельная производительность хлоратора.
При хлорировании лопаритового концентрата расплавленная ванна создается образующимися высококипящими хлоридами натрия, калия, кальция и редкоземельных элементов.
Примерный состав такого расплава, %: LnCl3 - 55; CaCl2 - 20; NaCl - 15, остальное - хлориды других элементов. Температура затвердевания расплава 520 °C. Тонкоизмельченный концентрат и нефтяной кокс подаются в расплав хлоридов, через который барботируют хлор, поступающий через фурмы в нижнюю часть хлоратора. Хлоратор представляет собой шахту прямоугольного сечения с высотой уровня расплава 3,1 - 3,2 м. По мере хлорирования избыточный расплав непрерывно сливается через переточный канал в копильник. Нагревается расплав с помощью графитовых электродов, смонтированных в стенки хлоратора. Хлорирование ведут при температуре 850 - 900 °C, среднем содержании концентрата в расплаве 1,5% и углерода ~ 5%. В этих условиях удельная производительность хлоратора по концентрату - 5 - 5,5 т/м2 сечения печи в сутки.
Особенностью хлорирования в расплаве является преобладание содержания CO2 над CO в газовой фазе (отношение CO2:CO ~ 16:1). Из этого следует, что реакции хлорирования оксидов в расплаве идут с образованием CO2, а реакция Будуара протекает лишь частично, так как пузырьки CO2 быстро удаляются из расплава, не успевая вступить в реакцию с взвешенными частицами кокса.
Испытывали различные системы конденсации компонентов парогазовой смеси (ПГС). Получила распространение система, в которой последовательно осуществляется первоначально конденсация твердых хлоридов (NbOCl3, NbCl5, TaCl5 и др.) в пылевых камерах при температурах на выходе из камер 200 - 140 °C, а затем жидких хлоридов (TiCl4, SiCl4) в оросительных конденсаторах с орошением охлажденным тетрахлоридом титана.
Схема солевого фильтра с аэролифтной циркуляцией расплава приведена ниже на рисунке 2.13, которая включает: 1 - корпус, футерованный шамотным кирпичом; 2 - каплеуловительная камера; 3 - инертная керамическая насадка; 4 - газоход; 5 - колосниковая решетка; 6 - аэролифтная труба; 7 - патрубок вывода ПГС; 8 - загрузочный бункер кусков NaCl.
С целью отделения хлоридов железа и алюминия и исключения их конденсации вместе с хлоридами ниобия и тантала перед пылевыми камерами устанавливают солевой фильтр. Его действие основано на образовании FeCl3 и AlCl3 с хлоридами натрия и калия легкоплавких комплексов типа MeFeCl4 и MeAlCl4, термически устойчивых и обладающих низким давлением паров Pпар при температурах 500 - 600 °C:
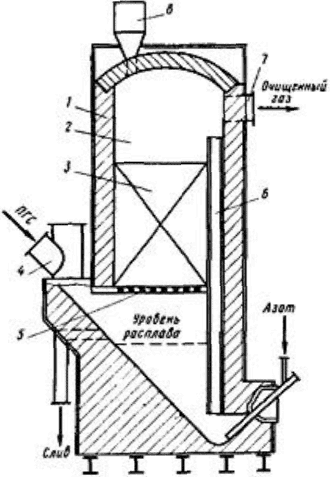
расплава
Над солевыми расплавами систем NaCl - FeCl3 - AlCl3 и KCl - FeCl3 - AlCl3, давление паров хлоридов NbOCl3, NbCl5, TaCl5, TiCl4, SiCl4, высокое, поэтому они не поглощаются расплавами солевого фильтра.
Расплав хлоридов в фильтре циркулирует с помощью аэролифтного устройства.
В фильтр периодически загружают смесь NaCl + KCl или отработанный электролит магниевых электролизеров. По мере накопления из фильтра сливается расплав, насыщенный хлоридами железа и алюминия.
В солевом фильтре помимо хлоридов железа и алюминия улавливаются твердые частицы (механический унос из хлоратора).
Конденсат твердых хлоридов имеет следующий примерный состав в пересчете на оксиды, % (по массе): (Nb,Ta)2O5 51 - 54; TiO2 1,0 - 1,8; Fe2O3 0,40 - 1,4; SiO2 0,43 - 1,4; Al2O3 0,64 - 0,8; ThO2 ~ 0,1; Ln2O3 0,9; C 0,5 - 2.
Часть тантала и ниобия попадает в конденсат жидкого TiCl4, где они находятся в растворе и частично в виде взвеси. При ректификационной очистке TiCl4 они остаются в кубовом остатке, из которого дополнительно извлекаются.
Таким образом, в результате хлорирования лопарита получают три продукта: плав, содержащий хлориды РЗМ, конденсат хлоридов тантала и ниобия и технический тетрахлорид титана.
Хлорная технология переработки лопарита обеспечивает извлечение 93 - 94% ниобия и 86 - 88% тантала в технические оксиды, 96,5 - 97% титана в технический тетрахлорид, извлечение 95,5 - 96% редкоземельных металлов в плав хлоридов [58, 59].
Плав хлоридов РЗЭ растворяют в воде, отделяют торий и продукты распада ториевого ряда соосаждением с хлоридом бария и осаждают групповой концентрат РЗМ в виде карбоната, который используется для разделения на индивидуальные элементы.
Сернокислотный способ
Сернокислотный способ основан на разложении лопаритового концентрата серной кислотой и разделении ценных составляющих с использованием различий в растворимости двойных сульфатов титана, ниобия и тантала, редкоземельных элементов с сульфатами щелочных металлов или аммония.
Концентрат разлагают (сульфатизируют) 95%-ной серной кислотой при температуре 150 - 250 °C. Расход кислоты - 2,78 т на 1 т тонкоизмельченного концентрата. Добавление сульфата аммония (0,2 т на 1 т концентрата) к серной кислоте предотвращает спекание реагирующей массы и повышает извлечение в раствор ниобия и тантала. Полное разложение концентрата достигается за 20 - 30 мин. К концу разложения получают полусухую массу.
Основные реакции, протекающие при разложении:
TiO2 + CaO + 3H2SO4 = CaTi(SO4)3 + 3H2O (2.29)
4TiO2 + Ln2O3 + 11H2SO4 = Ln2(SO4) x 4Ti(SO4)2 + 11H2O
(2.30)
Ниобий и тантал в присутствии больших количеств титана входят в состав двойных сульфатов титана в виде изоморфной примеси. Продукт сульфатизации выщелачивают водой. В твердой фазе остается подавляющая часть РЗЭ в форме малорастворимых двойных сульфатов Na2SO4·Ln2(SO4)3·2H2O и их изоморфной смеси с CaSO4. В раствор переходят титан (в виде TiOSO4), ниобий и тантал (вероятно, в форме сульфатов Э2O3(SO4)2).
Для отделения титана от ниобия и тантала используют осаждение сульфатом аммония малорастворимой двойной соли (NH4)2TiO(SO4)2·H2O. При суммарной концентрации H2SO4 + (NH4)2SO4 400 - 600 г/л растворимость соли равна 2,5 - 5 г/л. В осадок выделяется 70 - 80% титана от его содержания в растворе. Двойной сульфат титана используют как эффективный дубитель кожи. Термическим его разложением можно получить технический диоксид титана.
Из раствора, в котором остаются ниобий, тантал и часть титана, извлекают ниобий и тантал экстракцией.
Сернокислотный способ не обеспечивает столь четкого разделения всех ценных составляющих лопарита, какое достигается при хлорировании. Однако положительной его стороной является использование дешевого реагента и лучшие санитарные условия труда [58, 59].
Извлечение ниобия, тантала и РЗМ в конечные продукты примерно такое же, как в хлорном способе, извлечение титана ниже (~ 70%). Его можно повысить дополнительным извлечением титана из рафинатов после экстракционного извлечения ниобия и тантала.
К настоящему времени для переработки лопаритовых и пирохлоровых концентратов кроме сернокислотного метода разработаны несколько вариантов кислотной технологии: нитратно-сульфатный, нитратно-хлоридный, нитратно-фторидный, щелочно-сернокислотный. Наиболее привлекателен вариант щелочно-сернокислотной переработки лопарита, позволяющий с высокой селективностью отделить редкоземельные элементы и торий от титана, ниобия и тантала.
Щелочно-сернокислотная технология основана на предварительном разложении лопаритового концентрата в расплаве гидроксида натрия. В результате разложения редкие металлы, входящие в состав концентрата, превращаются в соединения, растворимые в разбавленных кислотах.
Процесс растворения концентратов в плавиковой кислоте с последующим экстракционным разделением ниобия и тантала в сульфатно-фторидной среде широко распространен в промышленности. В то же время ввиду дороговизны и недоступности плавиковой кислоты к бедному сырью этот способ неприменим.
2.20.3 Получение группового редкоземельного концентрата из апатитового концентрата
Несмотря на большой перечень разведанных в России месторождений фосфатных руд, в настоящее время перерабатываются практически только апатиты Хибинской группы и Ковдора. Это обусловлено высоким содержанием в них фосфора и отсутствием в составе карбонатов, что является определяющим для рентабельности производства минеральных удобрений. Основные игроки на рынке фосфатных удобрений России - ПАО "ФОСАГРО", ПАО "АКРОН", АО "МХК" ЕВРОХИМ и АО "ОХК УРАЛХИМ". Им принадлежат как заводы минеральных удобрений, так и горнодобывающие компании, разрабатывающие месторождения.
Переработка апатитового концентрата с получением минеральных удобрений проводится по азотнокислотной и сернокислотной схемам. В соответствии с технологией переработки РЗЭ извлекаются в нитратно-фосфатный раствор или в фосфогипс и экстракционную фосфорную кислоту.
Опытное производство с получением концентрата РЗЭ и индивидуальных соединений церия, лантана, неодима и концентрата среднетяжелой группы было создано на предприятии ПАО "Акрон" (г. Великий Новгород) с производительностью 200 т/год. На первой стадии РЗЭ извлекались из нитратно-фосфатного раствора в фосфатный концентрат нейтрализацией раствора аммиаком до pH 1,1 - 2,0, который затем растворялся в азотной кислоте и экстракцией на 100% трибутилфосфате (ТБФ) очищался от примесей и затем использовался в технологии разделения с получением индивидуальных соединений РЗЭ [59]. В настоящее время производство не работает.
В ИХТЦ "Русредмет" (Санкт-Петербург) в 2013 - 2014 г.г. разработана сорбционно-экстракционная технология извлечения РЗМ непосредственно в производственном процессе ОАО "ФосАгро-Череповец". [60]. Способ включает сорбцию с помощью сильнокислотного макропористого катионита Purolite C-150, осуществляемую в диапазоне температур 40 - 80 °C, промывку насыщенного редкоземельными элементами сорбента водой, десорбцию раствором нитрата аммония с получением товарного десорбата и дополнительную экстракционную очистку полученного десорбата 100%-ным ТБФ. Технология проверена на опытно-промышленной установке производительностью 12 т РЗМ/год. В 2014 году с выводом установки на проектную мощность была получена партия оксидов РЗМ объемом около 9 т, а ЭФК возвращена в цепочку производства удобрений.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду п. [66] Библиографии, а не [67]. |
Анализ информационно-патентной литературы за последние 10 лет показал, что в связи с бумом на рынке РЗМ в 2011 - 2012 г.г. появились новые исследования по извлечению РЗМ из фосфогипса и комплексной переработке ФГ с получением гипсового вяжущего и концентрата РЗЭ. Среди основных разработчиков следует упомянуть ООО "ЛИТ" ГК "Скайград" [61, 62], АО "ВНИИХТ" [63], ООО "МИЦ-Геосистемы" [64], ИХТРЭМС КНЦ РАН [65], ФГАОУ ВО "УрФУ" [66], ООО "Русредмет" [67] и другие.
Все описанные выше технологии основаны на сочетании методов промывки фосфогипса растворами кислот или солей с последующим выделением РЗЭ из промывного раствора или пульпы ФГ в виде концентрата методом осаждения подходящим реагентом, сорбции или экстракции.
Анализ рассмотренных технологий по извлечению РЗЭ из фосфогипса и последующему концентрированию с целью получения групповых концентратов, пригодных для дальнейшего разделения на группы и индивидуальные РЗМ, показал, что все известные технологии технически осуществимы и имеют право на реализацию. Однако экономически рентабельными будут только те, которые предусматривают комплексную переработку фосфогипса с получением не только РЗ, но и ассортимент продукции на основе отмытого от примесей гипса, имеющей высокую добавочную стоимость.
Такую технологию разработал, проверил на опытно-промышленной автоматизированной установке полного производственного цикла в течение месяца непрерывной работы на отвальном и свежем (полугидратном) фосфогипсе с получением опытных партий ГРЗК и гипса. Производительность установки: по ФГ - 41 кг/ч или 400 кг/смену, по РЗО >= 1,0 кг/смену.
Основные технические решения, принятые при разработке технологии и создании производства комплексной переработки ФПГ:
Для повышения степени извлечения РЗМ из фосфополугидрата (ФПГ) применен способ предварительной подготовки сырья переводом его в фосфодигидрат (ФДГ), позволяющий повысить степень извлечения РЗМ до 65 - 70% при использовании растворов серной кислоты концентрации 30 - 40 г/л. Такой режим выщелачивания позволяет практически не извлекать в раствор РЗЭ торий и продукты распада ториевого ряда (радий -226 и др.)
Дальнейшее извлечение РЗМ проводится в аппаратах колонного типа, работающих в режиме восходящей фильтрации растворов через псевдоожиженный слой сульфокатионита, ограниченный сверху фильтрующей перегородкой. Переключение колонн, работающих в режиме сорбции, с первой на вторую и далее происходит при достижении в ионите не менее 95% полной динамической обменной емкости (ПДОЕ), а в режиме десорбции - не более 0,05% от ПДОЕ. Маточники сорбции с концентрацией церия <= 0,05 г/л возвращают на промывку фосфогипса, а десорбции с концентрацией церия на выходе >= 0,25 г/л направляют на осаждение первичного концентрата (РЗК), а с церием <= 0,25 г/л - на десорбцию ионита в последующей колонне. Одновременно в режиме сорбции работают 3 - 4 колонны, а десорбции - 2 - 3. Маточник от осаждения РЗК нейтрализуют серной кислотой до pH 4,2 - 4,4 и возвращают на десорбцию. Такое ведение процесса позволяет получать на первой стадии процесса концентрат РЗМ, содержащий менее 5% примесей при низких удельных расходах реагентов [61, 62, 67].
Дальнейшая переработка первичного концентрата с очисткой от примесей производится экстракцией из нитратных растворов с использованием экстрагента ТБФ в разбавителе в каскаде центробежных экстракторов.
Для дальнейшего разделения группового концентрата (ГРЗК) на индивидуальные РЗМ используют упаренный реэкстракт.
В настоящее время технология реализуется в промышленном масштабе на базе Воскресенского завода минеральных удобрений.
2.20.4 Переработка монацитовых концентратов
Монацит относится к группе фосфатных минералов (фосфат церия и редкоземельных элементов, РЗЭ), содержащих уран, торий и РЗЭ [59]. Состав: (Ce, La, Y, Th) PO4; содержание тория может достигать 12%, соотношение La:Ce, как правило, близко к 1:1. Монацит является важнейшим источником тория и РЗЭ. Встречается в береговых и речных россыпях в ассоциации с цирконом, ильменитом и рутилом. Минералогия исходного монацитового сырья весьма сложна и непостоянна по соотношению минералов различных месторождений.
Разработка монацитовых россыпных месторождений отличается простотой. В результате обогащения и отделения от сопутствующих минералов методами грохочения и электромагнитной сепарации получают концентраты, содержащие 95 - 98% монацита. Для доводки концентратов и отделения от них циркона применяют флотационный метод обогащения.
Гидрометаллургическая переработка монацитового концентрата с целью извлечения из него тория, урана и РЗЭ включает в себя следующие основные операции:
- вскрытие исходного концентрата с получением соединений тория, урана и РЗЭ, растворимых в минеральных кислотах;
- перевод тория, урана и РЗЭ в раствор;
- отделение тория, урана и РЗЭ от фосфора;
- разделение тория, урана и РЗЭ;
Как отдельную стадию переработки монацитового концентрата необходимо выделить дезактивацию промежуточных растворов от продуктов радиоактивного распада тория и урана.
Таким образом, усовершенствование технологии переработки монацитовых концентратов сводится либо к разработке новых процессов для осуществления всех перечисленных выше стадий, либо к их модернизации с учетом современных достижений технологии гидрометаллургии редких и радиоактивных металлов.
Промышленное значение приобрели три основных метода вскрытия монацитового концентрата:
- сульфатизация;
- щелочная обработка (сплавление или спекание с гидроксидом или карбонатом натрия, обработка щелочными растворами NaOH;
Сернокислотный способ переработки монацитового концентрата состоит в разложении концентрата серной кислотой с последующим выщелачиванием водой сульфатов РЗЭ и тория. Из раствора раздельно выделяют соединения тория и РЗЭ.
Разложение. Измельченный монацитовый концентрат (0,15 - 0,1 мм) разлагают концентрированной серной кислотой при температуре 180 - 200 °C (1,5 - 2 т на 1 т концентрата, что в 2,5 - 3 раза превышает теоретически необходимое количество) в течение 2 - 4 ч. Разложение ведут в стальных или чугунных аппаратах периодического действия с мешалкой или в барабанных вращающихся сульфатизаторах с автоматической подачей серной кислоты и концентрата и непрерывной выгрузкой получаемого продукта.
Основные реакции, протекающие при разложении:
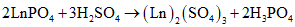 (2.31)
(2.31)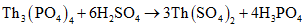 (2.32)
(2.32)После окончания разложения пастообразную реакционную массу выщелачивают в стальных освинцованных аппаратах холодной водой (10 л на 1 кг разлагаемого концентрата). Такое разбавление необходимо для обеспечения перевода в раствор сульфатов РЗЭ и тория.
Для выделения тория и РЗЭ из сульфатных растворов применяют способ ступенчатой нейтрализации растворов с осаждением фосфатов тория и РЗЭ, основанный на различии значений pH выделения фосфата тория и фосфатов лантаноидов: фосфат тория выделяется из сернокислых растворов при pH 1, в то время как фосфаты РЗЭ осаждаются при pH ~ 2,3.
В настоящее время сернокислотный способ вытесняется щелочным способом вскрытия, которому отдается предпочтение. Большинство перерабатывающих монацит предприятий в мире работают по щелочному методу.
В основе щелочного способа лежит реакция взаимодействия монацита с раствором гидроксида натрия:
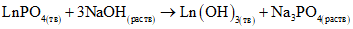 (2.33)
(2.33)Полное разложение монацита достигается при тонком измельчении концентрата (96,5 класса - 0,044 мм) с применением 45%-го раствора гидроксида натрия в количестве 1,5 кг NaOH на 1 кг монацита (что составляет 300% от теоретически необходимого количества) и обработке при температуре 140 °C в течение 3 ч. Повышение температуры разложения до 200 °C приводит к практически полному вскрытию. Концентрат разлагают гидроксидом натрия в стальных реакторах.
Из фильтрата после осаждения тория раствором гидроксида натрия осаждают смесь гидроксидов РЗЭ. Высушенный осадок гидроксидов лантаноидов имеет следующий примерный состав, %: РЗЭ - 73; Th - 0,05; U - 0,005; Fe - 0,002; Si - 0,4; P - 0,1; Cl - 7,9.
Преимущества щелочного метода перед методом разложения монацита серной кислотой - отделение уже на первой стадии фосфора от тория и лантаноидов с получением полезного побочного продукта - фосфата натрия. Однако сернокислотный метод экономичней и более универсален - применим к монацитовым концентратам различного происхождения.
Процесс хлорирования монацитового концентрата был описан в патентах Германии, Франции, Италии, Англии. Определенные положительные результаты были достигнуты австралийскими исследователями.
Наиболее важной и трудной задачей переработки монацита является разделение урана, тория и РЗЭ с получением их чистых соединений и/или в случае РЗЭ их смешанных концентратов.
Для разделения урана, тория и РЗЭ используют два основных промышленно апробированных метода: осадительный (различные варианты гидролитического осаждения или осаждение труднорастворимых соединений) и экстракционный (разделение урана, тория и РЗЭ жидкостной экстракцией органическими реагентами).
Торий обладает менее основными свойствами, чем РЗЭ, поэтому его первым выделяют из растворов минеральных кислот после их нейтрализации. При сернокислотном разложении монацита торий может быть выделен из раствора и отделен от РЗЭ нейтрализацией различными реагентами, аммиаком, гидроксидом натрия, оксидом магния, оксидами РЗЭ, а также значительным разбавлением водой [58, 59].
Наибольшее распространение для разделения урана, тория и РЗЭ получил метод жидкостной экстракции, позволяющий получать продукты ядерной чистоты. Этот метод был использован для разделения названных элементов при переработке монацита еще в 1940-х гг. С тех пор этот метод получил большое развитие и промышленное применение. Достаточно сказать, что практически все промышленные и вновь синтезированные в лабораториях экстрагенты были изучены для целей разделения этих элементов. Однако наиболее промышленно значимым процессом остается разделения урана, тория и РЗЭ с применением в качестве экстрагента трибутилфосфата (ТБФ). Также важную роль в процессах переработки растворов выщелачивания монацита играют ди-2-этилгексилфосфорная кислота (Д2ЭГФК), амины различного строения и четвертичные аммониевые соли (ЧАС).
Таким образом, рассмотренные способы переработки монацита позволяют сделать следующие заключения: целевыми компонентами, составляющими монацит и имеющими практическое применение в различных отраслях экономики, являются фосфор, уран, торий и РЗЭ.
Наиболее перспективными способами комплексной переработки монацита в промышленном масштабе с извлечением всех ценных компонентов: фосфора, урана, тория и РЗЭ остаются сульфатизация и щелочное разложение монацита. В то же время более перспективным при щелочном разложении монацита является карбонатная переработка продуктов разложения, а именно карбонатное выщелачивание тория и урана из смеси их гидратов с РЗЭ.
Основными проблемами переработки монацита в связи с его переменным составом остаются вскрытие исходного концентрата и разделение урана, тория и РЗЭ. Эти процессы нуждаются в дальнейшем совершенствовании, и именно в этом направлении развиваются исследования, проводимые в настоящее время в ведущих странах, занимающихся промышленной переработкой монацита.
Для процессов разделения урана, тория и РЗЭ методами, основанными на разнице в растворимости некоторых соединений перечисленных элементов, перспективным является исследование карбонатных или карбонатно-щелочных систем.
Для совершенствования процессов экстракционного извлечения урана, тория и РЗЭ из растворов выщелачивания сложного солевого состава наиболее перспективным остается применение синергетных смесей экстрагентов различных классов.
При разработке всех схем необходимо руководствоваться принципом максимального сокращения количества радиоактивных твердых отходов, поскольку захоронение их стоит дорого. Поэтому целесообразно максимально исключить осадительные операции, приводящие к "размазыванию" тория по твердым фазам, а также бороться за полноту выделения тория в виде компактных чистых соединений, удобных как для захоронения, так и для возможной реализации.
2.20.5 Методы переработки пирохлоровых и аналогичных по составу руд и концентратов, содержащих РЗМ
Насчитывается более 100 видов минералов, содержащих ниобий и тантал, из них не более 50 являются собственно ниобиевыми и танталовыми, остальные содержат ниобий и тантал в виде примесей. Наиболее важные минералы ниобия и тантала можно подразделить на две группы:
1) тантало-ниобаты - соли танталовой и ниобиевой кислот;
2) титано-тантало-ниобаты - сложные соли титановой, танталовой и ниобиевой кислот.
Важнейшим представителем второй группы минералов является: пирохлора-микролита и лопарит. Химически лопарит - это титанониобат редкоземельных, щелочных и щелочноземельных элементов. РЗЭ в нем представлены в основном цериевой подгруппой, а вторые - натрием и кальцием. Формула лопарита [Na,Ca,РЗЭ] [Ti, Nb]O3. Ряд пирохлора-микролита - это большое число оксофторониобатов и оксофторотанталатов которые можно описать общей примерной формулой [Na,Ca][Nb,Ta]2O6F. Важнейшие в промышленном отношении - это пирохлор [Na,Ca,РЗЭ]Nb2O6F и микролит [Na,Ca,РЗЭ]Ta2O6F. Это два крайних минерала Nb-Ta ряда.
В схемах переработки пирохлоровых карбонатитовых руд предусматриваются как гравитационные, так и флотационные процессы. Гравитационные процессы применяются при обогащении крупно- или средневкрапленных руд.
Разработан сернокислотный способ разложения лопаритового концентрата и разделения редкоземельных элементов, титана, ниобия и тантала с использованием различий в растворимости двойных сульфатов этих элементов.
Основной недостаток сернокислотного способа переработки лопаритового концентрата - не обеспечивается достаточно четкое разделение РЗЭ, Ti и Nb, Ta. Более глубокое разделение указанных элементов при переработке титано-тантало-ниобиевых концентратов достигается при вскрытии их путем хлорирования.
Описан способ переработки ниобиевых руд Bayan Obo методом сульфатизирующего обжига при 250 °C с последующим выщелачиванием при 60 °C. В результате присутствующие ниобий и РЗЭ переходят в раствор.
К настоящему времени, кроме сернокислотного, разработаны несколько вариантов кислотной технологии для переработки лопаритовых и пирохлоровых концентратов: нитратно-сульфатный, нитратно-хлоридный, нитратно-фторидный, щелочно-сернокислотный. Наиболее привлекателен вариант щелочно-сернокислотной переработки лопарита, позволяющий с высокой селективностью отделить редкоземельные элементы и торий от титана, ниобия и тантала. [59].
Щелочно-сернокислотная технология основана на предварительном разложении лопаритового концентрата в расплаве гидроксида натрия. В результате разложения редкие металлы, входящие в состав концентрата, превращаются в соединения, растворимые в разбавленных кислотах.
Процесс растворения концентратов в плавиковой кислоте с последующим экстракционным разделением ниобия и тантала в сульфатно-фторидной среде широко распространен в промышленности. В то же время ввиду дороговизны и недоступности плавиковой кислоты к бедному сырью этот способ неприменим.
2.20.6 Переработка эвдиалитового минерального сырья
Новым перспективным источником редкоземельного и циркониевого сырья в России может стать эвдиалитовый концентрат. Эвдиалит - цирконосиликат сложного состава, который содержит двуокись циркония, редкоземельные элементы, обогащенные тяжелыми металлами, а также гафний, ниобий и тантал и имеет следующий химический состав (в масс. %): SiO2 - 44,92; Na2O - 15,31; ZrO2 - 10,80; Al2O3 - 6,98; CaO - 4,92; Fe2O3 - 4,68; TiO2 - 2,27; MnO - 2,21; 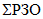 - 2,01; SrO - 1,95; K2O - 1,45; прочие - 2,50.
- 2,01; SrO - 1,95; K2O - 1,45; прочие - 2,50.
Комплексный характер эвдиалитового концентрата требует создания комплексной технологической схемы с извлечением максимально возможного количества всех ценных составляющих. Несмотря на то, что эвдиалит является легкоразлагаемым минералом, извлечение РЗЭ в раствор выщелачивания не превышает 65 - 75%, кремнеземистого геля - 45 - 80%. Извлечение циркония в раствор удается достичь лишь в жестких условиях. Объясняется это блокированием минерала кремнеземом, присутствием кислотонерастворимого циркония, образованием вторичных соединений циркония и т.д. Ранее проведенные исследования [67] показали, что при любых вариациях физико-химических и технологических параметров, включая автоклавную обработку и предварительную обработку эвдиалита плазмой по аналогии с цирконом, не удается извлечь в раствор более 45 - 80% кремнезема. Причем образующиеся при щелочной обработке эвдиалита гидролизованные формы циркония гораздо хуже, чем исходный эвдиалит, вскрываются в азотной кислоте (степень извлечения ZrO2 в раствор снижается до 50 - 70%).
Проведенные исследования с применением целенаправленного и эффективного механического воздействия на материал при низкотемпературном щелочном выщелачивании эвдиалитового концентрата показали, что щелочное выщелачивание механически активированного эвдиалитового концентрата в течение 2,5 минут при Мш : Мк = 800:10 позволяет извлечь в раствор до 60% кремния за 6 часов 40% раствором NaOH и при температуре 100° C. Повышение температуры щелочного выщелачивания до 120° C обеспечивает извлечение кремния в раствор на уровне 70% за 6 часов. При последующем кислотном выщелачивании продукта щелочной обработки - извлечение РЗМ составило 87%, циркония - более 80%, а извлечение кремния в азотнокислый раствор - составило менее 1%. Такие растворы пригодны для экстракционного и сорбционного извлечения РЗМ и циркония.
Еще одним известным вариантом технологии переработки эвдиалита является солянокислотный, включающий основные стадии: химическую очистку концентрата от нефелина, солянокислотное разложение концентрированной соляной кислотой в режиме постепенной загрузки, насыщение газообразным хлористым водородом части маточного раствора от кристаллизации солей до требуемой концентрации и возврат его на выщелачивание новых порций эвдиалита. Многократный оборот растворов позволяет резко повысить содержание в них ниобия и РЗЭ, что значительно упрощает их дальнейшее извлечение. Следующие стадии - экстракционное извлечение титана, ниобия и железа из растворов после выделения оксихлорида циркония и хлорида натрия, выделение хлорида стронция, получение жидкого стекла и т.д.
Общими недостатками солянокислотной и азотнокислотной схем переработки эвдиалита являются высокая коррозионная активность используемых сред и как следствие - высокие капитальные затраты на ее реализацию, большой расход азотной и соляной кислот, требующий также мер по их регенерации и повторному использованию. Также обращение с солянокислыми стоками требует особых мер по их утилизации и захоронению [59].
В настоящее время не создано промышленной технологии по переработке эвдиалитовых руд, разработаны лишь различные варианты технологических схем на стадии лабораторных исследований.
2.20.7 Использование техногенного редкоземельного сырья
Основная масса постоянных магнитов из сплавов системы Nd-Fe-B изготавливается по методу порошковой металлургии, включающего в себя большое число технологических переделов. Кроме этого, в силу природы физико-химических свойств РЗМ и их сплавов, этот материал обладает высокой химической активностью и склонностью к окислению. Все это обуславливает образование значительного количества отходов или брака. Поэтому в современных условиях, когда растут цены на РЗМ и возрастает их дефицитность, очень важно снизить потери за счет повторного вовлечения такого материала в производственный цикл.
В таблице 2.12 приведены основные технологические переделы при получении РЗПМ. Несмотря на то, что на каждой технологической операции наблюдается высокий выход материала на следующий передел, итоговая величина выхода материала в готовое изделие составляет не более 54,0%. Конечно, эту величину можно увеличить за счет оптимизации отдельных переделов, но величина суммарного выхода материала можно поднять до 70,0 - 75,0%. Переработка техногенных отходов магнитного производства РЗПМ может служить ценным источником РЗМ, так содержание РЗМ в различного вида отходах может составлять 25,0 - 40,0% по массе.
Таблица 2.12
Технологическая операция | Выход материала на следующий передел, % |
Подготовка шихты | 0,99 |
Выплавка | 0,95 |
Гомогенизация | 1,00 |
Дробление | 0,98 |
Охрупчивание | 0,99 |
Помол | 0,99 |
Прессование | 0,95 |
Спекание | 0,95 |
Термообработка | 1,00 |
Шлифовка | 0,92 |
Резка | 0,90 |
Шлифовка | 0,95 |
Покрытие | 0,98 |
Намагничивание | 0,97 |
Контроль | 0,90 |
Упаковка | 0,99 |
ИТОГ | 0,54 |
Основные технологические переделы получения спеченных редкоземельных магнитов по методу порошковой металлургии представлены на рисунке 2.14. На втором переделе методом сплавления в индукционных вакуумных печах из исходных компонентов в виде слитков РЗМ или их сплавов, железа, кобальта, бора (или ферробора), легирующих добавок получают компактный слиток заданного химического состава. Кроме получения материала требуемого состава для сплавов системы Nd-Fe-B очень важно получить слитки с явно выраженной дендритной зеренной структурой и с отсутствием в структуре материала крупных выделений 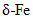 . На следующей стадии технологического процесса проводят дробление слитка для получения грубого порошка магнитного сплава с размером частиц менее 500 мкм. Дробление можно проводить механическим способом в различного вида дробилках (щековых, конусно-инерционных, валковых и т.д.), либо при помощи водородного диспергирования.
. На следующей стадии технологического процесса проводят дробление слитка для получения грубого порошка магнитного сплава с размером частиц менее 500 мкм. Дробление можно проводить механическим способом в различного вида дробилках (щековых, конусно-инерционных, валковых и т.д.), либо при помощи водородного диспергирования.
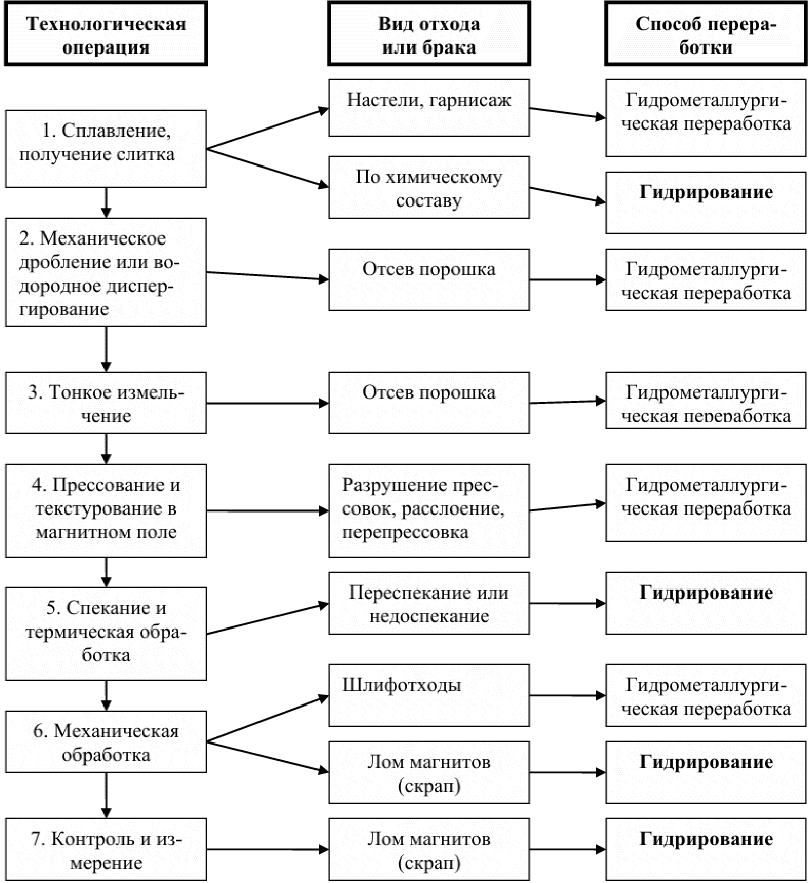
спеченных редкоземельных магнитов по методу порошковой
металлургии
Порошок, полученный после дробления слитков, направляется на тонкий помол для получения порошка, состоящего из монокристаллических частиц с размером около 1 - 5 мкм. Полученный тонкий порошок служит исходным материалом для изготовления пресс-заготовок. Текстурованные заготовки для спекания получают методом сухого или мокрого прессования в магнитном поле напряженностью не менее 640...800 кА/м.
Пресс-заготовки спекают в вакуумных печах с целью повышения плотности, получения необходимого сочетания магнитных свойств (коэрцитивной силы, остаточной намагниченности, индукции в рабочей точке и энергетического произведения), получения закрытой системы пор для уменьшения окисляемости образцов и повышения стабильности магнитных свойств. В вакуумных печах проводят также термическую обработку спеченных магнитов.
На завершающих стадиях изготовления спеченных магнитов изделия подвергаются механической обработке (шлифовка, резка), намагничиванию и измерению магнитных свойств.
На каждой стадии получения спеченных магнитов Nd-Fe-B возможно образование как отходов, так и брака магнитов. По усредненным оценкам выход годного продукта в готовое изделие составляет от 50 - 70% от исходного сырья, поэтому для повышения эффективности производства постоянных магнитов важно вовлечение отходов и брака магнитов в повторный производственный цикл.
Значительная доля отходов перерабатывается методами гидрометаллургии, которые включают в себя подготовку отходов к растворению, растворение их в кислотах, выделение РЗЭ и их осаждение в виде оксидов и фторидов. Наибольшую долю (до 70%) в отходах, перерабатываемых в гидрометаллургическом переделе, составляют отходы от шлифования в размер спеченных магнитов и магнитных систем.
Отсев порошка, образующегося при дроблении и мелком помоле, незначителен и определяется состоянием технологической культуры на конкретном производстве. Брак при прессовании, как правило, возникает при постановке на производство новых изделий и при смене прессового инструмента.
Все вышеперечисленные виды отходов характеризуются тем, что они сильно окислены. Но есть отходы, в составе которых содержание кислорода незначительно, а доля металлической фазы велика. Такие отходы целесообразно перерабатывать с использованием методов пирометаллургии или с помощью водородной обработки.
2.20.8 Технология получения РЗЭ из вторичного магнитного сырья
Перспективным источником РЗЭ является вторичное магнитное сырье (МС), к которому относятся отходы производства и потребления постоянных магнитов Nd-Fe-B и Sm-Co, а также магнитные материалы, выделенных из радиоэлектронного лома (РЭЛ). МС имеет сложный состав, который варьируется в широких пределах. Кроме лигатур и производных на базе интерметаллидов Nd(РЗЭ)2Fe14B, Sm(РЗЭ)Co5, Sm2(РЗЭ)Co17, где в качестве легирующих добавок РЗЭ чаще всего выступают празеодим, тербий и диспрозий, в нем также содержатся никель, медь, алюминий, кремний и другие примеси в виде металлов и оксидов. Основную массу МС составляют отходы от операции шлифования заготовок - шлифотходы, содержащие помимо магнитных материалов абразивные частицы шлифинструмента и водно-органические эмульсии смазочно-охлаждающих жидкостей (СОЖ). Выход шлифотходов от массы готовых магнитов оценивается в 10 - 40%.
Вовлечение МС в переработку позволяет: увеличить сырьевую базу РЗЭ; вернуть в производственный цикл наиболее ценные Nd, Tb и Dy; утилизировать пожароопасные шлифотходы, хранящиеся на складах заводов-изготовителей магнитов. Однако до настоящего времени уровень переработки МС в России не превышал 1% и поддерживался переплавкой крупнокусковых отходов в готовую продукцию или получением полиметаллических концентратов из РЭЛ.
Для решения проблемы рециклинга материалов магнитной и радиоэлектронной промышленности специалистами ООО "ЛИТ" (ГК "Скайград") совместно с ООО "ПромТехРециклинг" разработана и запатентована [69, 70] экономически эффективная гидрометаллургическая технология переработки МС, включающая:
- предварительную подготовку сырья - дробление/измельчение кусковых МС, очистку шлифотходов от абразивных частиц и СОЖ;
- растворение МС в растворе азотной кислоты с одновременной карбамидной денитрацией отходящих газов;
- экстракционное извлечение РЗЭ с получением группового редкоземельного концентрата (ГРЗК).
Технология принимает во внимание специфику ранее предложенных способов переработки МС, но в отличие от них характеризуется меньшими материало- и энергозатратами, низким содержанием токсичных веществ в отходящих газах, оперирует использованием высокоэффективного оборудования.
Согласно разработанной технологии предварительную подготовку шлифотходов осуществляют путем магнитной сепарации (для отделения немагнитной фракции абразивных частиц) с последующей ступенчатой вакуумной термообработкой магнитной фракции: сначала при температуре не выше 100 °C (для отгонки воды), а затем - при 300 - 350 °C (для отгонки масла СОЖ). При этом вакуумную термообработку ведут в присутствии добавки жидкого нефтяного парафина, снижающего температуру кипения труднолетучих составляющих масла. Указанная совокупность приемов позволяет сократить нагрузку на печное оборудование, избежать использования дорогостоящих печей нетиповой конструкции, предотвратить переход железа в окисленную форму, инертную по отношению к минеральным кислотам, что особенно важно при последующем гидрометаллургическом переделе с экстракционным извлечением суммы РЗЭ (гидратированные ионы Fe3+ являются высаливателями, увеличивающими эффективность экстракции).
Для перевода МС в жидкую форму порошки от стадии предварительной подготовки порционно вводят в раствор, содержащий 3,5 - 5,5 моль/л азотной кислоты и по меньшей мере стехиометрическое количество карбамида. Растворение ведут при температуре 55 - 65 °C и барботаже пульпы воздухом. Выбранные условия минимизируют выход нерастворимого остатка и расход реагентов на побочные реакции, исключают выпадение осадка нитрата карбамида, способствуют оптимальной интенсивности растворения МС, обеспечивают эффективную конверсию отходящих нитрозных газов в безвредные продукты (что позволяет избежать использования специального газоочистного оборудования, оснащенного дорогостоящими катализаторами на основе металлов платиновой группы). Процесс описывается следующими реакциями:
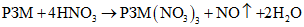 (2.34)
(2.34)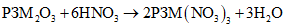 (2.35)
(2.35)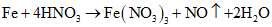 (2.36)
(2.36)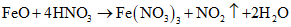 (2.37)
(2.37)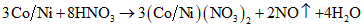 (2.38)
(2.38)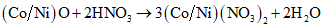 (2.39)
(2.39)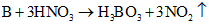 (2.40)
(2.40)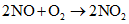 (2.41)
(2.41)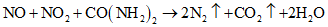 (2.42)
(2.42)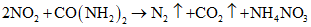 (2.43)
(2.43)Для завершения денитрации и дорастворения МС пульпу выдерживают при 70 - 75 °C в течение 30 мин. По окончании выдержки в жидкую часть пульпы переходит >= 99,5% РЗЭ, а в твердую - высшие окислы железа и механические примеси. Полученную пульпу при необходимости упаривают до достижения оптимальной концентрации Fe3+, доводят до кислотности 20 - 25 г/л, после чего разделяют фильтрацией. Нерастворимый остаток промывают водой и утилизируют, а раствор МС направляют дальнейший экстракционный передел.
Экстракционное извлечение РЗЭ из раствора МС реализуют в непрерывнодействующем противоточном каскаде центробежных экстракторов, наиболее экономичных с точки загрузки экстрагента и объема незавершенного производства по сравнению с экстракторами других типов. В качестве экстрагента используют раствор трибутилфосфата (ТБФ) в инертном разбавителе. Селективность извлечения обеспечивается свойством РЗЭ образовывать сольватные комплексы с ТБФ (экстрагироваться) в азотнокислой среде:
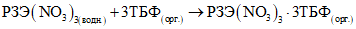 . (2.44)
. (2.44)Остальные компоненты раствора МС не экстрагируются (остаются в рафинате) и выполняют роль высаливателей. Обратное извлечение РЗЭ из органической фазы в водную (реэкстракция) происходит при контакте экстракта со слабым раствором кислоты:
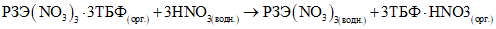 . (2.45)
. (2.45)Переход от экстракции к реэкстракции осуществляют через промежуточную стадию - стадию промывки экстракта - поскольку насыщенный экстрагент содержит некоторое количество соэмульгированных нередкоземельных примесей. В ходе промывки водой помимо очистки от примесей происходит и частичная реэкстракция РЗЭ, поэтому промывные воды (рафинат промывки) не выводят из процесса, а возвращают на стадию экстракции.
Высокое сквозное извлечение РЗЭ из раствора МС в реэкстракт (>= 99,5%) достигается многократным контактом водной и органической фаз в режиме противотока. В ходе работы каскада экстрагент, исходный раствор МС, промывной и реэкстрагирующий растворы непрерывно подаются в него дозирующими насосами, а продукционные растворы - рафинат и реэкстракт (раствор ГРЗК) - поступают в приемные емкости самотеком. Выходящий экстрагент возвращают в начало процесса.
Полученный ГРЗК содержит >= 99,9% основного вещества и пригоден для последующего экстракционного разделения на индивидуальные РЗЭ. Рафинаты от стадии экстракционного извлечения могут быть переработаны в попутную, в том числе Co-содержащую продукцию.
Технология прошла успешные испытания на опытно-промышленных участках ООО "ЛИТ" и ООО "ПромТехРециклинг". В результате испытаний получены опытные образцы продукции требуемого качества, подтверждены заявленные технологические показатели.
Технико-экономическая оценка разработанной технологий показала, что переработка МС на основе Nd-Fe-B характеризуется высокой рентабельностью даже при реализации неразделенного ГРЗК, а переработка МС на основе Sm-Co экономически целесообразна при глубоком разделении ГРЗК или попутном производстве дорогостоящего оксида кобальта (III).
2.20.9 Основные методы разделения концентратов РЗЭ на группы и индивидуальные элементы
Редкоземельные элементы в том или ином соотношении всегда встречаются вместе во всех сырьевых источниках, но практически никогда не потребляются в виде природной смеси. Поэтому их разделение вследствие близости свойств - сложная задача.
Исторически первым основным способом разделения и получения отдельных редкоземельных элементов был метод дробной кристаллизации. Суть дробной кристаллизации заключается в проведении большого числа стадий кристаллизации с разделением на каждой стадии твердой и жидкой фаз. Осадки при этом обогащаются менее растворимыми элементами, а растворы - более растворимыми. [58]. В эпоху первооткрывателей был хорошо известен способ разделения РЗЭ на цериевую и иттриевую группы (среднетяжелую) фракционным осаждением двойных сульфатов. Осаждение двойных сульфатов оказалось перспективным из-за значительной разницы в растворимости соединений РЗЭ в насыщенных растворах сульфатов щелочных элементов и аммония. До недавнего времени метод широко применялся на практике. Наименьшей растворимостью в насыщенных растворах сульфатов щелочных элементов обладают двойные сульфаты РЗЭ цериевой группы (La - Sm), немного лучше растворяются одноименные соединения Eu - Tb, а элементы иттриевой подгруппы Dy - Yb и Y наиболее растворимы. Обычно двойным сульфатам (некоторые авторы относят их к комплексным солям) приписывают формулу:
xR2(SO4)3·yM2SO4·zH2O (2.46)
где R - редкоземельный металл;
M - K, Na, NH4+;
x, y, z - переменные коэффициенты.
Для более четкого разделения в процессе осаждения двойных сульфатов было предложено добавлять в раствор комплексообразователь - двунатриевую соль этилендиаминтетрауксусной кислоты (трилон Б), этилендиаминтетрауксусную кислоту, ацетат аммония или [39]. С помощью такого процесса были получены 99,99% концентраты Gd, Dy, 99,9% - Ho, Lu и 97% Tb.
Методом дробной кристаллизации возможно разделение двойных нитратов РЗЭ и магния, аммония или марганца. Трудоемкий, длительный, процесс позволяет получить более чистые препараты отдельных РЗЭ, чем метод осаждения. Для разделения дробной кристаллизацией часто использовали броматы (Ln)BrO3·9H2O, диметилфосфаты Ln[(CH3)2PO4]3, двойные нитраты 2Ln(NO3)3·3Mg(NO3)2·24H2O, Ln(NO3)3·2NH4NO3·4H2O [19].
Метод осаждения гидроксидов также позволяет разделить РЗЭ на концентраты. Следует учитывать, что pH осаждения гидроксидов того или иного элемента из растворов зависит от прочности его соединений с анионами (комплексообразователями), присутствующими в этом растворе (с увеличением прочности комплекса pH осаждения смещается в более щелочную область), а также от начальной концентрации (увеличение концентрации иона смещает pH начала его осаждения в кислую область).
На практике четкого разделения не происходит, в нерастворенной части гидроксидов остаются изоморфно соосажденные лантаноиды начала группы. Аналогичная картина наблюдается при разделении путем постепенного повышения pH добавлением щелочи. Четкость разделения размывается за счет изоморфного соосаждения, кроме того, в производствах трудно поддерживать величину pH с точностью до 0,1 - 0,2 единиц.
Увеличить четкость разделения РЗЭ возможно применением гомогенного осаждения, в результате получаются концентраты индивидуальных элементов.
Для выделения лантаноидов переменной устойчивой валентности, отличной от +3, используют методы окисления-восстановления. В этих случаях свойства лантаноида с переменной валентностью существенно изменяются, и его отделение происходит легче. Например, для церия и европия.
Восстановлением до двухвалентного состояния цинком или электрохимическим восстановлением на графитовом катоде выделяют европий (самарий, иттербий). Двухвалентные РЗЭ проявляют свойства, сходные с ионами щелочноземельных элементов, образуя осадок с сульфатными анионами. Полученный сульфат европия конвертируется в карбонат с последующим растворением в соляной кислоте и повторением цикла восстановление-осаждение-конверсия. Этот метод использовался при получении высокочистого европия на московском заводе Полиметалл [74, 75].
Извлечение церия из суммы РЗЭ с получением его концентрата возможно окислением Ce(III) до Ce(IV). В качестве окислителей используются перекись водорода, элементарный хлор, бром, перманганат и бромат калия, висмутата натрия, а также метод электрохимического окисления на платиновом аноде.
ИС МЕГАНОРМ: примечание. Здесь и далее в официальном тексте документа, видимо, допущена опечатка: имеется в виду п. [60] Библиографии, а не [59]. |
Первоочередное отделение церия решает две задачи: получение достаточно чистого его концентрата, а также снижает нагрузку на последующие процессы получения индивидуальных РЗЭ или их концентратов. Практически все схемы получения индивидуальных РЗЭ включали предварительное отделение превалирующего в концентрате церия с получением 99,0 - 99,9 оксида церия (ссылка на Иртыш). Технология электрохимического окисления церия была реализована на Иртышском химико-металлургическом заводе при переработке лопаритового концентрата Соликамского магниевого завода (Казахстан), технология окисления церия раствором перекиси водорода - на ПАО "Акрон" при переработке концентрата РЗЭ, выделенного из апатита [59].
Современные схемы разделения лантаноидов основаны на использовании эффективных методов: жидкостной экстракции и ионного обмена.
Метод ионного обмена в настоящее время используется для концентрирования, разделения и глубокой очистки РЗМ (возможно получение соединения чистотой 6N и выше). Применяются различные типы катионообменных смол. Они представляют собой сильнокислотные катиониты, получаемые совместной полимеризацией стирола и дивинилбензола, и содержат активные группы SO3H. Разделение осуществляют методом элюентной хроматографии.
Сродство ионов лантаноидов к смоле убывает от La3+ к Lu3+, т.е. в порядке уменьшения размера ионов. Однако сродство к смоле ионов РЗЭ очень близко, что не обеспечивает достаточно эффективного разделения. Лучшее разделение достигается при использовании для вымывания растворов, содержащих органические соединения, образующие с ионами РЗЭ комплексы различной устойчивости.
Вымывание происходит в последовательности, соответствующей прочности анионных комплексов лантаноидов. По мере движения вымывающего раствора вдоль колонки (или ряда последовательно соединенных колонок) смесь катионов разделяется на отдельные сорбционные зоны (полосы), перемещающиеся с определенной скоростью к ее выходу. На выходе из системы колонок фильтрат собирают отдельными фракциями. Для вымывания применяют различные органические соединения, образующие комплексы с лантаноидами: лимонную кислоту, нитрилотриуксусную кислоту (НТА) и этилендиаминтетрауксусную кислоту (ЭДТА). Последнюю наиболее широко применяют при хроматографическом разделении РЗЭ.
Для регенерации ЭДТА растворы подкисляют до pH 0,5 - 1. При этом комплексные соединения лантаноидов разрушаются и осаждается малорастворимая ЭДТА.
Для организации процесса разделения в колонных аппаратах используют методы: фронтального анализа, позволяющего получить небольшие количества наименее сорбируемого элемента в чистом виде. Метод элюирования, при котором в колонне образуются отдельные зоны всех разделяемых элементов, которые с разной скоростью перемещаются вдоль колонны. При достаточной длине колонны на выходе можно получить все разделяемые элементы в чистом виде, однако увеличение длины колонны приводит к образованию весьма разбавленных растворов. Вытеснительная хроматография позволяет образовать в колонне ряд последовательных зон, в которых находятся все разделяемые элементы. Зоны продвигаются вдоль колонны с постоянной скоростью (после их формирования на определенной длине аппарата) в порядке роста сродства элемента к смоле для данного состава раствора - впереди находится наименее сорбируемый ион. Скорость продвижения зон определяется скоростью подачи раствора иона - вытеснителя, который обладает наибольшим сродством к смоле и вытесняет с нее ранее сорбированные ионы разделяемой смеси. В таком режиме можно получить все разделяемые ионы в чистом виде, отбирая выходящий из колонки раствор элемента данной зоны, отсекая порции раствора, соответствующие участкам перекрывания зон соседних по сорбируемости элементов (впереди - менее сорбируемый, позади - более сорбируемый).
Метод ионообменной хроматографии внес переворот в разделение РЗМ. Открылись возможности получения чистых (до нескольких девяток после запятой) препаратов индивидуальных РЗМ, в количествах, достигающих для таких элементов, как Gd, Sm, Y нескольких тонн. Их цена резко снизилась, что позволило расширить поиски областей их практического применения.
Метод хроматографии позволяет получить индивидуальные РЗЭ высокой степени чистоты, однако он малопроизводителен. Поэтому большей частью РЗЭ предварительно разделяют другими методами, применяя ионный обмен для разделения и очистки смесей близких элементов.
Экстракционные методы разделения основаны на разнице в прочности комплексов лантаноидов с экстрагентами и являются в настоящее время основными в технологических схемах разделения РЗЭ.
2.20.10 Экстракционное разделение редкоземельных элементов
Экстракция - это распределение данного элемента (его соли) между двумя несмешивающимися жидкими фазами, одна из которых - органическая. Экстракция элемента характеризуется коэффициентом распределения (D):
D = Cо/Cв (2.47)
где C1 - концентрация элемента 1,
индексы о и в относятся к органической и водной фазам.
Коэффициент разделения (селективности) 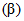 :
:
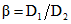 (2.48)
(2.48)где 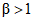 - элемент 1 преимущественно (по сравнению с элементом 2) переходит в органическую фазу.
- элемент 1 преимущественно (по сравнению с элементом 2) переходит в органическую фазу.
Коэффициент распределения (D) определяет преимущественное извлечение (последовательность) извлечения индивидуальных элементов в органическую фазу, коэффициент разделения  - число ступеней разделения в экстракционном каскаде, работающем в режиме противотока [71]. Многократное повторение процесса разделения в многоступенчатых, противоточных процессах приводит к практически полному разделению смеси элементов 1 и 2 (или группы элементов по границе элементов 1 - 2).
- число ступеней разделения в экстракционном каскаде, работающем в режиме противотока [71]. Многократное повторение процесса разделения в многоступенчатых, противоточных процессах приводит к практически полному разделению смеси элементов 1 и 2 (или группы элементов по границе элементов 1 - 2).
Известно три классических метода организации многоступенчатых процессов экстракционного разделения РЗЭ: 1) полупротивоток, 2) противоток, 3) экстракция с перекрестным током. Последний вариант практически не используется в промышленных схемах.
Полупротивоток характеризуется следующей организацией потоков водной и органической фаз: одна фаза находится в неподвижном состоянии, а вторая проходит через одну или N ступеней (ячеек) экстрактора, последовательно вымывая компоненты разделяемой смеси.
Для полупротивотока выделяют три основных способа организации процесса разделения.
1. Классический полупротивоток проводят следующим образом: на первую (нулевую) ступень вводят исходную смесь компонентов, а на все остальные ступени - промывной раствор. Органическая фаза (экстрагент) последовательно проходит через все ступени. Разделяемые компоненты смеси распределяются по ступеням каскада в соответствии с их величинами коэффициентов распределения.
2. Фронтальный - является зеркальным отражением классического полупротивотока. В этом случае разделяемая смесь проходит непрерывно через все ступени каскада и выходит из N-й ступени совместно с органической фазой. Последнюю вводят на нулевую ячейку при заполнении каскада исходным раствором.
3. Рациональный метод разделения - разделяемой смесью РЗЭ заполняют одну группу ячеек, а промывным раствором вторую группу ячеек. Органическая фаза последовательно протекает через все ячейки каскада. Все компоненты разделяемой смеси будут вымываться в порядке уменьшения величин коэффициентов распределения. При обращении фаз, когда неподвижной остается органическая фаза, а проходящей - водная, порядок вымывания меняется на противоположный: в первую очередь вымываются все хуже экстрагируемые компоненты.
Особенность полупротивоточных методов разделения смеси РЗЭ заключается в том, что они практически не отличаются от методов разделения ионным обменом или хроматографией. Это позволяет их использовать для получения особо чистых соединений индивидуальных РЗЭ, сколько угодно требуемой чистоты.
Противоток характеризуется движением обеих фаз через N ступеней (ячеек) экстрактора в противоположных направлениях (принцип полного противотока). При проведении полного противотока.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: текст п.п. 2.20.8 и 2.20.9 приведен дважды. |
2.20.8 Технология получения РЗЭ из вторичного магнитного сырья
Перспективным источником РЗЭ является вторичное магнитное сырье (МС), к которому относятся отходы производства и потребления постоянных магнитов Nd-Fe-B и Sm-Co, а также магнитные материалы, выделенных из радиоэлектронного лома (РЭЛ). МС имеет сложный состав, который варьируется в широких пределах. Кроме лигатур и производных на базе интерметаллидов Nd(РЗЭ)2Fe14B, Sm(РЗЭ)Co5, Sm2(РЗЭ)Co17, где в качестве легирующих добавок РЗЭ чаще всего выступают празеодим, тербий и диспрозий, в нем также содержатся никель, медь, алюминий, кремний и другие примеси в виде металлов и оксидов. Основную массу МС составляют отходы от операции шлифования заготовок - шлифотходы, содержащие помимо магнитных материалов абразивные частицы шлифинструмента и водно-органические эмульсии смазочно-охлаждающих жидкостей (СОЖ). Выход шлифотходов от массы готовых магнитов оценивается в 10 - 40%.
Вовлечение МС в переработку позволяет: увеличить сырьевую базу РЗЭ; вернуть в производственный цикл наиболее ценные Nd, Tb и Dy; утилизировать пожароопасные шлифотходы, хранящиеся на складах заводов-изготовителей магнитов. Однако до настоящего времени уровень переработки МС в России не превышал 1% и поддерживался переплавкой крупнокусковых отходов в готовую продукцию или получением полиметаллических концентратов из РЭЛ.
Для решения проблемы рециклинга материалов магнитной и радиоэлектронной промышленности специалистами ООО "ЛИТ" (ГК "Скайград") совместно с ООО "ПромТехРециклинг" разработана и запатентована [69, 70] гидрометаллургическая технология переработки МС, включающая:
1. предварительную подготовку сырья - дробление/измельчение кусковых МС, очистку шлифотходов от абразивных частиц и СОЖ;
2. растворение МС в растворе азотной кислоты с одновременной карбамидной денитрацией отходящих газов;
3. экстракционное извлечение РЗЭ с получением группового редкоземельного концентрата (ГРЗК).
Технология принимает во внимание специфику ранее предложенных способов переработки МС, но в отличие от них характеризуется меньшими материало- и энергозатратами, низким содержанием токсичных веществ в отходящих газах, оперирует использованием высокоэффективного оборудования.
Согласно разработанной технологии предварительную подготовку шлифотходов осуществляют путем магнитной сепарации (для отделения немагнитной фракции абразивных частиц) с последующей ступенчатой вакуумной термообработкой магнитной фракции: сначала при температуре не выше 100 °C (для отгонки воды), а затем - при 300 - 350 °C (для отгонки масла СОЖ). При этом вакуумную термообработку ведут в присутствии добавки жидкого нефтяного парафина, снижающего температуру кипения труднолетучих составляющих масла. Указанная совокупность приемов позволяет сократить нагрузку на печное оборудование, избежать использования дорогостоящих печей нетиповой конструкции, предотвратить переход железа в окисленную форму, инертную по отношению к минеральным кислотам, что особенно важно при последующем гидрометаллургическом переделе с экстракционным извлечением суммы РЗЭ (гидратированные ионы Fe3+ являются высаливателями, увеличивающими эффективность экстракции).
Для перевода МС в жидкую форму порошки от стадии предварительной подготовки порционно вводят в раствор, содержащий 3,5 - 5,5 моль/л азотной кислоты и по меньшей мере стехиометрическое количество карбамида. Растворение ведут при температуре 55 - 65 °C и барботаже пульпы воздухом. Выбранные условия минимизируют выход нерастворимого остатка и расход реагентов на побочные реакции, исключают выпадение осадка нитрата карбамида, способствуют оптимальной интенсивности растворения МС, обеспечивают эффективную конверсию отходящих нитрозных газов в безвредные продукты (что позволяет избежать использования специального газоочистного оборудования, оснащенного дорогостоящими катализаторами на основе металлов платиновой группы). Процесс описывается следующими реакциями:
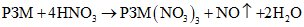 (2.49)
(2.49)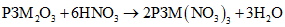 (2.50)
(2.50)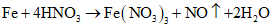 (2.51)
(2.51)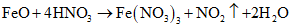 (2.52)
(2.52)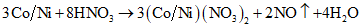 (2.53)
(2.53)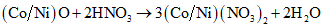 (2.54)
(2.54)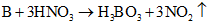 (2.55)
(2.55)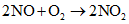 (2.56)
(2.56)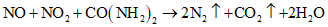 (2.57)
(2.57)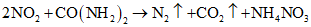 (2.58)
(2.58)Для завершения денитрации и дорастворения МС пульпу выдерживают при 70 - 75 °C в течение 30 мин. По окончании выдержки в жидкую часть пульпы переходит >= 99,5% РЗЭ, а в твердую - высшие окислы железа и механические примеси. Полученную пульпу при необходимости упаривают до достижения оптимальной концентрации Fe3+, доводят до кислотности 20 - 25 г/л, после чего разделяют фильтрацией. Нерастворимый остаток промывают водой и утилизируют, а раствор МС направляют дальнейший экстракционный передел.
Экстракционное извлечение РЗЭ из раствора МС реализуют в непрерывно действующем противоточном каскаде центробежных экстракторов, наиболее экономичных с точки загрузки экстрагента и объема незавершенного производства по сравнению с экстракторами других типов. В качестве экстрагента используют раствор трибутилфосфата (ТБФ) в инертном разбавителе. Селективность извлечения обеспечивается свойством РЗЭ образовывать сольватные комплексы с ТБФ (экстрагироваться) в азотнокислой среде:
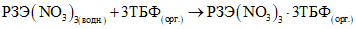 . (2.59)
. (2.59)Остальные компоненты раствора МС не экстрагируются (остаются в рафинате) и выполняют роль высаливателей. Обратное извлечение РЗЭ из органической фазы в водную (реэкстракция) происходит при контакте экстракта со слабым раствором кислоты:
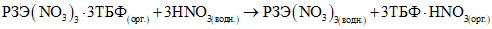 (2.60)
(2.60)Переход от экстракции к реэкстракции осуществляют через промежуточную стадию - стадию промывки экстракта - поскольку насыщенный экстрагент содержит некоторое количество соэмульгированных нередкоземельных примесей. В ходе промывки водой помимо очистки от примесей происходит и частичная реэкстракция РЗЭ, поэтому промывные воды (рафинат промывки) не выводят из процесса, а возвращают на стадию экстракции.
Высокое сквозное извлечение РЗЭ из раствора МС в реэкстракт (>= 99,5%) достигается многократным контактом водной и органической фаз в режиме противотока. В ходе работы каскада экстрагент, исходный раствор МС, промывной и реэкстрагирующий растворы непрерывно подаются в него дозирующими насосами, а продукционные растворы - рафинат и реэкстракт (раствор ГРЗК) - поступают в приемные емкости самотеком. Выходящий экстрагент возвращают в начало процесса.
Полученный ГРЗК содержит >= 99,9% основного вещества и пригоден для последующего экстракционного разделения на индивидуальные РЗЭ. Рафинаты от стадии экстракционного извлечения могут быть переработаны в попутную, в том числе Co-содержащую продукцию.
Технология прошла успешные испытания на опытно-промышленных участках ООО "ЛИТ" и ООО "ПромТехРециклинг".
2.20.9 Основные методы разделения концентратов РЗЭ на группы и индивидуальные элементы
Редкоземельные элементы в том или ином соотношении всегда встречаются вместе во всех сырьевых источниках, но практически никогда не потребляются в виде природной смеси. Поэтому их разделение вследствие близости свойств - сложная задача.
Исторически первым основным способом разделения и получения отдельных редкоземельных элементов был метод дробной кристаллизации. Суть дробной кристаллизации заключается в проведении большого числа стадий кристаллизации с разделением на каждой стадии твердой и жидкой фаз. Осадки при этом обогащаются менее растворимыми элементами, а растворы - более растворимыми. [58]. В эпоху первооткрывателей был хорошо известен способ разделения РЗЭ на цериевую и иттриевую группы (среднетяжелую) фракционным осаждением двойных сульфатов. Осаждение двойных сульфатов оказалось перспективным из-за значительной разницы в растворимости соединений РЗЭ в насыщенных растворах сульфатов щелочных элементов и аммония. До недавнего времени метод широко применялся на практике. Наименьшей растворимостью в насыщенных растворах сульфатов щелочных элементов обладают двойные сульфаты РЗЭ цериевой группы (La - Sm), немного лучше растворяются одноименные соединения Eu - Tb, а элементы иттриевой подгруппы Dy - Yb и Y наиболее растворимы. Обычно двойным сульфатам (некоторые авторы относят их к комплексным солям) приписывают формулу:
xR2(SO4)3·yM2SO4·zH2O (2.61),
где R - редкоземельный металл;
M - K, Na, NH4+;
x, y, z - переменные коэффициенты.
Для более четкого разделения в процессе осаждения двойных сульфатов было предложено добавлять в раствор комплексообразователь - двунатриевую соль этилендиаминтетрауксусной кислоты (трилон Б), этилендиаминтетрауксусную кислоту, ацетат аммония или [39]. С помощью такого процесса были получены 99,99% концентраты Gd, Dy, 99,9% - Ho, Lu и 97% Tb.
Методом дробной кристаллизации возможно разделение двойных нитратов РЗЭ и магния, аммония или марганца. Трудоемкий, длительный, процесс позволяет получить более чистые препараты отдельных РЗЭ, чем метод осаждения. Для разделения дробной кристаллизацией часто использовали броматы (Ln)BrO3·9H2O, диметилфосфаты Ln[(CH3)2PO4]3, двойные нитраты 2Ln(NO3)3·3Mg(NO3)2·24H2O, Ln(NO3)3·2NH4NO3·4H2O [19].
Метод осаждения гидроксидов также позволяет разделить РЗЭ на концентраты. Следует учитывать, что pH осаждения гидроксидов того или иного элемента из растворов зависит от прочности его соединений с анионами (комплексообразователями), присутствующими в этом растворе (с увеличением прочности комплекса pH осаждения смещается в более щелочную область), а также от начальной концентрации (увеличение концентрации иона смещает pH начала его осаждения в кислую область).
На практике четкого разделения не происходит, в нерастворенной части гидроксидов остаются изоморфно соосажденные лантаноиды начала группы. Аналогичная картина наблюдается при разделении путем постепенного повышения pH добавлением щелочи. Четкость разделения размывается за счет изоморфного соосаждения, кроме того, в производствах трудно поддерживать величину pH с точностью до 0,1 - 0,2 единиц.
Увеличить четкость разделения РЗЭ возможно применением гомогенного осаждения, в результате получаются концентраты индивидуальных элементов.
Для выделения лантаноидов переменной устойчивой валентности, отличной от +3, используют методы окисления-восстановления. В этих случаях свойства лантаноида с переменной валентностью существенно изменяются, и его отделение происходит легче. Например, для церия и европия.
Восстановлением до двухвалентного состояния цинком или электрохимическим восстановлением на графитовом катоде выделяют европий (самарий, иттербий). Двухвалентные РЗЭ проявляют свойства, сходные с ионами щелочноземельных элементов, образуя осадок с сульфатными анионами. Полученный сульфат европия конвертируется в карбонат с последующим растворением в соляной кислоте и повторением цикла восстановление-осаждение-конверсия. Этот метод использовался при получении высокочистого европия на московском заводе Полиметалл [74, 75].
Извлечение церия из суммы РЗЭ с получением его концентрата возможно окислением Ce(III) до Ce(IV). В качестве окислителей используются перекись водорода, элементарный хлор, бром, перманганат и бромат калия, висмутата натрия, а также метод электрохимического окисления на платиновом аноде.
Первоочередное отделение церия решает две задачи: получение достаточно чистого его концентрата, а также снижает нагрузку на последующие процессы получения индивидуальных РЗЭ или их концентратов. Практически все схемы получения индивидуальных РЗЭ включали предварительное отделение превалирующего в концентрате церия с получением 99,0 - 99,9 оксида церия (ссылка на Иртыш). Технология электрохимического окисления церия была реализована на Иртышском химико-металлургическом заводе при переработке лопаритового концентрата Соликамского магниевого завода (Казахстан), технология окисления церия раствором перекиси водорода - на ПАО "Акрон" при переработке концентрата РЗЭ, выделенного из апатита [59].
Современные схемы разделения лантаноидов основаны на использовании эффективных методов: жидкостной экстракции и ионного обмена.
Метод ионного обмена в настоящее время используется для концентрирования, разделения и глубокой очистки РЗМ (возможно получение соединения чистотой 6N и выше). Применяются различные типы катионообменных смол. Они представляют собой сильнокислотные катиониты, получаемые совместной полимеризацией стирола и дивинилбензола, и содержат активные группы SO3H. Разделение осуществляют методом элюентной хроматографии.
Сродство ионов лантаноидов к смоле убывает от La3+ к Lu3+, т.е. в порядке уменьшения размера ионов. Однако сродство к смоле ионов РЗЭ очень близко, что не обеспечивает достаточно эффективного разделения. Лучшее разделение достигается при использовании для вымывания растворов, содержащих органические соединения, образующие с ионами РЗЭ комплексы различной устойчивости.
Вымывание происходит в последовательности, соответствующей прочности анионных комплексов лантаноидов. По мере движения вымывающего раствора вдоль колонки (или ряда последовательно соединенных колонок) смесь катионов разделяется на отдельные сорбционные зоны (полосы), перемещающиеся с определенной скоростью к ее выходу. На выходе из системы колонок фильтрат собирают отдельными фракциями. Для вымывания применяют различные органические соединения, образующие комплексы с лантаноидами: лимонную кислоту, нитрилотриуксусную кислоту (НТА) и этилендиаминтетрауксусную кислоту (ЭДТА). Последнюю наиболее широко применяют при хроматографическом разделении РЗЭ.
Для регенерации ЭДТА растворы подкисляют до pH 0,5 - 1. При этом комплексные соединения лантаноидов разрушаются и осаждается малорастворимая ЭДТА.
Для организации процесса разделения в колонных аппаратах используют методы: фронтального анализа, позволяющего получить небольшие количества наименее сорбируемого элемента в чистом виде. Метод элюирования, при котором в колонне образуются отдельные зоны всех разделяемых элементов, которые с разной скоростью перемещаются вдоль колонны. При достаточной длине колонны на выходе можно получить все разделяемые элементы в чистом виде, однако увеличение длины колонны приводит к образованию весьма разбавленных растворов. Вытеснительная хроматография позволяет образовать в колонне ряд последовательных зон, в которых находятся все разделяемые элементы. Зоны продвигаются вдоль колонны с постоянной скоростью (после их формирования на определенной длине аппарата) в порядке роста сродства элемента к смоле для данного состава раствора - впереди находится наименее сорбируемый ион. Скорость продвижения зон определяется скоростью подачи раствора иона - вытеснителя, который обладает наибольшим сродством к смоле и вытесняет с нее ранее сорбированные ионы разделяемой смеси. В таком режиме можно получить все разделяемые ионы в чистом виде, отбирая выходящий из колонки раствор элемента данной зоны, отсекая порции раствора, соответствующие участкам перекрывания зон соседних по сорбируемости элементов (впереди - менее сорбируемый, позади - более сорбируемый).
Метод ионообменной хроматографии внес переворот в разделение РЗМ. Открылись возможности получения чистых (до нескольких девяток после запятой) препаратов индивидуальных РЗМ, в количествах, достигающих для таких элементов, как Gd, Sm, Y нескольких тонн. Их цена резко снизилась, что позволило расширить поиски областей их практического применения.
Метод хроматографии позволяет получить индивидуальные РЗЭ высокой степени чистоты, однако он малопроизводителен. Поэтому большей частью РЗЭ предварительно разделяют другими методами, применяя ионный обмен для разделения и очистки смесей близких элементов.
Экстракционные методы разделения основаны на разнице в прочности комплексов лантаноидов с экстрагентами и являются в настоящее время основными в технологических схемах разделения РЗЭ.
2.20.10 Экстракционное разделение редкоземельных элементов
Экстракция объединяет в одном каскаде два процесса - экстракционное извлечение и промывку. В этом случае исходный водный питающий раствор подают в центральную часть каскада, промывной раствор - в конец промывного каскада, а органическую фазу, проходящую противотоком к водной фазе - в начало экстракционного каскада.
Противоточный процесс разделения РЗЭ можно проводить тремя способами:
- по схеме простого противотока (экстракция одним растворителем);
- по схеме полного противотока (экстракция двумя растворителями);
- фракционной экстракцией с накоплением среднего компонента или некоторой смеси компонентов в центральной части противоточного каскада.
В соответствии с первым методом водная или органическая фаза, содержащая разделяемую смесь РЗЭ, движется противотоком органической фазе (соответственно водной фазе) через ячейки противоточного каскада. При такой организации процесса на одном экстракционном каскаде возможно получение одного чистого компонента и одного концентрата РЗЭ, обогащенного по второму компоненту (компонентам).
При использовании метода полного противотока экстракционный каскад разделяют на две части: экстракционную и промывную. Исходный раствор смеси РЗЭ подают в середину полного каскада, промывной раствор - на последнюю ступень промывной части каскада, а органическую фазу на первую ступень экстракционной части каскада. Промывной раствор, прошедший через промывную часть каскада, смешивается с питающим раствором в центральной части всего противоточного каскада. При такой организации потоков возрастает чистота разделяемых компонентов и при содержании только двух компонентов, достигается их полное разделение и получение соединений РЗЭ с заданной степенью чистоты.
Разделение с одновременным накоплением среднего компонента позволяет на одном экстракционном противоточном каскаде получать три чистых продукта. Для достижения этих целей коэффициенты распределения в промывной части каскада выбирают такими, чтобы для одного из разделяемых компонентов тройной смеси (например, компонента 2) коэффициент экстракции в экстракционной части каскада был больше 1, а в промывной - меньше 1. Процесс проводят до расчетного уровня накопления, а затем вместо исходного раствора подают промывной раствор и отмывают средний продукт от компонентов 1 и 3.
Применение этого метода позволяет в значительной степени сократить число экстракционных разделительных ступеней, снизить потребление экстрагента и улучшить экономические показатели экстракционного производства.
В настоящее время для экстракционного разделения РЗЭ используют растворы индивидуальных экстрагентов различных классов в инертном разбавителе, а также растворы их смесей подходящего состава. Наибольшее распространение получили следующие группы экстрагентов:
- нейтральные фосфорорганические соединения (НФОС);
- нейтральные соединения (НС);
- фосфорорганические кислоты (ФОК);
- карбоновые кислоты (КК);
- амины и соли аминов;
- четвертичные аммониевые соли (ЧАС);
- хелатные экстрагенты (ХЭ);
Экстракция смесями экстрагентов может быть отнесена к трем большим группам:
- экстракция синергетными смесями экстрагентов;
- бинарная экстракция;
- экстракция в присутствии хелатного или комплексообразующего агента.
В некоторых случаях для экстракции РЗЭ могут быть использованы тройные смеси экстрагентов, например, два нейтральных и один катионообменный или анионообменный. Зачастую второй нейтральный экстрагент играет роль модификатора для повышения растворимости экстрагируемого смешанного комплекса металла с двумя другими экстрагентами. Часто в этой роли используют высшие спирты (ВС) или ТБФ.
В технологии РЗЭ применяется синергетная экстракция. Это экстракция смесями двух экстрагентов, зародилась в середине 1950-х гг., и в настоящее время широко применяется для разделения РЗЭ. Ее особенностью является неаддитивное увеличение коэффициентов распределения и разделения целевых компонентов из растворов сложного солевого состава при использовании смеси двух экстрагентов различных классов.
При проведении бинарной экстракции применяются бинарные смеси анионообменного и катионообменного экстрагентов. Для бинарной экстракции в качестве экстрагента используют нерастворимые в водной фазе соли, состоящие из аниона органической кислоты, связанного с катионом органического основания, например, карбоксилат четвертичного аммониевого основания (ЧАО). Бинарный экстрагент образует прочную ионную связь между катионом и анионом только в определенной для каждой пары области pH равновесной водной фазы: в щелочных, нейтральных и слабокислых растворах. При понижении pH за счет введения в растворы неорганических кислот происходит протонизация органической кислоты и присоединение ее противоиона к катиону органического основания. В результате этого процесса, протекающего при повышении кислотности водного раствора, бинарный экстрагент распадается на смесь двух экстрагентов - анионообменного и катионообменного. Часто такие смеси проявляют синергетный эффект при извлечении РЗЭ из водных растворов. Соответственно бинарные экстрагенты будут также рассматриваться как смеси двух экстрагентов, образующиеся при определенных условиях экстракции.
Одним из вариантов экстракции РЗЭ является введение в водный раствор комплексообразователя того или иного типа, растворимого в водной фазе и образующего с ионом РЗМ комплексное соединение. Затем водорастворимый комплекс извлекают из водной фазы экстрагентом с образованием в органической фазе смешанного, как правило, комплексного соединения. Такая экстракция также будет рассматриваться как экстракция смесями экстрагентов.
В технологии разделения РЗЭ применяют экстракционные системы всех классов - нейтральные эфиры, органические производные фосфорной кислоты, органические кислоты и органические основания (амины), бинарные экстрагенты, ионные жидкости и хелатирующие экстрагенты [40]. Перечень промышленных экстрагентов, используемых в технологии разделения РЗЭ, приведен в таблице 2.13.
Таблица 2.13
в технологии разделения РЗЭ
Наименование Фирменное название | Химическое название | Химическая формула | Содержание, % |
Нейтральные фосфорорганические соединения (НФОС) | |||
ТБФ | Три-н-бутилфосфат | (n-C4H9O)3P=O | 100 |
Катионообменные экстрагенты | |||
Д2ЭГФК | Ди-(2-этилгексил)-фосфорная кислота | [(C6H13(C2H5)O]2P(O)OH | 67 - 99,8 |
ИДДФК | Изо-додецилфосфетановая кислота | 70 - 80 | |
ВИКК | Высшие  кислоты кислоты | H(CH2-CH2)n(C2H5)(C4H9)C(O)OH | > 98 |
Versatic 10 |  кислота кислота | R1R2R3C(O)OH | 99 |
Р-507, РС-88А М2ЭГ(2ЭГ)ФК | Моно-2-этилгексиловый эфир 2-этилгексил-фосфоновой кислоты | [(C6H13(C2H5)O](C6H13(C2H5)P(O)OH | |
CYANEX572 | Смесь бис-2,4,4-триметилпентил фосфиновая кислота и моно-2-этилгексил фосфоновый эфир моно-2-этилгексил фосфоновой кислоты, Диизобутилен | (CH3)2CHCH2CH2(CH3)CH2]2PO(OH (C6H13(C2H5)O](C6H13(C2H5))P(O)OH (CH3) 3CCH2C (CH3) = CH2 | 25 - 75 25 - 75 0 - 2 |
Анионообменные экстрагенты | |||
ТАМАН | Метилтриалкиламмоний нитрат | CH3(C7H15-C9H19)3NNO3 | > 96 |
ТАА | Триалкиламин | (C7H15-C9H19)3N | 70 - 98 |
 | Трикаприметиламмоний хлорид | (H3C)2NH-CH3)-Cl | >= 98 |
В экстракционной технологии разделения РЗЭ подбирают такие экстрагенты и их смеси, которые обеспечивают приемлемые (>= 1,5) коэффициенты разделения соседних элементов 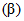 , высокое насыщение органической фазы без образования твердых солей и эмульсий при быстром разделении фаз, незатрудненную реэкстракцию и регенерацию экстрагента [58, 59].
, высокое насыщение органической фазы без образования твердых солей и эмульсий при быстром разделении фаз, незатрудненную реэкстракцию и регенерацию экстрагента [58, 59].
Новые возможности для эффективного разделения РЗЭ появились в связи с синтезом фосфорорганических экстрагентов, включающих нейтральные или кислые эфиры ортофосфорной кислоты или ее производных.
В этой связи остается актуальным поиск новых синергетных смесей широко известных и хорошо зарекомендовавших себя реагентов для решения новых задач по извлечению и разделению РЗЭ.
Таким образом, экстракционное разделение РЗЭ будет определяться следующими наиболее важными факторами:
- селективностью экстракционной системы, включающей как один экстракционный реагент, так и синергетную смесь экстрагентов;
- составом водной фазы, включающим прежде всего анионную составляющую водной среды (как правило, хлоридные, роданидные или нитратные среды, в отдельных случаях сульфатная среда);
- наличием высаливающих реагентов;
- наличием промышленных экстрагентов для подбора селективной экстракционной системы;
- методом экстракционного разделения или способом организации экстракционного каскада;
- подбором экстракционного оборудования для создания многоступенчатых противоточных (полупротивоточных) каскадов экстракторов (в настоящее время для этих целей используют, как правило, смесители-отстойники ящичного типа различной конструкции или центробежные экстракторы).
К перечисленным факторам необходимо добавить мероприятия по эффективному разделению фаз с целью разрушения микроэмульсий и повышения степени очистки и разделения РЗЭ в данной экстракционной системе, а также снижения потерь экстрагента. Важным фактором экономического порядка является стоимость экстрагентов, разбавителей, минеральных кислот, в среде которых проводят разделение, высаливателя. Также необходимо учитывать экологические аспекты жидкостной экстракции. Значительные затраты любого экстракционного передела связаны с мероприятиями по пожарной безопасности, так как практически большинство промышленно применяемых разбавителей пожароопасны.
При подборе оборудования для проведения жидкостной экстракции в коррозионно-активных средах необходимо учитывать стоимость материалов, из которых изготовлены экстракторы (в настоящее время это, как правило, полимерные материалы: полипропилен, фторопласт), их устойчивость к коррозионным средам и возможность их использования при повышенных температурах.
В практике разделения РЗЭ экстракцией большей частью процесс проводят в аппаратах типа "смеситель - отстойник", соединяемых в каскад. Однако с развитием инженерных технологий все большее применение находят экстрактора центробежного типа, что связано с их несомненным преимуществом в части экономии затрат на реактивы и незавершенное производство. Разделение ведут, используя различные известные способы: метод противотока и варианты динамических методов, полупротивоток [72, 73].
В промышленной практике для разделения используют преимущественно фосфорорганические экстрагенты - нейтральные эфиры и фосфорорганические кислоты в разбавителе. В качестве разбавителей используют углеводородную смесь с содержанием ароматических соединений <= 0,01% и фракционным составом: начало кипения - 150 - 240 °C, конец кипения - 253 - 305 °C. Наиболее широко известный экстрагент - ТБФ. При его использовании для разделения РЗЭ на подгруппы процесс ведут из слабокислых (HNO3 - 25 - 30 г/л) или азотнокислых растворов (6 - 8 NHNO3) и содержании РЗЭ в растворе >= 380 г/л, см. таблицу 2.14 ниже.
Таблица 2.14
двух соседних элементов при экстракции 50% ТБФ
Концентрация РЗЭ в водной фазе; г-экв/л | Фактор разделения | ||||||||
Ce/La | Pr/Ce | Nd/Pr | Sm/Nd | Gd/Sm | Dy/Gd | Ho/Dy | Er/Ho | Yb/Er | |
8,4 | 1,7 | 1,75 | 1,5 | 2,26 | 1.01 | 1,45 | 0,92 | 0,96 | 0,81 |
7,5 | - | - | - | - | - | 1,2 | 0,96 | 0,65 | - |
5,5 | - | - | - | 2,04 | 1,07 | 1,17 | 0,94 | 0,82 | - |
3,8 | - | - | - | 1,55 | 0,99 | 1,08 | 0,89 | 0,78 | - |
2,2 | - | - | - | 1,58 | 0,82 | 0,92 | 0,83 | 0,72 | - |
1.0 | - | - | - | 1,4 | 0,78 | 0,89 | 0,77 | 0,7 | 0,63 |
При этом иттрий попадает в подгруппу тяжелых РЗЭ (Dy-Lu). Помимо нитратных растворов, для разделения РЗЭ экстракцией ТБФ используют роданидно-хлоридные растворы (получение иттрия).
ИС МЕГАНОРМ: примечание. Нумерация пунктов дана в соответствии с официальным текстом документа. |
2.20.10 Общие схемы разделения редкоземельных элементов из суммарных концентратов
Выделенные из минерального сырья суммарные концентраты оксидов РЗЭ содержат иттрий и 14 элементов от лантана до лютеция. Для получения каждого индивидуального лантаноида необходимо провести разделение по линиям предыдущий Ln/данный Ln и последующий Ln/данный Ln. Для повышения эффективности выделения индивидуальных РЗЭ проводят их предварительное разделение из суммарных концентратов на группы или групповые концентраты. Традиционно выделяют группу легких РЗЭ (легкую группу): лантан, церий, празеодим, неодим, группу средних РЗЭ (среднюю группу): самарий, европий, гадолиний и группу тяжелых РЗЭ (тяжелую группу): от тербия до лютеция. Иттрий относят к той группе, в которой он концентрируется в разделительном процессе: либо к легкой, либо к тяжелой группе. Часто среднюю и тяжелую группу объединяют в одну среднетяжелую группу.
В соответствии с приведенной выше классификацией РЗЭ на группы, общие схемы разделения суммарных концентратов РЗЭ включают на первом этапе групповые разделения. Традиционно первым разделительным процессом является разделение концентрата РЗЭ на легкую и среднетяжелую группы по линии Nd/Sm, (см. рисунке 2.15), [59]. Иттрий в зависимости от состава разделительной системы может сопутствовать как легкой, так и тяжелой группам РЗЭ, что обозначено на рисунке заключением символа Y в круглые скобки - (Y).
Вторым разделительным процессом обычно является разделение среднетяжелой группы РЗЭ на среднюю и тяжелую группы по линии Gd/Tb или Tb/Dy. В дальнейшем выделение индивидуальных РЗЭ проводят для каждой группы отдельно с учетом химических свойств элементов, попадающих в ту или иную группу и потребительским запросом заказчика. Прежде всего это касается церия и европия, изменение валентных форм которых, позволяет их выделять из суммы легких (Ce) или средних (Eu) РЗЭ осадительными методами.
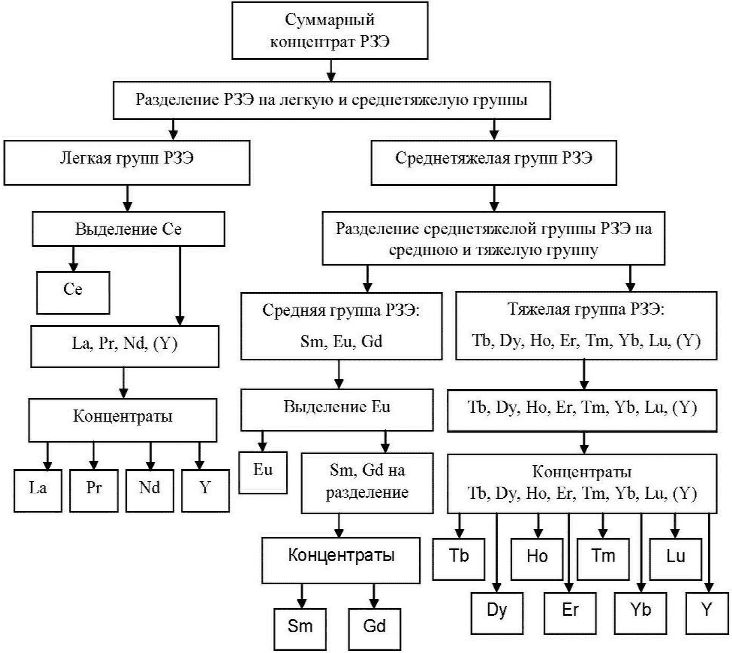
из суммарных концентратов, выделенных из различных видов
минерального сырья
После выделения церия и европия химическими методами для каждой группы РЗЭ проводят экстракционное разделение на индивидуальные элементы. В одном разделительном каскаде не удается получить чистыми все РЗЭ, процесс разделения может быть разбит на получение концентратов с высоким содержанием (как правило, более 60%) одного из разделяемой пары элементов и последующим выделением этих элементов из полученных концентратов в чистом виде.
Для тяжелой группы РЗЭ, включающей 7 из 14 РЗЭ и иттрий, проводят дополнительное разделение по линии Ho/Er, разграничивающей соответствующие тетрады: Gd, Tb, Dy, Ho и Er, Tm, Yb, Lu.
Таким образом, разделение тяжелой группы РЗЭ может быть проведено еще на две подгруппы с последующим выделением индивидуальных тяжелых РЗЭ и иттрия из этих подгрупп.
В общем случае при получении индивидуальных элементов из суммарных концентратов РЗЭ, содержащих 14 элементов и иттрий, необходимо осуществить многоступенчатый процесс разделения ближайших пар элементов в противоточных экстракционных каскадах с промывкой. Число ступеней в каскаде определяется коэффициентом разделения пары разделяемых элементов и чистотой получаемой продукции.
2.20.11 Аппаратура, принципы выбора типа экстракционного оборудования
Для проведения процесса экстракции предложено множество конструкций аппаратов, однако только некоторые из них нашли широкое применение в промышленности в целом, и в технологии РЗЭ в частности.
Аппаратура для экстракции может иметь разное конструктивное исполнение. Широко известны и распространены аппараты типа смеситель-отстойник, экстракторы колонного типа и центробежные экстракторы. По характеру изменения состава жидких фаз экстракционные аппараты подразделяются на две большие группы: экстракторы дифференциально-контактного типа с непрерывным изменением состава фаз и экстракторы ступенчатого типа с дискретным контактом фаз, в котором на каждой ступени происходит смешение, а затем разделение фаз.
Дифференциально-контактные экстракторы
В непрерывном дифференциально-контактном оборудовании противоток достигается благодаря различию в плотности водной и органической фаз. Эти аппараты, как правило не сложны по конструкции. Простейшим из них является распылительная колонна, в которой одна из фаз (дисперсная) распределяется в другой фазе (сплошной) в виде мелких капель. Этот экстрактор малоэффективен из-за захвата и уноса сплошной фазы дисперсной фазой. Эффективность экстракционной колонны характеризуется высотой эквивалентной теоретической ступени (ВЭТС). ВЭТС соответствует такому отрезку колонны, в котором выходящая органическая фаза равновесна с водной фазой, входящей с противоположного конца участка. Чтобы уменьшить ВЭТС колонны применяют насадку, которая уменьшает рециркуляцию сплошной фазы и способствует коалесценции и редиспергированию дисперсной фазы. Для этой же цели используют ситчатые тарелки. Наиболее эффективными оказались так называемые тарелки КРИМЗ, которые создают вращательное движение жидкости, приводящее к уменьшению продольного перемешивания.
В тарельчатых колонках органическая фаза (легкая) подается снизу через диспергатор, а водная - тяжелая, подается сверху. При движении вверх органическая фаза многократно дробится и коалесцирует, для этого в колонне устанавливают тарелки различного типа и насадочные устройства для интенсификации массообменного процесса, фазы в колонне могут перемешиваться воздухом или другим инертным газом. Органическая фаза вверху колонны попадает в отстойную зону и из нее самотеком выводится из колонны, водная фаза выводится из нижней зоны колонны, лежащей ниже подачи экстрагента эрлифтом или через гидрозатвор. Такая колонна имеет обычно большую ВЭТС в пределах 2,5 - 3,0 м и, соответственно, небольшое число ступеней [59]. На таких колоннах можно проводить экстракцию хорошо экстрагируемых веществ, имеющих большой коэффициент распределения.
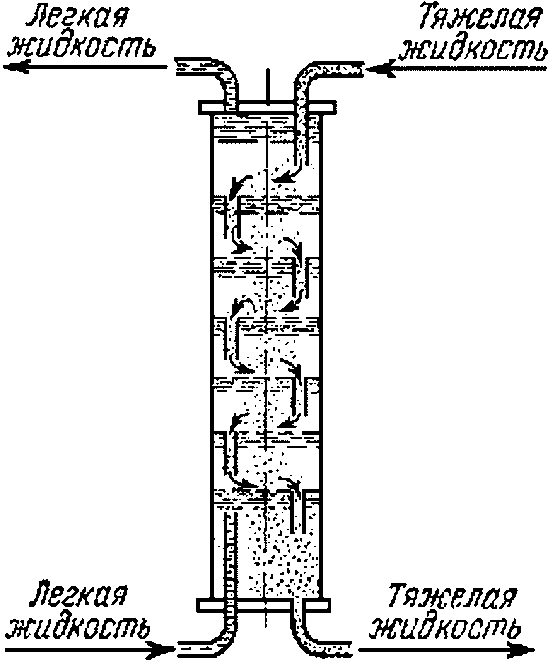
Рисунок 2.16 - Ситчатый колонный экстрактор
Смесительно-отстойные экстракторы
Каждая ступень смесительно-отстойного экстрактора состоит из смесителя, где жидкости перемешиваются до состояния, возможно более близкого к равновесному, и отстойника, где происходит отделение экстракта от рафината. В пределах ступени фазы движутся прямотоком друг к другу, но установка в целом, состоящая из любого числа последовательно соединенных ступеней, работает при противоточном движении фаз. Ступени аппарата располагаются в одной горизонтальной плоскости (рис. 2.17) или устанавливаются в виде каскада [59, 81].
1 - смеситель; 2 - отстойник; а - легкая фаза;
б - тяжелая фаза; в - конечный продукт (тяжелая фаза);
г - конечный продукт (легкая фаза)
Принцип работы смесительно-отстойного экстрактора: легкая фаза "а" подается в смеситель 1 первой ступени, куда параллельным током поступает тяжелая фаза из отстойника 2 следующей (второй) ступени. После смешения фазы расслаиваются в отстойнике первой ступени, из которого тяжелая фаза отводится в качестве конечного продукта "в", а легкая фаза направляется во вторую ступень. Здесь она смешивается со свежей тяжелой фазой "б" и отделяется от нее в отстойнике 2 второй ступени. Из этого отстойника сверху удаляется легкая фаза (конечный продукт "г"), а снизу отводится тяжелая фаза, поступающая на смешение в первую ступень.
Перемещение и смешение жидкостей может производиться не только с помощью механических мешалок, но и посредством насосов, инжекторов и другими способами. Точно также разделение фаз можно осуществлять не только в гравитационных отстойниках, но и в сепараторах центробежного типа, например, в гидроциклонах или центрифугах. Поэтому число вариантов конструкций смесительно-отстойных экстракторов велико.
Так, для того чтобы уменьшить площадь, занимаемую аппаратом, применяют компактные ящичные экстракторы. В ящичном экстракторе (рис. 2.18) все ступени расположены в общем корпусе прямоугольного сечения. Тяжелая фаза поступает в смеситель, расположенный в правом верхнем углу корпуса, и удаляется снизу из крайнего отстойника с левой стороны корпуса. Как видно из рисунка, в аппарате легкая фаза движется противотоком к тяжелой. Тяжелая фаза (см. сечение по А-А) удаляется через гидравлический затвор из нижней части отстойника в следующий смеситель, а легкая фаза переливается через порог и отводится из верхней части отстойника.
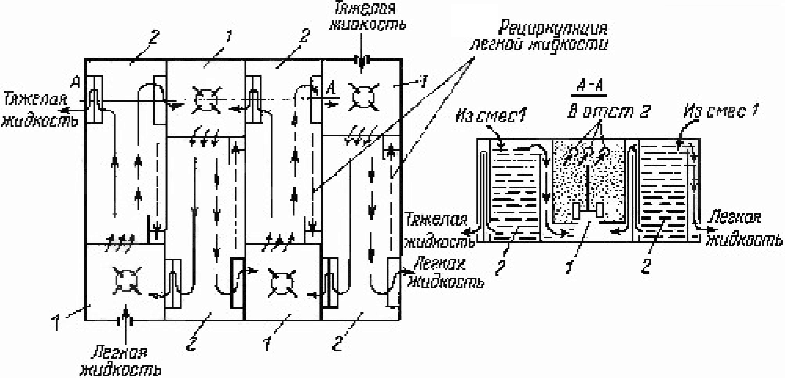
1 - смеситель; 2 - отстойник
экстрактора
В смесительно-отстойных экстракторах достигается интенсивное взаимодействие между фазами, причем эффективность каждой ступени может приближаться к одной теоретической ступени разделения. Эти аппараты хорошо приспособлены для обработки жидкостей при значительно отличающихся объемных расходах фаз, например, при соотношениях расходов 10:1 и более. Для уменьшения объемного соотношения фаз иногда используют частичную рециркуляцию фазы с меньшим объемным расходом из отстойника в смеситель каждой ступени, как показано пунктиром (рис. 2.17).
Важным достоинством смесителей-отстойников является возможность их эффективного применения для процессов экстракции, требующих большого числа ступеней. Смесительно-отстойные экстракторы занимают большую площадь, чем колонные аппараты, но зато требуют меньшей высоты производственного помещения (при горизонтальном расположении ступеней).
Недостатком смесителей-отстойников многих конструкций является медленное отставание в них жидкостей, что нежелательно при обработке дорогостоящих, взрывоопасных или легковоспламеняющихся веществ. Кроме того, наличие мешалок с приводом в каждой ступени усложняет конструкцию аппарата и приводит к повышению капитальных затрат и эксплуатационных расходов.
Центробежные экстракторы
Использование центробежных сил является эффективным средством улучшения не только смешения, но и разделения фаз при экстракции [72].
Принцип работы центробежного экстрактора: жидкости поступают под напором с противоположных концов в каналы быстро вращающегося вала 1, на котором закреплен ротор (барабан) 2. Плотность соединения труб для подвода жидкостей и вращающегося вала достигается с помощью сальников у торцов вала. Внутри ротора по всей его ширине размещена спиральная перегородка 3 из перфорированной ленты. В каналах между ее витками противотоком друг к другу движутся легкая и тяжелая фазы. При этом тяжелая фаза движется от оси к периферии ротора, а легкая фаза - от его периферии по направлению к оси.
Обе фазы перемешиваются, проходя сквозь отверстия спиралей, и разделяются в каналах под действием центробежных сил. Таким образом, смешение и сепарирование жидкостей протекают одновременно и многократно повторяются. Легкая фаза отводится у наружной поверхности ротора, а тяжелая - вблизи его оси. Обе фазы удаляются через раздельные отводные каналы вала, как показано на рис. 2.19.
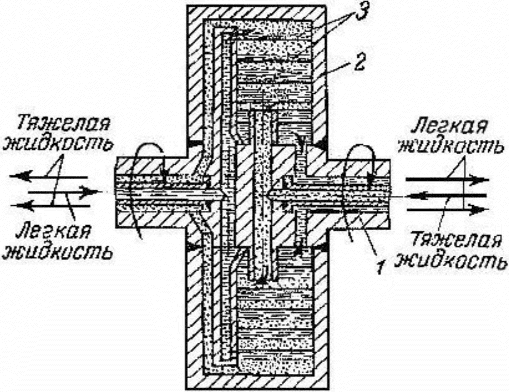
1 - вал; 2 - ротор (барабан); 3 - спиральные перегородки
из металлической перфорированной ленты
Центробежные экстракторы обладают существенными достоинствами. Эти аппараты весьма компактны и сочетают значительную производительность с высокой интенсивностью массопередачи. В них можно эффективно обрабатывать жидкости с небольшой разностью плотностей. Вместе с тем центробежные экстракторы отличаются малой удерживающей способностью и коротким временем пребывания жидкостей в аппарате. Эта особенность центробежных экстракторов обусловливает их успешное применение для экстракции легко разлагающихся веществ, например, антибиотиков (пенициллина и др.), чувствительных не только к нагреванию, но и к продолжительному пребыванию в растворе при нормальной температуре. Вместе с тем эти аппараты не пригодны для экстракции, сопровождаемой химической реакцией, когда требуется длительное время контакта фаз.
Производительность центробежных экстракторов определяется шириной ротора, а число получаемых теоретических ступеней - его диаметром. В промышленных центробежных экстракторах число оборотов ротора колеблется ориентировочно в пределах 1200 - 5000 мин-1, что ограничивает размеры ротора (барабана), диаметр которого не превышает 1,2 - 1,5 м.
В центробежных экстракторах основной выигрыш дает интенсификация разделения водной и органической фаз в поле действия центробежных сил [78 - 80].
Ступенчатые экстракторы состоят из отдельных ступеней, каждая из которых имеет зоны смешения и разделения. В зоне смешения осуществляются диспергирование и интенсивное перемешивание фаз, при этом происходит массопередача извлекаемого компонента из одной фазы в другую до концентрации, близкой к равновесной, после чего эмульсия поступает в зону разделения той же ступени. Таким образом, в каждой ступени обе фазы движутся прямотоком. После разделения жидкости, не контактируя между собой, поступают в зону смешения соседних ступеней так, что в целом по каскаду фазы движутся противотоком.
Одноступенчатые центробежные экстракторы имеют ряд преимуществ перед многоступенчатыми:
- легко компонуются установки с любым числом ступеней, ввод и вывод растворов могут проводиться в любую ступень и из любой ступени установки;
- легко осуществляется управление установкой с любым числом ступеней, достаточно просто определяется неисправная ступень;
- в каждой ступени может устанавливаться требуемое положение поверхности раздела фаз, что особенно важно, когда соотношение плотностей фаз меняется от ступени к ступени;
- при остановках каскада из одноступенчатых центробежных экстракторов растворы остаются в ступенях, фронт концентраций по каскаду не нарушается и последующий пуск с выходом на стационарный режим происходит очень быстро;
- конструкция проще конструкции многоступенчатого экстрактора и, что особенно важно, проще демонтаж, ремонт и замена неисправной ступени;
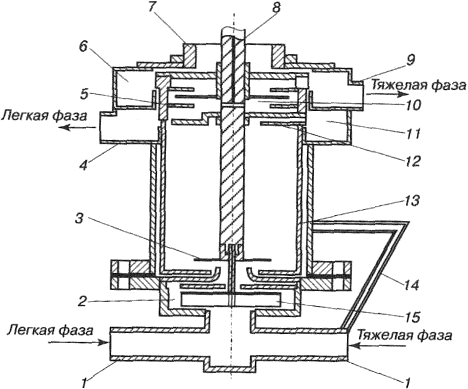
1 - патрубки ввода жидкостей; 2 - смесительная камера;
3 - отбойный диск; 4, 9 - патрубки вывода разделительных
фаз; 5 - переливной порог тяжелой фазы; 6 - сборник тяжелой
фазы; 7 - опора двигателя; 8 - канал подачи воздуха
для регулирования положения поверхности раздела фаз;
10 - гидрозатвор тяжелой фазы; 11 - сборник легкой фазы;
12 - переливной порог легкой фазы; 13 - ротор-сепаратор;
14 - аварийный перелив; 15 - турбинная мешалка
Рисунок 2.20 - Схема одноступенчатого центробежного
экстрактора SRL
Одноступенчатые центробежные экстракторы объединяются в противоточный каскад, на рис. 2.21 изображен многоступенчатый центробежный экстракционный аппарат ЭЦ 125-71, созданный по этому принципу.
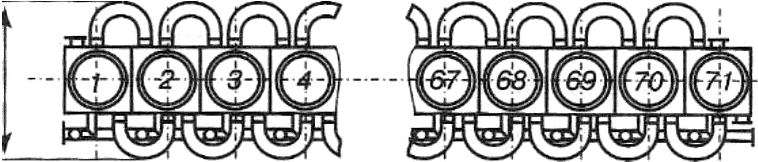
аппарат ЭЦ 125-71
2.20.12 Промышленные технологии разделения РЗЭ
Экстракционное разделение РЗЭ было реализовано в СССР при переработке: 1) лопаритового концентрата РЗЭ, получаемого на СМЗ (рис. 2.22); 2) концентрата, полученного из руд месторождения Меловое, Казахстан, п-ов Мангышлак (рис. 2.23) и иттросинхизитового концентрата руд Актюзского месторождения на Киргизском химико-металлургическом комбинате (КХМК) (п. Орловка, Киргизия). [74, 75].
В технологии разделения группового редкоземельного концентрата, выделенного из лопарита, реализованной на АО "ИРТЫШСКИЙ ХИМИКО-МЕТАЛЛУРГИЧЕСКИЙ ЗАВОД", Казахстан, на первой стадии из хлоридных растворов выделялся концентрат среднетяжелой группы с использованием экстрагента Д2ЭГФК (разделение по линии Sm/Nd), полученный концентрат легкой группы РЗМ конвертировался в нитраты, из него выделялся церий электрохимическим окислением на платиновом аноде с последующим выделением церия экстракцией на 100% ТБФ и получением оксида церия марки 99,998. Из рафината экстракции последовательным разделением по линиям La/Ce, Ce/Pr и Nd/Pr выделяли чистый оксид лантана, оксиды дидима и неодима экстракцией на 100% ТБФ. Из концентрата среднетяжелой группы выделяли европий восстановлением его порошком цинка, самарий, гадолиний и иттрий-экстракцией с использованием смеси Д2ЭГФК и ТБФ.
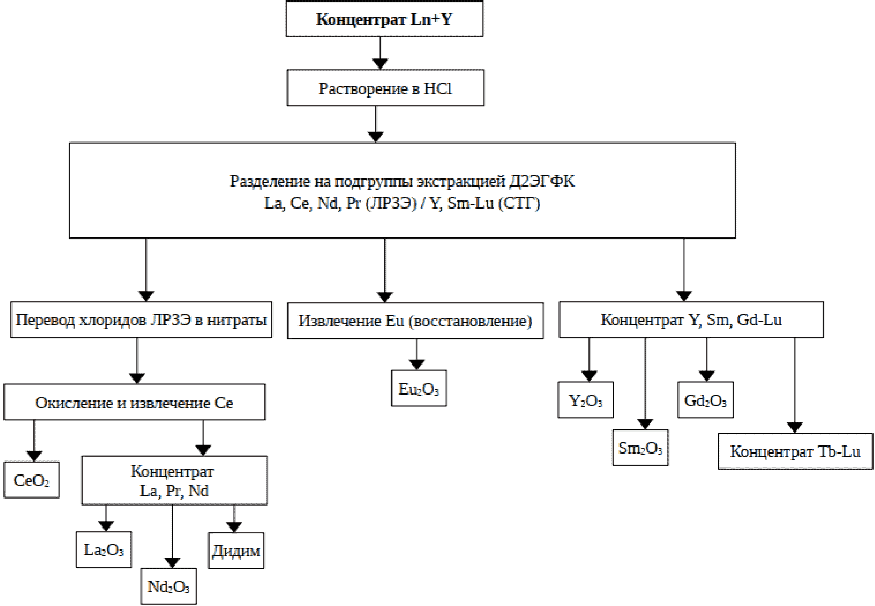
с получением индивидуальных РЗО
Производство по разделению группового концентрата РЗЭ месторождения Меловое было реализовано на двух заводах: разделение по линии Sm/Nd с получением концентрата легкой группы РЗЭ (церий-лантан-неодим-празеодим) проводилось на химико-металлургическом заводе ПО "ПХЗ" (г. Днепродзержинск, Украина), концентрат среднетяжелой группы (СТГ) перерабатывался на Московском заводе "Полиметалл" с получением высокочистых соединений самария, европия, гадолиния, иттрия, тербия, диспрозия. и концентратов тяжелой группы. Принципиальная схема разделения РЗЭ из концентрата Меловое представлена на Рисунке 2.23.
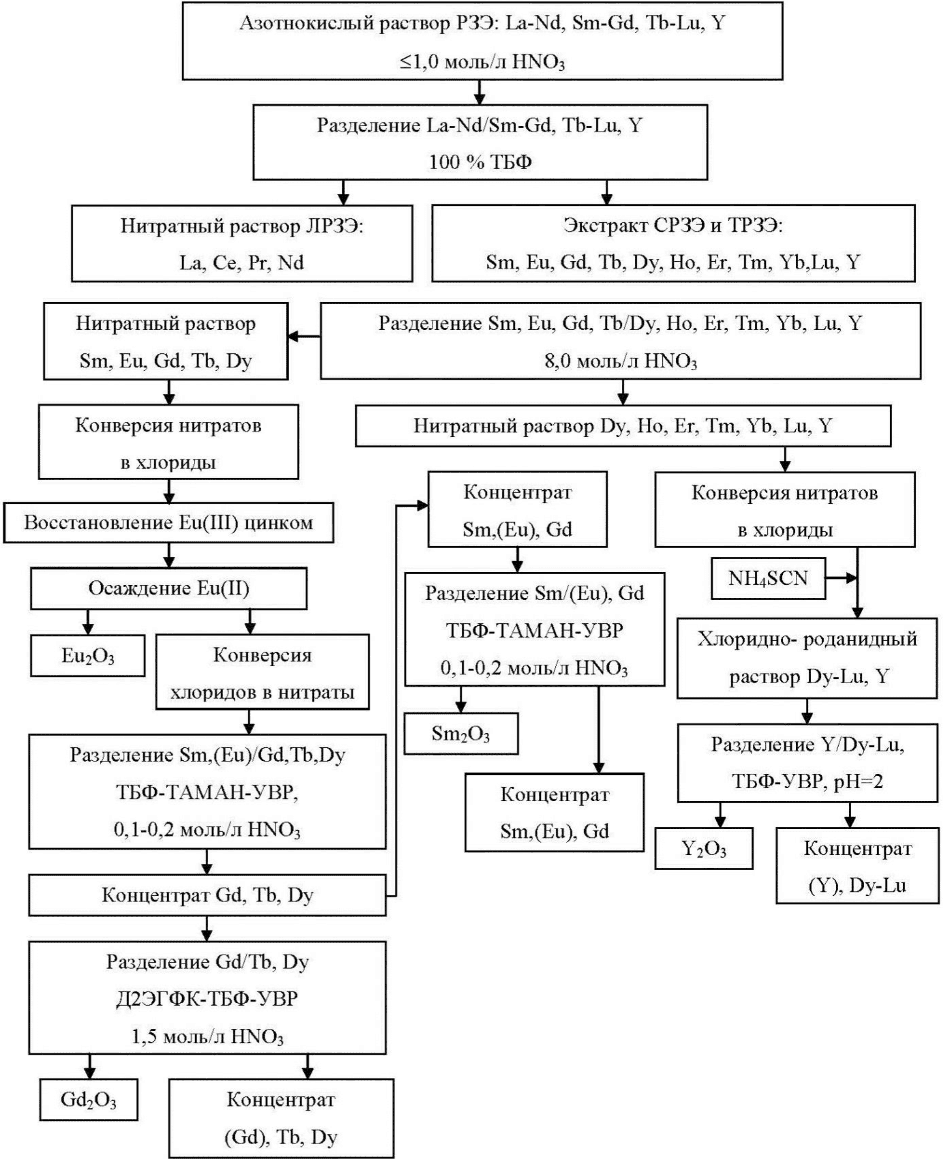
месторождения Меловое
Технология разделения подразумевала отделение легкой группы с помощью 100% ТБФ из нитратных сред при концентрации HNO3 < 1М по линии Sm/Nd и разделение по линии Dy/Tb при C(HNO3) = 8М. Легкую группу РЗЭ отделяли на 100% ТБФ в Днепродзержинске, ее направляли для производства катализаторов, а реэкстракт, содержащий СТГ отправляли на московском заводе Полиметалл. Дальнейшая переработка включала его упаривание с корректировкой состава раствора и разделение на концентрат средней и тяжелой группы (линия Dy/Tb) в системе Ln(NO3)3 - 100% ТБФ.
Реэкстракт каскада Dy/Tb переводили в хлориды, добавляли роданистую кислоту, отделяли Y с помощью 100% ТБФ, а затем разделяли концентрат, содержащий Tb - Lu по линии Tm/Er. Дальнейшее разделение реэкстракта проводили с использованием хроматографии, разделение рафината экстракции позволяло получить Dy (> 99.9%) и Er (< 99%).
Рафинат экстракции подвергался упариванию и отгонке азотной кислоты, затем денитрации, растворению в соляной кислоте и восстановлению основной массы европия порошком металлического цинка с переводом его в сульфат. Маточный раствор, содержащий остатки европия и остальные РЗЭ средней группы, переводили обратно в нитраты и вели разделение с помощью синергетной смеси ТАМАН - ТБФ по линии Eu/Gd. Реэкстракт каскада Eu/Gd повторно очищали и получали самарий марок СмО-Е (99.997%) и СмО-Ж (99.989%). Рафинат экстракции каскада Eu/Gd, содержащий Gd, Tb и Dy, разделяли с помощью Д2ЭГФК - ТБФ и получали гадолиний марок ГдО-5 (99.9%) и ГдО-6 (99.5%) и Tb (< 99.9%). Дальнейшая очистка отделенного европия позволяла получить продукт марки ЕвО-Ж (99.998%) [74, 75].
В технологии использовались дорогостоящие операции упаривания, за счет нескольких операций конверсии из нитратов в хлориды и наоборот был большой перерасход кислот и объем возвращаемых в процесс некондиционных растворов, а также образовывалось множество разноплановых отходов.
Улучшенная технология, предложенная ВНИИХТ, включала использование трех видов экстрагентов: ТБФ, ИДДФК и Versatic. В первую очередь из реэкстракта каскада Sm/Nd с помощью ТБФ отделяли Y по линии Y/Er. Из реэкстракта каскада Y/Er с помощью Versatic отделяли Y и получали концентрат тяжелых РЗЭ. Рафинат экстракции каскада Y/Er с помощью ИДДФК разделяли по линии Tb/Gd. Дальнейшее разделение рафината экстракции Tb/Gd с помощью ИДДФК и последующая очистка от Nd с помощью ТБФ позволяли получить Sm, с помощью смеси ТАМАН - ТБФ получали Eu и Gd. Разделение реэкстракта Tb/Gd с использованием исключительно ИДДФК по нескольким линиям позволяло получить Tb, Dy и Er [76].
По существовавшей на КХМК технологии редкоземельный концентрат смешивали с кальцинированной содой, шихту спекали при температуре 700 - 800 °C, спек измельчали до -0,1 мм, отмывали от водорастворимых солей, выщелачивали азотной кислотой и непосредственно из пульпы экстрагировали РЗЭ 100% ТБФ. После реэкстракции РЗЭ очищали от примесей железа, циркония, тория и других элементов гидролитическим методом, а затем экстракцией в системах с карбоновыми кислотами и ТБФ. Главным недостатком этой технологии являлись высокие потери РЗЭ (до 12%) и ТБФ (до 0,7 кг/кг РЗЭ) с отвальной рафинатной пульпой. Кроме того, значительную сложность представляла собой утилизация промстоков из-за наличия в ней ТБФ.
На первом иттриевом каскаде с применением высаливателя - нитрата алюминия - производилась деление по линии Nd/Sm. Реэкстракт первого иттриевого каскада упаривался и использовался как исходный раствор второго иттриевого каскада. Рафинат второго каскада содержал в основном Y (70 - 80%) и Er+Lu (20 - 30%). Он упаривался и служил исходным раствором 3-го иттриевого каскада. Реэкстракт после упаривания поступал на 4-й иттриевый каскад с целью доизвлечения иттрия и получения концентрата средних РЗЭ (Sm-Ho). Исходный раствор для 3-го каскада представлял собой смесь нитратов Y и Er+Lu с содержанием средних РЗЭ менее 2x10-3% каждого, Nd - менее 1x10-3%. Содержание иттрия в исходном растворе - 70 - 80%.
Принцип работы 3-го иттриевого каскада был основан на том, что реэкстракт, содержащий иттрий и смесь эрбий-лютеций подвергали орошению раствором аммонийной соли этилентриаминтетрауксусной кислоты (ЭДТК).
Принцип работы 4-го иттриевого каскада основывался на худшей экстракционной способности иттрия, в результате чего нитрат иттрия концентрировался в водной фазе, а средние РЗЭ (Sm-Ho) - в органической. Концентрат средних РЗЭ перерабатывался ионообменным способом на ионите КУ-28 с целью получения индивидуальных оксидов. Рафинат 4-го каскада после упаривания подмешивали к исходному раствору 2-го иттриевого каскада. Упаренный рафинат первого иттриевого каскада, содержащий нитраты лантана, церия, неодима и празеодима использовался как исходный раствор первого неодимового каскада. В системе 100% ТБФ-РЗЭ-HNO3 коэффициент разделения 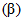 пары Nd/Pr не превышает 1,4, что не позволяет эффективно провести основную операцию первого неодимового каскада - из суммы легких РЗЭ выделить чистый неодим, поэтому для эффективного выделения неодима в экстракционную смесь введен высаливатель - нитрат алюминия, что повышает
пары Nd/Pr не превышает 1,4, что не позволяет эффективно провести основную операцию первого неодимового каскада - из суммы легких РЗЭ выделить чистый неодим, поэтому для эффективного выделения неодима в экстракционную смесь введен высаливатель - нитрат алюминия, что повышает 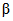 до 1,6. Окончательная очистка неодима производилась на 3-х каскадах, лантана - на двух. Реэкстракт первого лантанового каскада посылали на электрохимическое окисление церия, который окисляли на платиновом аноде с последующим выделением чистого церия на 100% ТБФ [75].
до 1,6. Окончательная очистка неодима производилась на 3-х каскадах, лантана - на двух. Реэкстракт первого лантанового каскада посылали на электрохимическое окисление церия, который окисляли на платиновом аноде с последующим выделением чистого церия на 100% ТБФ [75].
Технологии разделения РЗЭ, выделенного из бастнезита, монацита после очистки от радиоактивных примесей (дезактивации) и ионо-абсорбционных руд в Китае основана на экстракционной технологии из хлоридных сред с использованием экстрагента Р-507 (Моно-2-этилгексиловый эфир 2-этилгексил-фосфоновой кислоты - (М2ЭГ(2ЭГ)ФК), выделение иттрия проводится на первой стадии разделения нафтеновой кислотой, если групповой концентрат обогащен иттрием (Y >= 60%), или на последней стадии - если иттрия в концентрате мало [59]. Схемы 1 - 6 разделения приведены на рисунках 2.24 - 2.29.
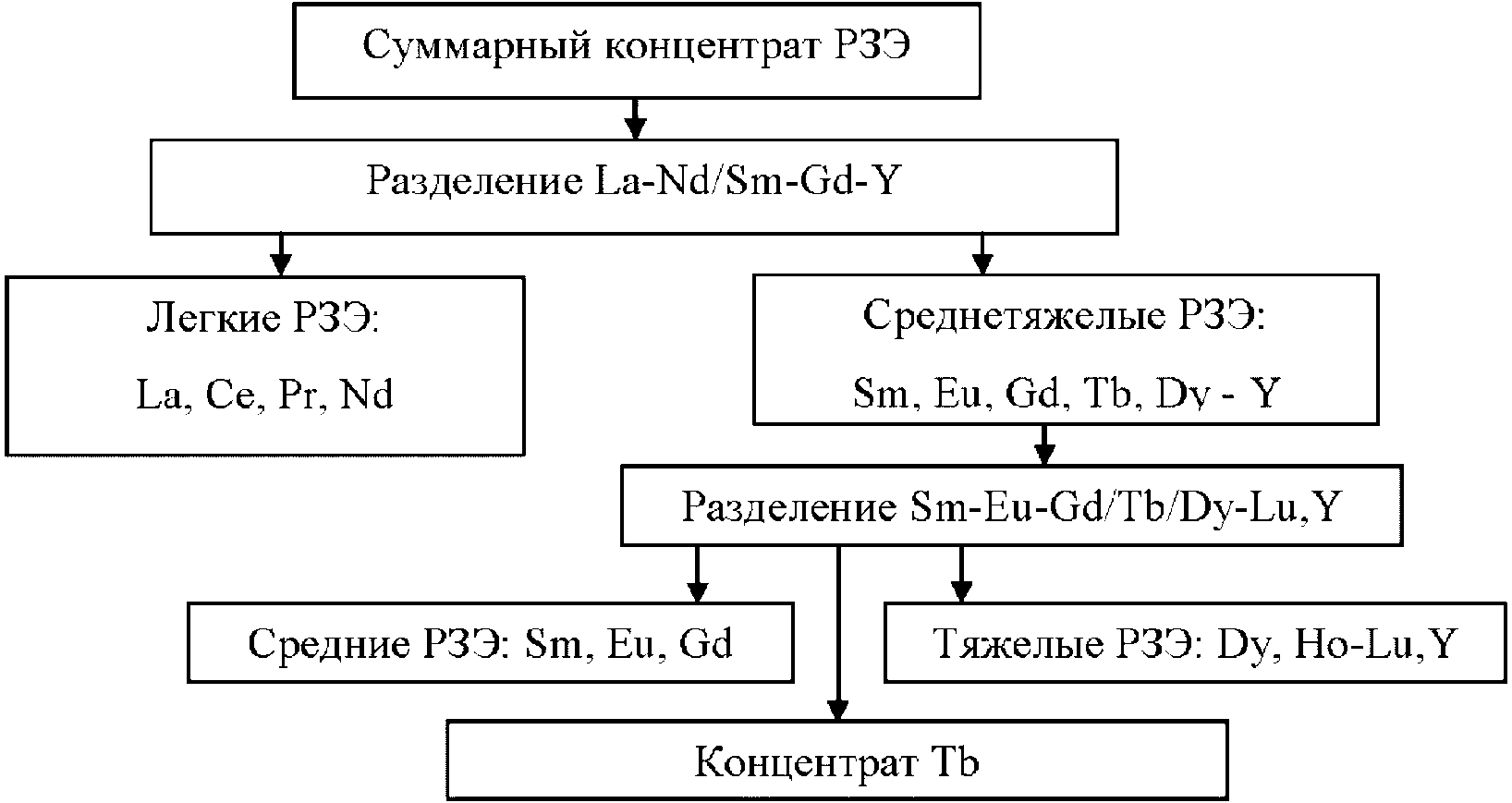
концентрата РЗЭ, реализованная на предприятиях в Китае
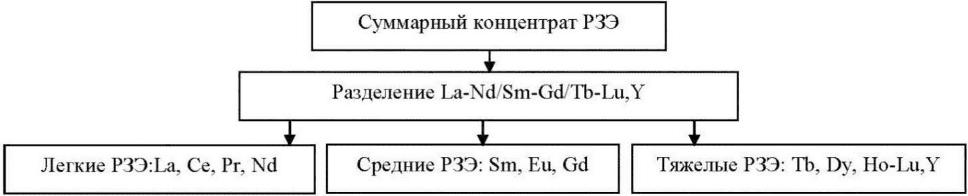
Рисунок 2.25 - Схема 2 разделения группового бастнезитового
концентрата РЗЭ, реализованная на предприятиях в Китае
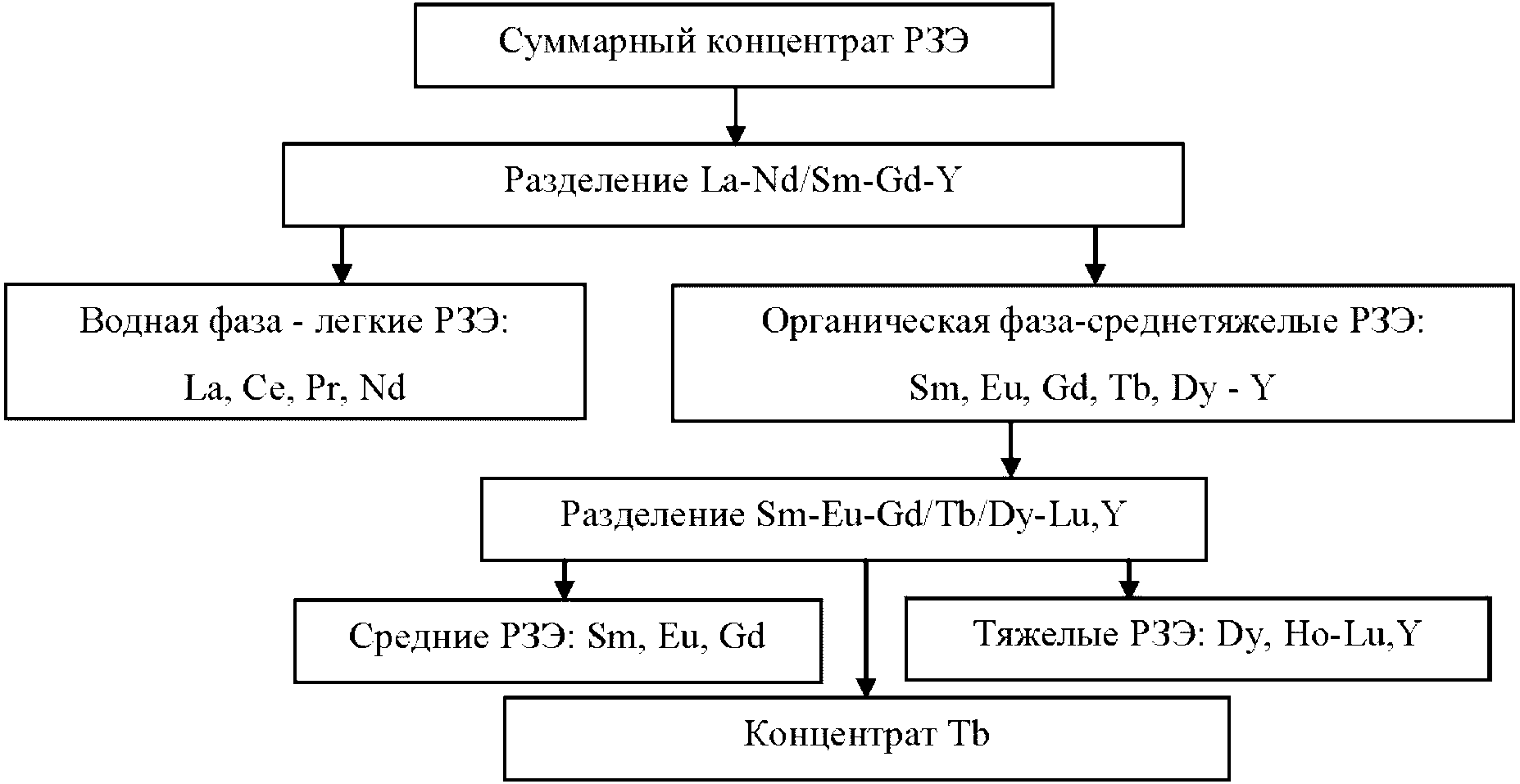
из ионных руд, реализованная на предприятиях в Китае
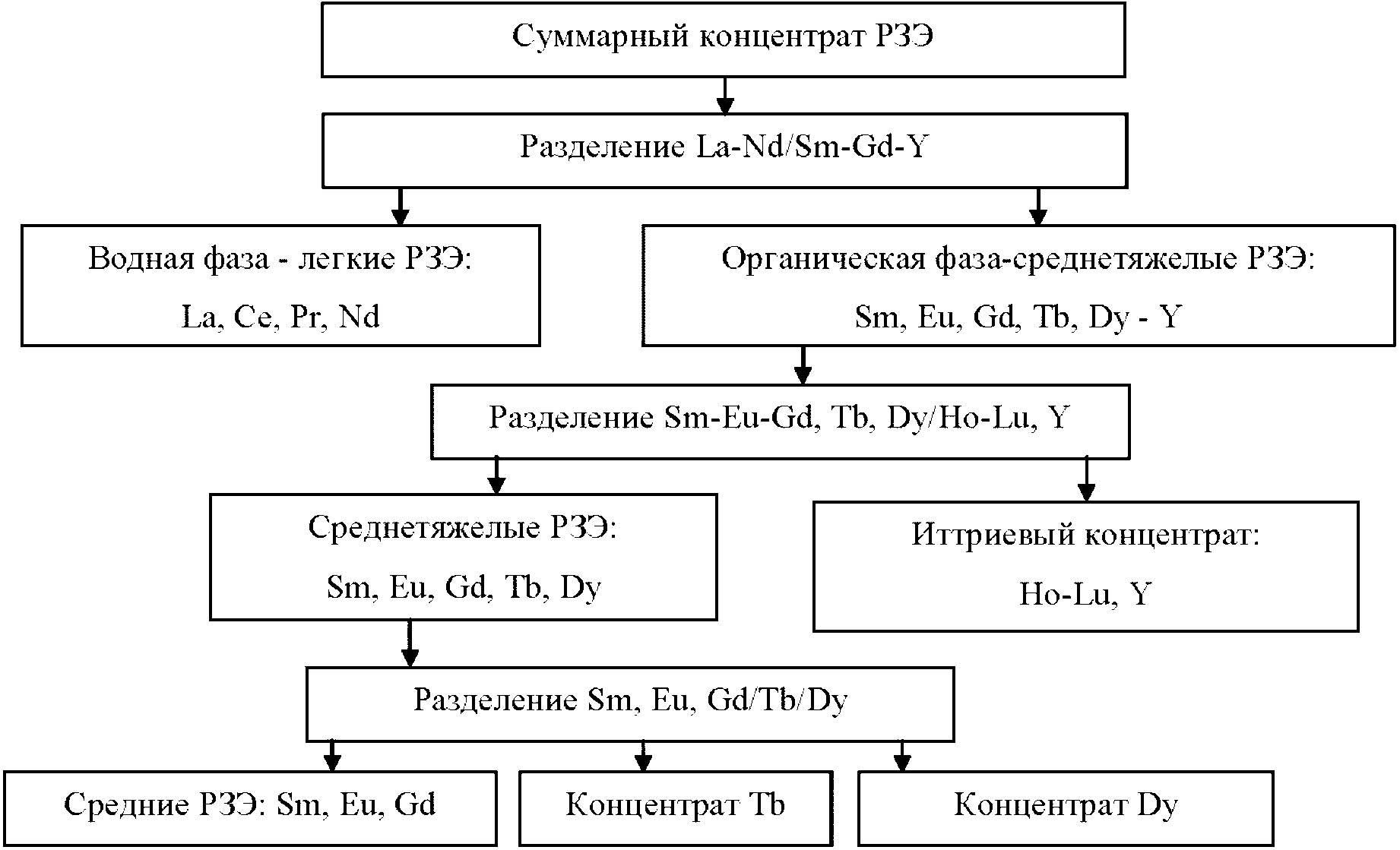
из ионных руд, реализованная на предприятиях в Китае
В процессе разделения, представленном на схеме 4, после отделения среднетяжелой группы из нее сначала выделяют иттриевый концентрат по линии Dy/Ho, а затем разделяют на три концентрата: средних РЗЭ (Sm, Eu, Gd), тербия и диспрозия. Из иттриевого концентрата затем выделяют чистый оксид Y2O3.
При групповом разделении концентрата, полученного из ионных руд с низким содержанием иттрия, используют схему 3, в соответствии с которой выделяемый из среднетяжелой группы концентрат тяжелых РЗЭ содержит более 70% иттрия. Дальнейшую очистку иттрия от примесей тяжелых РЗЭ проводят с использованием экстракционной системы с нафтеновой кислотой из солянокислых растворов.
Система нафтеновая кислота - водные растворы РЗЭ в HCl может быть использована и для группового разделения концентратов ионных руд со средним содержанием иттрия. Особенностью таких концентратов является практически одинаковое содержание в них La и Y. Это обуславливает коэффициент разделения La/Y близкий к 1, поэтому иттрий при разделении концентрируется с элементами легкой группы. Для эффективного отделения иттрия из таких концентратов предложена схема 5 разделения РЗЭ, представленная на рисунке 2.28.
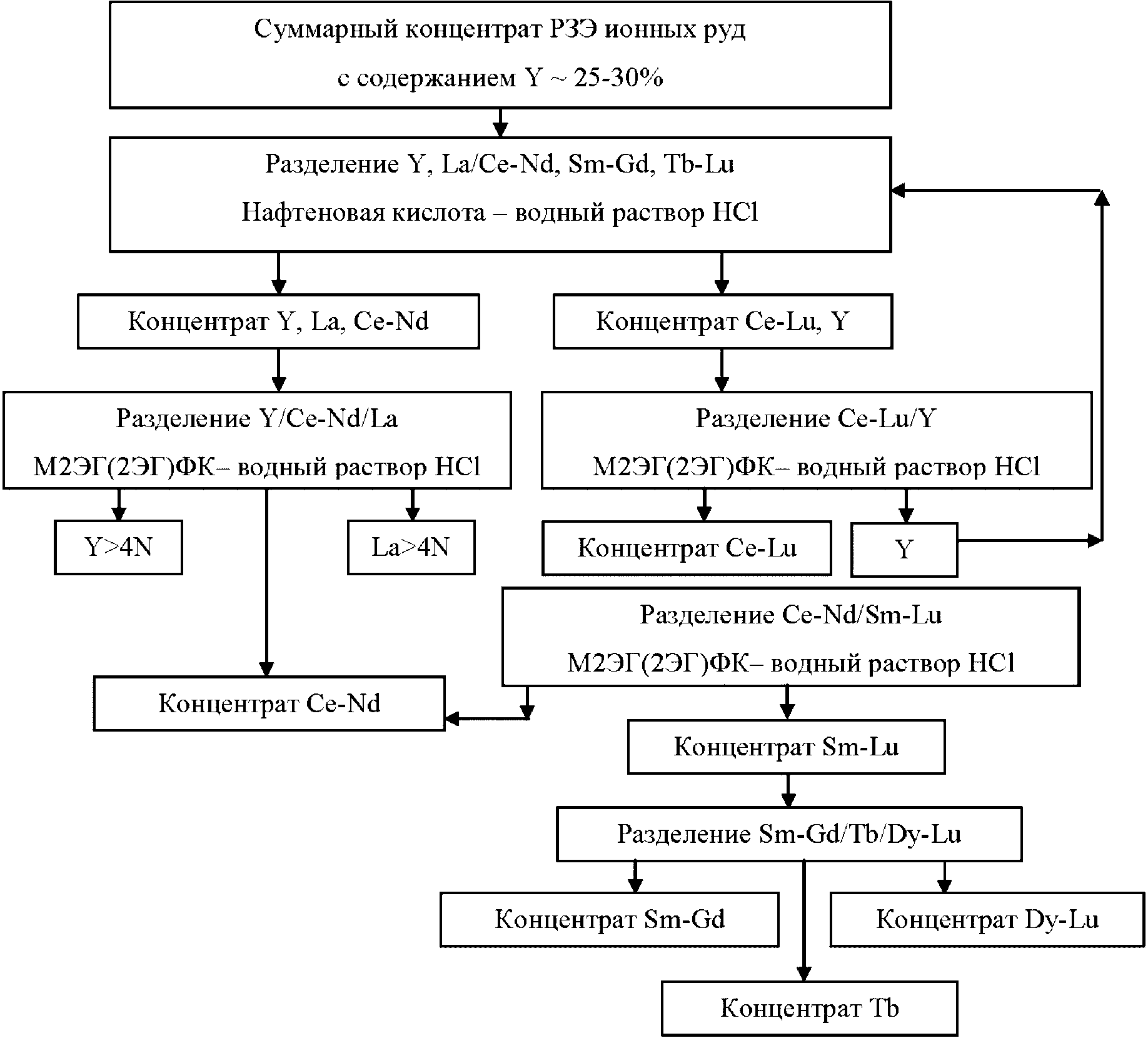
из ионных руд, реализованная на предприятиях в Китае
Для разделения концентрата РЗЭ, полученного из ионных руд с высоким содержанием иттрия, более 60%, в Китае используют схему 6, представленную на рисунке 2.29. Эта схема также использует два экстрагента для групповых разделений: на первом этапе нафтеновую кислоту, а на втором этапе М2ЭГ(2ЭГ)ФК. Разделение проводят в солянокислых средах с различной концентрацией HCl. Изменение состава исходного концентрата РЗЭ в пользу высокого содержания в нем иттрия позволяет уже на втором разделительном каскаде получать иттрий, чистотой более 99,99%.
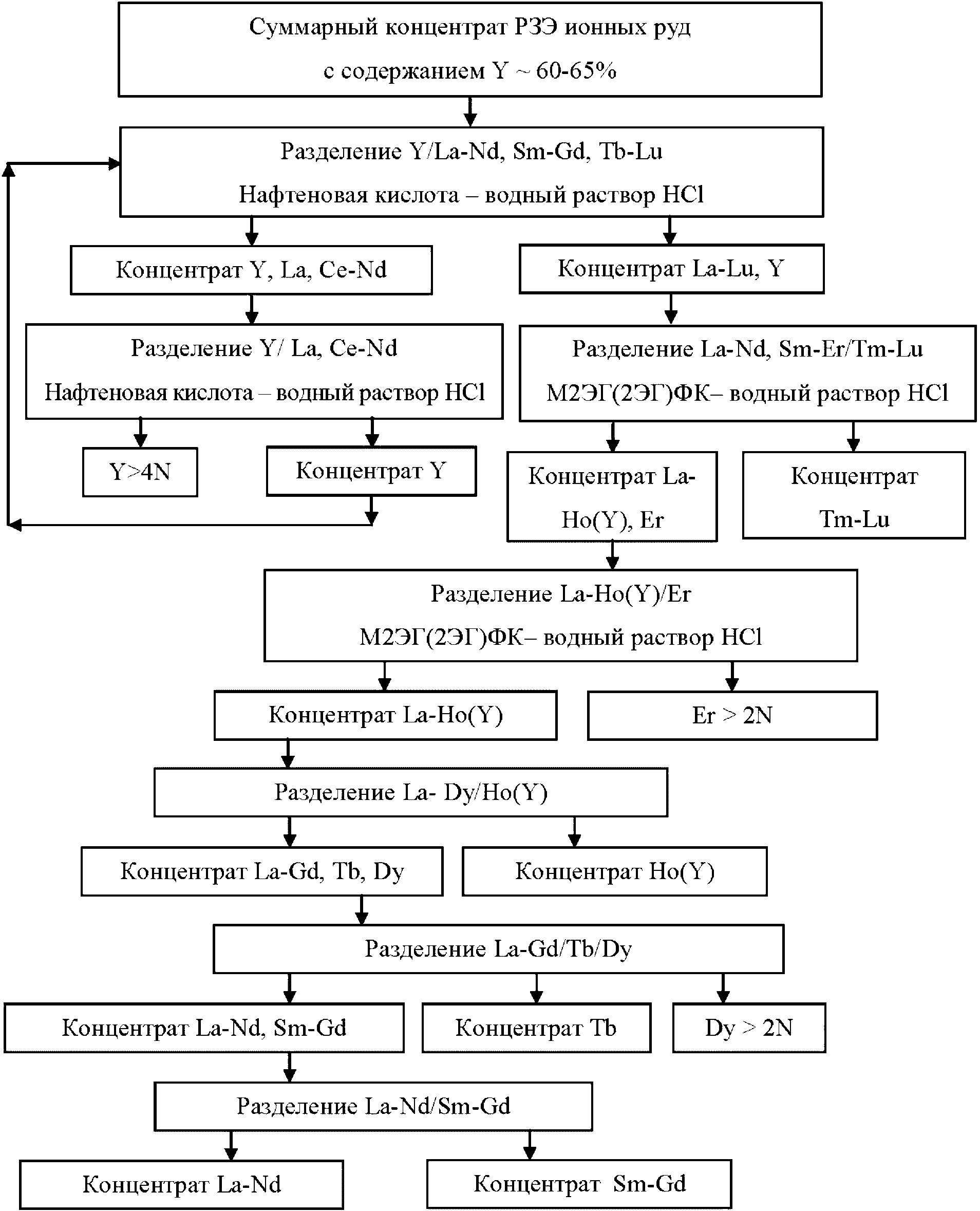
из ионных руд, реализованная на предприятиях в Китае
Рассмотренные выше схемы разделения исходных концентратов РЗЭ, полученных из минерального сырья, построены по одной общей схеме, позволяющей предварительно разделить все РЗЭ и иттрий на три большие группы: легких, средних и тяжелых РЗЭ. Иттрий, как правило, попадает при разделении в группу тяжелых РЗЭ (поэтому ее называют иттриевой группой).
Необходимо отметить, что разделительные процессы в Китае проводят преимущественно из хлоридных сред, в то время как групповое разделение в отечественных схемах проводят в нитратных средах. Исключение составляет переход от нитратных сред к хлоридным на стадии осадительного выделения Eu. В настоящее время выделение европия при разделении средней группы РЗЭ предложено проводить экстракционным методом без изменения его валентного состояния, например, с использованием той же синергетной смеси ТАМАН+ТБФ в УВР. Однако это потребует увеличения числа разделительных ступеней при проведении процесса в противоточных каскадах с получением только двух продуктов. При переходе к так называемым трехпродуктовым каскадам разделение сразу трех компонентов Sm, Eu и Gd позволит избежать наращивания числа ступеней разделительного каскада, но может сказаться на производительности.
В соответствии с общей схемой разделения исходных концентратов РЗЭ (рис. 2.4) дальнейшее выделение индивидуальных элементов проводят исходя из состава каждой группы, на которые был разделен первоначальный концентрат. Поэтому ниже рассмотрены схемы разделения РЗЭ легкой, средней и тяжелой групп, которые также могут быть проведены различными методами.
2.20.13 Разделение РЗЭ легкой группы: La, Ce, Pr, Nd
Для разделения РЗЭ легкой группы на индивидуальные элементы используют различные экстракционные системы, среди которых необходимо выделить растворы ТБФ в разбавителе, например, УВР, для азотнокислых сред и органические кислоты - карбоновые и фосфорсодержащие - для хлоридных растворов.
В Китае для разделения La, Ce, Pr, Nd в солянокислых средах используют экстракционные системы с органическими кислотами, в частности, нафтеновую кислоту, Д2ЭГФК и М2ЭГ(2ЭГ)ФК. Церий в некоторых случаях выделяют из смеси легких РЗЭ окислительно-восстановительным методом до экстракционного разделения. Для повышения эффективности работы экстракционного каскада разделение проводят по двум линиям с получением трех продуктов в одном процессе.
При разделении концентрата легких РЗЭ, полученного при переработке бастнезита и монацита, с содержанием в нем церия (~ 50%) и лантана (~ 25 - 30%) более 80% используют схемы 1 и 2, представленные на рисунках 2.30 и 2.31.
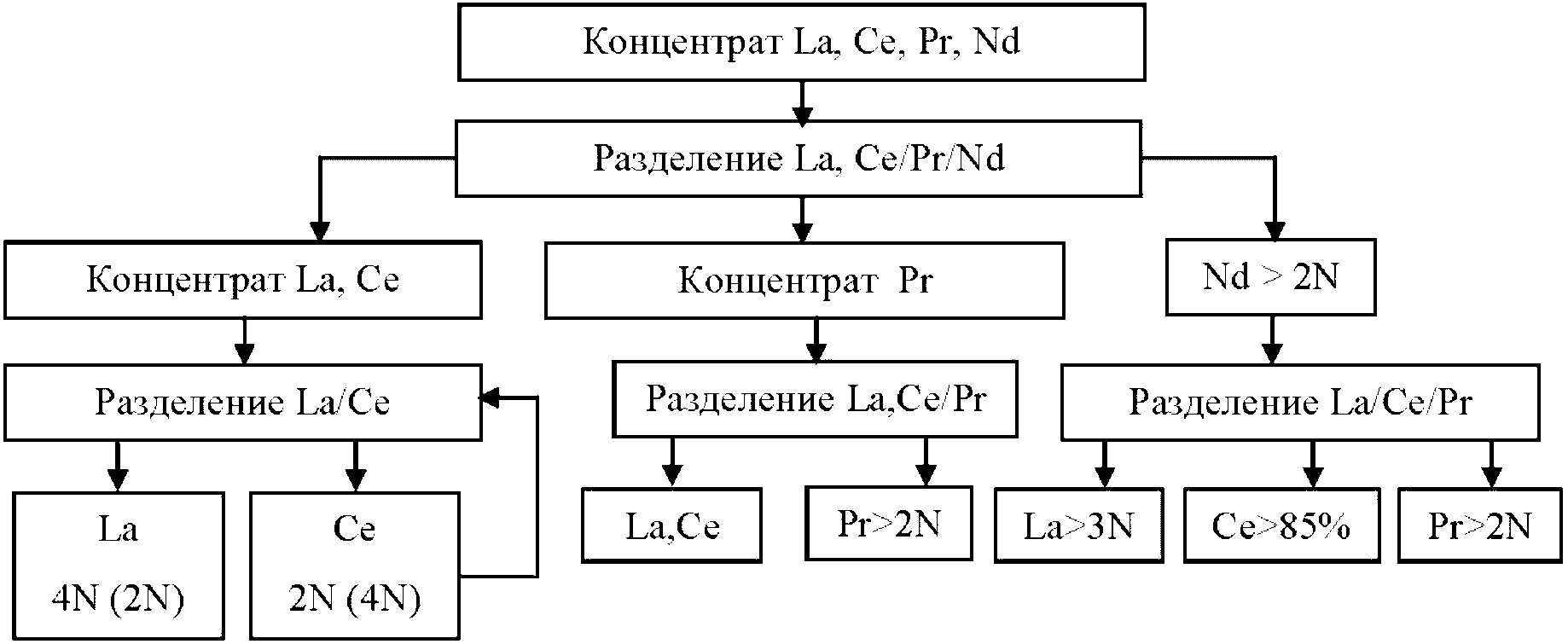
группы, полученного из бастнезита или монацита
Экстракцию проводят в системе М2ЭГ(2ЭГ) ФК в УВР - LnCl3 - HCl - H2O.
Согласно схеме 2, рисунок 2.31, на первом каскаде проводят разделение по линии Pr/Nd с получением чистого неодима и концентрата, содержащего лантан, церий и празеодим. На втором каскаде проводят разделение по двум линиям La/Ce и Ce/Pr с получением трех продуктов: чистых лантана празеодима и цериевого концентрата, содержащего более 85% церия.
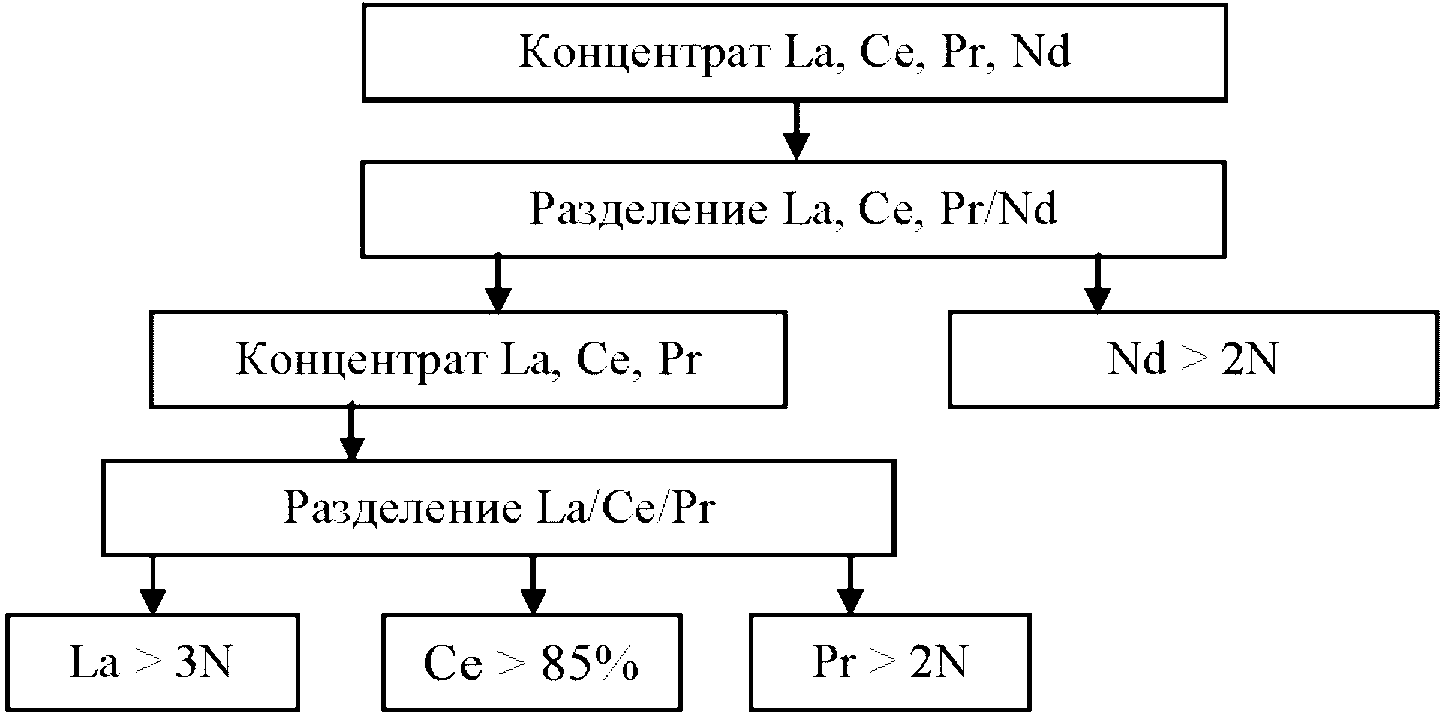
группы, полученного из бастнезита или монацита
Для концентратов легких РЗЭ с низким содержанием церия, например, полученным из ионных руд (Ce ~ 1 - 5%), разделение на индивидуальные элементы проводят по схеме 3, представленной на рисунке 2.32.
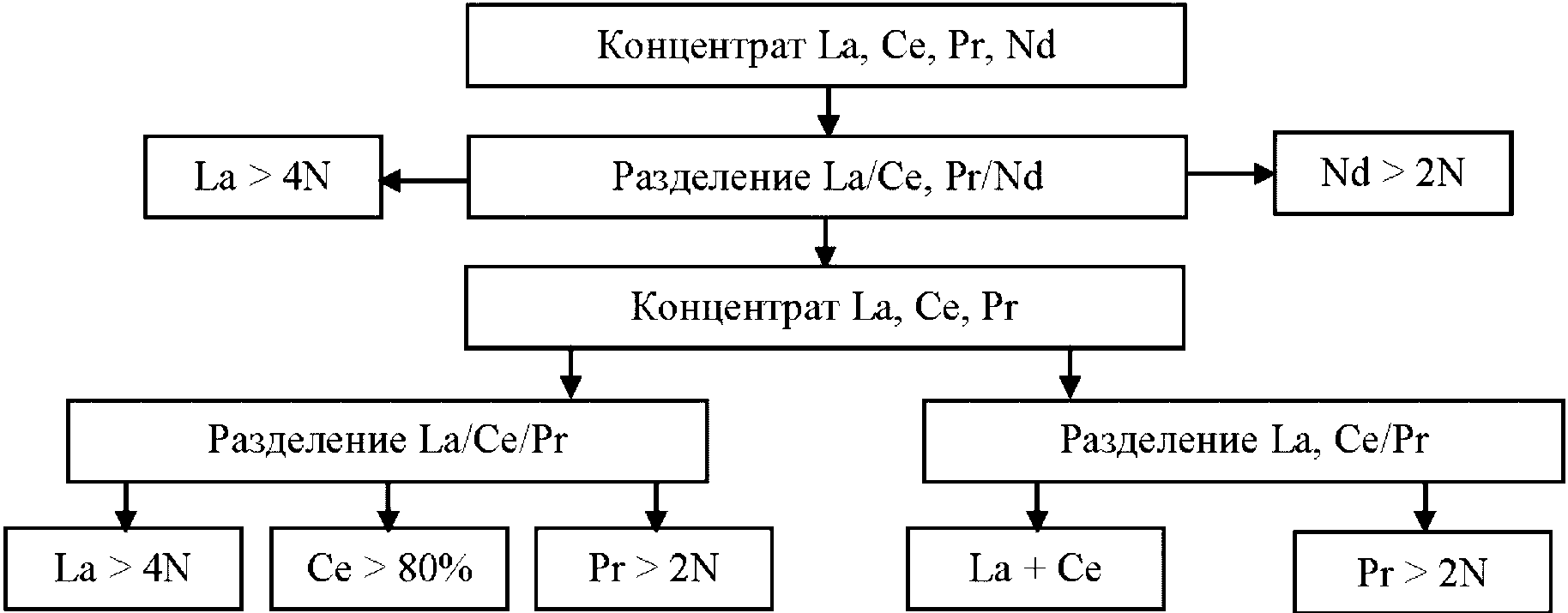
группы, полученного из бастнезита или монацита
Экстракционное разделение концентрата легкой группы РЗЭ с использованием экстракции ТБФ из нитратных растворов применяли при переработке апатитовых концентратов, рисунок 2.33.
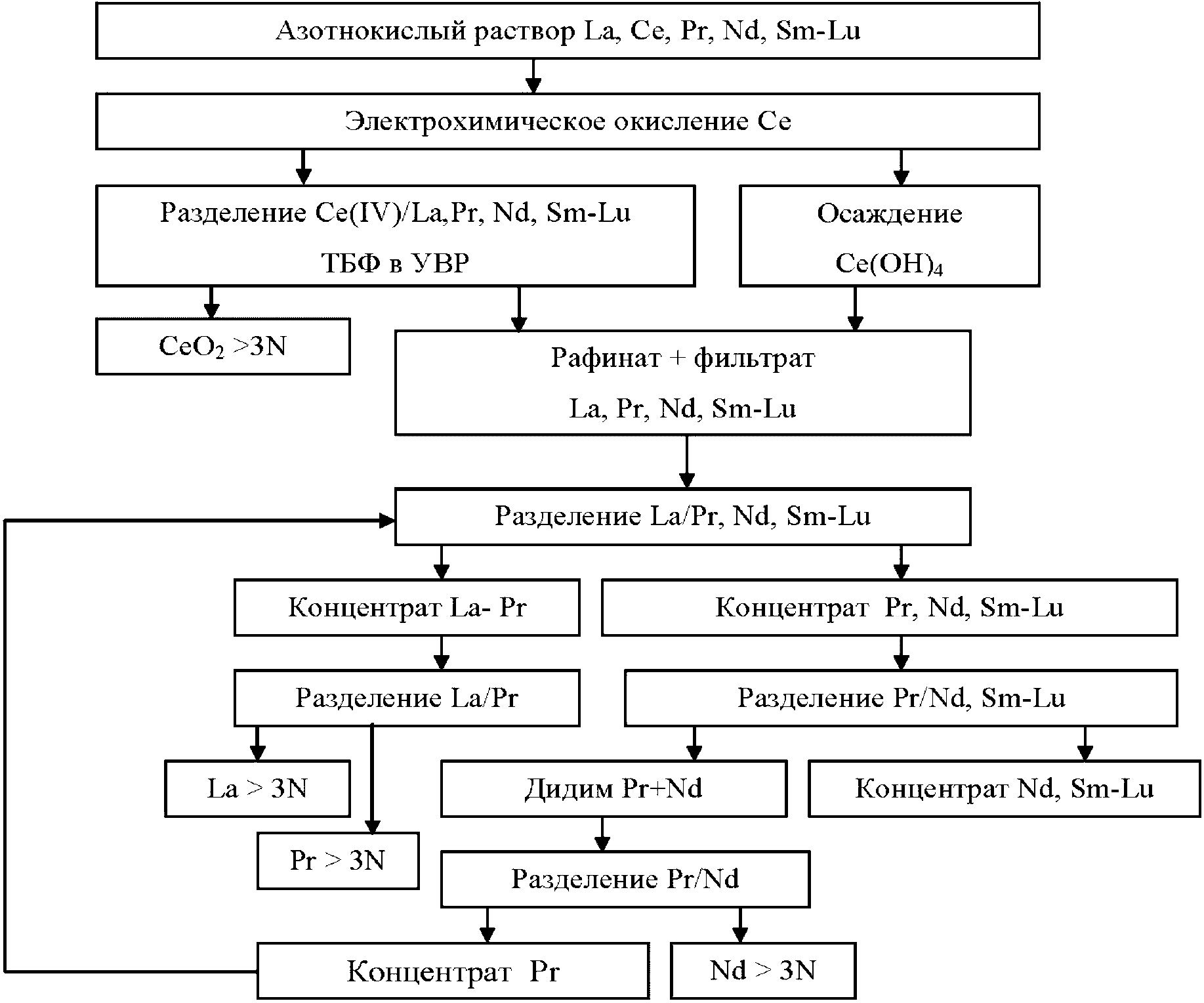
легкой группы, полученного из апатита
После экстракционной очистки от нередкоземельных примесей экстракцией 100%-ным ТБФ из 1,5 - 1,7 моль/л HNO3 и промывки экстракта водным раствором, содержащим 0,75 моль/л NH4NO3, проводят реэкстракцию РЗЭ подкисленной HNO3 водой. Реэкстракт подают на электрохимическое окисление церия, после которого нитратный раствор разделяют на две части. Из одной части осаждают Ce(IV) аммиаком с получением 95%-ного концентрата. Вторую часть направляют на экстракционное выделение Ce(IV) с использованием ТБФ в керосине в качестве экстрагента. Ce(IV) экстрагируют в органическую фазу, в то время как трехвалентные РЗЭ остаются в рафинате экстракции. Из экстракта осаждают гидроксид церия с последующим получением из него CeO2 чистотой 99,9%. Рафинат экстракции объединяют с фильтратом, полученным на стадии выделения цериевого концентрата, и проводят экстракционное разделение на индивидуальные элементы.
2.20.14 Разделение редкоземельных элементов средней группы: Sm, Eu, Gd
Разделение РЗЭ средней и тяжелой групп возможно по линиям Gd/Tb, Tb/Dy и даже Dy/Ho, так что дальнейшее разделение на индивидуальные элементы может включать не только выделение самария, европия и гадолиния, но и тербия, и в некоторых случаях даже диспрозия.
Для разделения РЗЭ средней группы используются нитратные и хлоридные среды, как это уже было показано на примере разделения РЗЭ легкой группы. В качестве экстрагентов используются как индивидуальные экстрагенты, например, фосфорсодержащие кислоты, НФОС, так и смеси экстрагентов, например, ТАМАН-ТБФ, Д2ЭГФК-ТБФ, Cynex-572-ТБФ [36, 59].
Учитывая возможность простого восстановления Eu(III) до Eu(II), во многих разделительных схемах европий из смеси РЗЭ средней группы выделяется восстановительно-осадительным методом (переработка концентрата СТГ месторождения Меловое).
Для проведения экстракционного разделения использовали противоточные каскады с промывкой, содержащие 70 - 80 разделительных ступеней в каждом каскаде. В качестве экстракторов применяли смесители-отстойники ящичного типа. Один из каскадов представлял собой каскад центробежных экстракторов ЭЦ 125. Технологически рафинат или реэкстракт предыдущего каскада являлся исходным раствором для последующего. Для корректировки растворов при переходе от одного каскада к другому осуществляли упаривание до требуемой концентрации РЗЭ. Технические решения по разделению РЗЭ средней группы по описанной выше схеме были защищены авторскими свидетельствами СССР на изобретение.
Развитие описанной технологической схемы разделения средних и некоторых тяжелых РЗЭ заключалось в замене дорогостоящего и энергозатратного процесса межкаскадного упаривания при корректировке рафинатов экстракции или реэкстрактов на осаждение РЗЭ карбонатом натрия с последующим растворением карбонатов РЗЭ до требуемой концентрации в азотной кислоте.
В Китае при переработке концентрата средних РЗЭ, выделенного из монацита или ионных руд, разделение средней группы РЗЭ на индивидуальные элементы в хлоридных растворах проводится согласно схеме рисунка 2.34. Экстракционное разделение Sm, Eu и Gd проводят из солянокислых растворов с использованием в качестве экстрагента растворов Д2ЭГФК в УВР на одном экстракционном каскаде с получением трех продуктов: самария и гадолиния чистотой более 2N, и концентрата Eu с содержанием от 6% до 40% в зависимости от состава исходного сырья. Дальнейшая переработка такого концентрата проводится восстановительно-осадительным методом до получения Eu2O3 флуоресцентного качества [59].
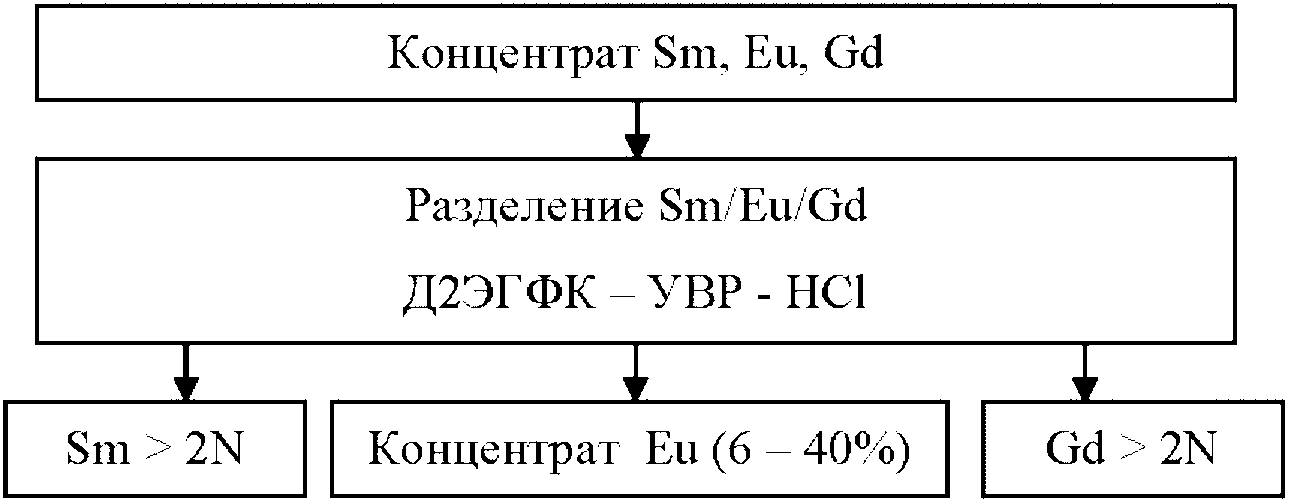
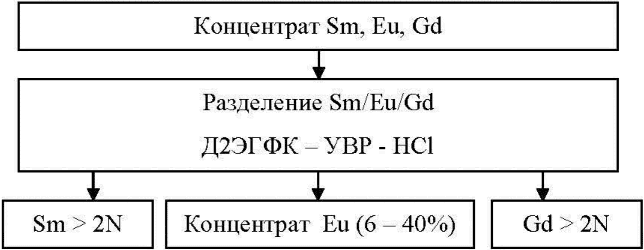
полученных из монацита и ионных руд в Китае
2.20.15 Разделение РЗЭ тяжелой группы: Tb - Lu
Как было описано выше, разделение среднетяжелой группы ведется по линиям Gd/Tb, Tb/Dy или Dy/Ho, поэтому выделение, например, тербия и диспрозия может проводиться при разделении концентратов РЗЭ средней группы. В то же время в тяжелую группу РЗЭ, как правило, попадает иттрий. Выделение иттрия из смесей РЗЭ также можно отнести к процессам разделения РЗЭ тяжелой группы.
Для разделения РЗЭ тяжелой группы в основном используются нитратные и хлоридные среды. Однако при выделении иттрия могут быть использованы роданидные или хлоридно-роданидные растворы с экстракцией на ТБФ.
При переработке концентратов тяжелых РЗЭ из них в первую очередь стараются извлечь в чистом виде Tb, Dy, Er, Y. Поэтому общие схемы разделения включают в основном получение обогащенных концентратов РЗЭ третьей тетрады и иттрия и экстракционное выделение из них требуемых элементов.
На рисунке 2.35 представлена схема экстракционного выделения эрбия и диспрозия из азотнокислых растворов иттрий-эрбиевого концентрата с попутным получением обогащенных концентратов других тяжелых РЗЭ и иттрия, и с использованием 1,2 моль/л растворов ИДДФК в РЭД-3 в качестве экстрагента на всех разделительных каскадах.
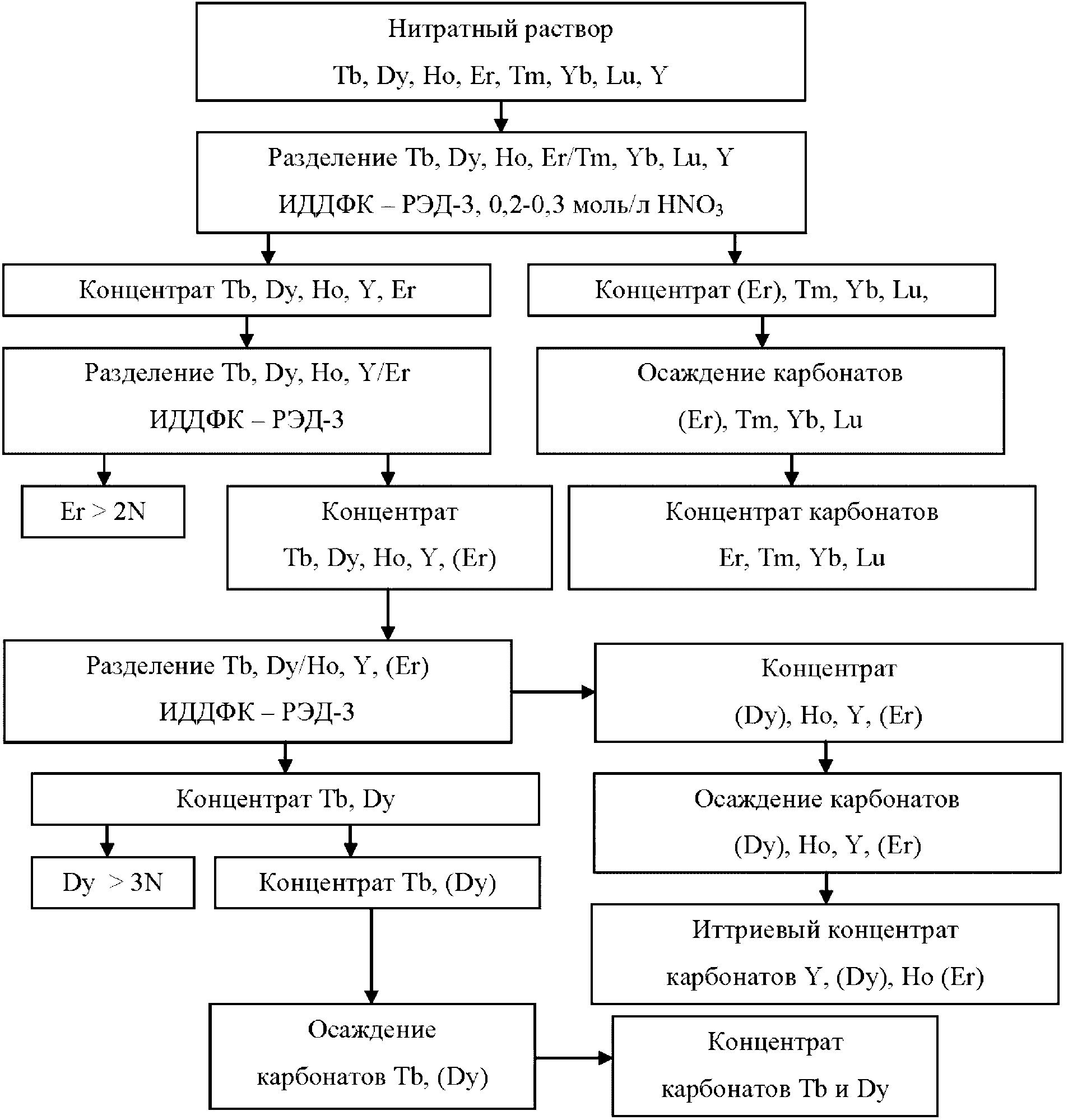
концентрата, полученного при переработке различного
минерального сырья
Другие по составу концентраты, полученные по схеме, могут быть направлены на выделение индивидуальных РЗЭ и иттрия. Стадия осаждения карбонатов РЗЭ позволяет исключить из схемы межкаскадные упарки водных рафинатов или реэкстрактов.
Для получения чистых оксидов тяжелых РЗЭ в рассмотренной схеме используют противоточные экстракционные каскады с промывкой и орошением их промывной и рафинатной части.
Известны способы экстракционного разделения РЗЭ с использованием фосфиновых кислот в смеси с солями тетраалкиламмония, арилфосфоновыми или алкилфосфоновыми кислотами или эфирами.
Экстракционное разделение РЗЭ с использованием алкилфосфиновых кислот впервые было запатентовано французами Jean-Louis Sabot, Alain Rollat. В дальнейшем этот процесс был запатентован и в других странах.
Указанные экстрагенты используют в чистом виде или в виде растворов, содержащих от 5 до 100 об. % экстрагента, в алифатических или ароматических углеводородах, керосине, хлорированных углеводородах. Для повышения растворимости в органическую фазу могут быть добавлены спирты, эфиры фосфорной или фосфиновых кислот, фосфиноксиды или сульфоксиды в количестве от 3 до 20 об. %.
Экстракцию проводят из водных растворов с содержанием суммы РЗЭ в пересчете на оксиды от 20 до 500 г/л при кислотности водной фазы от 0,01 до 3,0 моль/л азотной кислоты. pH водной фазы не может быть ниже 3. Для корректировки pH используют гидроксид натрия или аммиачную воду. Экстракцию проводят в интервале температур от 10 °C до 50 °C, преимущественно при 20 - 40 °C. Экстракцию РЗЭ алкилфосфиновыми кислотами можно также проводить из водных растворов серной, соляной и хлорной кислот.
2.20.16 Универсальная технология разделения РЗЭ
В настоящее время единственным российским промышленным производителем оксидов и других соединений индивидуальных РЗЭ из отечественного сырья является ГК "Скайград" (ООО "ЛИТ", ООО "Скайград Инновации" и др.).
В основе производства ГК "Скайград" - собственная универсальная технология [73, 82], инициативно разработанная специалистами холдинга в период 2011 - 2018 гг. Сущность технологии заключается в том, что на первом этапе из исходного ГРЗК после растворения в азотной кислоте извлекают основной компонент - церий - путем его электрохимического окисления с последующей экстракцией. Лантан, празеодим, неодим и элементы среднетяжелой группы последовательно выделяют экстракционным разделением ГРЗК после извлечения церия. При этом на всех стадиях экстракционного передела в качестве экстрагента используют 70 - 75 об. % раствор ТБФ в жидком нефтяном парафине фракции C10-13 (ПНЖ C10-13). Оксиды индивидуальных РЗЭ получают осаждением карбонатов из соответствующих рафинатов/реэкстрактов с дальнейшей фильтрацией, сушкой и прокалкой осадка [77].
Электрохимические и экстракционные процессы на производстве осуществляются с помощью уникального оборудования, созданного ГК "Скайград":
- двухкамерных электролизеров с разделяющей катодное и анодное пространство пористой корундовой диафрагмой, изготовленной плазмохимическим методом, и титановыми анодами с активирующим покрытием из диоксида иридия [83];
- каскадов центробежных экстракторов [78, 79, 80], оснащенных автоматизированной системой управления, позволяющими операторам дистанционно контролировать текущее состояние, включать/выключать оборудования, изменять режим его работы.
Использование центробежных экстракторов, как наиболее экономичного в отношении объемов загрузки экстрагента и незавершенного производства экстракционного оборудования, является существенным отличием технологии ГК "Скайград" от промышленных технологий Китая, Европы и США, где экстракционное разделение реализуют в стандартных смесительно-отстойных экстракторах ящичного типа (размещение которых при аналогичной производительности требует в 7 - 10 раз больших заводских площадей).
Универсальность технологии обусловлена возможностью вариативности состава сырья (допускается использование ГРЗК: производства ОАО "СМЗ", извлеченного из отвального фосфогипса ОАО "ВМУ", полученного при освоении месторождения Томтор и др.) и степени чистоты продукции в зависимости от заданных требований. Ассортимент продукции включает азотнокислые растворы, карбонаты, оксиды индивидуальных РЗЭ и их смесей, может быть расширен в соответствии с пожеланиями заказчика. Блок-схема технологического процесса приведена на рисунке 2.36, удельные нормы расходов реагентов и электроэнергии - в таблице 2.15, перечень и характеристики выпускаемой продукции - в таблице 2.16.
Таблица 2.15
ГРЗК легкой группы РЗЭ (в пересчете на оксиды)
Наименование | Единица измерения | Цена, руб./ед. | Норма расхода | |
Ед./кг РЗО | Руб./кг | |||
Азотная кислота (57%) | кг | 14 | 1,2 | 16,8 |
Перекись водорода, техническая, марка А (37,5%) | кг | 40 | 0,133 | 5,3 |
Аммиак водный, 25% | кг | 12 | 1,83 | 22 |
Углекислый газ сжиженный | кг | 14 | 1 | 14 |
Вода питьевая | м3 | 30 | 0,03 | 0,8 |
Вода деионизированная | м3 | 120 | 10 | 0,3 |
ТБФ | кг | 322 | 0,009 | 2,9 |
ПНЖ C10-13 | кг | 62,2 | 0,003 | 0,187 |
Тара для продукции | шт. | 155 | 0,0067 | 1,03 |
ИТОГО ПО РЕАГЕНТАМ | 63,5 | |||
Электроэнергия | кВт·ч | 4,974 | 18,3 | 90,78 |
ИТОГО | 154,28 | |||
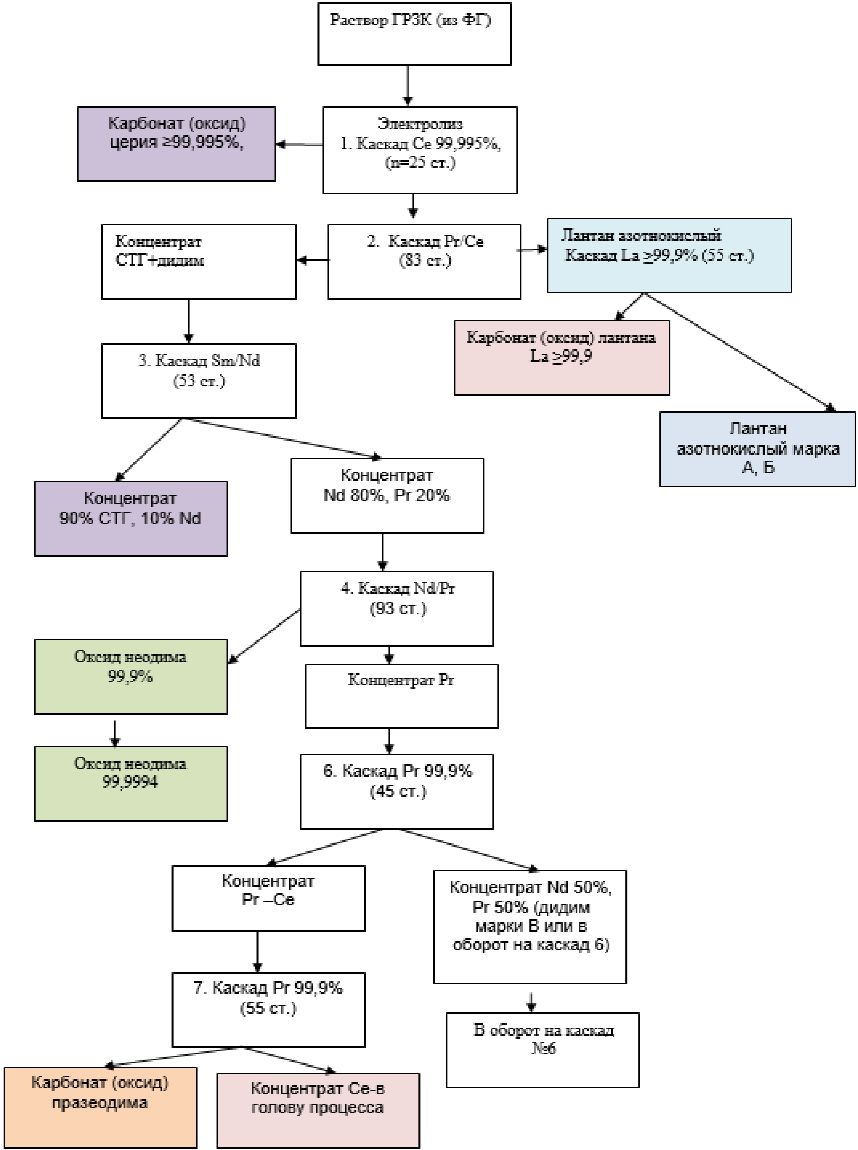
разделения ГРЗК ГК "Скайград"
Таблица 2.16
ГК "Скайград"
Наименование | Технические условия | Содержание основного РЗЭ в |
Азотнокислый раствор лантана | ТУ 20.13.65-001-92697718-2018 | 90 (марка А) 70 (марка Б) 65 (марка В) |
Оксид лантана | ТУ 20.13.65-002-92697718-2018 | 99,9997 (марка Г) 99,9990 (марка Д) 99,9896 (марка Ж) 99,8958 (марка Л) |
Оксид церия | ТУ 20.13.65-003-92697718-2018 | 99,995 (марка Д) 99,980 (марка Ж) 99,800 (марка Л) |
Карбонат церия влажный | ТУ 20.13.65-002-92697718-2018 | 99,9 (марки О, К, Л) |
Полировальный порошок "Skypolish" | ТУ 20.13.65-002-92697718-2018 | 98 (марки ЦК, ЦУ, ЦМ, ЦД, ЦДУ) |
Аммония-церия (IV) нитрат | В разработке | - |
Карбонат празеодима | В разработке | 70 - 80 |
Оксид неодима | ТУ 20.13.65-004-92697718-2018 ТУ 20.13.65-010-92697718-2020 | 99,999 (марка А) 99,99 (марка Б) 99,9 (марка В) 99,5 (марка Г) |
Неодеканоат неодима | ТУ 20.14.33-011-92697718-2020 | 99,5 (марки А, Б, В) |
Хлорид неодима | ТУ 20.13.65-015-92697718-2023 | 99,9 (марки А, Б) |
Оксид дидима | ТУ 20.13.65-007-92697718-2018 | 89 Nd2O3 (марка А) 74 Nd2O3 (марка Б) 74 Nd2O3 (марка В) |
Концентрат СТГ РЗЭ | В разработке | - |
Технология реализована на экспериментальном производстве ООО "ЛИТ". Производство освоено в 2018 г. и выведено на мощность 150 т/год в пересчете на оксиды РЗЭ.
2.21.1 Сырьевые ресурсы
Магний - один из наиболее распространенных в природе химических элементов: содержание его в земной коре по разным оценкам составляет от 1,90 до 2,35% (8 место по распространенности). Подтвержденные мировые запасы этого химического элемента составляют 2243 млрд т, при этом магний, содержащийся в водах Мирового океана составляет ~ 1800 млрд т. В природе магний находится в двух формах соединений: оксидной и солевой. Оксидные формы представлены в основном в виде силикатов и карбонатов, солевые - в виде хлоридных и сульфатных солей. В таблице 2.17 приведены минеральные формы соединений магния, имеющие промышленное значение.
Таблица 2.17
Минерал | Формула | Содержание Mg в минерале, % | |
Оксидные формы | Силикаты: Оливин (форстерит, дунит) Серпентин | 2MgO·SiO2 | 34,6 |
3MgO·2SiO2·2H2O | 26,3 | ||
Карбонаты Магнезит Доломит | MgCO3 | 28,8 | |
MgCO3*CaCO3 | 13,2 | ||
Гидрооксид Брусит | Mg(OH)2 | 41,6 | |
Солевые формы | Хлориды Бишофит Карналлит | MgCl2·6H2O | 12,0 |
KCl·MgCl2·6H2O | 8,8 | ||
Сульфаты Кизерит Лангбейнит Каинит | MgSO4·H2O | 17,6 | |
2MgSO4·K2SO4 | 11,7 | ||
MgSO4·KCl | 9,8 |
Как правило, оксидные формы магнезиальных минералов являются продуктами, образующимися в результате выветривания и/или гидротермальных метаморфоз оливина. Оливин является магматической породой и, как следствие, занимает одно из первых мест по распространенности среди минералов. По этой причине запасы производных от оливина пород также достаточно велики: карбонатные породы (доломит+магнезит) ~ 25 - 30 млрд т. Значительно менее распространен брусит, его разведанные запасы составляют 20 - 30 млн т, при этом более 50% бруситовых руд представлены минералами с содержанием кальция 22 - 30%. Для производства металлического магния методом термического восстановления используется исключительно доломит. Производства, использующие магнезит или силикаты магния для получения хлористого магния с его последующим электролизом, в настоящее время не функционируют.
Промышленная разработка месторождений оксидных форм магния ведется открытым способом и характеризуется достаточно простой технологией обогащения сырья.
Источниками хлоридов и сульфатов магния являются ископаемые соли, а также соли входящие в состав вод Мирового океана и соляных озер. Если не принимать во внимание морские водоемы, то 60 - 61% запасов представлены хлоридными солями, 10 - 15% - смешанными (хлоридно-сульфатными), 17 - 20% солями, содержащимися в воде соляных озер. В качестве важнейшего сырьевого минерала следует выделить карналлит KCl·MgCl2·6H2O. Разведанные запасы ископаемого карналлита без учета Северной Америки составляют приблизительно 10 млрд тонн, сосредоточенные в крупных месторождениях России, Конго, Германии, Испании. В настоящий момент из карналлита производится 4% от общего количества металлического магния: Россия - 20 тыс т/год, Израиль - 20 тыс т/год.
Выбор технологии производства магния во многом определяется видом располагаемого магниевого сырья. В случае оксидных минералов может применяться как прямое термическое восстановление магния, так и электролиз хлорида магния, получаемого из силиката, карбоната или гидрооксида магния. В случае переработки сырья содержащего хлорид магния наиболее целесообразным методом получения металлического магния является электролиз. Таким образом, в зависимости от типа металлургического передела (стадии получения металлического магния) все существующие либо существовавшие технологии получения магния разделяются на электролизные и термические. При оценке конкурентоспособности различных технологических схем одним из важных факторов является доступность сырья и объемы его запасов.
2.21.2 Способы производства металлического магния
Методы термического восстановления.
Основной химической реакцией, протекающей в данном типе технологических процессов, является
2CaO·MgO + Si = Ca2SiO4 + 2Mg (г) (2.62)
Поскольку CaO используется для связывания оксида кремния в двухкальциевый силикат, в качестве магнезиального сырья используют кальцинированный доломит. В качестве восстановителя применяется ферросилиций (Si 75 - 78%). Модификации процесса с использованием альтернативных восстановителей (карбида кремния, кокса, низкосортного силумина и др.) в промышленном масштабе не были реализованы.
Термическое восстановление предполагает удаление образующегося магния из зоны реакции в виде паров, поэтому процесс проводят при температуре не менее 1150 °C в условиях вакуума. Пары магния конденсируются в холодной части реактора либо в отдельном конденсаторном узле. Далее порошкообразный конденсат ("crown magnesium") расплавляется и подвергается рафинированию. Основные отличия той или иной модификации процесса заключается в нюансах аппаратурного оформления и способом подвода тепла.
Pidgeon процесс
Доломит после кальцинации и помола, смешивают с молотым ферросилицием, формуют в брикеты, которыми наполняют реторты (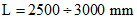 ,
, 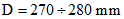 ). Далее реторты (16 - 20 шт.) размещают в печи, вакуумируют и нагревают. Подвод тепла от топочных газов внутрь реторты осуществляется через ее стенку. Процесс проводится при температуре 1150 - 1200 °C и остаточном давлении 0,05 - 0,06 мм. рт. ст. После завершения реакции реторту охлаждают, разбирают, производят выгрузку магниевого конденсата ("crown magnesium"), силиката кальция и остатков ферросилиция (Si 20%). Магний направляется на переплавку. Периодичность процесса, большое количество операций обслуживания, способ подвода тепла определяют основные недостатки данной технологии: увеличение размеров реторты невозможно из-за ухудшения теплопередачи, производительность процесса составляет 66 - 70 кг/сутки на реторту, коэффициент эффективности использования топлива 12 - 15%, производительность труда - 25 т/год на человека. Следует отметить, что среди китайских производителей, использующих в основном Pidgeon процесс, средний показатель производительности составляет 25 - 40 т/год на человека.
). Далее реторты (16 - 20 шт.) размещают в печи, вакуумируют и нагревают. Подвод тепла от топочных газов внутрь реторты осуществляется через ее стенку. Процесс проводится при температуре 1150 - 1200 °C и остаточном давлении 0,05 - 0,06 мм. рт. ст. После завершения реакции реторту охлаждают, разбирают, производят выгрузку магниевого конденсата ("crown magnesium"), силиката кальция и остатков ферросилиция (Si 20%). Магний направляется на переплавку. Периодичность процесса, большое количество операций обслуживания, способ подвода тепла определяют основные недостатки данной технологии: увеличение размеров реторты невозможно из-за ухудшения теплопередачи, производительность процесса составляет 66 - 70 кг/сутки на реторту, коэффициент эффективности использования топлива 12 - 15%, производительность труда - 25 т/год на человека. Следует отметить, что среди китайских производителей, использующих в основном Pidgeon процесс, средний показатель производительности составляет 25 - 40 т/год на человека.
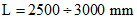 ,
, 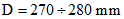 ). Далее реторты (16 - 20 шт.) размещают в печи, вакуумируют и нагревают. Подвод тепла от топочных газов внутрь реторты осуществляется через ее стенку. Процесс проводится при температуре 1150 - 1200 °C и остаточном давлении 0,05 - 0,06 мм. рт. ст. После завершения реакции реторту охлаждают, разбирают, производят выгрузку магниевого конденсата ("crown magnesium"), силиката кальция и остатков ферросилиция (Si 20%). Магний направляется на переплавку. Периодичность процесса, большое количество операций обслуживания, способ подвода тепла определяют основные недостатки данной технологии: увеличение размеров реторты невозможно из-за ухудшения теплопередачи, производительность процесса составляет 66 - 70 кг/сутки на реторту, коэффициент эффективности использования топлива 12 - 15%, производительность труда - 25 т/год на человека. Следует отметить, что среди китайских производителей, использующих в основном Pidgeon процесс, средний показатель производительности составляет 25 - 40 т/год на человека.
). Далее реторты (16 - 20 шт.) размещают в печи, вакуумируют и нагревают. Подвод тепла от топочных газов внутрь реторты осуществляется через ее стенку. Процесс проводится при температуре 1150 - 1200 °C и остаточном давлении 0,05 - 0,06 мм. рт. ст. После завершения реакции реторту охлаждают, разбирают, производят выгрузку магниевого конденсата ("crown magnesium"), силиката кальция и остатков ферросилиция (Si 20%). Магний направляется на переплавку. Периодичность процесса, большое количество операций обслуживания, способ подвода тепла определяют основные недостатки данной технологии: увеличение размеров реторты невозможно из-за ухудшения теплопередачи, производительность процесса составляет 66 - 70 кг/сутки на реторту, коэффициент эффективности использования топлива 12 - 15%, производительность труда - 25 т/год на человека. Следует отметить, что среди китайских производителей, использующих в основном Pidgeon процесс, средний показатель производительности составляет 25 - 40 т/год на человека.Похожие условия и показатели имеет процесс, в которой используется реактор Бользано. В данном случае принципиальным отличием является применение электрического нагрева и увеличенный объем реторты. Первое приводит к увеличению эффективности использования энергии, второе увеличивает производительность реактора 2 т/день. Несмотря на увеличение размеров реактора, и в данном варианте трудно осуществить полную механизацию и автоматизацию процесса, что является причиной низкого показателя производительности труда 25 т/год на человека.
Процесс Magneterm
Главное отличие данной технологии состоит в том, что реакция восстановления магния протекает в жидкой фазе расплавленного алюмосиликата кальция. Для этого в реактор вместе с кальцинированным доломитом и ферросилицием вводят кальцинированный глинозем, таким образом, чтобы в шлаке сохранялись молярные соотношения
CaO:SiO2 >= 2; Al2O3:SiO2 >= 1. Процесс проводят при остаточном давлении 4 - 7 Па при температуре 1900 °C. По мере накопления производят слив шлака и обедненного ферросилиция. Обогрев реактора осуществляют электрическим током, пропускаемым через шлаковую ванну. Процесс является полунепрерывным, все операции в нем механизированы и автоматизированы. В результате этого производительность реактора Magneterm составляет 14 т/день.
Технология производства магния электролизом
Электролиз хлорида магния является исторически первым методом, который был использован для получения магния в промышленном масштабе. За долгие годы промышленного применения процесс был хорошо изучен и оптимизирован применительно к схемам переработки различных видов сырья.
Электролиз хлорида магния протекает по реакции
MgCl2 = Mg + Cl2 (2.63)
Процесс ведут, пропуская постоянный ток через расплав хлоридов щелочных металлов, в состав которого входит хлорид магния. При этом поддерживается температура 690 - 710 °C, в результате выделяющийся на катоде металл извлекается из электролизера в жидком виде, а хлор собирается в трубопроводах и транспортируется на дальнейшую переработку. По мере расходования хлорида магния в электролизер загружается дегидратированные соли: хлорид магния, либо карналлит.
Принципиальные различия в технологических схемах электролизных производств проявляются на стадии подготовки сырья в зависимости от его типа. В случае применения в качестве магниевого сырья растворов хлорида магния либо бишофита, либо карналлита главной задачей на предварительных стадиях технологии является дегидратация сырья.
Производство металлического магния из хлоридного и оксидного сырья методом электролиза расплава хлорида магния состоит из следующих основных переделов:
- Получение чистых растворов хлорида магния;
- Синтез карналлита из концентрированных хлормагниевых растворов и хлористого калия, получаемого из отработанного электролита;
- Обезвоживание синтетического карналлита в токе топочных газов, полученных от сжигания природного газа или обезвоживания бишофита в токе сухого 100% HCl;
- Получение безводного карналлита или бишофита;
- Электролиз безводного карналлита или бишофита с получением магния - сырца, анодного хлоргаза и отработанного электролита;
- Рафинирование магния и разливка его на чушки;
- Дробление отходов;
- Переработка анодного хлоргаза с получением концентрированной соляной кислоты, возвращаемой на выщелачивание оксида магния из оксидного сырья или на производство раствора хлорида кальция при переработке бишофита или карналлита.
Процесс Norsk Hydro
Технология, используемая Norsk Hydro в Норвегии, использует магниевые рассолы, получаемые из отходов производства поташа в Германии. Рассолы сначала обрабатываются сульфидом натрия, хлоридом кальция и хлоридом бария с целью удаления тяжелых металлов и сульфатов осаждением и фильтрацией. Очищенные растворы нагревают, концентрируют (до содержания 45 - 50% MgCl2) и обезвоживают до получения безводного хлорида магния. Часть хлора возвращается в цикл, часть продается. Степень извлечения магния составляет 97%.
Процесс IG-Farben
Технология основана на хлорировании MgO, полученного после прокалки доломита в присутствии углерода. Получаемый хлорид магния подается на стадию электролиза.
Процесс MagCan
Технология основана на взаимодействии MgCO3 (магнезита) с хлором в присутствии оксида углерода (II). Получаемый расплав подается на стадию электролиза;
Технология Magnola и Русмаг
Технология Magnola и Русмаг основана на солянокислом разложении серпентинита с получением концентрированного раствора хлорида магния, поставляемого в дальнейшем на стадию обезвоживания и электролиз. Кек оксидов и гидроксидов Si, Ni, Fe, Cr, полученных в процессе очистки раствора подвергаются гидрометаллургической переработки с получением чистого оксида кремния (белой сажи) концентратов окислов Ni, Fe, Cr.
Электролитическое получение магния из карналлита
Процесс разработан в СССР. Основным сырьем для производства магния в России до сегодняшнего времени служит карналлит Верхнекамского месторождения калиевого-магниевых хлористых солей. Магниевый завод в г. Калуш в Украине использовал хлормагниевые щелока, полученные в результате обессульфачивания сульфатных щелоков хлористым кальцием, как отходы производства, образующиеся при получении сульфата калия из полиминеральных руд Прикарпатья. В Израиле магниевый завод работает на садочном карналлите, получаемом в результате стадийного упаривания воды Мертвого моря в прудовых отстойниках энергией солнца. Суть общего технологического процесса производства магния на этих трех заводах, работающих на различных источниках сырья, в конечном счете состоит в получении 6-ти водного карналлита KCl*MgCl2*6H2O путем рекристаллизации минералов карналлита или синтезирования их из хлоркалиевых или хлормагниевых растворов.
Производство синтетического карналлита
На первой стадии производится растворение природного карналлита в растворяющем щелоке, предварительно нагретом до 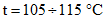 за счет тепла паров вакуумкристаллизационных установок (ВКУ). Суспензия из растворителя направляется на сгущение и фильтрацию. Солевой шлам, представляет собой галитовый остаток (20% KCl и 80% NaCl). Растворы хлористого магния и хлористого калия поступают на выпарную и вакуум кристаллизационную установку. Кристаллизация карналлита осуществляется в пятикорпусной ВКУ, состоящей из пяти последовательно расположенных вертикальных аппаратов с двойным циркуляционным контуром. Наличие пяти корпусов ВКУ обеспечивает требуемый средний размер частиц
за счет тепла паров вакуумкристаллизационных установок (ВКУ). Суспензия из растворителя направляется на сгущение и фильтрацию. Солевой шлам, представляет собой галитовый остаток (20% KCl и 80% NaCl). Растворы хлористого магния и хлористого калия поступают на выпарную и вакуум кристаллизационную установку. Кристаллизация карналлита осуществляется в пятикорпусной ВКУ, состоящей из пяти последовательно расположенных вертикальных аппаратов с двойным циркуляционным контуром. Наличие пяти корпусов ВКУ обеспечивает требуемый средний размер частиц 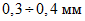 . Синтетический карналлит после центрифуг с массовой долей гигроскопической воды не более 3% направляется на стадию обезвоживания.
. Синтетический карналлит после центрифуг с массовой долей гигроскопической воды не более 3% направляется на стадию обезвоживания.
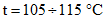 за счет тепла паров вакуумкристаллизационных установок (ВКУ). Суспензия из растворителя направляется на сгущение и фильтрацию. Солевой шлам, представляет собой галитовый остаток (20% KCl и 80% NaCl). Растворы хлористого магния и хлористого калия поступают на выпарную и вакуум кристаллизационную установку. Кристаллизация карналлита осуществляется в пятикорпусной ВКУ, состоящей из пяти последовательно расположенных вертикальных аппаратов с двойным циркуляционным контуром. Наличие пяти корпусов ВКУ обеспечивает требуемый средний размер частиц
за счет тепла паров вакуумкристаллизационных установок (ВКУ). Суспензия из растворителя направляется на сгущение и фильтрацию. Солевой шлам, представляет собой галитовый остаток (20% KCl и 80% NaCl). Растворы хлористого магния и хлористого калия поступают на выпарную и вакуум кристаллизационную установку. Кристаллизация карналлита осуществляется в пятикорпусной ВКУ, состоящей из пяти последовательно расположенных вертикальных аппаратов с двойным циркуляционным контуром. Наличие пяти корпусов ВКУ обеспечивает требуемый средний размер частиц 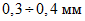 . Синтетический карналлит после центрифуг с массовой долей гигроскопической воды не более 3% направляется на стадию обезвоживания.
. Синтетический карналлит после центрифуг с массовой долей гигроскопической воды не более 3% направляется на стадию обезвоживания.Обезвоживание карналлита
Синтетический карналлит обезвоживается в печах кипящего слоя (КС) или во вращающихся трубчатых печах. Обезвоживание осуществляется топочными газами за счет сжигания природного газа в камерных топках печей кипящего слоя путем нагрева его последовательно до температуры 120 °C - 210 °C.
В процессе нагревания карналлита происходит термическое разложение шестиводного карналлита до двухводного:
А) 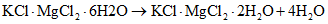 (2.64)
(2.64)
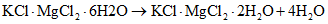 (2.64)
(2.64)Б) 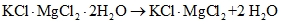 (2.65)
(2.65)
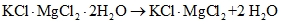 (2.65)
(2.65)Обезвоживание карналлита сопровождается гидролизом хлорида магния:
MgCl2 + H2O = MgOHCl + HCl (2.66)
Для подавления реакции термогидролиза хлорида магния, с образованием оксида магния, в горелочное устройство второй и третьей топок вводится газообразный хлористый водород. Повышение концентрации хлористого водорода в топочных газах второй и третьей камер печи кипящего слоя приводит к подавлению реакции гидролиза карналлита по реакции:
MgOHCl + HCl = MgCl2 + H2O (2.67)
На выходе газов из печей КС предусмотрена сухая пылеочистка с возвратом продукта в бункера обезвоженного карналлита, а затем мокрая очистка газов от хлористого водорода и остаточного хлора в двухступенчатых полых абсорберах орошаемых абсорбентом.
Полученный в отделении обезвоженный продукт на вторую стадию обезвоживания.
Получение безводного карналлита
Безводный карналлит получают в электропечах. Расплавление карналлита происходит за счет тепла, выделяющегося при протекании электрического тока через расплавленный карналлит. Одновременно с расплавлением в плавильниках агрегатов идет обезвоживание карналлита:
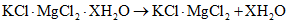 (2.68)
(2.68)которое сопровождается гидролизом хлористого магния с образованием оксида магния и хлористого водорода. Гидролиз хлористого магния протекает в две стадии:
а) при температуре не более 550 °C по реакции:
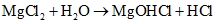 (2.69)
(2.69)б) при температуре более 550 °C гидрооксихлорид магния (MgOHCl) разлагается на оксид магния и хлористый водород:
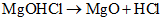 (2.70)
(2.70)Для хлорирования образовавшегося при обезвоживании оксида магния в расплав камеры перегрева через фурмы подается газообразный хлор.
Расплав безводного карналлита в вакуумных ковшах транспортируется в отделение электролиза.
Электролиз безводного карналлита
Процесс электролитического получения магния включает разложение под действием электрического тока хлорид магния, имеющий наименьшее напряжение разложения по сравнению с другими компонентами хлоридной системы (MgCl2-KCl-NaCl), что обеспечивает его электролитическое разложение в первую очередь. На катоде протекают процессы восстановления катионов магния из анионных комплексов по результирующим реакциям:
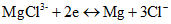 (2.71)
(2.71)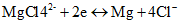 (2.72)
(2.72)На аноде происходит разряд ионов хлора: 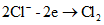 .
.
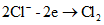 .
.Процесс электролитического получения магния и хлора осуществляется в поточной линии, состоящей из головного миксера, 3-х рафинировочных электролизеров, 31-го проточного электролизера, разделительного миксера с насосом-дозатором для создания потока расплава электролита и магния в аппаратах поточной линии.
Отбираемый от электролизеров анодный хлоргаз по магистральным хлорпроводам, направляется на очистку и использование в производстве титана, ниобия, тантала и РЗМ.
Рафинирование магния
В отделении рафинирования магний сырец из вакуумных ковшей заливается в рафинировочную камеру печи непрерывного рафинирования (ПНР), или в печи СМТ, где он очищается от электролита электролизных ванн и от твердых взвесей MgO в нагретом электролите, после чего кондукционным электромагнитным насосом разливается в изложницы двух литейных конвейеров. Для защиты от горения струи металла при разливке используют смесь газов: 1% SO2 + 99% N2, которая подается под кожух конвейера в зону разливки.
Воздух, отсасываемый от кожухов литейных конвейеров, содержащий оксид магния, очищается на фильтрующих элементах в рамных ионно-обменных фильтров.
В России и за рубежом были приняты различные технологические схемы получения металлического кальция: электролиз хлористого кальция; металлотермическое восстановление оксида кальция. В каждом из этих двух способов есть свои положительные и отрицательные стороны. Электролитический способ основан на электролитическом выделении кальция из хлорида на медно-кальциевом катоде с последующей дистилляцией кальция из этого сплава.
Для электролизного метода преимуществами являются высокий выход (70 - 80%) и чистота продукта (свыше 99%), главным недостатком - большая энергоемкость. Схема электролитического получения кальция является многооперационной и экологически небезопасной. В технологии используется большое количество реагентов и материалов. При использовании способа металлотермии в качестве восстановителя может применяться алюминий или кремний. В соответствии с этим процессы разделяются на алюминотермические и силикотермические. Схема металлотермического восстановления более гибкая и экологически менее опасная. Достоинство металлотермического метода - малый расход электроэнергии и отсутствие вредных выбросов, недостаток - более низкий выход (55 - 65%). Несмотря на отмеченный недостаток, на данный момент лидером в мировом производстве металлического кальция является именно алюминотермический способ, не имеющий ни газовых, ни жидких вредных выбросов, что немаловажно в экологическом плане. Чистота металлического кальция, полученного алюминотермическим восстановлением, находится на уровне 98,4 - 99,8% Ca, а электролитическим - до 99,9% Ca. В настоящее время в мире большинство предприятий использует алюминотермический способ получения металлического кальция. Однако российские предприятия в большинстве случаев производят кальций электролизным методом. Китайские производители, ранее также использовавшие электролиз, в настоящее время переходят на металлотермический способ. Основной причиной перехода на новый способ производства явилась экономия: стоимость 1 т кальция при алюминотермическом способе производства значительно ниже, чем при электролизе. Кроме того, для использования в металлургической промышленности (основном потребителе металлического кальция) не требуется кальций высокой чистоты.
Приготовление известкового молока
Для приготовления известкового молока используется строительная известь с содержанием CaO, согласно ГОСТ 9179-2018, и вода. Известь поступает на предприятие, разгружается в закрытом складе и далее перегружается в приемный бункер. Перед подачей на гашение известь при необходимости предварительно измельчается. При разгрузке, дроблении и измельчении извести возможно ее пыление. Для очистки воздуха от известковой пыли в цехе установлено газоочистное оборудование (циклоны, орошаемые газоходы и пр.), уловленная пыль используется в процессе приготовления известкового молока.
Негашеная известь поступает на стадию гашения, куда одновременно подается вода в необходимом количестве. Полученное известковое молоко направляется в расходные емкости и используется для технологических нужд предприятия.
Процесс производства известкового молока более подробно описан в ИТС НДТ 7 "Производство извести".
Получение порошка хлорида кальция
Известковое молоко направляется в механические абсорберы, где производится его хлорирование анодными газами. Полученная пульпа фильтруется через фильтр-прессы. После фильтрования чистый раствор хлористого кальция направляется в распылительные сушильные башни для обезвоживания при температуре 450 °C. В результате обезвоживания получается сухой порошок хлористого кальция с содержанием основного вещества 94 - 96%. В качестве теплоагента в сушильных башнях используется горячий воздух, полученный путем сжигания природного газа. Далее порошок хлористого кальция направляется на электролиз.
Получение кальциево-медного сплава электролитическим способом
Электролиз расплава хлористого кальция на жидкометаллическом медном катоде с целью получения медно-кальциевого сплава:
Сплавы с медью, содержащие до 60% кальция, имеют плотность свыше 2,1 т/м3, благодаря чему они удерживаются на дне ванн. Электролитом служит расплав, содержащий 80 - 85% хлористого кальция и 20 - 15% хлористого калия. Электролиз ведут при температурах 650 - 715 °C в чугунных или стальных ваннах. Анодами служат пакеты из графитовых блоков. Газообразный хлор, образующийся в процессе электролиза солей, используется далее в производстве для хлорирования известкового молока.
Электролизные ванны обмурованы снаружи шамотным кирпичом Ш-5 и Ш-8, теплоизоляция ванн выполнена из асбестоцемента.
Электролизные ванны ежедневно зачищаются от шлаков, содержащих медь, кальций, графит, железо. Металлургические шлаки, съемы и пыль от электролизного передела кальциевого производства хранятся на специальной площадке, по мере готовности к транспортировке, отгружаются потребителям на предприятия по производству меди.
Полученный на переделе электролиза медно-кальциевый сплав из ванн под вакуумом переливается в металлические загрузочные стаканы и направляется на дистилляцию.
Получение кальция в слитке методом дистилляции
Кальций возгоняют из сплава в стальных ретортах, помещенных в электропечи, при температуре 950 - 1200 °C под вакуумом. Пары кальция конденсируются в верхней части реторт на размещенных в головке реторт приемных цилиндрах, охлаждаемых проточной водой. Процесс ведут до содержания в сплаве 20% кальция, остаток от возгонки возвращают обратно на электролиз. Для изготовления приемных цилиндров используется сталь тонколистовая кровельная. Для защиты нагреваемой части реторт применяется обмазка из огнеупорных молотых материалов на жидком стекле. Изнутри дистилляционные реторты и загрузочные стаканы покрываются слоем гидроокиси кальция для исключения прилипания металлического кальция к приемному цилиндру. Для отделения паров кальция от паров меди при дистилляции сплава реторты снаряжаются фильтрами из колец Рашига.
Дистилляционные электропечи обмурованы шамотным кирпичом Ш-5, ШЛ, НТ.
Обслуживание реторт предусматривает ремонт и замену неисправных металлических частей и деталей. Подвергшиеся коррозии стаканы реторт и загрузочные стаканы при невозможности их ремонта заменяются.
Для создания необходимого для технологического процесса вакуума применяются вакуумные насосы, имеющие масляные картеры, заполненные вакуумным маслом. В процессе эксплуатации насосов вакуумное масло увлажняется и загрязняется механическими примесями.
Полученный в результате вакуумной дистилляции кальций направляется на дальнейшую обработку для получения готовой продукции в виде слитков, стружки, крупки, гранул, кусков, прутка и КИП.
Общие сведения
Энергетические ресурсы делятся на две главные категории: невозобновляемые и возобновляемые. К невозобновляемым энергетическим ресурсам относятся углеводородные топлива: уголь, нефть, природный газ, горючие сланцы, водород, ядерное топливо и т.д. Современная энергетика в основном базируется на горючих ископаемых: угле, нефти, природном газе. Энергию получают тремя путями: производя тепло сжиганием топлива, прямым преобразованием тепловой энергии и получением специального вида энергии - электроэнергии. По существу, электроэнергия является вторичным энергоресурсом и выполняет роль посредника между источниками и потребителями энергии. Главными недостатками получения энергии является возможное негативное воздействие на окружающую среду.
Потребности в энергоресурсах значительно отличаются для различных технологий получения редких металлов. Они зависят от качества сырья и продукции, использования скрытого тепла или тепла отходящих газов и производства промежуточной продукции.
Основные экологические проблемы при производстве РМ связаны с загрязнением воздуха и воды и образованием опасных отходов. На предприятиях обычно устанавливают собственные водоочистные сооружения и используют замкнутые системы водооборота.
Для восполнения объемов оборотной воды, используемой в технологическом процессе, и потерь, связанных с испарением, могут собираться поверхностные стоки, а также дренажные стоки с полигонов захоронения отходов. Если позволяют объемы воды, выводимой из производственного процесса, может добавляться финальный этап кристаллизации, что позволяет полностью исключить сбросы загрязняющих веществ в принимающие водные объекты.
Многие виды отходов повторно используются в производстве, но основным видом, оказывающим значительное воздействие на окружающую среду, являются остаточные продукты выщелачивания. Для подотрасли характерны некоторые локальные аспекты, такие как шум и вибрация. В связи с тем, что ряд потоков твердых и жидких отходов являются опасными, существует значительный риск загрязнения почвы.
Уровни потребления ресурсов имеющихся на сегодняшний день технологий приведены в Приложении В.
Получаемые в пирометаллургических процессах выбросы в атмосферу либо улавливаются в виде дымовых газов, либо отходят в виде неорганизованных выбросов в зависимости от возраста установки и используемой технологии. Выбросы дымовых газов обычно контролируются либо в непрерывном режиме, либо периодически, и по ним представляется соответствующая отчетность. Большее беспокойство вызывают неорганизованные выбросы, которые необходимо улавливать. Также улавливаются возгоны и испарения в гидрометаллургических циклах.
К основным типам выбросов в атмосферу от производства редких металлов относятся:
- диоксид серы (SO2), иные соединения серы и кислотные пары;
- оксиды азота (NOx) и иные его соединения;
- металлы и их соединения;
- хлор, HCl, CO, фосген;
- летучие органические соединения и ПХДД/Ф;
- карбонат натрия;
- аммиак;
- пыли.
Иные загрязнители пренебрежимо малы, потому что они либо не присутствуют в производственном процессе, либо немедленно нейтрализуются (например, фтор или фториды), либо встречаются в низких концентрациях (органика). Определенные объемы загрязняющих веществ выбрасываются в составе пылей. Источники выбросов определяются используемыми технологиями (см. таблицу 3.1). К ним относятся:
- транспортировка, погрузка/разгрузка и подготовка сырья;
- обжиг/спекание и сернокислотная установка (большинство выбросов происходят во время незапланированных остановок);
- пирометаллургические операции: возгонка (спекание, обжиг), плавка и рафинирование;
- гидрометаллургические операции: выщелачивание, экстракция, сорбция, очистка и электролиз;
- механическая обработка: измельчение, размол и гранулирование;
- литье.
Другие загрязняющие вещества не имеют видимого значения для промышленности, потому что они не присутствуют в производственном процессе, сразу нейтрализуются (например, хлор или HCl) или потому, что их концентрация слишком мала (например, CO). Выбросы в значительной степени связаны с пылью.
Таблица 3.1
Компонент | Обжиг и иные пирометаллургические процессы | Выщелачивание и очистка | Электролиз | Механическая обработка | Литье и т.п. | Сернокислотная установка |
Оксиды и сульфаты серы | (кислотные пары) | |||||
Оксиды азота | НП | НП | НП | |||
Пыль и металлы | НП | |||||
Хлор, хлориды, ЛОС | НП | НП | НП | НП | ||
Примечание: (1) Прямые выбросы с этапов обжига или плавки подвергаются обработке и/или передаются на этапы газоочистки и на сернокислотную установку; по-прежнему остаются значимыми остаточные выбросы диоксида серы или оксидов азота с сернокислотной установки. Для этих источников также достаточно значимы неорганизованные и неуловленные выбросы. | ||||||
Помимо технологических выбросов, образуются неорганизованные выбросы. Основными источниками неорганизованных выбросов (см. таблицу 3.2) являются:
- пыль, образующаяся при хранении, погрузке/разгрузке и обработке концентратов;
- утечки из обжиговых и плавильных печей;
- аэрозоли и пыли, содержащиеся в отходящих газах от ванн выщелачивания и очистки;
- отходящие газы градирен для устройств выщелачивания, и очистки экстракционных установок;
- отходящие газы градирен процесса электролиза;
- прочие.
Таблица 3.2
Источник | Объем, т/год | Удельные выбросы, г/т РМ |
Пыль от хранения, погрузки/разгрузки и обработки концентратов и огарка | < 0,25 | 0,25 - 0,75 |
Аэрозоли и пыли из отходящих газов от ванн выщелачивания и очистки | < 2 | 1 - 9 |
Отходящие газы градирен для устройств выщелачивания и очистки | < 4 | 2 - 16 |
Отходящие газы градирен процесса электролиза (0,8 т/год) | < 5 | 3 - 20 |
Хотя неорганизованные выбросы трудно измерить и оценить, существуют некоторые успешно применяемые методы.
3.1.1.1 Оксиды азота
Этапы обжига и плавки являются потенциальными источниками образования оксидов азота (NOx). Оксиды азота (NOx) могут образовываться из соединений азота, присутствующих в концентратах, или из азота воздуха при высокой температуре. Получаемая серная кислота может поглощать большую часть NOx, что может негативно влиять на качество серной кислоты. Если после обжига наблюдается высокий уровень NOx, из экологических соображений и для поддержания качества продукта может потребоваться очистка газов, образующихся при обжиге. Другие печи, использующие кислородно-топливные горелки, могут также демонстрировать снижение NOx. Диапазон значений концентрации для всех процессов составляет от 10 до 120 мг/нм3.
3.1.1.2 Пыль и металлы
Вынос пыли от обжига или иных пирометаллургических процессов является потенциальным источником как организованных, так и неорганизованных выбросов. Пирометаллургические газы улавливаются и обрабатываются сначала в процессе газоочистки и затем при производстве серной кислоты. Пыль удаляется из газа и возвращается в технологический процесс.
Газы после разбрызгивающих или оросительных систем, используемых из мест выгрузки огарка и слива металла, также являются потенциальными источниками выбросов. В этих точках с целью предотвращения неорганизованных выбросов необходимо осуществлять максимально возможное улавливание отходящих газов и их очистку. Диапазон значений выбросов пыли из данных источников составляет от менее 1 мг/нм3 до 15 мг/нм3.
Аспирация реакторов на этапах выщелачивания, экстракции и очистки может привести к выбросу аэрозолей, которые можно при необходимости (при наличии регулярного контроля) улавливать с помощью скрубберов или туманоуловителей/демистеров. Выбросы, содержащие опасные вещества (водород), контролируют в местах возможных выбросов. Эти выбросы постоянно улавливают и пропускают через устройства газоочистки, например, скрубберы и туманоуловители (в системах мокрой очистки), и рукавные фильтры (в системах сухой очистки).
В цехе электролиза образуются выбросы аэрозолей, которые могут содержать металлы в растворенном виде. Диапазон значений выбросов пыли и паров из данных источников составляет от 0,2 до 1,25 мг/нм3.
В то время как для контролируемых выбросов всегда установлены определенные источники и эти выбросы можно улавливать, подвергать очистке и возвращать в процесс, неорганизованные выбросы распространяются практически по всей производственной площадке. Основными источниками неорганизованных выбросов являются места хранения и транспортировки материалов, пыль, оседающая на транспортных средствах, проездах или на открытых участках рабочей зоны, где никаких мер по их предупреждению и сокращению обычно не предпринимается. Сокращение неорганизованных выбросов достигается благодаря реализации следующих мероприятий, как:
- обновление систем улавливания и фильтрации отходящих газов;
- сокращение времени остановка печи путем усовершенствования процессов футеровки (соответственно, сокращение времени запуска и остановка, когда за ограниченный отрезок времени происходят значительные выбросы);
- укрытие/размещение внутри строений мест доставки, хранения материала, установка там газоулавливающих систем;
- усовершенствование обращения с материалами (например, путем увлажнения сыпучих материалов до и во время погрузки) и сокращение частоты транспортных операций (например, путем использования более мощных погрузчиков);
- установка обязательной мойки автотранспортных средств (для внутрицехового и внешнего транспорта);
- укрепление покрытий площадок и подъездных путей и оптимизация их уборки.
При производстве редких металлов основными загрязняющими веществами, содержащимися в стоках, являются металлы и их соединения, а также материалы в форме суспензии.
Другие вещества, попадающие в воду в значительных количествах - это хлориды, фториды и сульфаты.
Потоками сточных вод, в которых могут содержаться вышеуказанные вещества, являются:
- стоки с этапов обжига и газоочистки: мокрые скрубберы, мокрые электрофильтры, этап извлечения ртути;
- случайные утечки из различных гидрометаллургических процессов.
Другими потенциально загрязненными потоками сточных вод, которые собираются и повторно используются как промывочная вода при фильтрации (если позволяет их качество), являются:
- стоки, образующиеся при промывке анодов и катодов;
- уплотняющая вода из вакуумных насосов;
- общие операции, включая чистку оборудования, мытье полов и т.п.;
- слив из охлаждающих контуров (обычно следующих за некоторыми закрытыми циклами водооборота);
- ливневые и поверхностные стоки (прежде всего в зонах хранения) и стоки с крыш;
- вода, подаваемая с полигонов отходов и подземных полостей.
3.1.2.1 Стоки с водоочистных сооружений
В общем случае системы мокрой газоочистки эксплуатируются при замкнутом цикле оборота жидкости.
В мокрых скрубберах производится очистка кислых насыщенных SO2 растворов, образующихся в процессе обжига. В скруббере удаляются фториды, хлориды, следы ртути (если имеется) и селена и некоторые частицы, которые проходят механическую газоочистку. Во избежание накопления загрязняющих веществ некоторое количество жидкости непрерывно сливают из скруббера.
Металлы и их соединения, и материалы в виде суспензии являются основными загрязнителями в воду.
Другими важными веществами, которые попадают в воду являются хлориды, фториды и сульфаты.
Возможными потоками сточных вод, которые содержат вышеупомянутые вещества, являются:
- сточные воды от мокрых скрубберов;
- сточные воды от мокрых электрофильтров;
- уплотняющей воды из насосов;
- общие операции, в том числе очистки оборудования, полов и т.д.;
- выделения из контура охлаждающей воды;
- дождевые стоки с поверхности (в частности, мест хранения) и крыши.
В мокрых электрофильтрах также образуются кислые растворы. После фильтрации их перерабатывают. Некоторое количество жидкости сливают из данного контура, чтобы удалить накапливающиеся частицы загрязняющих веществ. Перед сливом данную жидкость обрабатывают и анализируют.
Продувочная жидкость в определенных количествах содержит взвешенные твердые частицы и растворенные соли. Продувочную жидкость перед сбросом очищают либо локально, либо в центральной водоочистной установке с целью удаления твердых и растворенных веществ. Место утилизации отделенных материалов зависит от источника происхождения сточных вод.
3.1.2.2 Сточные воды от газоочистки
Как правило, влажные газоочистные системы работают с рециркуляцией жидкости. Контролируемый отбор поддерживает количество взвешенных твердых частиц и растворенных солей в определенных заданных пределах. Абсорбера либо обрабатывают отдельно или в комплексе завода по обработке воды для удаления твердых и растворенных частиц перед выгрузкой. Назначение отделенного материала зависит от происхождения сточных вод. В мокрых электрофильтрах также будет образовываться кислая скрубберная жидкость. Она будет рециркулировать после фильтрации. Некоторую жидкость следует спустить из циркуляции, чтобы удалить накопленные загрязнения. Этот раствор обрабатывают и анализируют перед сбросом.
Таблица 3.3
Источники отработанной воды и технологии их переработки
Наименование процесса | Операция/источник | Возможное использование/обработка |
Главный | Дождевая вода с дорог, тротуаров, крыш, от мытья дорог, грузового автотранспорта и т.д. | Установка обработки воды, затем удаление или рециркуляция |
Плавильные операции | Вода охлаждения печей, машин и оборудования | Рециркуляция |
Система очистки газа | Конденсат от охлаждения газа и водного скруббера Конденсат от удаления ртути | Удаление суспензии, остаток как исходный материал. После удаления ртути на очистку воды. Рециркуляция |
Завод серной кислоты | Вода от охлаждения оборудования. Протечки | Рециркуляция На установку обработки воды |
Склад сырья | Поверхностная вода (дождевая) | На установку обработки воды |
Общее оборудование | Ремонт | На установку обработки воды |
Установка очистки воды | Обработка сточной воды | Остаток для текущего использования/сброс |
3.1.2.3 Слив электролита и экстрагентных фаз
Электролит и экстракционные фазы можно сливать из ванн и с целью контроля накопления примесей, например, магния, которые могут отрицательно влиять на работу электролитических ванн. Поток, обращающийся через электролитические ванны, относится к тому же закрытому водному контуру, к которому принадлежат этапы выщелачивания и очистки. Серная кислота, образующаяся во время электролиза, поступает в процесс выщелачивания, а оставшаяся часть жидкости очищается и подается на электролиз.
Стоки из цикла электролиза, выщелачивания, экстракции и очистки являются сильнокислыми и взвешенные твердые частицы в высокой концентрации. Объем стоков зависит от состава цинковых концентратов, используемых на этапе обжига. Элементы, которые склонны накапливаться в контуре, особенно магний, определяют объем сливаемой жидкости и необходимость ее очистки. Стоки из этой системы можно перерабатывать с целью извлечения Mg, Na, K, хлоридов и фторидов.
В таблице 3.4 представлены сводные данные по потенциальным источникам сточных вод и технологиям их переработки.
Таблица 3.4
Этап техпроцесса | Операция/источник | Использование/переработка |
Общие операции | Ливневые стоки с дорог, площадок, крыш, мокрая уборка дорог, мытье грузовиков и т.д. | Повторное использование и/или переработка на водоочистной установке |
Обжиг/мокрая газоочистка | Мокрая очистка газов из обжиговой печи | Водоочистная установка |
Выщелачивание | Общие операции, включая мокрую газоочистку | Возврат на выщелачивание |
Экстракция | Отстаивание, очистка | Возврат на экстракцию |
Сорбция | Отстаивание, очистка | Возврат на сорбцию |
Очистка | Общие операции | Возврат на выщелачивание |
Электролиз | Чистка ванн, анодов и катодов | Возврат на выщелачивание |
Все технологические установки | Техобслуживание | Водоочистная установка |
Водоочистная установка | Очистка стоков | Для некоторых методов повторное применение/сброс |
Производство металлов приводит к образованию ряда побочных продуктов, остаточных продуктов и отходов. Твердые остаточные продукты, образующиеся при реализации различных процессов и этапов очистки, могут использоваться по трем направлениям:
- повторное использование в данном процессе или на предыдущих процессах;
- переработка на последующих этапах с целью извлечения других металлов;
- окончательная утилизация после переработки, обеспечивающей безопасную утилизацию.
Значимыми являются следующие образующиеся твердые отходы:
- твердые остаточные продукты с высоким содержанием металлов, образующиеся в процессах выщелачивания, экстракции очистки и электролиза цинка. Эти продукты обычно повторно перерабатываются на соответствующем этапе технологического процесса.
Пыль или шлам от обработки газов используются в качестве сырья для производства других металлов, таких, как Ge, Ga, In или могут быть возвращены на переплавку или в контур выщелачивания для извлечения свинца и олова.
Селеновые остатки возникают из предварительной обработки ртутных или селеновых потоков от газовой очистки.
Тугоплавкие металлы имеют высокую точку плавления и также характеризуются другими специфическими физико-химическими свойствами, такими как высокая плотность, инертность, коррозионная и кислотная стойкость. Например, цирконий имеет способность захватить медленные нейтроны, что дает этому металлу важную роль в строительстве атомных реакторов. Тугоплавкие металлы производятся и как металлический слиток (стержни) с использованием электронно-лучевых печей и как металлический порошок в качестве исходного материала для порошковой металлургии типа прессованием или спеканием.
В разделе 2 проведен обзор общих методов, используемых при производстве редких металлов. Тяжелые металлы переносятся в процесс в виде микроэлементов в первичное или вторичное сырье. Металлы с температурой кипения ниже температуры процесса будут выделяться в виде газов в виде пара металлов, которые частично конденсируются и окисляются, чтобы образовать часть пыли и дыма из камеры обжига. Пары металлов и отходящие газы, образующиеся при плавке или рафинировании тугоплавких металлов в электронно-лучевой печи, собираются вакуумной системой и затем конденсируются интенсивным охлаждением. Другим экологическим воздействием производства тугоплавких металлов, таких как тантал, цирконий и гафний, являются радиоактивные уровни некоторых сырьевых материалов. Также следует учитывать токсикологию некоторых тугоплавких металлов, например, хрома, марганца и ванадия.
Производство тугоплавких металлов обычно требует высоких температур. Экологическое воздействие на воздух, воду и землю может быть классифицировано как следующее.
Потребление сырья и энергии.
Выбросы в атмосферу:
- выбросы пыли и дымов от плавки, производства твердосплавов и карбидов;
- другие выбросы в атмосферу - Аммиак (NH3), кислотный дым (HCl), фтористый водород (HF);
- ЛОС и тяжелые металлы.
Шум и вибрация.
Твердые остатки, отходы и полупродукты:
- пыль, дымы и шлам;
- шлак.
Сброс воды:
- перелив воды из скрубберов;
- сточные воды от грануляции шлака и металла;
- утечка из циклов охлаждающей воды.
Имеющиеся данные о потреблении сырья и энергии для производства тугоплавких металлов представлены в виде удельных входных факторов на основе тонны производственного продукта в следующих таблицах.
Таблица 3.5
Потребление сырья и энергии для производства тугоплавких
металлов в качестве конкретных факторов воды
Руда и концентраты, кг/т | н.о. |
Потребление энергии кВт/т | 1000 - 15 000 (APT* - производство) 3500 - 12 000 (производство карбида) 1500 - 2500 (цинк процесс) |
Газ, м3/т | н.о. |
Вода, м3/т | н.о. |
Порошок Al, кг/т | n.r |
Порошок кальция, кг/т | n.r |
Другие, кг/т | н.о |
APT - паровольфрамат аммония, н.о. - данные отсутствуют, n.r. - не имеет значения в этом процессе производства. | |
В таблице 3.6 представлена информация о данных процесса для плавки тугоплавких металлов в электронно-лучевой печи. В электронно-лучевых печах электронные пушки создают высокоэнергетические электроны, которые передают энергию на загрузку в печи, чтобы обеспечить ее плавление.
Таблица 3.6
в электронно-лучевой печи
Металл | Емкость тигля, т | Мощность печи, МВт | Производительность т/ч | Потребление энергии кВт/т |
Ниобий | 0,5 - 2 | < 1,2 | 0,02 - 0,4 | 6000 - 15 000 |
Тантал | 0,5 - 2 | < 1,2 | 0,02 - 0,4 | 6000 - 15 000 |
Молибден | 0,02 - 0,1 | < 5000 | ||
Вольфрам | 0,02 - 0,1 | < 5000 | ||
Титан | 0,2 - 0,1 | 1000 |
Электронно-лучевые печи используются для плавления и/или очистки тугоплавких металлов, таких как ванадий, ниобий и тантал, металлов, таких как молибден и вольфрам, а также реактивных металлов, таких как цирконий и гафний.
Уровни потребления ресурсов имеющихся на сегодняшний день технологий приведены в Приложении В.
3.2.2.1 Выбросы в атмосферу
Согласно необходимому сырью и используемым операциям, например, дробление, сушка, плавка, разделение металлов и шлаков, прокаливание, восстановление водорода, цементация и обработка продукта, одним из наиболее важных источников воздействия на окружающую среду являются выбросы пыли и дыма. Выбросы пыли как в трубу или в виде неорганизованных утечек являются важными, поскольку вредные металлические соединения, такие как марганец и кобальт, могут быть частью пыли. Выгрузка и хранение сырья могут привести к образованию пыли, когда материал подается из различных источников, таких как барабаны, пластиковые пакеты или гибкие промежуточные контейнеры (FIBC), в бункеры. Пыль и дым, которые образуются при плавке или плавлении, например, титана, или при производстве порошка, собираются напыльниками и переносятся в систему пылеулавливания (например, тканевым фильтром или скруббером). Выбросы через трубу, как правило, контролируются постоянно или периодически на местах или консультантами за пределами площадки и сообщаются компетентным органам.
3.2.2.2 Сбросы в водные объекты
Для производства тугоплавких металлов сбросы в воду очень зависят от процесса и системы борьбы с загрязнением, а также от типа используемой очистки сточных вод. Существуют различные системы водоподготовки и очистки сточных вод. На некоторых заводах используется центральная станция очистки сточных вод, в которой вода из разных производственных процессов, а также поверхностная сточная вода будут очищаться вместе. В других установках используется отдельная система очистки дождевой воды и специальных процессов обработки для различных потоков сточных вод. Основными загрязнителями воды являются взвешенные твердые вещества и соединения металлов. Сточные воды обрабатывают для удаления растворенных металлов и твердых веществ и рециркулируют или повторно используют в максимально возможной степени в процессе. Возможные потоки сточных вод:
- поверхностные стоки и дренажные воды;
- сточные воды из мокрых скрубберов;
- сточные воды из шлаков и металлического гранулирования;
- охлаждающая вода.
Загрязненную воду обычно ведут к загустителю или отстойному водоему для осаждения взвешенных твердых частиц.
Стадии осаждения часто используются для удаления металлических соединений из воды. Взвешенные твердые вещества в основном состоят из очень мелких частиц, поэтому может потребоваться добавить флокулянт для облегчения осаждения в загустителях. После обработки в загустителе или отстойном водоеме взвешенные твердые вещества обычно ниже 20 мг/л, что позволяет повторно использовать в скрубберах, в качестве охлаждающей воды или в качестве технологической воды для других целей.
3.2.2.3 Сводные данные о выбросах/сбросах производства тугоплавких металлов
Принимая во внимание различные процессы, используемые при производстве тугоплавких металлов, в следующей таблице дается обзор экологических данных по выбросам в атмосферу, воду и землю. Различие между использованием первичного и вторичного сырья заключается в том, что вторичные тугоплавкие металлы могут быть напрямую использованы в производстве стали и сплавов, в том числе феррониобий (ванадий) без затрат на основное их производство.
Таблица 3.7
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Вольфрам | мг/нм3 | |||||
Первичные материалы | Пыль | Склад руды и пересыпка | < 10 | - Система охлаждения воды сконструирована как оборотная, и не контактирует с материалами. - Сбросная вода из скруббера контролируется на W и NH4 и при необходимости обрабатывается для снижения их концентрации | - Пыль, уловленная в системе пылеулавливания, возвращается в процесс. - Отходы от кристаллизации и сушки APT | - Выбросы пыли обычно ниже представленных ELV (20 мг/нм3, так как порошок вольфрама ценный материал. - Только доступные запыленности выбросов исключительно в диапазоне 1 - 3 мг/нм3. - Эти данные являются точными для производства вольфрамовых порошка и карбида. - Аммиачные соединения - очень пахнущая субстанция, что может стать проблемой |
Пыль | Кальцинация | 1 - 6 | ||||
Пыль | Восстановление водородом | < 5 | ||||
Пыль | Пыление | < 10 | ||||
Пыль | Продукт пересыпки | < 10 | ||||
Пыль | Неорганизованные выбросы при погрузке и выгрузке. Витание мелких частиц | |||||
NH3 | Неорганизованные дымы распада аммиачных продуктов от кальцинации | < 60 | ||||
H2 | Возможен риск воспламенения от водородных дымов | |||||
Вторичные материалы | Пыль | Аналогично как для первичных материалов | < 10 | Система охлаждения воды сконструирована как оборотная, и не контактирует с материалами | Кобальт обычно добавляют к твердой металлосодержащей пыли | |
Zn | Дымы цинка из процессов дистилляции | n.a. | ||||
Co | Дымы кобальта из процессов дистилляции (CO-часть металлоскрапа) | < 1 | ||||
Таблица 3.8
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Ванадий | мг/нм3 | |||||
Первичные материалы | Пыль | От приготовления шихты, например, измельчение | < 10 | Нет доступной информации по образованию сбросной воды | - Пыль, уловленная в системе пылеулавливания. - Хвосты выщелачивания. - Нет доступной информации по образованию отходов | - Порошок кальция, используемый как восстановитель должен складироваться очень осторожно, так как имеется высокая пожароопасность |
Пыль | От смешения солей щелочных металлов для обжига | < 3 | ||||
Ca | Остатки кальция могут выделяться при использовании порошка кальция как восстановителя | n.a. | ||||
Al | Остатки алюминия могут выделяться при использовании порошка кальция как восстановителя | n.a. | ||||
Вторичные материалы | Возможны различные выбросы от химических процессов в зависимости от исходных материалов и технологии. Данные недоступны. | Нет доступной информации по образованию сбросной воды | Нет доступной информации по образованию отходов | |||
Молибден | мг/нм3 | |||||
Первичные материалы | Пыль | От перегрузки и приготовления шихты на складе, очищенные в мешочном фильтре | < 10 | Нет доступной информации по образованию сбросной воды | Нет доступной информации по образованию отходов | Согласно международной классификации, триоксид молибдена (MoO3) классифицируется и как вредный (XN) |
Пыль | Неорганизованные дымы распада аммиачных продуктов от кальцинации | n.a. | ||||
Mo | Дымы | n.a. | ||||
H2 | Возможные риски возгорания от водородных дымов | |||||
Вторичные материалы | Возможны различные выбросы от химических процессов в зависимости от исходных материалов и технологии. Данные недоступны | Нет доступной информации по образованию сбросной воды | Нет доступной информации по образованию отходов | |||
Таблица 3.9
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Титан | мг/нм3 | |||||
Первичные материалы | Пыль | < 10 | - Жидкие стоки образовываются в мокром скруббере. Эти стоки могут содержать HCl, TTC и NaOH. - Жидкие стоки появляются единожды при использовании охлаждающей воды через основание или при продувке закрытой системы охлаждающей воды реакционных резервуаров и тиглей в плавильных печах. - Моющая отходы вода. - Кислотное выщелачивание и промывка. - Очищающий сток хлорид титана | - Пыль, собираемая в системе пылеулавливания. - Пыль содержит титан, диоксид титана и оксид натрия. - Некоторые плавильные печные тигли охлаждаются жидким натрий-калиевым сплавом (NaK) и небольшим количеством окисленных этих материалов, образующихся в виде шлама. Шлам взаимодействует с водой, и образовавшаяся жидкость выгружается на завод по очистке стоков | - Частицы титана состоят из относительно грубых частиц, которые быстро оседают и представляют пожароопасность. - Частая очистка обеспечивает отсутствие накопления, и пыль обычно продают как побочный продукт. - TTC (тетрахлорид титана) | |
Пыль | Пыль, содержащая титановые включения, соль и, возможно, небольшие количества натрия образовывается при сливе расплава из реактора | |||||
Пыль | Неорганические выбросы | n.a. | ||||
Пары кислоты | Пары соляной, плавиковой и азотной кислоты | n.a. | ||||
TiOCl | Пары гидрозолей TTC в контакте с влажным воздухом образуют туман, содержащий диоксид титана, оксихлорид титана (TiOCl) | |||||
TTK | Аргон, используемый для создания инертной атмосферы в реакторе, захватывает следы TTC и натрия | |||||
TiO2 NaO | Дымы от очистки крышек реакторов, содержащие диоксид титана и оксид натрия | |||||
Cl | < 5 | |||||
Вторичные материалы | Выбросы сопоставимы с вышеприведенными выбросами в атмосферу | Сточные воды аналогичны, как и для первичных материалов | Отходы как для первичных материалов | |||
Таблица 3.10
Выбросы при производстве тантала
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Тантал | мг/нм3 | |||||
Первичные материалы | Пыль | Склад и перегрузка исходных материалов | < 10 | - Система охлаждающей воды для электронно-лучевой печи сконструирована как замкнутый цикл и не имеет контакта с материалами. - Информация не доступна об образовании других стоков. | - Пыль, собираемая в системе пылеулавливания рециркулирует в процесс. - Нет доступной информации об образовании других отходов | - Эти данные подходят для производства порошка тантала и его карбида. - Аммиачные соединения имеют сильный запах, который может создать проблему. - Некоторые материалы тантала имеют высокую радиоактивность. - HF (фтористый водород) высокотоксичен и легко абсорбируется на поверхности контакта |
Пыль | Кальцинация | < 5 | ||||
Пыль | Восстановление водородом | < 5 | ||||
Пыль | Карбонизация | < 5 | ||||
Пыль | Пыление | < 10 | ||||
Пыль | Продукты перегрузки (тонкая пыль) | < 10 | ||||
Пыль | Неорганизованные выбросы при загрузке и выгрузке печи. Витание мелких частиц | n.a. | ||||
NH3 | Трубные и/или неорганизованные аммиачные дымы от кальцинации | < 60 | ||||
HF | Водород-фтор | < 1 | ||||
H2 | Возможна пожароопасность от водородных дымов | |||||
Вторичные материалы | Пыль | Так же, как и при первичных материалах | - Система охлаждающей воды для электронно-лучевой печи сконструирована как замкнутый цикл и не имеет контакта с материалами. - Выщелачивание сплава тантала и промывка. - Выщелачивание шлама и промывка. - Кислотная мойка танталового порошка и промывка. - Выщелачивание конденсатора и промывка | - Пыль, собираемая в системе пылеулавливания рециркулирует в процесс - Нет доступной информации об образовании других отходов | - HF (фтористый водород) высокотоксичен и легко абсорбируется на поверхности контакта. - Склад перегрузка HF должны это учитывать. - Кобальт обычно добавляют в твердый металлический порошок | |
H2 | Возможна пожароопасность от водородных дымов | |||||
NH3 | Трубные и/или неорганизованные аммиачные дымы от кальцинации | < 60 | ||||
HF | Водород-фтор | < 1 | ||||
Следы металлов Co, MnO, Ni и Ag могут быть в скрапе тантала и могут быть удалены | Ni < 1 Co < 1 | |||||
Таблица 3.11
Выбросы при производстве ниобия
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Ниобий | мг/нм3 | |||||
Первичные материалы | Пыль | От всех источников, очищенных в мешочном фильтре | < 10 | Нет доступной информации об образовании стоков | - Пыль, собираемая в системе пылеулавливания. - Шлак от восстановления в вакуумной печи. - Известно, что пирохлор, который является значительным сырьевым ресурсом, может иметь высокий уровень радиоактивности и поэтому термический плавильный процесс потенциально экологически грязен с должным вниманием к удалению шлака. - Нет доступной информации об образовании отходов | - Ниобий и его соединения имеют очень низкую токсичность. - HF (плавиковая кислота) очень токсична и может легко абсорбироваться на контактной поверхности. - Следа и перегрузка HF должны выполняться расчетливо |
Пыль | < 5 | |||||
Пыль | От производства карбидов ниобия | < 5 | ||||
Пыль | Неорганизованные выбросы | n.a. | ||||
VOC | От жидкой экстракции | n.a. | ||||
NF | Выбросы NF | < 1 | ||||
HCl | < 10 | |||||
Al | Алюминиевые остатки могут быть отделены просеиванием порошка для использования как восстановитель | < 5 | ||||
Другие выбросы зависят от исходного сырья и процесса. Дополнительные сведения недоступны. | ||||||
Вторичные материалы | Пыль | От всех источников, очищенных в мешочном фильтре | < 10 | Нет доступной информации об образовании стоков | Нет доступной информации об образовании отходов | - HF (фтористый водород) высокотоксичен и легко абсорбируется на поверхности контакта. - Склад перегрузка HF должны это учитывать. - Кобальт обычно добавляют в твердый металлический порошок |
HF | Выбросы HF при копании | < 1 | ||||
Другие выбросы зависят от исходного сырья и процесса. Дополнительные сведения недоступны | - HF (фтористый водород) высокотоксичен и легко абсорбируется на поверхности контакта. - Склад, перегрузка HF должны это учитывать | |||||
Таблица 3.12
Выбросы при производстве рения, циркония и гафния
Тугоплавкие металлы | Выбросы в атмосферу | Сброс в воду | Образование, рециклинг или повторная переработка отходов | Примечание | ||
Рений | мг/нм3 | |||||
Первичные материалы | Пыль | От всех источников, очищенных в мешочном фильтре | < 10 | - Формирование стоков. - Нет доступной информации об образовании стоков | Пыль, собираемая в системе пылеулавливания | - Рений и его соединения имеют очень низкий уровень токсичности |
Пыль | < 5 | |||||
Пыль | Неорганизованные выбросы | n.a. | ||||
Другие выбросы зависят от исходного сырья и процесса. Дополнительные сведения недоступны. | ||||||
Вторичные материалы | Выбросы зависят от использованного сырья и процесса. Данные недоступны. | - Нет доступной информации об образовании стоков | - Нет доступной информации об образовании отходов | - | ||
Цирконий и гафний | мг/нм3 | - | - | - | ||
Первичные материалы | Пыль | От всех источников, очищенных в мешочном фильтре | < 10 | - Нет доступной информации об образовании стоков | - Zr и Hf также ассоциируются с радиоактивными металлами (уран, полоний и торий), которые могут быть в остатке - Кислотное выщелачивание при производстве металлического циркония и сплав - Бросовая кислот - Нет доступной информации об образовании отходов | - Получение циркония имеет значительный экологический риск, связанный с его остаточной радиоактивностью от радиоактивных металлов (уран, полоний и торий), находящихся в тяжелом песке, который используется как сырье. Уровень радиации не публикуется |
Пыль | Неорганизованные выбросы | n.a. | ||||
F | Неорганизованные выбросы | n.a. | ||||
Радиоактивность от циркония | n.a. | |||||
Хлорирующий процесс для части циркониевого концентрата и возгонки тетрахлорида циркония требует строгих ограничительных процедур. Другие выбросы зависят от исходного сырья и процесса. Дополнительные сведения недоступны | ||||||
Вторичные материалы | Выбросы зависят от использованного сырья и процесса. Данные недоступны | - Нет доступной информации об образовании стоков | - Нет доступной информации об образовании стоков | - | ||
Таблица 3.13
AXIONIT DLE
Продукт | Выбросы в атмосферу | Сбросы в воду | ||
Загрязняющее вещество | Единицы измерения | Значение, не более | Загрязняющее вещество | |
Карбонат лития | Натрий гидроксид (натр едкий) | мг/нм3 | 0,4 | сбросы в поверхностный водный объект отсутствуют (рафинат закачивается в скважину) |
Хлорид лития | Натрий гидроксид (натр едкий) | мг/нм3 | 0,4 | сбросы в поверхностный водный объект отсутствуют (рафинат закачивается в скважину) |
Гидроксид лития | Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | 0,2 | сбросы в поверхностный водный объект отсутствуют (рафинат закачивается в скважину) |
Натрий гидроксид (натр едкий) | мг/нм3 | 0,4 | ||
Хлор | мг/нм3 | 0,1 | ||
Термин "наилучшие доступные технологии" (НДТ) определен в Федеральном законе от 10 января 2002 г. N 7 ФЗ "Об охране окружающей среды" [1].
Под технологией в целом понимают совокупность методов обработки, изготовления, изменения состояния, свойств и формы сырья, материалов или полупродуктов, осуществляемых в процессе производства продукции. Здесь имеют в виду и собственно технологию, и способ, с помощью которого описываемый объект спроектирован, построен, эксплуатируется и выводится из эксплуатации. Это не только технология производства, но и различные технические и нетехнические методы повышения экологической результативности (экологический менеджмент, управленческие решения).
Под доступной понимают экономически целесообразную технологию, которая достигла уровня, позволяющего обеспечить ее внедрение в той отрасли цветной металлургии, которая отвечает за производство редких металлов, с учетом экономической и технической обоснованности, затрат и преимуществ; при этом технология должна быть реализована хотя бы на двух предприятиях отрасли.
Под наилучшей понимают технологию, обеспечивающую охрану окружающей среды и ресурсосбережение (ресурсы здесь - сырье, вода, энергия) в максимальной мере.
Порядок определения технологии в качестве НДТ определен постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458 "О порядке определения технологии в качестве наилучшей доступной технологии, а также разработки, актуализации и опубликования информационно-технических справочников по наилучшим доступным технологиям" [5], на основании которого Министерство промышленности и торговли Российской Федерации разработало Методические рекомендации по определению технологии в качестве наилучшей доступной технологии.
Согласно перечисленным документам при отнесении технологических процессов, технических способов и методов, оборудования к НДТ необходимо руководствоваться следующими критериями:
а) наименьший уровень негативного воздействия на окружающую среду в расчете на единицу времени или объем производимой продукции (товара), выполняемой работы, оказываемой услуги либо соответствие другим показателям воздействия на окружающую среду, предусмотренным международными договорами Российской Федерации; приоритетным, оказывающим наименьшие отрицательные воздействия на окружающую среду, рекомендовано считать воздействие от отходов, затем выбросов в воду и загрязнение почвы; воздействие от выбросов в воздух рекомендовано рассматривать как фактор, имеющий наибольший отрицательный эффект;
б) экономическая эффективность внедрения и эксплуатации; анализ экономической эффективности заключается в оценке затрат на внедрение и эксплуатацию технологии и выгоды от ее внедрения методом анализа затрат и выгод; в процессе оценки целесообразно разделять объекты на новые и действующие;
в) применение ресурсо- и энергосберегающих методов;
г) период внедрения;
д) промышленное внедрение технологических процессов, оборудования, технических способов, методов на двух и более объектах в Российской Федерации, оказывающих негативное воздействие на окружающую среду.
В качестве источников информации о применяемых на практике технологиях, относящихся к НДТ, использованы сведения, полученные в результате анкетирования предприятий отрасли, результаты научно-исследовательских работ, а также информация, полученная в ходе консультаций с профильными экспертами.
Наилучшие доступные технологии и методы, а также - в необходимых случаях - соответствующие им технологические показатели (значения концентрации выбросов) определены технической рабочей группой применительно к следующим основным процесса производства:
1) процессы подготовки сырья и его опробование: сушка, дробление, смешение, спекание и кальцинация;
2) процесс спекания и кальцинация, выщелачивание;
3) методы разделения;
4) гидрометаллургические технологии.
В настоящем разделе рассмотрены вопросы, касающиеся оценки затрат промышленных предприятий по производству редких металлов на реализацию отдельных природоохранных мероприятий, в том числе на приобретение, монтаж, наладку и эксплуатацию оборудования, которое обеспечивает сокращение эмиссий загрязняющих веществ в окружающую среду.
Приводимые данные получены из различных источников: от предприятий, поставщиков технологий и оборудования, консультантов. Использованы открытые данные, почерпнутые из сети Интернет, корпоративных докладов и отчетов, научно-технической литературы и др. Однако эта информация не является универсальной и не может быть использована для достоверной оценки необходимых будущих вложений каждого конкретного предприятия в технологии и оборудование, которые позволят сократить выбросы загрязняющих веществ в окружающую среду. Она отражает лишь примерный масштаб необходимых затрат для реализации природоохранных мероприятий.
Зачастую имеющиеся данные не позволяют дифференцировать затраты по отдельным их компонентам, т.е. разделить общую сумму на затраты, относящиеся к природоохранным мероприятиям, и на затраты, связанные с общей модернизацией производства и пусконаладочными работами. Таким образом, оценка фактического объема ресурсов, направленных на охрану окружающей среды, крайне затруднительна, поскольку природоохранные мероприятия, как правило, сопряжены с производственным процессом. Единственными "чистыми" затратами являются затраты и технологии, которые не имеют иных целей, кроме как уменьшение и предотвращение эмиссий загрязняющих веществ в окружающую среду.
Однако само по себе наличие более детальной информации не является однозначной гарантией применимости имеющихся сведений для оценки требуемых предприятиями вложений в технологии и оборудование природоохранного значения. Помимо масштаба предприятия и особенностей технологического процесса производства редких металлов, существенное влияние на потенциальные расходы оказывают и другие факторы:
- логистика и развитость транспортной инфраструктуры, оказывающие непосредственное воздействие на поставку материалов и продукции;
- прямые операционные издержки, связанные, например, с особенностями трудового законодательства и местного рынка труда, климатическими условиями, удаленностью отдельных цехов и участков, наличием и стоимостью энергии и инфраструктуры, специальными требованиями по охране окружающей среды;
- расходы, связанные со сбытом и доступом на рынок, на масштаб которого влияет также развитость транспортной инфраструктуры, климатические условия, структура рынка и ограничения, обусловленные выходом на новые рынки;
- принципиально важна для производства редких металлов конъюнктура рынка: стоимость сырья и используемых в производстве материалов, цена конечной продукции и ее динамика, объем спроса и возможности для расширения производства;
- индивидуальные особенности конкретного инвестиционного проекта: график и протяженность инвестиций во времени, условия поставки и различные сроки эксплуатации оборудования, доступность энергетической и иной инфраструктуры, процентная ставка и доступность кредитных ресурсов, корпоративная структура.
Указанные факторы свидетельствуют о том, что полные и достоверные экономические расчеты возможны только с учетом местных условий и ключевых параметров, влияющих на финансовые показатели предприятий.
В настоящее время в Российской Федерации немаловажную роль в оценке достоверности сведений о затратах предприятий оказывает высокая волатильность валютных и финансовых рынков. Поэтому необходима корректировка данных, так как годовая процентная ставка, расходы на ссудные выплаты, уровень инфляции и валютные курсы в текущий момент времени могут быть несопоставимы с условиями, в которых ранее предприятия осуществляли соответствующие вложения.
Необходимо принимать во внимание и тот факт, что затраты на модернизацию предприятия, с одной стороны, могут содержать значительный валютный вклад, связанный с приобретением, монтажом, наладкой и зачастую эксплуатацией природоохранного и иного оборудования (и технологий), который ввиду существенного изменения курса валют в рублевом эквиваленте значительно увеличивается. С другой стороны, рублевые затраты на строительство, приобретение работ и услуг на местном рынке, административные расходы подвержены инфляции. Все это важно учитывать при оценке будущих затрат на модернизацию предприятия и его экологическую результативность. Нельзя не считаться с тем, что строительство отдельных объектов затягивается на годы с момента выделения средств, инфляция влияет на заработную плату, растут административные расходы и стоимость материалов, следовательно, объем затрат увеличивается по сравнению с первоначально утвержденным.
Подытоживая вышесказанное, важно подчеркнуть, что фактические расходы на внедрение природоохранных мероприятий и технологий в производство редких металлов зависит от общей экономической ситуации, налогового режима, доступности финансовых ресурсов, наличия льгот и субсидий, конкретного предприятия и конкретного оборудования.
Ресурсы, которые предприятие может направить на модернизацию производства и реализацию природоохранных мероприятий, зависят в первую очередь от конъюнктуры рынка. На этом рынке отдельные предприятия не имеют возможности влиять на цену конечной продукции, чтобы хотя бы частично компенсировать затраты на внедрение эффективных технологий и реализацию природоохранных мероприятий. Они не могут также переложить часть своих издержек на поставщиков сырья за счет снижения ими цен на сырье.
Затраты на экологические мероприятия различного рода неизбежно приводят к увеличению эксплуатационных расходов, но, как правило, не дают такого повышения эффективности производственного процесса, которое может быть получено в результате внедрения мер, направленных на коренную модернизацию производственного процесса. Вместе с тем такой подход связан со значительными капитальными вложениями, остановкой производства и прочими негативными факторами.
Собственный экономический потенциал природоохранных мероприятий незначителен. Сюда можно отнести и внедрение малоотходных технологий, и производство побочной продукции, и полезное использование отходов, образующихся в основном производстве. К тому же производство побочных продуктов не имеет устойчивого спроса, потенциал выхода на внешние рынки практически бесперспективен с экономической точки зрения. Затраты же на такое производство неизбежны, поскольку существует необходимость поддержания оборудования в рабочем состоянии, выделения средств на материалы и энергию.
Таким образом, с точки зрения возмещения затрат наиболее целесообразны комплексные меры, предусматривающие экологическую модернизацию производства с перенастройкой производственного процесса в целом, оптимизацией отдельных его звеньев и расширением объемов производства.
В настоящем разделе рассматриваются вопросы, связанные с оценкой затрат промышленных предприятий редкометалльной подотрасли на реализацию отдельных природоохранных мероприятий, включая приобретение, монтаж, наладку и эксплуатацию оборудования, обеспечивающего сокращение эмиссий загрязняющих веществ в окружающую среду.
Данные, приведенные в настоящем разделе, получены из различных источников, в том числе от предприятий, поставщиков технологий и оборудования, консультантов. Кроме того, для оценки затрат могут использоваться результаты исследований и иная опубликованная информация (корпоративные доклады и отчеты, журналы, открытые источники в сети Интернет, материалы конференций и др.). Однако информация из упомянутых источников не является универсальной и не может быть использована для хоть сколько-нибудь достоверной оценки необходимых будущих вложений конкретного предприятия в оборудование и технологии в целях сокращения эмиссий загрязняющих веществ в окружающую среду, а отражает лишь примерный масштаб затрат, которые могут возникать при реализации отдельных природоохранных проектов.
Зачастую имеющиеся данные агрегированы и не позволяют однозначно определить ключевые компоненты затрат и, тем самым провести разграничение между затратами на природоохранные мероприятия и затратами, связанными с общей модернизацией производственного процесса и пусконаладочными работами. Единственными "чистыми" затратами природоохранного характера являются затраты на оборудование и технологии "на конце трубы", которые, как правило, не имеют иных целей, кроме уменьшения или предотвращения эмиссий загрязняющих веществ в окружающую среду. Учитывая, что наиболее результативные природоохранные мероприятия оказываются интегрированными в производственный процесс, оценка фактического объема ресурсов, направленных на охрану окружающей среды, представляется крайне затруднительной.
Кроме того, в силу высокой специфичности производственных объектов, само по себе наличие более детальной информации не всегда гарантирует применимость имеющихся данных для оценки требующихся вложений российских металлургических предприятий в технологии и оборудование природоохранного назначения. Помимо масштаба предприятия и особенностей производственного процесса, существенное влияние на потенциальные расходы, связанные с внедрением природоохранных методов и технологий, и оценку экологической результативности конкретного инвестиционного проекта оказывает целый ряд иных факторов, в том числе:
- логистика и развитость транспортной инфраструктуры, оказывающие прямое воздействие на затраты на поставку материалов и продукции;
- прямые операционные издержки, которые могут быть связаны с особенностями трудового законодательства и местного рынка труда, климатическими условиями, удаленностью отдельных цехов и подразделений, наличием (или стоимостью) энергии и инфраструктуры, специальными требованиями по охране окружающей среды;
- расходы, связанные со сбытом и доступом на рынок, влияние на масштаб которых также оказывают развитость транспортной инфраструктуры, климатические условия, структура рынка и ограничения, связанные с выходом на новые рынки;
- конъюнктура рынка, в том числе цена конечной продукции и ее динамика, стоимость сырья и иных используемых в производстве материалов, объем спроса и возможности для расширения производства;
- индивидуальные особенности конкретного инвестиционного проекта, в том числе график и протяженность инвестиций во времени, параметры поставки и различные сроки эксплуатации оборудования, доступность энергетической и иной инфраструктуры, процентная ставка и доступность кредитных ресурсов, корпоративная структура.
Приведенные выше факторы свидетельствуют, что получить надежные данные по расходам, связанным с внедрением природоохранных методов и технологий, которые могли бы быть использованы без опасности существенного искажения результатов, крайне затруднительно. Полные и достоверные экономические расчеты в любом случае будут возможны только с учетом всех местных условий и ключевых параметров, влияющих на финансовые результаты предприятия.
В российских условиях существенное влияние на достоверность и применимость сведений о затратах компаний отрасли производства РМ на природоохранные мероприятия оказывает высокая волатильность валютных и финансовых рынков. Вследствие этого необходима существенная корректировка имеющихся данных о затратах, поскольку годовая процентная ставка, расходы на ссудные выплаты, уровень инфляции и валютные курсы в текущем периоде окажутся несопоставимы с условиями, в которых компаниями ранее осуществлялись соответствующие вложения. Представленные в настоящем разделе сведения о прошлых инвестициях российских предприятий - производителей РМ в рублевом эквиваленте зачастую агрегированы и приводятся в виде общего объема вложений в модернизацию конкретного производства, приведшую в числе прочего к повышению его экологической результативности. Поэтому их непосредственное применение для прогнозирования будущих затрат во многих случаях может привести к получению недостоверных результатов и значительному занижению требуемого объема инвестиций.
Затраты на модернизацию предприятий, как правило, содержат значительный валютный компонент, связанный с приобретением, монтажом, наладкой и в некоторых случаях эксплуатацией импортного, в том числе природоохранного, оборудования/технологий, который в силу существенного изменения курсов валют в текущих условиях в рублевом эквиваленте может увеличиться почти кратно. В свою очередь, рублевый компонент, увязываемый со строительством, приобретением работ и услуг на местном рынке, административными расходами и т.д., подвергается воздействию инфляции, что также требует учета при оценке будущих затрат на модернизацию производства и повышение его экологической результативности. Это определяется рядом факторов. Например, многие природоохранные мероприятия связаны со строительством, которое может занимать годы с момента выделения средств в зависимости от размера предприятия и сложности технологических процессов; инфляция, воздействующая на заработную плату, административные расходы и стоимость материалов, может приводить к существенному увеличению объема необходимых затрат в сравнении с первоначально утвержденными.
Сообразный инфляции рост ключевой ставки Банка России и, как следствие, увеличение процентных ставок по розничным кредитам предприятиям обусловливают, по меньшей мере удлинение периода окупаемости инвестиционных проектов и тем самым влияют на оценку доступности вложений в природоохранные мероприятия, оборудование и технологии для конкретных производителей.
Описанные обстоятельства необходимо принимать во внимание при подготовке и принятии решений о реализации природоохранных мероприятий и внедрении методов и технологий, обеспечивающих сокращение эмиссий загрязняющих веществ в окружающую среду. Приведенные в настоящем разделе объемы затрат российских предприятий - производителей РМ позволяют получить лишь некоторое представление о потенциальных объемах требуемых инвестиций. Вместе с тем, фактические расходы, связанные с внедрением природоохранных технологий в производство, напрямую зависят от текущих условий, в том числе от общей экономической ситуации, налогового режима, доступности финансовых ресурсов, наличия льгот и субсидий, технических характеристик предприятия и конкретного оборудования.
Ресурсы, которые предприятия отрасли могут направить на модернизацию производств и реализацию природоохранных мероприятий, напрямую зависят от конъюнктуры рынка редких металлов, являющейся глобальным биржевым товаром. На таком рынке компании-производители редких металлов не обладают хоть сколько-нибудь существенной рыночной властью и не имеют возможности по отдельности воздействовать на цену конечной продукции, что позволило бы в той или иной степени переложить понесенные в связи с реализацией природоохранных мероприятий и внедрением экологически эффективных технологий затраты на потребителя. Также отсутствует и обратная возможность - перенесения части издержек на реализацию природоохранных мероприятий на поставщиков сырья за счет снижения последними цен на сырье - цены на концентраты.
Это означает, что возможности по компенсации любых существенных затрат, понесенных в связи с реализацией природоохранных мероприятий компаниями-производителями редких металлов, в значительной мере ограничены и преимущественно могут быть реализованы одним способом - за счет увеличения объемов производства.
Усовершенствования "на конце трубы", которые изначально могут казаться относительно более дешевыми и не требовать существенных временных затрат на реализацию, в большинстве случаев приводят к увеличению эксплуатационных расходов и не дают такого повышения эффективности производственного процесса, которое может быть получено в результате внедрения мер, интегрированных в технологический процесс производства продукции. Это также свидетельствует в пользу выбора проектов коренной модернизации производственного процесса при определении мер, направленных на сокращение эмиссий загрязняющих веществ в окружающую среду. Вместе с тем такой подход связан со значительными капитальными вложениями и иными потерями ввиду необходимости временной остановки производства и перестройки производственного процесса в целом, что обусловливает снижение привлекательности полномасштабной модернизации производства при неблагоприятной рыночной конъюнктуре.
Собственный экономический потенциал природоохранных мероприятий, таких как, например, внедрение малоотходных технологий, производство побочной продукции и/или полезное использование образующихся в основном производственном процессе отходов в российских условиях следует признать скорее незначительным. С одной стороны, природоохранные технологии во многих случаях характеризуются высокой энергоемкостью, а поддержание оборудования в функциональном состоянии требует регулярных затрат на расходные материалы и комплектующие и иных эксплуатационных затрат; в некоторых случаях при производстве побочной продукции, такой, например, как серная кислота, значительные издержки могут возникать и в связи с необходимостью хранения и транспортировки агрессивного вещества. С другой стороны, низкая емкость российских рынков не обеспечивает достаточного спроса для вывода побочных производств на экономически эффективный уровень и не сможет гарантировать устойчивое потребление продукции вновь вводимых производственных мощностей, а потенциал выхода на внешние рынки ограничен и малоперспективен с экономической точки зрения.
Таким образом, наибольшим потенциалом с точки зрения возмещения затрат, понесенных в связи с внедрением на предприятии новых природоохранных методов и технологий, обладают комплексные меры, увязывающие экологическую модернизацию производства с перенастройкой производственного процесса в целом, оптимизацией отдельных его звеньев и расширением объемов производства. В этом случае высокие начальные затраты на внедрение интегрированных в производственный процесс природоохранных мер и технологий могут быть в конечном счете возмещены за счет увеличения объемов производимой продукции, повышения эффективности и снижения удельных эксплуатационных расходов. Однако на практике обособление экологической составляющей в рамках таких встроенных в технологический процесс мероприятий на фоне других капитальных и эксплуатационных расходов представляет собой достаточно сложную задачу.
В свою очередь потенциал прямой монетизации природоохранных мероприятий во многом определяется наличием или отсутствием соответствующих рынков сбыта и, как правило, в отраслях тяжелой промышленности, в том числе в цветной металлургии и производстве редких металлов.
4.1.4.1 Инвестиционные затраты по переработке фосфогипса
В качестве примера приведены обоснование и затраты на создание производственного цикла переработки фосфогипса.
Фосфогипс - неизбежный крупнотоннажный отход производства минеральных удобрений, образующийся при переработке апатитового концентрата по сернокислотной технологии.
Разработана технология комплексной переработки фосфогипса, которая состоит из следующих технологических этапов:
1. очистка фосфогипса от остаточного содержания кислых солей (фосфатов, сульфатов и фторидов) и выделения РЗЭ методом кучного выщелачивания;
2. концентрирование РЗЭ на катионите;
3. экстракционное разделение РЗЭ с получением концентрата церия, оксидов лантана, неодима, а также концентратов легкой и средней группы.
Разработана безотходная комплексная технология переработки отвалов фосфогипса с попутным извлечением РЗМ, которая была проверена в лабораторных условиях на отвальном фосфогипсе ОАО "Гомельский химический завод" и на фосфогипсе, взятом из процесса производства экстракционной фосфорной кислоты ОАО "Воскресенские минеральные удобрения", в режиме полной циркуляции оборотной воды с получением опытных партий строительного (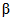 - полугидрата сульфата кальция), высокопрочного гипса (
- полугидрата сульфата кальция), высокопрочного гипса ( - полугидрата сульфата кальция) и редкоземельного концентрата.
- полугидрата сульфата кальция) и редкоземельного концентрата.
Сущность технологии:
1. Отмывка фосфогипса осуществляется разбавленным раствором серной кислоты с получением:
- отмытого фосфогипса;
- сернокислого раствора, содержащего примеси фосфора, фтора и РЗЭ.
2. Переработка сернокислого раствора производится с получением:
- РЗК товарной чистоты;
- пульпы гипса.
3. Переработка отмытого фосфогипса производится нейтрализацией известью с последующим получением гипсового вяжущего, а также изделий из него.
4. Переработка РЗК (в перспективе) производится с получением групповых концентратов РЗО, индивидуальных соединений РЗЭ и изделий на их основе.
Комплексная технология переработки фосфогипса не имеет отходов и может работать в автономном режиме.
Блок-схема комплексной технологии переработки фосфогипса с получением высокопрочного гипсового вяжущего изделий на его основе и РЗК приведена на рисунке 6.2.
По результатам лабораторных испытаний гипсовое вяжущее, полученное из отмытого и нейтрализованного фосфогипса, соответствовало по всем показателям требованиям ГОСТ 23789-79.
Настоящий раздел содержит перечень кратких описаний НДТ, применяемых при производстве редких, а также щелочноземельных металлов на различных этапах технологического процесса.
НДТ в рамках раздела сгруппированы в подразделы в соответствии с целями их применения, например, НДТ для повышения эффективности использования энергии, НДТ для предотвращения или снижения неорганизованных выбросов и др.
Технологии/методы, перечисленные и описанные в настоящем документе в качестве наилучших доступных технологий (НДТ), не являются ни предписывающими, ни исчерпывающими. Могут использоваться другие технологии/методы, которые гарантируют, по крайней мере, эквивалентный уровень охраны окружающей среды. При выборе НДТ необходимо обращать внимание на указанное конкретное производство (передел/установку), для которого должна применяться соответствующая НДТ. Также для каждой НДТ, где необходимо, указаны ограничения применимости. Если не указано иное, НДТ являются общеприменимы в рамках рассматриваемых видов деятельности.
Технологические показатели приняты в виде концентраций, что соответствует положениям нормативной правовой базы.
Наименования веществ приведены в соответствии с распоряжением Правительства РФ от 20.10.2023 N 2909-р "Об утверждении перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды и признании утратившими силу некоторых Постановлений Правительства РФ".
НДТ 1. Повышение общей результативности природоохранной деятельности. Внедрение и поддержание системы экологического менеджмента (СЭМ), соответствующей требованиям ГОСТ Р ИСО 14001 <1> или ISO 14001 <1>, а также поддержание в качестве составляющей СЭМ системы управления эксплуатацией, ориентированной на поддержание эффективности систем пылеподавления и пылеулавливания и разработка плана мероприятий по неорганизованным выбросам, предусматривающего, в том числе инвентаризацию наиболее характерных источников неорганизованных выбросов.
--------------------------------
<1> Соответствие системы менеджмента указанным стандартам не означает ее обязательную сертификацию.
НДТ 2. Повышение эффективности использования энергии: использование комбинации двух или более методов, приведенных в таблице 5.1.
Метод/оборудование | Применимость | |
а) | Система управления энергоэффективностью (например, в соответствии с требованиями международного стандарта ISO 50001) | Общеприменимо |
б) | Использование избыточного тепла (например, пара, горячей воды или горячего воздуха), образующегося при реализации основных процессов | Применяется для пирометаллургических процессов |
в) | Повышение температуры выщелачивающих растворов с использованием пара или горячей воды за счет избыточного тепла | Применяется для гидрометаллургических процессов |
г) | Подача на горелки воздуха, обогащенного кислородом, для уменьшения потребления энергии за счет автогенного процесса обжига и нагрева при спекании материалов | Применяется для печей, в которых используется сырье, содержащее серу или углерод |
д) | Низкотемпературная сушка концентратов и влажного сырья перед плавкой | Общеприменимо |
е) | Теплоизоляция объектов или оборудования, функционирующих при высоких температурах, например, трубопроводов пара и горячей воды, технологического оборудования | При необходимости |
ж) | Использование тепла, образующегося при производстве серной кислоты из диоксида серы, для предварительного нагрева газа, используемого на заводе серной кислоты, или для выработки пара и/или горячей воды | Применяется для заводов по производству цветных металлов, включающих производство серной кислоты или жидкого SO2 |
з) | Использование высокоэффективных электродвигателей, оборудованных частотными преобразователями, для таких устройств, как, например, вентиляторы | Общеприменимо |
и) | Системы контроля, которые автоматически активируют включение местных отсосов пыли или отходящих газов только при возникновении выбросов | |
к) | Использование автоматизированной информационно-измерительной системы учета энергоресурсов (АИИС УЭ) | Общеприменимо |
л) | Установка энергоэффективных электроосветительных приборов | Общеприменимо |
м) | Автоматизация установок приточной вентиляции | Общеприменимо |
НДТ 3. Обеспечение стабильности производственного процесса: внедрение системы автоматизированного контроля и использование комбинации двух или более методов, приведенных в таблице 5.2.
Метод/оборудование | Применимость | |
а) | Проверка и сортировка исходных материалов в соответствии с требованиями, определяемыми используемым технологическим оборудованием и применяемыми методами сокращения загрязнения | Общеприменимо |
б) | Тщательное перемешивание различных материалов, входящих в состав шихты для достижения оптимальной эффективности переработки и сокращения выбросов и отходов | |
в) | Системы взвешивания и дозирования шихты | |
г) | Использование микропроцессорных устройств для контроля скорости подачи материала, ключевых технологических параметров, включая сигнализацию, условий сжигания и подачи дополнительного газа | |
д) | Непрерывный инструментальный контроль температуры, давления в печи и подачи газа | |
е) | Контроль критических параметров процессов, реализуемых на установках очистки воздуха, таких как температура газа, количество подаваемых реагентов, падение давления, ток и напряжение на электрофильтре, объем подачи и pH жидкости в мокром скруббере, состав подаваемого газа (например, O2, CO, ЛОС) | |
ж) | Контроль содержания пыли в отходящих газах перед их подачей на завод серной кислоты | |
з) | Непрерывный инструментальный контроль уровня вибрации для обнаружения завалов и возможных отказов оборудования | Применяется для заводов, включающих производство серной кислоты или жидкого SO2 |
и) | Непрерывный инструментальный контроль силы тока, напряжения и температуры электрических контактов | Общеприменим (при необходимости) |
к) | Контроль и регулирование температуры для предотвращения образования выбросов металлов и оксидов металлов из-за перегрева | Применяются для процессов электролиза |
л) | Использование микропроцессорных устройств для контроля подачи реагентов и работы очистного оборудования, включая инструментальный контроль температуры, мутности, pH, электропроводности и объемов стока | Применяются для установок очистки сточных вод |
НДТ 4. Уменьшение неорганизованных выбросов, образующихся при хранении сырья, заключается в использовании комбинации двух или более методов, приведенных в таблице 5.3.
Метод/оборудование | Применимость | |
а) | Использование закрытых помещений или емкостей/бункеров | Применяется для пылящих материалов, таких как концентраты, флюсы и пульпа |
б) | Сооружение укрытий над площадками хранения | Применяется для непылящих материалов, таких как концентраты, флюсы, твердое топливо, крупнотоннажные насыпные материалы и кокс, а также вторичного сырья, содержащего растворимые в воде органические соединения |
в) | Герметичная упаковка или пылеподавление | Применяется для хранения пылящих материалов, а также вторичного сырья, содержащего растворимые в воде органические соединения |
г) | Сооружение укрытий над пролетами | Применяется при гранулировании/агломерации материала |
д) | Размещение устройств для улавливания пыли/газов в точках загрузки и перегрузки | Применяется в местах складирования пылящих материалов |
е) | Использование для сооружения емкостей строительных материалов, устойчивых к загружаемым материалам | Общеприменимо |
ж) | Применение надежных систем обнаружения утечек и индикации уровня заполнения емкостей с подачей сигналов для предотвращения их переполнения | Общеприменимо |
з) | Хранение концентрированной серной кислоты и других едких и вызывающих коррозию веществ в емкостях с двойными стенками или в емкостях, размещенных внутри устойчивого к воздействию агрессивных сред обвалования | Общеприменимо |
и) | Проектирование площадок для хранения таким образом, чтобы любые утечки опасных веществ из емкостей и систем доставки удерживались внутри обвалования, способного вместить объем жидкости, равный по крайней мере объему наибольшей емкости, размещенной внутри обвалования. Площадка для хранения должна быть обвалована и иметь покрытие, не подверженное значительному воздействию хранящегося агрессивного материала на обоснованный в проекте срок | Общеприменимо |
к) | Сбор и обработка эмиссий, образующихся при хранении, с помощью систем, предназначенных для обращения с химическими веществами, которые подлежат хранению. Вода, использованная для смыва пыли, также должна собираться и очищаться перед сбросом | Общеприменимо при хранении газов. При хранении жидкостей любые утечки должны собираться и обрабатываться |
л) | Регулярная уборка и, при необходимости, увлажнение площадки хранения | Общеприменимо |
м) | Хранение материалов там, где это возможно, в одном штабеле вместо нескольких | Применяется при складировании на открытом воздухе |
н) | Использование нефтеловушек и песколовушек в дренаже открытых площадок хранения. Использование для хранения материалов, которые могут содержать нефтепродукты (например, замасленной стружки), площадок с отбортовкой и противофильтрационными мероприятиями, препятствующими распространение опасных веществ в окружающую среду | Применяется при складировании на открытом воздухе |
НДТ 5. Уменьшение неорганизованных эмиссий, образующихся при обработке и транспортировке сырья. Использование комбинации двух или более методов, приведенных в таблице 5.4.
Метод/оборудование | Применимость | |
а) | Сооружение закрытых конвейеров или пневматических систем для транспортировки и обработки пылящих концентратов, флюсов и пульпы или использовать системы пылеподавления | Общеприменимо |
б) | Сооружение конвейеров для непылящих твердых материалов под навесами | |
в) | Установка устройств для сбора пыли в пунктах доставки, вентиляционных отверстиях, пневматических транспортных системах и точках перегрузки на конвейерах передачи и их подключение к системе газоочистки | Применяется при использовании пылящих материалов |
г) | Использование для обращения с измельченными или водорастворимыми материалами закрытых мешков или других видов тары | Общеприменимо |
д) | Использование специальных контейнеров для транспортировки уложенных на поддонах материалов | |
е) | Разбрызгивание воды для увлажнения материалов в местах их обработки | При необходимости и возможности осуществления |
ж) | Использование оптимальных маршрутов транспортировки | Общеприменимо |
з) | При возможности уменьшение высоты падения с конвейерных лент, механических лопат или захватов | |
и) | Регулировка скорости открытых ленточных конвейеров | Применяется при использовании открытых ленточных конвейеров |
к) | Минимизация скорости спуска или свободного падения материалов с высоты | Общеприменимо |
л) | Размещение передающих конвейеров и трубопроводов на безопасных открытых площадках выше уровня земной поверхности с целью оперативного обнаружения утечек и предупреждения повреждений транспортными средствами и другим оборудованием. Если для перемещения неопасных материалов используются подземные трубопроводы, местоположение их трасс должно быть документально зафиксировано и отмечено на местности соответствующими предупреждающими знаками; должны применяться системы безопасного ведения земляных работ | |
м) | Мойка колес и шасси транспортных средств, используемых для доставки или обработки пылящих материалов | Не применяется в условиях, которые могут привести к обледенению |
н) | Проведение плановых кампаний по уборке дорог | Общеприменимо |
о) | Разделение несовместимых материалов (например, окислителей и органических материалов) | |
п) | Минимизация материальных потоков между процессами | |
р) | Тара для транспортировки порошковых и сыпучих материалов должна изготавливаться из прочных материалов, обеспечивающих ее целостность при погрузочно-разгрузочных операциях | Общеприменимо |
НДТ 6. Предупреждение или сокращение неорганизованные выбросов: оптимизация параметров эффективности улавливания и очистки отходящих газов и использование комбинации двух или более методов, приведенных в таблице 5.5.
Метод/оборудование | Применимость | |
а) | Использование закрытых печей, оснащенных системами пылеулавливания, или оснащение печей и другого технологического оборудования вытяжными системами | Применение может быть ограничено соображениями безопасности (например, типом/конструкцией печи, наличием угрозы взрыва) |
б) | Оснащение печей и конверторов системами отведения газов в точках загрузки и выгрузки | Применение может быть ограничено соображениями безопасности (например, типом/конструкцией печи, наличием угрозы взрыва) |
в) | Сбор пыли и испарений в местах перегрузки пылящих материалов (например, в точках загрузки и выгрузки печей, на литейных лотках) | Общеприменим |
г) | Оптимизация конструкции и технологии эксплуатации вытяжных устройств и газоходов с целью улавливания газов, возникающих при загрузке шихты и отходящих от разогретого металла; выдача и перемещение расплавов сульфидов или шлаков по закрытым желобам | Для существующих заводов применение может быть ограничено имеющимся пространством и сложившейся планировкой размещения объектов в цехах |
д) | Сооружение укрытий печей/реакторов и другого технологического оборудования, например, с помощью местной аспирации, для улавливания выбросов при загрузочных операциях и выдаче расплавов | Для существующих заводов применение может быть ограничено имеющимся пространством и сложившейся планировкой размещения объектов в цехах |
е) | Использование систем, позволяющих подавать сырье небольшими порциями | Применяется только для полузакрытых печей |
ж) | Очистка улавливаемых отходящих газов с помощью систем, сконструированных с учетом особенностей их состава | Общеприменимо |
з) | Аспирационные системы надлежит блокировать с пусковыми устройствами технологического оборудования, исключающих его работу при отключенной вентиляции | Общеприменимо |
НДТ 7. Предотвращение или сокращение неорганизованных выбросов от подготовки и предварительной обработки материалов: использование одного из или комбинации методов, приведенных в таблице 5.6.
Метод/оборудование | Применимость | |
а) | Закрываемые конвейерная или пневматическая системы передачи для пылящего материала | Общеприменимо |
б) | Закрываемое оборудование. При использовании пылящих материалов выбросы собирают и направляют в систему газоочистки | Применяется только для подачи смесей, подготовленных с использованием системы, включающей бункер с дозатором или взвешиванием |
в) | Смешение сырья осуществляется в закрытом здании | Применяется только для пылящих материалов. Для существующих установок это может быть затруднено из-за недостаточного пространства |
НДТ 8. Предотвращение или уменьшение неорганизованных выбросов от загрузки сырья редких металлов до получения огарка или опека: использование одного или комбинации методов, приведенных в таблице 5.7.
Метод/оборудование | Применимость | |
а) | Герметичная система загрузки, такая как двойной колокол, закрытые конвейеры и питатель, оснащенные системой отвода газа | Общеприменимо |
б) | Изолированные или отгороженные печи с уплотнением подачи сырья | Уплотнительная дверь применима только для процессов с прерывистой подачей и выходом |
в) | Эксплуатация печи и газовые маршруты под разряжением и с достаточной скоростью отвода газа для предотвращения повышения давления | Общеприменимо |
г) | Уплотнение сочленений с газоходом и леткой при загрузке и выпуске металла | Общеприменимо |
д) | Полная герметизация с системой отвода газа | Применяется для новых заводов. При реконструкции действующих установок применение может быть затруднено из-за потребности в помещениях |
е) | Поддержание герметичности печи | Общеприменимо |
ж) | Поддержание температуры в печи на минимально необходимом уровне | Общеприменимо |
з) | Система газоотвода для загрузки и сочленения с системой фильтрации | Общеприменимо |
и) | Предварительная подготовка пылевидного сырья, например, гранулирование | Применяется только когда процесс и печь может использовать гранулированное сырье |
к) | Установка домика (укрытия для ковшей при выпуске) | Общеприменимо |
НДТ 11. Сокращение неорганизованных выбросов, образующихся при промывке, разделении твердых и жидких фракций и очистке, заключается в использовании одного из или комбинации методов, приведенных в таблице 5.8.
Метод/оборудование | Применимость | |
а) | Укрытие емкости крышкой | Общеприменимо |
б) | Укрытие впускных и выпускных лотков для технологической жидкости | Общеприменимо |
в) | Соединение емкостей с механической вытяжной централизованной системой газоочистки или с локальными системами для одной емкости | Общеприменимо |
НДТ 12. Использование в электролизерах добавок, особенно пенообразующих агентов, в целях уменьшения неорганизованных выбросов паров, образующихся при электроизвлечении.
5.2.2.1 Общие НДТ для производства редких металлов
НДТ 13. Предотвращение выбросов NO, NO2 от пирометаллургических процессов при производстве продукции, которая входит в область применения настоящего справочника НДТ: использование методов, приведенных в таблице 5.9.
Метод/оборудование | Применимость | |
а) | Горелки с низкими выбросами NOx | Общеприменимо |
б) | Кислородно-топливные горелки | Общеприменимо |
Таблица 5.10
Технологический показатель: выбросы NO, NO2
от пирометаллургических процессов
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
НДТ 14. Использование природного газа в качестве топлива при сушке сырья в сушильных башнях в потоке горячих топочных газов.
Таблица 5.11
Технологический показатель: выбросы NO, NO2 от использования
природного газа в качестве топлива при сушке сырья
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
НДТ 15. Сокращение выбросов в воздух пыли (взвешенных веществ) от подготовки сырья (например, прием, обработка, хранение, измерение, перемешивание, смешивание, сушка, измельчение, просеивание) в производстве продукции, которая входит в область применения настоящего справочника НДТ: использование одной или несколько газоочистных установок.
Таблица 5.12
Технологический показатель НДТ 15: выбросы взвешенных
веществ от процессов подготовки сырья
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 40 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
НДТ 16. Сокращение выбросов, образующихся при производстве оксидов металлов, которые входят в область применения данного справочника НДТ: использование одного из методов, приведенных в таблице 5.13.
Метод/оборудование | Применимость | |
а) | Мокрый скруббер | Общеприменим |
б) | Центробежная система | Общеприменим |
Таблица 5.14
Технологический показатель НДТ 16. Выбросы металлосодержащей
пыли, образующиеся при выщелачивании, очистке и электролизе
Параметр | Единица измерения | Средний уровень выбросов для НДТ |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 40 |
Таблица 5.15
Технологический показатель НДТ 16. Выбросы, образующиеся
при гидролизе
Параметр | Единица измерения | Средний уровень выбросов для НДТ |
Аммиак (азота гидрид) | мг/нм3 | <= 30 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 |
НДТ 17. Сокращение выбросов от загрузки, обжига, плавки и получения огарков и спеков в производстве продукции, которая входит в область применения настоящего справочника НДТ: использование одной или нескольких газоочистных установок.
Таблица 5.16
Технологические показатели НДТ 17: выбросы от процессов
загрузки, плавки и выпуска металла
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Аммиак (азота гидрид) | мг/нм3 | <= 100 |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 30 |
Серы диоксид | мг/нм3 | <= 60 |
НДТ 18. Сокращения выбросов при производстве концентратов (карбонатов) РЗМ. НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.17
Технологические показатели НДТ 18
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 30 |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) | мг/нм3 | <= 5 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 5 |
НДТ 19. Сокращение выбросов органических соединений в атмосферу из сушки исходного материала и процесса обжига, спекания и плавки при производстве продукции, которая входит в область применения настоящего справочника НДТ: использование одного из или комбинации методов, приведенных в таблице 5.18.
Метод/оборудование | Применимость | |
а) | Выбирать и подавать сырье в соответствии с печью и используемыми методами подавления выбросов | Общеприменимо |
б) | Оптимизировать условия сгорания для уменьшения выбросов органических соединений | Общеприменимо |
НДТ 20. Сокращение выбросов ПХДД/Ф и ЛОС в воздухе при комбинированных технологиях переработки нетрадиционного сырья редких и элементов: применение методов, приведенных в таблице 5.19.
Метод/оборудование | Применимость | |
а) | Выбор и подача сырья в соответствии с печью, использующей методы подавления выбросов | Общеприменимо |
б) | Системы загрузки сырья небольшими порциями | Применяется только для полузакрытых печей |
в) | Внутренняя система горелки | Применяется только для печей |
г) | Фор-камера или рекуператор | Общеприменимо |
д) | Избегать систем дымоотсоса с высокой запыленностью поверхности при температуре > 250 °C | Общеприменимо |
е) | Использование эффективной системы сбора пыли | Общеприменимо |
ж) | Использование инжекции кислорода в верхней зоне печи | Общеприменимо |
з) | Оптимизировать условия сгорания для подавления выбросов органических соединений | Общеприменимо |
5.2.2.2 Производство циркония и гафния
НДТ 21. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении фторцирконата, фторгафната калия в производстве циркония и гафния методом фторирования.
НДТ предусматривает использование одной или нескольких газоочистных установок различного типа (циклонов, скрубберов).
Таблица 5.20
Технологический показатель НДТ 21: выбросы взвешенных
веществ и газов при подготовке сырья (прием, обработка,
хранение, перемешивание, смешивание, сушка) при получении
фторцирконата, фторгафната калия в производстве
циркония и гафния
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Аммиак (азота гидрид) | мг/нм3 | <= 275 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 52 |
Фтористый водород, растворимые фториды (фториды неорганические хорошо растворимые): натрия фторид (натрий фтористый); натрия гексафторидсиликат | мг/нм3 | <= 235 |
Серы диоксид | мг/нм3 | <= 18 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 38 |
НДТ 22. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении технического тетрахлорида циркония в производстве циркония методом хлорирования.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.21
Технологический показатель НДТ 22: выбросы при подготовке
сырья (прием, обработка, хранение, перемешивание,
смешивание, сушка) при получении технического тетрахлорида
циркония в производстве циркония методом хлорирования
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлор | мг/нм3 | <= 365 |
Цирконий | мг/нм3 | <= 40 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 160 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) | мг/нм3 | <= 40 |
НДТ 23. Получение порошка циркония и гафния электролитическим методом фторирования (дробление катодного осадка, обработка в растворах углеаммонийных солей, флотация порошка, кислотная обработка раствором серной кислоты, сушка порошка) в производстве циркония и гафния.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.22
Технологический показатель НДТ 23: выбросы при получении
порошка циркония и гафния электролитического
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Аммиак (азота гидрид) | мг/нм3 | <= 275 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
НДТ 24. Разделение хлоридов циркония и гафния (солевая очистка, ректификация и отгонка, абсорбционная очистка) при получении тетрахлорида циркония очищенного в производстве циркония методом хлорирования, НДТ предусматривает использование одной или нескольких газоочистных установок различного типа (скрубберов).
Таблица 5.23
Технологический показатель НДТ 24: выбросы взвешенных
веществ и газов при подготовке сырья (прием, обработка,
хранение, перемешивание, смешивание, сушка) при получении
технического тетрахлорида циркония в производстве
циркония методом хлорирования
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Цирконий | мг/нм3 | <= 40 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 160 |
НДТ предусматривает использование герметичных электролизеров и использование одной или нескольких газоочистных установок.
Таблица 5.24
Технологический показатель НДТ 25: выбросы взвешенных
веществ от процесса электролиза расплава солей
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлор | мг/нм3 | <= 100,0 |
Фтористый водород, растворимые фториды (фториды неорганические хорошо растворимые): натрия фторид (натрий фтористый); натрия гексафторидсиликат | мг/нм3 | <= 190,0 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
НДТ 26. Восстановление циркония из тетрахлорида циркония магнийтермическим способом (конденсация, кристаллизация, спекание) при получении циркониевой губки в производстве циркония методом хлорирования.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.25
Технологический показатель НДТ 26: выбросы
при восстановлении циркония (конденсация, кристаллизация,
спекание) при получении циркониевой губки в производстве
циркония методом хлорирования
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Цирконий | мг/нм3 | <= 40 |
5.2.2.3 Производство кальция
НДТ 27. Применение извести (негашеной) для приготовления известкового молока, НДТ предусматривает содержание CaO в извести не менее 70%.
Таблица 5.26
Технологические показатели НДТ 27: выбросы взвешенных
веществ от процессов дробления, измельчения сырья (извести
негашеной) при приготовлении известкового молока
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 20 |
НДТ предусматривает использование двухступенчатого механического абсорбера.
Таблица 5.27
Технологические показатели НДТ 28: выбросы от абсорбции
примесей, газов, аэрозолей при получении порошка
хлористого кальция
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 230 |
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.28
Технологические показатели НДТ 29: выбросы при сушке
хлористого кальция в потоке топочных газов
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 180 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 240 |
НДТ 30. Электролиз расплава хлористого кальция для получения медно-кальциевого сплава, НДТ предусматривает использование двухступенчатого механического абсорбера.
Таблица 5.29
Технологические показатели НДТ 30: выбросы при электролизе
хлористого кальция
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 230 |
5.2.2.4 Производство титана
НДТ 31. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание) при получении титанового шлака.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.30
Технологический показатель НДТ 31: подготовка сырья
(прием, обработка, хранение, смешивание) при получении
титанового шлака
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
НДТ предусматривает использование трехступенчатой очистки газов (две ступени - циклонная очистка, третья ступень рукавный фильтр тонкой очистки).
Таблица 5.31
Технологический показатель НДТ 32: процесс плавки и выпуска
расплава титанового шлака
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 750 |
НДТ 33. Сокращение выбросов в процессе приготовления трехкомпонентной титансодержащей шихты (сушка материалов, дробление материалов, помол, перемешивание).
НДТ предусматривает использование одной или нескольких газоочистных установок (рукавные фильтры).
Таблица 5.32
Технологический показатель НДТ 33: процесс приготовления
трехкомпонентной титансодержащей шихты (сушка материалов,
дробление материалов, помол, перемешивание)
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
НДТ 34. Подготовка сырья (прием, обработка, хранение, хлорирование) при получении технического тетрахлорида титана в производстве титана губчатого магнийтермическим способом.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.33
Технологический показатель НДТ 34. Подготовка сырья
(прием, обработка, хранение, хлорирование) при получении
технического тетрахлорида титана в производстве титана
губчатого магнийтермическим способом
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлор | мг/нм3 | <= 276 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 395 |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 160 |
НДТ 35. Восстановление титана из тетрахлорида титана магнийтермическим способом (восстановление, дистилляция) при получении титановой губки в производстве титана губчатого магнийтермическим способом.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.34
Технологический показатель НДТ 35: выбросы
при восстановлении титана в производстве титана губчатого
магнийтермическим способом.
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 50 |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 10 |
НДТ 36. Подготовка шихтовых материалов (первичных и вторичных) для производства титановых сплавов (очистка в кислотном растворе, обезжиривание, дробеметная обработка, нагрев, измельчение, навешивание, прессование, сушка).
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.35
Технологические показатели НДТ 36: выбросы при подготовке
шихтовых материалов (первичных и вторичных) для производства
титановых сплавов
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 50 |
Серы диоксид | мг/нм3 | <= 60 |
Серная кислота (по молекуле H2SO4) | мг/нм3 | <= 50 |
НДТ 37. Производство титановых слитков (загрузка, плавление в вакуумных печах, выгрузка, охлаждение, шоопирование, обработка).
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.36
Технологические показатели НДТ 37: выбросы при производстве
титановых слитков
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
диАлюминий триоксид /в пересчете на алюминий/ | мг/нм3 | <= 50 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 |
НДТ 38. Производство титановых изделий и полуфабрикатов (нагрев, ковка, штамповка, отжиг, прокатка, прессование, правка, травление, механическая обработка, резка).
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.37
Технологические показатели НДТ 38: выбросы при производстве
титановых изделий и полуфабрикатов (нагрев, ковка,
штамповка, отжиг, прокатка, прессование, правка,
травление, механическая обработка, резка)
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 |
Минеральное масло (масло минеральное нефтяное): веретенное, машинное, цилиндровое и иные | мг/нм3 | <= 50 |
Серы диоксид | мг/нм3 | <= 60 |
Натрий гидроксид (натр едкий) | мг/нм3 | <= 50 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 50 |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 50 |
Серная кислота (по молекуле H2SO4) | мг/нм3 | <= 50 |
НДТ 39. Получение высокопроцентного ферротитана в индукционных печах (загрузка шихты, плавление, разливка, дробление).
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.38
Технологические показатели НДТ 39: выбросы при производстве
ферротитана
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 |
Серы диоксид | мг/нм3 | <= 60 |
5.2.2.5 Производство магния
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.39
Технологические показатели НДТ 40: выбросы при сушке
(обезвоживании) карналлита в потоке топочных газов
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 180 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 240 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 |
Серы диоксид | мг/нм3 | <= 30 |
Хлор | мг/нм3 | <= 20 |
НДТ 41. Хлорирование обезвоженного искусственного карналлита анодными газами для получения безводного очищенного искусственного карналлита.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.40
Технологические показатели НДТ 41: выбросы от абсорбции
примесей, газов, аэрозолей при получении очищенного
искусственного карналлита
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 300 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 230 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 |
НДТ предусматривает использование герметичных электролизеров и использование одной или нескольких газоочистных установок.
Таблица 5.41
Технологические показатели НДТ 42: выбросы при электролизе
искусственного карналлита
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 300 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 100 |
Таблица 5.42
Технологические показатели: выбросы при производстве магния
и магниевых сплавов
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 40 |
Серы диоксид | мг/нм3 | <= 170 |
Магний оксид (окись магния) | мг/нм3 | <= 5 |
Хлор | мг/нм3 | <= 10 |
5.2.2.6 Производство теллура
НДТ 44. Снижение содержания взвешенных веществ в выбросах при производстве теллура с использование одной или нескольких газоочистных установок.
Таблица 5.43
Технологические показатели НДТ 44: взвешенные вещества
в выбросах при производстве теллура
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
5.2.2.7 Производство ниобия и тантала, а также их соединений
НДТ 45. Хлорирование лопаритового концентрата и пекового кокса с получением технических пентахлоридов ниобия и тантала, пульпы тетрахлорида титана и плава хлоридов РЗМ.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.44
Технологические показатели НДТ 45: выбросы от абсорбции
примесей, газов, аэрозолей при получении технических
пентахлоридов ниобия и тантала
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 10 |
Хлор | мг/нм3 | <= 20 |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 170 |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 100 |
НДТ 46. Разделение технических пентахлоридов ниобия и тантала (ректификацией) с получением индивидуальных пентахлоридов ниобия и тантала.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.45
Технологические показатели НДТ 46: выбросы от
ректификационного разделения пентахлоридов ниобия и тантала
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 10 |
Хлор | мг/нм3 | <= 20 |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 170 |
НДТ 47. Сокращение выбросов в процессе подготовки шихты (сушка материалов, загрузка, перемешивание) и проведение восстановительной плавки ниобия и тантала из пентаоксида ниобия и тантала.
НДТ предусматривает использование одной или нескольких газоочистных установок.
Таблица 5.46
Технологические показатели НДТ 47: выбросы от подготовки
шихты и восстановительной плавки
Параметр | Единица измерений | Средний уровень выбросов для НДТ |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
НДТ 48. Предотвращение загрязнения почвы и грунтовых вод, дробления, просеивания и операций классификации: использование одного из или комбинации методов, приведенных в таблице 5.47.
Метод/оборудование | |
а) | Водонепроницаемая обвалованная площадка для емкостей, используемых при выщелачивании |
б) | Водонепроницаемая обвалованная площадка для емкостей, используемых при очистке |
в) | Система защитного обвалования цехов электролиза |
г) | Использование системы оборотного водоснабжения для охлаждения оборудования |
Д) | Использование кислотостойкой поверхности пола и системы для сбора кислотных проливов |
НДТ 49. Сокращение потребления воды и предотвращение образования сточных вод заключается в использовании одного из или комбинации методов, приведенных в таблице 5.48.
Метод/оборудование | Применимость | |
а) | Возврат стоков от процесса очистки/утечек жидкостей с обжиговой печи, сернокислотной установки, электролизеров и литейной на стадию выщелачивания | При отсутствии ограничений |
б) | Возврат стоков от процесса очистки/утечек жидкостей с этапов выщелачивания и очистки, от промывки фильтрационного кека и влажной газоочистки на этапы выщелачивания и/или очистки |
НДТ 50. Предотвращение образования сточных вод: использование одного из или комбинации методов, приведенных в таблице 5.49.
Метод/оборудование | Применимость | |
а) | Измерение объемов используемой и сбрасываемой воды | Общеприменимо |
б) | Возврат в технологический процесс воды, использованной для промывки (в том числе промывки анодов и катодов), и разлитой воды | Общеприменимо |
в) | Повторное использование слабых кислот из стоков, образующихся в мокрых электростатических фильтрах и мокрых скрубберах | Применяется в зависимости от содержания в сточных водах металлов и твердых веществ |
г) | Использование очищенных поверхностных стоков | Общеприменимо |
д) | Использование системы охлаждения с замкнутым контуром | Применение может быть ограничено технологическими соображениями, когда требуется низкая температура |
е) |  воды, проходящей через очистные сооружения воды, проходящей через очистные сооружения | Применяется в зависимости от содержания солей |
НДТ 51. Предотвращение загрязнения незагрязненных вод и сокращение сбросов загрязняющих веществ в водные объекты: отделение незагрязненных стоков от других сточных вод, которые требуют очистки.
Применимость НДТ 51: отделение незагрязненных ливневых стоков может быть неприменимо на существующих установках.
НДТ 52. Сокращение сбросов загрязняющих веществ со сточными водами: очистка сточных вод, образующихся при производстве редких и металлов с целью удаления металлов и сульфатов с использованием одного из или комбинации методов, приведенных в таблице 5.50.
Метод/оборудование | Применимость | |
а) | Химическое осаждение | Общеприменимо |
б) | Седиментация | |
в) | Фильтрация |
Таблица 5.51
Технологические показатели: средний уровень концентраций
загрязняющих веществ в прямых сбросах, образующихся при
производстве редких металлов, в принимающие водные объекты
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
Алюминий | мг/дм3 | <= 0,3 |
Никель | мг/дм3 | <= 0,3 |
Титан | мг/дм3 | <= 0,1 |
Цинк | мг/дм3 | <= 0,08 |
Хлорид-ион | мг/дм3 | <= 1800 |
Фторид-ион | мг/дм3 | <= 4,0 |
Нитрат-ион | мг/дм3 | <= 100,0 |
Сульфат-ион | мг/дм3 | <= 500,0 |
Нитрит-ион | мг/дм3 | <= 3,3 |
Взвешенные вещества | мг/дм3 | <= 30,0 |
В случае замкнутого цикла водооборота показатели не применяются | ||
В связи со спецификой производства магния из обогащенного карналлита приведен дополнительный перечень технологических показателей для производства данного вида продукции (таблица 5.52).
Таблица 5.52
концентраций загрязняющих веществ в прямых сбросах,
образующихся при производстве магния
из обогащенного карналлита
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
Магний | мг/дм3 | <= 140,0 |
Калий | мг/дм3 | <= 140,0 |
Кальций | мг/дм3 | <= 950,0 |
Натрий | мг/дм3 | <= 280,0 |
В случае замкнутого цикла водооборота показатели не применяются. | ||
Для предприятий, осуществляющих прием хозяйственно-бытовых стоков от сторонних организаций и не относящихся к области применения ИТС НДТ 10 "Очистка сточных вод с использованием централизованных систем водоотведения поселений, городских округов" дополнительный перечень веществ приведен в таблице 5.53.
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
БПК полн. | мг/дм3 | <= 4,0 |
АСПАВ (анионные синтетические поверхностно-активные вещества) | мг/дм3 | <= 0,1 |
Фосфат-ион | мг/дм3 | <= 1,0 |
Хлорат-ион | мг/дм3 | <= 1,0 |
ХПК | мг/дм3 | <= 40,0 |
В случае замкнутого цикла водооборота показатели не применяются | ||
НДТ 53. Предотвращение образования сточных вод при щелочном выщелачивании: повторное использование воды от кристаллизации раствора соли щелочного металла.
НДТ 54. Сокращение количества отходов, направляемых на захоронение от производства продукции, которая входит в область применения настоящего справочника НДТ: организация операций на месте, с целью упрощения повторного использования остатков или, если это невозможно, их направление на рециклинг с использованием одного из или комбинации методов, приведенных в таблице 5.54.
Метод/оборудование | Применимость | |
а) | Переработка остатков и отходов в специальных установках для получения материалов | |
б) | Обработка остатков и отходов для использования в других областях | Общеприменимо |
в) | Вторичное использование пыли из системы удаления пыли в процессе производства обжига, спекания | Общеприменимо |
г) | Повторное использование пыли, образующейся при хранении и подаче концентрата | Общеприменимо |
д) | Восстановление Se и Te от влажной или сухой очистки газов из пыли/шлама | Применимость может быть ограничена количеством присутствующей ртути |
е) | Восстановление металлов из шлама очистки сточных вод | Прямая переплавка шлама от установки очистки сточных вод может быть ограничена наличием нежелательных в плавке элементов, таких как As, Cd и Tl |
ж) | Использование титансодержащих отходов в рудно-термической плавке титанового концентрата в качестве добавки | Общеприменимо |
з) | Переработка остатков титановых сплавов (разделка, сортировка, очистка, обезжиривание, измельчение, сепарация) для вовлечения в производство продукции |
НДТ 55. Повторное использование или восстановление серной кислоты, полученной от процесса обжига сульфидных концентратов: использование одного из или комбинации методов, приведенных в таблице 5.55.
Метод/оборудование | Применимость | |
а) | Повторное использование в качестве сырья на химическом заводе | Применимость может быть ограничена в зависимости от наличия местного химического завода |
б) | Производство гипса | Используется, только если примеси, присутствующие в регенерации кислоты, не оказывают влияния на качество гипса, или гипс более низкого качества может быть использован для других целей, таких как составляющая флюса |
в) | Производство сульфата натрия | Применяется только для процесса выщелачивания |
НДТ 56. Обработка отходов выщелачивания с целью обеспечения их пригодности для конечной утилизации: их пирометаллургическая обработка в вельц-печи.
Применимость: применимо только для отходов выщелачивания нейтральным растворителем с незначительным содержанием феррита цинка и/или драгоценных металлов в невысокой концентрации.
НДТ предусматривает использование рукавного фильтра.
Таблица 5.56
Технологический показатель НДТ 57. Выбросы, образующиеся
при гранулировании и переработке пылевидного сырья
Параметр | Единица измерения | Средний уровень выбросов для НДТ |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 50 |
Применимость: применимо только для потоков в технологии DLE (бедный элюат, пермеат на десорбцию, грязный элюат, рафинат на сорбцию)
Одним из наиболее перспективных методов переработки сырьевых источников и получения чистых металлов является фторидная технология.
Важное место занимает создание рентабельного способа переработки ильменитовых, лопаритовых, танталит-колумбитовых, вольфрамсодержащих и молибденитовых концентратов с комплексным извлечением редких металлов, и их высокочистых соединений - оксидов, нитридов и карбидов.
Особое внимание следует уделить разработке фторидного способа вскрытия оксидных и сульфидных концентратов, способов разделения и электролитической переработки безводных фторидов титана, ниобия, тантала, молибдена, вольфрама, рения, редкоземельных элементов, кремния и бора с выделением элементного фтора, направляемого в качестве основного реагента в процесс фторирования исходных концентратов.
В качестве сырьевых источников могут быть выбраны титансодержащие шлаки восстановительной плавки ильменитовых концентратов Иршанского и Верхнеднепровского месторождений (Украина), лопаритовые концентраты Ловозерского месторождения (Россия, Кольский полуостров), молибденитовые концентраты Сорского ГОК (Россия, Хакасия) и др. В Томской области (Россия) возобновился интерес к разработке Туганского месторождения комплексного полиметаллического сырья с созданием производства с целью выпуска ильменитовых и цирконовых концентратов.
При создании фторидного способа переработки полиметаллических концентратов:
- предложены одно- и двухстадийные способы фторирования полиметаллических концентратов;
- для разделения фторидов металлов с незначительной разностью температур их кипения и отделения инертных газов, а также фторидов примесей предложен способ их разделения по молекулярным массам с использованием каскада газовых центрифуг, которые широко используются в промышленном масштабе в атомной промышленности при разделении изотопов урана;
- для переработки безводных фторидов обоснован электролитический способ получения редких металлов и элементного фтора из расплава эвтектики фторидных солей.
Фторидный способ переработки минерального сырья с использованием в качестве основного реагента рециклируемого элементного фтора может быть использован в производстве высокочистых порошков металлов, их оксидов, нитридов и карбидов практически всех редкометалльных химических элементов, образующих летучие фториды.
Фторирование с использованием в качестве основного реагента рециклируемого элементного фтора, разделение фторидов редких металлов, летучих фторидов примесей и инертных газов по их молекулярным массам в каскаде газовых центрифуг, применение электролитического извлечения редких металлов и элементного фтора из безводных фторидов в низкоплавком расплаве фторидных солей являются новым направлением развития производства редких высокочистых металлов и новых конструкционных керамических материалов на основе их карбидов, нитридов, силицидов, боридов, карбосилицидов и композиционных материалов на основе этих соединений.
Фторидная технология заключается в смешивании исходного сырья в виде порошка с твердым фторирующим реагентом и обработке во фторопластовых реакторах со стальным кожухом закрытого типа при температурах 140 - 190 °C при избыточном давлении. При этом в качестве фторирующего агента используют смесь бифторида (гидродифторида) аммония (NH4HF2) и фтористоводородной кислоты в количестве, достаточном для полного поглощения выделяющегося аммиака.
Перспективным методом переработки эвдиалитового концентрата может являться его разложение минеральной (соляной или азотной) кислотой при ее расходе 90 - 110% от стехиометрического количества с последующей термической обработкой и водным выщелачиванием получаемого геля в автоклавных условиях при температуре 175 - 250 °C в течение 1 - 4 ч. При этом в раствор переходят редкоземельные элементы, а в нерастворимый остаток - соединения циркония, которые выделяют из остатка путем мокрого гравитационного сепарирования. Извлечение ZrO2 данным методом составляет более 71%.
Заслуживает внимания вариант технологии переработки эвдиалитового концентрата, предусматривающая совмещение процессов разложения с экстракцией циркония. ТБФ, насыщенный азотной кислотой, вводят на стадию разложения. Соотношение Т:Ж поддерживают 1:8 - 10 (Ж = О + В). Отношение водной и органической фаз при этом составляет 1:1 - 0,5. Степень извлечения циркония за счет перевода его в органическую фазу повышалась до 95 - 99%. Реэкстракцию циркония из органической фазы проводят слабым (3 - 4%) раствором азотной кислоты. В дальнейшем из растворов аммиаком осаждали гидратированный оксид циркония.
Фториды РЗЭ получают обезвоживанием гидратированных солей, осажденных из растворов или действием фтористого водорода на оксиды РЗЭ.
Фториды РЗЭ осаждают из азотнокислых или солянокислых растворов плавиковой кислотой. Некоторые РЗЭ (лантан, церий и др.) выделяются в виде полугидратов LnO3·0,5H2O, другие (празеодим, неодим) - без кристаллизационной воды. При нагревании раствора с осадком фторидов с помощью инфракрасной лампы гидратированные фториды превращаются в безводные. Отфильтрованные и промытые спиртом осадки затем сушат при 400 °C в атмосфере сухого аргона. Полученные этим способом фториды содержат примесь оксифторидов LnOF. Исключить их образование можно сушкой в токе HF. Более чистые фториды получают действием фтористого водорода на оксиды при 550 - 575 °C:
Ln2O3 + 6HF = 2LnF3 + 3H2O (6.1)
Фторирование таблеток оксидов проводят в трубе из никеля или сплава 70% Ni + 30% Cu, через которую навстречу потоку газа перемещаются лодочки с оксидами. Можно проводить фторирование оксидов в кипящем слое. Фториды, в отличие от хлоридов, малогигроскопичны, что облегчает работу с ними.
Также карбонаты, гидроксиды или активные оксиды РЗМ, полученные разложением оксалатов или карбонатов при температуре не выше 600 °C, гидрофторируют фтористым водородом при температуре 380 - 550 °C. Известен способ получения фторидов редкоземельных металлов взаимодействием с фтористоводородной кислотой или ее солями в кислой водной среде. Однако высокая коррозионная активность среды, содержащей плавиковую кислоту, создает значительные трудности при создании оборудования для получения фторидов редкоземельных элементов и требует применения дорогостоящих конструкционных материалов. Кроме того, фториды РЗМ, получаемые так называемым мокрым способом, содержат значительное количество оксофторидов, если их при сушке и прокалке не обрабатывать безводным фтористым водородом, при этом также увеличивается их себестоимость.
Разработан способ получения фторидов РЗМ и иттрия из их оксидов длительной обработкой (в течение 8 ч) газообразным фтористым водородом при 600 - 700 °C. Недостатком данного способа является значительная коррозия аппаратуры вследствие высокой температуры обработки оксидов, что приводит к загрязнению фторидов РЗМ и длительности процесса фторирования, требующего большого расхода фтористого водорода, и, следовательно, ухудшает экономические показатели процесса.
Сущность рассматриваемого способа получения фторидов РЗМ и иттрия заключается в том, что в качестве исходных материалов используют оксалаты, гидроксиды, карбонаты и оксиды РЗМ и иттрия, которые обрабатывают безводным фтористым водородом при температуре от 350 °C до 550 °C. Причем отличие от прототипа, позволяющее снизить температуру обработки оксидов фтористым водородом и ее длительность, заключается в том, что предварительная прокалка солей РЗМ и иттрия производится при температуре не более 600 °C, что делает возможным получение активных оксидов, из которых при вышеуказанных температурах удается получить фториды, не содержащие кислородсодержащие соединения.
Данный способ позволяет получить более чистые фториды редкоземельных металлов и иттрия при меньшем расходе HF и меньшей температуре фторирования, что значительно снижает коррозию оборудования.
Выполнен большой объем научно-исследовательских работ по фторированию ильменитовых шлаков и лопаритовых концентратов с получением нелетучих фторидов. Разработаны и проведены испытания по разделению летучих фторидов титана, ниобия и тантала, и технологии получения их из фторидов. В числе новых схем переработки сульфидных концентратов исследован процесс фторирования молибденитовых сульфидных концентратов. Значительные работы проведены по фторидной переработке оксидных концентратов редких металлов (рутиловые, танталит-колумбитовые, вольфрамитовые и шеелитовые). Фторидные технологии являются перспективными и во многих случаях готовыми для промышленной реализации.
В промышленной практике применяют пять методов обогащения литиевых руд: крупнокусковое обогащение, термическое обогащение (декрипитация), гравитационное и магнитное обогащение, флотация.
Нетрадиционными источниками литиевого сырья за рубежом рассматриваются гекторитовые глины, ядарит, геотермальные воды действующих электростанций, нефтепромысловые рассолы и морская вода.
Для переработки литиевых руд и концентратов традиционно используют четыре способа: сульфатный, известковый, хлорирующий обжиг и сернокислотный.
Хлорирующий обжиг был использован для переработки лепидолит и сподуменсодержащих концентратов. Обожженный при температуре 800 °C материал (лепидолит + NH4Cl + CaCO3) выщелачивали водой, из раствора при последующем упаривании кристаллизуется смесь хлоридов лития и кальция, которая может быть использована для электролиза или получения гидроксида лития методом каустификации. В промышленном масштабе способ был освоен в США для извлечения лития из сподуменового концентрата.
По гидрометаллургической технологии, названной процессом Sileach, тонкоизмельченный флюорит (CaF2) смешивают со слюдой и выщелачивают в серной кислоте при температуре 95 - 115 °C в течение 4 ч при атмосферном давлении. Процесс предусматривает регенерацию серной кислоты. В лабораторных тестах Sileach при проведении процесса в течение 4 ч извлечение лития из альфа-сподумена достигало 92%.
В настоящее время перспективной инновационной технологией является автоклавное выщелачивание сподуменовых концентратов, разработанная группой Metso Outotec. В мире в настоящее время строится около 10 химико-металлургических заводов, в том числе химико-металлургический завод ООО "Халмек Литиум" на территории Тульской области. Этот способ предусматривает получение карбоната лития в результате автоклавного выщелачивания этого минерала концентрированным раствором Na2CO3. Продуктами реакции являются карбонат лития и алюмосиликат натрия, которые под давлением обрабатываются двуокисью углерода для перевода Li2CO3 в растворимый LiHCO3. Раствор последнего после отделения от нерастворимого остатка алюмосиликатов декарбонизируют нагреванием с выделением Li2CO3 и возвращением в процесс CO2. Данная технология позволяет существенно сократить технологический процесс получения лития из сподуменовых концентратов: непосредственное щелочное (содовое) выщелачивание для экстракции лития и получения литийсодержащего раствора, из которого потом путем кристаллизации получают литиевый продукт. Кроме того, данный процесс выщелачивания является более безопасным для окружающей среды: в нем не используются кислоты или сульфаты, не образуются нежелательные соли и другие побочные продукты, отходы представляют собой химически инертные или нейтральные минеральные остатки, которые можно переработать или утилизировать.
Для извлечения ценных компонентов из рассолов предложены различные методы, из которых можно выделить следующие схемы: классическую галургическую схему переработки рассолов с многостадийной упаркой и смешанную, в которой используются осадительные методы, сорбция, экстракция и другие.
К наиболее простым для промышленного освоения относятся литиеносные рассолы хлоридного натриевого типа (оз. Сильвер-Пик, США), в которых содержание солей магния и кальция невелико. В мировой практике освоены технологии их переработки, основной принцип которых - предварительное концентрирование рассолов по литию в испарительных бассейнах до получения литиевого концентрата, пригодного для осаждения из него карбоната лития раствором соды.
Особое место в ряду исходного сырья для получения металлов (лития, рубидия, цезия, стронция, калия, магния), а также бора, брома и йода занимают рассолы хлоридного кальциево-магниевого типа (рапа Большого Соленого озера, США). Для рассолов хлоридно-магниевого типа характерны минимальные концентрации хлорида кальция (рассолы Китая).
Во всех случаях конечным продуктом будет соль лития. Наиболее распространенный конечный продукт - карбонат лития, который служит исходным материалом для получения других соединений, в частности, хлорида лития, из которого производится металлический литий. Одни из способов получения лития является металлотермическое восстановление его соли. Ниже приводим инновационную технологическую схему по получению металлического лития совмещенным процессом "диссоциация - восстановление" карбоната лития алюминием (см. рисунок 6.1).
1. Диссоциация карбоната лития:
- температура - от 700 °C до 740 °C;
- время синтеза - 3 - 3,5 ч;
- остаточное давление - 15 - 20 Па;
- контрвакуум печного пространства - нет.
2. Алюминотермическое восстановление оксида лития:
- температура - 940 - 950 °C;
- время восстановления - 2 - 2,5 ч;
- остаточное давление - 10 - 15 Па;
- контрвакуум печного пространства - 13,3 кПа.
3. Алюминотермическое восстановление смеси алюминатов лития:
- температура - 1200 - 1250 °C;
- время восстановления - 3 - 3,5 ч;
- остаточное давление - 1,3 - 10 Па;
- контрвакуум печного пространства - 10 кПа.
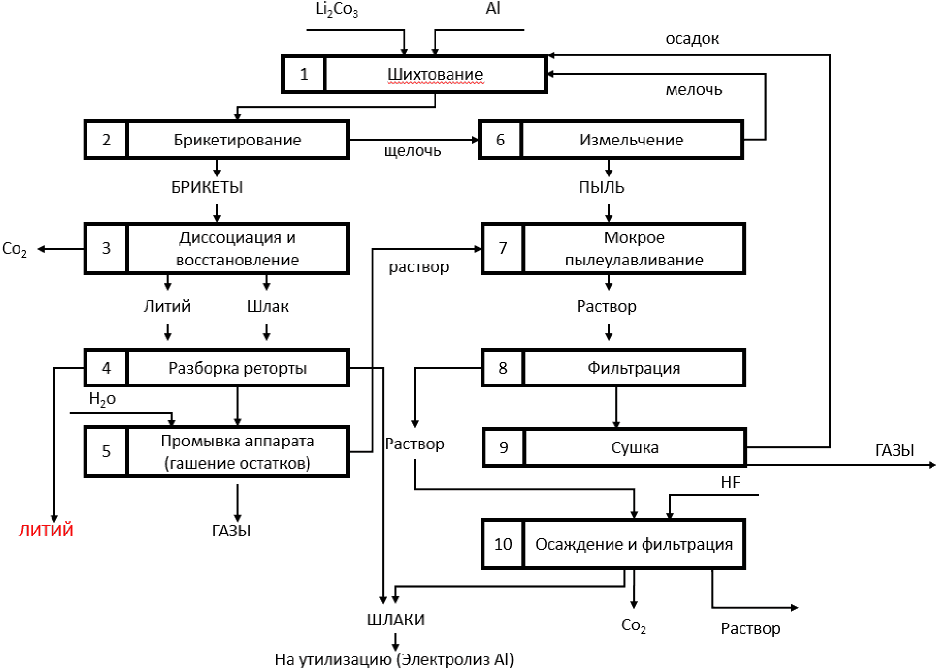
совмещенным процессом "диссоциация - восстановление"
карбоната лития
Для получения лития алюминотермическим восстановлением оксида лития в вакууме в качестве аппарата-аналога может быть применена вакуумная шахтная ретортная печь для дистилляции кальция из медно-кальциевого сплава.
6.3 Комбинированная сорбционно-экстракционная технология переработки суммарных концентратов РЗМ с получением высокочистых соединений (на примере легкой группы РЗМ)
Огромное разнообразие сырья РЗМ - природного и техногенного - определяет необходимость создания комбинированной схемы, основные элементы которой могли быть положены в основу локальных технологий. Была разработана промышленная технология современного уровня, которая позволит получать высокочистые индивидуальные соединения РЗМ из бедных руд и техногенных отходов и повысить экологический уровень предприятий. Основные приемы для достижения этой цели - максимальное использование экологически чистых сорбционных методов разделения и очистки РЗМ при рациональном применении экстракционных приемов разделения близких по свойствам металлов. При разработке промышленной технологии применительно к РЗМ-сырью в значительной степени учитывался весь огромный опыт урановой и золотодобывающей отраслей промышленности, включая как технологические, так и аппаратурные решения. Еще одним основанием для развития сорбционных процессов в сфере РЗМ являются блестящие достижения последних лет в области синтеза высокоселективных сорбентов мировыми разработчиками смол, в том числе ионитов с регулируемой на стадии синтеза пористостью, сорбентов, импрегнированных высокоселективными экстрагентами целевого назначения, хелатных и модифицированных смол. Расширение ассортимента смол позволяет существенно облегчить создание принципиально новой промышленной технологии с применением промышленно выпускаемых сорбентов.
Разработанная инновационная комбинированная сорбционно-экстракционная технология переработки любого вида сырья, содержащего РЗМ, с получением высокочистых (99,99%) соединений РЗМ легкой группы состоит из трех основных составляющих - головной сорбционной операции, экстракционного разделения внутри схемы и тонкой очистки от примесей на завершающих стадиях разработанной технологии. Головная операция - это использование сильнокислотного пористого сульфокатионита в голове процесса для отделения РЗМ от основных примесей. Новизна процесса состоит в том, что для десорбции суммы РЗМ с катионита Lewatit MonoPlus SP112 использован раствор четырехвалентного церия, что позволяет практически полностью вытеснить сумму РЗМ с ионита, но при этом поддерживать "сбросную" (менее 0,0005 г/л) концентрацию церия (IV) в растворе после колонны. Этот процесс фронтально-градиентного вытеснения РЗМ легкой группы из фазы смолы обеспечивает количественное отделение церия (IV) от остальных элементов. Сорбированный церий (IV) снимается с катионита раствором азотной кислоты в элюат, который подвергается экстракционной обработке, а реэкстракт направляется на получение соединения высокочистого церия путем тонкой очистки от примесей нередкоземельных металлов. В качестве экстрагента использован реагент из класса четвертичного аммониевого основания. Показано также, что применение вместо экстрагента Aliquat 336 сильноосновного анионита пористой структуры снижает показатели очистки, что обусловлено восстановительными свойствами углеводородной матрицы анионита.
Следующая технологическая новизна состоит в использовании комплексона типа трилон-Б для избирательного связывания суммы празеодима и неодима в комплексные соединения с последующим пропусканием водно-органической системы через слабокислотный катионит. Лантан при этом полностью сорбируется, а связанные в комплекс два металла проходят в фильтрат сорбции. Далее элюат лантана подвергается тонкой очистке от нередкоземельных металлов, а закомплексованные катионы празеодима и неодима после регенерации ЭДТА (этилендиаминтетрауксусной кислоты) подвергаются экстракционному, ставшему уже традиционным, процессу разделения. Реэкстракты этих двух металлов для получения высокочистых соединений также подвергаются тонкой очистке от примесей нередкоземельных металлов.
В конечном итоге третья технологическая новизна разработанного процесса получения высокочистых соединений РЗМ из любого сырья состоит в использовании для заключительной очистки импрегнированных и хелатных смол. Так, применение сорбента, импрегнированного экстрагентом бис-(2,4,4-триметилпентил) фосфиновой кислотой и маркированного как Lewatit TP272, для тонкой очистки от примесей индивидуальных элюатов и реэкстрактов РЗМ легкой группы позволило стабильно получать высокочистые соединения (99,99%) легкой группы. Эта технология прошла проверку в масштабе пилотных испытаний, в результате чего данные лабораторных исследований были полностью подтверждены в балансовых опытах. Разработанная технология получения высокочистых соединений РЗМ использует стандартное оборудование - сорбционные колонны ПИК с плотным слоем сорбента, реакторное оборудование и т.п. Причем процессы тонкой очистки проводятся в реакторном статическом варианте в аппаратах с перемешиванием ионообменных фаз и последующим отделением смол на сетках.
Таким образом, разработанная технология обладает элементами новизны и по сравнению с традиционной экстракционной схемой в ней повышена экологическая составляющая. Более того, предложенная схема эффективна как при переработке суммарных концентратов РЗМ с целью получения высокочистых соединений, так и для переработки техногенного сырья, в том числе с низким содержанием суммы РЗМ в этом сырье, например, для переработки отходов или промпродуктов, получаемых в производстве минеральных удобрений.
Золошлаковые отвалы (ЗШО) являются источником загрязнения окружающей среды, в то же время они содержат целый ряд ценных компонентов (германий, галлий, скандий, РЗМ).
Разработана технология извлечения скандия и редких земель из ЗШО методом кучного выщелачивания (КВ). Из-за низкого содержания ценных компонентов в исходном материале другие методы извлечения представляются априори нерентабельными, так как требуют больших затрат.
Основное отличие разработанного метода от традиционного КВ состоит в предварительной подготовке ЗШО к кучному выщелачиванию. Как известно, ЗШО - это дисперсный продукт, который в естественном виде непригоден для КВ из-за проблем плохой фильтрации и кольматации. Для извлечения РЗМ и скандия, и обеспечения дренажа штабеля ЗШО гранулировали с серной кислотой, которая выполняла функции связующего и вскрывающего реагента. В результате исследований получены прочные и устойчивые к разрушению гранулы, пригодные для дальнейшей переработки методом КВ. Редкие земли извлекали из продуктивных растворов КВ сорбцией в колонке на ионитах в динамическом режиме. Десорбцию ценных компонентов со смолы проводили в две стадии: растворами нитрата аммония для очистки от примесей и сульфата аммония для десорбции РЗЭ. Первичный концентрат редких земель осаждали из десорбатов щавелевой кислотой.
Определены оптимальные параметры процессов грануляции ЗШО, обеспечивающих получение гранул, пригодных для укладки в штабель и выщелачивания в режиме КВ, сорбции РЗМ на ионообменной смоле, десорбции и осаждения чернового концентрата. Извлечение РЗМ на стадии КВ составило 55%, на стадиях сорбции и десорбции - 90%. Извлечение скандия на стадиях сорбции и десорбции составило 99,6%.
На основании проведенных исследований в лабораторном и укрупненном масштабах совместно с МГТУ им. Н.Э. Баумана на Дорогобужской ТЭЦ создана опытная установка по переработке ЗШО.
Промышленно освоены две технологии переработки апатитового концентрата (АК) - сернокислотная и азотнокислотная. В зависимости от принятой технологии переработки, присутствующие в АК РЗМ концентрируются в азотно-фосфорнокислом растворе (АФР) или в фосфогипсе. По стандартной технологии переработки АК по азотнокислотной технологии АФР охлаждают, выделяют нитрат кальция кристаллизацией, аммонизируют, упаривают и направляют на получение удобрений. Большая часть РЗМ остается в составе удобрений. Для выделения РЗМ после вымораживания нитрата кальция и отделения фтора проводят селективное выделение гидратно-фосфатных осадков при pH = 1,1 - 2,0. Дальнейшая переработка гидрофосфатов проводится экстракцией из растворов, содержащих до 350 - 450 г/л нитрата аммония с использованием 100% ТБФ.
Анализ информационно-патентной литературы за последние 10 лет показал, что появились новые исследования по извлечению РЗМ из фосфогипса и комплексной переработке ФГ с получением гипсового вяжущего и концентрата РЗЭ. Все описанные технологии основаны на сочетании методов промывки фосфогипса растворами кислот или солей с последующим выделением РЗМ из промывного раствора или пульпы ФГ в виде концентрата методом осаждения подходящим реагентом, сорбции или экстракции. Все известные технологии технически осуществимы и имеют право на реализацию, однако экономически рентабельными будут только те, которые предусматривают комплексную переработку фосфогипса с получением не только РЗМ, но и гипсового вяжущего и изделий на его базе, имеющих высокую добавочную стоимость [33].
Основные технические решения, принятые при разработке технологии и создании производства комплексной переработки ФПГ
Для повышения степени извлечения РЗМ из ФПГ применен способ предварительной подготовки сырья переводом его в ФДГ, позволяющий повысить степень извлечения РЗМ до 65 - 70% при использовании растворов серной кислоты концентрации 30 - 40 г/л.
Дальнейшее извлечение РЗМ проводится в аппаратах колонного типа, работающих в режиме восходящей фильтрации растворов через псевдоожиженный слой сульфокатионита, ограниченный сверху фильтрующей перегородкой. Переключение колонн, работающих в режиме сорбции, с первой на вторую и далее происходит при достижении в ионите не менее 95% полной динамической обменной емкости (ПДОЕ), а в режиме десорбции - не более 0,05% от ПДОЕ. Маточники сорбции с концентрацией церия <= 0,05 г/л возвращают на промывку фосфогипса, а десорбции с концентрацией церия на выходе >= 0,25 г/л направляют на осаждение первичного концентрата (РЗК), а с церием <= 0,25 г/л - на десорбцию ионита в последующей колонне. Одновременно в режиме сорбции работают 3 - 4 колонны, а десорбции - 2 - 3. Маточник от осаждения РЗК нейтрализуют серной кислотой до pH 4,2 - 4,4 и возвращают на десорбцию.
Такое ведение процесса позволяет получать на первой стадии процесса концентрат РЗМ, содержащий менее 5% примесей при низких удельных расходах реагентов.
Дальнейшая переработка первичного концентрата с очисткой от примесей производится экстракцией из нитратных растворов с высаливателем с использованием экстрагента ТБФ в разбавителе в каскаде центробежных экстракторов.
Для дальнейшего разделения группового концентрата (ГРЗК) на индивидуальные РЗМ используют упаренный реэкстракт.
Технология проверена на лабораторной и опытно-промышленной автоматизированной установке полного производственного цикла в течение месяца непрерывной работы на отвальном и свежем (полугидратном) фосфогипсе с получением опытных партий ГРЗК. Производительность установки: по ФГ - 41 кг/ч или 400 кг/смену, по РЗО >= 1,0 кг/смену.
Удельные нормы расхода реагентов и электроэнергии на производство приведены в таблице 6.1, а технологическая блок-схема - на рисунке 6.2.
Таблица 6.1
или на 1 кг ГРЗК
Расходные материалы | Норма расхода | Цена | Сумма расходов | ||
кг/т ФГ | кг/кг РЗО | руб/кг | руб/т ФГ | руб/кг РЗО | |
Кислота серная | 66,16 | 21,92 | 6 | 396,94 | 131,5 |
Аммиачная вода 25% | 0,73 | 0,24 | 30 | 21,96 | 7,28 |
Карбонат аммония | 8,46 | 2,8 | 60 | 507,37 | 168,08 |
Ионообменная смола т/т | 0,004 | 0,001 | 150 | 0,63 | 0,21 |
Известь гашеная | 50,94 | 16,87 | 10 | 509,36 | 168,74 |
Кислота азотная 57% | 8,01 | 2,65 | 30 | 240,18 | 79,57 |
Трибутилфосфат (ТБФ) | 0,001 | 0,0002 | 900 | 0,6 | 0,2 |
Парафин нефтяной жидкий (C10 - C13) | 0,002 | 0,0006 | 200 | 0,34 | 0,11 |
Аммиачная селитра | 9,77 | 3,24 | 15 | 146,6 | 48,57 |
Газ природный, м3 | 33,99 | 11,26 | 8 | 271,91 | 90,08 |
Электроэнергия, кВт/ч | 24,89 | 8,25 | 7 | 174,26 | 57,73 |
Итого, руб. | 2270,15 | 752,07 | |||
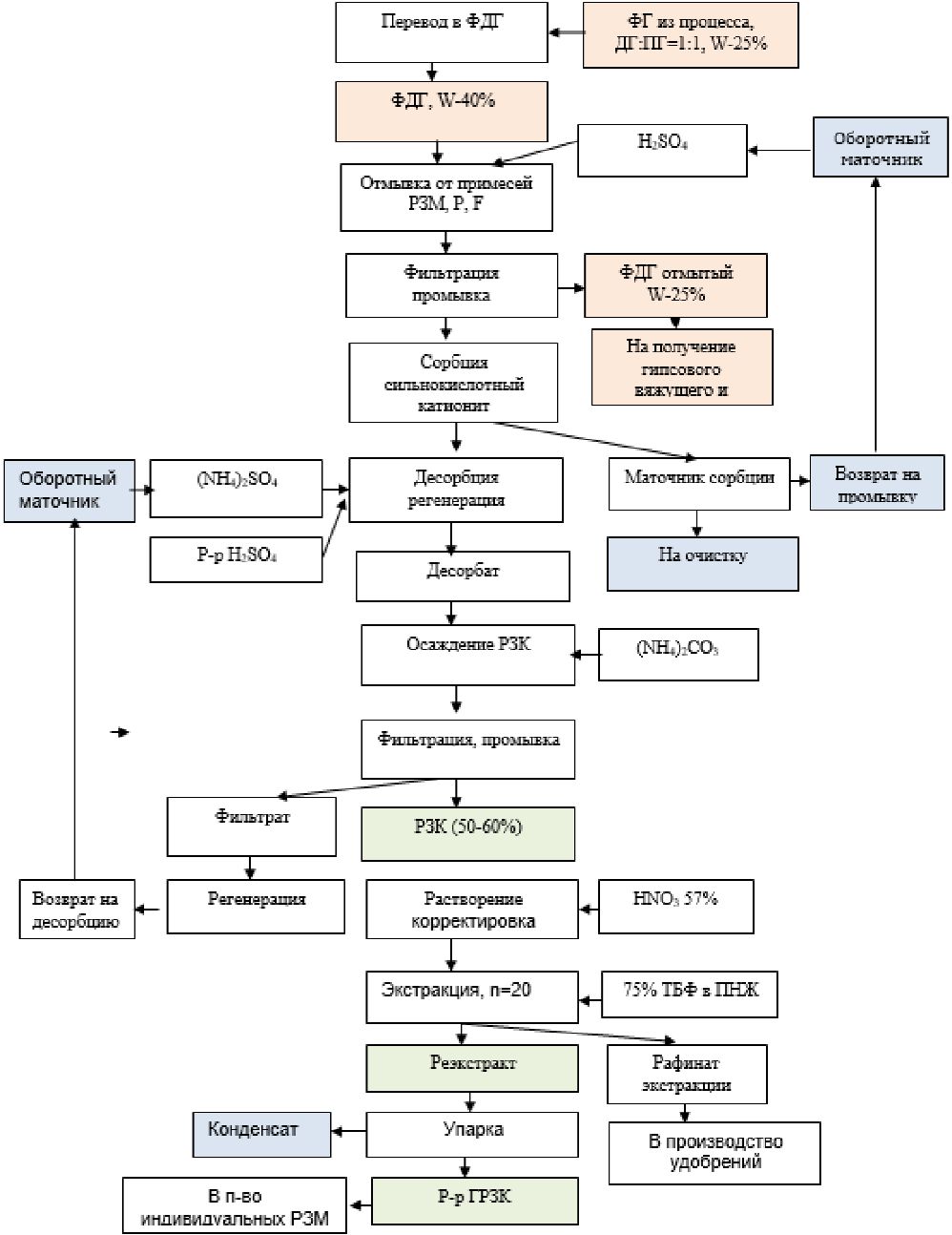
с получением ГРЗК и отмытого от примесей ФДГ
В разделе "Промышленные технологии разделения РЗЭ" приведена промышленная схема разделения ГРЗК при объеме переработки 150 т РЗО в год. Используемый для переработки ГРЗК не лимитируется по составу и может быть получен при переработки любого типа сырья с получением РЗМ-продукции заданного состава.
При увеличении объема переработки ГРЗК до 1000 - 2000 т РЗО в год схема разделения меняется: на первом этапе экстракционным разделением получают концентраты церия-лантана, дидима и СТГ. Из концентрата СТГ и дидима последовательно выделяют дидим и СТГ, а затем делят дидим с получением неодима и празеодима; из концентрата церия-лантана (сырье для производства мишметалла и катализатора крекинга нефти) - можно получать азотнокислые растворы лантана 3-х марок, лантан или церий, режим работы каскада выбирается расчетным путем [71]. Электрохимическому окислению подвергают только то количество церия, которое потребляют в России для производства специального стекла и катализаторов нефтехимии. Для разделения используется 7 каскадов экстракции, 472 ступени, экстрагент - 75% ТБФ в ПНЖ, 5 электролизеров конструкции Skycel-500 [83]. Блок-схема разделения приведена на рис. 6.3.
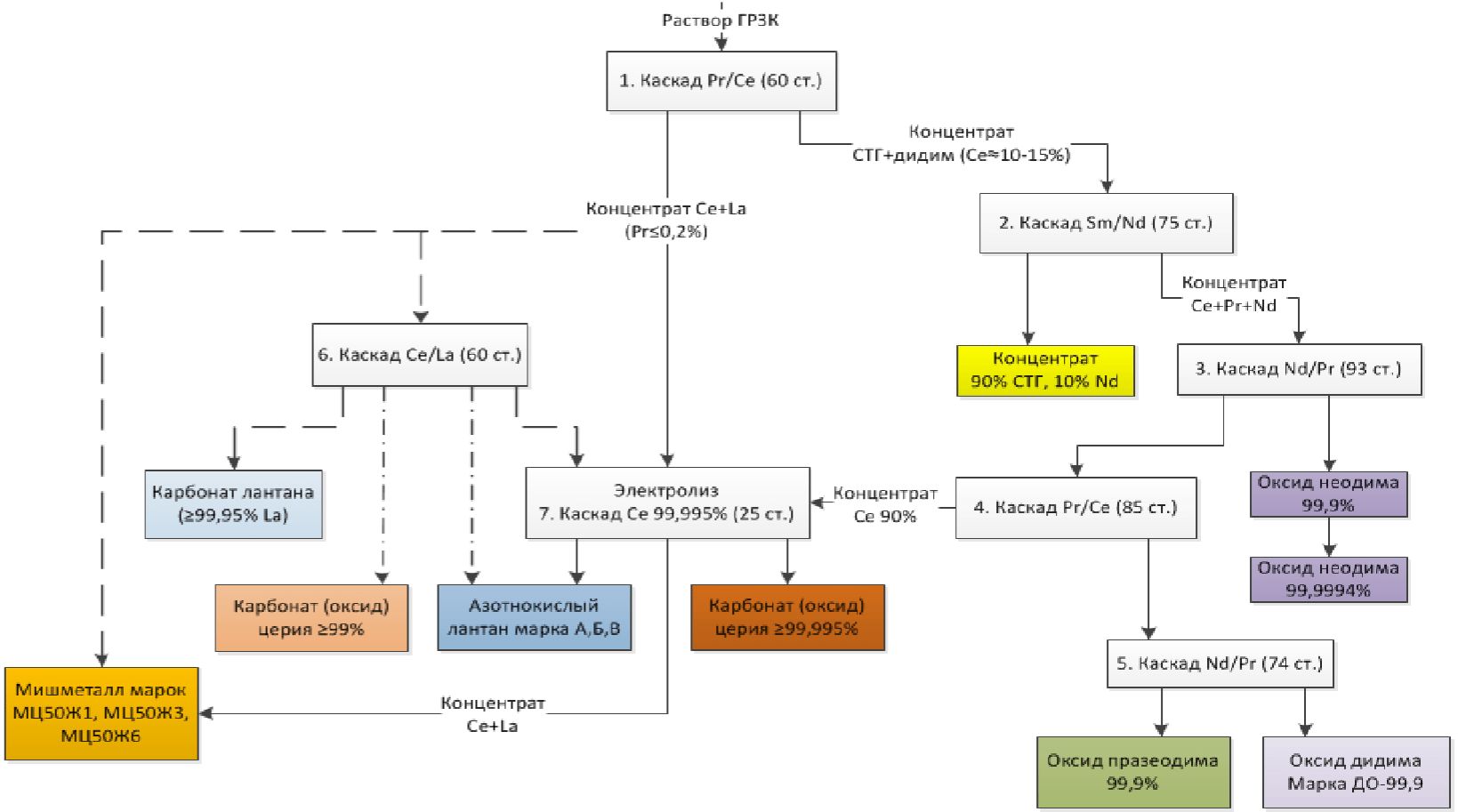
с получением РЗЭ легкой группы (лантана, церия, неодима,
празеодима) - вариант 2, экстрагент - 75% ТБФ в ПНЖ
Технология разделения смешанного концентрата СТГ, выделенного из апатитового и лопаритового концентрата в соотношении 1:1 с получением индивидуальных элементов реализована в двух вариантах.
В первом варианте процесс проводится в нитратной среде с использованием экстрагентов класса фосфорорганических кислот  и солей ЧАО в смеси с ТБФ с последовательным разделением по линиям Tb/Gd, Eu/Sm, Gd/Eu, Er/Y, Y/Ho, Ho/Dy и Dy/Tb с получением оксидов самария, европия, гадолиния, тербия, диспрозия и иттрия, а также концентратов тяжелой групп РЗМ (Er, Yb, Tm, Y и Ho, Y, Dy). Оксид европия из концентрата после разделения выделяют восстановлением цинком из хлоридной среды или экстракцией.
и солей ЧАО в смеси с ТБФ с последовательным разделением по линиям Tb/Gd, Eu/Sm, Gd/Eu, Er/Y, Y/Ho, Ho/Dy и Dy/Tb с получением оксидов самария, европия, гадолиния, тербия, диспрозия и иттрия, а также концентратов тяжелой групп РЗМ (Er, Yb, Tm, Y и Ho, Y, Dy). Оксид европия из концентрата после разделения выделяют восстановлением цинком из хлоридной среды или экстракцией.
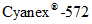 и солей ЧАО в смеси с ТБФ с последовательным разделением по линиям Tb/Gd, Eu/Sm, Gd/Eu, Er/Y, Y/Ho, Ho/Dy и Dy/Tb с получением оксидов самария, европия, гадолиния, тербия, диспрозия и иттрия, а также концентратов тяжелой групп РЗМ (Er, Yb, Tm, Y и Ho, Y, Dy). Оксид европия из концентрата после разделения выделяют восстановлением цинком из хлоридной среды или экстракцией.
и солей ЧАО в смеси с ТБФ с последовательным разделением по линиям Tb/Gd, Eu/Sm, Gd/Eu, Er/Y, Y/Ho, Ho/Dy и Dy/Tb с получением оксидов самария, европия, гадолиния, тербия, диспрозия и иттрия, а также концентратов тяжелой групп РЗМ (Er, Yb, Tm, Y и Ho, Y, Dy). Оксид европия из концентрата после разделения выделяют восстановлением цинком из хлоридной среды или экстракцией.Во втором варианте процесс проводится в хлоридной среде с использованием в качестве экстрагента фосфоновой кислоты P-507 и карбоновой кислоты в смеси с ТБФ в разбавителе по линиям Tb/Gd, Eu/Sm, Gd/Eu, Tb/Y, Ho/Dy, и Dy/Tb с получением оксидов самария, европия, гадолиния, тербия, диспрозия и иттрия, концентрата тяжелой группы. Оксид европия из концентрата выделяют электрохимическим восстановлением с последующим восстановлением цинком. Блок-схемы разделения для двух вариантов приведены на рис. 6.4 - 6.5.
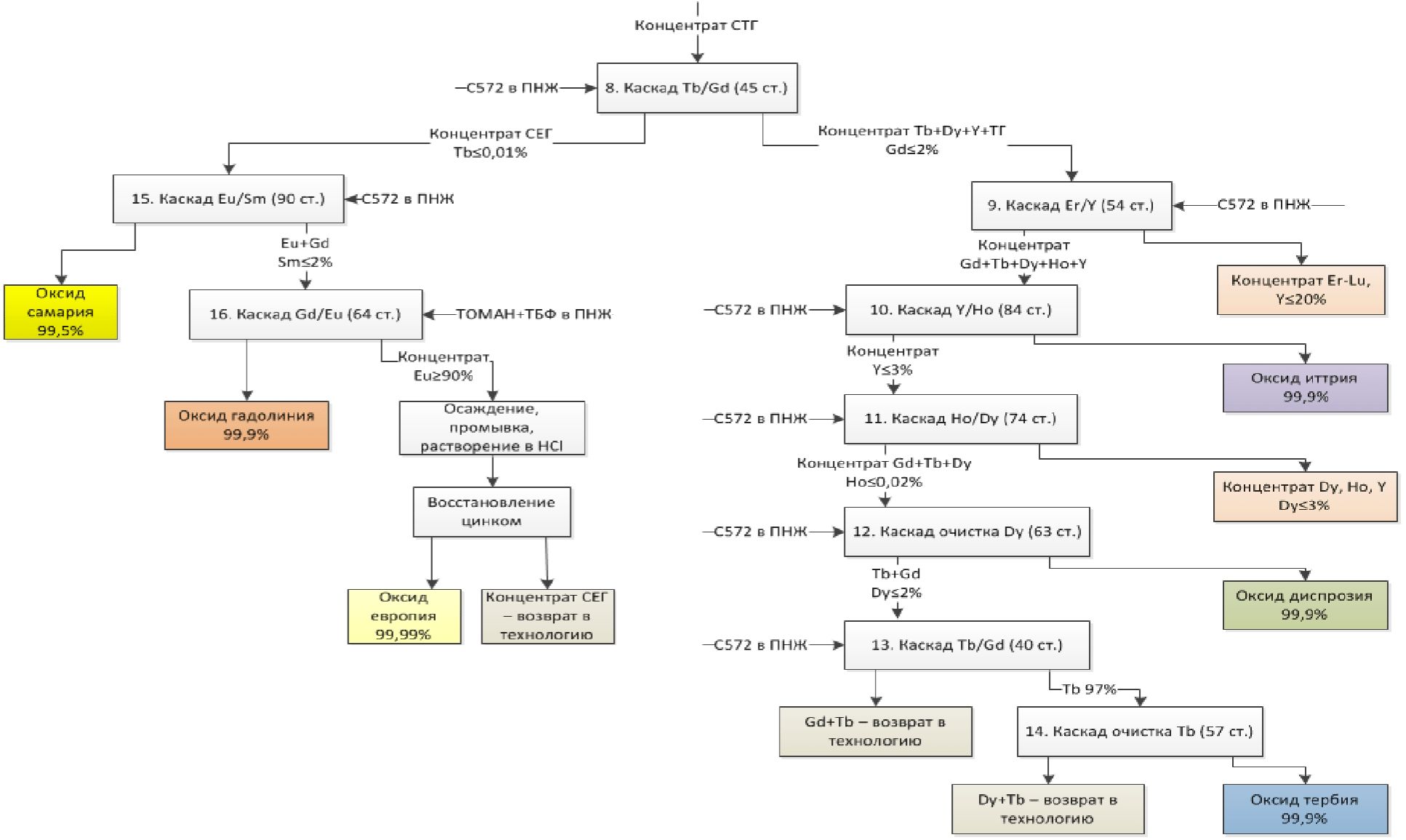
концентрата СТГ с получением самария, европия, гадолиния,
тербия, диспрозия и иттрия - вариант 1, всего 9 каскадов
разделения, ступеней 571
концентрата СТГ с получением самария, европия, гадолиния,
тербия, диспрозия и иттрия - вариант 2, всего 9 каскадов
разделения, ступеней 551
Гидроксиды редкоземельных и радиоактивных элементов (РЗЭ(OH)3, РЭ(OH)3, являются промежуточными продуктами при щелочной переработке монацита и ксенотима. Для дальнейшей переработки полученный гидроксидный кек, содержащий РЗЭ(OH)3 и РЭ(OH)3 растворяют в азотной или соляной кислоте. При нейтрализации полученных кислотных растворов накапливается большое количество растворов хлорида или нитрата натрия. И поэтому вопрос о сокращении большого количества отходов, а также уменьшение затрат на реагенты остается открытым.
В данном способе предложены кислоты, используемые для вскрытия гидроксидного кека, заменить хлоридом аммония (NH4Cl) и переводить его в водорастворимые хлориды твердофазным методом при нагревании. NH4Cl является нетоксичным, удобным и безопасным реагентом при хранении. При относительно низких температурах NH4Cl химически активен и позволяет осуществить процесс хлорирования во всем объеме реакционной массы, а его избыток может быть легко регенерирован и повторно использован.
Предварительно было изучено взаимодействие РЗЭ(OH)3 и РЭ(OH)3 с NH4Cl при нагревании. Для исследования взаимодействия La (OH)3 с NH4Cl применяли термогравиметрический анализ. Продукты взаимодействия определяли с использованием рентгенофазового анализа.
При нагревании смеси РЗЭ(OH)3 и NH4Cl на кривых ДТА имеются три эндотермических эффекта. Вне зависимости от соотношения компонентов всегда присутствует обратимый эффект полиморфного превращения NH4Cl, второй эндоэффект является результатом реакции хлорирования, а третий эндоэффект результатом разложения комплексных соединений с образованием безводных хлоридов РЗЭ. Соединения урана ведут себя подобно РЗЭ(OH)3, а соединение тория не вступает в реакцию хлорирования. Таким образом, при спекании гидроксидного кека с NH4Cl будут образовываться водорастворимые хлориды РЗЭ, что может быть использовано для отделения их от тория.
На основании полученных экспериментальных результатов предложена принципиальная пооперационная схема процесса получения концентрата РЗЭ из гидроксидного кека, образующегося при щелочной переработке монацитового концентрата.
Твердофазное спекание гидроксидного кека с NH4Cl, взятого в массовом соотношении 1:3, проводили при температуре 300 °C. Далее полученный хлоридный спек нагревали до 350 °C для перевода в газообразное состояние и удаления из системы избыточного NH4Cl. Газовая фаза направляется на десублимацию для регенерации NH4Cl. Спек хлоридов редкоземельных и радиоактивных элементов является конечным продуктом и может использоваться для последующего разделения на компоненты известными методами. По разработанной технологической схеме проведены укрупненные лабораторные и полупромышленные испытания.
Широко распространенными способами переработки монацитовых концентратов являются щелочной и сернокислотный методы. Одним из наиболее исследованных методов выделения и очистки РЗЭ из растворов выщелачивания является жидкостная экстракция с трибутилфосфатом (ТБФ). Разложение азотной кислотой при атмосферном давлении малоэффективно, поэтому в работе приведены результаты исследований процесса вскрытия монацитового концентрата при повышенных давлениях.
В качестве исходного продукта использовали монацитовый концентрат техногенного месторождения в г. Красноуфимске, Россия.
Основным параметром, характеризующим эффективность протекания процесса, приняли степень вскрытия ( , %) по РЗЭ.
, %) по РЗЭ.
Процесс автоклавного выщелачивания тория и суммы РЗЭ из монацитового концентрата (проба 1) был исследован при различных температурах в автоклаве (453, 473 и 493) К и постоянной концентрации азотной кислоты 6 М и продолжительности процесса 120 мин. Увеличение температуры процесса мало влияет на извлечение тория из монацита и незначительно повышает извлечение суммы РЗЭ. При увеличении времени реагирования извлечение РЗЭ растет нелинейно, а извлечение тория практически не зависит от времени реагирования.
Исследования по влиянию концентрации азотной кислоты проводили при концентрациях (3, 6, 9) М и постоянных температуре в автоклаве 473 К и продолжительности процесса 120 мин. Увеличение концентрации HNO3 с 6 до 9 М повышает извлечение суммы РЗЭ с 24% до 47%, а тория - лишь с 7% до 11% соответственно.
Результаты исследований азотнокислотного автоклавного способа вскрытия монацитового концентрата с использованием перемешивания на укрупненной установке были изложены в статье. При условиях: 9 М HNO3, 473 К, 150 мин, была достигнута степень извлечения РЗЭ на уровне 55 - 60%.
Для исследования возможности интенсификации исследуемого процесса были проведены эксперименты с применением микроволнового метода нагрева. Условия растворения следующие: 473 К, соотношение Т:Ж = 1:10, концентрированная азотная кислота, время проведения процесса - 60 мин. Избыточное давление при этих условиях поднималось до 1,5 - 1,6 МПа.
В целом образец 2 оказался более легковскрываемым азотной кислотой, чем образец 1. Степени вскрытия легких РЗЭ незначительно отличаются от степеней вскрытия тяжелых РЗЭ, т.е. РЗЭ вскрываются достаточно равномерно. Степени вскрытия балластных компонентов либо отличаются в большую сторону для пробы 2, либо отличаются незначительно. При этом степень вскрытия радиоактивных компонентов для тория составила 48% для пробы 1 и 62% для пробы 2. Степени вскрытия урана составили 58% для пробы 1 и 61% - для пробы 2.
Проведенные исследования показывают, что, несмотря на недостаточно высокие степени вскрытия монацита, при применении ряда методов интенсификации процесса азотнокислотного автоклавного выщелачивания монацита степень извлечения РЗЭ значительно увеличивается (с ~ 20% до 60%). Дальнейший поиск способов увеличения показателей эффективности процесса (химической активации, механоактивации и т.д.) делает рассматриваемый метод перспективным.
6.9 Универсальная экстракционная технология разделения ниобия и тантала при переработке колумбито-танталитовых концентратов различного состава
Вовлечение в производство новых источников ниобий-танталового сырья потребовало разработать эффективные технологий получения продукции на основе ниобия и тантала.
В рамках выполнения работы в качестве исходного сырья привлечен колумбитовый концентрат; соотношение Nb2O5:Ta2O5 в данном сырье близко 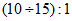 ; а также природный колумбито-танталит, в котором указанное соотношение близко к 1:1. Следует отметить, что колумбито-танталиты различного происхождения и химического состава широко распространены на мировом рынке ниобий- и танталсодержащего сырья.
; а также природный колумбито-танталит, в котором указанное соотношение близко к 1:1. Следует отметить, что колумбито-танталиты различного происхождения и химического состава широко распространены на мировом рынке ниобий- и танталсодержащего сырья.
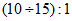 ; а также природный колумбито-танталит, в котором указанное соотношение близко к 1:1. Следует отметить, что колумбито-танталиты различного происхождения и химического состава широко распространены на мировом рынке ниобий- и танталсодержащего сырья.
; а также природный колумбито-танталит, в котором указанное соотношение близко к 1:1. Следует отметить, что колумбито-танталиты различного происхождения и химического состава широко распространены на мировом рынке ниобий- и танталсодержащего сырья.Промышленной переработки собственных колумбито-танталитовых концентратов в нашей стране не было, а опыт переработки лопарита к колумбито-танталитам малоприменим из-за существенного отличия минералогического и химического составов.
Эксперименты проводили с колумбитовым концентратом состава, масс. %: Nb2O5 - 50,5; Ta2O5 - 4,1; Fe - 12,6; Mn - 1,9; W - 0,5; Si - 3,6; Al - 0,35; Ca - 0,07; Ti - 1,7; Zr - 0,6; Sn <= 0,2; и колумбито-танталитом состава, масс. %: Nb2O5 - 41,0; Ta2O5 - 24,7; Fe - 14,1; Mn - 2,9; W - 1,3; Si - 0,47; Al - 0,2; Ca - 0,4; Ti - 0,6; Zr - 0,09; Sn < 2,5. Как видно из данных химического состава, содержание Nb2O5 в обоих материалах близко (50,5% и 41,0% (масс.) соответственно), однако значительно различается содержание Ta2O5 (4,1 и 24,7% (масс.)).
Технологическая схема предлагаемой технологии включает следующие основные стадии: сульфатно-фторидное вскрытие сырья  экстракционное разделение ниобия и тантала с очисткой их от примесей
экстракционное разделение ниобия и тантала с очисткой их от примесей  получение Nb2O5 и Ta2O5.
получение Nb2O5 и Ta2O5.
Показано, что определяющим условием для успешной организации экстракционного передела при переработке редкометалльных материалов, содержащих Nb2O5 и Ta2O5 в соотношении от 10:1 (например, колумбитовый концентрат Зашихинского месторождения) до 1:1 (природный колумбито-танталит), является процесс вскрытия исходного сырья. Предварительными испытаниями установлены параметры сульфатно-фторидного вскрытия обоих материалов: температура, концентрация и расход фтористоводородной кислоты, а также содержание в смеси до 350 - 400 г/л серной кислоты положительно влияет на степень извлечения Nb2O5 и Ta2O5 как из колумбитового концентрата, так и из колумбито-танталита. При использовании фтористоводородной кислоты в избытке 30 - 34% от стехиометрически необходимого через 6 ч в раствор переходит не менее 93 - 95% Nb2O5 и Ta2O5. В итоге при вскрытии необходимо выдержать такие условия, чтобы в исходном растворе на экстракционное разделение концентрация Nb2O5 находилась на уровне не менее 100 - 120 г/л, H2SO4 ~ 300 - 320 г/л, F- - 220 - 240 г/л, Ta2O5 - фактическая концентрация. Задачей последующей стадии гибкого экстракционного процесса является создание таких условий, при которых осуществляется разделение Nb2O5 и Ta2O5 на одном технологическом оборудовании с целью снижения капитальных и эксплуатационных затрат при организации переработки колумбито-танталитовых концентратов различного состава.
В связи с этим для переработки ниобий- и танталсодержащих растворов после вскрытия колумбитового концентрата и/или колумбито-танталита, содержащих Nb2O5 и Ta2O5 в соотношении от 10:1 до 1:1 (масс. %), была выбрана схема с коллективной экстракцией ниобия и тантала, промывкой насыщенного экстракта и последующим разделением элементов на стадии селективной реэкстракции и экстракционным разделением Nb2O5 и H2SO4 из образующегося реэкстракта ниобия; в качестве экстрагента использовался октанол-1.
Далее были проведены укрупненные непрерывные испытания предлагаемой технологии на многоступенчатом экстракционном каскаде, содержащем экстракторы типа смеситель-отстойник, на котором отработаны режимы экстракции, промывки, реэкстракции ниобия и тантала, экстракционного разделения Nb2O5 и H2SO4 с получением реэкстрактов ниобия и тантала требуемого для получения оксида ниобия (содержание основного вещества - не менее 99,8%) и оксида тантала (содержание основного вещества - не менее 99,5%) качества. Изучено распределение Nb2O5 и Ta2O5 в органической и водной фазах по камерам экстракционного каскада. Анализ полученных экспериментальных данных показывает, что процесс экстракции идет эффективно на 10 - 12 ступенях. Для стадии промывки насыщенного экстракта достаточно 5 - 6 ступеней, для селективной реэкстракции ниобия - 20 ступеней; для реэкстракции тантала - 6 - 8 ступеней, для экстракционного разделения Nb2O5 и H2SO4 из образующегося реэкстракта ниобия - 15 ступеней. Установлено, что в оптимальных условиях экстракционного процесса содержание целевых компонентов в реэкстракте ниобия: Nb2O5 - 130 - 150 г/л, Ta2O5 - < 0,05 г/л; в реэкстракте тантала: Ta2O5 - 15 - 80 г/л, Nb2O5 - < 0,05 г/л. Потери целевых компонентов с рафинатом не превышают 0,1%. После осаждения, промывки, просушки и прокалки получены экспериментальные образцы оксида ниобия чистотой не менее 99,8% и оксида тантала чистотой не менее 99,5%, торгующиеся на российском и мировом рынках редких металлов.
Исследованиями показано, что количество степеней в экстракционном каскаде и конструкция отдельной ступени не отличаются как при переработке колумбитового концентрата, так и при использовании богатого колумбито-танталита, отличаются только режимы проведения экстракционного процесса. Используются одинаковые рабочие растворы. При этом изменяется только соотношение потоков органической и водной фаз О:В в контурах экстракционного каскада. Например, в растворе после вскрытия колумбитового концентрата содержится больше ниобия, таким образом, соотношение О:В при реэкстракции ниобия будет другим (больше реэкстрагирующего раствора).
Таким образом, предложенный способ вскрытия и экстракционного разделения ниобия и тантала позволяет реализовать гибкий технологический процесс, позволяющий перерабатывать редкометалльные концентраты, содержащие Nb2O5 и Ta2O5 в соотношении от 10:1 до 1:1 (масс. %).
Однако следует отметить, что объем готовой продукции при переработке редкометалльных концентратов, содержащих ниобий и тантал в соотношениях 10:1 и 1:1, будет различным и, таким образом, технико-экономические показатели будут отличаться и требовать дополнительного уточнения для каждого вида исходного сырья.
Одним из перспективных источников добычи скандия является попутное его извлечение из маточных растворов сорбции урана.
Об отечественной технологии извлечения Sc при переработке урановых руд впервые было упомянуто в докладе сотрудников ВНИИХТ на конференции в Сан-Пауло в 1970 г. Скандий извлекали в процессе экстракционной переработки глинисто-пиритных руд, содержащих уран, фосфор, РЗЭ.
При решении задачи комплексной переработки урановых руд неизбежно возникает вопрос очистки получаемой сопутствующей урану продукции от радиоактивности. Необходимо учитывать, что в технологических растворах присутствуют не только уран и торий, но и продукты их радиационного распада, концентрация которых изменяется в соответствии с их периодами полураспада.
Попутное извлечение скандия при добыче урана методом подземного скважинного выщелачивания предусматривает переработку возвратных растворов после сорбции урана и включает в себя следующие основные операции: сорбционное концентрирование скандия на ионообменных смолах, последующую отмывку ионообменных смол от примесей, десорбцию скандия, осаждение радиоактивных примесей, экстракционную очистку и дезактивацию полупродуктов, осаждение товарных концентратов.
Были проведены исследования экстракционного разделения скандия и тория в рамках разработки промышленной технологии попутного извлечения скандия при добыче урана методом подземного скважинного выщелачивания с получением оксида скандия.
Образцы чернового концентрата (ЧК) скандия для изучения экстракционного разделения скандия и тория были получены из фильтратов сорбции урана на АО "Далур" при проведении стендовых комплексных испытаний.
Известно, что азотнокислотное растворение является традиционным в схемах получения оксида скандия. Выбор способа вскрытия (использование серной или азотной кислот, концентрация) определяется, также условиями последующего экстракционного извлечения урана и тория.
Проведено исследование процесса выделения тория из раствора после азотнокислотного растворения первичного концентрата скандия. Установлено, что основной вклад в радиоактивную составляющую вносит изотоп уранового ряда Th-230. Объемная радиоактивность раствора по изотопу Th-230 составляет 1200 Бк/см3. Доля изотопов Ra-226, Ra-228, Th-228 составляет, %: 0,001; 0,001; 0,2. После растворения чернового концентрата получен раствор с концентрациями ~ 5 г/дм3 Sc и ~ 4 г/дм3 Th.
Для выделения тория методом жидкостной экстракции из азотнокислых сред после растворения ЧК скандия в лабораторных условиях изучена возможность применения систем экстрагентов, включающих реагенты из класса нейтральных фосфорорганических соединений на основе Cyanex 923 и ТБФ в керосине.
Для системы Cyanex 923 установлены условия наиболее эффективного избирательного извлечения тория - концентрация азотной кислоты 250 - 270 г/дм3, соотношение фаз 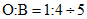 . Коэффициент разделения Th и Sc составил от 34 до 312 в зависимости от концентрации тория и скандия в растворе. Для увеличения степени извлечения тория и снижения потерь скандия рекомендовано увеличить соотношение фаз и количество ступеней экстракции.
. Коэффициент разделения Th и Sc составил от 34 до 312 в зависимости от концентрации тория и скандия в растворе. Для увеличения степени извлечения тория и снижения потерь скандия рекомендовано увеличить соотношение фаз и количество ступеней экстракции.
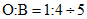 . Коэффициент разделения Th и Sc составил от 34 до 312 в зависимости от концентрации тория и скандия в растворе. Для увеличения степени извлечения тория и снижения потерь скандия рекомендовано увеличить соотношение фаз и количество ступеней экстракции.
. Коэффициент разделения Th и Sc составил от 34 до 312 в зависимости от концентрации тория и скандия в растворе. Для увеличения степени извлечения тория и снижения потерь скандия рекомендовано увеличить соотношение фаз и количество ступеней экстракции.Показана принципиальная возможность применения 40%-ного раствора ТБФ в керосине для снижения радиоактивности скандийсодержащего раствора. При концентрации азотной кислоты 120 г/дм3 удалось снизить активность на 98,5%, однако потери Sc при этом составили 26,5%. Для снижения потерь скандия и повышения степени очистки от тория рекомендовано повысить концентрацию азотной кислоты в исходном растворе до значения 230 - 270 г/дм3.
Выполненные исследования по влиянию концентрации HNO3, NH4NO3 на извлечение Th, Sc и Y показали преимущественное извлечение тория 50%-ным раствором ТБФ в широком диапазоне изменения кислотности и солевого фона исходного раствора. Наиболее благоприятными условиями извлечения тория являются интервал концентраций азотной кислоты 220 - 290 г/дм3 и нитратов более 4 моль/дм3.
Для дополнительной очистки от тория растворов промежуточных скандийсодержащих продуктов возможно использование смеси 7,5% Cyanex 923 + 7,5% ТБФ, а также 40%-ный раствор ТБФ в керосине. В обоих случаях обеспечивается необходимый уровень активности образцов оксида скандия (<= 1 Бк/г). При этом первый экстрагент обеспечивает процесс разделения Sc и Th при меньшем количестве стадий экстракции (5 стадий) по сравнению со вторым, но при большей степени соэкстракции скандия - до 30%. Экстрагент 40% ТБФ обеспечивает очистку от тория при 8 стадиях экстракции, но при меньшем соизвлечении Sc - 14,2%.
Полученные результаты очистки скандия от радиоактивных примесей подтвердили эффективность экстракции радионуклидов в системе 40 - 50% ТБФ в керосине. Достигнуто остаточное содержание тория в рафинатах экстракции - C(Th) = 5 мг/л без существенных потерь скандия. При этом соотношение Sc и Th в рафинате экстракции радионуклидов увеличилось относительно исходного раствора выщелачивания чернового скандиевого концентрата с 2,1 до 1500.
Из очищенного от тория раствора были получены образцы оксида скандия, соответствующие требованиям ТУ 95.148-77 на оксид скандия с содержанием Sc2O3 99,0%.
Химический состав образца оксида скандия приведен в таблице 6.2.
Таблица 6.2
Содержание примесей, в пересчете на оксиды, %, не более | ||
ТУ 95.148-77 | По результатам испытаний | |
Железо | 0,05 | 0,04 |
Алюминий | 0,01 | 0,01 |
Кальций | 0,05 | 0,05 |
Медь | 0,01 | 0,01 |
Кремний | 0,05 | 0,05 |
Марганец | 0,01 | 0,01 |
Магний | 0,01 | 0,01 |
Иттрий | 0,05 | 0,05 |
Иттербий | 0,05 | 0,05 |
Цирконий | 0,1 | 0,05 |
Титан | 0,05 | 0,05 |
Фосфор | 0,02 | 0,01 |
Особенностью руды участка Буранный месторождения Томтор является наличие большого количества ценных компонентов (Nb, полный спектр элементов редкоземельной группы (РЗЭ)), высокая дисперсность, тесное взаимное срастание минеральных фаз и связь одного и того же полезного компонента с несколькими минералами (минералы группы крандаллита, монацит, пирохлор), а также наличие нескольких разновидностей одноименных минералов (пирохлора, монацита, группы крандаллита), различающихся по своим физико-механическим и физико-химическим свойствам.
Руда участка Буранный месторождения Томтор крайне изменчива по содержанию основных элементов, в частности, содержание Nb в исследованных технологических пробах изменяется от 1,12 до 13,3%, 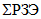 - от 5,33 до 28,27%. Руды участка Буранный месторождения Томтор относятся к рудам редких металлов пирохлор-крандаллит-монацитового типа. Преобладающим классом соединений в составе руды являются фосфаты (более 90%), в подчиненном количестве присутствуют классы оксидов, гидроксидов, сульфидов и силикатов. Основным минералом-концентратором Nb является изоморфный ряд Ba-Sr пирохлоров различной степени измененности (от первичных до полностью преобразованных). Содержание пирохлора в исходной руде варьируется от 0,7% до 20%, в среднем составляет 6,5%. В подчиненном количестве присутствуют ниобийсодержащие минералы: рутил, ильменорутил, колумбит. Для элементов редкоземельной группы к основным минералам относятся монацит (0 - 25%, в среднем - 21,4%), Zr-ксенотим, Sc-циркон, минералы группы крандаллита (в среднем - 43,7%, в том числе гойяцит (3 - 32%, в среднем - 15%), горсейксит (16 - 53%, в среднем - 28,0%), флоренсит (0 - 3%, в среднем - 0,6%), собственно крандаллит (1,0 - 11,2%, в среднем - 4,2%)).
- от 5,33 до 28,27%. Руды участка Буранный месторождения Томтор относятся к рудам редких металлов пирохлор-крандаллит-монацитового типа. Преобладающим классом соединений в составе руды являются фосфаты (более 90%), в подчиненном количестве присутствуют классы оксидов, гидроксидов, сульфидов и силикатов. Основным минералом-концентратором Nb является изоморфный ряд Ba-Sr пирохлоров различной степени измененности (от первичных до полностью преобразованных). Содержание пирохлора в исходной руде варьируется от 0,7% до 20%, в среднем составляет 6,5%. В подчиненном количестве присутствуют ниобийсодержащие минералы: рутил, ильменорутил, колумбит. Для элементов редкоземельной группы к основным минералам относятся монацит (0 - 25%, в среднем - 21,4%), Zr-ксенотим, Sc-циркон, минералы группы крандаллита (в среднем - 43,7%, в том числе гойяцит (3 - 32%, в среднем - 15%), горсейксит (16 - 53%, в среднем - 28,0%), флоренсит (0 - 3%, в среднем - 0,6%), собственно крандаллит (1,0 - 11,2%, в среднем - 4,2%)).
Исследована возможность обогащения руды флотационными, гравитационными и радиометрическими методами. Применение процессов обогащения не позволяет получить концентраты с приемлемыми показателями качества и извлечения, что обусловливает применение гидрометаллургических процессов для переработки всего объема руды.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду рисунок 6.6, а не 6.2. |
Разработана и проверена в опытно-промышленном масштабе технология переработки руды Томторского месторождения (участок Буранный). Данная технология обеспечивает высокие степени извлечения полезных компонентов (Nb и РЗЭ), простоту, надежность и экологическую безопасность при реализации в промышленных масштабах и включает следующие стадии (рисунок 6.2):
- рудоподготовка (дробление и измельчение руды);
- вскрытие руды раствором гидроксида натрия с последующим водным выщелачиванием. Фосфатные минералы в руде вскрываются едким натром с получением смеси гидроокислов РЗЭ и других гидроокислов в твердом остатке. Пульпа из реакторов щелочного вскрытия разбавляется водой для того, чтобы растворить тринатрийфосфат, образовавшийся в процессе щелочного вскрытия. При этом в раствор переводятся такие элементы, как фосфор, алюминий и частично кремний и ванадий;
- выщелачивание РЗЭ из кека щелочного вскрытия раствором минеральной (например, соляной или азотной) кислоты. При этом в раствор переходят все РЗЭ, а также такие примесные элементы, как железо, торий, уран;
- очистка раствора РЗЭ от примесей с использованием перекиси водорода, известняка и сульфидсодержащего реагента. Раствор РЗЭ содержит в качестве примесей такие элементы, как железо, алюминий, кремний, ванадий, титан, свинец, торий, уран и др. Для перевода Fe (II) в Fe (III) в раствор добавляют пероксид водорода, после чего осуществляют осаждение всех примесей в виде гидроксидов с использованием пульпы карбоната кальция. Очистка от свинца производится путем добавления сульфидсодержащего реагента с получением осадка сульфидов тяжелых цветных металлов. Очищенный раствор РЗЭ направляют на получение чернового концентрата РЗЭ, кек - в отход;
- осаждение чернового концентрата гидроксидов РЗЭ с использованием извести. Для осаждения РЗЭ в виде гидроксидов очищенный от примесей раствор РЗЭ смешивают с пульпой гидроксида кальция. Черновой концентрат направляют на растворение в азотной кислоте, а маточный раствор - на регенерацию минеральной кислоты;
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду рисунок 6.7, а не 6.3. |
- растворение осадка РЗЭ в азотной кислоте и экстракционное разделение РЗЭ. Осадок РЗЭ растворяют в азотной кислоте, полученный азотнокислый раствор РЗЭ направляют на групповое разделение (Рисунок 6.3) с использованием ТБФ в качестве экстрагента, с получением следующих продуктов: раствор нитратов среднетяжелой группы РЗЭ, раствор нитратов лантана-церия, раствор нитратов празеодима-неодима, раствор нитрата празеодима, раствор нитрата неодима. После этого проводят осаждение РЗЭ в виде карбонатов, при необходимости осуществляют сушку карбонатов РЗЭ и прокаливание до оксидов РЗЭ;
- выщелачивание Nb из кека выщелачивания РЗЭ фторсодержащим кислым раствором (например, раствором плавиковой кислоты, смесью серной и плавиковой кислот и др.). При этом в раствор переходят ниобий и такие примесные элементы, как титан, железо, кремний и фосфор. Раствор направляют на жидкостную экстракцию ниобия, а кек выщелачивания отправляют в отход;
- выделение Nb из кислого раствора выщелачивания методом жидкостной экстракции с использованием 1-октанола. Ниобий в виде фторниобиевой кислоты экстрагируют октанолом из кислого раствора, содержащего фториды ниобия, титана, кремния, фосфора и железа. Ниобий (в виде фторниобиевой кислоты) селективно извлекается в органическую фазу, а все примеси остаются в рафинате. Полученный реэкстракт ниобия отправляют на получения пентаоксида ниобия;
- получение пентаоксида ниобия. Водный раствор фторниобиевой кислоты, полученный после экстракции, направляют на получение пентаоксида ниобия (например, методом пирогидролиза или методом осаждения гидроксида ниобия с последующим прокаливанием осадка до пентаоксида);
- регенерация раствора гидроксида натрия с участка щелочного вскрытия - водного выщелачивания. Раствор гидроксида натрия, содержащий в качестве примесей фосфаты, алюминаты, силикаты ванадаты, карбонаты натрия, регенерируют с использованием извести. Раствор щелочи, очищенный от примесей, направляют на упаривание и возвращают на стадию щелочного вскрытия руды. Осадок примесей, представляющий собой в основном смесь фосфата и гидроксида кальция, направляется в отход;
- регенерация раствора минеральной кислоты из раствора солей после осаждения РЗЭ с использованием серной кислоты. Регенерацию минеральной кислоты производят из маточного раствора осаждения чернового концентрата гидроксидов РЗЭ, содержащего в основном соли щелочных (натрия) и щелочноземельных металлов (кальция и стронция). Упаренный маточный раствор смешивают с концентрированной серной кислотой, осадок сульфатов щелочных и щелочноземельных металлов отправляют в отход, раствор регенерированной минеральной кислоты возвращают на стадию выщелачивания РЗЭ.
Готовой продукцией технологии являются пентаоксид ниобия, смесь карбонатов лантана и церия, оксиды празеодима и неодима, смесь карбонатов РЗЭ среднетяжелой группы.
Отходами технологии являются промытые кеки фильтрации, основными компонентами которых являются нерастворимые фосфаты, сульфаты, фториды и гидроксо-фториды металлов, которые отправляют в хвостохранилище либо иной объект размещения отходов.
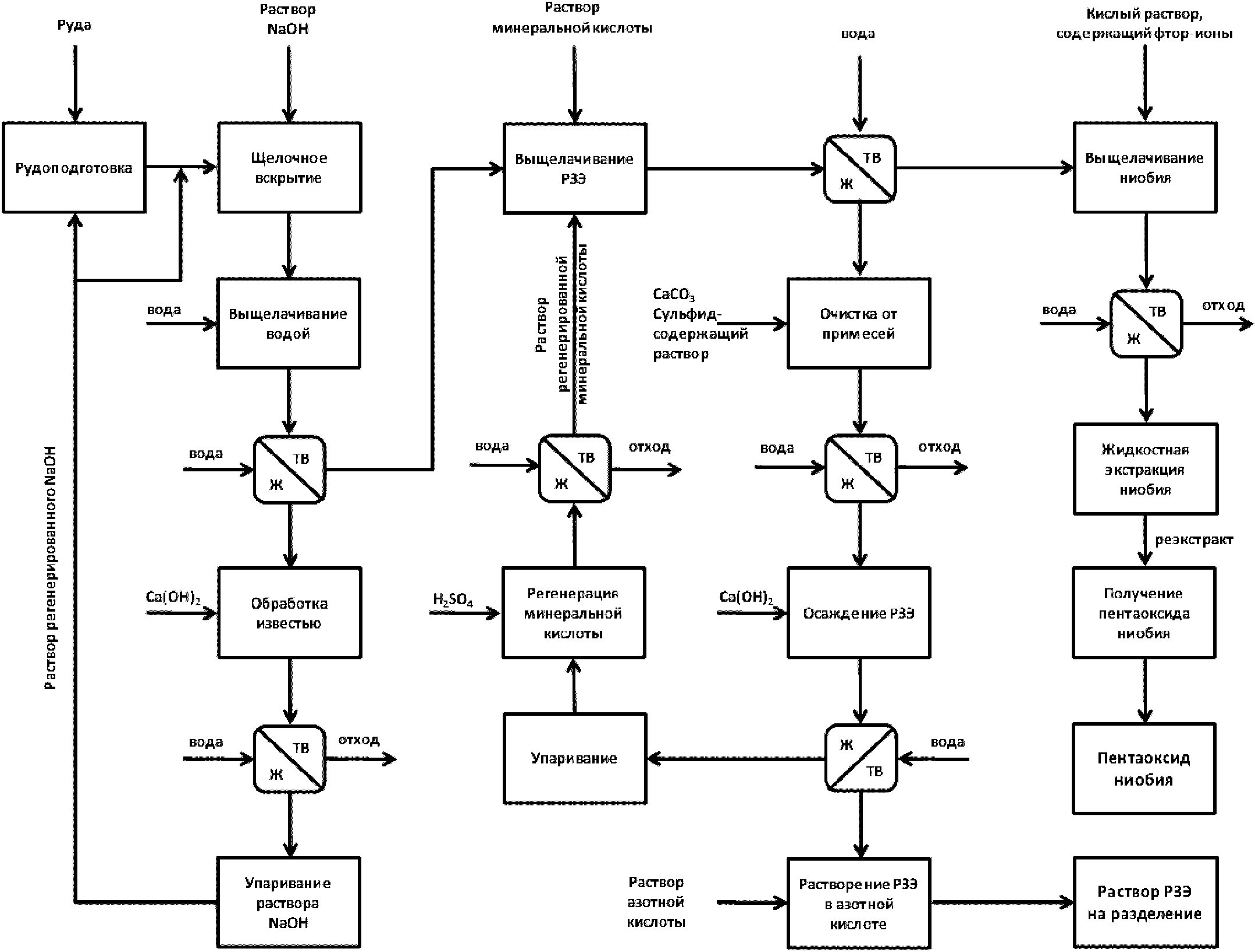
месторождения Томтор
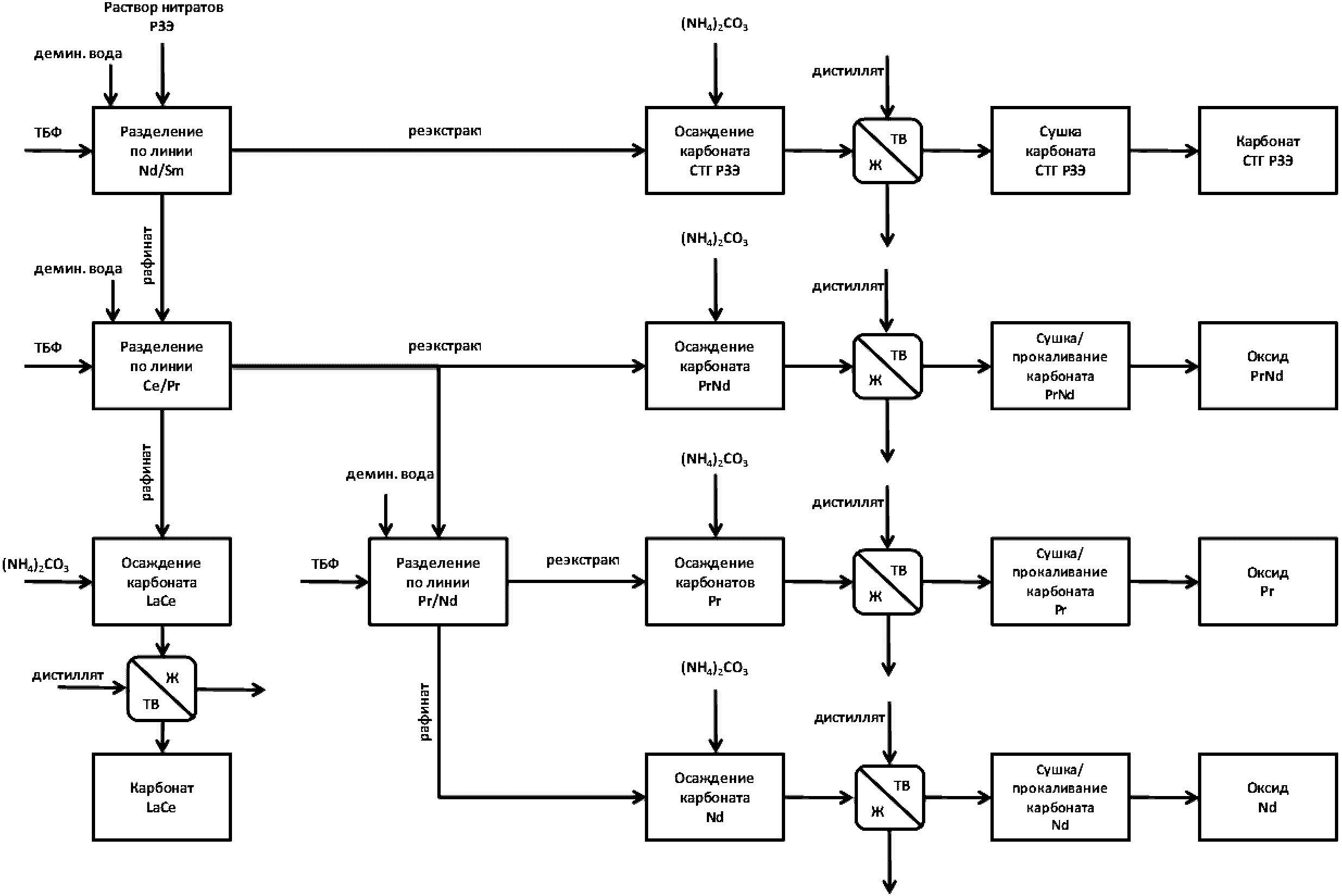
разделения РЗЭ
Информационно-технический справочник по наилучшим доступным технологиям "Производство редких и редкоземельных металлов" подготовлен в соответствии с распоряжением Правительства Российской Федерации от 10 июня 2022 г. N 1537-р "Об утверждении поэтапного графика актуализации информационно-технических справочников по наилучшим доступным технологиям" и правилами определения технологии в качестве наилучшей доступной технологии, а также разработки, актуализации и опубликования информационно-технических справочников по наилучшим доступным технологиям, утвержденных постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458.
При подготовке настоящего справочника в максимально возможной степени были учтены положения окончательного проекта второй редакции справочника Европейского союза по наилучшим доступным технологиям для предприятий цветной металлургии (Best Available Techniques (BAT) Reference Document for the Non-Ferrous Metals Industries, final draft, October 2014), включая краткие описания (заключения) по НДТ.
Для определения условий нормирования отечественных предприятий необходима оценка достигнутых отраслью показателей ресурсо- и энергоэффективности и экологической результативности. В целях сбора информации о применяемых на промышленных предприятиях технологических процессах, оборудовании, об источниках загрязнения окружающей среды, технологических, технических и организационных мероприятиях, направленных на снижение загрязнения окружающей среды и повышение энергоэффективности и ресурсосбережения, были подготовлены анкеты для предприятий, которые были направлены в адреса всех предприятий по производству редких металлов.
Технологические показатели НДТ определялись на основе результатов обработки данных, представленных предприятиями при анкетировании и по специальным дополнительным запросам.
По ряду показателей при написании справочника НДТ были использованы также зарубежные материалы: справочник Европейского союза по наилучшим доступным технологиям для предприятий цветной металлургии, статистические сборники, результаты научно-исследовательских и диссертационных работ, иные источники, а также информация, полученная в ходе консультаций с экспертами в области производства редких металлов.
(обязательное)
ДЛЯ КОТОРЫХ УСТАНАВЛИВАЮТСЯ ТЕХНОЛОГИЧЕСКИЕ ПОКАЗАТЕЛИ
Маркерные вещества для атмосферного воздуха:
Таблица А.1
Общие НДТ для производства редких металлов
Азота оксид (азот (II) оксид; азот монооксид) |
Азота диоксид (двуокись азота; пероксид азота) |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Аммиак (азота гидрид) |
Хлор |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) |
Серы диоксид |
Таблица А.2
Производство циркония и гафния
Аммиак (азота гидрид) |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид |
Фтористый водород, растворимые фториды (фториды неорганические хорошо растворимые): натрия фторид (натрий фтористый); натрия гексафторидсиликат |
Азота оксид (азот (II) оксид; азот монооксид) |
Азота диоксид (двуокись азота; пероксид азота) |
Серы диоксид |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) |
Хлор |
Цирконий |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) |
Таблица А.3
Производство кальция
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Азота оксид (азот (II) оксид; азот монооксид) |
Азота диоксид (двуокись азота; пероксид азота) |
Хлор |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) |
Таблица А.4
Производство титана
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Азота оксид (азот (II) оксид; азот монооксид) |
Азота диоксид (двуокись азота; пероксид азота) |
Серы диоксид |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) |
Хлор |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ |
Фосген (карбонилдихлорид) |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид |
Серная кислота (по молекуле H2SO4) |
диАлюминий триоксид /в пересчете на алюминий/ |
Минеральное масло (масло минеральное нефтяное): веретенное, машинное, цилиндровое и иные |
Таблица А.5
Производство магния
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Азота оксид (азот (II) оксид; азот монооксид) |
Азота диоксид (двуокись азота; пероксид азота) |
Серы диоксид |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) |
Хлор |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ |
Магний оксид (окись магния) |
Таблица А.6
Производство теллура
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) |
Таблица А.7
Гранулирование и переработка пылевидного сырья
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов |
Маркерные вещества для сбросов:
Таблица А.8
Маркерные вещества при производстве редких металлов
Алюминий |
Никель |
Титан |
Цинк |
Хлорид-ион |
Фторид-ион |
Нитрат-ион |
Сульфат-ион |
Нитрит-ион |
Взвешенные вещества |
Таблица А.9
Дополнительные маркерные вещества при производстве магния
из обогащенного карналлита
Магний |
Калий |
Кальций |
Натрий |
Таблица А.10
Дополнительные маркерные вещества для предприятий,
осуществляющих прием хозяйственно-бытовых стоков
от сторонних организаций и не относящихся к области
применения ИТС НДТ 10 "Очистка сточных вод
с использованием централизованных систем
водоотведения поселений, городских округов"
БПК полн. |
АСПАВ (анионные синтетические поверхностно-активные вещества) |
Фосфат-ион |
Хлорат-ион |
ХПК |
(обязательное)
Таблица Б.1
Перечень технологических показателей при производстве редких
и щелочноземельных металлов
Производственный процесс | Наименование загрязняющего вещества | Единица измерения | Величина |
Пирометаллургические процессы производства продукции, которая входит в область применения настоящего справочника НДТ (НДТ 13) | Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Сушка сырья в сушильных башнях в потоке горячих топочных газов с использованием природного газа в качестве топлива (НДТ 14) | Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 |
Подготовка сырья (например, прием, обработка, хранение, измерение, перемешивание, смешивание, сушка, измельчение, просеивание) в производстве продукции, которая входит в область применения настоящего справочника (НДТ 15) | Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 40 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 | |
Производство оксидов металлов (выщелачивание, очистка и электролиз), которые входят в область применения данного справочника (НДТ 16) | Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 40 |
Производство оксидов металлов (гидролиз), которые входят в область применения данного справочника (НДТ 16) | Аммиак (азота гидрид) | мг/нм3 | <= 30 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 | |
Загрузка, обжиг, плавка и получение огарков и спеков в производстве продукции, которая входит в область применения настоящего справочника НДТ (НДТ 17) | Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Аммиак (азота гидрид) | мг/нм3 | <= 100 | |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 50 | |
Хлор | мг/нм3 | <= 30 | |
Серы диоксид | мг/нм3 | <= 60 | |
Производство концентратов (карбонатов) РЗМ (НДТ 18) | Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 30 |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) | мг/нм3 | <= 5 | |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 5 | |
Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении фторцирконата, фторгафната калия в производстве циркония и гафния методом фторирования (НДТ 21) | Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Аммиак (азота гидрид) | мг/нм3 | <= 275 | |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 | |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 52 | |
Серы диоксид | мг/нм3 | <= 18 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 38 | |
Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении технического тетрахлорида циркония в производстве циркония методом хлорирования (НДТ 22) | Хлор | мг/нм3 | <= 365 |
Цирконий | мг/нм3 | <= 40 | |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 160 | |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 | |
Карбонат натрия (динатрий карбонат; натрий углекислый; натриевая соль угольной кислоты) | мг/нм3 | <= 40 | |
Получение порошка циркония и гафния электролитического методом фторирования (дробление катодного осадка, обработка в растворах углеаммонийных солей, флотация порошка, кислотная обработка раствором серной кислоты, сушка порошка) в производстве циркония и гафния (НДТ 23) | Аммиак (азота гидрид) | мг/нм3 | <= 275 |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в настоящем разделе) | мг/нм3 | <= 50 | |
Разделение хлоридов циркония и гафния (солевая очистка, ректификация и отгонка, абсорбционная очистка) при получении тетрахлорида циркония очищенного в производстве циркония методом хлорирования (НДТ 24) | Цирконий | мг/нм3 | <= 40 |
Получение катодного осадка циркония и гафния методом электролиза в расплаве солей (НДТ 25) | Хлор | мг/нм3 | <= 100 |
Фтористый водород, растворимые фториды (фториды неорганические хорошо растворимые): натрия фторид (натрий фтористый); натрия гексафторид силикат | мг/нм3 | <= 190 | |
Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 | |
Восстановление циркония из тетрахлорида циркония магнийтермическим способом (конденсация, кристаллизация, спекание) при получении циркониевой губки в производстве циркония методом хлорирования (НДТ 26) | Цирконий | мг/нм3 | <= 40 |
Применение извести (негашеной) для приготовления известкового молока (НДТ 27) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 20 |
Хлорирование известкового молока анодными газами для получения раствора хлористого кальция (НДТ 28) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 230 | |
Сушка раствора хлористого кальция для получения сухого порошка хлористого кальция (НДТ 29) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 180 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Электролиз расплава хлористого кальция для получения медно-кальциевого сплава (НДТ 30) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 230 | |
Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание) при получении титанового шлака (НДТ 31) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Процесс плавки и выпуска расплава титанового шлака (НДТ 32) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 750 |
Процесс приготовления трехкомпонентной титансодержащей шихты (сушка материалов, дробление материалов, помол, перемешивание) (НДТ 33) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
Подготовка сырья (прием, обработка, хранение, хлорирование) при получении технического тетрахлорида титана в производстве титана губчатого магнийтермическим способом (НДТ 34) | Хлор | мг/нм3 | <= 276 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 395 | |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 160 | |
Восстановление титана из тетрахлорида титана магнийтермическим способом (восстановление, дистилляция) при получении титановой губки в производстве титана губчатого магнийтермическим способом (НДТ 35) | Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 50 |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 10 | |
Подготовка шихтовых материалов (первичных и вторичных) для производства титановых сплавов (очистка в кислотном растворе, обезжиривание, дробеметная обработка, нагрев, измельчение, навешивание, прессование, сушка) (НДТ 36) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 | |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 50 | |
Серы диоксид | мг/нм3 | <= 60 | |
Серная кислота (по молекуле H2SO4) | мг/нм3 | <= 50 | |
Производство титановых слитков (загрузка, плавление в вакуумных печах, выгрузка, охлаждение, шоопирование, обработка) (НДТ 37) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
диАлюминий триоксид /в пересчете на алюминий/ | мг/нм3 | <= 50 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 | |
Производство титановых изделий и полуфабрикатов (нагрев, ковка, штамповка, отжиг, прокатка, прессование, правка, травление, механическая обработка, резка) (НДТ 38) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 | |
Минеральное масло (масло минеральное нефтяное): веретенное, машинное, цилиндровое и иные | мг/нм3 | <= 50 | |
Серы диоксид | мг/нм3 | <= 60 | |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 50 | |
Фториды газообразные /в пересчете на фтор/: гидрофторид (водород фторид, фтороводород); кремний тетрафторид | мг/нм3 | <= 50 | |
Серная кислота (по молекуле H2SO4) | мг/нм3 | <= 50 | |
Получение высокопроцентного ферротитана в индукционных печах (загрузка шихты, плавление, разливка, дробление) (НДТ 39) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 60 | |
Серы диоксид | мг/нм3 | <= 60 | |
Обезвоживание обогащенного карналлита во вращающихся печах и печах кипящего слоя (НДТ 40) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 180 |
Азота оксид (азот (II) оксид; азот монооксид) | мг/нм3 | <= 60 | |
Азота диоксид (двуокись азота; пероксид азота) | мг/нм3 | <= 60 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 240 | |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 | |
Серы диоксид | мг/нм3 | <= 30 | |
Хлор | мг/нм3 | <= 20 | |
Хлорирование обезвоженного искусственного карналлита анодными газами для получения безводного очищенного искусственного карналлита (НДТ 41) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 300 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 230 | |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 30 | |
Электролиз расплава обезвоженного карналлита с получением первичного магния (НДТ 42) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 50 |
Хлор | мг/нм3 | <= 300 | |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 100 | |
Рафинирование и литье магния и сплавов (НДТ 43) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 40 | |
Серы диоксид | мг/нм3 | <= 170 | |
Магний оксид (окись магния) | мг/нм3 | <= 5 | |
Хлор | мг/нм3 | <= 10 | |
Производство теллура (НДТ 44) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 60 |
Абсорбция примесей, газов, аэрозолей при получении технических пентахлоридов ниобия и тантала (НДТ 45) | Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 10 |
Хлор | мг/нм3 | <= 20 | |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 170 | |
Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 100 | |
Разделение технических пентахлоридов ниобия и тантала (НДТ 46) | Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | <= 10 |
Хлор | мг/нм3 | <= 20 | |
Фосген (карбонилдихлорид) | мг/нм3 | <= 2 | |
Углерода оксид (углерод окись; углерод моноокись; угарный газ) | мг/нм3 | <= 170 | |
Процесс подготовки шихты (сушка материалов, загрузка, перемешивание) и проведение восстановительной плавки ниобия и тантала из пентаоксида ниобия и тантала (НДТ 47) | Взвешенные вещества (разнородные по составу твердые частицы, содержащиеся в выбросах загрязняющих веществ и не поименованные в разделе I перечня загрязняющих веществ, в отношении которых применяются меры государственного регулирования в области охраны окружающей среды, утвержденного распоряжением Правительства Российской Федерации от 20 октября 2023 г. N 2909-р) | мг/нм3 | <= 40 |
Гранулирование и переработка пылевидного сырья (НДТ 56) | Пыль неорганическая с содержанием кремния менее 20, 20 - 70, а также более 70 процентов | мг/нм3 | <= 50 |
Прямое извлечение лития технологии прямого извлечения лития AXIONIT DLE (НДТ 58) | Натрий гидроксид (натр едкий) | мг/нм3 | 0,4 |
Хлористый водород (гидрохлорид, водород хлорид) /по молекуле HCl/ | мг/нм3 | 0,2 | |
Хлор | мг/нм3 | 0,1 |
Технологические показатели загрязняющих веществ в сбросах в водные объекты, соответствующие НДТ.
Таблица Б.2
Наименование загрязняющего вещества | Единица измерения | Величина |
Алюминий | мг/дм3 | <= 0,3 |
Никель | мг/дм3 | <= 0,3 |
Титан | мг/дм3 | <= 0,1 |
Цинк | мг/дм3 | <= 0,08 |
Хлорид-ион | мг/дм3 | <= 1800 |
Фторид-ион | мг/дм3 | <= 4,0 |
Нитрат-ион | мг/дм3 | <= 100,0 |
Сульфат-ион | мг/дм3 | <= 500,0 |
Нитрит-ион | мг/дм3 | <= 3,3 |
Таблица Б.3
Технологические показатели: средний уровень концентраций
загрязняющих веществ в прямых сбросах, образующихся
при производстве редких металлов, в принимающие
водные объекты
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
Алюминий | мг/дм3 | <= 0,3 |
Никель | мг/дм3 | <= 0,3 |
Титан | мг/дм3 | <= 0,1 |
Цинк | мг/дм3 | <= 0,08 |
Хлорид-ион | мг/дм3 | <= 1800 |
Фторид-ион | мг/дм3 | <= 4,0 |
Нитрат-ион | мг/дм3 | <= 100,0 |
Сульфат-ион | мг/дм3 | <= 500,0 |
Нитрит-ион | мг/дм3 | <= 3,3 |
Взвешенные вещества | мг/дм3 | <= 30,0 |
В случае замкнутого цикла водооборота показатели не применяются | ||
Таблица Б.4
Дополнительные технологические показатели: средний уровень
концентраций загрязняющих веществ в прямых сбросах,
образующихся при производстве магния
из обогащенного карналлита
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
Магний | мг/дм3 | <= 140,0 |
Калий | мг/дм3 | <= 140,0 |
Кальций | мг/дм3 | <= 950,0 |
Натрий | мг/дм3 | <= 280,0 |
В случае замкнутого цикла водооборота показатели не применяются. | ||
Таблица Б.5
Дополнительные технологические показатели: для предприятий,
осуществляющих прием хозяйственно-бытовых стоков
от сторонних организаций и не относящихся к области
применения ИТС НДТ 10 "Очистка сточных вод
с использованием централизованных систем водоотведения
поселений, городских округов"
Параметр | Единица измерения | Концентрация загрязняющего вещества <1> |
БПК полн. | мг/дм3 | <= 4,0 |
АСПАВ (анионные синтетические поверхностно-активные вещества) | мг/дм3 | <= 0,1 |
Фосфат-ион | мг/дм3 | <= 1,0 |
Хлорат-ион | мг/дм3 | <= 1,0 |
ХПК | мг/дм3 | <= 40,0 |
В случае замкнутого цикла водооборота показатели не применяются | ||
(обязательное)
В.1 НДТ общего характера
НДТ 1. Повышение общей результативности природоохранной деятельности.
НДТ 2. Повышение эффективности использования энергии.
НДТ 3. Обеспечение стабильности производственного процесса.
В.2 Предотвращение и снижение эмиссий
НДТ 4. Уменьшение неорганизованных выбросов, образующихся при хранении сырья.
НДТ 5. Уменьшение неорганизованных эмиссий, образующихся при обработке и транспортировке сырья.
НДТ 6. Предупреждение или сокращение неорганизованных выбросов.
НДТ 7. Предотвращение или сокращение неорганизованных выбросов от подготовки и предварительной обработки материалов.
НДТ 8. Предотвращение или уменьшение неорганизованных выбросов от загрузки сырья редких металлов до получения огарка или спека.
НДТ 9. Использование мокрой шихты для обжиговой печи.
НДТ 10. Выполнение операций при пониженном давлении при обработке огарка.
НДТ 11. Сокращение неорганизованных выбросов, образующихся при промывке, разделении твердых и жидких фракций и очистке.
НДТ 12. Использование в электролизерах добавок, особенно пенообразующих агентов, в целях уменьшения неорганизованных выбросов паров, образующихся при электроизвлечении.
НДТ 13. Предотвращение выбросов NO, NO2 от пирометаллургических процессов.
НДТ 14. Использование природного газа в качестве топлива при сушке сырья в сушильных башнях в потоке горячих топочных газов.
НДТ 15. Сокращение выбросов в воздух пыли (взвешенных веществ) от подготовки сырья (например, прием, обработка, хранение, измерение, перемешивание, смешивание, сушка, измельчение, просеивание).
НДТ 16. Сокращение выбросов, образующихся при производстве оксидов металлов.
НДТ 17. Сокращение выбросов от загрузки, обжига, плавки и получения огарков и спеков.
НДТ 18. Сокращения выбросов при производстве концентратов (карбонатов) РЗМ.
НДТ 19. Сокращение выбросов органических соединений в атмосферу из сушки исходного материала и процесса обжига, спекания и плавки.
НДТ 20. Сокращение выбросов ПХДД/Ф и ЛОС в воздухе при комбинированных технологиях переработки нетрадиционного сырья редких и элементов.
НДТ 21. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении фторцирконата, фторгафната калия в производстве циркония и гафния методом фторирования.
НДТ 22. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении технического тетрахлорида циркония в производстве циркония методом хлорирования.
НДТ 23. Получение порошка циркония и гафния электролитического методом фторирования (дробление катодного осадка, обработка в растворах углеаммонийных солей, флотация порошка, кислотная обработка раствором серной кислоты, сушка порошка) в производстве циркония и гафния.
НДТ 24. Разделение хлоридов циркония и гафния (солевая очистка, ректификация и отгонка, абсорбционная очистка) при получении тетрахлорида циркония очищенного в производстве циркония методом хлорирования.
НДТ 25. Получение катодного осадка циркония и гафния методом электролиза в расплаве солей.
НДТ 26. Восстановление циркония из тетрахлорида циркония магнийтермическим способом (конденсация, кристаллизация, спекание) при получении циркониевой губки в производстве циркония методом хлорирования.
НДТ 27. Применение извести (негашеной) для приготовления известкового молока.
НДТ 28. Хлорирование известкового молока анодными газами для получения раствора хлористого кальция.
НДТ 29. Сушка раствора хлористого кальция для получения сухого порошка хлористого кальция.
НДТ 30. Электролиз расплава хлористого кальция для получения медно-кальциевого сплава.
НДТ 31. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание) при получении титанового шлака.
НДТ 32. Процесс плавки и выпуска расплава титанового шлака.
НДТ 33. Сокращение выбросов в процессе приготовления трехкомпонентной титансодержащей шихты (сушка материалов, дробление материалов, помол, перемешивание).
НДТ 34. Подготовка сырья (прием, обработка, хранение, хлорирование) при получении технического тетрахлорида титана в производстве титана губчатого магнийтермическим способом.
НДТ 35. Восстановление титана из тетрахлорида титана магнийтермическим способом (восстановление, дистилляция) при получении титановой губки в производстве титана губчатого магнийтермическим способом.
НДТ 36. Подготовка шихтовых материалов (первичных и вторичных) для производства титановых сплавов (очистка в кислотном растворе, обезжиривание, дробеметная обработка, нагрев, измельчение, навешивание, прессование, сушка).
НДТ 37. Производство титановых слитков (загрузка, плавление в вакуумных печах, выгрузка, охлаждение, шоопирование, обработка).
НДТ 38. Производство титановых изделий и полуфабрикатов (нагрев, ковка, штамповка, отжиг, прокатка, прессование, правка, травление, механическая обработка, резка).
НДТ 39. Получение высокопроцентного ферротитана в индукционных печах (загрузка шихты, плавление, разливка, дробление).
НДТ 40. Обезвоживание обогащенного карналлита во вращающихся печах и печах кипящего слоя.
НДТ 41. Хлорирование обезвоженного искусственного карналлита анодными газами для получения безводного очищенного искусственного карналлита.
НДТ 42. Электролиз расплава обезвоженного карналлита с получением первичного магния.
НДТ 43. Снижение выбросов при рафинировании и литье магния и сплавов.
НДТ 44. Снижение содержания взвешенных веществ в выбросах при производстве теллура с использование одной или нескольких газоочистных установок.
НДТ 45. Хлорирование лопаритового концентрата и пекового кокса с получением технических пентахлоридов ниобия и тантала, пульпы тетрахлорида титана и плава хлоридов РЗМ.
НДТ 46. Разделение технических пентахлоридов ниобия и тантала (ректификацией) с получением индивидуальных пентахлоридов ниобия и тантала.
НДТ 47. Сокращение выбросов в процессе подготовки шихты (сушка материалов, загрузка, перемешивание) и проведение восстановительной плавки ниобия и тантала из пентаоксида ниобия и тантала.
НДТ 48. Предотвращение загрязнения почвы и грунтовых вод, дробления, просеивания и операций классификации.
НДТ 49. Сокращение потребления воды и предотвращение образования сточных вод.
НДТ 50. Предотвращение образования сточных вод.
НДТ 51. Предотвращение загрязнения незагрязненных вод и сокращение сбросов загрязняющих веществ в водные объекты: отделение незагрязненных стоков от других сточных вод, которые требуют очистки.
НДТ 52. Сокращение сбросов загрязняющих веществ со сточными водами.
НДТ 53. Предотвращение образования сточных вод при щелочном выщелачивании: повторное использование воды от кристаллизации раствора соли щелочного металла.
НДТ 54. Сокращение количества отходов, направляемых на захоронение от производства продукции, которая входит в область применения настоящего справочника НДТ.
НДТ 55. Повторное использование или восстановление серной кислоты, полученной от процесса обжига сульфидных концентратов.
НДТ 56. Обработка отходов выщелачивания с целью обеспечения их пригодности для конечной утилизации: их пирометаллургическая обработка в вельц-печи.
НДТ 57. Гранулирование и переработка пылевидного сырья.
НДТ 58. Рецикловые потоки и возврат рафината в технологии прямого извлечения лития AXIONIT DLE.
(обязательное)
Г.1 Краткая характеристика отрасли с точки зрения ресурсо- и энергопотребления
Вопросы использования энергии при оценке НДТ в цветной металлургии в целом и при производстве РМ, а также щелочноземельных металлов в частности, имеют существенное значение. Так, например, существенная доля в общем производстве РМ обеспечивается за счет вторичных ресурсов. Поскольку удельные прямые выбросы плавильных заводов, перерабатывающих лом, в 3 раза ниже, чем выбросы плавильных заводов, работающих на первичном сырье, изготовление РМ из вторичных материалов исключает выбросы десятки тысяч тонн загрязняющих веществ и CO2.
Основным методом повышения энергоэффективности является использование систем энергоменеджмента, описанных в международном стандарте ISO 50001 или национальном стандарте ГОСТ Р ИСО 50001.
Г.2 Основные технологические процессы, связанные с использованием энергии
Утилизация энергии и тепла широко применяется при производстве РМ. Пирометаллургические процессы обжига, агломерации, плавки обычно сопровождаются интенсивным выделением тепла, содержащегося, в частности, в отходящих газах. Поэтому для утилизации тепла используются регенеративные и рекуперативные горелки, теплообменники и котлы. Пар или электроэнергия могут вырабатываться на заводе как для собственного использования, так и для внешних потребителей, например, для муниципальных систем отопления, и для подогрева материалов или газообразного топлива. Технологии, применяемые для рекуперации тепла на различных объектах, могут существенно различаться. Их характеристики зависят от целого ряда факторов, таких как эксергетический КПД, возможные направления использования тепла и электроэнергии на промплощадке или рядом с ней, масштаба производства и способности газов или содержащихся в них компонентов откладываться или осаждаться в теплообменниках.
Ниже приведены примеры методов, которые могут быть использованы для применяемых технологических процессов производства РМ.
Горячие газы, образующиеся при плавке или обжиге сульфидных руд, почти всегда проходят через паровые котлы. Получаемый пар может использоваться для производства электроэнергии или для отопления. Помимо генерации электроэнергии, пар используется в процессе сушки материалов, а остаточное тепло используется для предварительного подогрева воздуха, поступающего для поддержания горения в процессах спекания и плавки.
Использование в горелках обогащенного кислородом воздуха или кислорода сокращает потребление энергии за счет возможности энергоемких процессов обжига и плавки. Объемы отходящих газов существенно сокращаются, что позволяет применять вентиляторы меньших размеров и т.п.
Материал футеровки печи может также влиять на энергетический баланс плавки. Имеются данные о положительном эффекте применения легких огнеупорных материалов, снижающих теплопроводность и нагрев производственного помещения. При этом необходимо сбалансировать получаемые от этого выгоды со сроком службы футеровки, инфильтрацией металлов в футеровку.
Производство серной кислоты из диоксида серы, образующегося на стадиях обжига и плавки, - экзотермический процесс, включающий несколько стадий охлаждения газа.
Важным методом является охлаждение отходящих газов перед подачей в рукавный фильтр, поскольку оно обеспечивает температурную защиту фильтра и допускает более широкий выбор материалов для его изготовления. В некоторых случаях на этой стадии возможна утилизация тепла.
Часто практикуется использование тепла газов или пара для увеличения температуры выщелачивающих растворов. В некоторых случаях часть газового потока может отводиться на скруббер для отдачи тепла в воду, которая затем используется для целей выщелачивания. Охлажденный газ затем возвращается в основной поток для дальнейшей очистки.
Преимущества предварительного нагрева воздуха, подаваемого для поддержания горения, подтверждены многими документами. Если воздух подогревается на 400 °C, рост температуры пламени составляет 200 °C, а если предварительный подогрев составляет 500 °C, температура пламени растет на 300 °C. Такое увеличение температуры пламени обеспечивает более высокую эффективность плавки и сокращение потребления энергии. Имеются сведения о регенеративных горелках, подогревающих подаваемый воздух до 900 °C, что сокращает потребление энергии на 70%. Этот метод хорошо освоен, и достигнутый срок окупаемости составляет менее одного года.
Во многих обстоятельствах предварительная сушка сырья обеспечивает энергосбережение, потому что скрытое тепло, аккумулируемое в образующемся паре, не теряется, кроме того, уменьшается объем газов, следовательно, вентиляторы и газоочистки тоже могут быть меньшими по размеру и потреблять меньше энергии. Горячие газы, улавливаемые над литейными желобами, могут использоваться для поддержания горения.
Поскольку эти методы экономии являются примерами экономии на отдельных компонентах установок, их применение и экономическая эффективность зависят от специфических условий конкретной промышленной площадки и технологического процесса.
Г.3 Уровни потребления
Ниже приведены показатели входных потоков (материальные и энергетические ресурсы) и выходных потоков (товарная продукция, полупродукт, вторичные ресурсы, отходы и т.д.) для различных технологий производства.
Г.3.1. Производство слитков тантала
Таблица Г.1
Наименование технологического процесса: подготовка шихты
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Пентаоксид тантала | 1003,0 | кг | Шихта для восстановительной плавки | 1000,0 | кг |
Электроэнергия | 400 | кВт*ч |
Таблица Г.2
Наименование технологического процесса: восстановительная
плавка
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Шихта | 1220 | кг | Слитки чернового тантала | 1000,0 | кг |
Электроэнергия | 100 | кВт*ч | Отходы (шлак) | 167,6 | кг |
Таблица Г.3
Наименование технологического процесса: извлечение и чистка
слитков, маркирование и взвешивание слитков
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Слитки чернового тантала | 1005,7 | кг | Слитки чернового тантала | 1000,0 | кг |
Электроэнергия | 500 | кВт*ч | Обороты тантала | 5,7 | кг |
Таблица Г.4
Наименование технологического процесса: рафинировочная
плавка тантала
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Черновой тантал | 1595,5 | кг | Слиток тантала | 1000,0 | кг |
Электроэнергия | 100000 | кВт*ч | Обороты тантала | 454,3 | кг |
Конденсат | 10 | т | |||
Производственная вода | 1000 | м3 |
Г.3.2 Производство порошка циркония электролитического
Таблица Г.5
Наименование технологического процесса: получение
фторцирконата калия
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- концентрат цирконовый; | 1,86 | Т | - фторцирконат калия | 3,47 | т |
- обороты циркониевые | 2,4 | Т | Полупродукт: | ||
- пульпа гидроксида циркония | 4,5 | м3 | |||
Материалы: | Отходы: | ||||
- калий хлористый 98%; | 4,64 | Т | - промышленные стоки | 205,6 | м3 |
- мазут топочный; | 1,04 | Т | |||
- кислота кремнефтористоводородная; | 0,586 | Т | |||
- аммиак 25%; | 0,45 | Т | |||
- молоко известковое; | 53,6 | м3 | |||
- кислота фтористоводородная; | 0,964 | Т | |||
- калий кремнефтористый | 2,116 | Т | |||
Энергоресурсы: | |||||
- электроэнергия; | 10460 | кВт*ч | |||
- вода оборотная; | 6376 | м3 | |||
- сжатый воздух; | 18000 | м3 | |||
- вода техническая; | 50 | м3 | |||
- пар; | 69 | Гкал | |||
- конденсат | 97 | Т |
Таблица Г.6
Наименование технологического процесса: получение катодного
осадка циркония методом электролиза, получение порошка
циркония электролитического
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- фторцирконат калия | 4,61 | т | - порошок циркония электролитический | 1 | т |
Полупродукт: | |||||
- обороты циркониевые | 2,7 | т | |||
Материалы: | Отходы: | ||||
- калий хлористый; | 2,45 | т | - фильтровальные полотна; | 0,239 | т |
- соль углеаммонийная; | 0,45 | т | - промышленные стоки | 94 | м3 |
- молоко известковое; | 36 | м3 | |||
- аммиак 25%; | 0,75 | т | |||
- кислота серная; | 0,1 | т | |||
- блок графитовый | 0,239 | т | |||
Энергоресурсы: | |||||
- электроэнергия; | 49000 | кВт*ч | |||
- вода оборотная; | 5233 | м3 | |||
- сжатый воздух; | 18032 | м3 | |||
- вода хозпитьевая; | 50 | м3 | |||
- конденсат; | 3,8 | т | |||
- пар | 4,312 | Гкл |
Г.3.3 Производство слитков ниобия
Таблица Г.7
Наименование технологического процесса: подготовка шихты
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
1. Сырье, материалы: | Продукт: | ||||
- пентаоксид ниобия; | 676,523 | кг | - однородная механическая смесь исходных материалов шихты. | 1000 | кг |
- кальциевые гранулы; литые полуфабрикат; | |||||
- крупка алюминиевая первичная; | 198,896 | кг | |||
- диоксид циркония | 152,896 | кг | |||
2. Энергоресурсы: | |||||
- электроэнергия | 20000 | кВт*ч |
Таблица Г.8
Наименование технологического процесса: проведение
восстановительной плавки и слив шлака
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
1. Сырье, материалы: | Продукт: | ||||
- однородная механическая смесь исходных материалов шихты | 1530 | кг | - расплав чернового ниобия | 1000 | кг |
2. Энергоресурсы: | |||||
- электроэнергия; | 60000 | кВт*ч | |||
- вода техническая; | 300 | м3 | |||
- конденсат | 9,0 | т |
Таблица Г.9
Наименование технологического процесса: извлечение и чистка
слитков. Маркирование и взвешивание слитков
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
1. Сырье, материалы: | Продукт: | ||||
- расплав чернового ниобия | 1115 | Кг | - слитки чернового ниобия. | 1000 | ч/к |
2. Энергоресурсы: | Обороты: | ||||
- электроэнергия | 10000 | кВт*ч | - стружка ниобиевая; | 34,6 | кг |
- возгоны ниобия | 78,540 | кг |
Г.3.4 Производство слитков кальция
Таблица Г.10
Наименование технологического процесса: приготовление
известкового молока
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Известь | 1440,9 | кг | Известковое молоко | 1000,0 | кг |
Электроэнергия | 55,0 | кВт*ч | Пульпа для переработки | 342,5 | кг |
Вода техническая | 0,511 | м3 |
Таблица Г.11
Наименование технологического процесса: получение порошка
кальция хлористого
Входной поток | Значение | Ед. изм. | Выходной | Значение | Ед. изм. |
Известковое молоко | 1111,1 | кг | Порошок кальция хлористого | 1000,0 | кг |
Теплоэнергия (пар) | 0,275 | Гкал | Порошок кальция хлористого (потери) | 31,86 | кг |
Кислота соляная абгазная | 0,791 | Кек известковый | 53,1 | кг | |
Электроэнергия | 1222,59 | кВт*ч | Кек гидратный | 21,24 | кг |
Хлорвоздушная смесь | 30 | мг/м3 |
Таблица Г.12
Наименование технологического процесса: получение
кальциево-медного сплава электролитическим способом
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Порошок кальция хлористого | 1047,7 | кг | Сплав медно-кальциевый | 1000,0 | кг |
Сплав медно-кальциевый (оборот) | 221,7 | кг | Шламы кальциевого производства | 5,4 | кг |
Электроэнергия | 15116,29 | кВт*ч | Хлорвоздушная смесь (направляется на участок получения кальция хлористого) | 30,0 | мг/м3 |
Вода оборотная | 40,5 | м3 | Сплав медно-кальциевый (оборот) | 221,7 | кг |
Таблица Г.13
Наименование технологического процесса: получение кальция
в слитке методом дистилляции
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сплав медно-кальциевый | 1245,4 | кг | Слиток кальция | 1000,0 | кг |
Электроэнергия | 4650,0 | кВт*ч | Сплав медно-кальциевый (оборот) | 221,7 | кг |
Вода оборотная | 110,0 | м3 | Примеси | 23,7 | кг |
Сжатый воздух | 5877,5 | м3 |
Г.3.5 Производство губки циркониевой
Таблица Г.14
Наименование технологического процесса: получение
тетрахлорида циркония технического
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- бадделеитовый порошок; | 0,468 | т | - тетрахлорид циркония технический | 1 | т |
- обороты циркониевые | 0,062 | т | |||
Материалы: | Отходы: | ||||
- калий хлористый; | 0,03 | т | - плав хлоридов; | 0,25 | т |
- углерод технический; | 0,06 | т | - отработанный орошающий раствор с газоочистных установок; | 7,07 | м3 |
- натрий едкий; | 0,05 | т | |||
- хлор жидкий; | 0,65 | т | |||
- сода кальцинированная | 0,29 | т | - твердые обороты (огарок) | 0,003 | т |
Энергоресурсы: | |||||
- электроэнергия; | 2508 | кВт*ч | |||
- вода оборотная; | 0,01 | м3 | |||
- сжатый воздух; | 314 | м3 | |||
- вода техническая; | 8,4 | м3 | |||
- природный газ | 0,149 | тмк |
Таблица Г.15
Наименование технологического процесса: получение
тетрахлорида циркония очищенного (разделение хлоридов
циркония и гафния)
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- тетрахлорид циркония технический; | 1,11 | т | - тетрахлорид циркония очищенный | 1 | т |
- обороты циркониевые | 0,07 | т | Полупродукт: | ||
- гафниевый концентрат | 0,03 | т | |||
Материалы: | Отходы: | ||||
- калий хлористый; | 0,067 | т | - плав хлоридов | 0,17 | т |
- алюминий хлористый | 0,1 | т | |||
Энергоресурсы: | |||||
- электроэнергия; | 5418 | кВт*ч | |||
- вода оборотная; | 101 | м3 | |||
- сжатый воздух | 15,9 | м3 |
Таблица Г.16
Наименование технологического процесса: получение
циркониевой губки
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- тетрахлорид циркония очищенный | 2,79 | т | - губка циркониевая | 1 | т |
Материалы: | Отходы: | - | |||
- магний МГ-90 | 1,05 | т | Обороты: | 0,04 | т |
Энергоресурсы: | - гарнисажная губка; | 0,021 | т | ||
- электроэнергия; | 19351 | кВт*ч | - возгоны губки; | 0,023 | т |
- вода оборотная; | 2209 | м3 | - магний (лом); | 0,49 | т |
- сжатый воздух | 398 | м3 | - хлористый магний | 2,23 | т |
Г.3.6 Производство порошка гафния электролитического
Таблица Г.17
Наименование технологического процесса: получение
гидроксида гафния
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье (полупродукт): | Продукт: | ||||
- азотнокислый раствор гафния с участка экстракции | 7,2 м3 | м3 | - гидроксид гафния | 1000 | кг |
Материалы: | Промышленные стоки | 99,2 | м3 | ||
- натр едкий технический | 1,8 | т | |||
Энергоресурсы: | |||||
- электроэнергия; | 139,7 | кВт*ч | |||
- конденсат; | 92,2 | т | |||
- сжатый воздух | 205,3 | м3 |
Таблица Г.18
Наименование технологического процесса: получение
фторгафната калия
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье (полупродукт): | Продукт: | ||||
- фторгафнат калия. | 1000 | кг | |||
- гидроксид гафния | 1428,8 | кг | Промышленные стоки | 15,6 | м3 |
Материалы: | |||||
- калий хлористый; | 1,5 | т | |||
- кислота фтористо-водородная; | 0,6 | т | |||
- молоко известковое (CaO); | 8,1 | м3 | |||
- аммиак 25% | 0,3 | т | |||
Энергоресурсы: | |||||
- электроэнергия; | 128,2 | кВт*ч | |||
- пар; | 1,8 | Гкал | |||
- конденсат; | 4,8 | т | |||
- сжатый воздух; | 2,3 | м3 | |||
- оборотная вода | 206,7 | м3 |
Таблица Г.19
Наименование технологического процесса: получение катодного
осадка гафния в электролизере, получение электролитического
порошка гафния
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- фторгафнат калия | 4460 | кг | - порошок гафния электролитический. | 1000 | кг |
Обороты гафниевые: | |||||
- твердые; | 680 | кг | |||
- растворы (пульпа) | 19,2 | м3 | |||
Материалы: | Отходы: | ||||
- калий хлористый 98%; | 1,2 | т | - промышленные стоки | 62,6 | м3 |
- аргон жидкий; | 350 | кг | |||
- натрий хлористый; | 800 | кг | |||
- аммиак 25%; | 0,8 | т | |||
- кислота серная техническая; | 0,12 | т | |||
- известковое молоко (CaO); | 28 | м3 | |||
- соль углеаммонийная | 0,45 | т | |||
Энергоресурсы: | |||||
- электроэнергия; | 73000 | кВт*ч | |||
- пар; | 4,5 | Гкал | |||
- конденсат; | 3,8 | т | |||
- сжатый воздух; | 29400 | м3 | |||
- вода оборотная; | 8820 | м3 | |||
- хозпитьевая вода | 50 | м3 |
Г.3.7 Производство оксидов Pr и Nd
Таблица Г.20
Получение пентаоксида Nb и коллективного концентрата РЗЭ
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Крандаллит-монацитовая руда | 150000 - 168000 | т/год | Коллективный концентрат РЗЭ (влажный) | 60000 - 65000 | т/год |
Дизельное топливо | 4800 - 5000 | т/год | Пентаоксид Nb | 10 000 - 15 000 | т/год |
Пар | 800 000 - 900 000 | т/год | Отходы | 1 000 000 - 1 200 000 | т/год |
Электроэнергия | 60 000 - 65 000 | тыс, кВт·ч/год |
Таблица Г.21
Получение оксидов Pr и Nd, оксидов РЗЭ среднетяжелой группы
в коллективном концентрате
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Осадок РЗЭ | 60000 - 65000 | т/год | Оксиды Pr и Nd | 3 000 - 3 500 | т/год |
Пар | 260 000 - 280 000 | т/год | Оксиды РЗЭ среднетяжелой группы в коллективном концентрате | 2 000 - 2 500 | т/год |
Электроэнергия | 85 000 - 90 000 | тыс. кВт·ч/год |
Г.3.8 Производство селена и теллура
Таблица Г.22
Наименование технологического процесса: производство селена
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Электроэнергия | 1078751 | кВт*ч | Селен технический | 184,0 | т |
Пар | 3868 | Гкал | |||
Шлам обезмеженный | 1 743,733 | т. |
Таблица Г.23
Наименование технологического процесса: производство теллура
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Гидроксид теллура | 180000 | кг | Теллур специальной чистоты | 55000 | кг |
Тигли стеклоуглеродные | 480 | шт | |||
Электроэнергия | 882504 | кВт*ч. | |||
Пар | 156 | Гкал | |||
Воздух сжатый | 72108 | м3 | |||
Порошок алюминиевый | 10260 | кг | |||
Натр едкий (в пересчете на 100%) | 138012 | кг | |||
натрий сернистый | 11064 | кг | |||
шлак содистый | 208000 | кг |
Г.3.9 Производство РЗЭ, пентаоксиды и титана губчатого
Таблица Г.24
Наименование технологического процесса: подготовка сырья
Входной поток = | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Пековый кокс кусковой | 1333 | т | Пековый кокс молотый | 1326 | т |
Электроэнергия | 394 | Тыс. кВт·ч |
Таблица Г.25
Наименование технологического процесса: хлорирование
лопаритового концентрата
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Лопаритовый концентрат | 9472 | Т | Технические хлориды | 1529 | т |
Электроэнергия | 16150 | тыс. кВт. ч | Плав хлоридов РЗМ | 2740 | т |
В том числе: | Тетрахлорид титана технический | 8059 | т | ||
Технические хлориды тантала, ниобия | 9597 | тыс. кВт. ч | |||
Плав хлоридов РЗМ | 1012 | тыс. кВт. ч | |||
Тетрахлорид титана технический | 5541 | тыс. кВт. ч |
Таблица Г.26
Наименование технологического процесса: растворение
и карбонизация плава хлоридов РЗМ
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Плав хлоридов РЗМ | 2739 | т | Карбонаты РЗМ | 2629 | т |
Электроэнергия | 1457 | Тыс. кВт·ч |
Таблица Г.27
Наименование технологического процесса: производство
очищенного тетрахлорида титана
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Технический тетрахлорид титана | 7701 | т | Тетрахлорид титана очищенный | 7607 | т |
Электроэнергия | 1445 | Тыс. кВт·ч |
Таблица Г.28
Наименование технологического процесса: производство
губчатого титана
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Тетрахлорид титана очищенный | 7602 | т | Титан губчатый | 1883 | т |
Электроэнергия | 14788 | тыс. кВт·ч |
Таблица Г.29
Наименование технологического процесса: производство
пентахлоридов ниобия технического и тантала технического
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Технические хлориды | 1534 | т | Пентахлорид ниобия технический | 1404 | т |
Электроэнергия | 10890 | тыс. кВт·ч | Пентахлорид тантала технический | 45 | т |
В том числе | |||||
на пентахлорид ниобия | 6903 | тыс. кВт·ч | |||
на пентахлорид тантала | 4077 | тыс. кВт·ч |
Таблица Г.30
Наименование технологического процесса: производство
пентаоксида ниобия
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
пентахлорид ниобия технический | 1343 | т | пентаоксид ниобия | 652 | т |
Электроэнергия | 3594 | Тыс. кВт·ч |
Таблица Г.31
Наименование технологического процесса: Производство
пентаоксида тантала
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Пентахлорид тантала технический | 25,7 | т | Пентаоксид тантала | 24,9 | т |
Электроэнергия | 455,8 | тыс. кВт·ч |
Г.3.10 Производство магния и сплавов
Таблица Г.32
Наименование технологического процесса: обезвоживание
обогащенного карналлита во вращающихся печах и печах
кипящего слоя
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Обогащенный карналлит (содержание 31,8% MgCl2) | 250303 | т | Карналлит обезвоженный | 142375 | т |
Природный газ | 15070 | тмк | |||
Электроэнергия | 16662 | тыс, кВт·ч |
Таблица Г.33
Наименование технологического процесса: хлорирование
расплава обезвоженного карналлита
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Карналлит обезвоженный | 137381 | т | Карналлит безводный | 131824 | т |
Электроэнергия | 57194 | тыс. кВт·ч | - | - | - |
Таблица Г.34
Наименование технологического процесса: электролиз
безводного карналлита
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Безводный карналлит | 131325 | т | Магний-сырец | 17660 | т |
Электроэнергия | 258194 | тыс, кВт·ч | - | - | - |
Таблица Г.35
Наименование технологического процесса: производство
магния и сплавов
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Магний-сырец | 17655 | т | Магний и сплавы | 17421 | - |
Электроэнергия | 8304 | тыс. кВт. час | - | - | - |
Г.3.11 Производство соединений лития по технологии AXIONIT DLE
Таблица Г.36
Наименование технологического процесса: получение
карбоната лития
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- гидроминеральный рассол | 3920 | т | - карбонат лития | 1 | т |
Материалы: | Рафинат (в скважину) | 4091 | т | ||
- техническая вода | 168,9 | м3 | |||
- натр едкий технический | 0,252 | т | Отходы: | ||
- осадок рафината | 0,2 | т | |||
- кислота соляная (35% раствор) | 1,218 | т | - осадок водоподготовки | 0,008 | т |
- карбонат натрия | 1,646 | т | |||
Энергоресурсы: | |||||
- электроэнергия | 8440 | кВт*ч | |||
- пар | 23,51 | т | |||
- вода теплофикационная | 827,3 | т | |||
- вода оборотная | 2414 | м3 |
Таблица Г.37
Наименование технологического процесса: получение
хлорида лития
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- гидроминеральный рассол | 3116 | т | - хлорид лития | 1 | т |
Материалы: | Рафинат (в скважину) | 3249 | т | ||
- техническая вода | 134,3 | м3 | |||
- натр едкий технический | 0,2 | т | Отходы: | ||
- осадок рафината | 0,16 | т | |||
- кислота соляная (35% раствор) | 0,034 | т | - осадок водоподготовки | 0,006 | т |
Энергоресурсы: | |||||
- электроэнергия | 6710 | кВт*ч | |||
- пар | 18,69 | т | |||
- вода теплофикационная | 657,7 | т | |||
- вода оборотная | 1919 | м3 |
Таблица Г.38
Наименование технологического процесса: получение
гидроксида лития
Входной поток | Значение | Ед. изм. | Выходной поток | Значение | Ед. изм. |
Сырье: | Продукт: | ||||
- гидроминеральный рассол | 5517 | т | - гидроксид лития | 1 | т |
Материалы: | - хлороводород | 0,86 | т | ||
- техническая вода | 136,1 | м3 | |||
- натр едкий технический | 0,229 | т | Рафинат (в скважину) | 5652 | т |
- кислота соляная (35% раствор) | 0,081 | т | Отходы: | ||
- осадок рафината | 0,16 | т | |||
Энергоресурсы: | - осадок водоподготовки | 0,006 | т | ||
- электроэнергия | 9210 | кВт*ч | |||
- пар | 33,10 | т | |||
- вода теплофикационная | 1164 | т | |||
- вода оборотная | 2220 | м3 |
Также информация об уровнях потребления сырья, материалов и энергоресурсов при производстве РМ приведена в разделе 3.1.1 справочника (см. таблицы 3.1 - 3.8).
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: имеется в виду таблица 3.13, а не 3.16. |
Информация об уровнях потребления сырья, материалов и энергоресурсов при производстве РМ приведена в разделах 3.2 и 3.2.1 справочника (см. таблицы 3.9 - 3.16).
Г.4 Наилучшие доступные технологии, направленные на повышение энергоэффективности и оптимизацию и сокращение ресурсопотребления
Наилучшие доступные технологии для производства РМ, направленные на повышение энергоэффективности и оптимизацию и сокращение ресурсопотребления, приведены в разделе 5: НДТ 2, НДТ 8, НДТ 45, НДТ 46, НДТ 49, НДТ 50, НДТ 51, НДТ 52, НДТ 53, НДТ 58.
Г.5 Показатели ресурсной и энергетической эффективности
Г.5.1 Производство слитков тантала
ИС МЕГАНОРМ: примечание. Здесь и далее нумерация пунктов дана в соответствии с официальным текстом документа. |
5.1.1 Подготовка шихты (шихта для восстановительной плавки)
Таблица Г.39
Наименование ресурса | Ед. измерения <*> | Значение |
Пентаоксид тантала | т/т | 1,003 |
Электроэнергия | кВт*ч/т | 400 |
5.1.2 Восстановительная плавка (слитки чернового тантала)
Таблица Г.40
Наименование ресурса | Ед. измерения <*> | Значение |
Шихта | т/т | 1,003 |
Электроэнергия | кВт*ч/т | 100 |
5.1.3 Рафинировочная плавка тантала (слиток тантала)
Таблица Г.41
Наименование ресурса | Ед. измерения <*> | Значение |
Черновой тантал | т/т | 1,595 |
Электроэнергия | кВт*ч/т | 100000 |
Конденсат | т/т | 10 |
Производственная вода | м3/т | 1000 |
Г.5.2 Производство порошка циркония электролитического
5.2.1 Получение фторцирконата калия (фторцирконат калия)
Таблица Г.42
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | ||
- бадделеитовый порошок ПБ-0 | т/т (в пересчете на Zr) | 0,8 |
- обороты циркониевые | т/т (в пересчете на Zr) | 0,5 |
Энергоресурсы: | ||
- электроэнергия; | МВтч/т | 10,6 |
- вода оборотная; | м3/т | 6201 |
- сжатый воздух; | м3/т | 22345 |
- пар; | Гкал/т | 67,08 |
- конденсат | т/т | 84,78 |
5.2.2 Получение катодного осадка циркония методом электролиза, получение порошка циркония электролитического (порошок циркония электролитический)
Таблица Г.43
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | ||
- фторцирконат калия | т/т (в пересчете на Zr) | 1,3 |
Энергоресурсы: | ||
- электроэнергия; | МВтч/т | 53,3 |
- вода оборотная; | м3/т | 5139 |
- сжатый воздух; | м3/т | 28549 |
- пар; | Гкал/т | 4,3 |
- конденсат | т/т | 2,4 |
Г.5.3 Производство слитков ниобия
5.3.1 Проведение восстановительной плавки и слив шлака (расплав чернового ниобия)
Таблица Г.44
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | т/т | 1,53 |
- однородная механическая смесь исходных материалов шихты | ||
Энергоресурсы: | ||
- электроэнергия; | кВтч/т | 60000 |
- вода техническая; | м3/т | 300 |
- конденсат | т/т | 9 |
5.3.2 Извлечение и чистка слитков. Маркирование и взвешивание слитков (слитки чернового ниобия)
Таблица Г.45
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | ||
- расплав чернового ниобия | т/т | 1,115 |
Энергоресурсы: | ||
- электроэнергия | кВтч/т | 10000 |
Г.5.4 производство слитков кальция
5.4.1 Получение порошка кальция хлористого (порошок кальция хлористого)
Таблица Г.46
Наименование ресурса | Ед. измерения <*> | Значение |
Известковое молоко | т/т | 1,111 |
Теплоэнергия (пар) | Гкал/т | 0,275 |
Кислота соляная абгазная | т/т | 0,791 |
Электроэнергия | кВт*ч/т | 1222,59 |
5.4.2 Получение кальциево-медного сплава электролитическим способом (сплав медно-кальциевый)
Таблица Г.47
Наименование ресурса | Ед. измерения <*> | Значение |
Порошок кальция хлористого | т/т | 1,047 |
Сплав медно-кальциевый (оборот) | т/т | 0,222 |
Вода оборотная | м3/т | 40,5 |
Электроэнергия | кВт*ч/т | 15116,29 |
5.4.3 Получение кальция в слитке методом дистилляции (слиток кальция)
Таблица Г.48
Наименование ресурса | Ед. измерения <*> | Значение |
Сплав медно-кальциевый | т/т | 1,245 |
Вода оборотная | м3/т | 110 |
Сжатый воздух | м3/т | 5877,5 |
Электроэнергия | кВт*ч/т | 4650 |
Г.5.5 Производство губки циркониевой
5.5.1 Наименование технологического процесса: получение циркониевой губки (губка циркониевая)
Таблица Г.49
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | ||
- тетрахлорид циркония очищенный | т/т | 2,79 |
Материалы: | ||
- магний | т/т | 1,05 |
Энергоресурсы: | ||
- электроэнергия; | кВтч/т | 19351 |
- вода оборотная; | м3/т | 2209 |
- сжатый воздух | м3/т | 398 |
Г.5.6 Производство порошка гафния электролитического
5.6.1 Получение катодного осадка гафния в электролизере, получение электролитического порошка гафния (порошок гафния электролитический)
Таблица Г.50
Наименование ресурса | Ед. измерения <*> | Значение |
Сырье: | ||
- фторгафнат калия | т/т | 4,460 |
Материалы: | т/т | |
- калий хлористый 98%; | т/т | 1,2 |
- аргон жидкий; | т/т | 0,350 |
- натрий хлористый; | т/т | 0,8 |
- аммиак 25%; | т/т | 0,8 |
- кислота серная техническая; | т/т | 0,12 |
- известковое молоко (CaO); | м3/т | 28 |
- соль углеаммонийная | т/т | 0,45 |
Энергоресурсы: | ||
- электроэнергия; | кВтч/т | 73000 |
- вода оборотная; | м3/т | 8820 |
- сжатый воздух; | м3/т | 29400 |
- пар; | Гкал/т | 4,5 |
- конденсат | т/т | 3,8 |
Г.5.7 Производство оксидов Pr и Nd
5.7.1 Получение пентаоксида Nb и коллективного концентрата РЗЭ
Таблица Г.51
Наименование ресурса | Ед. измерения <*> | Значение <*> |
Крандаллит-монацитовая руда | т/т | 2,50 - 2,58 |
11,2 - 15 | ||
Дизельное топливо | т/т | 0,08 |
0,33 - 0,48 | ||
Пар | т/т | 13,33 - 13,85 |
60 - 80 | ||
Электроэнергия | кВт*ч/т | 1 |
4,33 - 6 | ||
5.7.2 Получение оксидов Pr и Nd, оксидов РЗЭ среднетяжелой группы в коллективном концентрате
Таблица Г.52
Наименование ресурса | Ед. измерения <*> | Значение <*> |
Осадок РЗЭ | т/т | 18,57 - 20 |
26 - 30 | ||
Пар | т/т | 80 - 86,67 |
112 - 130 | ||
Электроэнергия | кВт*ч/т | 25,71 - 28,33 |
36 - 42,5 | ||
Г.5.8 Производство селена и теллура
5.8.1 Производство селена (селен технический)
Таблица Г.53
Наименование ресурса | Ед. измерения <*> | Значение |
Шлам обезмеженный | т/т | 9476,81 |
Пар | Гкал/т | 21,02 |
Электроэнергия | кВт*ч/т | 5862,80 |
5.8.2 Производство теллура (теллур специальной чистоты)
Таблица Г.54
Наименование ресурса | Ед. измерения <*> | Значение |
Гидроксид теллура | кг/кг | 3,273 |
Тигли стеклоуглеродные | шт/кг | 0,009 |
Порошок алюминиевый | кг/кг | 0,187 |
Натр едкий (в пересчете на 100%) | кг/кг | 2,509 |
Натрий сернистый | кг/кг | 0,201 |
Шлак содистый | кг/кг | 3,782 |
Пар | Гкал/кг | 0,003 |
Воздух сжатый | м3/кг | 1,311 |
Электроэнергия | кВт*ч/кг | 16,046 |
Г.5.9 Производство титана губчатого
Таблица Г.55
Наименование ресурса | Ед. измерения <*> | Значение |
Тетрахлорид титана очищенный | т/т | 4,04 |
Электроэнергия | тыс. кВт·ч/т | 7,85 |
Г.5.10 Производство магния и сплавов
Таблица Г.56
Наименование ресурса | Ед. измерения <*> | Значение |
Магний-сырец | т/т | 1,01 |
Электроэнергия | тыс. кВт·ч/т | 0,48 |
Г.5.11 Производство соединений лития по технологии AXIONIT DLE
Г.5.11.1 Производство карбоната лития
Таблица Г.57
Наименование ресурса | Ед. измерения <*> | Значение |
Гидроминеральное сырье | т/т | 3 920 |
Техническая вода | м3/т | 168,9 |
Едкий натр (в пересчете на 100%) | т/т | 0,252 |
Кислота соляная (35% р-р) | т/т | 1,218 |
Карбонат натрия | т/т | 1,646 |
Вода оборотная | м3/т | 2 414 |
Пар | т/т | 23,51 |
Вода теплофикационная | т/т | 827,3 |
Электроэнергия | кВт*ч/т | 8440 |
Г.5.11.2 Производство хлорида лития
Таблица Г.58
Наименование ресурса | Ед. измерения <*> | Значение |
Гидроминеральное сырье | т/т | 3116 |
Техническая вода | м3/т | 134,3 |
Едкий натр (в пересчете на 100%) | т/т | 0,200 |
Кислота соляная (35% р-р) | т/т | 0,034 |
Вода оборотная | м3/т | 1 919 |
Пар | т/т | 18,69 |
Вода теплофикационная | т/т | 657,7 |
Электроэнергия | кВт*ч/т | 6710 |
Г.5.11.3 Производство гидроксида лития
Таблица Г.59
Наименование ресурса | Ед. измерения <*> | Значение |
Гидроминеральное сырье | т/т | 5517 |
Техническая вода | м3/т | 136,1 |
Едкий натр (в пересчете на 100%) | т/т | 0,229 |
Кислота соляная (35% р-р) | т/т | 0,081 |
Вода оборотная | м3/т | 2220 |
Пар | т/т | 33,10 |
Вода теплофикационная | т/т | 1164 |
Электроэнергия | кВт*ч/т | 9210 |
ИС МЕГАНОРМ: примечание. Нумерация пунктов дана в соответствии с официальным текстом документа. |
Г.5 Экономические аспекты реализации НДТ, направленные на повышение энергоэффективности и оптимизацию и сокращение ресурсопотребления
Собственный экономический потенциал природоохранных мероприятий, таких как, например, внедрение малоотходных технологий, производство побочной продукции и (или) полезное использование образующихся в основном производственном процессе отходов в российских условиях следует признать скорее незначительным. С одной стороны, природоохранные технологии во многих случаях характеризуются высокой энергоемкостью, а поддержание оборудования в функциональном состоянии требует регулярных затрат на расходные материалы и комплектующие и иных эксплуатационных затрат; в некоторых случаях при производстве побочной продукции, например, такой как серная кислота, значительные издержки могут возникать и в связи с необходимостью хранения и транспортировки агрессивного вещества. С другой стороны, низкая емкость российских рынков не обеспечивает достаточного спроса для вывода побочных производств на экономически эффективный уровень и не сможет гарантировать устойчивое потребление продукции вновь вводимых производственных мощностей, а потенциал выхода на внешние рынки ограничен и малоперспективен с экономической точки зрения.
Таким образом, наибольшим потенциалом с точки зрения возмещения затрат, понесенных в связи с внедрением на предприятии новых природоохранных методов и технологий, обладают комплексные меры, увязывающие экологическую модернизацию производства с перенастройкой производственного процесса в целом, оптимизацией отдельных его звеньев и расширением объемов производства. В этом случае высокие начальные затраты на внедрение интегрированных в производственный процесс природоохранных мер и технологий могут быть в конечном счете возмещены за счет увеличения объемов производимой продукции, повышения эффективности и снижения удельных эксплуатационных расходов. Однако на практике обособление экологической составляющей в рамках таких встроенных в технологический процесс мероприятий на фоне других капитальных и эксплуатационных расходов представляет собой достаточно сложную задачу.
(обязательное)
ИНДИКАТИВНЫЕ ПОКАЗАТЕЛИ УДЕЛЬНЫХ ВЫБРОСОВ ПАРНИКОВЫХ ГАЗОВ
Д.1 Введение
Цель по достижению углеродной нейтральности при устойчивом росте экономики России заявлена в стратегии социально-экономического развития Российской Федерации с низким уровнем выбросов парниковых газов до 2050 года (далее - Стратегия низкоуглеродного развития РФ) [87], подготовленной в рамках указа Президента РФ [88].
В соответствии со Стратегией низкоуглеродного развития РФ прогнозируется два сценария с разными подходами по адаптации российской экономики к глобальному энергопереходу:
1. Инерционный сценарий предусматривает реализацию уже принятых решений по достижению национальных целей и задач отраслевых документов стратегического планирования. Дополнительные меры, прямым или косвенным результатом которых является сокращение выбросов парниковых газов, этим сценарием не рассматриваются.
2. Целевой (интенсивный) сценарий предусматривает дополнительные меры по декарбонизации отраслей экономики и увеличению поглощающей способности управляемых экосистем. Этим сценарием глобальный энергопереход рассматривается как один из факторов обеспечения конкурентоспособности российской экономики в глобальном масштабе.
Реализация целевого (интенсивного) сценария приведет в 2050 г. к сокращению нетто-выбросов парниковых газов на 60% по сравнению с уровнем 2019 г. и на 80% по сравнению с уровнем 1990 г. Это позволит последовательно повышать амбициозность определяемых на национальном уровне вкладов Российской Федерации в реализацию Парижского соглашения (в случае обеспечения соответствия международным стандартам российской системы углеродного регулирования, критериев устойчивых проектов и уровня поглощающей способности управляемых экосистем).
Набор и значения индикаторов реализации Стратегии низкоуглеродного развития РФ ведется с использованием, в т.ч. показателей выбросов парниковых газов, выраженных в млн тонн эквивалента углекислого газа.
Показатели массы выбросов и поглощений парниковых газов в сценариях Стратегии низкоуглеродного развития РФ приведены в таблице Д.1.
Таблица Д.1
(млн тонн эквивалента углекислого газа)
Наименование показателей | Факт - 2019 год | План - 2030 год | План - 2050 год |
Инерционный сценарий | |||
Выбросы парниковых газов | 2119 | 2253 | 2521 |
Поглощения | -535 | -535 | -535 |
Нетто-выбросы | 1584 | 1718 | 1986 |
Целевой (интенсивный) сценарий | |||
Выбросы парниковых газов | 2119 | 2212 | 1830 |
Поглощения | -535 | -539 | -1200 |
Нетто-выбросы | 1584 | 1673 | 630 |
В целях реализации Стратегии низкоуглеродного развития РФ [87] необходимо установить показатели удельных выбросов парниковых газов, которые послужат ориентирами достижения углеродной нейтральности в углеродоемких отраслях промышленности.
Д.2 Краткая характеристика отрасли с точки зрения выбросов парниковых газов
Основными источниками прямых выбросов в производстве редких металлов являются:
- Энергоемкие пирометаллургические процессы. Плавка руд при высоких температурах (часто выше 1000 °C) требует значительного количества энергии. При использовании ископаемого топлива (уголь, природный газ, мазут) в печах напрямую выделяется CO2;
- В процессах восстановления оксидов металлов (например, в производстве ферросплавов редкоземельных металлов) часто применяют кокс, уголь или графит. Реакции восстановления сопровождаются прямым выбросом CO2 и иногда CO.
- Химические реакции при обогащении и переработке руд. При кислотном выщелачивании (например, соляной или серной кислотой) некоторых руд может происходить выделение CO2, если руды содержат карбонатные минералы (кальцит, доломит и др.).
- Электролиз с использованием анодов на основе углерода. В некоторых процессах получения чистых металлов (например, при рафинировании) применяется электролиз с углеродными анодами. При этом углерод анода окисляется с образованием CO2 или CO.
- Обжиг руд и концентратов. На стадии подготовки сырья (например, при обжиге монацита или бастнезита - руд РЗЭ) происходит разложение карбонатов и гидроксидов с выделением CO2 и H2O.
Кроме того, для отрасли характерны косвенные энергетические выбросы парниковых газов, связанные с потреблением электрической и тепловой энергии, производимой на энергетических предприятиях.
Д.3 Индикативные показатели удельных выбросов парниковых газов
Ввиду отсутствия проведенного бенчмаркинга индикативные показатели удельных выбросов парниковых газов для различных производственных процессов редких и редкоземельных сформированы на основе данных из открытых источников.
Индикативные (ориентировочные) показатели удельных выбросов парниковых газов (ПГ) при производстве редких металлов - включая редкоземельные элементы (РЗЭ), литий, кобальт, ниобий, тантал, галлий, индий и др. - варьируются в широких пределах в зависимости от:
- типа металла,
- состава руды,
- технологии переработки (гидрометаллургия/пирометаллургия),
- источника энергии,
- уровня улавливания и переработки отходов.
В Таблицах Д2 - Д6 приведены ориентировочные значения удельных прямых (Scope 1) и общих (Scope 1+2) выбросов CO2 - эквивалента на 1 кг произведенного металла, основанные на данных из научных публикаций, отчетов Международного энергетического агентства (IEA), U.S. DOE, EU JRC, а также отраслевых LCA-исследований.
Таблица Д.2
при производстве РЗМ (Источники: IEA (2021), "The Role
of Critical Minerals in Clean Energy Transitions";
NREL (2022); EU JRC (2020))
Металл/Группа | Удельные выбросы (CO2 - экв./кг металла) | Примечания |
Смешанные РЗЭ (оксиды) | 10 - 40 кг CO2 - экв./кг | Зависит от месторождения (Байань - Обо выше выбросы из-за фосфатов и тория) |
Неодим (Nd) | 25 - 50 кг CO2 - экв./кг | Включая разделение и восстановление |
Диспрозий (Dy) | до 200 кг CO2 - экв./кг | Из-за сложного разделения и низкой концентрации |
Пирометаллургия | 15 - 30 кг CO2 - экв./кг | Прямые выбросы от кокса и печей |
Таблица Д.3
Удельные выбросы парниковых газов производственных процессов
при производстве лития (Источники: U.S. DOE (2023),
"National Blueprint for Lithium Batteries")
Форма | Удельные выбросы | Примечания |
Литий из рассолов (Южная Америка) | 5 - 15 кг CO2 - экв./кг Li2CO3 | В основном Scope 2 (электроэнергия для насосов и испарения) |
Литий из руды (сподумен, Австралия) | 15 - 30 кг CO2 - экв./кг Li2CO3 | Высокая энергоемкость обжига и кислотной обработки |
Металлический литий | 30 - 50 кг CO2 - экв./кг | Электролиз расплавленных солей - энергоемкий |
Таблица Д.4
Удельные выбросы парниковых газов производственных процессов
при производстве кобальта (Источники: U.S. DOE (2023),
"National Blueprint for Lithium Batteries")
Процесс | Удельные выбросы |
Катодный кобальт (рафинированный) | 20 - 40 кг CO2 - экв./кг |
Кобальт из сульфидных руд (Конго и др.) | до 60 кг CO2 - экв./кг при углях в энергосистеме |
Таблица Д.5
Удельные выбросы парниковых газов производственных процессов
при производстве тантала и ниобия
(Источники: U.S. DOE (2023))
Металл | Удельные выбросы |
Тантал (Ta2O5 или металлический) | 30 - 100 кг CO2 - экв./кг |
Ниобий (FeNb сплав) | 5 - 15 кг CO2 - экв./кг |
Таблица Д.6
при производстве галлия и индия (Источники: U.S. DOE (2023))
Металл | Удельные выбросы |
Галлий | 100 - 300 кг CO2 - экв./кг |
Индий | 200 - 500 кг CO2 - экв./кг |
(обязательное)
"ПРОИЗВОДСТВО РЕДКИХ И РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ"
Е.1 Краткое описание области применения НДТ
Настоящий справочник НДТ распространяется на следующие основные виды деятельности:
- процессы производства легких редких металлов;
- процессы производства рассеянных редких металлов;
- процессы производства тугоплавких редких металлов;
- процессы производства редкоземельных металлов;
- процессы производства щелочноземельных металлов (магний и кальций).
Справочник не распространяется на:
- добычу и обогащение руд и продуктов, содержащих редкие металлы
- процессы производства радиоактивных металлов;
- вопросы, которые касаются исключительно обеспечения промышленной безопасности или охраны труда.
Е.2 Перечень наилучших доступных технологий и маркерных веществ
Заключение содержит перечень кратких описаний НДТ, применяемых при производстве редких и редкоземельных металлов на различных этапах технологического процесса.
Технологии/методы, перечисленные и описанные в настоящем документе в качестве наилучших доступных технологий (НДТ), не являются ни предписывающими, ни исчерпывающими. Могут использоваться другие технологии/методы, которые гарантируют, по крайней мере, эквивалентный уровень охраны окружающей среды.
При выборе НДТ необходимо обращать внимание на указанное в заключении по НДТ конкретное производство (передел/установку), для которого должна применяться соответствующая НДТ. Также для каждой НДТ, где необходимо, указаны ограничения применимости включенных в заключение по НДТ методов. Если не указано иное, заключения по НДТ являются общеприменимыми в рамках рассматриваемых видов деятельности.
НДТ общего характера
НДТ 1. Повышение общей результативности природоохранной деятельности.
НДТ 2. Повышение эффективности использования энергии.
НДТ 3. Обеспечение стабильности производственного процесса.
Предотвращение и снижение эмиссий
НДТ 4. Уменьшение неорганизованных выбросов, образующихся при хранении сырья.
НДТ 5. Уменьшение неорганизованных эмиссий, образующихся при обработке и транспортировке сырья.
НДТ 6. Предупреждение или сокращение неорганизованных выбросов.
НДТ 7. Предотвращение или сокращение неорганизованных выбросов от подготовки и предварительной обработки материалов.
НДТ 8. Предотвращение или уменьшение неорганизованных выбросов от загрузки сырья редких металлов до получения огарка или спека.
НДТ 9. Использование мокрой шихты для обжиговой печи.
НДТ 10. Выполнение операций при пониженном давлении при обработке огарка.
НДТ 11. Сокращение неорганизованных выбросов, образующихся при промывке, разделении твердых и жидких фракций и очистке.
НДТ 12. Использование в электролизерах добавок, особенно пенообразующих агентов, в целях уменьшения неорганизованных выбросов паров, образующихся при электроизвлечении.
НДТ 13. Предотвращение выбросов NO, NO2 от пирометаллургических процессов.
НДТ 14. Использование природного газа в качестве топлива при сушке сырья в сушильных башнях в потоке горячих топочных газов.
НДТ 15. Сокращение выбросов в воздух пыли (взвешенных веществ) от подготовки сырья (например, прием, обработка, хранение, измерение, перемешивание, смешивание, сушка, измельчение, просеивание).
НДТ 16. Сокращение выбросов, образующихся при производстве оксидов металлов.
НДТ 17. Сокращение выбросов от загрузки, обжига, плавки и получения огарков и спеков.
НДТ 18. Сокращения выбросов при производстве концентратов (карбонатов) РЗМ.
НДТ 19. Сокращение выбросов органических соединений в атмосферу из сушки исходного материала и процесса обжига, спекания и плавки.
НДТ 20. Сокращение выбросов ПХДД/Ф и ЛОС в воздухе при комбинированных технологиях переработки нетрадиционного сырья редких и элементов.
НДТ 21. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении фторцирконата, фторгафната калия в производстве циркония и гафния методом фторирования.
НДТ 22. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание, сушка) при получении технического тетрахлорида циркония в производстве циркония методом хлорирования.
НДТ 23. Получение порошка циркония и гафния электролитического методом фторирования (дробление катодного осадка, обработка в растворах углеаммонийных солей, флотация порошка, кислотная обработка раствором серной кислоты, сушка порошка) в производстве циркония и гафния.
НДТ 24. Разделение хлоридов циркония и гафния (солевая очистка, ректификация и отгонка, абсорбционная очистка) при получении тетрахлорида циркония очищенного в производстве циркония методом хлорирования.
НДТ 25. Получение катодного осадка циркония и гафния методом электролиза в расплаве солей.
НДТ 26. Восстановление циркония из тетрахлорида циркония магнийтермическим способом (конденсация, кристаллизация, спекание) при получении циркониевой губки в производстве циркония методом хлорирования.
НДТ 27. Применение извести (негашеной) для приготовления известкового молока.
НДТ 28. Хлорирование известкового молока анодными газами для получения раствора хлористого кальция.
НДТ 29. Сушка раствора хлористого кальция для получения сухого порошка хлористого кальция.
НДТ 30. Электролиз расплава хлористого кальция для получения медно-кальциевого сплава.
НДТ 31. Подготовка сырья (прием, обработка, хранение, перемешивание, смешивание) при получении титанового шлака.
НДТ 32. Процесс плавки и выпуска расплава титанового шлака.
НДТ 33. Сокращение выбросов в процессе приготовления трехкомпонентной титансодержащей шихты (сушка материалов, дробление материалов, помол, перемешивание).
НДТ 34. Подготовка сырья (прием, обработка, хранение, хлорирование) при получении технического тетрахлорида титана в производстве титана губчатого магнийтермическим способом.
НДТ 35. Восстановление титана из тетрахлорида титана магнийтермическим способом (восстановление, дистилляция) при получении титановой губки в производстве титана губчатого магнийтермическим способом.
НДТ 36. Подготовка шихтовых материалов (первичных и вторичных) для производства титановых сплавов (очистка в кислотном растворе, обезжиривание, дробеметная обработка, нагрев, измельчение, навешивание, прессование, сушка).
НДТ 37. Производство титановых слитков (загрузка, плавление в вакуумных печах, выгрузка, охлаждение, шоопирование, обработка).
НДТ 38. Производство титановых изделий и полуфабрикатов (нагрев, ковка, штамповка, отжиг, прокатка, прессование, правка, травление, механическая обработка, резка).
НДТ 39. Получение высокопроцентного ферротитана в индукционных печах (загрузка шихты, плавление, разливка, дробление).
НДТ 40. Обезвоживание обогащенного карналлита во вращающихся печах и печах кипящего слоя.
НДТ 41. Хлорирование обезвоженного искусственного карналлита анодными газами для получения безводного очищенного искусственного карналлита.
НДТ 42. Электролиз расплава обезвоженного карналлита с получением первичного магния.
НДТ 43. Снижение выбросов при рафинировании и литье магния и сплавов.
НДТ 44. Снижение содержания взвешенных веществ в выбросах при производстве теллура с использование одной или нескольких газоочистных установок.
НДТ 45. Хлорирование лопаритового концентрата и пекового кокса с получением технических пентахлоридов ниобия и тантала, пульпы тетрахлорида титана и плава хлоридов РЗМ.
НДТ 46. Разделение технических пентахлоридов ниобия и тантала (ректификацией) с получением индивидуальных пентахлоридов ниобия и тантала.
НДТ 47. Сокращение выбросов в процессе подготовки шихты (сушка материалов, загрузка, перемешивание) и проведение восстановительной плавки ниобия и тантала из пентаоксида ниобия и тантала.
НДТ 48. Предотвращение загрязнения почвы и грунтовых вод, дробления, просеивания и операций классификации.
НДТ 49. Сокращение потребления воды и предотвращение образования сточных вод.
НДТ 50. Предотвращение образования сточных вод.
НДТ 51. Предотвращение загрязнения незагрязненных вод и сокращение сбросов загрязняющих веществ в водные объекты: отделение незагрязненных стоков от других сточных вод, которые требуют очистки.
НДТ 52. Сокращение сбросов загрязняющих веществ со сточными водами.
НДТ 53. Предотвращение образования сточных вод при щелочном выщелачивании: повторное использование воды от кристаллизации раствора соли щелочного металла.
НДТ 54. Сокращение количества отходов, направляемых на захоронение от производства продукции, которая входит в область применения настоящего справочника НДТ.
НДТ 55. Повторное использование или восстановление серной кислоты, полученной от процесса обжига сульфидных концентратов.
НДТ 56. Обработка отходов выщелачивания с целью обеспечения их пригодности для конечной утилизации: их пирометаллургическая обработка в вельц-печи.
НДТ 57. Гранулирование и переработка пылевидного сырья.
НДТ 58. Рецикловые потоки и возврат рафината в технологии прямого извлечения лития AXIONIT DLE.
Е.3 Ресурсная и энергетическая эффективность
Вопросы использования энергии при оценке НДТ в цветной металлургии в целом и при производстве РМ, а также щелочноземельных металлов в частности, имеют существенное значение. Так, например, существенная доля в общем производстве РМ обеспечивается за счет вторичных ресурсов. Поскольку удельные прямые выбросы плавильных заводов, перерабатывающих лом, в 3 раза ниже, чем выбросы плавильных заводов, работающих на первичном сырье, изготовление РМ из вторичных материалов исключает выбросы десятки тысяч тонн загрязняющих веществ и CO2.
Основным методом повышения энергоэффективности является использование систем энергоменеджмента, описанных в международном стандарте ISO 50001 или национальном стандарте ГОСТ Р ИСО 50001.
Показатели входных потоков (материальные и энергетические ресурсы) и выходных потоков (товарная продукция, полупродукт, вторичные ресурсы, отходы и т.д.) для различных технологий производства приведены в Приложении Г.
Е.4 Индикативные показатели удельных выбросов парниковых газов
Основными источниками прямых выбросов в производстве редких металлов являются:
- Энергоемкие пирометаллургические процессы. Плавка руд при высоких температурах (часто выше 1000 °C) требует значительного количества энергии. При использовании ископаемого топлива (уголь, природный газ, мазут) в печах напрямую выделяется CO2;
- В процессах восстановления оксидов металлов (например, в производстве ферросплавов редкоземельных металлов) часто применяют кокс, уголь или графит. Реакции восстановления сопровождаются прямым выбросом CO2 и иногда CO.
- Химические реакции при обогащении и переработке руд. При кислотном выщелачивании (например, соляной или серной кислотой) некоторых руд может происходить выделение CO2, если руды содержат карбонатные минералы (кальцит, доломит и др.).
- Электролиз с использованием анодов на основе углерода. В некоторых процессах получения чистых металлов (например, при рафинировании) применяется электролиз с углеродными анодами. При этом углерод анода окисляется с образованием CO2 или CO.
- Обжиг руд и концентратов. На стадии подготовки сырья (например, при обжиге монацита или бастнезита - руд РЗЭ) происходит разложение карбонатов и гидроксидов с выделением CO2 и H2O.
Кроме того, для отрасли характерны косвенные энергетические выбросы парниковых газов, связанные с потреблением электрической и тепловой энергии, производимой на энергетических предприятиях.
[1] Об охране окружающей среды (в ред. от 03 июля 2016 с изм. и доп., вступ. в силу с 01 марта 2017): Федеральный закон от 10 января 2002 N 7-ФЗ.
[2] ГОСТ Р 113.00.03-2019 Наилучшие доступные технологии. Структура информационно-технического справочника. - М., 2019.
[3] ГОСТ Р 113.00.04-2024 Наилучшие доступные технологии. Формат описания технологий. - М., 2024.
[4] ГОСТ Р 113.00.12-2023 Наилучшие доступные технологии. Термины и определения. - М., 2023.
[5] Правила определения технологии в качестве наилучшей доступной технологии, а также разработки, актуализации и опубликования информационно-технических справочников по наилучшим доступным технологиям. Утверждены постановлением Правительства Российской Федерации от 23 декабря 2014 г. N 1458.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: Приказ Минпромторга России от 23.08.2019 имеет номер 3134, а не 665. |
[6] Методические рекомендации по определению технологии в качестве наилучшей доступной технологии. Утверждены приказом Министерства промышленности и торговли Российской Федерации от 23 августа 2019 г. N 665.
[7] О поэтапном графике создания в 2015 - 2017 гг. справочников наилучших доступных технологий: Распоряжение Правительства Российской Федерации от 31 октября 2014 г. N 2178-р.
[8] Рубидий. Свойства химических элементов [Электронный ресурс]. - Режим доступа: http://chem100.ru/elem.php?n=37 (дата обращения: 21.11.2024).
[9] О цезии на сайте Российского нефтяного союза [Электронный ресурс]. - Режим доступа: http://www.centrrns.ru/cvetmet/caesium (дата обращения: 21.11.2024).
[10] Месторождение титана [Электронный ресурс]. - Режим доступа: http://www.cmmarket.ru/markets/tiworld.html (дата обращения: 21.11.2024).
[11] Месторождение титана [Электронный ресурс]. - Режим доступа: http://mining-media.ru/ru/article/ekonomic/559-perspektivy-osvoeniya-titanovogo-syrya-v-rossii (дата обращения: 21.11.2024).
[13] Audi, G., Bersillon, O., Blachot, J., Wapstra, A.H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. - 2003.
[14] Патент N 2838285 C1 Российская Федерация, МПК C01G 39/02, C22B 34/34, C22B 7/00, C22B 3/12, C22B 3/28, B09B 101/95. Способ получения оксида молибдена из отработанных молибден-кобальтовых катализаторов на носителе из оксида алюминия: N 2024118028: заявл. 28.06.2024: опубл. 14.04.2025 / А.М. Абрамов, Ю.Б. Соболь Ж.Н. Галиева; заявитель ООО "ЛИТ"
ИС МЕГАНОРМ: примечание. Здесь и далее нумерация пунктов дана в соответствии с официальным текстом документа. |
[16] Химическая энциклопедия: в 5 т. - М.: Советская энциклопедия, 1995. - Т. 4.
[19] Мохосоев, М.В., Базарова, Ж.Г. Сложные оксиды молибдена и вольфрама с элементами I - IV групп. - М., 1990.
[20] Глинка, Н.Л. Общая химия. - М.: Химия, 1977.
[21] Кременецкий, А. Завод на вулкане / Белоконева О. // Наука и жизнь. - Наука и жизнь. - 2000. - N 11.
[22] Коровин, С.С., Букин, В.И., Федоров, П.И., Резник, А.М. Редкие и рассеянные элементы / под общ. ред. Коровина С.С. // Химия и технология. - М.: МИСИС, 2003.
[23] Химическая энциклопедия: в 5 т. / гл. ред. Зефиров Н.С. - М.: Советская энциклопедия, 1995.
[24] Карелин, В.А., Карелин, А.И. Фторидная технология переработки концентратов редких металлов: монография. - Томск: Изд-во НТЛ, 2004. - 221 с.
[25] Химическая энциклопедия: в 5 т. / гл. ред. Кнунянц И.Л. - М.: Советская энциклопедия, 1988.
[26] Тарасов, А.В. Производство цветных металлов и сплавов: справочник: в 3 т. Производство легких, редких цветных и драгоценных металлов. - М.: ИКЦ "Академкнига", 2007.
[27] Тарасов, А.В. Минеральное сырье, новые технологии и развитие производства тугоплавких редких металлов в России и странах СНГ // Цветные металлы. - 2011. - N 6.
[28] Michael, E. Wieser, Norman Holden, Tyler, B. Coplen, John, K.  , Michael Berglund, Willi A. Brand, Paul De
, Michael Berglund, Willi A. Brand, Paul De  , Manfred
, Manfred  , Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O'Connor, Thomas Walczyk, Shige Yoneda, Xiang-Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. - 2013.
, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O'Connor, Thomas Walczyk, Shige Yoneda, Xiang-Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. - 2013.
 , Michael Berglund, Willi A. Brand, Paul De
, Michael Berglund, Willi A. Brand, Paul De  , Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O'Connor, Thomas Walczyk, Shige Yoneda, Xiang-Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. - 2013.
, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O'Connor, Thomas Walczyk, Shige Yoneda, Xiang-Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. - 2013.[29] Hakobyan, K.Y., Tarasov, A.V., Kovgan, P.A New technology for the treatment of molybdenum sulfide concentrates // Vanced processing of metals and materials. - 2006.
[30] Larry, D. Cunningham. USGS Minerals Information: Niobium (Columbium) and Tantalum. - 2012.
[31] Гедгагов, Э.И., Тарасов, А.В., Гиганов, В.Г., Лунькова, М.А. Разработка инновационной сорбционно-экстракционной технологии получения высокочистых (99,99%) соединений редкоземельных металлов при переработке суммарных концентратов (на примере легкой группы) // Цветные металлы. - 2017. - N 8.
[32] Окунев, А.И., Кирр, Л.Д., Скопов, Г.В. Извлечение германия и других элементов-спутников из пыли медеплавильного производства (к 50-летию со дня внедрения технологии) // Цветные металлы. - 2011. - N 10.
[33] Комплексная технология переработки фосфогипса с получением РЗК и гипсового вяжущего: разработка технологии и оборудования, перспективы освоения производства / А.М. Абрамов, О.И. Волобуев, Ж.Н. Галиева [и др.] // Минерально-сырьевая база металлов высоких технологий. Освоение, воспроизводство, использование: Труды Научно-практической конференции, Москва, 03 - 04 декабря 2019 года - М.: ФГБУ "ВИМС", 2020. - С. 8 - 12.
[34] Разработка универсальной технологии и оборудования для разделения редкоземельных концентратов в каскадах центробежных экстракторов, освоение производства / Ж.Н. Галиева, А.М. Абрамов, Ю.Б. Соболь [и др.] // Химическая промышленность сегодня. - 2019. - N 3. - С. 54 - 60.
[35] Универсальная технология разделения РЗЭ экстракцией в центробежных экстракторах из концентратов, полученных из отечественного минерального сырья: разработка технологии и оборудования, освоение производства, перспективы развития / Ж.Н. Галиева, А.М. Абрамов, Ю.Б. Соболь, В.О. Геря // Разведка и охрана недр. - 2020. - N 3. - С. 56 - 60.
[36] Экстракционное разделение редкоземельных элементов средней группы изомолярными смесями  и
и  из нитратных сред / С.С. Шулин, Ж.Н. Галиева, С.В. Чижевская [и др.] // Неорганические материалы. - 2018. - Т. 54, N 5. - С. 538 - 542. - DOI 10.7868/S0002337X18050160.
из нитратных сред / С.С. Шулин, Ж.Н. Галиева, С.В. Чижевская [и др.] // Неорганические материалы. - 2018. - Т. 54, N 5. - С. 538 - 542. - DOI 10.7868/S0002337X18050160.
 и
и  из нитратных сред / С.С. Шулин, Ж.Н. Галиева, С.В. Чижевская [и др.] // Неорганические материалы. - 2018. - Т. 54, N 5. - С. 538 - 542. - DOI 10.7868/S0002337X18050160.
из нитратных сред / С.С. Шулин, Ж.Н. Галиева, С.В. Чижевская [и др.] // Неорганические материалы. - 2018. - Т. 54, N 5. - С. 538 - 542. - DOI 10.7868/S0002337X18050160.[37] US Geological Survey. Mineral commodity summaries 2025 // US Geological Survey. - 2025. - С. 180 - 181.
[38] Таллий / [Электронный ресурс] // Казцинк: [сайт]. - URL: https://www.kazzinc.com/rus/o-proizvodstve/vidy-produktsii/tallij (дата обращения: 30.07.2025).]
[39] Редкоземельные металлы / А.И. Михайличенко, Е.Б. Михлин, Ю.Б. Патрикеев. - М.: Металлургия, 1987. - 229 с.
[40] Металлургия редкоземельных металлов: учебник для среднего профессионального образования / Е.Г. Поляков, А.В. Нечаев, А.В. Смирнов. - 2-е изд., стер. - Москва: Издательство Юрайт, 2023. - 501 с.
[41] Распоряжение Правительства Российской Федерации от 30 августа 2022 г. N 2473-р.
[42] Распоряжение Правительства Российской Федерации от 11 июля 2024 г. N 1838-р.
[43] Скороваров Д.И., Голобородов В.Н., Ласкорин Б.Н. и др. Способ получения лигатуры Al-Sc. А.с. СССР N 873692 // Открытия, изобр., пром. образцы и товар, знаки. 1983. N 4.
[45] Государственный доклад "О состоянии и использовании минерально-сырьевых ресурсов Российской Федерации в 2023 г. М., ВИМС, 2023.
[46] Химическая энциклопедия в пяти томах. Под ред. И.Л. Кнунянца. Большая российская энциклопедия. 1988 - 1998.
[47] Машковцев Г.А., Быховский Л.З., Онтоева Т.Д. Минеральное сырье для металлов высоких технологий. Разведка и охрана недр. 2020. N 2. С. 10 - 24.
[48] Семенов А.А., Ухов С.А., Вахрин В.В., Ивановских К.В., Беляков М.И., Лизунов А.В., Сафиуллина А.М., Кучеров О.А., Иванец Д.В. Перспективы извлечения германия из альтернативного сырья // Вопросы атомной науки и техники. Серия: Материаловедение и новые материалы. 2024. N 1 (122). С. 101 - 123.
[49] Пироженко К.Ю. Сорбционное извлечение скандия из возвратных растворов скважинного подземного выщелачивания урана. Автореф. дисс. на соиск. уч. степ. к.т.н. М., МИСиС. 2016 г. 26 с.
[50] Weiwei Wang, Yoko Pranolo, Chu Yong Cheng. Metallurgical processes for scandium recovery from various resources: A review. Hydrometallurgy 108 (2011) 100 - 108.
[51] Москвитин В.И., Махов С.В. Способ получения лигатуры алюминий - скандий и флюс для получения лигатуры алюминий - скандий. Межд. Патент WO 03/042418 от 22.05.2003.
[53] Liu Q., Baker P., Zhao H. Titanium sponge production technology in China. InVenkatesh, V. et al. (Eds), Proceedings of the 13th World Conference on Titanium: The Minerals, Metals & Materials Society. 2016. Pp. 177 - 182.
[54] Hudon G, Filippou D. Chapter 4 - Chemical processes for the production of titanium tetrachloride as precursor of titanium metal in Extractive Metallurgy of Titanium Conventional and Recent Advances in Extraction and Production of Titanium Metal, 2020, Pages 47 - 62.
[55] B.W. Jiang, Z.X. Cai, Q.G. Wen, "Comparative Analysis of Several Magnesium Reduction Cell Technologies in Titanium Sponge Production", Light Metals, 9 (2014), 65 - 67.
ИС МЕГАНОРМ: примечание. В официальном тексте документа, видимо, допущена опечатка: один и тот же текст повторяется дважды. |
[56] B.W. Jiang, Z.X. Cai, Q.G. Wen, "Comparative Analysis of Several Magnesium Reduction Cell Technologies in Titanium Sponge Production", Light Metals, 9 (2014), 65 - 67.
[57] Производство соединений скандия при комплексной переработке различных руд / В.В. Шаталов, В.И. Никонов, Л.Г. Соловьева, А.П. Паршин // ВНИИХТ - 50 лет: Юбилей, сб. тр.: 1951 - 2001. - М.: ЦНИИатоминформ, 2001. - С. 307 - 311.
[58] Зеликман, А.Н. Металлургия редких металлов: Учеб. для вузов по / А.Н. Зеликман, Б.Г. Коршунов. - 2 изд., доп. и перераб. - 432 с.
[59] Поляков, Г.Е. Металлургия редкоземельных металлов / Г.Е. Поляков, А.В. Нечаев, А.В. Смирнов - М.: Металлургиздат, 2018. - 732 с.
[60] Процесс извлечения РЗЭ из экстракционной фосфорной кислоты на ОАО "ФосАгро-Череповец" / А.С. Сибилев, С.В. Шестаков, А.Б. Козырев [и др.] // Химическая технология. - 2015. - Т. 16, N 4. - С. 201 - 205.
[61] Патент N 2770118 C1 Российская Федерация, МПК C22B 3/08, C22B 59/00. Способ извлечения редкоземельных металлов из полугидратного фосфогипса: N 2021118567: заявл. 25.06.2021: опубл. 14.04.2022 / Ж.Н. Галиева, А.М. Абрамов, Ю.Б. Соболь [и др.]; заявитель ООО "Скайград Инновации".
[62] Патент N 2802843 C1 Российская Федерация, МПК C22B 59/00, C01F 17/00. Установка для извлечения редкоземельных металлов из фосфогипса и получения гипсового сырья для производства стройматериалов: N 2022134773: заявл. 28.12.2022: опубл. 04.09.2023 / Ж.Н. Галиева, О.И. Волобуев, А.М. Абрамов [и др.]; заявитель ООО "Скайград Инновации".
[63] Патент N 2665512 C1 Российская Федерация, МПК C22B 3/08, C22B 59/00. Способ переработки фосфогипса: N 2017115339: заявл. 02.05.2017: опубл. 30.08.2018 / В.Ю. Кольцов, П.Ю. Новиков, Т.В. Власова [и др.]; заявитель АО "ВНИИХТ".
[64] Патент N 2526907 C1 Российская Федерация, МПК C22B 59/00, C22B 3/08, C22B 3/44. Способ извлечения редкоземельных металлов из фосфогипса: N 2013112469/02: заявл. 20.03.2013: опубл. 27.08.2014 / А.М. Рябинский, А.М. Копылков, А.В. Канцель [и др.]; заявитель ООО "МИЦ-Геосистемы".
[65] Патент N 2458999 C1 Российская Федерация, МПК C22B 59/00, C22B 3/08, C22B 3/24. Способ переработки фосфогипса для производства концентрата редкоземельных элементов (РЗЭ) и гипса: N 2011117233/02: заявл. 28.04.2011: опубл. 20.08.2012 / Э.П. Локшин, О.А. Тареева, В.Т. Калинников; заявитель ИХТРЭМС КНЦ РАН.
[66] Патент N 2663512 C1 Российская Федерация, МПК C22B 59/00, C22B 3/08, C22B 3/24. Способ извлечения редкоземельных элементов из фосфогипса: N 2017141684: заявл. 29.11.2017: опубл. 07.08.2018 / А.В. Нечаев, С.В. Шестаков, А.С. Сибилев, А.В. Смирнов; заявитель ООО "НПК "Русредмет".
[67] Перспективы переработки техногенных отходов производства минеральных удобрений из фосфоритов и апатитов с получением индивидуальных РЗМ / А.М. Абрамов, Ж.Н. Галиева, Ю.Б. Соболь, А.З. Зарганаев // Разведка и охрана недр. - 2022. - N 12. - С. 31 - 40. - DOI 10.53085/0034-026X_2022_12_31.
[68] Исследование возможности эффективного щелочного вскрытия эвдиалитового концентрата с применением механоактивации / О.В. Хохлова, Е.В. Богатырева, П.А. Любахин [и др.] // Вестник РАЕН. - 2015. - Т. 15, N 4. - С. 50 - 52.
[69]. Патент N 2817728 C1 Российская Федерация, МПК C22B 7/00, C22B 59/00, C01F 17/17. Способ переработки вторичного магнитного сырья, содержащего редкоземельные металлы: N 2023122567: заявл. 30.08.2023: опубл. 19.04.2024 / Ж.Н. Галиева, А.А. Семенов, Д.Д. Микрюкова; заявитель ООО "ЛИТ", ООО "ПромТехРециклинг".
[70]. Патент N 2820293 C1 Российская Федерация, МПК B22F 9/02. Способ подготовки шлифотходов производства постоянных магнитов к дальнейшей переработке: N 2023126999: заявл. 20.10.2023: опубл. 03.06.2024 / Ж.Н. Галиева, А.А. Семенов, Д.Д. Микрюкова; заявитель ООО "ЛИТ", ООО "ПромТехРециклинг"
[71] Вольдман, Г.М. Основы экстракционных и ионообменных процессов гидрометаллургии. - М.: Металлургия, 1982. - 376 с.
[72] Кузнецов, Г.И. Центробежные экстракторы ЦЕНТРЭК / Г.И. Кузнецов, А.А. Пушков, А.В. Косогоров. - М.: РХТУ им. Менделеева - 214 с.
[73] Патент N 2693714 C1 Российская Федерация, МПК C22B 59/00, C01F 17/00, C22B 3/38. Способ экстракционного разделения редкоземельных элементов: N 2018146343: заявл. 25.12.2018: опубл. 04.07.2019 / Ж.Н. Галиева, А.М. Абрамов, Ю.Б. Соболь [и др.]; заявитель ООО "ЛИТ".
[74] Косынкин, В.Д. Прошлое и будущее редкоземельного производства в России / В.Д. Косынкин, Ю.М. Трубаков, Г.А. Сарычев // Евразийское Научное Объединение. - 2015. - Т. 1, N 6 (6). - С. 49 - 60.
[75] Косынкин, В.Д. О мировом и российском редкоземельном производстве / В.Д. Косынкин, Ю.М. Трубаков, Г.А. Сарычев // ВНИИХТ - 65 лет: Сб. науч. тр.: 1951 - 2016. - М.: Випресс, 2016. - С. 38 - 55.
[76] Патент N 2319666 C2 Российская Федерация, МПК C01F 17/00. Способ экстракционного разделения редкоземельных элементов: N 2006101608/15: заявл. 23.01.2006: опубл. 20.03.2008 / Т.Т. Федулова, А.К. Селивановский, В.Д. Косынкин [и др.]; заявитель ОАО "ЧМЗ", ФГУП "ВНИИХТ".
[77] Патент N 2693176 C1 Российская Федерация, МПК C01F 17/00, C01B 32/60. Способ получения карбонатов редкоземельных элементов: N 2018147104: заявл. 28.12.2018: опубл. 01.07.2019 / В.О. Геря, Б.А. Быданов, А.В. Алдушкин [и др.]; заявитель ООО "ЛИТ".
[78] Патент N 150234 U1 Российская Федерация, МПК B01D 11/00. Центробежный экстрактор: N 2013146616/05: заявл. 15.09.2014: опубл. 10.02.2015 / А.М. Абрамов, Ю.Б. Соболь, А.А. Ячменев [и др.]; заявитель ООО "САГА-Сервис".
[79] Патент N 2566137 C2 Российская Федерация, МПК B01D 11/04. Центробежный экстрактор: N 2013146615/05: заявл. 22.10.2013: опубл. 20.10.2015 / А.М. Абрамов, Ю.Б. Соболь, А.А. Ячменев [и др.]; заявитель ООО "САГА-Сервис".
[80] Патент N 2832904 C1 Российская Федерация, МПК B01D 11/04. Центробежный экстрактор с позиционированием трубок вывода легкой фазы: N 2023133928: заявл. 19.12.2023: опубл. 09.01.2025 / А.М. Абрамов, Ю.Б. Соболь, Ж.Н. Галиева [и др.]; заявитель ООО "ЛИТ".
[81] Касаткин А.Г. Основные процессы и аппараты химической технологии: Учеб. для вузов. - 10-е изд., стереотипное, доработанное. - М.: ТИД "Альянс", 2004. - 753 с.
[82] Патент N 2623542 C1 Российская Федерация, МПК C22B 59/00, C25C 1/22. Способ электрохимического окисления церия: N 2016133027: заявл. 10.08.2016: опубл. 27.06.2017 / А.М. Абрамов, Ю.Б. Соболь, Ж.Н. Галиева [и др.]; заявитель ООО "ЛИТ".
[83] Патент N 2605751 C1 Российская Федерация, МПК C25B 9/08. Электролизер: N 2015157101/04: заявл. 30.12.2015: опубл. 27.12.2016 / А.М. Абрамов, Ю.Б. Соболь, Ж.Н. Галиева [и др.]; заявитель ООО "ЛИТ".
[85] [Семенов А.А., Цурика А.А., Ухов С.А., Лизунов А.В., Сафиулина А.М., Тананаев И.Г. Тиохлорирование - перспективный метод переработки сырья редких металлов. Научно-технический журнал "Аналитика". 2023. Том 13, N 4. С. 282 - 292.
[86] Семенов А.А., Цурика А.А., Ухов С.А., Лизунов А.В., Сафиуллина А.М., Тананаев И.Г. Тиохлорирование в технологии титана, циркония и гафния. Вопросы атомной науки и техники. Сер.: Материаловедение и новые материалы. 2023, Т. 11, N 1, с. 86 - 110.
[87] Распоряжение Правительства РФ от 29.10.2021 N 3052-р "Об утверждении стратегии социально-экономического развития Российской Федерации с низким уровнем выбросов парниковых газов до 2050 года".
[88] Указ Президента Российской Федерации от 4 ноября 2020 г. N 666 "О сокращении выбросов парниковых газов".