СПРАВКА
Источник публикации
М.: ФГБУ "Институт стандартизации", 2025
Примечание к документу
Документ включен в Перечень международных и региональных (межгосударственных) стандартов, а в случае их отсутствия - национальных (государственных) стандартов, в результате применения которых на добровольной основе обеспечивается соблюдение требований технического регламента Таможенного союза "О безопасности парфюмерно-косметической продукции" (ТР ТС 009/2011) (Решение Коллегии Евразийской экономической комиссии от 22.12.2020 N 177).
Документ вводится в действие с 01.11.2026 с правом досрочного применения.
Название документа
"ГОСТ 34852-2022. Межгосударственный стандарт. Методы испытаний на цитотоксичность. Оценка начальных доз для испытаний на острую пероральную системную токсичность. Серия по испытаниям и оценке N 129"
(введен в действие Приказом Росстандарта от 24.11.2025 N 1468-ст)
"ГОСТ 34852-2022. Межгосударственный стандарт. Методы испытаний на цитотоксичность. Оценка начальных доз для испытаний на острую пероральную системную токсичность. Серия по испытаниям и оценке N 129"
(введен в действие Приказом Росстандарта от 24.11.2025 N 1468-ст)
Содержание
Приказом Федерального
агентства по техническому
регулированию и метрологии
от 24 ноября 2025 г. N 1468-ст
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ НА ЦИТОТОКСИЧНОСТЬ
ОЦЕНКА НАЧАЛЬНЫХ ДОЗ ДЛЯ ИСПЫТАНИЙ
НА ОСТРУЮ ПЕРОРАЛЬНУЮ СИСТЕМНУЮ ТОКСИЧНОСТЬ.
СЕРИЯ ПО ИСПЫТАНИЯМ И ОЦЕНКЕ N 129
Test methods for cytotoxicity. Evaluation of starting
doses for acute oral systemic toxicity tests.
Series on testing and assessment N 129
(ENV/JM/MONO(2010)20,
Guidance document on using cytotoxicity tests to estimate
starting doses for acute oral systemic toxicity tests -
Series on Testing and Assessment N 129, MOD)
ГОСТ 34852-2022
МКС 71.040.10;
Дата введения
1 ноября 2026 года
с правом досрочного применения
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены".
1 РАЗРАБОТАН Республиканским унитарным предприятием "Белорусский государственный институт метрологии" (БелГИМ) на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 5
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации по результатам голосования в АИС МГС (протокол от 16 мая 2022 г. N 151-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Армения | AM | ЗАО "Национальный орган по стандартизации и метрологии" Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узбекское агентство по техническому регулированию |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 24 ноября 2025 г. N 1468-ст межгосударственный стандарт ГОСТ 34852-2022 введен в действие в качестве национального стандарта Российской Федерации с 1 ноября 2026 г. с правом досрочного применения
5 Настоящий стандарт является модифицированным по отношению к международному документу ENV/JM/MONO(2010)20 "Руководство по применению методов испытаний на цитотоксичность для оценки начальных доз при исследовании острой пероральной системной токсичности. Серия по испытаниям и оценке N 129" ("Guidance document on using cytotoxicity tests to estimate starting doses for acute oral systemic toxicity tests - Series on Testing and Assessment N 129", MOD) путем изменения его структуры для приведения в соответствие с правилами, установленными в ГОСТ 1.5-2001 (подразделы 4.2 и 4.3).
Наименование настоящего стандарта изменено относительно наименования указанного международного документа для увязки с наименованиями, принятыми в существующем комплексе межгосударственных стандартов.
В тексте стандарта библиографические ссылки приведены не в порядке возрастания из-за особенностей построения примененного международного документа.
Приложения в настоящем стандарте обозначены согласно требованиям ГОСТ 1.5-2001, так как их обозначения в примененном международном документе противоречат практике межгосударственной стандартизации.
Международный документ разработан Международной организацией экономического сотрудничества и развития (OECD).
Сопоставление структуры настоящего стандарта со структурой указанного международного документа приведено в дополнительном приложении ДА
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
В ходе реализации ряда национальных и международных исследовательских проектов была подтверждена взаимосвязь между цитотоксическими последствиями химического воздействия, доступными для наблюдения в условиях in vitro, и фактами острой летальности, которые могут иметь место при подобном воздействии in vivo. Программа многоцентрового исследования цитотоксичности in vitro (Multicentre Evaluation of In vitro Cytotoxicity - MEIC), запущенная в 1989 г. Скандинавским обществом клеточной токсикологии, на примере испытаний 50 эталонных веществ показала возможность достоверного прогнозирования уровня летальности при острой пероральной токсичности у человека [1]. В основу программы MEIC была положена гипотеза о том, что базовые цитотоксические свойства веществ, обнаруживаемые посредством методов испытаний in vitro, в существенной мере обуславливают развитие токсических проявлений in vivo и что моделирование острой пероральной токсичности in vivo возможно с использованием систем in vitro на основе клеточных культур.
Механистическая основа сходства между смертью подопытного животного и гибелью испытуемого клеточного материала заключается в том, что все клетки, независимо от того, функционируют они как часть организма животного или как часть клеточной культуры, выращенной in vitro, имеют одинаковые клеточные механизмы; например, это касается энергообразования или поддержания целостности клеточной мембраны. Применимость значений IC50, полученных при реализации программы MEIC in vitro для прогнозирования уровня летального воздействия веществ при пероральной токсичности, оценивалась исходя из сведений об уровне летальных концентраций (lethal concentrations - LC) для крови/сыворотки человека (LC), полученных по данным трех различных типов наблюдений, а именно: 1) значений LC при острой токсичности, измеренных в клинических условиях; 2) значений LC при острой токсичности, измеренных посмертно при патолого-анатомическом исследовании; 3) пиковых значений LC, определенных по аппроксимированным кривым изменения значений LC50 для периода времени, следующего за токсическим воздействием. Анализ методом частичных наименьших квадратов показал, что значения IC50, полученные при применении различных методов исследования (в общей сложности до 61), обеспечивают построение достоверных прогнозов по указанным трем наборам данных LC с коэффициентами детерминации (R2) 0,77; 0,76 и 0,83 соответственно [4].
Другой национальной инициативой стало ведение Реестра цитотоксичности (Registry of Cytotoxicity - RC), специализированной базы данных, сформированной центром Германии по документированию и оценке методов испытаний, альтернативных опытам на животных (Zentralstelle zur Erfassung und Bewertung von Ersatz- und  zum Tierversuch - ZEBET), при Федеральном институте по оценке рисков (Bundesinstitut
zum Tierversuch - ZEBET), при Федеральном институте по оценке рисков (Bundesinstitut  Risikobewertung - BfR), в которую включаются значения LD50 при острой пероральной токсичности у грызунов и которая содержит опубликованные значения концентрации IC50 по результатам различных испытаний in vitro на цитотоксичность для 347 веществ [6], [7].
Risikobewertung - BfR), в которую включаются значения LD50 при острой пероральной токсичности у грызунов и которая содержит опубликованные значения концентрации IC50 по результатам различных испытаний in vitro на цитотоксичность для 347 веществ [6], [7].
 zum Tierversuch - ZEBET), при Федеральном институте по оценке рисков (Bundesinstitut
zum Tierversuch - ZEBET), при Федеральном институте по оценке рисков (Bundesinstitut Согласно [6], [7] Хиллом проведены вычисления линейной регрессии с использованием логарифмически преобразованных значений IC50 (в мМ) и логарифмически преобразованных значений LD50 для пероральной токсичности у грызунов (в ммоль/кг) с целью сознания модели построения прогнозов для значений LD50 при острой пероральной токсичности в соответствии с доступными значениями IC50 (R2 = 0,45; p < 0,001 для наклона кривой). Приемлемый интервал прогнозирования для значений LD50 эмпирическим путем был установлен Хиллом [6], [7] как приблизительно половина порядка величины по обе стороны наиболее соответствующей линейной регрессии (т.е. +/- log 5, или +/- 0,699). Данный интервал прогнозирования базировался на восьми опубликованных линейных регрессиях, вычисленных с использованием значений цитотоксичности для клеток млекопитающих IC50 по различным токсическим показателям in vitro в пределах приблизительно восьми порядков величины, а также значений LD50 при пероральной токсичности для крыс, мышей или для крыс и мышей в совокупности. 73% (252/347) веществ, включенных в RC, попадают в указанный интервал.
Данные, полученные BfR-ZEBET, а также при реализации MEIC рассматривались на семинаре, проводившемся в 1996 г., в ходе которого обсуждалось использование данных по цитотоксичности, получаемых in vitro, для установления начальной дозы химических веществ при проведении испытаний на острую пероральную интоксикацию у грызунов и, таким образом, сокращения числа подопытных животных, необходимых для достоверной классификации и маркировки этих веществ [17].
В последующем концепция использования таких данных для определения значений начальной дозы при испытаниях на грызунах в очередной раз обсуждалась в рамках Международного практического семинара по применению методов in vitro для оценки последствий острой системной токсичности, организованного Межведомственным координационным комитетом по валидации альтернативных методов (ICCVAM) при поддержке Национальной программы по токсикологии США (National Toxicology Program - NTP), американского Национального института по изучению санитарного состояния окружающей среды (National Institute of Environmental Health Sciences - NIEHS) и Управления по охране окружающей среды США (US Environmental Protection Agency - EPA), состоявшегося в Арлингтоне, США, в октябре 2000 г. [12]. По итогам мероприятия было принято решение о целесообразности дальнейшего изучения метода.
Центром NTP по оценке альтернативных токсикологических методов (NTP Center for the Evaluation of Alternative Toxicological Methods - NICEATM) было налажено сотрудничество с Европейским центром по валидации альтернативных методов (European Centre for the Validation of Alternative Methods - ECVAM), который является одним из подразделений научно-исследовательского центра при Европейской комиссии, с целью более тщательного анализа применимости реакции цитотоксичности как инструмента для определения начальной дозы химических веществ в рамках исследований уровня летальности при острой пероральной токсичности. NICEATM и ECVAM обеспечили проведение межлабораторных валидационных исследований для оценки двух стандартизованных методов исследования базовой цитотоксичности в условиях in vitro на примере 72 эталонных веществ, для которых имелись достоверные данные, полученные in vivo. Основываясь на результатах исследований, ICCVAM и ECVAM рекомендовали к применению разработанную ранее для целей RC математическую модель регрессии, использующую значения IC50, полученные путем определения базовой цитотоксичности in vitro, для расчета предполагаемого значения LD50, которое может рассматриваться в качестве начальной дозы в методе определения класса острой токсичности (Acute Toxic Class - ATC) [15] или методе "вверх и вниз" (Up-and-Down Procedure - UDP) [14], [18]. Моделирование с использованием эталонных веществ показало, что применение реакций цитотоксичности in vitro для оценки значений LD50, которые будут использоваться в качестве начальной дозы химических веществ, потенциально позволяют сократить необходимое число подопытных животных на величину до 28% при исследовании с веществ, способных вызывать острую пероральную токсичность, и даже до 50% при исследовании веществ, не требующих классификации как опасные.
Валидационные исследования в целях изучения общей эффективности и возможных ограничений применения стандартных испытаний на цитотоксичность при определении значений начальной дозы для испытаний на острую пероральную токсичность проводились NICEATM-ECVAM с использованием 72 веществ, каждому из которых был присвоен соответствующий код, на базе трех различных лабораторий [9]. В качестве объекта испытаний для совместных исследований NICEATM-ECVAM были выбраны фибробласты мыши BALB/c (3T3) и нормальные эпидермальные кератиноциты человека (normal human epidermal keratinocytes - NHK), а в качестве значимого показателя, по которому выполнялась оценка цитотоксической способности того или иного вещества, было принято поглощение клетками нейтрального красного красителя (neutral red uptake - NRU). Соблюдение данных условий было предусмотрено соответствующими рекомендациями, включенными в базовый руководящий документ ICCVAM [13] и подготовленными в отношении обоих методов с учетом воспроизводимых результатов предварительно выполненных работ [13]. По итогам валидационных исследований NICEATM-ECVAM было принято решение рекомендовать указанные методы для повсеместного применения регулирующими органами и учреждениями здравоохранения США перед испытаниями на острую токсичность с использованием крыс [11] <1>. Установлено, что в случае надлежащего применения данных методов для определения начальной дозы исследуемых веществ количество животных для проведения каждого такого испытания может быть сокращено до 50% [9], [10]. Подготовленные рекомендации согласуются с выводами, сделанными независимой международной экспертной группой, в соответствии с заключением которой рассматриваемые методы продемонстрировали уровень надежности и воспроизводимости, достаточный с точки зрения возможности применения их в рамках подхода, основанного на оценке по совокупности имеющихся свидетельств, с целью определения значений начальной дозы для проведения испытаний на острую пероральную интоксикацию [10].
--------------------------------
<1> См. официальные замечания в части применения рекомендаций ICCVAM по адресу: http://iccvam.niehs.nih.gov/methods/acutetox/inv_nru_recommend.htm.
Настоящий стандарт устанавливает методы определения базовой цитотоксичности исследуемых веществ in vitro путем определения поглощения нейтрального красного (NRU) и вычислений с учетом данных, полученных в условиях in vitro, оптимальных значений начальной дозы, которые впоследствии могут быть использованы для проведения исследований острой пероральной системной токсичности in vivo.
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 конфлюэнтность (confluence): Состояние, в котором клетки культуры объединяются с другими клетками этой же культуры, формируя сплошной слой (монослой). Конфлюэнтность определяют как процент покрытия клетками тканевой культуры рабочей поверхности емкости, в которой они выращиваются (например, клеточный монослой имеет конфлюэнтность 80%).
2.2 коэффициент вариации (coefficient of variation): Статистический показатель прецизионности исследования. Значение данной величины выражается в процентах и вычисляется следующим образом: (стандартное отклонение/среднее значение) x 100%.
2.3 коэффициент детерминации (coefficient of determination): Коэффициент, который в линейной регрессии указывает на количественное соотношение дисперсии зависимых значений Y и X. Значение коэффициента может варьироваться от нуля до единицы и обычно обозначается как R2. Так, например, запись R2 = 0,45 означает, что 45% дисперсии Y может быть объяснено дисперсией X, а 45% дисперсии X - дисперсией Y.
2.4 летучесть (volatility): Способность исследуемой химической продукции/вещества испаряться. Общим признаком повышенной летучести веществ в случае применения методов испытаний на основе оценки NRU является расхождение (в процентах) средних значений ОП540 для двух колонок на испытательном планшете (т.е. повышенная летучесть способствует загрязнению колонки, ближайшей к лункам с наибольшей концентрацией исследуемого вещества). Если такое расхождение превышает 15%, можно предположить о повышенной летучести исследуемой химической продукции/вещества, в особенности если снижение значения ОП540 существенно вблизи лунок с максимальной используемой концентрацией вещества. Повышенная летучесть может наблюдаться при проведении испытаний соединений, значение относительной плотности которых составляет меньше единицы.
2.5 оптическая плотность; ОП540 (optical density (OD540)): Поглощающая способность (т.е. результат измерения ОП540) для полученного в ходе испытания показателя NRU окрашенного раствора (колориметрический показатель), измеряемая на длине волны (540 +/- 10) нм с помощью спектрофотометрического микропланшетного ридера относительно пустых лунок в качестве контрольных.
2.6 оценка по совокупности имеющихся свидетельств (weight-of-evidence): Подход, предусматривающий оценивание на основе рассмотрения преимуществ и недостатков имеющейся информации как основу для подготовки заключения, которое не обязательно представляется очевидным, исходя из отдельных полученных данных. При определении начальной дозы следует учитывать как данные, полученные in vitro, так и любые другие существующие данные и информацию, например прогнозные данные согласно модели поиска количественных соотношений "структура - активность" (QSAR), значения LD50 для химически близких веществ, а также другие имеющиеся данные для оценки значения дозы, близкого к фактическому значению LD50.
2.7 поглощение нейтрального красного; NRU (Neutral red uptake (NRU)): Достигаемая концентрация нейтрального красного красителя в лизосомах жизнеспособных клеток. Изменение свойств поверхности клеток или лизосомальных мембран под воздействием токсических агентов повышает уязвимость лизосом, а также приводит к другим деструктивным последствиям, которые постепенно становятся необратимыми. Применение метода испытания на основе оценки NRU позволяет эффективно различать жизнеспособные, поврежденные и погибшие клетки в силу того, что под действием описанных выше процессов происходит снижение способности клеток к поглощению и связыванию нейтрального красного, которое может быть определено как изменение оптической плотности посредством абсорбционной спектрофотометрии.
2.8 растворимость (solubility): Количество исследуемого вещества, которое может быть растворено (или приведено в состояние однородной взвеси) в питательной среде или растворителе. В основу рекомендованного протокола определения растворимости положено соответствующее руководство U. S. EPA [5], которое предусматривает проведение испытаний с целью контроля способности к растворению в определенном растворителе, начиная с относительно высокой концентрации и продолжая с более низкими концентрациями, которые получают путем последовательного добавления растворителя в большем количестве для растворения вещества. Испытания заканчиваются на этапе, когда полученный раствор становится прозрачным, без каких-либо признаков помутнения или осадка.
2.9 регрессия RC (RC regression) [6], [7]: log (LD50) = 0,435 log (IC50) + 0,625; формула для определения значения LD50, выраженного в ммоль/кг (массы тела), с использованием значения IC50, выраженного в мМ. Формула выведена с использованием 347 значений IC50 и LD50 пероральной токсичности (по результатам опытов на 282 крысах и 65 мышах), заимствованных из RC.
2.10 регрессия RC по количеству вещества (в миллимолях) только по данным опытов на крысах (RC rat-only millimole regression): log (LD50) = 0,439 log (IC50) + 0,621; формула для определения значения LD50, выраженного в ммоль/кг (массы тела), с использованием значения IC50, выраженного в мМ. Формула выведена с использованием значений IC50 (в мМ) и LD50 острой пероральной токсичности (в ммоль/кг) по результатам испытаний на крысах для 282 веществ из базы данных RC [6], [7].
2.11 регрессия RC по массе только по данным опытов на крысах (RC rat-only weight regression): log (LD50) = 0,372 log (IC50) + 2,024; формула для определения значения LD50, выраженного в мг/кг (массы тела), с использованием значения IC50, выраженного в мкг/мл. Формула выведена с использованием значений IC50 (в мкг/мл) и LD50 острой пероральной токсичности (в мг/кг) по результатам испытаний на крысах для 282 веществ из базы данных RC [6], [7].
2.12 функция Хилла (Hill function): Значения IC50 определяются в зависимости от получаемого эффекта на концентрацию вещества с применением функции Хилла, которая представляет собой основанную на использовании четырех параметров логико-математическую модель, связывающую концентрацию исследуемого вещества с биологическим ответом (как правило, с сигмоидальной конфигурацией):
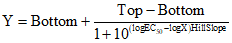 ,
,где Y - это эффект (т.е. сохраняющаяся жизнеспособность, %);
X - концентрация вещества, явившаяся причиной эффекта;
Bottom - минимальный эффект (жизнеспособность - 0%, максимальная токсичность);
Top - максимальный эффект (максимальная жизнеспособность);
EC50 - концентрация вещества при эффекте посередине между значениями Top и Bottom;
HillSlope - параметр, определяющий наклон кривой. Если Top = 100% жизнеспособности, а Bottom = 0% жизнеспособности, то значение EC50 должно совпадать со значением IC50.
2.13 функция Хилла (преобразованная) (Hill function (rearranged)): В некоторых случаях зависимость "доза - эффект" не всегда удовлетворяет функции Хилла. Для достижения соответствия математической модели минимальный эффект (Bottom) в таких случаях может устанавливаться произвольно (т.е. без ограничения его каким-либо конкретным значениям). В то же время, если Bottom /= 0, значение EC50, получаемое в соответствии с функцией Хилла, будет не совпадать со значением IC50, поскольку функция Хилла рассматривает EC50 как точку, расположенную посередине между Top и Bottom. Это означает, что для функции Хилла, применяемой при выполнении расчетов на основе программного обеспечения  с целью получения такого значения концентрации, которое соответствовало бы IC50, должны быть выполнены следующие преобразования:
с целью получения такого значения концентрации, которое соответствовало бы IC50, должны быть выполнены следующие преобразования:
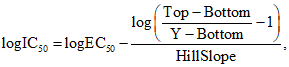
где IC50 - концентрация, соответствующая 50%-ному уровню токсичности;
EC50 - концентрация, обеспечивающая получение эффекта посередине между Top и Bottom;
Top - максимальный эффект (максимальная жизнеспособность);
Bottom - минимальный эффект (жизнеспособность - 0%, максимальная токсичность), Y = 50 (т.е. 50%-ный эффект);
HillSlope - параметр, определяющий наклон кривой эффекта. Значение X в стандартной формуле для функции Хилла в результате преобразования заменяется значением IC50.
2.14 цитотоксичность (cytotoxicity): Неблагоприятные эффекты, обусловленные воздействием на структуры и/или процессы клетки, существенно важные для ее жизнеспособности, пролиферации и/или функционирования. Для большинства видов химической продукции/веществ токсичность является следствием неспецифичного поражения базовых клеточных функций (т.е. митохондрий, целостности цитоплазматической мембраны и т.п.), что может в итоге приводить к нарушению функционирования определенных органов и/или смерти организма. Такие воздействия могут вовлекать в патологический процесс целостность мембран и цитоскелета, клеточный метаболизм, синтез и реакции разложения или выделения клеточных компонентов и продуктов, ионный обмен, а также деление клеток.
2.15 IC50: Концентрация исследуемой химической продукции/вещества, при которой наблюдается 50% снижения измеряемого показателя (т.е. жизнеспособности клеток).
2.16 LD50: Расчетное значение дозы, способной приводить к гибели 50% подопытных животных (крыс и мышей) при введении пероральным путем. Значения LD50 используются в качестве опорных при проведении испытаний in vitro.
3.1 Общая информация
3.1.1 Метод оценки базовой цитотоксичности веществ in vitro по показателю NRU появился благодаря свойству жизнеспособных клеток связывать и удерживать суправитальный краситель - нейтральный красный [2]. Нейтральный красный (NR) обладает слабыми катионными свойствами и легко диффундирует через клеточную мембрану, накапливаясь в лизосомах, где он путем электростатического взаимодействия связывается с их анионной матрицей. Воздействие токсических веществ может изменять поверхность клеток или лизосомальных мембран, что повышает уязвимость лизосом, а также приводит к иным деструктивным последствиям, которые постепенно становятся необратимыми. Такие неблагоприятные эффекты могут выражаться в гибели клеток и/или замедлении их роста, что приводит впоследствии к снижению количества NR, удерживаемого клеточной культурой. С учетом того, что концентрация NR, десорбирующегося клеточной культурой, прямо пропорциональна количеству жизнеспособных клеток в ней, цитотоксичность выражается как зависимое от концентрации снижение потребления NR после химического воздействия. При оценке показателя NRU используют 96-луночный планшет, позволяющий проводить параллельные измерения образцов с восемью различными концентрациями исследуемого вещества.
3.1.2 Данные, полученные при выполнении испытаний in vitro, в дальнейшем могут быть использованы для определения начальной дозы в процессе исследований острой системной пероральной токсичности. Начальная доза in vivo, таким образом, определяется как значение LD50, вычисляемое путем подстановки значения IC50, полученного in vitro, в формулу регрессии, выведенную с учетом сведений о 282 различных веществах, для которых были доступны как значения LD50, установленные по итогам проведенных ранее исследований последствий пероральной токсичности у крыс, так и значения IC50 in vitro из базы данных RC [9]. Для 72 химических веществ, которые стали объектом валидационного исследования NICEATM/ECVAM по определению базовой цитотоксичности in vitro, межлабораторная воспроизводимость показателя IC50, определяемого с использованием усредненного коэффициента вариации, составила 47% для метода на основе оценки NRU с применением клеток 3T3 (далее - метод NRU 3T3) и 28% для метода на основе оценки NRU с применением клеток NHK (далее - метод NRU NHK). Компьютерное моделирование испытаний на острую системную пероральную токсичность при воздействии исследуемых веществ позволило установить, что сокращение испытаний на животных, оцениваемое путем сравнения необходимого количества подопытных животных в случае использования начальной дозы, определяемой по показателю NRU, и количества подопытных животных в случае использования начальной дозы, предлагаемой по умолчанию, остается сопоставимым независимо от конкретного выбранного метода определения начальной дозы: NRU 3T3 или NRU NHK [9]. Валидационные исследования NICEATM-ECVAM [9] - [11] показали, что оба указанных метода пригодны для применения на практике и обеспечивают достижение поставленной цели. Сходство результатов, касающихся сокращения применяемых животных, в методе NRU 3T3 и методе NRU NHK обусловлено общей близостью полученных значений IC50 (а именно 85% (61/72) веществ, использованных для валидационного исследования NICEATM-ECVAM, продемонстрировало значения 3T3 и NHK NRU IC50, относящиеся к одному и тому же порядку величины [9]), а также минимизацией имеющихся различий за счет использования логарифмического уравнения регрессии для вычисления предполагаемого значения LD50.
3.1.3 Заметнее всего такое сокращение проявляется для химической продукции со значением LD50 > 5 000 мг/кг. Благодаря применению цитотоксического подхода для определения начальной дозы количество животных, необходимое для исследований по методу UDP, может быть уменьшено на величину до 50% по сравнению с количеством животных, необходимых при использовании обычно рекомендуемого значения [14]. Такой результат может быть достигнут, если исследование цитотоксичности выполняется до начала других исследований и данные, полученные in vitro, указывают на значение LD50 > 5000 мг/кг. Таким образом, начальная доза при исследовании по методу UDP составит 5000 мг/кг вместо принятых по умолчанию 175 мг/кг и, соответственно, для определения значения LD50 достаточно использования трех подопытных животных вместо шести [8]. В среднем при исследованиях химических веществ с LD50 > 5000 мг/кг необходимое количество подопытных животных сокращается на величину до 22% из расчета на каждое испытание для метода UDP и на величину до 28% из расчета на каждое испытание для метода ATC [15]. Анализ показателей токсичности, проведенный под эгидой Европейского союза, показал, что большинство используемых в промышленной сфере веществ, когда-либо ранее подвергавшихся исследованиям для целей законодательного регулирования, характеризуются значением LD50 > 2000 мг/кг. 87% химической продукции, включенной в базу данных новой химической продукции, которую ведет Институт охраны здоровья и защиты потребителей (Institute for Health and Consumer Protection - IHCP, DG-JRC, Ispra (Италия) (http://ecb.jrc.it)), также демонстрирует значение LD50 > 2000 мг/кг [3]. Несмотря на то что сокращение количества подопытных животных в случае применения метода фиксированной дозы (Fixed Dose Procedure) [16] не оценивалось в рамках валидационного исследования NICEATM-ECVAM, следует полагать, что для такой оценки были бы в полной мере справедливы критерии, приведенные выше.
3.2 Ограничения
3.2.1 Ограничения методов на основе оценки NRU in vitro в большей степени связаны с различиями системного характера, существующими между организмом животного и клеточной культурой. Организм животного и клеточная культура различаются в том, что касается путей поступления токсичного или иного вещества в клетку, их последующего распределения внутри клетки, метаболизма и выделения. После перорального введения в организм животного токсичное вещество усваивается, проходя через его пищеварительный тракт. Токсичное вещество может обладать или не обладать способностью к связыванию с белками сыворотки крови, что, в свою очередь, снижает вероятность его попадания в тот или иной орган-мишень. Оно также может подвергнуться метаболизму еще до того, как попадет в орган-мишень, по пути к органу-мишени и/или сразу после попадания в него, кроме того, оно само или его метаболиты могут быть выведены из организма, прежде чем успеют достигнуть органа-мишени. Как следствие, наиболее чувствительные целевые органы-мишени могут либо вовсе не испытывать воздействия активного метаболита, либо испытывать его воздействие в течение очень ограниченного времени, либо испытывать воздействие очень малых его количеств по сравнению с введенной дозой.
3.2.2 Напротив, при работе с клеточной культурой исследуемое вещество вступает в непосредственный контакт с клетками-мишенями, так что единственным препятствием на его пути становятся собственные мембраны клеток и мембраны внутриклеточных органелл. Клеточные культуры могут содержать или не содержать белки сыворотки крови, что снижает вероятность попадания токсичного вещества к предполагаемому месту его воздействия. Клетки 3T3 и NHK не способны либо лишь в малой степени способны к метаболизации ксенобиотических соединений. Все, что выделяется клетками культуры, остается в питательной среде и, таким образом, может попадать в другие соседние клетки. Как следствие, действие исследуемого вещества на клетки культуры (в отличие от клеток организма животного) может продолжаться в течение всего времени выполнения протокола исследований. Различия организма животного и клеточной культуры также могут заключаться в части мишени, на которую воздействует токсичное вещество. В то время как вещество, обладающее токсичными свойствами, может деструктивным образом воздействовать на определенный орган-мишень in vivo, аналогичный механизм воздействия может не проявляться в культуре клеток, если эти клетки были получены из тканей, значительно отличающихся от тканей органа-мишени. Так, например, не следует ожидать, что вещество, способное нарушать передачу сигнала нейрорецепторами у животных, будет оказывать аналогичное токсическое воздействие на клетки культур 3T3 или NHK. Если, несмотря на это, выраженные токсические проявления все же наблюдаются в подобного рода клеточных культурах, то, вероятно, они являются результатом действия иного механизма или требуют иного соотношения концентрации, чем при испытаниях in vivo.
4.1 Оценка показателя NRU осуществляется в формате "доза - эффект" и необходима для определения такой концентрации вещества, которая приводит к 50%-ному уменьшению значения NRU в сравнении с контрольными пробами (т.е. для определения значения IC50). Полученное значение IC50 используется в формате линейной регрессии для вычисления значения LD50 при пероральном воздействии (дозы, приводящей к летальности 50% подопытных животных), которое, в свою очередь, используется для определения начальной дозы при исследованиях острой системной токсичности при пероральном воздействии с использованием крыс по методу UDP, или методу ATC, или методу FDP.
Такое применение методов испытаний на основе оценки NRU в рамках подхода, предусматривающего оценку по совокупности имеющихся свидетельств, для определения начальных доз при исследованиях острой системной токсичности при пероральном воздействии позволяет сократить число подопытных животных, а в случае с веществами, являющимися относительно токсичными, также сократить число животных, которые могут погибнуть или для которых можно потребовать гуманной эвтаназии вследствие тяжело протекающих последствий токсического воздействия. При определении начальных доз следует учитывать как данные, полученные in vitro, так и любые другие доступные данные и информацию, например полученные согласно модели количественных соотношений "структура - активность" (QSAR), значения LD50 для родственных химических веществ, а также любые другие имеющиеся сведения, использование которых может способствовать установлению значения дозы, близкого к фактическому значению LD50 для соответствующего вещества.
4.2 Протоколы стандартизованных методов испытаний [19] подробно описывают порядок выполнения испытаний, предусматривающих измерение NRU, с использованием культур клеток крысы или человека. Методы определения базовой цитотоксичности путем оценки NRU in vitro предусматривают экспозицию клеточной культуры с добавлением исследуемого вещества в течение 48 ч. По истечении указанного времени исследуемое вещество смывают с клеточного материала, а клетки подвергают инкубированию с нейтральным красным красителем (NR). Концентрацию красителя NR, извлеченного из клеток, определяют посредством спектрофотометрии; [19] описывает методы исследований токсичности веществ на основе оценки NRU с использованием как иммортализованной линии клеток грызунов (3T3), так и первичных клеток человека (NHK). При проведении валидационного исследования было установлено, что использование клеток обоих типов обеспечивает получение аналогичных результатов, тем не менее оценка NRU с применением клеток 3T3 является менее дорогостоящей и затратной по времени, чем оценка NRU с применением клеток NHK. Описаны также методы, которые могут применяться для подготовки и разбавления веществ, подлежащих исследованию по методу на основе оценки NRU in vitro, а также многоэтапные процедуры определения их растворимости с целью выбора наиболее эффективного разбавителя для данных веществ. Поскольку метод с применением клеток NHK требует особого внимания к выбору питательной среды, для клеток культуры в настоящий стандарт включена процедура предварительной оценки пригодности питательных сред (см. приложение А).
Это начальный этап испытаний на цитотоксичность, необходимый для определения начальных доз, применяемых на основном этапе части испытаний. Испытание на основе оценки NRU предполагает использование восьми концентраций исследуемого вещества или положительной контрольной пробы (ПК), получаемых путем экспоненциального разбавления исходного раствора исследуемого вещества таким образом, чтобы охватить достаточно широкий диапазон концентраций (см. 5.7.2, 5.7.3, 5.8.1, 5.8.2, 5.8.3, 5.9.1).
Основной этап испытания на цитотоксичность вещества предназначен для определения соответствующего ему значения IC50 (см. приложение Б). Значение концентрации, ближайшее к значению IC50, установленное на этапе выбора диапазона значений, является центральной точкой для всех остальных значений концентрации, используемых при выполнении основного этапа испытания. По сравнению с этапом выбора диапазона значений на основном этапе испытания используются меньшие значения коэффициента разбавления для испытуемых концентраций (см. 5.9.2).
Клетки
5.2.1 Клеточный материал, относящийся к перевиваемой линии фибробластов мыши, BALB/c 3T3, клон 31, должен быть получен из признанных национальных/международных хранилищ клеточных культур.
5.2.2 Для всех банков клеток и культур клеток, используемых в испытаниях, должно быть подтверждено отсутствие их контаминации микоплазмой или бактериями, а также должен регулярно осуществляться контроль (как в соответствии со специальными протоколами лаборатории, так и согласно стандартным операционным процедурам (СОП)).
Требования СОП подлежат соблюдению лабораториями во всех аспектах, связанных с использованием культур клеток. В повседневной практике для пассирования клеток BALB/c 3T3 следует использовать питательную среду с высоким содержанием глюкозы (4,5 г/л) - модифицированную по способу Дульбекко среду Игла (DMEM) с добавлением 10%-ной не инактивированной нагреванием сыворотки новорожденных телят <1> (NCS) и 4 мМ L-глютамина. Антибиотики должны использоваться в питательной среде, содержащей исследуемое вещество (см. 5.16.2). Правильное приготовление культуральной среды предусматривает корректировку pH (например, путем добавления натрия бикарбоната) и тщательный контроль ее осмотических свойств. Культивирование клеток следует осуществлять при температуре (37 +/- 1) °C, относительной влажности воздуха (90 +/- 10)% и содержании CO2 в воздухе (5,0 +/- 1,0)%. Условия для клеток культуры должны обеспечивать соответствие фактических клеточных циклов временному интервалу, известному по предшествующим наблюдениям за используемой линией клеток. Известная по предыдущим наблюдениям в ходе валидационного исследования NICEATM-ECVAM продолжительность клеточного цикла (времени деления) для линии клеток 3T3 составляет приблизительно 18 ч (среднее значение по данным трех лабораторий) (см. [9] (пункт 2.3.1.1)).
--------------------------------
<1> Допускается также применение телячьей сыворотки [11].
5.4.1 Клетки 3T3, взятые из банка клеток, где они сохраняются в криогенных условиях, нуждаются по меньшей мере в двухкратном пересеве, перед тем как они смогут быть использованы для проведения испытаний по методу на основе оценки NRU. По достижении конфлюэнтности на уровне 50% - 80% клетки подвергают трипсинизации для последующего извлечения из колбы. При пассировании клеток 3T3, хранившихся при низкой температуре, общее число пассажей не должно превышать приблизительно 18 во избежание фенотипических и генотипических изменений, вероятность которых возрастает по мере увеличения возраста культуры.
5.4.2 Клетки, помещенные в питательную среду для повседневных исследований, распределяют по лункам 96-луночного микропланшета для культивирования тканей, соблюдая плотность 2,0 - 3,0 x 10 клеток/100 мкл/лунку. Рекомендуемая схема посева клеток на 96-луночный планшет приведена в приложении В. Период культивации должен составлять (24 +/- 2) ч, что позволяет сформировать в лунках менее чем наполовину (< 50%) конфлюэнтный монослой. Инкубирование в течение указанного времени обеспечивает необходимый выход и плотное соединение клеток для перехода к фазе экспоненциального роста.
Клетки
5.5.1 При испытании на цитотоксичность веществ клетки культуры BALB/c 3T3 могут быть заменены первичными нетрансформированными нормальными эпидермальными кератиноцитами человека (NHK). Клеточный материал NHK должен выращиваться из сохраняемых в криогенных условиях первичных или вторичных пулированных неонатальных клеток крайней плоти человека, приобретаемых исключительно у коммерческих поставщиков, а не получаемых самостоятельно из первичной культуры донорских тканей.
5.5.2 Для всех банков клеток и культур клеток, используемых в исследованиях, должно быть подтверждено отсутствие их контаминации микоплазмой или бактериями, а также должен регулярно осуществляться контроль (как в соответствии со специальными протоколами лаборатории, так и согласно стандартным операционным процедурам (СОП)).
Требования СОП подлежат соблюдению лабораториями во всех аспектах, связанных с использованием культур клеток. В повседневной практике для пассирования клеток NHK следует использовать бессывороточную базальную питательную среду для выращивания кератиноцитов, обогащенную 0,0001 нг/мл рекомбинантного эпидермального фактора роста человека, 5 мкг/мл инсулина, 0.5 мкг/мл гидрокортизона, 30 мкг/мл гентамицина, 15 нг/мл амфотерицина B, 0,10 мМ кальция, а также 30 мкг/мл экстракта гипофиза быка (например,  ,
,  , а также
, а также  ). Инкубирование клеток следует осуществлять при температуре (37 +/- 1) °C, относительной влажности воздуха (90 +/- 10)% и содержании CO2 в воздухе (5,0 +/- 1,0)%. Условия для клеточных культур должны обеспечивать соответствие клеточных циклов временному интервалу, известному по предшествующим наблюдениям за используемой линией клеток. Известная по предыдущим наблюдениям в ходе валидационных исследований NICEATM-ECVAM продолжительность клеточного цикла (времени деления) для клеток NHK составляет приблизительно 19 ч (среднее значение по данным трех лабораторий) (см. [9] (пункт 2.3.1.2)).
). Инкубирование клеток следует осуществлять при температуре (37 +/- 1) °C, относительной влажности воздуха (90 +/- 10)% и содержании CO2 в воздухе (5,0 +/- 1,0)%. Условия для клеточных культур должны обеспечивать соответствие клеточных циклов временному интервалу, известному по предшествующим наблюдениям за используемой линией клеток. Известная по предыдущим наблюдениям в ходе валидационных исследований NICEATM-ECVAM продолжительность клеточного цикла (времени деления) для клеток NHK составляет приблизительно 19 ч (среднее значение по данным трех лабораторий) (см. [9] (пункт 2.3.1.2)).
 ,
,  , а также
, а также  ). Инкубирование клеток следует осуществлять при температуре (37 +/- 1) °C, относительной влажности воздуха (90 +/- 10)% и содержании CO2 в воздухе (5,0 +/- 1,0)%. Условия для клеточных культур должны обеспечивать соответствие клеточных циклов временному интервалу, известному по предшествующим наблюдениям за используемой линией клеток. Известная по предыдущим наблюдениям в ходе валидационных исследований NICEATM-ECVAM продолжительность клеточного цикла (времени деления) для клеток NHK составляет приблизительно 19 ч (среднее значение по данным трех лабораторий) (см. [9] (пункт 2.3.1.2)).
). Инкубирование клеток следует осуществлять при температуре (37 +/- 1) °C, относительной влажности воздуха (90 +/- 10)% и содержании CO2 в воздухе (5,0 +/- 1,0)%. Условия для клеточных культур должны обеспечивать соответствие клеточных циклов временному интервалу, известному по предшествующим наблюдениям за используемой линией клеток. Известная по предыдущим наблюдениям в ходе валидационных исследований NICEATM-ECVAM продолжительность клеточного цикла (времени деления) для клеток NHK составляет приблизительно 19 ч (среднее значение по данным трех лабораторий) (см. [9] (пункт 2.3.1.2)).5.7.1 Клетки NHK (пулированные, из замороженного резерва) размножают в колбах для выращивания тканей с площадью роста 25 см2. После того как достигнута конфлюэнтность от 50% до 80%, клетки перед извлечением из колб подвергают трипсинизации (останавливают трипсинизацию добавлением трипсин-нейтрализующего раствора).
5.7.2 Приготавливают клеточную суспензию в концентрации (1,6 - 2,0) x 104 клеток/мл в питательной среде для NHK, предназначенной для повседневных исследований. Помещают по 125 мкл клеточной суспензии (2,0 - 2,5) x 103 клеток/лунку) в рабочие лунки 96-луночного микропланшета для культивирования тканей. Рекомендуемая схема посева клеток на 96-луночный планшет приведена в приложении В. Помещают по 125 мкл питательной среды для повседневных исследований в периферийные "контрольные" лунки планшета.
5.7.3 Культивируют клетки в течение 48 - 72 ч [температура (37 +/- 1) °C, относительная влажность воздуха (90 +/- 10)%, содержание CO2 в воздухе (5,0 +/- 1,0)%] таким образом, чтобы клетки сформировали монослой, конфлюэнтность которого более чем 20%. Инкубирование в течение этого времени обеспечивает необходимый выход и плотное соединение клеток для перехода к фазе экспоненциального роста.
Приготовление растворов исследуемых веществ
5.8.1 Перед приготовлением растворов и разбавлений исследуемых веществ их выдерживают при комнатной температуре в течение времени, достаточного для достижения температурного равновесия с окружающей средой. Свежие растворы исследуемых веществ приготавливают каждый раз непосредственно перед их использованием. Не следует использовать растворы, оставшиеся от предыдущих испытаний. Растворы должны быть прозрачными, в них не должно быть заметного осадка. Рекомендуется микроскопическая оценка растворов исследуемых веществ, позволяющая визуально оценивать растворимость исследуемого вещества. Общий объем исходного раствора каждого исследуемого вещества должен составлять не менее 1 - 2 мл для обеспечения заполнения всех рабочих лунок одиночного 96-луночного планшета. Приготавливать растворы рекомендуется при красном или желтом освещении, чтобы исключить разложение исследуемых веществ под воздействием света (см. приложение Д).
5.8.2 Предпочтительными растворителями для исследуемых веществ являются используемая питательная среда, а также диметилсульфоксид (ДМСО) и этанол. См. протокол контроля растворимости в приложении Г и соответствующие физико-химические характеристики исследуемых веществ в приложении Д. При приготовлении растворов исследуемых веществ в питательной среде необходимо следовать этапам (уровням) растворимости 1, 2 и 3, описанным в приложении Г. При растворении веществ в ДМСО или этаноле важно следить за тем, чтобы конечная концентрация ДМСО или этанола в растворе, добавляемом к клеткам, не превышала 0,5% (по объему) для контрольных проб (VCs), а также для всех восьми установленных значений концентрации исследуемого вещества. Концентрация ДМСО или этанола должна соответствовать минимальной концентрации, необходимой для растворения исследуемого вещества.
5.8.3 Приготавливают исходный раствор для каждого исследуемого вещества, концентрация которого должна соответствовать максимальной концентрации, установленной по результатам контроля растворимости (см. приложение Г). Максимальная концентрация исследуемого вещества, добавляемого к клеткам на этапе выбора диапазона значений, должна быть следующей:
- 0,5 максимальной концентрации, установленной при контроле растворимости, если вещество растворяется в питательной среде; или
- 1/200 максимальной концентрации, установленной при контроле растворимости, если вещество растворяется в ДМСО или этаноле.
5.9.1 Приведенная схема логарифмического разбавления применима для подготовки исследуемых веществ с целью выбора диапазона значений их дозы (см. 3.1.3).
5.9.2 Растворяют исследуемое вещество в ДМСО или этаноле в концентрации 200 мг/мл для получения исходного раствора (см. рисунок Г.1 (приложение Г)). Приготавливают семь растворов путем последовательного разбавления, каждый раз уменьшая концентрацию вещества на одну логарифмическую единицу (например, 0,1 мл раствора в 0,9 мл растворителя).
5.9.3 Каждое значение концентрации должно в 200 раз превышать соответствующее значение концентрации, используемое при испытании. Разбавляют растворы в соотношении 1:100, добавляя к одной части растворенного исследуемого вещества в каждой пробирке 99 частей питательной среды (например, 0,1 мл раствора исследуемого вещества в ДМСО или этаноле + 9,9 мл среды), чтобы получить восемь значений концентрации 2X для добавления к клеткам. Каждое разбавление с концентрацией 2X исследуемого вещества, таким образом, должно содержать 1% (по объему) растворителя.
5.9.4 Каждая лунка планшета с суспензией клеток 3T3 до добавления в нее раствора исследуемого вещества уже содержит 50 мкл питательной среды для повседневных исследований. Это означает, что при внесении в указанные лунки 50 мкл любого из указанных выше разбавлений 2X исследуемого вещества (например, для получения максимальной требуемой концентрации вещества в лунке 1,000 мкг/мл) объем, в котором разведено вещество, должен увеличиться до 100 мкл, а концентрация использованного растворителя в лунках должна составить 0,5% (по объему).
5.9.5 Каждая лунка планшета с суспензией клеток NHK до добавления в нее раствора исследуемого вещества уже содержит 125 мкл питательной среды для повседневных исследований. Это означает, что при внесении в указанные лунки 125 мкл любого из указанных выше разбавлений 2X исследуемого вещества (например, для получения максимальной требуемой концентрации вещества в лунке 1,000 мкг/мл) объем, в котором разведено вещество, должен увеличиться до 250 мкл, а концентрация растворителя в лунках должна составить 0,5% (по объему).
5.9.6 Следует иметь в виду, что исследуемое вещество, растворенное в питательной среде или в растворителе, может давать осадок при смешении с питательной средой для повседневных исследований.
5.10.1 Коэффициент разбавления при выполнении основного этапа испытания (см. 3.2.1) должен быть меньшим, чем на этапе выбора диапазона значений дозы. Для целей токсикологических исследований рекомендуются и применяются последовательные разбавления, выполняемые в геометрической прогрессии со знаменателем, равным корню n-степени из 10, преимуществом которых является возможность легкого сопоставления результатов независимых экспериментов с большими или малыми коэффициентами благодаря тому, что они представляют идентичные значения концентрации. Так, использование коэффициента 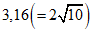 обеспечивает два эквивалентных шага разбавления,
обеспечивает два эквивалентных шага разбавления, 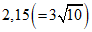 - три,
- три, 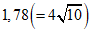 - четыре,
- четыре, 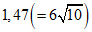 - шесть, а
- шесть, а 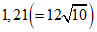 - 12 шагов соответственно (см. таблицу 1). С учетом погрешностей дозирования 1,21 - это наименьшее значение коэффициента прогрессии, которое может быть применено на практике. Например, для того чтобы приготовить серию разбавлений с коэффициентом 1,47, к 1 части раствора (по объему) с максимальной концентрацией вещества добавляют 0,47 части (по объему) разбавителя. После достижения состояния равновесия к 1 части (по объему) данного раствора добавляют следующие 0,47 части (по объему) разбавителя и т.д. [13].
- 12 шагов соответственно (см. таблицу 1). С учетом погрешностей дозирования 1,21 - это наименьшее значение коэффициента прогрессии, которое может быть применено на практике. Например, для того чтобы приготовить серию разбавлений с коэффициентом 1,47, к 1 части раствора (по объему) с максимальной концентрацией вещества добавляют 0,47 части (по объему) разбавителя. После достижения состояния равновесия к 1 части (по объему) данного раствора добавляют следующие 0,47 части (по объему) разбавителя и т.д. [13].
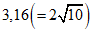 обеспечивает два эквивалентных шага разбавления,
обеспечивает два эквивалентных шага разбавления, 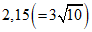 - три,
- три, 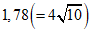 - четыре,
- четыре, 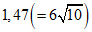 - шесть, а
- шесть, а 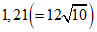 - 12 шагов соответственно (см. таблицу 1). С учетом погрешностей дозирования 1,21 - это наименьшее значение коэффициента прогрессии, которое может быть применено на практике. Например, для того чтобы приготовить серию разбавлений с коэффициентом 1,47, к 1 части раствора (по объему) с максимальной концентрацией вещества добавляют 0,47 части (по объему) разбавителя. После достижения состояния равновесия к 1 части (по объему) данного раствора добавляют следующие 0,47 части (по объему) разбавителя и т.д. [13].
- 12 шагов соответственно (см. таблицу 1). С учетом погрешностей дозирования 1,21 - это наименьшее значение коэффициента прогрессии, которое может быть применено на практике. Например, для того чтобы приготовить серию разбавлений с коэффициентом 1,47, к 1 части раствора (по объему) с максимальной концентрацией вещества добавляют 0,47 части (по объему) разбавителя. После достижения состояния равновесия к 1 части (по объему) данного раствора добавляют следующие 0,47 части (по объему) разбавителя и т.д. [13].Таблица 1
Максимальные дозы исследуемых веществ, подготовленных
с использованием питательной среды для повседневных
исследований, для основного этапа испытания
Количество последовательных разбавлений (коэффициент разбавления) | Единицы концентрации <1> | |||||||||||||||||
2 (3,16) | 10, 31,6, 100 | |||||||||||||||||
3 (2,15) | 10, 21,5, 46,4, 100 | |||||||||||||||||
4 (1,78) | 10, 17,8, 31,7, 56,4, 100 | |||||||||||||||||
6 (1,47) | 10, 14,7, 21,5, 31,6, 46,4, 68,1, 100 | |||||||||||||||||
12 (1,21) | 10, 12,1, 14,7, 17,8, 21,5, 26,1, 31,6, 38,3, 46,4, 56,2, 68,1, 82,5, 100 | |||||||||||||||||
Растворение исследуемых веществ в питательной среде
5.10.2 Максимальное значение концентрации исследуемого вещества в исходном растворе в питательной среде для проведения основного этапа испытания должно соответствовать 100 мг/мл либо максимальной растворимой дозе, деленной на 2. Если на этапе выбора диапазона значений дозы (см. 5.13.1) признаки, указывающие на наличие цитотоксичности, были минимальными или отсутствовали, максимальное значение дозы для проведения основного этапа испытания определяют следующим образом:
a) Навеску исследуемого вещества помещают в стеклянную пробирку (стекло является предпочтительным материалом, однако использование пробирок из полистирола также допускается) и добавляют питательную среду, предназначенную для повседневных исследований, в количестве, необходимом для получения концентрации, равной 200 мг/мл. Если при использовании раствора с концентрацией 200 мг/мл для выбора диапазона значений дозы не выявляются признаки цитотоксичности, для проведения основного этапа испытания может быть приготовлен исходный раствор с концентрацией 500 мг/мл. Перемешивают раствор способом, которым удалось добиться растворения вещества при проведении контроля растворимости (см. приложение Г).
b) Если вещество полностью растворилось в питательной среде, то последовательно приготавливают семь дополнительных растворов для дозирования на основе исходного раствора 2X с концентрацией 200 мг/мл (или с более высокой концентрацией).
c) Если исследуемое вещество является нерастворимым в питательной среде при концентрации 200 мг/мл, продолжают небольшими увеличивающимися порциями добавлять питательную среду для растворения вещества, используя последовательность процедур, описанных в приложении Г. Если в разбавлениях, полученных на основе 2X, образуется осадок, испытание продолжают и надлежащим образом регистрируют и документируют соответствующие наблюдения. Более радикальные меры по обеспечению растворимости вещества могут при необходимости предприниматься с учетом результатов, полученных на этапе выбора диапазона доз.
d) Используют раствор с наибольшей концентрацией растворенного вещества в качестве исходного для последовательного приготовления из него семи дополнительных растворов для дозирования.
Максимальные дозы исследуемых веществ, подготовленных с использованием ДМСО или этанола, при проведении основного этапа испытания
5.10.3 Если при использовании раствора с концентрацией 200 мг/мл для выбора диапазона значений дозы не выявляются признаки цитотоксичности, для проведения основного этапа испытания может быть приготовлен исходный раствор с концентрацией 500 мг/мл. Максимальную концентрацию вещества для основного этапа испытания можно определить, исходя из максимальной концентрации ДМСО или этанола, которая может быть добавлена к питательной среде, при которой не проявляется цитотоксичность (т.е. 0,5% об.). Это означает, что наибольшая концентрация исследуемого вещества в растворе, добавляемом к клеткам на этапе выполнения основного этапа испытания, должна быть <= 2,5 мг/мл в зависимости от их максимальной растворимости в соответствующем растворителе.
a) Навеску исследуемого вещества помещают в стеклянную пробирку и добавляют соответствующий растворитель (выбор растворителя осуществляется по результатам предварительного контроля растворимости (см. приложение Г)) в количестве, необходимом для получения раствора с концентрацией 500 мг/мл. Перемешивают раствор исследуемого вещества с применением последовательности процедур, описанной в приложении Г. Если достигнута полная растворимость в растворителе, последовательно приготавливают семь дополнительных растворов для дозирования из исходного раствора 200X с концентрацией 500 мг/мл.
b) Если исследуемое вещество является нерастворимым в растворителе при концентрации 500 мг/мл, продолжают небольшими увеличивающимися порциями добавлять растворитель для растворения вещества, снова используя последовательность процедур перемешивания, описанную в приложении Г.
c) Используют раствор с наибольшей концентрацией растворенного вещества в качестве исходного для последовательного приготовления из него семи дополнительных растворов для дозирования. Если в разбавлениях, полученных на основе 2X, образуется осадок, испытание продолжают и надлежащим образом регистрируют и документируют соответствующие наблюдения.
Концентрации исследуемого вещества
Контрольные пробы
5.11.1 Положительная контрольная проба (ПК): натрия лаурилсульфат (CASRN 151-21-3) <1>. Подготавливают отдельный 96-луночный планшет с раствором ПК в восьми разных концентрациях, обеспечивающих построение полноценной кривой "доза - эффект" вместо получения точечных значений. Использование данного планшета может быть полезно для выявления и устранения проблем, которые могут возникнуть при проведении испытания (см. приложение Д). Наличие одного планшета, содержащего ПК, считается достаточным для работы с несколькими планшетами, которые содержат исследуемые вещества. Планшет, содержащий ПК, подвергают тем же операциями в том же порядке, что и планшеты, содержащие исследуемые вещества.
--------------------------------
<1> В качестве положительной пробы могут использоваться другие вещества в том случае, если их цитотоксическое воздействие хорошо изучено и подробно описано, а также результаты всех подобных испытаний укладываются в диапазон значений IC50, полученных лабораторией по итогам предшествующих наблюдений (см. [11] (пункт 3.1.3)).
5.11.2 Контрольная проба вещества-носителя (VC): проба VC представляет собой питательную среду для повседневных исследований, если исследуемые вещества растворяются в питательной среде. Для исследуемых веществ, растворяемых с использованием ДМСО или этанола, VC должна состоять из питательной среды для повседневных исследований с таким же содержанием в ней растворителя (0,5% об.), который вносится в лунки 96-луночных планшетов.
Выбор диапазона значений дозы
Вещества исследуют при восьми значениях концентрации их в растворах (см. 5.10.1), получаемых логарифмическим разбавлением исходного раствора (например, 1:10, 1:100, 1:1 000). Если при выборе диапазона значений дозы не получены объективные доказательства цитотоксичности, позволяющие вычислить значение IC50, следует повторить испытание с использованием более высоких доз исследуемого вещества. Если определение цитотоксичности вещества ограничивается его растворимостью, следует предпринять другие действия по обеспечению растворимости вещества для повышения концентрации приготавливаемого исходного раствора (см. приложение Г).
5.13.1 Используют значение IC50, полученное на этапе выбора доз, в качестве среднего значения диапазона концентрации, увеличивают и уменьшают степень разведений на одинаковую величину. Альтернативно в качестве такого среднего значения может быть выбрано имеющееся значение концентрации исследуемого вещества, ближайшее к значению IC50, установленному на этапе выбора доз.
5.13.2 Для получения последовательных значений концентрации на этапе выполнения основного этапа испытания используют меньший коэффициент разбавления, чем при выборе диапазона значений доз (например, коэффициент 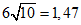 ). Для аппроксимации значений коэффициента разбавления можно ориентироваться на наклон кривой "концентрация - эффект", построенной на этапе выбора доз.
). Для аппроксимации значений коэффициента разбавления можно ориентироваться на наклон кривой "концентрация - эффект", построенной на этапе выбора доз.
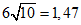 ). Для аппроксимации значений коэффициента разбавления можно ориентироваться на наклон кривой "концентрация - эффект", построенной на этапе выбора доз.
). Для аппроксимации значений коэффициента разбавления можно ориентироваться на наклон кривой "концентрация - эффект", построенной на этапе выбора доз.5.13.3 Испытание должно охватывать весь диапазон значений концентрации, заданный относительно IC50 (> 0%- и < 100%-ного воздействия), предпочтительно несколько точек с постепенно изменяющимся эффектом, но не менее двух точек по обе стороны от значения IC50; при этом следует избегать слишком большого (например, > 6) числа значений концентрации ближе к пределам рассматриваемого диапазона концентраций.
5.13.4 Выполняют не менее двух раз основной этап испытания для каждого вещества и усредняют полученные значения IC50.
День 1
5.14.1 Приготавливают клеточную суспензию и распределяют ее по лункам планшета (см. 5.4.2).
День 2
5.14.2 По истечении периода инкубирования отделяют от клеток и удаляют с планшета питательную среду для повседневных исследований, осторожно переворачивая для этого планшет. Аккуратно промокают планшет стерильной бумажной салфеткой для удаления остатков питательной среды. Добавляют 50 мкл раствора исследуемого вещества в среде для разбавления (DMEM без сыворотки, 4 мМ L-глютамина, 200 МЕ/мл пенициллина, 200 мкг/мл стрептомицина) в опытные лунки и соответствующие контрольные лунки. Добавляют 50 мкл среды для разбавления в лунки, предназначенные для VC, и соответствующие контрольные лунки. Рекомендуемая схема посева клеток на 96-луночный планшет приведена в приложении В. Инкубируют клетки в течение (48 +/- 0,5) ч.
День 4
Микроскопическое наблюдение
5.14.3 По истечении не менее 46 ч воздействия изучают каждый планшет с помощью фазово-контрастного микроскопа для выявления систематических погрешностей посева клеток и оценки показателей роста контрольных клеток и клеток, подвергшихся обработке. Регистрируют все изменения в морфологии клеток, обусловленные цитотоксическим воздействием исследуемого вещества, используют данные результаты в качестве количественных показателей цитотоксичности. Сомнительные показатели роста контрольных клеток могут указывать на ошибки, допущенные при проведении эксперимента, и являться основанием для исключения образца для количественных определений. Проводят испытание по методу на основе оценки NRU (см. 5.16.1 - 5.16.6).
День 1
День 3
5.15.2 По истечении периода инкубирования питательную среду для повседневных исследований NHK с рабочего планшета не удаляют. Добавляют по 125 мкл раствора исследуемого вещества в заданной концентрации в питательной среде для повседневных исследований (см. 5.8.3) в соответствующие лунки планшета. Инкубируют клетки в течение (48 +/- 0,5) ч.
День 5
Микроскопическое наблюдение
5.15.3 Микроскопическое исследование клеток NHK выполняют в соответствии с указаниями, приведенными в 5.14.3 для клеток 3T3.
5.16.1 Для клеток обоих видов: после инкубирования планшет осторожно переворачивают для удаления из лунок питательной среды и тщательно промывают лунки с клетками предварительно подогретым фосфатным буферным солевым раствором Дульбекко (D-PBS) в количестве из расчета 250 мкл/лунку. Удаляют промывной раствор, перевернув планшет, и промокают досуха бумажными салфетками.
5.16.2 Для клеток 3T3: добавляют 250 мкл раствора нейтрального красного красителя с концентрацией 25 мкг/мл в DMEM с добавлением 5% NCS, 4 мМ L-глютамина, 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина во все лунки планшета (в том числе контрольные) и проводят инкубирование при температуре (37 +/- 1) °C, относительной влажности (90 +/- 10)% и содержании CO2 в воздухе на уровне (5,0 +/- 1,0)% в течение (3,0 +/- 0,1) ч (для продолжения процедуры с использованием клеток 3T3 переходят к 5.16.4).
5.16.3 Для клеток NHK: добавляют 250 мкл раствора красителя NR с концентрацией 33 мкл/мл в питательной среде для повседневных исследований NHK во все лунки планшета (в том числе контрольные) и проводят инкубирование при температуре (37 +/- 1) °C, относительной влажности (90 +/- 10)% и содержании CO2 в воздухе на уровне (5,0 +/- 1,0% в течение (3,0 +/- 0,1) ч (для продолжения процедуры с использованием клеток NHK переходят к 5.16.4).
5.16.4 После инкубирования удаляют с планшета питательную среду, содержащую NR, и тщательно промывают лунки предварительно подогретым D-PBS в количестве из расчета 250 мкл/лунку. Удаляют раствор из лунок, как указано выше. Добавляют по 100 мкл раствора для десорбции NR (свежеприготовленного из 49 частей воды + 50 частей этанола + 1 части ледяной уксусной кислоты) во все лунки (в том числе контрольные) для экстрагирования красителя.
5.16.5 Планшеты интенсивно встряхивают в шейкере для микропланшетов в течение 20 - 45 мин. В процессе обработки содержимое планшетов должно быть защищено от воздействия света. После извлечения планшетов из шейкера/миксера они должны отстояться в течение не менее пяти минут. Перед тем как приступить к анализу содержимого планшета, необходимо позаботиться о том, чтобы в нем не оставалось пузырьков.
5.16.6 Измеряют световое поглощение (оптическую плотность, ОП) по истечении 60 мин после добавления раствора для десорбции NR в каждую лунку на длине волны (540 +/- 10) нм (ОП540) с помощью микропланшетного ридера (спектрофотометра), используя пустые лунки как контрольные. Сохраняют полученные данные в соответствующем электронном формате для последующего изучения.
6.1.1 Применяют биологический/научный подход для определения непригодных для исследования лунок (например, лунок без клеток, лунок с контаминированными культурами, лунок с остатками исследуемого вещества), которые должны быть исключены из дальнейшего анализа.
6.1.2 После вычитания значения ОП540 холостых лунок вычисляют показатель жизнеспособности клеток для каждой лунки с исследуемым веществом как долю в процентах от среднего значения ОП540 для VC. Жизнеспособность клеток может вычисляться с использованием электронной таблицы (например, в формате  ). В оптимальном случае восемь использованных значений концентрации для каждого исследуемого вещества должны охватывать весь диапазон эффекта, от его отсутствия до полного подавления жизнеспособности клеток.
). В оптимальном случае восемь использованных значений концентрации для каждого исследуемого вещества должны охватывать весь диапазон эффекта, от его отсутствия до полного подавления жизнеспособности клеток.
 ). В оптимальном случае восемь использованных значений концентрации для каждого исследуемого вещества должны охватывать весь диапазон эффекта, от его отсутствия до полного подавления жизнеспособности клеток.
). В оптимальном случае восемь использованных значений концентрации для каждого исследуемого вещества должны охватывать весь диапазон эффекта, от его отсутствия до полного подавления жизнеспособности клеток.6.1.3 Выполняют анализ на основе функции Хилла полученных параллельно данных жизнеспособности для каждого значения концентрации с использованием соответствующего статистического программного обеспечения (например,  http://www.graphpad.com/prism/Prism.htm) для вычисления значения IC50 для каждого исследуемого вещества. Рекомендуется использовать функцию Хилла в связи с тем, что при вычислениях реализуется вся имеющаяся информация о соотношении "доза - эффект", а не данные по отдельным точкам, окружающим значение IC50. Кроме того, использование функции Хилла позволяет определить наклон кривой "доза - эффект" (см. раздел 2 и приложение Д).
http://www.graphpad.com/prism/Prism.htm) для вычисления значения IC50 для каждого исследуемого вещества. Рекомендуется использовать функцию Хилла в связи с тем, что при вычислениях реализуется вся имеющаяся информация о соотношении "доза - эффект", а не данные по отдельным точкам, окружающим значение IC50. Кроме того, использование функции Хилла позволяет определить наклон кривой "доза - эффект" (см. раздел 2 и приложение Д).
 http://www.graphpad.com/prism/Prism.htm) для вычисления значения IC50 для каждого исследуемого вещества. Рекомендуется использовать функцию Хилла в связи с тем, что при вычислениях реализуется вся имеющаяся информация о соотношении "доза - эффект", а не данные по отдельным точкам, окружающим значение IC50. Кроме того, использование функции Хилла позволяет определить наклон кривой "доза - эффект" (см. раздел 2 и приложение Д).
http://www.graphpad.com/prism/Prism.htm) для вычисления значения IC50 для каждого исследуемого вещества. Рекомендуется использовать функцию Хилла в связи с тем, что при вычислениях реализуется вся имеющаяся информация о соотношении "доза - эффект", а не данные по отдельным точкам, окружающим значение IC50. Кроме того, использование функции Хилла позволяет определить наклон кривой "доза - эффект" (см. раздел 2 и приложение Д).Критерии приемлемости результатов испытаний
6.2.1 Среднее скорректированное значение поглощения левой (VC1) и среднее скорректированное значение поглощения правой (VC 2) колонок для VC (см. рекомендуемую схему посева клеток на 96-луночный планшет в приложении В) не должны отличаться более чем на 15% от среднего скорректированного значения поглощения всех VC.
6.2.2 Должно быть включено по меньшей мере одно вычисленное значение цитотоксичности, соответствующее значению жизнеспособности > 0% и <= 50%, а также одно вычисленное значение цитотоксичности, соответствующее значению жизнеспособности > 50% и < 100%. Исключение: если испытание включало только одну точку в диапазоне между 0 и 100% и использовалось наименьшее на практике значение коэффициента разбавления (т.е. 1,21), а также при этом выполнялись все остальные критерии приемлемости, то результаты испытания следует считать приемлемыми.
6.3.1 Аппроксимирующая кривая "доза - эффект" для ПК должна демонстрировать значение R2 (коэффициент детерминации) >= 0,85 для соответствия модели Хилла.
6.3.2 Значение IC50 для ПК должно находиться в пределах +/- 2,5 среднеквадратического отклонения (СО), установленного по данным предыдущих наблюдений лаборатории. Для формирования собственной минимальной базы данных предыдущих наблюдений необходимо иметь результаты исследований по меньшей мере десяти ПК [11].
Прогнозируемые результаты
Для двух методов на основе оценки NRU значения ОП540 контрольных лунок должны составлять приблизительно 0,05 [9]. Скорректированное значение ОП540 для VC в среднем может равняться 0,476 +/- 0,117 (СО) для метода с применением клеток 3T3 и 0,685 +/- 0,175 (СО) для метода с применением клеток NHK [9]. Значения IC50 для ПК (натрия лаурилсульфата) должны составлять 41,5 +/- 4,8 (СО) мкг/мл (n = 233) для метода с применением клеток 3T3 и 3,11 +/- 0,72 мкг/мл (n = 114) для метода с применением клеток NHK. В приложении Б приведена типичная кривая "доза - эффект" для натрия лаурилсульфата при проведении испытания по методу с применением клеток 3T3. В ходе валидационного исследования NICEATM/ECVAM по определению базовой цитотоксичности in vitro значения IC50 для исследуемых веществ находились в диапазоне от 0,005 до 38,878 мкг/мл (от 1,1 x 10-5 до 422 мМ) для метода с применением клеток 3T3 и от 0,00005 до 49,800 мкг/мл (от 6,4 x 10-8 до 49,800 мМ) для метода с применением клеток NHK [9] соответственно.
Определение начальных доз для испытаний на острую системную пероральную токсичность (см. приложение Е)
6.5.1 Сопоставление регрессии IC50-LD50 с использованием значений IC50, полученных при применении методов на основе оценки NRU с использованием клеток 3T3 или NHK для 47 химических веществ, приведенных одновременно в базе данных RC и в валидационном исследовании NICEATM-ECVAM, показало, что вычисленная регрессия существенно не отличалась от известной регрессии для данных 47 веществ, установленной согласно RC (p = 0,642 для регрессии NRU 3T3 и p = 0,759 для регрессии NRU NHK). Таким образом, могут быть использованы значения IC50 согласно NRU 3T3 или значения IC50 согласно NRU NHK. Для вычисления значения log LD50, ммоль/кг, на основе значения IC50, мМ, используют следующую формулу регрессии:
log LD50 (ммоль/кг) = 0,439 log IC50 (мМ) + 0,621 [9].
Преобразуют log LD50 в значение LD50, а затем переводят его в мг/кг, умножая на значение молекулярной массы исследуемого вещества.
6.5.2 Значение начальной дозы по методу UDP равняется ближайшему значению, меньшему, чем расчетное значение LD50, исходя из принятой по умолчанию прогрессии дозы. Прогрессия дозы, принятая по умолчанию для UDP, имеет следующий вид: 1,75, 5,5, 17,5, 55, 175, 550 и 2 000 мг/кг при использовании предела в 2000 мг/кг и 1,75, 5,5, 17,5, 55, 175, 550, 1750 и 5000 мг/кг при использовании предела в 5000 мг/кг соответственно [14].
6.5.3 Значение начальной дозы по методу ATC и предварительного исследования согласно методу FDP также равняется ближайшему значению дозы, меньшему, чем расчетное значение LD50, исходя из принятой по умолчанию прогрессии дозы. Прогрессия дозы, принятая по умолчанию для методов ATC и FDP, соответствует значениям 5, 50, 300 или 2000 мг/кг при использовании предела в 2000 мг/кг или 5, 50, 300, 2000 или 5000 мг/кг при использовании предела в 5000 мг/кг соответственно [9], [10].
6.5.4 Для веществ с неизвестной молекулярной массой значения IC50, мкг/мл, могут быть использованы в следующей формуле регрессии для определения значения LD50, мг/кг:
log LD50 (мг/кг) = 0,372 log IC50 (мкг/мл) + 2,024 [9].
Отчет об испытаниях должен включать в себя следующую информацию о проведении испытаний и об исследуемом веществе:
Исследуемые и контрольные вещества:
- наименование (наименования) химической продукции/вещества, синонимы, регистрационный номер CAS, молекулярную массу по формуле соединения, если она известна;
- сведения о степени чистоты и составе вещества или смеси веществ (в процентах по массе);
- физико-химические характеристики (например, сведения об агрегатном состоянии, летучести, показателе pH, стабильности, классе химических веществ, растворимости в воде);
- сведения о способе, применяемом для повышения растворимости исследуемых/контрольных веществ перед началом испытания (например, перемешивание, обработка в ультразвуковой ванне, нагревание, измельчение), если он применяется.
Растворитель:
- наименование растворителя;
- обоснование выбора растворителя;
- степень растворимости исследуемого вещества в выбранном растворителе;
- процентное содержание растворителя в среде для обработки образцов и контрольных пробах вещества-носителя.
Клетки:
- сведения об использованном виде клеток и источнике клеточного материала;
- сведения, подтверждающие отсутствие заражения микоплазмой или бактериальной контаминации;
- количество пассажей клеток.
Условия испытаний (1); экспериментальные данные:
- даты начала и завершения испытания;
- подробное описание примененной процедуры испытаний;
- описание любых изменений, внесенных в процедуру испытаний;
- ссылки на данные прошлых наблюдений для примененной модели исследования (например, растворитель или ПК);
- описание использованных критериев оценки.
Условия испытаний (2); информация о клеточной культуре:
- номера партий и наименования изготовителей реактивов, сывороток, питательных сред, добавок, рабочих культур и т.п.);
- состав питательной среды для повседневных исследований, используемой при выращивании клеточных культур и нанесении исследуемого вещества.
Условия испытаний (3); инкубирование до и после обработки:
- сведения об условиях инкубирования [температура (37 +/- 1) °C, относительная влажность (90 +/- 10)%, содержание CO2 в воздухе (5,0 +/- 1,0)%];
- продолжительность инкубирования (предварительного, последующего).
Условия испытаний (4); обработка исследуемым веществом:
- обоснование выбора используемых значений концентрации исследуемого вещества;
- сведения о растворимости исследуемого вещества и обоснование выбора наибольшего значения концентрации;
- состав среды для обработки;
- продолжительность обработки исследуемым веществом.
Условия испытаний (5); контроль жизнеспособности с помощью NR:
- состав среды для обработки, содержащей NR;
- продолжительность инкубирования с NR;
- сведения об условиях инкубирования [температура (37 +/- 1) °C, относительная влажность (90 +/- 10)%, содержание CO2 в воздухе (5,0 +/- 1,0)%];
- условия экстрагирования NR (экстрагирующий агент, продолжительность);
- использованное значение длины волны при спектрофотометрическом считывании оптического пропускания NR.
Информация о лице/организации, осуществлявших финансирование, и лаборатории, проводившей испытания:
- наименование/имя и адрес организации/лица, осуществлявших финансирование, лаборатории, проводившей испытания, имя руководителя исследования, а также имена технических специалистов, принимавших участие в исследовании;
- обоснование выбора метода испытаний и конкретного применяемого протокола.
Пригодность метода испытаний:
- процедура, применявшаяся для подтверждения пригодности (т.е. точности и надежности) метода испытания с течением времени (например, использование данных ПК).
Критерии приемлемости испытаний:
- допустимые расхождения для VC между каждой колонкой лунок планшета и средним значением для обоих колонок;
- допустимые установленные пределы для параллельных определений ПК на основе данных прошлых наблюдений (включая обобщенные данные по всем предыдущим исследованиям);
- количество точек токсического воздействия по обе стороны от значения IC50 (т.е. количество точек, в которых жизнеспособность > 0 и <= 50%, а также жизнеспособность > 50 и < 100%).
Результаты:
- представление данных в табличной форме с разбивкой по отдельным пробам (например, значения IC50 для контрольных веществ и ПК, абсолютные и скорректированные значения OD540 в виде таблицы, включая, если требуется, данные повторных аналогичных экспериментов, а также средние значения и значения среднеквадратичных отклонений для каждого эксперимента).
Описание других наблюдавшихся явлений:
- сведения о морфологии клеток, появлении осадка, образовании кристаллов NR и т.п.
Анализ результатов. Выводы
(обязательное)
НОРМАЛЬНЫХ ЭПИДЕРМАЛЬНЫХ КЕРАТИНОЦИТОВ ЧЕЛОВЕКА (NHK)
Базальная питательная среда для кератиноцитов, а также предлагаемые изготовителями специальные добавки к ней требуют предварительной оценки в целях подтверждения пригодности указанных материалов для испытаний по методу NRU NHK. Для каждой партии таких питательной среды или добавок, запланированных к приобретению, от изготовителя должны быть получены соответствующие данные испытаний, проводимых в рамках контроля качества (КК).
А.1 Испытательная система
А.1.1 Контроль по методу NRU NHK с целью анализа характеристик роста клеток NHK и токсичности натрия лаурилсульфата in vitro на основе определенных значений IC50 проводят для всех подлежащих проверке сочетаний питательной среды/добавок. Проверке подлежит каждое сочетание питательной среды/добавок, которое планируется использовать для последующих испытаний по данному методу.
А.1.2 Для этого выращивают культуры NHK в проверяемых сочетаниях питательной среды/добавок, а затем пересевают полученные клетки в сроки, соответствующие трем различным дням, на 96-луночные планшеты (по 1 планшету в день) для проведения трех последовательных испытаний на цитотоксичность натрия лаурилсульфата с использованием соответствующих сочетаний испытываемой питательной среды/добавок, а также (если имеется) контрольного сочетания питательной среды/добавок, характеристики которых уже были подтверждены ранее.
А.2 Методы испытаний
А.2.1 Культуры NHK получают из сохраняемых в криогенных условиях клеток, высевая их в отдельные колбы для выращивания тканевых культур с площадью роста 25 см2, применяя сочетание питательной среды/добавок с подтвержденными характеристиками (контрольную среду) и каждое из подлежащих проверке сочетаний питательной среды/добавок.
А.2.2 Приготавливают суспензию из свежеразмороженного клеточного материала в 9 мл контрольной среды, а затем помещают полученную клеточную суспензию в колбы для выращивания тканевых культур с площадью роста 25 см2, содержащие предварительно подогретую контрольную или испытываемую питательную среду. Посев в колбы производят с плотностью (1 колба/плотность/среда) 1 x 104, 5 x 103 и 2,5 x 103 клеток.
А.2.3 Пересевают клетки в сроки, соответствующие трем различным дням, на 96-луночные планшеты для выполнения трех последовательных измерений NRU (всего три планшета [по одному в день] для каждого проверяемого и каждого контрольного сочетания питательной среды/добавок).
А.2.4 Порядок посева клеток и применения к ним натрия лаурилсульфата должен соответствовать процедурам, описанным в 5.4.2, с учетом требований по достижению необходимого уровня конфлюэнтности клеточного слоя. Перед переносом клеток на 96-луночные планшеты их количество, содержащееся в каждой колбе, следует надлежащим образом регистрировать. В качестве дополнительного показателя, служащего для проверки качества, можно также измерять достигаемое время удвоения числа клеток.
А.3 Порядок проведения испытаний
А.3.1 При приготовлении растворов натрия лаурилсульфата следует руководствоваться общими требованиями, предусмотренными для испытаний химических соединений в питательной среде для проведения повседневных исследований на кератиноцитах. Проверку клеток, культивируемых в контрольной питательной среде и в каждом сочетании испытываемых питательной среды/добавок на их чувствительность к воздействию натрия лаурилсульфата, следует осуществлять параллельно.
А.3.2 Значения концентрации натрия лаурилсульфата при этом были такими же, как использовавшиеся при испытании контрольной питательной среды/добавок ранее, или близкими к ним. При проведении соответствующего валидационного исследования in vitro используемое значение концентрации натрия лаурилсульфата составляло 0,6 - 20,0 мкг/мл [9].
А.4 Микроскопическая оценка
Перед тем как приступить к измерениям NRU, регистрируют изменения в морфологии клеток, обусловленные цитотоксическим воздействием натрия лаурилсульфата. В дополнение к основной микроскопической оценке состояния клеточных культур выполняют также следующие специальные наблюдения:
Общие наблюдения за состоянием клеточных культур:
- скорость роста популяции клеток (например, высокая, умеренная, низкая);
- процент конфлюэнтности (например, по итогам однодневных наблюдений);
- количество митотических фигур (например, в среднем в пределах поля наблюдения);
- контаминация (присутствует/отсутствует).
Наблюдения за морфологией клеток:
- общее наблюдаемое состояние (например, хорошее, удовлетворительное, неудовлетворительное);
- формирование колоний (например, плотные/четко очерченные колонии, умеренно выраженные, несвязанные/мигрирующие клетки);
- распределение клеток (например, равномерное/неравномерное);
- наличие измененных клеток [например, удлиненных, вакуолизированных, некротических, пятнистых, пузырчатых (в среднем в пределах поля наблюдения)].
А.5 Анализ данных и оценка результатов
А.5.1 См. критерии приемлемости результатов испытаний (6.2.1, 6.2.2, 6.3.1, 6.3.2) для определения пригодности планшета к последующему анализу. Кроме того, должны учитываться следующие критерии:
- среднее скорректированное значение ОП540 для проб с NR.
Примечание - Целевой диапазон для скорректированного среднего значения ОП540 = 0,248 - 1,123 для VC (диапазон = среднее ОП540 +/- среднеквадратичное отклонение в размере 2,5; среднее = 0,685; СО = 0,175; N = 114 [9]);
- морфология клеток и конфлюэнтность для проб с VC по окончании 48-часового периода обработки;
- время удвоения клеток NHK.
А.5.2 Основываясь на установленных путем наблюдения ростовых характеристиках клеток, а также результатах испытаний в дополнение к сравнению с результатами контроля качества, проведенного изготовителем питательной среды, принимают решение о приемлемости или неприемлемости соответствующих сочетаний питательной среды/добавок для использования в дальнейших исследованиях.
(справочное)
ДЛЯ НАТРИЯ ЛАУРИЛСУЛЬФАТА ПРИ ПРОВЕДЕНИИ ИСПЫТАНИЙ
НА ПОГЛОЩЕНИЕ НЕЙТРАЛЬНОГО КРАСНОГО С ИСПОЛЬЗОВАНИЕМ
ФИБРОБЛАСТОВ МЫШИ BALB/C 3T3
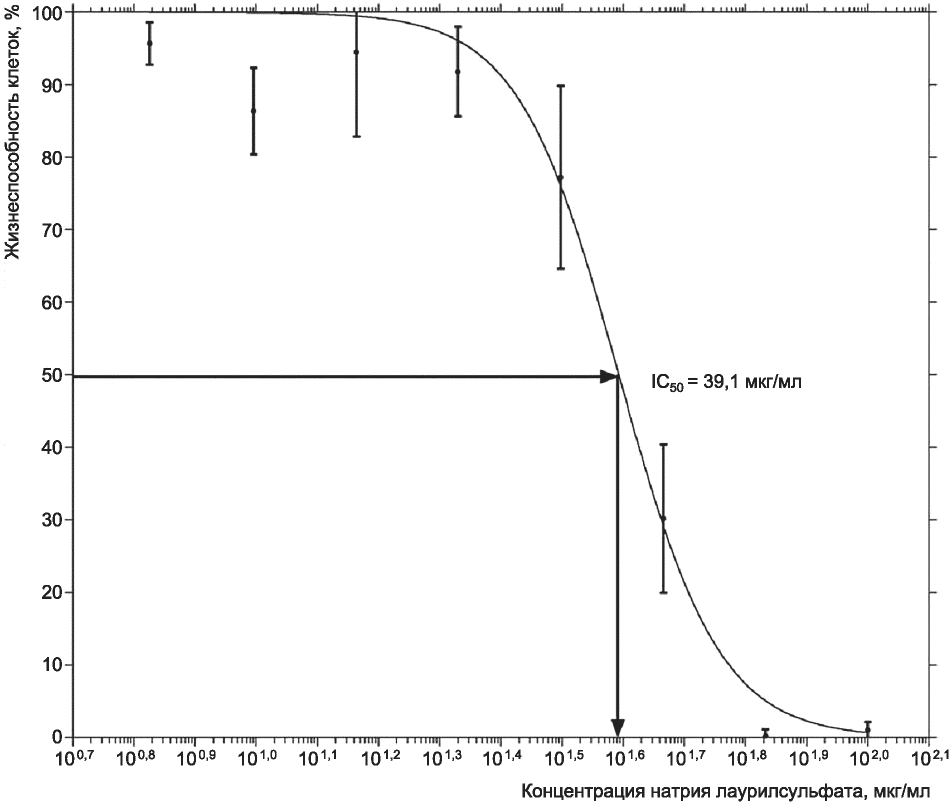
Точками и планками погрешности на рисунке показаны средние значения и среднеквадратичные отклонения соответственно для эффекта, отражающего жизнеспособность клеток в процентах, по результатам для шести параллельно обрабатываемых лунок планшета с каждым из восьми значений концентрации, а именно: 6,8, 10, 14,7, 21,5, 31,6, 46,4, 68,1 и 100 мкг/мл. Кривая демонстрирует соответствие зависимости "концентрация - эффект" функции Хилла.
(справочное)
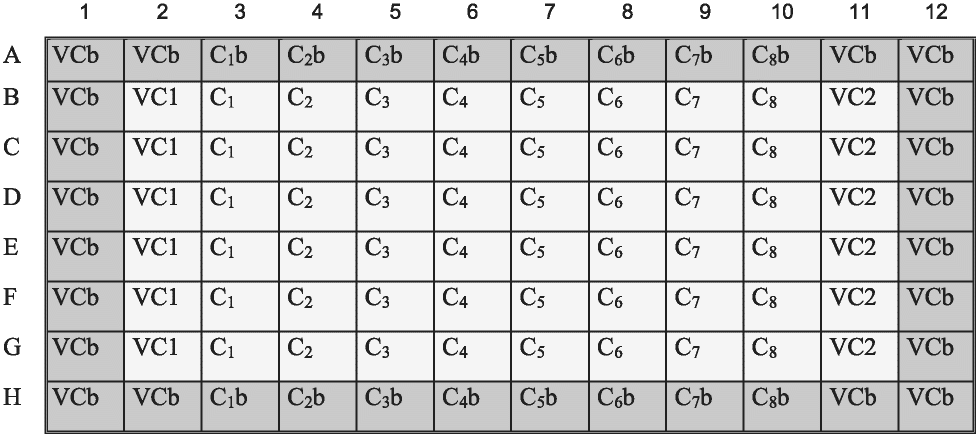
Использование 96-луночного планшета при работе с ПК и пробами исследуемого вещества
Строки с A по H в таблице, приведенной выше, представляют собой восемь рядов лунок 96-луночного планшета, а столбцы с 1 по 12 - 12 колонок 96-луночного планшета соответственно.
Обозначения VC1 и VC2 используются для указания левых (VC1) и правых (VC2) лунок с контрольной пробой вещества-носителя, в которых содержатся только клетки, питательная среда для повседневных исследований и соответствующий растворитель (если используется). Обозначение VCb указывает на контрольные лунки с веществом-носителем, в которых содержатся только питательная среда для повседневных исследований и соответствующий растворитель (если используется), без добавления клеток.
Обозначения C1 - C8 соответствуют восьми концентрациям исследуемого вещества или положительной контрольной пробе (натрия лаурилсульфата). C1 соответствует наибольшей, а C8 - наименьшей концентрации. Для каждого исследуемого значения концентрации предусмотрены шесть параллельно обрабатываемых лунок. Лунки, обозначаемые как Cxb, являются контрольными и содержат только исследуемое вещество или ПК, без добавления клеток.
(обязательное)
Г.1 Определение растворимости исследуемых веществ
Г.1.1 Данный протокол предназначен для определения растворителя, при использовании которого достигается наибольшая возможная концентрация исследуемого вещества в растворе, обеспечивающая равномерное поступление последнего в клетки при проведении испытаний на базовую цитотоксичность в условиях in vitro.
Г.1.2 Процедура контроля растворимости базируется на опробовании растворения исследуемого вещества в различных растворителях с использованием операций смешивания с увеличивающейся интенсивностью. К числу возможных растворителей в порядке убывания приоритетности относят используемую питательную среду для культивирования клеток, ДМСО и этанол. Способность конкретного исследуемого вещества к растворению оценивают посредством визуального наблюдения с использованием микроскопа. Вещество считают полностью растворившимся при условии достижения полной прозрачности раствора и отсутствия в нем каких-либо признаков помутнения или осадка (см. 5.8.1).
Г.1.3 Контроль растворимости вещества представляет собой последовательный, поэтапный процесс, направленный на определение наиболее подходящего растворителя, который может быть использован при проведении дальнейших исследований. Каждый этап представляет собой опробование растворения исследуемого вещества в одном или нескольких растворителях при концентрации вещества, обеспечивающей поступление его в одинаковой концентрации (независимо от используемого растворителя) в клетки (с добавлением 0,5% об. ДМСО или этанола для веществ, нерастворимых непосредственно в питательной среде). Если исследуемое вещество не растворяется, объем растворителя увеличивают таким образом, чтобы добиться десятикратного уменьшения концентрации исследуемого вещества; эту последовательность операций смешивания при необходимости повторяют до тех пор, пока не удастся достигнуть растворения при более низких значениях концентрации вещества. Если на одном и том же этапе контроля вещество параллельно смешивается со всеми растворителями и при этом подтверждается полная растворимость более чем в одном растворителе, предпочтительный выбор растворителя следующий: питательная среда, ДМСО, этанол. Если на каком-либо этапе вещество растворяется как в питательной среде, так и в ДМСО, то в качестве растворителя выбирают питательную среду. Если вещество не растворяется в питательной среде, однако растворяется в ДМСО и этаноле, то в качестве растворителя выбирают ДМСО.
Г.2 Последовательный (поэтапный) процесс определения растворимости
Г.2.1 Этап 1. Взвешивают 100 мг исследуемого вещества и помещают навеску в стеклянную пробирку. Добавляют в пробирку приблизительно 0,5 мл питательной среды для получения значения концентрации 200 мг/мл. Перемешивают раствор. Если вещество полностью растворилось, дополнительные операции по его растворению выполнять не требуется.
Г.2.2 Этап 2. Если исследуемое вещество не удалось полностью растворить на этапе 1 при значении концентрации 200 мг/мл, переходят к выполнению этапа 2. Взвешивают 10 мг исследуемого вещества и помещают навеску в стеклянную пробирку. Добавляют приблизительно 0,5 мл питательной среды для получения значения концентрации 20 мг/мл. Перемешивают раствор. Если вещество полностью растворилось, дополнительные операции по его растворению выполнять не требуется.
Г.2.3 Этап 3. Если исследуемое вещество не удалось полностью растворить на этапе 2 при значении концентрации 20 мг/мл, переходят к выполнению этапа 3. Добавляют достаточное количество питательной среды, как правило приблизительно 4,5 мл, для получения значения концентрации вещества 2 мг/мл и снова пробуют растворить его, применяя рекомендуемую последовательность операций смешивания. Если исследуемое вещество полностью растворилось в питательной среде при значении концентрации 2 мг/мл, дальнейшие операции выполнять не требуется. Если исследуемое вещество не удалось растворить в питательной среде, взвешивают 100 мг вещества и помещают навеску в другую стеклянную пробирку, в которую затем добавляют приблизительно 0,5 мл ДМСО для получения значения концентрации 200 мг/мл, и перемешивают раствор. Если исследуемое вещество не удалось полностью растворить в ДМСО, взвешивают 100 мг вещества и помещают навеску в следующую стеклянную пробирку, в которую затем добавляют приблизительно 0,5 мл этанола для получения значения концентрации 200 мг/мл, и перемешивают раствор. Если вещество удалось растворить в одном из используемых растворителей, дополнительные операции по его растворению выполнять не требуется.
Г.2.4 Этап 4. Если вещество не удается растворить ни в соответствующей питательной среде, ни в ДМСО, ни в этаноле на этапе 3, переходят к выполнению этапа 4. Добавляют к трем (или четырем) растворам, полученным на этапе 2, количество растворителя, достаточное для десятикратного увеличения их объема, и предпринимают очередную попытку растворения вещества с применением рекомендуемой последовательности операций смешивания. Если вещество полностью растворилось, какие-либо дополнительные операции по его растворению выполнять не требуется. Если исследуемое вещество не удалось полностью растворить, переходят к выполнению этапа 5 и при необходимости этапа 6, используя ДМСО и этанол.
Г.2.5 Этап 5. Разбавляют растворы, полученные на этапе 4, ДМСО или этанолом, доводя общий объем раствора до 50 мл, и предпринимают очередную попытку растворения вещества с применением рекомендуемой последовательности операций смешивания.
Г.2.6 Этап 6. Взвешивают две пробы по 10 мг каждая исследуемого вещества, добавляют к навескам приблизительно по 50 мл ДМСО или этанола для получения значения концентрации 200 мкг/мл и далее выполняют рекомендуемые операции смешивания.
Г.3 Операции смешивания
Для растворения исследуемого вещества операции смешивания рекомендуется выполнять в следующей последовательности:
b) В случае, если исследуемое вещество не растворилось, обрабатывают раствор в ультразвуковой ванне в течение времени, не превышающего 5 мин.
c) Если исследуемое вещество не растворяется путем ультразвуковой обработки, подогревают раствор при 37 °C на водяной бане или в углекислотном инкубаторе в течение 5 - 60 мин. В процессе подогрева раствор допускается перемешивать (если подогрев осуществляется с помощью углекислотного инкубатора, перемешивание раствора также способствует поддержанию соответствующего значения pH).
d) Переходят к выполнению этапа 2 (а также, при необходимости, этапов 3 - 6 и повторяют операции смешивания согласно a) и b).
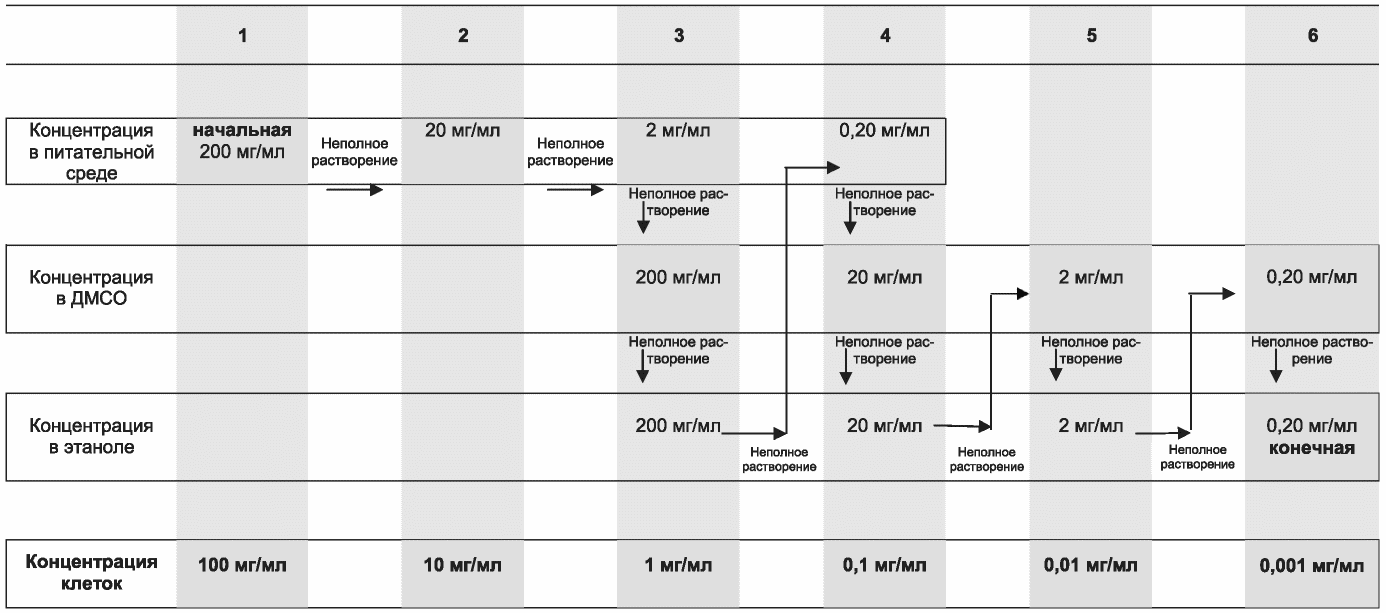
исследуемого вещества в питательной среде,
диметилсульфоксиде (ДМСО) или этаноле
Испытания начинают при значении концентрации исследуемого вещества 200 мг/мл в питательной среде для культивирования клеток и продолжают до достижения значения концентрации 0,2 мг/мл с использованием этанола, если данное вещество не удается полностью растворить в питательной среде. Испытания прекращают на любом этапе после достижения полного растворения вещества.
(справочное)
Д.1 Успешность реализации методов на основе оценки NRU зависит от надлежащей пролиферации клеточного материала, уровня цитотоксичности, достаточного для вычисления значения IC50, отсутствия кристаллов NR и соответствия полученных данных зависимости "концентрация - эффект" функции Хилла. При воздействии исследуемой химической продукции/вещества клетки должны находиться в стадии экспоненциального роста. Контрольные значения ОП540 в общем случае должны соответствовать 0,3 или более, тем не менее более низкие измеренные значения ОП540 также могут быть признаны допустимыми при условии, что клетки выглядят здоровыми и обеспечивают корректный эффект на воздействие натрия лаурилсульфата. Если ни одно из перечисленных условий не выполняется, то вероятной причиной этому могут быть контаминации клеточного материала микоплазмой (либо, например, бактериями, грибами), не соответствующие требованиям условия проведения эксперимента (температура, содержание CO2, влажность), а также неправильный выбор питательной среды или отдельных ее компонентов (например, сыворотки для 3T3 или ростовой фактор для NHK). Конфлюэнтность 100% на момент завершения периода экспозиции считается приемлемой для клеток 3T3, но является нежелательной для клеток NHK. Конфлюэнтные клетки NHK вырабатывают ростовые факторы, которые ингибируют рост и стимулируют клеточную дифференциацию.
Д.2 Растворимость зачастую выступает как ограничивающий фактор для достижения достаточного уровня цитотоксичности для вычисления IC50, особенно в случае относительно малотоксичных исследуемых веществ. Нерастворимые вещества могут образовывать осадок или пленку непосредственно в сосудах с исходным раствором или в лунках, куда помещаются клеточные культуры. Растворители, отличные от указанных в приведенном протоколе, могут использоваться при условии, что в выбранной концентрации они не вызывают цитотоксического воздействия. Способность исследуемого вещества к растворению также может быть повышена за счет перемешивания или нагревания раствора в течение более длительного (чем обычно) периода времени. Пользователи должны иметь в виду, что несоразмерный уровень токсичности, который иногда отмечается при исследовании летучих веществ, в действительности представляет собой артефакт вследствие распространения вещества по воздуху за пределы рабочих лунок. Снижение жизнеспособности культур с VC в лунках, расположенных рядом с лунками с наибольшей концентрацией исследуемого вещества, может свидетельствовать о его активном испарении (см. расположение лунок VC 1 согласно рекомендуемой схеме посева на 96-луночный планшет в приложении В). Тем не менее достоверная цитотоксичность для некоторых летучих агентов может быть получена при использовании тонкой полимерной пленки, которую используют в качестве защитного покрытия лунок с целью удержания паров вещества и снижения вероятности загрязнения ими соседних лунок с VC.
Д.3 Нерастворимые вещества, а также вещества, не обладающие достаточной стабильностью в водной среде, являются несовместимыми с испытательными системами. Результаты, получаемые при исследованиях летучих веществ, могут считаться приемлемыми, если для планшетов с пробами используется полимерная пленка, проницаемая для CO2. Исследование веществ, которые могут обладать коррозионными (разъедающими) свойствами, не проводится ввиду отсутствия нормативных требований по исследованию острой пероральной системной токсичности для известных разъедающих веществ. В случае применения метода NRU 3T3 токсичность веществ, которые хорошо связываются с белками сыворотки, может быть занижена, поскольку питательная среда содержит 5% сыворотки в период воздействия исследуемым веществом. Токсичность веществ, избирательно воздействующих на лизосомы, напротив, может быть завышена, поскольку они могут влиять на связывание NR и, соответственно, на его количество, которое способно удерживаться клеткой. Исследования веществ красного цвета (а также других веществ, обладающих выраженной окраской), которые поглощают свет в диапазоне оптической плотности, характерном для NR, могут приводить к получению искаженных результатов, если после промывки существенное количество таких веществ остается в клетках и эти вещества растворяются в том же растворителе, который используется для растворения NR.
Д.4 В случае образования кристаллов NR они препятствуют правильным измерениям значений ОП540. Измеренные значения ОП540 холостых лунок могут отклоняться от обычно наблюдаемого значения 0,05, достигая 0,10 или более. Правильное приготовление и хранение раствора NR являются важными факторами для сведения к минимуму образования кристаллов. Вследствие этого раствор красителя NR всегда должен быть свежеприготовленным, фильтрованным, поддерживаемым при температуре 37 °C до его добавления к клеткам.
Д.5 Результаты вычисления соответствующего значения IC50 зависят от соответствия данных зависимости "концентрация - эффект" функции Хилла. Токсические вещества, для которых характерно действие в течение одной фазы клеточного цикла, могут приводить к показателям зависимости "концентрация - эффект", для которых процент жизнеспособности колеблется в широких пределах относительно 50% по мере увеличения логарифмических значений дозы на этапе ее выбора. В подобной ситуации при проведении основного этапа испытания желательно сосредоточиться на минимальных значениях концентрации, обеспечивающих 50%-ное снижение жизнеспособности. Данные зависимости "концентрация - эффект", для которых при увеличении концентрации процент жизнеспособности выходит на плато вместо того, чтобы уменьшиться до 0%, как правило, плохо согласуются с функцией Хилла (т.е. R2 < 0,9). Согласованность в целом улучшается, если внести поправки в параметр Bottom функции Хилла, не ограничивая его 0%-ной жизнеспособностью. В этом случае, однако, значение EC50 для стандартной функции Хилла уже не будет соответствовать концентрации, при которой происходит снижение жизнеспособности на 50%. Следовательно, для корректного вычисления значения IC50 функция Хилла должна быть преобразована следующим образом:
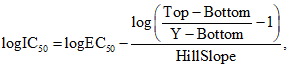
где IC50 - концентрация, соответствующая 50%-ному уровню токсичности, EC50 - концентрация, обеспечивающая получение эффекта посередине между максимальным и минимальным значениями (Top и Bottom); Top - максимальная жизнеспособность, %, Bottom - минимальная жизнеспособность (максимальный уровень токсичности), Y = 50 (т.е. 50%-ный эффект), а HillSlope - параметр, определяющий наклон кривой отклика. Значение X в стандартной формуле, которая описывает функцию Хилла, в результате преобразования заменяется значением IC50.
Д.6 Достоверность прогнозирования значений LD50 при пероральном воздействии у крыс и определение значений начальной дозы при проведении испытаний на острую пероральную системную токсичность с применением методов на основе оценки NRU in vitro оцениваются как низкая для веществ, механизм развития токсического воздействия которых не проявляет себя в клетках 3T3 или NHK. К подобного рода токсическим механизмам могут относиться специфические, опосредуемые рецепторами процессы в центральной нервной системе или сердце [9].
Д.7 Методы на основе оценки NRU in vitro могут применяться для широкого диапазона химических веществ при условии, что они способны растворяться непосредственно в питательной среде для культивирования клеток или нетоксичном растворителе (требуемой концентрации) и не взаимодействуют с питательной средой. Несмотря на то что методы могут применяться для смесей веществ, оценка их в рамках валидационного исследования не проводилась. Токсичность веществ, механизм воздействия которых не проявляет себя в клетках 3T3 или NHK (например, веществ с узким нейротоксическим или кардиотоксическим действием), с большой вероятностью может быть занижена в случае применения данных методов. В этой связи до выведения наиболее подходящих для решения подобной задачи клеточных линий результаты исследований базовой цитотоксичности для таких веществ могут не отражать весь спектр вероятных воздействий in vivo.
(справочное)
ДЛЯ ИСПЫТАНИЙ НА ОСТРУЮ ПЕРОРАЛЬНУЮ СИСТЕМНУЮ ТОКСИЧНОСТЬ
(См. определение значений начальных доз для испытаний на острую пероральную системную токсичность в 6.5.1 - 6.5.4.)
Пример для значения IC50 в мМ
(см. рисунок Е.1 для наглядного представления)
1,1,2-Трихлорэтан (МВ = 133,4).
NRU 3T3 IC50 = 153,3 мМ.
log LD50 (ммоль/кг) = 0,439 log IC50 (мМ) + 0,621.
Регрессия RC в миллимолях только по данным опытов на крысах [9].
log LD50 (ммоль/кг) = (0,439 x 2,186) + 0,621.
LD50 (ммоль/кг) = 1,580.
LD50 = 38,019 ммоль/кг.
Расчетное значение LD50 = 38,019 ммоль/кг x 133,4 мг/моль.
Расчетное значение LD50 = 5072 мг/кг.
Начальная доза для метода UDP
Значения дозы по умолчанию: 1,75, 5,5, 17,5, 55, 175, 550 и 2000 мг/кг (предел 2000 мг/кг).
1,75, 5,5, 17,5, 55, 175, 550, 1750 и 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 5072 мг/кг; значение начальной дозы = 5000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50.
Начальная доза для метода ATC
Значения дозы по умолчанию: 5, 50, 300 и 2 000 мг/кг (предел 2000 мг/кг).
5, 50, 300, 2000 и 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 5072 мг/кг; значение начальной дозы = 5000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50.
Начальная доза для метода FDP
Значения дозы по умолчанию: 5, 50, 300 и 2000 мг/кг (предел 2000 мг/кг).
5, 50, 300, 2000 и 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 5072 мг/кг; значение начальной дозы для предварительного исследования = 5000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50.
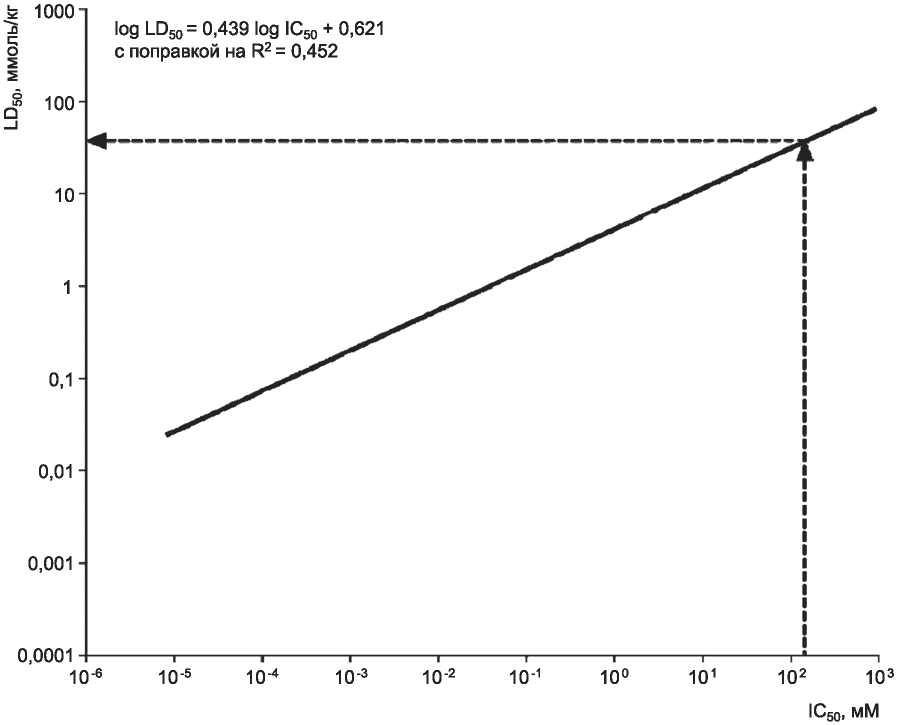
Прерывистыми линиями показана корреляция
значений IC50 и LD50 на линии регрессии
опытов на крысах. Корреляция значений IC50
и расчетных значений LD50
Пример для значения IC50 в мкг/мл
(см. рисунок Е.2 для наглядного представления).
1,1,2-Трихлорэтан (МВ = 133,4).
NRU 3T3 IC50 = 20 453 мкг/мл.
log LD50 (мг/кг) = 0,372 log IC50 (мкг/мл) + 2,024.
Регрессия RC по массе только по данным опытов на крысах [9].
log LD50 (мг/кг) = (0,372 x 4,311) + 2,024.
log LD50 (мг/кг) = 3,628.
LD50 = 4246 мг/кг.
Начальная доза для метода UDP
Значения дозы по умолчанию: 1,75, 5,5, 17,5, 55, 175, 550 и 2000 мг/кг (предел 2000 мг/кг).
1,75, 5,5, 17,5, 55, 175, 550, 1750 и 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 4246 мг/кг; значение начальной дозы = 2000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50, при использовании предела 2000 мг/кг; значение начальной дозы = 1750 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50, при использовании предела 5000 мг/кг.
Начальная доза для метода ATC
Значения дозы по умолчанию: 5, 50, 300 или 2000 мг/кг (предел 2000 мг/кг).
5, 50, 300, 2000 или 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 4246 мг/кг; значение начальной дозы = 2000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50, при использовании предела 2000 или 5000 мг/кг.
Начальная доза для метода FDP
Значения дозы по умолчанию: 5, 50, 300 или 2000 мг/кг (предел 2000 мг/кг).
5, 50, 300, 2000 или 5000 мг/кг (предел 5000 мг/кг).
Расчетное значение LD50 = 4246 мг/кг; значение начальной дозы для предварительного исследования = 2000 мг/кг, ближайшее значение дозы по умолчанию меньше, чем расчетное значение LD50, при использовании предела 2000 или 5000 мг/кг.
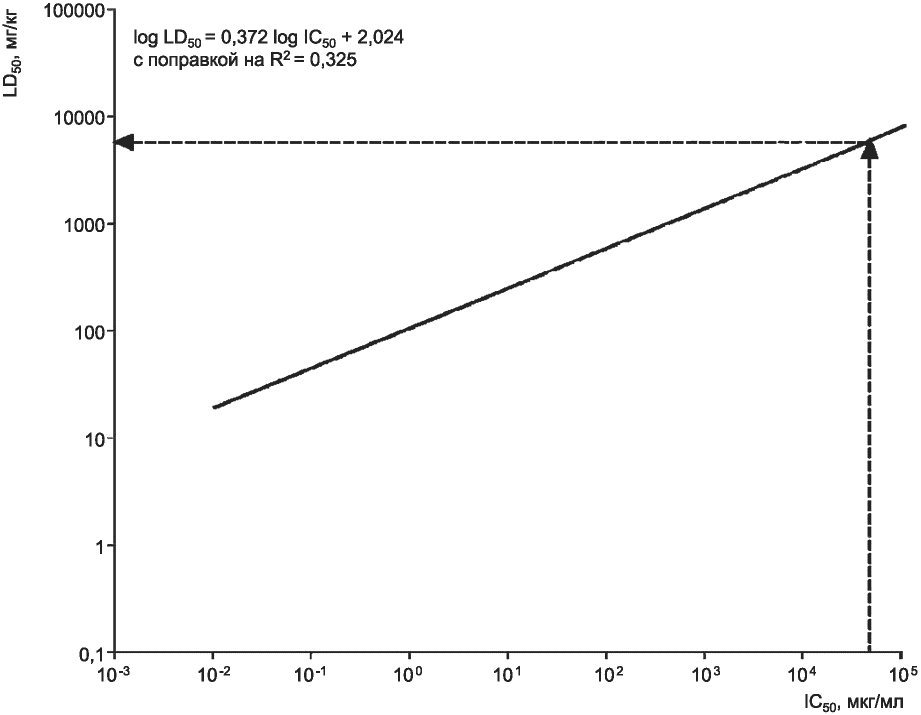
Прерывистыми линиями показана корреляция
значений IC50 и LD50 на линии регрессии
опытов на крысах. Корреляция значений IC50
и расчетных значений LD50
(справочное)
ПРОВЕДЕННОГО NICEATM-ECVAM ВАЛИДАЦИОННОГО ИССЛЕДОВАНИЯ
МЕТОДОВ ОПРЕДЕЛЕНИЯ БАЗОВОЙ ЦИТОТОКСИЧНОСТИ
Исследованная химическая продукция | Регистрационный номер CAS | NRU 3T3 IC50, мкг/мл <1> | NRU NHK IC50, мкг/мл <1> | Класс химической продукции <4> | |
1,1,1-Трихлорэтан | 71-55-6 | 17 248 | 8 122 <5> | 12 078 | Органические соединения; галогенизированные углеводороды |
2-Пропанол | 67-63-0 | 3 618 | 5 364 | 5 105 | Органические соединения; спирты |
5-Аминосалициловая кислота | 89-57-6 | 1 667 | 46,7 | 3 429 | Органические соединения; карбоновые кислоты; фенолы |
Ацетаминофен | 103-90-2 | 47,7 | 518 | 2 163 | Органические соединения; амиды |
Ацетонитрил | 75-05-8 | 7 951 | 9 528 | 3 598 | Органические соединения; нитрилы |
Ацетилсалициловая кислота | 50-78-2 | 676 | 605 | 1 506 | Органические соединения; карбоновые кислоты; фенолы |
Аминоптерин | 54-62-6 | 0,006 | 669 | 7 | Органические соединения; гетероциклические соединения |
Амитриптилин гидрохлорид | 549-18-8 | 7,05 | 8,96 | 348 | Органические соединения; полициклические соединения |
Мышьяка триоксид | 1327-53-3 | 1,96 | 5,26 | 25 | Неорганические соединения; соединения мышьяка |
Атропина сульфат | 5908-99-6 | 76 | 81,8 | 819 | Органические соединения; гетероциклические соединения |
Борная кислота | 10043-35-3 | 1 850 | 421 | 3 426 | Неорганические соединения; соединения бора, кислоты |
Бусульфан | 55-98-1 | 77,7 | 260 | 12 | Органические соединения; спирты; ациклические углеводороды; соединения серы |
Кадмия II хлорид | 10108-64-2 | 0,518 | 1,84 | 135 | Неорганические соединения; соединения кадмия |
Кофеин | 58-08-2 | 153 | 638 | 310 | Органические соединения; гетероциклические соединения |
Карбамазепин | 298-46-4 | 103 | 83,2 | 2 805 | Органические соединения; гетероциклические соединения |
Углерода тетрахлорид | 56-23-5 | НД | НД | 3 783 | Органические соединения; галогенизированные углеводороды |
Хлоральгидрат | 302-17-0 | 183 | 133 | 638 | Органические соединения; спирты |
Хлорамфеникол | 56-75-7 | 128 | 348 | 3 491 | Органические соединения; спирты; циклические углеводороды; нитросоединения |
Лимонная кислота | 77-92-9 | 796 | 400 | 5 929 | Органические соединения; карбоновые кислоты |
Колхицин | 64-86-8 | 0,034 | 0,007 | 15 (мыши) | Органические соединения; полициклические соединения |
Меди сульфат пентагидрат | 7758-99-8 | 42,1 | 197 | 474 | Неорганические соединения; соединения серы; соединения металлов |
Циклогексимид | 66-81-9 | 0,187 | 0,073 | 2 | Органические соединения; гетероциклические соединения |
Дибутилфталат | 84-74-2 | 49,7 | 28,7 | 8 892 | Органические соединения; карбоновые кислоты |
Дихлорвос | 62-73-7 | 17,7 | 10,7 | 59 | Органические соединения; фосфорорганические соединения |
Диэтилфталат | 84-66-2 | 107 | 120 | 9 311 | Органические соединения; карбоновые кислоты |
Дигоксин | 20830-75-5 | 466 | 0,001 | 28 | Органические соединения; полициклические соединения; карбогидраты |
Диметилформамид | 68-12-2 | 5 224 | 7 760 | 5 309 | Органические соединения; амиды; карбоновые кислоты |
Дикват дибромид моногидрат | 6385-62-2 | 8,04 | 4,48 | 160 | Органические соединения; гетероциклические соединения |
Дисульфотон | 298-04-4 | 133 | 270 | 5 | Органические соединения; фосфорорганические соединения; соединения серы |
Эндосульфан | 115-29-7 | 6,35 | 2,13 | 28 | Органические соединения; гетероциклические соединения; соединения серы |
Эпинефрина битартрат | 51-42-3 | 59 | 87,4 | 4 (мыши) | Органические соединения; спирты; амины |
Этанол | 64-17-5 | 6 523 | 10 018 | 11 324 | Органические соединения; спирты |
Этиленгликоль | 107-21-1 | 24 317 | 41 852 | 7 161 | Органические соединения; спирты |
Фенпропатрин | 39515-41-8 | 24,2 | 2,43 | 76 | Органические соединения; нитрилы; эфиры; сложные эфиры |
Гиббереллиновая кислота | 77-06-5 | 7 810 <5> | 2 856 | 6 040 | Органические соединения; полициклические соединения |
Глютетимид | 77-21-4 | 174 | 174 | 600 | Органические соединения; гетероциклические соединения |
Глицерин | 56-81-5 | 24 655 | 24 730 | 19 770 | Органические соединения; спирты |
Галоперидол | 52-86-8 | 6,13 | 3,36 | 330 | Органические соединения; кетоны |
Гексахлорофен | 70-30-4 | 4,19 | 0,029 | 82 | Органические соединения; циклические углеводороды; фенолы |
Молочная кислота | 50-21-5 | 3 044 | 1304 | 3 639 | Органические соединения; карбоновые кислоты |
Линдан | 58-89-9 | 108 | 18,7 | 100 | Органические соединения; галогенизированные углеводороды |
Лития I карбонат | 554-13-2 | 562 <5> | 468 | 590 | Неорганические соединения; соединения лития; алкилы; соединения углерода |
Мепробамат | 57-53-4 | 519 | 357 | 1 387 | Органические соединения; карбоновые кислоты |
Ртути II хлорид | 7487-94-7 | 4,12 | 5,8 | 40 | Неорганические соединения; соединения ртути; соединения хлора |
Метанол | 67-56-1 | НД | 1 529 <6> | 8 710 | Органические соединения; спирты |
Никотин | 54-11-5 | 361 | 107 | 70 | Органические соединения; гетероциклические соединения |
Паракват | 1910-42-5 | 20,1 | 61,6 | 93 | Органические соединения; гетероциклические соединения |
Паратион | 56-38-2 | 37,4 | 30,3 | 6 | Органические соединения; фосфорорганические соединения; соединения серы |
Фенобарбитал | 50-06-6 | 573 | 448 | 224 | Органические соединения; гетероциклические соединения |
Фенол | 108-95-2 | 66,3 | 75 | 548 | Органические соединения; фенолы |
Фенилтиомочевина | 103-85-5 | 79 | 336 | 3 | Органические соединения; соединения серы; мочевина |
Физостигмин | 57-47-6 | 25,8 | 88,5 | 5 | Органические соединения; карбоновые кислоты; гетероциклические соединения |
Калия цианид | 151-50-8 | 34,6 | 29 | 7 | Неорганические соединения; соединения калия; соединения азота |
Калия хлорид | 7447-40-7 | 3 551 | 2 237 | 2 799 | Неорганические соединения; соединения калия; соединения хлора |
Прокаинамида гидрохлорид | 51-06-9 | 441 | 1 741 | 1 950 | Органические соединения; карбоновые кислоты; амиды |
Пропанол | 3506-09-0 | 13,9 | 35,3 | 466 | Органические соединения; спирты; амины; полициклические соединения |
Пропилпарабен | 94-13-3 | 26,1 | 16,6 | 6 332 (мыши) | Органические соединения; карбоновые кислоты; фенолы |
Натрия арсенит | 7784-46-5 | 0,759 | 0,477 | 44 | Неорганические соединения; соединения мышьяка; соединения натрия |
Натрия хлорид | 7647-14-5 | 4 730 | 1 997 | 4 046 | Неорганические соединения; соединения натрия; соединения хлора |
Натрия дихромат дигидрат | 7789-12-0 | 0,587 | 0,721 | 51 | Неорганические соединения; соединения натрия; соединения хрома |
Натрия фторид | 7681-49-4 | 78 | 49,8 | 127 | Неорганические соединения; соединения натрия; соединения фтора |
Натрия гипохлорит | 7681-52-9 | 1 103 | 1 502 | 10 328 | Неорганические соединения; соединения натрия; кислородсодержащие соединения; соединения хлора |
Натрия оксалат | 62-76-0 | 37,7 | 337 | 633 | Органические соединения; карбоновые кислоты; соединения натрия |
Натрия селенат | 13413-01-0 | 29 | 10,2 | 3 | Неорганические соединения; соединения натрия; соединения селена |
Стрихнин | 57-24-9 | 158 | 62,5 | 6 | Органические соединения; гетероциклические соединения |
Таллия I сульфат | 7446-18-6 | 5,74 | 0,152 | 25 | Неорганические соединения; соединения металлов; соединения серы |
Трихлоруксусная кислота | 76-03-9 | 902 | 413 | 5 229 | Органические соединения; карбоновые кислоты |
Триэтиленмеламин | 51-18-3 | 0,272 | 1,85 | 4 | Органические соединения; гетероциклические соединения |
Трифенилтина гидрооксид | 76-87-9 | 0,017 | 0,01 | 329 | Органические соединения; металлорганические соединения |
Вальпроевая кислота | 99-66-1 | 916 | 512 | 995 | Органические соединения; карбоновые кислоты; липиды |
Верапамила гидрохлорид | 152-11-4 | 34,9 | 66,5 | 111 | Органические соединения; амины |
Ксилен | 1330-20-7 | 721 <5> | 466 <5> | 4 667 | Органические соединения; циклические углеводороды |
Сокращения: 3T3 - фибробласты BALB/c 3T3; CAS - Реферативная служба по химии (Chemical Abstracts Service); NHK - нормальные эпидермальные кератиноциты человека; NRU - поглощение нейтрального красного; НД - нет данных. <1> Среднее геометрическое значение IC50 средних геометрических значений, полученных в лабораториях (по данным трех лабораторий, если не указано иное). <2> Основано на средних геометрических приемлемых значениях LD50 для взрослых лабораторных крыс, если не указано иное. <4> Соответствующий класс каждой исследуемой химической продукции присвоен на основе стандартной схемы классификации, которая реализована в системе классификации Национальной медицинской библиотеки США, принятой для медицинских предметных заголовков (Medicine Medical Subject Headings - MeSH) (http://www.nlm.nih.gov/mesh/meshhome.html). | |||||
(справочное)
ПРИМЕНЕННОГО В НЕМ МЕЖДУНАРОДНОГО ДОКУМЕНТА
Таблица ДА.1
Структура настоящего стандарта | Структура международного документа | |||
Разделы | Пункты | Перечисления | Пункты | Перечисления |
1 - 10 | - | |||
- | - | 16 | - | |
- | - | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | Приложение 1 | - | ||
- | 11 | - | ||
- | 12 | - | ||
- | 13 | - | ||
- | 14 | - | ||
- | 15 | - | ||
- | 16 | - | ||
- | 17 | - | ||
- | 18 | - | ||
- | 19 | - | ||
- | 20 | - | ||
- | 21 | - | ||
- | 22 | - | ||
- | 23 | - | ||
- | 24 | - | ||
- | 25 | - | ||
- | 26 | - | ||
- | 27 | - | ||
- | 28 | - | ||
- | 29 | - | ||
- | 30 | - | ||
- | 31 | - | ||
- | 32 | - | ||
- | 33 | - | ||
- | 34 | - | ||
- | 35 | - | ||
- | 36 | - | ||
- | 37 | - | ||
- | 38 | - | ||
- | 39 | - | ||
- | 40 | - | ||
- | 41 | - | ||
- | 42 | - | ||
- | 43 | - | ||
- | 44 | - | ||
- | 45 | - | ||
- | 46 | - | ||
- | 47 | - | ||
- | 48 | - | ||
- | 49 | - | ||
- | 50 | - | ||
- | 46 | - | ||
- | 47 | - | ||
- | 48 | - | ||
- | 49 | - | ||
- | 50 | - | ||
- | 51 | - | ||
- | 52 | - | ||
- | 53 | - | ||
- | 54 | - | ||
- | 55 | - | ||
- | 56 | - | ||
- | 57 | - | ||
- | 58 | - | ||
- | 59 | - | ||
- | 60 | - | ||
- | 61 | - | ||
- | 62 | - | ||
- | 63 | - | ||
- | 64 | - | ||
- | 65 | - | ||
- | 66 | - | ||
- | 67 | - | ||
- | 68 | - | ||
- | 69 | - | ||
- | Приложение 2 | - | ||
- | Приложение 3 | - | ||
- | Приложение 4 | - | ||
- | Приложение 5 | - | ||
- | Приложение 6 | - | ||
- | Приложение 7 | - | ||
- | Приложение 8 | - | ||
Литература | ||||
Bondesson, I., Ekwall, B., Hellberg, S., Romert, L., Stenberg, K., Walum, E. (1989), MEIC - A new international multicenter project to evaluate the relevance to human toxicity of in vitro cytotoxicity tests. Cell. Biol. Toxicol. 5:331-347 (Новый международный мультиинституциональный проект для оценивания значимости результатов цитотоксических испытаний in vitro при определении токсичности веществ для человека) | |
Borenfreund, E., and Puerner, J.A. (1985), Toxicity determination in vitro by morphological alterations and neutral red absorption. Toxicology Letters 24:119-124 (Определение токсичности in vitro на основе данных о морфологических изменениях и поглощении нейтрального красного) | |
Bulgheroni, A., Kinsner-Ovaskainen, A., Hoffmann, S., Hartung, T., Prieto, P. (2009), Estimation of acute oral toxicity using the No Observed Adverse Effect Level (NOAEL) from the 28 day repeated dose toxicity studies in rats. Regul Toxicol Pharmacol Feb; 53(1): 16-9 (Оценка острой оральной токсичности по уровню, не вызывающему видимых неблагоприятных воздействий (NOAEL), в соответствии с данными 28-дневных испытаний на токсичность повторной дозы с использованием крыс в качестве подопытных животных) | |
Ekwall, B., Ekwall, B.,  , M. (2000), MEIC evaluation of acute systemic toxicity: Part VIII. Multivariate partial least squares evaluation, including the selection of a battery cell line tests with a good prediction of human acute lethal peak blood concentrations for 50 chemicals. ATLA, 28:201-234 (Оценка MEIC для острой системной токсичности. Часть VIII. Многовекторная оценка по методу частичных наименьших квадратов, включая комплексные исследования на клеточных линиях с высокой достоверностью прогнозирования летальных пиковых концентраций, вызывающих острую интоксикацию, в крови человека для 50 различных химических веществ) , M. (2000), MEIC evaluation of acute systemic toxicity: Part VIII. Multivariate partial least squares evaluation, including the selection of a battery cell line tests with a good prediction of human acute lethal peak blood concentrations for 50 chemicals. ATLA, 28:201-234 (Оценка MEIC для острой системной токсичности. Часть VIII. Многовекторная оценка по методу частичных наименьших квадратов, включая комплексные исследования на клеточных линиях с высокой достоверностью прогнозирования летальных пиковых концентраций, вызывающих острую интоксикацию, в крови человека для 50 различных химических веществ) | |
US EPA (1996), Product Properties Test Guidelines. OPPTS 830.7840 Water Solubility: Column Elution Method; Shake Flask Method. Office of Prevention, Pesticides and Toxic Substances. EPA 712-C-98-041. Available: [http://www.epa.gov/opptsfrs/publications/OPPTS_Harmonized/830_Product_Properties_Test_Guidelines/Series/830-7840.pdf] (Определение растворимости в воде. Метод элюирования в колонке, метод встряхивания колбы) | |
Halle, W. (1998),  in Zellkulturen in Zellkulturen  (LD50) zur Einsparung von Tierversuchen. Life Sciences/Lebenswissenschaften, Volume 1, (LD50) zur Einsparung von Tierversuchen. Life Sciences/Lebenswissenschaften, Volume 1, | |
Halle, W. (2003), The Registry of Cytotoxicity: Toxicity testing in cell cultures to predict acute toxicity (LD50) and to reduce testing in animals. Alternatives to Laboratory Animals 31:89-198. (English translation of Halle 1998) (Реестр цитотоксических веществ. Испытания токсичности на клеточных культурах для прогнозирования уровня острой токсичности (LD50) в целях сокращения объемов опытов, проводимых на животных. Перевод на английский язык текста, опубликованного Halle в 1998 г.) | |
ICCVAM. 2009. Report on the ICCVAM-NICEATM/ECVAM/JaCVAM Scientific Workshop on Acute Chemical Safety Testing: Advancing In Vitro Approaches and Humane Endpoints for Systemic Toxicity Evaluations. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available: http://iccvam.niehs.nih.gov/methods/acutetox/toxwksp-rpt.htm (Отчет об итогах научно-практического семинара ICCVAM-NICEATM/ECVAM/JaCVAM по исследованиям опасности веществ, обладающих острым токсическим воздействием. Новое в области применения методов исследования in vitro и данных о критических показателях воздействия на человека для оценивания уровня системной токсичности) | |
ICCVAM (2006a), Background Review Document: In Vitro Basal Cytotoxicity Test Methods for Estimating Acute Oral Systemic Toxicity. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available: [http://iccvam.niehs.nih.gov/methods/acutetox/inv_nru_brd.htm] (Справочный обзорный документ. Методы исследования базовой цитотоксичности in vitro для определения уровня острой пероральной системной токсичности) | |
ICCVAM (2006b), Peer Review Panel Report: The Use of In Vitro Basal Cytotoxicity Test Methods for Estimating Starting Doses for Acute Oral Systemic Toxicity Testing. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available [http://iccvam.niehs.nih.gov/methods/acutetox/inv_nru_scpeerrev.htm] (Отчет независимой группы экспертов. Применение методов исследования базовой цитотоксичности in vitro для определения значений начальной дозы при исследованиях острой пероральной системной токсичности) | |
ICCVAM (2006c), ICCVAM Test Method Evaluation Report: In Vitro Cytotoxicity Test Methods for Estimating Starting Doses for Acute Oral Systemic Toxicity Tests. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available: [http://iccvam.niehs.nih.gov/methods/acutetox/inv_nru_tmer.htm] (Отчет об оценке методов исследований. Применение методов исследования базовой цитотоксичности in vitro для определения значений начальной дозы при исследованиях острой пероральной системной токсичности) | |
ICCVAM (2001a), Report of the International Workshop on In Vitro Methods for Assessing Acute Systemic Toxicity. NIH Publication No. 01-4499. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available: [http://iccvam.niehs.nih.gov/methods/acutetox/inv_cyto_wksp.htm] (Отчет о проведении международного семинара по методам оценивания последствий острой системной токсичности in vitro) | |
ICCVAM (2001b), Guidance Document on Using In Vitro Data to Estimate In Vivo Starting Doses for Acute Toxicity. NIH Publication No. 01-4500. Research Triangle Park, NC: National Institute for Environmental Health Sciences. Available: http://iccvam.niehs.nih.gov/methods/acutetox/inv_cyto_guide.htm] (Руководящий документ по использованию данных in vitro для оценивания значений начальной дозы при исследовании острой токсичности in vivo) | |
[14] <1> | OECD. 2008, Acute Oral Toxicity - Up-and-Down Procedure. OECD Guideline for Testing of Chemicals No. 425, Paris, France. Available at: [http://www.oecd.org/env/testguidelines] (Острая пероральная системная токсичность. Метод "вверх и вниз") |
[15] <2> | OECD. 2001a. Acute Oral Toxicity - Acute Toxic Class Method. OECD Guideline For Testing of Chemicals No. 423, Paris, France. Available at: [http://www.oecd.org/env/testguidelines] (Острая токсичность при пероральной токсичности. Метод определения класса острой токсичности) |
[16] <3> | OECD (2001b), Acute Oral Toxicity - Fixed Dose Procedure. OECD Guideline for Testing of Chemicals No. 420, OECD, Paris. Available at: [http://www.oecd.org/env/testguidelines] (Острая пероральная системная токсичность. Методика "фиксированной дозы") |
Seibert, H., Balls, M., Fentem, J.H., Bianchi, V., Clothier, R.H., Dierickx, P.J., Ekwall B., Garle, J.J.,  , M.J., Gribaldo, L., , M.J., Gribaldo, L., | |
Spielmann, H., Genschow, E., Liebsch, M., and Halle, W. (1999), Determination of the starting dose for acute oral toxicity (LD50) testing in the up and down procedure (UDP) from cytotoxicity data. Altern. Lab. Anim. 27:957-966 (Определение начальной дозы вещества при оценивании острой пероральной токсичности (LD50) по методу "вверх и вниз" (UDP) с использованием данных о его цитотоксичности) | |
Stokes, W., Casati, S., Strickland, J., Paris, M. (2008), Neutral Red Uptake Cytotoxicity Tests for Estimating Starting Doses for Acute Oral Toxicity Tests. Cur. Protocol. Toxicol. 36: 20.4.1-20.4.20. UN (2007), United Nations Globally Harmonized System of Classification and Labelling of Chemicals (GHS), ST/SG/AC. 10/30, UN New York and Geneva. Available: [http://www.unece.org/trans/danger/publi/ghs/ghs_welcome_e.html] (Испытания на поглощение нейтрального красного при определении значений начальной дозы для исследований острой пероральной системной токсичности) |
--------------------------------
<1> Принят ГОСТ 34557-2019.
<2> Принят ГОСТ 32644-2014.
УДК 661:615.099:006.354 | MOD | |
Ключевые слова: химическая продукция, цитотоксичность, острая пероральная системная токсичность, метод NRU 3T3, метод NRU NHK | ||