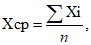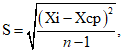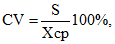СПРАВКА
Источник публикации
"Бюллетень нормативных и методических документов Госсанэпиднадзора", выпуск 3 (93), сентябрь 2023
Примечание к документу
Название документа
"МР 4.2.0287-22. 4.2. Методические рекомендации. Методы контроля. Биологические и микробиологические факторы. Организация внутреннего контроля качества в лабораториях, проводящих исследования на специфические антитела к вирусу кори методом иммуноферментного анализа"
(утв. Роспотребнадзором 30.05.2022)
"МР 4.2.0287-22. 4.2. Методические рекомендации. Методы контроля. Биологические и микробиологические факторы. Организация внутреннего контроля качества в лабораториях, проводящих исследования на специфические антитела к вирусу кори методом иммуноферментного анализа"
(утв. Роспотребнадзором 30.05.2022)
Содержание
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
А.Ю.ПОПОВА
30 мая 2022 года
4.2. МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ
И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
ОРГАНИЗАЦИЯ ВНУТРЕННЕГО КОНТРОЛЯ КАЧЕСТВА В ЛАБОРАТОРИЯХ,
ПРОВОДЯЩИХ ИССЛЕДОВАНИЯ НА СПЕЦИФИЧЕСКИЕ АНТИТЕЛА
К ВИРУСУ КОРИ МЕТОДОМ ИММУНОФЕРМЕНТНОГО АНАЛИЗА
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
МР 4.2.0287-22
1. Разработаны ФБУН "Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г.Н. Габричевского" Роспотребнадзора (А.П. Топтыгина, Т.А. Мамаева, М.А. Смердова, М.А. Наумова, Н.В. Тураева, О.В. Цвиркун, Т.С. Чехляева); ФБУН "Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера" Роспотребнадзора (Н.В. Железнова, М.А. Бичурина).
2. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 30 мая 2022 г.
3. Введены впервые.
1.1. В настоящих методических рекомендациях (далее - МР) представлен алгоритм проведения внутреннего контроля качества (далее - ВКК) лабораторных исследований, направленных на выявление специфических антител классов IgM и IgG к вирусу кори методом иммуноферментного анализа (далее - ИФА) с применением внутренних контрольных препаратов (далее - ВКП).
1.2. В МР использована система ВКК, позволяющая определять достоверность получаемых результатов и анализировать с помощью карты Леви-Дженнингса данные, полученные при обследовании больных и переболевших корью, а также привитых против этой инфекции. Алгоритм может применяться при использовании различных контрольных препаратов:
- - собственного изготовления, приготовленных на основе пула положительных сывороток;
- коммерческих препаратов;
- при проведении анализов на тест-системах других производителей.
1.3. МР предназначены для специалистов органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также могут быть использованы научными и медицинскими организациями, исследующими гуморальный иммунитет к антигенам вируса кори методом ИФА.
2.1. Контроль качества лабораторных исследований является одной из важнейших составляющих работы современных клинико-диагностических лабораторий. Проведение мероприятий по ВКК является необходимым условием работы лабораторий, входящих в лабораторную сеть Всемирной организации здравоохранения (далее - ВОЗ) по кори и краснухе.
В рамках международной программы по надзору за корью и краснухой организована единая лабораторная сеть, включающая 10 субнациональных лабораторий в Российской Федерации и 10 лабораторий в странах СНГ [6, 7], в задачи которой входит подтверждение диагноза "корь" с использованием единого протокола исследования методом ИФА в соответствии с рекомендациями ВОЗ [8]. Отсутствие единого контрольного препарата при проведении ВКК и появление ложноположительных антител у лиц с аутоиммунными процессами потребовали усовершенствования контроля качества (далее - КК) исследований методом ИФА и увеличения кратности обследования пациентов на этапе элиминации инфекции [9 - 14].
2.2. Данные серологического мониторинга, а также выборочное изучение состояния специфического гуморального иммунитета к вирусу кори методом ИФА позволяют объективно оценить фактическую защищенность от кори лиц декретированных возрастов и профессиональных групп на территориях всех субъектов Российской Федерации в соответствии с санитарно-эпидемиологическими требованиями <1> и методическими документами <2>. При этом особое значение в лабораторных исследованиях имеют вопросы стабильности определения IgG-антител методом ИФА, позволяющие не только получать достоверную информацию, но и сопоставлять результаты разных исследователей [4, 14].
--------------------------------
<1> Пункт 2727 глава XXXV СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденных постановлением Главного государственного санитарного врача Российской Федерации от 28.01.2021 N 4 (зарегистрировано Минюстом России 15.02.2021, регистрационный N 62500).
<2> МУ 3.1.2943-11 "Организация и проведение серологического мониторинга и состояния коллективного иммунитета к инфекциям, управляемым средствами специфической профилактики (дифтерия, столбняк, коклюш, корь, краснуха, эпидемический паротит, полиомиелит, гепатит B)", утвержденные руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации 15.07.2011.
2.3. Определение восприимчивости к вирусу кори зависит от чувствительности и специфичности тест-систем, используемых в ИФА, а также от правильности интерпретации полученных результатов с учетом клинических и эпидемиологических данных <3> [4, 8].
--------------------------------
<3> Приказ Минздрава Российской Федерации от 07.02.2000 N 45 "О системе мер по повышению качества клинических лабораторных исследований в учреждениях здравоохранения Российской Федерации"; ОСТ 91500.13.0001 "Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов", утвержденный приказом Минздрава России от 26.05.2003 N 220.
При наличии случайных и систематических ошибок при проведении лабораторных исследований необходимо проведение процедур КК, одним из составных частей которого является ВКК. Система ВКК является оперативной формой контроля, данные которой свидетельствуют о степени достоверности полученных результатов.
Необходимость введения контрольного препарата для совершенствования системы ВКК исследований по определению антител к вирусу кори количественным и качественным методом ИФА обусловлена наличием нескольких сертифицированных в Российской Федерации тест-систем, различающихся по своим техническим характеристикам, а также наличием нескольких серий в пределах каждой тест-системы в течение одного года, что затрудняет анализ данных в рамках всей страны в течение длительного временного периода.
Имеющиеся в коммерческих наборах для ИФА внутритестовые контроли не обеспечивают выявления всех ошибок, которые могут повлиять на конечный результат. Использование ВКК в ИФА предусмотрено плановыми мероприятиями ВОЗ во всех лабораториях, входящих в международную лабораторную сеть (около 700 лабораторий) по надзору за корью и краснухой [9].
До ноября 2015 года лаборатории, входящие в лабораторную сеть по кори Российской Федерации и стран СНГ, готовили контрольные образцы для проведения ВКК, используя собственный банк положительных сывороток. Положительные сыворотки, обладая разной специфической активностью, не являются стандартными образцами, и использование их с целью КК может влиять на достоверность получаемых результатов.
2.4. Материально-техническое обеспечение метода ИФА с применением ВКП представлено в приложении 1 к настоящим МР.
контроля качества
3.1. При проведении неколичественными методами ИФА каждой серии лабораторных исследований по определению противокоревых антител с помощью ИФА рекомендуется выполнять контрольные измерения, отображать их результаты на контрольных картах Леви-Дженнингса и на основании полученных данных принимать решение о степени достоверности полученных результатов [8].
Основной целью ВКК является выявление, оценка и оперативное устранение ошибок, возникающих в процессе лабораторных исследований. Данные ошибки могут быть связаны со сбоем в используемой аналитической системе, условиями окружающей среды и работой оператора.
Оперативная информация о напряженности специфического иммунитета необходима при расследовании последствий иммунизации и оценки уровня иммунитета населения к кори для проведения дополнительной вакцинации серонегативных лиц в индикаторных группах или ревакцинации.
Для лабораторий, входящих в лабораторную сеть ВОЗ по кори и краснухе, введение и использование в повседневной практике процедур ВКК является обязательным условием получения и продления аккредитации ВОЗ.
3.3. Факторами, влияющими на достоверность результатов при использовании положительных сывороток в качестве контрольных материалов, являются:
- объем образца и/или реагентов;
- качество аналита;
- соблюдение температурных режимов на всех этапах исследования, в том числе при хранении и транспортировке образцов;
- время инкубации и получения результатов;
- правильность записей и передачи результатов;
- тип и качество используемой тест-системы (в частности, тип встроенных в тест-систему контролей);
- проблемы с калибровкой средств измерений;
- особенности работы оператора, проводящего исследования.
- отсутствие стандартного алгоритма проведения мероприятий по ВКК.
3.4. В Российской Федерации разработаны ВКП <4> для исследования IgM-антител к вирусу кори (далее - ВКП-IgM) и IgG-антител (далее - ВКП-IgG) <5>, которые безвозмездно предоставляются в лаборатории, сертифицированные ВОЗ для диагностики кори и краснухи.
--------------------------------
3.5. Контрольные препараты для ВКК исследований могут быть:
- нативными, приготовленными на основе банка положительных сывороток;
- лиофилизированными, приготовленными промышленным способом для одной лаборатории или лабораторной сети (некоммерческие);
- лиофилизированными, приготовленными промышленным способом и находящимися в свободной продаже (коммерческие).
Условия при проведении ВКК серологических исследований вне зависимости от типа препарата [8]:
- контрольные материалы готовятся из биологического материала, родственного исследуемым образцам;
- рабочий раствор контрольного препарата (цельный или его рабочее разведение) не должен содержать нецелевые маркеры;
- процедура получения рабочего раствора должна быть последовательна (разведение исходного препарата, тестирование цельного препарата и его разведений в ИФА, определение сходимости), а полученные результаты воспроизводимы;
- контрольный препарат исследуется в аналитических сериях и условиях, как пробы пациентов;
- контрольный препарат должен проходить все этапы подготовки к проведению процедуры ВКК при переходе на новую тест-систему.
3.6. Проведение процедуры ВКК осуществляется в соответствии с алгоритмом ВКК исследований IgM и IgG к вирусу кори методом ИФА с использованием контрольных препаратов согласно приложению 2 к настоящим МР).
Приготовление рабочего раствора контрольных препаратов осуществляется согласно инструкции по их использованию. Контрольный препарат готовится в достаточном для проведения ВКК количестве.
Этапы приготовления и использования рабочего раствора контрольного препарата:
1) выбор рабочего разведения контрольного препарата осуществляют его двукратным титрованием с применением отрицательной донорской сыворотки (далее - ОДС) и тестированием полученных образцов методом ИФА. Подобранное рабочее разведение контрольного препарата должно находиться в диапазоне 2 - 3 cut off <6> (о.е.) в случае определения IgM или в диапазоне 0,5 - 1,5 о.е. при определении IgG;
2) после выбора рабочего разведения контрольного препарата (он может быть цельным, если отвечает вышеуказанным условиям) переходят к процедуре ВКК. Исследуют внутрисерийную сходимость результатов измерений контрольного препарата путем оценки результатов измерений 10 независимых проб подобранного ранее рабочего раствора контрольного препарата методом ИФА в одной аналитической серии на одном планшете с расчетом коэффициента вариации (CV10) по формулам (приложение 3 к настоящим МР). Показатель CV10 контрольного препарата не должен превышать 8% по ГОСТ Р 53133.1 - 4;
3) при выполнении правила CV10 < 8% контрольный препарат (цельный или его рабочее разведение) разливают по 20 мкл (объем, достаточный на одну постановку ИФА), замораживают и хранят при температуре (от минус 25 °C до минус 30 °C) не более 3 мес;
4) оценивается воспроизводимость результатов по результатам измерений 20 проб цельного или выбранного рабочего разведения контрольного препарата в разных аналитических сериях методом ИФА с расчетом коэффициента вариации (CV20) по ГОСТ Р 53133.1 - 4 (приложение 3 к настоящим МР). Результаты могут быть получены одним оператором в течение 20 дней, или 10 дней при проведении 2 измерений в день, или несколькими сотрудниками, которые обычно выполняют анализ в лаборатории;
5) по результатам измерений 20 проб рабочего раствора контрольного препарата с использованием формул (приложение 3 к настоящим МР) строят контрольную карту Леви-Дженнингса. Алгоритм построения контрольной карты представлен в приложении 4 к настоящим МР. Контрольная карта используется для осуществления оперативного (текущего) контроля качества результатов исследования образцов. С этой целью в каждой аналитической серии образцов исследуют готовый контрольный образец с соблюдением процедур, предусмотренных инструкцией к тест-системе;
6) интерпретацию результатов проводят с использованием правил Вестгарда <7> (приложение 5 к настоящим МР). Правила Вестгарда [18] предназначены для проверки стабильности работы аналитической системы и используются при оценке приемлемости результатов анализа образцов.
--------------------------------
<6> Cut off или отсечка - уровень оптической плотности (в единицах оптической плотности), отсекающий отрицательное и положительное значение при тестировании проб сыворотки крови.
<7> Правила Вестгарда позволяют регистрировать отклонение полученного значения протестированного контрольного препарата в пределах колебания среднеквадратического отклонения (S) +/- 2S или +/- 3S, а также позволяют установить систему отслеживания динамики таких отклонений в указанном промежутке.
Для использования правил Вестгарда соблюдаются следующие условия:
1) рабочий раствор контрольного препарата должен соответствовать используемой тест-системе и положениям, изложенным в п. 3.4;
2) карта Леви-Дженнингса должна представлять собой графическую систему, где среднее значение рабочего раствора контрольного препарата и среднеквадратические отклонения (S) были определены на основе 20 повторных измерений рабочего раствора контрольного препарата с помощью используемой тест-системы;
3) учет результатов, полученных методом ИФА, может осуществляться только при соблюдении критериев валидации внутритестовых контролей, установленных производителем используемой тест-системы.
Система правил Вестгарда применяется для интерпретации карт Леви-Дженнингса с двумя или более контролями в каждой аналитической серии, но она может быть использована и в исследованиях с одним контролем. Если результат тестирования контрольного препарата нарушает правила Вестгарда, причины такого отклонения должны быть расследованы и, при необходимости, исследование проведено повторно.
лабораторных исследований на наличие специфических IgM и IgG
антител к вирусу кори методом иммуноферментного анализа
с применением контрольных препаратов <8>
--------------------------------
4.1. Характеристика контрольных препаратов ВКП-IgM и ВКП-IgG, используемых для примера проведения внутреннего контроля качества лабораторных исследований на наличие специфических IgM и IgG антител к вирусу кори методом ИФА:
- ВКП-IgM - лиофилизированный контрольный препарат для оценки качества лабораторных исследований на наличие специфических антител класса M к вирусу кори;
- ВКП - лиофилизированный контрольный препарат для оценки качества лабораторных исследований на наличие специфических антител класса G к вирусу кори.
Дополнительно используется препарат ОДС, представляющий собой отрицательную донорскую сыворотку, не содержащую IgM/IgG к вирусу кори, который используется для приготовления разведений контрольных препаратов ВКП-IgM и ВКП-IgG.
ВКП-IgM и ВКП-IgG, а также ОДС изготавливают на основе сыворотки крови человека, инактивированной прогреванием (56 °C в течение 1 часа). Препараты не должны содержать HBsAg, антител к ВГС, T. Pallidum, ВИЧ-1,2, антиген p24 ВИЧ-1.
Примеры показателей специфической активности препаратов, полученных при аттестации контрольных препаратов с использованием тест-систем разных форматов ("indirect" и "capture"), приводятся в табл.
Таблица
препаратов ВКП-IgM и ВКП-IgG <9>
--------------------------------
<9> Показатели специфической активности (ОП, о.е.) для IgM и (ОП, о.е.) и значения МЕ/мл для IgG в контрольных препаратах (ВКП-IgM и ВКП-IgG) были определены при проведении 24 измерений каждого образца [13].
Контрольный препарат | Тест-система | Среднее значение ОП (о.е.) | Дисперсия (D) | t-статистика | t-критическое | Уровень значимости (p) |
ВКП-IgM | Тест-система 1 (формат "indirect") | 2,83 | 0,02 | 59,78 | 2,03 | 7,85E-30 (< 0,05) |
Тест-система 2 (формат "capture") | 0,70 | 0,007 | ||||
ВКП-IgG | Тест-система 1 | 0,89 | 0,018 | 3,32 | 2,03 | 0,0398 (< 0,05) |
Тест-система 2 | 0,76 | 0,040 |
Для возможности использования наборов разной модификации и разных производителей рекомендуется использовать оптическую плотность (далее - ОП) рабочего раствора контрольного препарата (цельного или его разведения) для неколичественного метода определения IgM в интервале 2 - 3 cut off (о.е.) используемой тест-системы [14].
4.2. Оценка качества лабораторных исследований на наличие специфических антител класса M к вирусу кори с применением контрольного препарата ВКП-IgM и проведение процедур ВКК осуществляется в соответствии с приложением 2 к настоящим МР.
4.3. Оценка качества лабораторных исследований на наличие специфических антител класса G к вирусу кори качественным и количественным методом ИФА с использованием контрольного препарата ВКП-IgG осуществляется в соответствии с приложением 2 к настоящим МР.
к МР 4.2.0287-22
ДЛЯ СЕРОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ <10>
--------------------------------
<10> Примечание. Допускается использование препаратов и оборудования с аналогичными или лучшими характеристиками.
1. Материалы:
- тест-системы для определения концентрации антител к вирусу кори методом ИФА, зарегистрированные в Российской Федерации в установленном порядке <11>;
- ВКП-IgM - лиофильно высушенный препарат, содержащий IgM к вирусу кори;
- ВКП-IgG - лиофильно высушенный препарат, содержащий IgG к вирусу кори;
- ОДС - лиофильно высушенная отрицательная донорская сыворотка;
- вода дистиллированная.
--------------------------------
<11> Постановление Правительства Российской Федерации от 27.12.2012 N 1416 "Об утверждении Правил государственной регистрации медицинских изделий".
2. Оборудование для серологических исследований:
- ламинарный бокс с биологической защитой 2-го класса;
- термостатируемый шейкер для планшетов;
- спектрофотометр, позволяющий проводить измерения оптической плотности растворов в лунках планшета в двухволновом режиме: при основной длине волны 450 нм и длине волны сравнения в диапазоне 620 - 655 нм;
- термостат, поддерживающий температуру (37 +/- 1) °C;
- дозаторы полуавтоматические одноканальные и многоканальные с переменным или фиксированным объемом со сменными наконечниками, позволяющими отбирать объемы жидкости от 5 до 1000 мкл;
- промыватель планшетов ручной или автоматический;
- вортекс для перемешивания содержимого пробирок;
- флаконы стеклянные вместимостью 15 мл;
- бумага фильтровальная лабораторная;
- цилиндр мерный 2-го класса точности вместимостью 1000 мл.
к МР 4.2.0287-22
ИССЛЕДОВАНИЙ IgM И IgG К ВИРУСУ КОРИ МЕТОДОМ ИФА
С ИСПОЛЬЗОВАНИЕМ КОНТРОЛЬНЫХ ПРЕПАРАТОВ
1. Алгоритм внутрилабораторного контроля качества исследований IgM к вирусу кори методом ИФА с использованием контрольных препаратов включает в себя следующие этапы:
1.1. Лиофилизированный контрольный препарат ВКП-IgM необходимо восстановить добавлением 200 мкл дистиллированной воды, тщательно перемешивают.
1.2. Приготовить 2-кратные разведения контрольного препарата ВКП-IgM от 1:2 до 1:128 с использованием ОДС для исследования в 4 параллелях. Разведения тщательно перемешать на вортексе.
1.3. Провести ИФА с применением полученных разведений контрольного препарата ВКП-IgM, согласно инструкции к используемой тест-системе.
1.4. Используя полученные данные, вычислить средний показатель ОП для 4 значений каждого из разведений ВКП-IgM.
1.5. По результатам построить график, где на оси ординат (Y) откладывают средние значения ОП разведений контрольного препарата ВКП-IgM, на оси абсцисс (X) - разведения контрольного препарата ВКП-IgM.
1.6. Определить рабочее разведение контрольного препарата ВКП-IgM, которое устанавливается с помощью построенного графика. Для этого вычисляют значения ОП, равные 2 - 3 значениям cut off. Любое разведение контрольного препарата, находящееся в данном диапазоне ОП, может быть определено как рабочее.
Пример определения разведений препарата ВКП-IgM с использованием тест-систем двух форматов - "indirect" и "capture" - указан на рисунке 2.1.
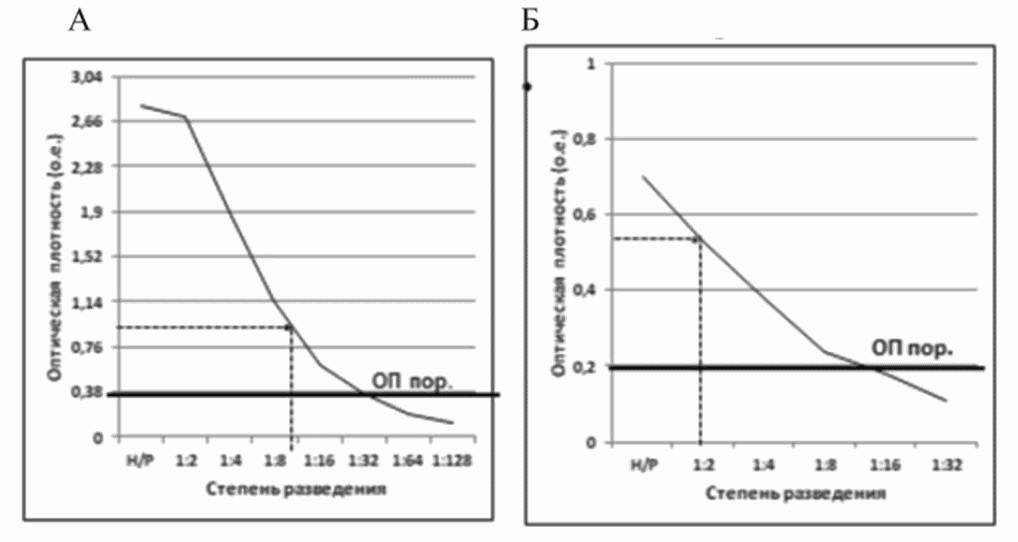
контрольного препарата ВКП-IgM в тест-системах двух
форматов: "indirect" (A) и "capture" (B)
Примечание: пунктирные линии, пересекающие кривую линию зависимости активности контрольного препарата от его разведения, на оси ординат (Y) показывают значение ОП разведения контрольного препарата, а на оси абсцисс (X) - разведение.
Для тест-системы "indirect"-формата разведение контрольного препарата ВКП-IgM 1:10 (ОП = 0,96 о.е.), специфическая активность которого находится в диапазоне 2 - 3 x ОПпор. (0,76 - 1,14 о.е.), является рабочим разведением (далее - рабочий раствор).
Для тест-системы "capture"-формата разведение контрольного препарата ВКП-IgM 1:2 (ОП = 0,56 о.е.), специфическая активность которого находится в диапазоне 2 - 3 x cut off (0,4 - 0,6 о.е.), является рабочим разведением (далее - рабочий раствор).
1.7. Провести оценку внутрисерийной сходимости результатов путем анализа 10 проб каждого подобранного рабочего разведения для каждой тест-системы.
1.8. На основе полученных результатов рассчитать показатель CV10 по формуле (см. приложение 3 к настоящим МР).
Пример результатов определения сходимости значений рабочего раствора ВКП-IgM, полученных с помощью тест-систем разных форматов: "indirect" - CV = S/Xср x 100% = 4,616%; "capture" - CV = S/Xср x 100% = 7,009% - указан в таблице 2.1.
Таблица 2.1
раствора ВКП-IgM, полученные с помощью тест-систем
разных форматов
Формат тест-систем | Оптическая плотность (о.е.) | |||||||||
"indirect" | 0,91 | 0,86 | 0,99 | 0,93 | 0,91 | 0,95 | 0,91 | 0,94 | 0,84 | 0,91 |
"capture" | 0,53 | 0,6 | 0,52 | 0,58 | 0,5 | 0,49 | 0,53 | 0,51 | 0,57 | 0,5 |
1.9. Определить воспроизводимость значения путем анализа результатов 20 проб рабочего разведения ВКП-IgM. Варианты получения значений 20 проб (см. подпункт 4 пункта 3.6).
В качестве примера приведем данные, полученные с помощью тест-систем двух форматов: "indirect" и "capture" (табл. 2.2).
Таблица 2.2
20 проб рабочего раствора ВКП-IgM
Формат тест-систем | Оптическая плотность (о.е.) | |||||||||
"indirect" | 1,23 | 1,14 | 0,99 | 1,16 | 0,91 | 0,95 | 1,25 | 0,94 | 1,15 | 0,91 |
0,91 | 0,86 | 1,19 | 0,93 | 1,25 | 0,96 | 0,91 | 1,23 | 0,84 | 1,12 | |
"capture" | 0,46 | 0,6 | 0,49 | 0,58 | 0,63 | 0,49 | 0,69 | 0,51 | 0,57 | 0,66 |
0,53 | 0,61 | 0,52 | 0,6 | 0,5 | 0,68 | 0,53 | 0,48 | 0,59 | 0,5 | |
1.10. На основе полученных результатов рассчитать показатель CV20 по формуле (приложение 3 к настоящим МР).
Пример: показатели CV20 рабочего раствора контрольного препарата ВКП-IgM по результатам, полученным с помощью тест-систем "indirect"- и "capture"-формата, составляют 13,87% и 12,595% соответственно и не превышают 14,2%, что позволяет приступить к построению контрольной карты.
1.11. Рассчитать среднюю арифметическую величину Xср, среднеквадратическое отклонение S, контрольные пределы: Xср +/- 1S, Xср +/- 2S и Xср +/- 3S.
Пример рассчитанных значений контрольных показателей рабочего раствора ВКП-IgM для тест-систем "indirect"- и "capture"-формата, необходимых для построения контрольной карты Леви-Дженнингса, указан в таблице 2.3.
Таблица 2.3
ВКП-IgM для тест-систем "indirect"- и "capture"-формата
Показатель | "indirect", ОП (о.е.) | "capture", ОП (о.е.) |
Xср | 1,044 | 0,56 |
Ст. откл. (S) | 0,145 | 0,071 |
X + 1S | 1,189 | 0,631 |
X - 1S | 0,899 | 0,489 |
X + 2S | 1,334 | 0,702 |
X - 2S | 0,754 | 0,418 |
X + 3S | 1,479 | 0,773 |
X - 3S | 0,609 | 0,347 |
1.12. Построить контрольные карты Леви-Дженнингса (приложение 4 к настоящим МР).
Пример: на рис. 2.2 представлена контрольная карта и результаты оперативного контроля ВКП-IgM в разведении 1:10, который подвергался процедурам, предусмотренным инструкцией для исследуемых образцов при постановке тест-системы "indirect"-формата.
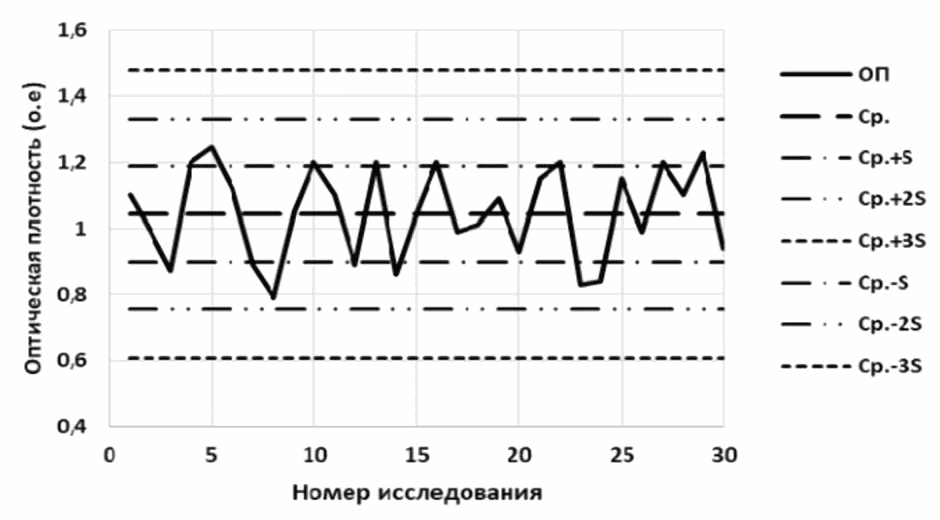
при определении IgM-антител к вирусу кори методом ИФА
с использованием контрольного препарата ВКП-IgM
Показатели ОП рабочего раствора ВКП-IgM нанести на карту, на оси абсцисс (X) которой находится номер исследования (в реальном режиме - дата исследования), а на оси ординат (Y) - значения определяемого контрольного раствора ОП (о.е.).
1.13. Результаты работы аналитической системы оценить в соответствии с правилами Вестгарда (см. приложение 5 к настоящим МР).
1.14. В результате при использовании контрольного препарата ВКП-IgM, предлагаемого в данном примере, для оценки качества лабораторных исследований на наличие специфических антител класса M к вирусу кори рекомендовано рабочее разведение 1:10 для тест-системы "indirect"-формата и разведение 1:2 для тест-системы "capture"-формата.
2. Алгоритм внутрилабораторного контроля качества исследований IgG-антител к вирусу кори методом ИФА с использованием контрольных препаратов включает в себя следующие этапы:
2.1. Лиофильно высушенный препарат ВКП-IgG, содержащий IgG к вирусу кори, восстановить добавлением 200 мкл дистиллированной воды и тщательно перемешать.
2.2. Приготовить 2-кратные разведения контрольного препарата с 1:2 до 1:8 с использованием ОДС, тщательно перемешать на вортексе.
2.3. Осуществить тестирование в ИФА приготовленных разведений, включая исходный цельный препарат в трех повторах.
2.4. Используя полученные данные, вычислить средний показатель ОП для 3 повторов исходного препарата и каждого разведения, после чего построить график, где ось ординат (Y) - средние значения ОП; ось абсцисс (X) - степень разведения образца.
2.5. Далее выбрать рабочее разведение контрольного препарата.
В качестве примера: результаты исследования ВКП-IgG с использованием тест-системы 1 и тест-системы 2, сертифицированных в Российской Федерации (рис. 2.3), показали, что поскольку в тест-системе 1 за величину cut-off принято значение калибратора 0,15 МЕ/мл, соответствующее ОП = 0,108 о.е., то условиям, принятым для контрольного материала на IgM в 2 - 3 cut-off, удовлетворяет разведение 1:2 (ОП = 0,312 о.е.). Данное значение находится в нелинейном участке калибровочной кривой, в котором резко возрастает погрешность измерения, и не удовлетворяет условию нахождения в диапазоне ОП 0,5 - 1,5 о.е., принятом для контрольных препаратов на IgG [17]. Этому условию удовлетворяет цельный контрольный образец (ОП = 0,814 о.е.), так как определяемые значения оказываются в линейной области калибровочной кривой.
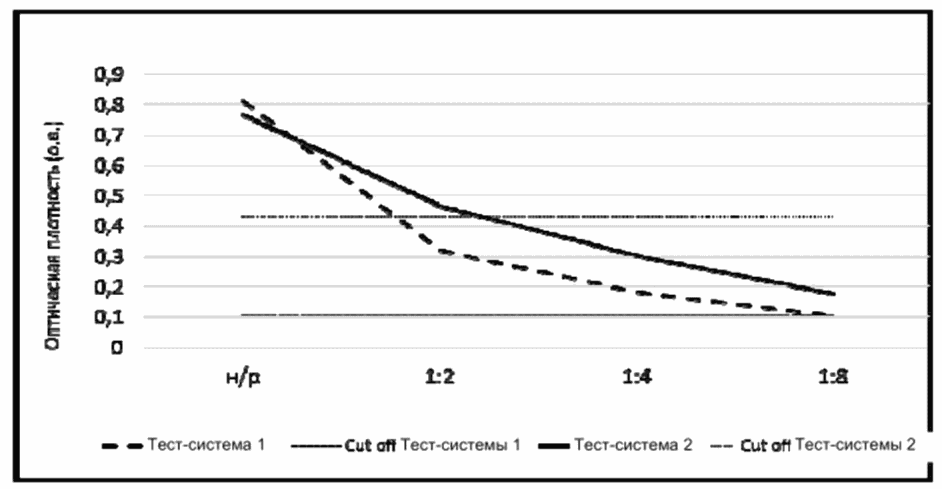
разведения в разных тест-системах
Рассчитанная концентрация контрольного препарата для исследования IgG-антител не должна находиться в зоне значений (точек) калибровочных образцов, входящих в состав набора реагентов, по которым строится калибровочный график от точки к точке. Было доказано, что попадание значения контрольного образца в область точки калибратора резко повышает значение коэффициента вариации [20]. При тестировании ВКП-IgG получили ОП = 0,814 о.е., что соответствует 0,81 +/- 0,13 МЕ/мл, следовательно он не попадает на точки калибраторов с концентрацией 0,5 и 1 МЕ/мл, что важно при проведении исследования количественным способом. В тест-системе 2 за величину cut-off принято значение калибратора 0,15 МЕ/мл, соответствующее ОП = 0,433 о.е.
Условиям, принятым для контрольного материала на IgM в 2 - 3 cut-off, не удовлетворяет даже цельный контрольный образец, так как в этой тест-системе его ОП = 0,765 о.е., что составляет лишь 1,8 cut-off. ОП цельного контрольного образца удовлетворяет условию нахождения в диапазоне ОП 0,5 - 1,5 о.е., а рассчитанная концентрация ВКП-IgG составляет в этой тест-системе 0,72 МЕ/мл, следовательно, он не попадает на точки калибраторов. В результате проведенных исследований было показано, что для оценки сходимости результатов, построения контрольных карт и проведения оперативного контроля при исследовании IgG-антител критерий в 2 - 3 cut-off не подходит. Следует ориентироваться на критерий попадания ОП контрольного препарата (цельного или его разведения) в диапазон 0,5 - 1,5 о.е. и непопадания на точки калибраторов при количественном методе оценки результатов.
В качестве примера представлены исследования с применением ВКП-IgG в тест-системе 1, зарегистрированной в Российской Федерации. В данном случае цельный препарат ВКП-IgG удовлетворяет критерию попадания измеренной ОП в интервал 0,5 - 1,5 о.е. и не попадает в зону точек калибратора.
2.6. Оценить внутрисерийную сходимость результатов 10 измерений контрольного препарата ВКП-IgG в одной аналитической серии методом ИФА.
2.7. На основе полученных результатов рассчитать показатель CV10 по формуле (приложение 3 к настоящим МР). Результаты можно учитывать двумя способами: качественным в ОП (о.е.) и количественным (МЕ/мл).
В таблице 2.4 представлен пример 10 измерений контрольного препарата ВКП-IgG.
Таблица 2.4
контрольного препарата
N | ОП (о.е.) | МЕ/мл |
1 | 0,818 | 0,73 |
2 | 0,795 | 0,71 |
3 | 0,851 | 0,76 |
4 | 0,941 | 0,84 |
5 | 0,739 | 0,66 |
6 | 0,818 | 0,73 |
7 | 0,795 | 0,71 |
8 | 0,840 | 0,75 |
9 | 0,806 | 0,72 |
10 | 0,739 | 0,66 |
Xср | 0,814 | 0,73 |
Ст. откл. (S) | 0,058 | 0,05 |
2.8. Результаты расчетов определения сходимости значений ВКП занести в таблицу. Шаблон таблицы для внесения результатов сходимости измерений ВКП представлен в приложении 6 к настоящим МР.
Показатели CV10 контрольного препарата не должны превышать 8% (см. подпункт 2 пункта 3.6). В рассматриваемом примере CV10 для качественного учета ОП (о.е.) оказался равным 7,1%, а для количественного учета (МЕ/мл) 7,15%. Рассчитанные характеристики удовлетворяют заданному критерию в 8%, что позволяет перейти к следующему этапу. Если полученное значение CV10 превышает 8%, следует найти причину и устранить ее.
2.9. Далее провести оценку воспроизводимости результатов путем анализа тестирования 20 проб цельного контрольного препарата ВКП-IgG методом ИФА (варианты получения значений 20 проб аналогичны указанным для случая ВЛК на IgM-корь, см. подпункт 4 пункта 3.6).
2.10. Используя полученные результаты, рассчитать значения CV20, среднюю арифметическую величину Xср, среднеквадратическое отклонение S, контрольные пределы: Xср +/- 1S, Xср +/- 2S и Xср +/- 3S по формулам (приложение 3 к настоящим МР).
Рассчитанные параметры рассматриваемого примера, необходимые для построения контрольной карты Леви-Дженнингса, представлены в табл. 2.5.
Таблица 2.5
Показатель | ВКП-IgG | |
МЕ/мл | ОП | |
Xср ВЛК | 0,810 | 0,896 |
Ст. откл. (S) | 0,136 | 0,165 |
X + 1S | 0,947 | 1,061 |
X - 1S | 0,675 | 0,731 |
X + 2S | 1,083 | 1,226 |
X - 2S | 0,539 | 0,566 |
X + 3S | 1,218 | 1,392 |
X - 3S | 0,404 | 0,401 |
Значение CV20 не должно превышать 19%. В рассмотренном примере полученные значения для качественного способа составили 18,412%, а для количественного способа определения IgG - 16,74%, что в обоих случаях удовлетворяет требованию. Следовательно, полученные результаты позволяют построить контрольные карты Леви-Дженнингса для качественного ОП (о.е.) и, при необходимости, количественного (МЕ/мл) способов определения IgG-антител к кори методом ИФА соответственно (см. приложение 4 к настоящим МР).
2.11. Построенные контрольные карты использовать для осуществления оперативного (текущего) контроля качества результатов исследования образцов на предмет выявления IgG-антител к вирусу кори методом ИФА. С этой целью в каждой аналитической серии в одной лунке исследовать препарат ВКП-IgG, который подвергается всем процедурам, предусмотренным инструкцией для исследуемых образцов, и измерить показатель оптической плотности (качественная оценка) или рассчитать концентрацию ВЛК (количественная оценка результатов). Полученные результаты нанести на контрольную карту с указанием даты постановки вручную или используя стандартный пакет программ.
2.12. Стабильность работы аналитической системы оценивать согласно правилам Вестгарда [18] (приложение 5 к настоящим МР).
На рис. 2.4 и 2.5 представлены в качестве примера заполненные контрольные карты по результатам измерения ВКП-IgG количественным и качественным способом методом ИФА.
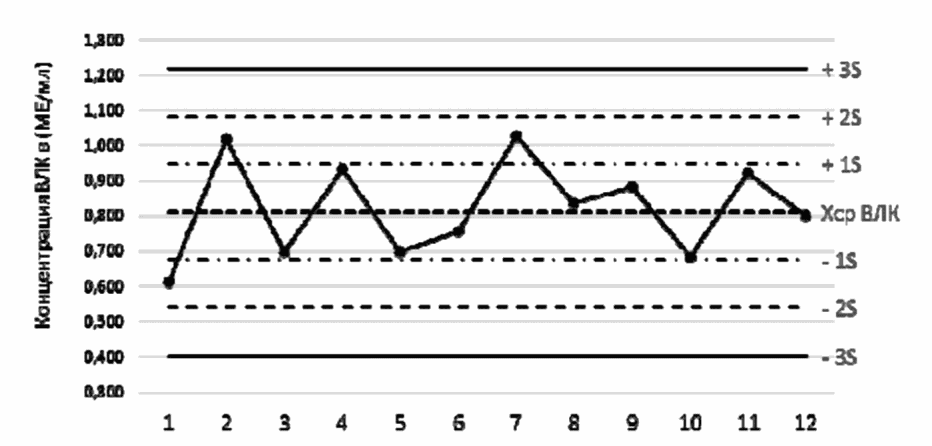
концентрации антител класса IgG к вирусу кори
количественным методом
Примечание: ось ординат (Y) - результаты тестирования контрольного препарата при каждом эксперименте; ось абсцисс (X) - номер опыта (в реальном режиме следует ставить дату проведения эксперимента).
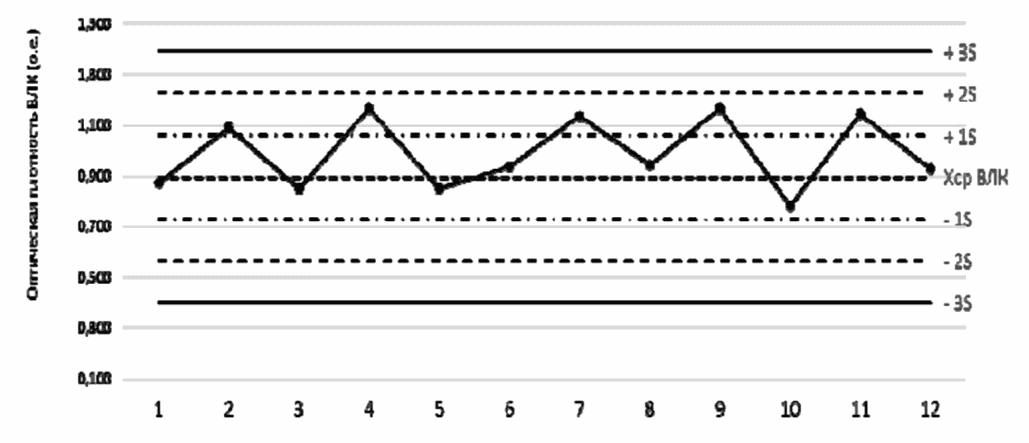
уровня антител класса IgG к вирусу кори качественным методом
Примечание: ось ординат (Y) - результаты тестирования контрольного препарата при каждом эксперименте; ось абсцисс (X) - номер опыта (в реальном режиме следует ставить дату проведения эксперимента).
Результаты измерений ВКП-IgG находились в соответствии с контрольными правилами, что свидетельствует о правильности проведения исследования IgG-антител к вирусу кори методом ИФА.
3. Алгоритм внутрилабораторного контроля качества исследований IgM- и IgG-антител к вирусу кори методом ИФА с использованием контрольных препаратов представлен на схеме (рис. 2.6).
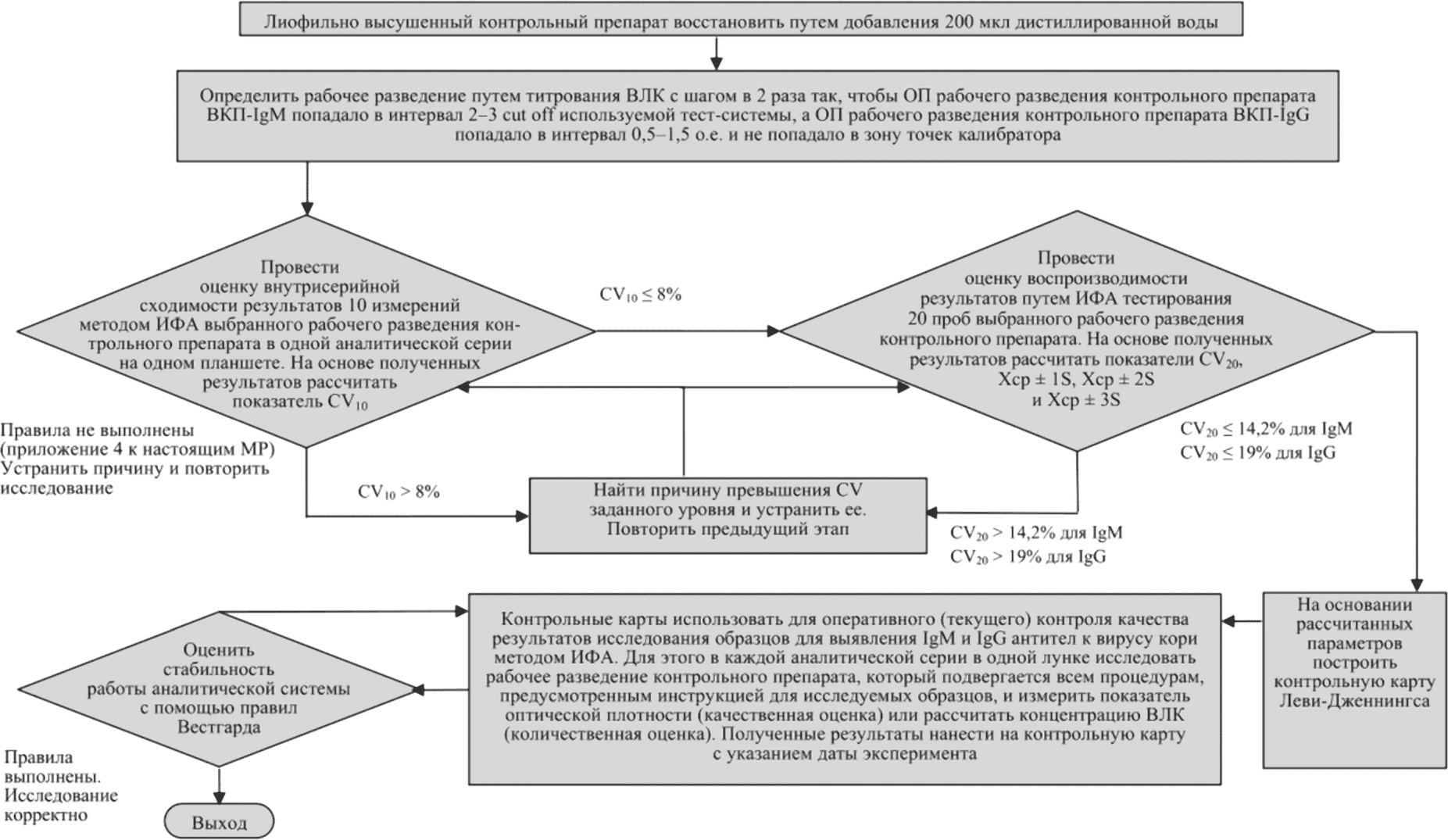
исследований IgM- и IgG-антител к вирусу кори методом ИФА
с использованием контрольных препаратов
к МР 4.2.0287-22
НЕОБХОДИМЫХ ДЛЯ ПОСТРОЕНИЯ КОНТРОЛЬНОЙ КАРТЫ
1. Для расчета среднего значения Xср (1), среднеквадратического отклонения S (2), коэффициента вариации CV (3) образцов следует использовать формулы:
где: Xi - результат конкретного i-го измерения из n выполненных в ОП (о.е.) или концентрация (МЕ/мл);
Xср - среднее значение ОП (о.е.) или концентрация (МЕ/мл);
n - общее количество измерений;
S - среднеквадратическое отклонение ОП (о.е.) или концентрация (МЕ/мл);
CV - коэффициент вариации ОП (о.е.) или концентрация (МЕ/мл).
к МР 4.2.0287-22
1. Карта Леви-Дженнингса - графическая система, позволяющая представить результаты анализа контрольных образцов при проведении исследований ежедневно, а также при проведении исследований на разных аналитических сериях, в сравнении с величиной средней арифметической Xср и среднеквадратического отклонения S, рассчитанных на основе 20 повторных измерений контрольного образца.
2. Для построения карты Леви-Дженнингса необходимо: рассчитать ОПср. для качественного учета результатов или МЕ/мл для количественного учета результатов, рассчитать среднюю концентрацию, их среднеквадратические отклонения S, его контрольные пределы +/- 1S, +/- 2S, +/- 3S и коэффициент вариации CV20 по формулам, представленным в приложении 2 к настоящим МР.
3. Затем данные, полученные согласно п. 2, представить на графике, через середину оси ординат которого проводят линию, соответствующую средней арифметической величине Xср, и параллельно этой линии отмечаются линии, соответствующие контрольным пределам:
Xср +/- 1S - контрольный предел - "1 среднеквадратическое отклонение";
Xср +/- 2S - контрольный предел - "2 среднеквадратических отклонения";
Xср +/- 3S - контрольный предел - "3 среднеквадратических отклонения".
4. По оси абсцисс откладываются даты проведения эксперимента.
5. Расчеты могут быть выполнены с использованием компьютерных программ.
6. Образец карты Леви-Дженнингса представлен на рис. 4.1.
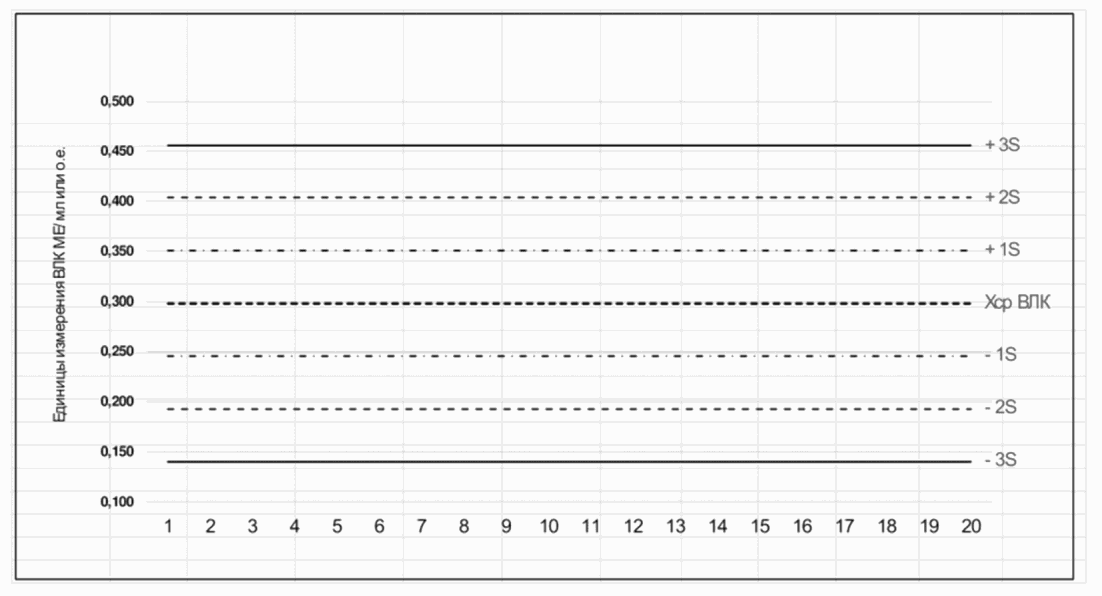
к МР 4.2.0287-22
ПРИ ИССЛЕДОВАНИЯХ ОБРАЗЦОВ НА АНТИТЕЛА К ВИРУСУ КОРИ (ИФА),
С ИСПОЛЬЗОВАНИЕМ ПРАВИЛ ВЕСТГАРДА
N | Карта. Правила Вестгарда | Проблема | Устранение | |
1 | Карта 1 | Правило Вестгарда 12S | Результат одного измерения находится за пределами (+2S) или (-2S) от среднего значения контроля (Xср). Правило Вестгарда 12S предупреждает о наличии случайной ошибки в данной аналитической системе | Сравнить полученный результат с данными, полученными в предыдущих аналитических сериях. Если не выявляется никакой закономерности, то можно сделать вывод о том, что нарушение вызвано случайной ошибкой и результаты пациентов могут быть выданы. При этом около 4,5% контрольных результатов могут находиться в пределах 2S - 3S [18] |
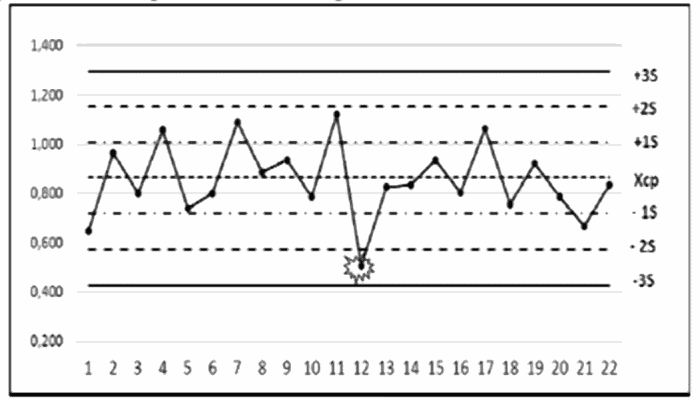 | ||||
Точка 12 | ||||
2 | Карта 2 | Правило Вестгарда 13S | Результат одного измерения находится за пределами (+3S) или (-3S) от среднего значения контроля (Xср). Правило Вестгарда 13S предупреждает о наличии недопустимой случайной ошибки или начале большой систематической ошибки (сдвиг) | Отбраковать аналитическую серию, проверить работу оборудования, работу оператора, валидацию внутри тестовых контролей и осуществить повторную постановку |
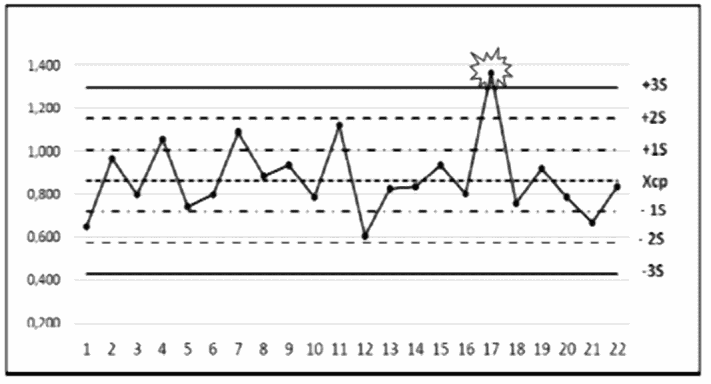 | ||||
Точка 17 | ||||
3 | Карта 3 | Правило Вестгарда R4S/1* | 1 вариант. Результат одного измерения (точка 5) находится на расстоянии >= 4S от предыдущего измерения (точка 4). 2 вариант. Результат одного измерения (точка 11) находится на расстоянии >= 4S от предыдущего измерения (точка 10). Правило Вестгарда R4S предупреждает о наличии случайной ошибки | Проверить работу оборудования, работу оператора, валидацию внутри тестовых контролей. 1 вариант. Если измерение (точка 5) >= (-2S), а предыдущее значение (точка 4) >= (+2S), то осуществляем перестановку отрицательных результатов, которые попали в интервал (ОПкр. - 20%). 2 вариант. Если последнее измерение (точка 11) >= (+2S), а предыдущее значение (точка 10) >= (-2S), то осуществляем перестановку положительных результатов, которые попали в интервал (ОПкр. + 20%) [18] |
(см. примечание) | ||||
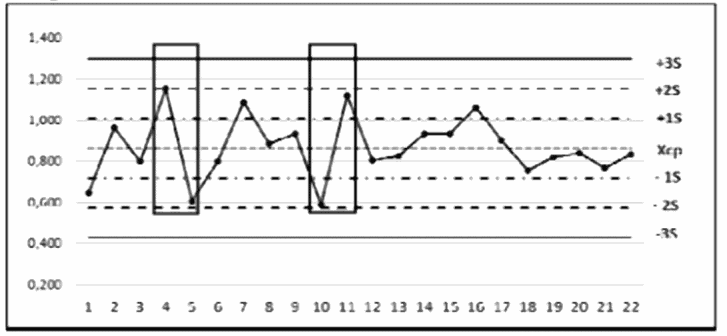 | ||||
Точки: 4, 5 и 10, 11 | ||||
4 | Карта 4 | Правило Вестгарда 41S | Результаты последовательных четырех измерений находятся по одну сторону за пределами (+1S) или (-1S) от среднего значения контроля (Xср). Правило Вестгарда 41S предупреждает о наличии систематической ошибки | При нарушении правила 41S необязательно отменять полученные результаты и проводить повторное измерение. Правило Вестгарда 41S выявляет небольшие систематические ошибки (смещение или дрейф). Такие ошибки могут быть устранены при технической проверке оборудования, проведении инструктажа для оператора, проверке валидации внутри тестовых контролей |
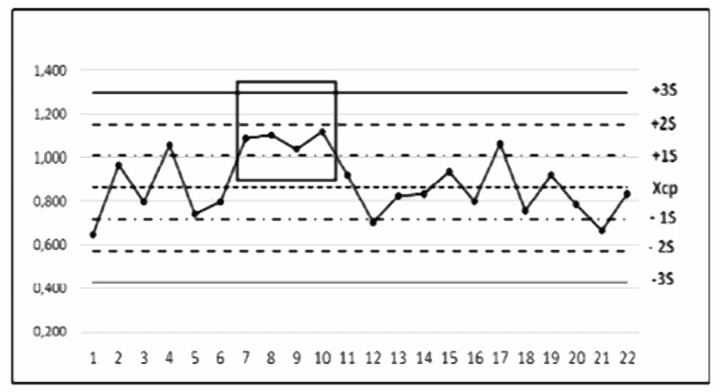 | ||||
Точки 7 - 10 | ||||
5 | Карта 5 | Правило Вестгарда 22S | Результаты последовательных двух измерений находятся по одну сторону за пределами (+2S) или (-2S) от среднего значения контроля (Xср). Правило Вестгарда 22S предупреждает о наличии систематической ошибки | Проверить работу оборудования, работу оператора; валидацию внутри тестовых контролей. Если измерение больше (+2S), то осуществляем перестановку положительных результатов, которые попали в интервал (ОПкр. + 20%). Если измерение ниже (-2S), то осуществляем перестановку отрицательных результатов, которые попали в интервал (ОПкр. - 20%) [18] |
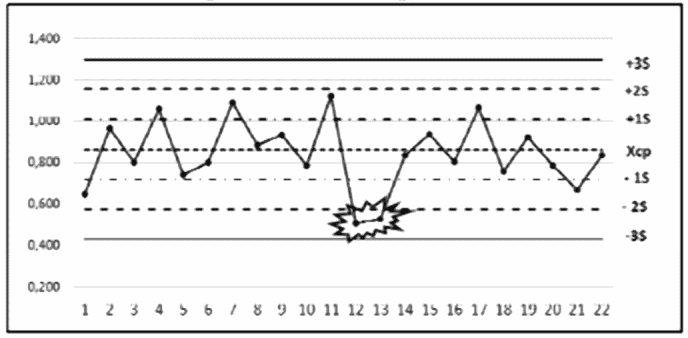 | ||||
Точки 12 - 13 | ||||
6 | Карта 6 | Правило Вестгарда 10x | Результаты последовательных десяти измерений находятся по одну сторону от среднего значения контроля (Xср) независимо от контрольных пределов, в которых они находятся. Правило Вестгарда 10x предупреждает о наличии систематической ошибки | При нарушении правила 10x необязательно отменять полученные результаты и проводить повторное измерение. Правило Вестгарда 10x выявляет небольшие систематические ошибки (смещение или дрейф). Такие ошибки могут быть устранены при технической проверке оборудования, проведении инструктажа для оператора, проверке валидации внутри тестовых контролей, проверке контроля в 2 аналитических системах. /2* (примечание) |
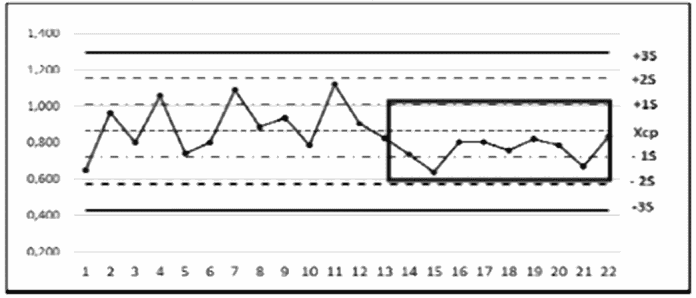 | ||||
См. на точки 13 - 22 | ||||
Примечание: "/1*" - правило Вестгарда R4S может также применяться при использовании контроля в 2 повторах в одной аналитической серии: результат одного измерения находится на расстоянии >= 4S от другого измерения при соблюдении критериев валидации внутри тестовых контролей. Предполагаемая причина - ошибка при постановке. Устранение - повторить постановку. "/2*" - проверка контроля в 2 аналитических системах (наборах одной серии): а) приготовить новый рабочий раствор контроля; б) вновь приготовленный и ранее используемый контроли внести в плашки (нового и используемого), провести реакцию. Если результаты ОП обоих контролей, полученные на новом наборе одинаковы и находятся в зоне пересечения Xср и выше, а на используемом наборе получены одинаково низкие показатели (ниже Xср), то причиной ошибки (10x) является используемый набор. При этом показатели внутри тестовых контролей и калибраторов также снижаются. Если результаты нового контроля выше результатов используемого контроля в обоих наборах, то причиной ошибки (10x) является сам используемый контроль, который следует приготовить заново с построением новой операционной карты. | ||||
к МР 4.2.0287-22
(рекомендуемый образец)
РЕЗУЛЬТАТОВ СХОДИМОСТИ ИЗМЕРЕНИЙ ВКП
Дата | Название т/с | Серия т/с | Серия ВКП | Значение ВКП по паспорту ОП/МЕ/мл | Значение ВКП в опыте ОП/Ме/мл | CV% по паспорту ОП/МЕ/мл | CV% рассчитанный ОП/Ме/мл | Вывод |
1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. Постановление Правительства Российской Федерации от 27.12.2012 N 1416 "Об утверждении Правил государственной регистрации медицинских изделий".
3. СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
4. МУ 3.1.2943-11 "Организация и проведение серологического мониторинга и состояния коллективного иммунитета к инфекциям, управляемым средствами специфической профилактики (дифтерия, столбняк, коклюш, корь, краснуха, эпидемический паротит, полиомиелит, гепатит B)".
5. ГОСТ Р 53133.1 - 4 "Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований".
6. Национальный план мероприятий по реализации программы "Элиминация кори и краснухи, достижение спорадической заболеваемости эпидемическим паротитом в Российской Федерации (2021 - 2025 гг.)".
7. Тихонова Н.Т., Мамаева Т.А., Шульга С.В., Ежлова Е.Б., Лыткина И.Н., Цвиркун О.В., Герасимова А.Г. Лабораторное обеспечение Программы ликвидации эндемичной кори в Российской Федерации // Эпидемиология и вакцинопрофилактика. 2011. N 1. С. 36 - 39.
8. WHO. Manual for the Laboratory-based Surveillance of Measles, Rubella, and Congenital Rubella Syndrome; 3nd ed. Geneva. Switzerland: WHO, 2018.
9. European Centre for Disease Prevention and Control (ECDC). Epidemiological update: Measles - monitoring European outbreaks, 7 July 2017. Stockholm: ECDC; [Accessed 31 Aug 2017]. Available from: https://ecdc.europa.eu/en/news-events/epidemiological-update-measles-monitoring-european-outbreaks-7-july-2017.
10. Filia A., Bella A., Del Manso M., Baggieri M., Magurano F., Rota M.C. Ongoing outbreak with well over 4,000 measles cases in Italy from January to end August 2017 - what is making elimination so difficult? Euro Surveill. 2017. Vol. 22 (37), P. 30614.
11. World Health Organization Regional Office for Europe (WHO/Europe). Fifth Meeting of the European Regional Verification Commission for Measles and Rubella Elimination (RVC) 24 - 26 October 2016, Copenhagen, Denmark. Copenhagen: WHO/Europe; [Accessed 31 Aug 2017]. Available from: http://www.euro.who.int/_data/assets/pdf_file/0005/330917/5th-RVC-meeting-report.pdf?ua=1.
12. Топтыгина А.П., Мамаева Т.А., Алешкин В.А. Особенности специфического гуморального иммунного ответа против вируса кори // Инфекция и иммунитет. 2013. Т. 3. N 3. С. 243 - 250.
13. Цвиркун О.В., Герасимова А.Г., Тихонова Н.Т., Ежлова Е.Б., Мельникова А.А., Дубовицкая Е.Л., Орлова А.А., Басов А.А., Фролов Р.А. Заболеваемость корью в разных возрастных группах в период элиминации инфекции // Эпидемиология и вакцинопрофилактика. 2017. Т. 16. N 3. С. 18 - 25.
14. Мамаева Т.А., Железнова Н.В., Наумова М.А., Говорухина М.В., Калашикова Н.А., Бичурина М.А., Мукомолов С.Л. Алгоритм лабораторного подтверждения и дифференциальной диагностики коревой инфекции в период элиминации кори в Российской Федерации // Инфекция и иммунитет. 2015. Т. 5. N 1. С. 55 - 62.
15. Голева О.В., Самойлова И.Г., Мурина Е.А., Мундруева А.А. Особенности противокоревого иммунитета у населения Санкт-Петербурга // Эпидемиология и вакцинопрофилактика. 2012. N 6. С. 25 - 29.
16. Топтыгина А.П., Смердова М.А., Наумова М.А., Владимирова Н.П., Мамаева Т.А. Влияние особенностей популяционного иммунитета на структуру заболеваемости корью и краснухой // Инфекция и иммунитет. 2018. Т. 8. N 3. С. 341 - 348.
17. Нетесова И.Г., Бобкова М.Р. Проведение внутрилабораторного контроля качества неколичественных методов иммуноферментного анализа // Справочник заведующего КДЛ. 2011. N 6. С. 9 - 15.
18. Westgard, J.O. Design of internal quality control for reference value studies // Clin Chem Lab Med 2004. Vol. 42. P. 863 - 867.
19. Мамаева Т.А., Железнова Н.В., Наумова М.А., Чехляева Т.С., Воробейчиков Е.В., М. Бен Маму, Алешкин В.А. Совершенствование контроля качества исследований методом ИФА при лабораторном подтверждении кори и краснухи на этапе элиминации этих инфекций // Инфекция и иммунитет. 2017. Т. 7. N 1. С. 69 - 78.
20. Смердова М.А., Мамаева Т.А., Наумова М.А., Корецкий К.А., Иванов Д.С., Топтыгина А.П. Опыт проведения внутрилабораторного контроля качества при определении антител класса G к вирусу кори методом иммуноферментного анализа с помощью контрольного материала // Российский иммунологический журнал. 2019. Т. 13 (22). N 4. С. 1402 - 1410.