СПРАВКА
Источник публикации
Документ опубликован не был
Примечание к документу
В соответствии с Приказом Минздрава России от 29.10.2015 N 771 данный документ введен в действие с 1 января 2016 года.
Текст документа приведен в соответствии с публикацией на сайте http://femb.ru/feml, и разделен в Информационном банке на отдельные фармакопейные статьи.
Название документа
Фармакопейная статья "Вакцина сибиреязвенная комбинированная. ФС.3.3.1.0017.15"
("Государственная фармакопея Российской Федерации. XIII издание. Том III")
Фармакопейная статья "Вакцина сибиреязвенная комбинированная. ФС.3.3.1.0017.15"
("Государственная фармакопея Российской Федерации. XIII издание. Том III")
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Вакцина сибиреязвенная комбинированная | ФС.3.3.1.0017.15 Взамен ГФ Х, ст. 713 ФС 42-3297-96 |
Настоящая фармакопейная статья распространяется на вакцину сибиреязвенную комбинированную, лиофилизат для приготовления суспензии для подкожного введения, представляющую собой лиофилизированную в стабилизирующей среде смесь взвеси живых спор вакцинного штамма Bacillus anthracis СТИ-1 и концентрированного протективного сибиреязвенного антигена (ПА), адсорбированного на геле алюминия гидроксида.
Вакцина предназначена для профилактики сибирской язвы и обеспечивает развитие специфического иммунитета продолжительностью до 1 года.
Вакцинный штамм В. anthracis СТИ-1 должен иметь типичные культуральные, морфологические, биохимические и генетические свойства; должен обладать остаточной вирулентностью для морских свинок (при введении 50 млн. спор) и белых мышей (10 млн. спор); должен вызывать гибель 50-70% животных; должен быть специфически безопасным для кроликов при введении им 250 млн. спор; индекс иммунитета для морских свинок должен быть не ниже 10000.
Перед приготовлением очередной серии вакцинного штамма проводят его анимализацию путем пассажа через организм морской свинки с последующим отбором типичных колоний, выросших на плотной питательной среде при посеве селезенки.
Технология изготовления вакцины сибиреязвенной комбинированной состоит из получения посевной культуры B. anthracis СТИ-1; глубинного культивирования посевной культуры B. anthracis СТИ-1 для получения нативной споровой культуры; приготовления концентрированной споровой взвеси; приготовления концентрированного протективного антигена (ПА) методом сепарирования нативной культуры штамма B. anthracis СТИ-1 с последующим концентрированием и стерилизующей фильтрацией на установках ультрафильтрации или методом микрофильтрации; сорбции концентрированного ПА на геле алюминия гидроксида; стабилизации сорбированного ПА формальдегидом с последующей отмывкой 0,9% раствором натрия хлорида; смешивания сорбированного концентрированного ПА с концентратом споровой культуры B. anthracis СТИ-1 с последующим розливом, замораживанием, сублимационным высушиванием, герметизацией и упаковкой препарата. В качестве стабилизатора используется сахароза, разрешенная для использования при производстве иммунобиологических лекарственных препаратов.
На стадиях приготовления посевной и нативных культур контролируют pH, концентрацию спор, отсутствие посторонней микрофлоры. Качество ПА определяют по следующим показателям: стерильность, pH, содержание общего азота, алюминия гидроксида и формальдегида.
Описание. Пористая масса серовато-белого цвета.
Восстановленный препарат - гомогенная суспензия серовато-бежевого цвета без посторонних примесей и включений.
Подлинность. Определение подлинности вакцинного штамма В. anthracis СТИ-1 проводят микроскопическим методом. В мазках, окрашенных по Цилю-Нильсену, должны наблюдаться овальные споры розового цвета с красным ободком по периферии.
Определение подлинности ПА проводят методом иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Методика изложена в разделе "Специфическая активность".
Время растворения. Вакцина должна полностью растворяться течение 5 мин в 5 мл 0,9% раствора натрия хлорида при встряхивании.
Время седиментационной устойчивости. Суспензия не должна расслаиваться в течение 5 мин. Определение проводят в соответствии с ОФС "Лекарственные формы для парентерального применения".
Размер частиц. Суспензия должна свободно проходить в шприц через иглу N 0840. Определение проводят в соответствии с ОФС "Лекарственные формы для парентерального применения".
pH. От 7,1 до 7,3. Определение проводят потенциометрическим методом в соответствии с ОФС "Ионометрия". Для испытания используют содержимое 5 ампул (флаконов) препарата, разведенного в 25 мл 0,9% раствора натрия хлорида, pH (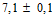 ).
).
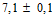 ).
).Средняя масса и отклонение от средней массы. Коэффициент вариации массы вакцины в ампулах (флаконах) должен быть не более 5%. Определение проводят в соответствии с ОФС "Однородность массы дозированных лекарственных форм".
Потеря в массе при высушивании. Не более 5,0%. Определение проводят в соответствии с ОФС "Потеря в массе при высушивании".
Общий азот. Не более 0,4 мг/мл. Определение проводят в соответствии с ОФС "Определение общего азота с реактивом Несслера в иммунобиологических лекарственных препаратах".
Алюминия гидроксид. Не более 2,7 мг/мл алюминия (III). Определение проводят в соответствии с ОФС "Определение ионов алюминия в сорбированных иммунобиологических лекарственных препаратах".
Формальдегид. Не более 0,001%. Определение проводят в соответствии с ОФС "Количественное определение формальдегида в иммунобиологических лекарственных препаратах".
Полнота сорбции антигена. Надосадочная жидкость должна содержать не более 25 ЕА/мл (единиц активности в мл). Содержимое ампулы (флакона) ресуспендируют в 5 мл 0,9% раствора натрия хлорида, перемешивают и отделяют осадок центрифугированием при 2000 об/мин в течение 30 мин. Отбирают 1 мл надосадочной жидкости и разводят в 2; 4 и 8 раз 0,2 М фосфатным буферным раствором, pH (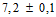 ). Определение полноты сорбции антигена проводят в реакции иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Приготовление агара, постановку реакции и расчет результатов анализа проводят, как описано в разделе "Специфическая активность".
). Определение полноты сорбции антигена проводят в реакции иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Приготовление агара, постановку реакции и расчет результатов анализа проводят, как описано в разделе "Специфическая активность".
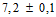 ). Определение полноты сорбции антигена проводят в реакции иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Приготовление агара, постановку реакции и расчет результатов анализа проводят, как описано в разделе "Специфическая активность".
). Определение полноты сорбции антигена проводят в реакции иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Приготовление агара, постановку реакции и расчет результатов анализа проводят, как описано в разделе "Специфическая активность".Полноту сорбции оценивают по максимальному разведению супернатанта, при котором еще образуется видимая линия преципитации с иммуноглобулином противосибиреязвенным, и выражают в единицах активности, содержащихся в 1 мл (ЕА/мл).
Отсутствие посторонних микроорганизмов и грибов. Вакцина не должна содержать посторонних микроорганизмов и грибов. Определение проводят, в соответствии с ФС "Вакцина сибиреязвенная живая".
Специфическая безопасность. Вакцина должна быть безопасной. Вакцину растворяют в 5 мл 0,9% натрия хлорида для инъекций. Испытание проводят по методике, описанной в ФС "Вакцина сибиреязвенная живая". Животным вводят вакцину подкожно в область внутренней поверхности каждого бедра в объеме 1,25 мл (общий объем - 2,5 мл).
1. Количество живых спор. Процент живых спор на плотной питательной среде должен составлять не менее 30 от расчетной концентрации. В 1 мл препарата после ресуспендирования расчетная концентрация составляет (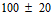 ) млн. спор B. anthracis СТИ-1.
) млн. спор B. anthracis СТИ-1.
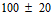 ) млн. спор B. anthracis СТИ-1.
) млн. спор B. anthracis СТИ-1.В каждую из 3 ампул (флаконов) вносят 5 мл воды очищенной, встряхивают до образования гомогенной взвеси. Далее определение проводят по методике в соответствии с ФС "Вакцина сибиреязвенная живая".
2. Активность (ПА. Активность ПА должна быть не менее 50 ЕА/мл.
Определение проводят методом иммунодиффузии в агаре по Оухтерлони с иммуноглобулином противосибиреязвенным лошадиным. Для приготовления агара к 1 л 0,1 М фосфатного буферного раствора, pH (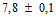 ) добавляют 1% агара, 1% желатина и 0,25% раствор фенола. Агар стерилизуют 15 мин при температуре (
) добавляют 1% агара, 1% желатина и 0,25% раствор фенола. Агар стерилизуют 15 мин при температуре ( ) °С и в горячем виде осветляют центрифугированием при 2000 об/мин в течение 5 мин. Готовый агар разливают в чашки Петри, помещенные на строго горизонтальную поверхность, слоем толщиной 6 мм. Стерильным штампом-пробойником вырезают 1 центральную и 6 радиальных лунок, расстояние между центрами которых составляет 10 мм (можно выполнять этот этап по трафарету). Агар из лунок удаляют.
) °С и в горячем виде осветляют центрифугированием при 2000 об/мин в течение 5 мин. Готовый агар разливают в чашки Петри, помещенные на строго горизонтальную поверхность, слоем толщиной 6 мм. Стерильным штампом-пробойником вырезают 1 центральную и 6 радиальных лунок, расстояние между центрами которых составляет 10 мм (можно выполнять этот этап по трафарету). Агар из лунок удаляют.
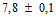 ) добавляют 1% агара, 1% желатина и 0,25% раствор фенола. Агар стерилизуют 15 мин при температуре (
) добавляют 1% агара, 1% желатина и 0,25% раствор фенола. Агар стерилизуют 15 мин при температуре (Вакцину последовательно разводят 0,2 М фосфатным буферным раствором, pH ( ), до разведений 1:2; 1:4; 1:6; 1:8. В центральную лунку вносят 0,04 мл цельного иммуноглобулина противосибиреязвенного лошадиного, а в радиальные лунки по часовой стрелке - все разведения вакцины, начиная с цельного неразведенного препарата. Чашки помещают в эксикатор, содержащий воду очищенную, при температуре (
), до разведений 1:2; 1:4; 1:6; 1:8. В центральную лунку вносят 0,04 мл цельного иммуноглобулина противосибиреязвенного лошадиного, а в радиальные лунки по часовой стрелке - все разведения вакцины, начиная с цельного неразведенного препарата. Чашки помещают в эксикатор, содержащий воду очищенную, при температуре ( ) °С в течение 3 сут. Предварительный учет результатов проводят через 24 ч, окончательный - на 3 сут.
) °С в течение 3 сут. Предварительный учет результатов проводят через 24 ч, окончательный - на 3 сут.
 ), до разведений 1:2; 1:4; 1:6; 1:8. В центральную лунку вносят 0,04 мл цельного иммуноглобулина противосибиреязвенного лошадиного, а в радиальные лунки по часовой стрелке - все разведения вакцины, начиная с цельного неразведенного препарата. Чашки помещают в эксикатор, содержащий воду очищенную, при температуре (
), до разведений 1:2; 1:4; 1:6; 1:8. В центральную лунку вносят 0,04 мл цельного иммуноглобулина противосибиреязвенного лошадиного, а в радиальные лунки по часовой стрелке - все разведения вакцины, начиная с цельного неразведенного препарата. Чашки помещают в эксикатор, содержащий воду очищенную, при температуре (Активность ПА оценивают по максимальному разведению вакцины, при котором образуется видимая линия преципитации с иммуноглобулином противосибиреязвенным, и выражают в единицах активности (ЕА/мл).
Расчет ПА (А) в ЕА/мл проводят по формуле:
где: T - разведение вакцины, при котором наблюдается видимая линия преципитации;
V - объем пробы, внесенный в лунку, мл.
3. Иммуногенность для морских свинок. Индекс иммунитета должен быть не менее 25000 (отношение величины LD50 заражающего тест-штамма B. anthracis 71/12 для иммунизированных животных к величине LD50 для неиммунизированных животных). В 4 образца с вакциной вносят по 5 мл 0,9% раствора натрия хлорида для инъекций, встряхивают до образования гомогенной взвеси. Иммунизирующую дозу в объеме 0,5 мл вводят морским свинкам подкожно в область внутренней поверхности бедра. Далее определение проводят в соответствии с ФС "Вакцина сибиреязвенная живая".
4. Иммуногенность для кроликов. Препарат должен предохранять от гибели не менее 8 из 10 кроликов, привитых подкожно одной человеческой дозой вакцины, при подкожном инфицировании 100 LD50 вирулентного штамма сибиреязвенного микроба.
Испытание проводят на кроликах обоего пола массой (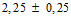 ) кг. Животных иммунизируют однократно подкожно в область внутренней поверхности бедра в объеме 0,5 мл (одна человеческая доза вакцины). Одновременно 3 контрольным кроликам вводят по 0,5 мл стерильного 0,9% раствора натрия хлорида.
) кг. Животных иммунизируют однократно подкожно в область внутренней поверхности бедра в объеме 0,5 мл (одна человеческая доза вакцины). Одновременно 3 контрольным кроликам вводят по 0,5 мл стерильного 0,9% раствора натрия хлорида.
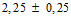 ) кг. Животных иммунизируют однократно подкожно в область внутренней поверхности бедра в объеме 0,5 мл (одна человеческая доза вакцины). Одновременно 3 контрольным кроликам вводят по 0,5 мл стерильного 0,9% раствора натрия хлорида.
) кг. Животных иммунизируют однократно подкожно в область внутренней поверхности бедра в объеме 0,5 мл (одна человеческая доза вакцины). Одновременно 3 контрольным кроликам вводят по 0,5 мл стерильного 0,9% раствора натрия хлорида.Для определения LD50 тест-культуры B. anthracis Ч-7 интактных кроликов инфицируют дозами 101; 102; 103 и 104 спор. Каждую дозу вводят не менее чем 3 кроликам подкожно в паховую область задней конечности в объеме 1 мл. Наблюдение за животными проводят в течение 10 сут. Рассчитывают LD50 по методу Кербера в модификации И.П.Ашмарина.
Через 10 сут. кроликов (10 иммунизированных и 3 контрольных - неиммунизированных) заражают 100 LD50 споровой культуры B. anthracis Ч-7. Наблюдение за животными проводят в течение 10 сут. Погибших животных вскрывают и делают посев 0,1 мл крови из сердца на чашки Петри с агаром Хоттингера, pH (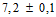 ). Сибиреязвенную инфекцию подтверждают в случае обнаружения роста, характерного для сибиреязвенного микроба. Зараженные контрольные (неиммунизированные) кролики должны погибнуть в течение 3 сут.
). Сибиреязвенную инфекцию подтверждают в случае обнаружения роста, характерного для сибиреязвенного микроба. Зараженные контрольные (неиммунизированные) кролики должны погибнуть в течение 3 сут.
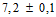 ). Сибиреязвенную инфекцию подтверждают в случае обнаружения роста, характерного для сибиреязвенного микроба. Зараженные контрольные (неиммунизированные) кролики должны погибнуть в течение 3 сут.
). Сибиреязвенную инфекцию подтверждают в случае обнаружения роста, характерного для сибиреязвенного микроба. Зараженные контрольные (неиммунизированные) кролики должны погибнуть в течение 3 сут.Растворители, выпускаемые в комплекте с препаратом. 0,9% раствор натрия хлорида.
Упаковка и маркировка. В соответствии с ОФС "Иммунобиологические лекарственные препараты".
Транспортирование и хранение. При температуре от 2 до 8°С.