СПРАВКА
Источник публикации
Документ опубликован не был
Примечание к документу
Текст документа приведен в соответствии с публикацией на сайте https://minzdrav.gov.ru/ по состоянию на 21.08.2023.
В соответствии с Приказом Минздрава России от 20.07.2023 N 377 данный документ введен в действие с 01.09.2023.
Название документа
"ФС.2.1.0430. Фармакопейная статья. Кандесартана цилексетил. Кандесартан"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание")
"ФС.2.1.0430. Фармакопейная статья. Кандесартана цилексетил. Кандесартан"
(утв. и введена в действие Приказом Минздрава России от 20.07.2023 N 377)
("Государственная фармакопея Российской Федерации. XV издание")
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Кандесартана цилексетил Кандесартан Candesartani cilexetili | ФС.2.1.0430 |
Вводится впервые |
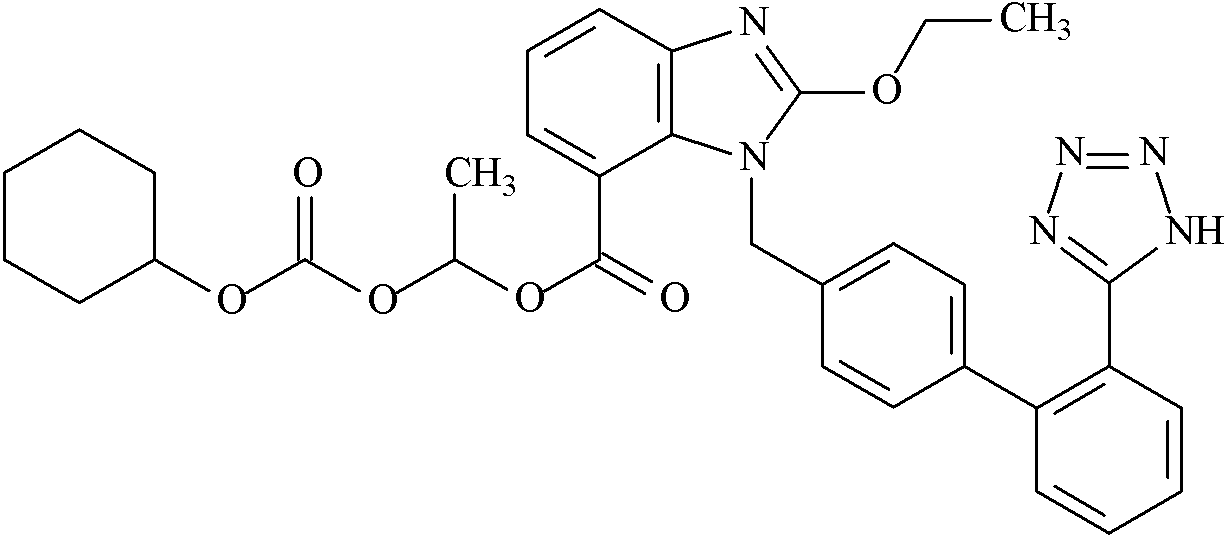
C33H34N6O6 [145040-37-5] | М.м. 610,66 |
[(1RS)-1-{[(Циклогексилокси)карбонил]окси}этил](1-{[2'-(1H-1,2,3,4-тетразол-5-ил)[1,1'-бифенил]-4-ил]метил}-2-этокси-1H-1,3-бензодиазол-7-карбоксилат).
Содержит не менее 99,0% и не более 101,0% кандесартана цилексетила в пересчете на безводное и свободное от остаточных органических растворителей вещество.
Производителям кандесартана цилексетила необходимо проводить оценку риска образования N-нитрозаминов и загрязнения ими в процессе производства. При выявлении потенциального риска процесс производства должен быть изменен, чтобы исключить или минимизировать загрязнение.
Описание. Белый или почти белый кристаллический порошок.
<*> Проявляет полиморфизм.
--------------------------------
<*> Приводится для информации.
Растворимость. Легко растворим в метиленхлориде, мало растворим в этаноле, практически нерастворим в воде.
ИК-спектрометрия (ОФС "Спектрометрия в средней инфракрасной области"). Инфракрасный спектр субстанции в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру фармакопейного стандартного образца кандесартана цилексетила.
Если спектры различаются, испытуемую субстанцию и стандартный образец по отдельности растворяют в этаноле, выпаривают досуха и записывают спектры сухих остатков.
Родственные примеси. Определение проводят методом ВЭЖХ (ОФС "Высокоэффективная жидкостная хроматография").
Все растворы используют свежеприготовленными.
Подвижная фаза А (ПФА). Уксусная кислота ледяная - вода - ацетонитрил 10:430:570.
Подвижная фаза Б (ПФБ). Уксусная кислота ледяная - вода - ацетонитрил 10:100:900.
Растворитель. Вода - ацетонитрил 40:60.
Испытуемый раствор. В мерную колбу вместимостью 50 мл помещают 20 мг субстанции, растворяют в растворителе, перемешивают и доводят объем раствора тем же растворителем до метки.
Раствор сравнения. В мерную колбу вместимостью 50 мл помещают 1,0 мл испытуемого раствора и доводят объем раствора растворителем до метки. В мерную колбу вместимостью 20 мл помещают 1,0 мл полученного раствора и доводят объем раствора растворителем до метки.
Раствор для проверки разделительной способности хроматографической системы. В мерную колбу вместимостью 10 мл помещают 5 мг фармакопейного стандартного образца кандесартана цилексетила для проверки пригодности хроматографической системы, содержащего примеси A, B и F, растворяют в растворителе и доводят объем раствора растворителем до метки.
Раствор для идентификации пиков. В мерную колбу вместимостью 5 мл помещают 2,5 мг фармакопейного стандартного образца кандесартана цилексетила для идентификации пиков, содержащего примеси G и H, растворяют в растворителе и доводят объем раствора растворителем до метки.
Примечание
Примесь A: этил(1-{[2'-(1H-1,2,3,4-тетразол-5-ил)[1,1'-бифенил]-4-ил]метил}-2-этокси-1H-1,3-бензодиазол-7-карбоксилат) [139481-58-6].
Примесь B: [(1RS)-1-{[(циклогексилокси)карбонил]окси}этил](2-оксо-1-{[2'-(1H-1,2,3,4-тетразол-5-ил)[1,1'-бифенил]-4-ил]метил}-2,3-дигидро-1H-1,3-бензодиазол-7-карбоксилат) [869631-11-8].
Примесь F: N2-ethyl candesartan cilexetil, [(1RS)-1-{[(циклогексилокси)карбонил]окси}этил](1-{[2'-(2H-2-этил-1,2,3,4-тетразол-5-ил)[1,1'-бифенил]-4-ил]метил}-2-этокси-1H-1,3-бензодиазол-7-карбоксилат) [914613-36-8].
Примесь G: 1-{[2'-(1H-1,2,3,4-тетразол-5-ил)[1,1'-бифенил]-4-ил]метил}-2-этокси-1H-1,3-бензодиазол-7-карбоновая кислота [139481-59-7].
Примесь H: [(1RS)-1-{[(циклогексилокси)карбонил]окси}этил][1-({2'-[1H-1-(трифенилметил)-1,2,3,4-тетразол-5-ил][1,1'-бифенил]-4-ил}метил)-2-этокси-1H-1,3-бензодиазол-7-карбоксилат] [170791-09-0].
Хроматографические условия
Колонка | 150 x 3,9 мм, силикагель октадецилсилильный для хроматографии, 4 мкм; |
Температура колонки | 25 °C; |
Скорость потока | 0,8 мл/мин; |
Детектор | спектрофотометрический, 254 нм; |
Объем пробы | 10 мкл. |
Режим хроматографирования
Время, мин | ПФА, % | ПФБ, % |
0 - 3 | 100 | 0 |
3 - 33 |  | 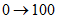 |
33 - 40 | 0 | 100 |
40 - 50 | 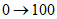 | 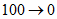 |
Хроматографируют раствор для проверки разделительной способности хроматографической системы, раствор для идентификации пиков, раствор сравнения и испытуемый раствор.
Относительное время удерживания соединений. Кандесартана цилексетил - 1 (около 11 мин); примесь G - около 0,2; примесь A - около 0,4; примесь B - около 0,5; примесь F - около 2,0; примесь H - около 3,5.
Идентификация примесей. Для идентификации пиков примесей A, B и F используют относительное время удерживания соединений, хроматограмму, прилагаемую к фармакопейному стандартному образцу кандесартана цилексетила для проверки пригодности хроматографической системы, и хроматограмму раствора для проверки разделительной способности хроматографической системы. Для идентификации пиков примесей G и H используют относительное время удерживания соединений, хроматограмму, прилагаемую к фармакопейному стандартному образцу кандесартана для идентификации пиков, и хроматограмму раствора для идентификации примесей.
Пригодность хроматографической системы. На хроматограмме раствора для проверки разделительной способности хроматографической системы разрешение (RS) между пиками примесей A и B должно быть не менее 4,0.
Поправочные коэффициенты. Для расчета содержания площади пиков следующих примесей умножаются на соответствующие поправочные коэффициенты: примеси A и G - 0,7; примесь H - 1,6.
Допустимое содержание примесей. На хроматограмме испытуемого раствора:
- площадь пика примеси B не должна более чем в три раза превышать площадь основного пика на хроматограмме раствора сравнения (не более 0,3%);
- площадь пика каждой из примесей F и G не должна более чем в два раза превышать площадь основного пика на хроматограмме раствора сравнения (не более 0,2%);
- площадь пика каждой из примесей A и H не должна более чем в полтора раза превышать площадь основного пика на хроматограмме раствора сравнения (не более 0,15%);
- площадь пика любой другой примеси не должна превышать площадь основного пика на хроматограмме раствора сравнения (не более 0,1%);
- сумма площадей пиков всех примесей не должна превышать шестикратную площадь основного пика на хроматограмме раствора сравнения (не более 0,6%).
Не учитывают пики, площадь которых менее 0,5 площади основного пика на хроматограмме раствора сравнения (менее 0,05%).
N-нитрозамины. Определение проводят в соответствии с ОФС "Примеси N-нитрозаминов".
Допустимое содержание примесей:
- N-нитрозодиметиламин (НДМА) - не более 0,03 мкг/г;
- N-нитрозодиэтиламин (НДЭА) - не более 0,02 мкг/г.
Вода. Не более 0,3% (ОФС "Определение воды", метод 1). Для определения используют 60 мг (точная навеска) субстанции.
Сульфатная зола. Не более 0,1% (ОФС "Сульфатная зола"). Для определения используют 1 г (точная навеска) субстанции.
Тяжелые металлы. Не более 0,002% Определение проводят в соответствии с ОФС "Тяжелые металлы" (метод 3Б) в зольном остатке, полученном в испытании "Сульфатная зола", с использованием эталонного раствора 2.
Остаточные органические растворители. В соответствии с требованиями ОФС "Остаточные органические растворители".
Микробиологическая чистота. В соответствии с требованиями ОФС "Микробиологическая чистота".
Определение проводят методом титриметрии (ОФС "Титриметрия (титриметрические методы анализа)").
Растворяют 0,5 г (точная навеска) субстанции в 60 мл уксусной кислоты безводной и немедленно титруют 0,1 М раствором хлорной кислоты. Конечную точку титрования определяют потенциометрически (ОФС "Потенциометрическое титрование") по первому перегибу на кривой титрования.
1 мл 0,1 М раствора хлорной кислоты соответствует 61,07 мг кандесартана цилексетила C33H34N6O6.
В защищенном от света месте.