Скачать Методические рекомендации 10-5ФЦ/2557 Качественное и количественное определение генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания и пищевом сырье с использованием сухих наборов реагентов серии RT-ПЦР-ядро
Дата актуализации: 01.01.2021

 Методические рекомендации 10-5ФЦ/2557
Методические рекомендации 10-5ФЦ/2557
Качественное и количественное определение генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания и пищевом сырье с использованием "сухих" наборов реагентов серии "RT-ПЦР-ядро"
| Обозначение: |  Методические рекомендации 10-5ФЦ/2557 Методические рекомендации 10-5ФЦ/2557 |
| Обозначение англ: |  Recommended Practice 10-5ФЦ/2557 Recommended Practice 10-5ФЦ/2557 |
| Статус: | введен впервые |
| Название рус.: | Качественное и количественное определение генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания и пищевом сырье с использованием "сухих" наборов реагентов серии "RT-ПЦР-ядро" |
| Дата добавления в базу: | 01.01.2019 |
| Дата актуализации: | 01.01.2021 |
| Область применения: | Методические рекомендации подготовлены для выявления и количественного определения генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания и пищевом сырье методом ПЦР в режиме реального времени с помощью "сухих" наборов реагентов серии "RT-ПЦР-ядро" производства ООО "Компания "Биоком". Методические рекомендации предназначены для применения в лабораторных организаций Роспотребнадзора, осуществляющих контроль за качеством и безопасностью продовольственного сырья и пищевых продуктов, в т.ч. импортируемых в Российскую Федерацию, в лабораториях других организаций, аккредитованных в установленном порядке. |
| Оглавление: | 1. Общие положения и область применения 2. Нормативные ссылки 3. Сущность метода 3.1. Качественное определение ГМИ 3.2. Количественное определение ГМИ 4. Получение результатов при проведении ПЦР в режиме реального времени 5. Особенности проведения работ в ПЦР-лаборатории, в которой используется метод ПЦР в режиме реального времени 5.1. Помещение лаборатории 5.2. Оборудование 5.3. Требования к проведению исследований 5.4. Требования к персоналу 6. Аппаратура, материалы и реагенты 6.1. Аппаратура и материалы 6.1. Реагенты 7. Отбор, хранение и подготовка проб пищевых продуктов для анализа 7.1. Отбор и подготовка к анализу жидких и полужидких материалов исследования (соусы, пасты, майонезы и пр.) 7.2. Отбор и подготовка к анализу сухих сыпучих материалов исследования (мука, белковый изолят и пр.) 7.3. Отбор и подготовка к анализу материалов исследования плотной консистенции (колбаса, сыр, растительные ткани, чипсы, поп-корн, соевый шрот, фуражная кукуруза и пр.) 7.4. Условия хранения и транспортирования образцов 8. Порядок проведения исследования 8.1. Выделение ДНК из образцов продуктов и сырья с использованием набора реагентов серии "Silica" 8.2. Качественное определение генетически модифицированной ДНК методом ПЦР в режиме реального времени 8.3. Количественное определение генетически модифицированной ДНК сои линии 40-3-2 методом ПЦР в режиме реального времени 9. Интерпретация результатов анализа 9.1. Качественное определение ГМИ 9.2. Количественное определение ГМИ Приложение 1. Характеристики амплификатора Smart Cycler II, которые являются существенными при его использовании для проведения массовых исследований Приложение 2. Характеристики генетически-модифицированных растений, зарегистрированных Минздравом России и разрешенных для применения в пищевой промышленности и реализации населению |
| Разработан: | ООО Компания Биоком ФГУЗ Федеральный центр гигиены и эпидемиологии Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека ЗАО Сэйдж |
| Утверждён: | 09.09.2005 Главный врач ФГУЗ Федеральный центр гигиены и эпидемиологии Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (10-5ФЦ/2557) |
| Издан: | Федеральный центр гигиены и эпидемиологии Роспотребнадзора (2006 г. ) |
| Нормативные ссылки: |
|








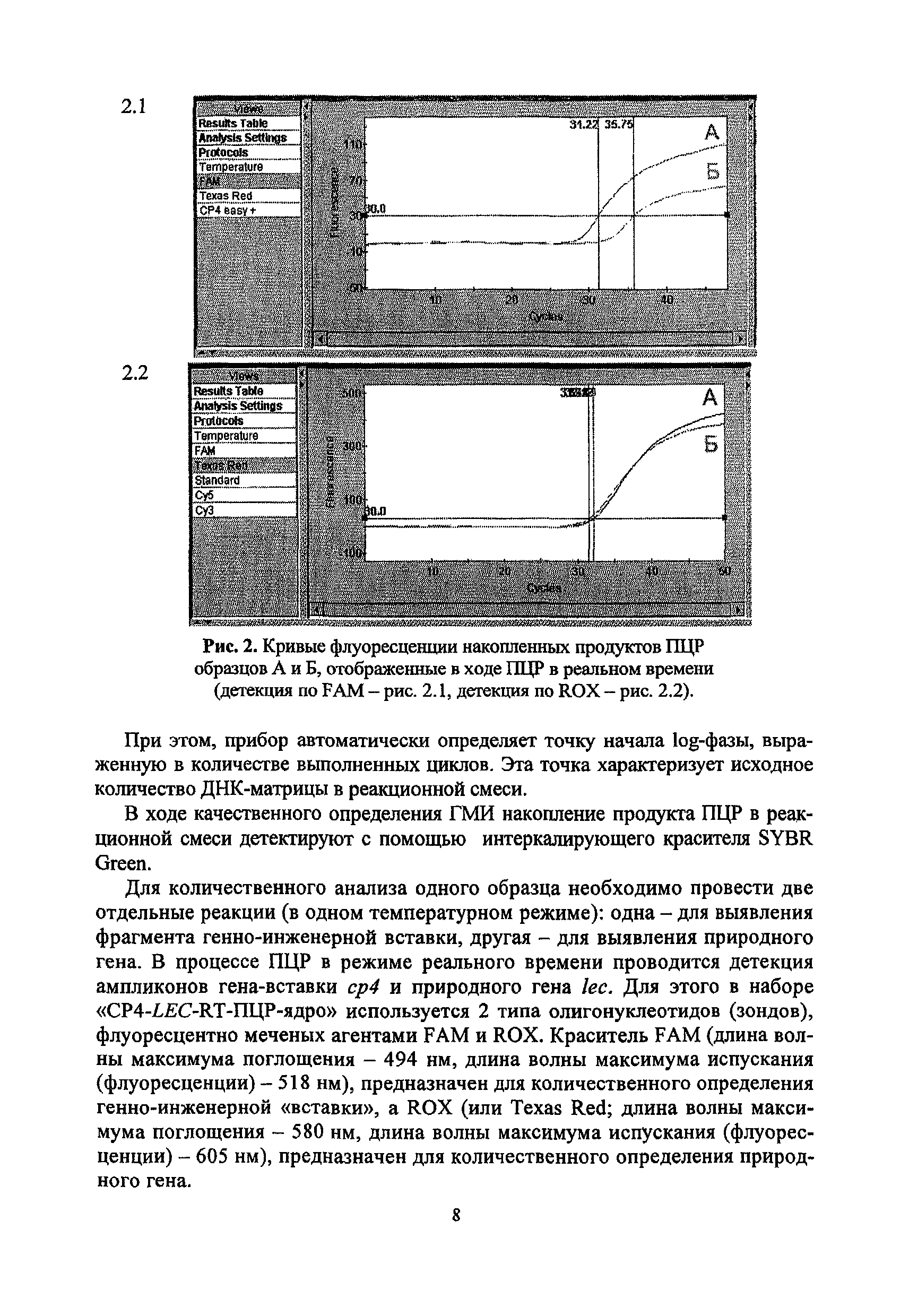










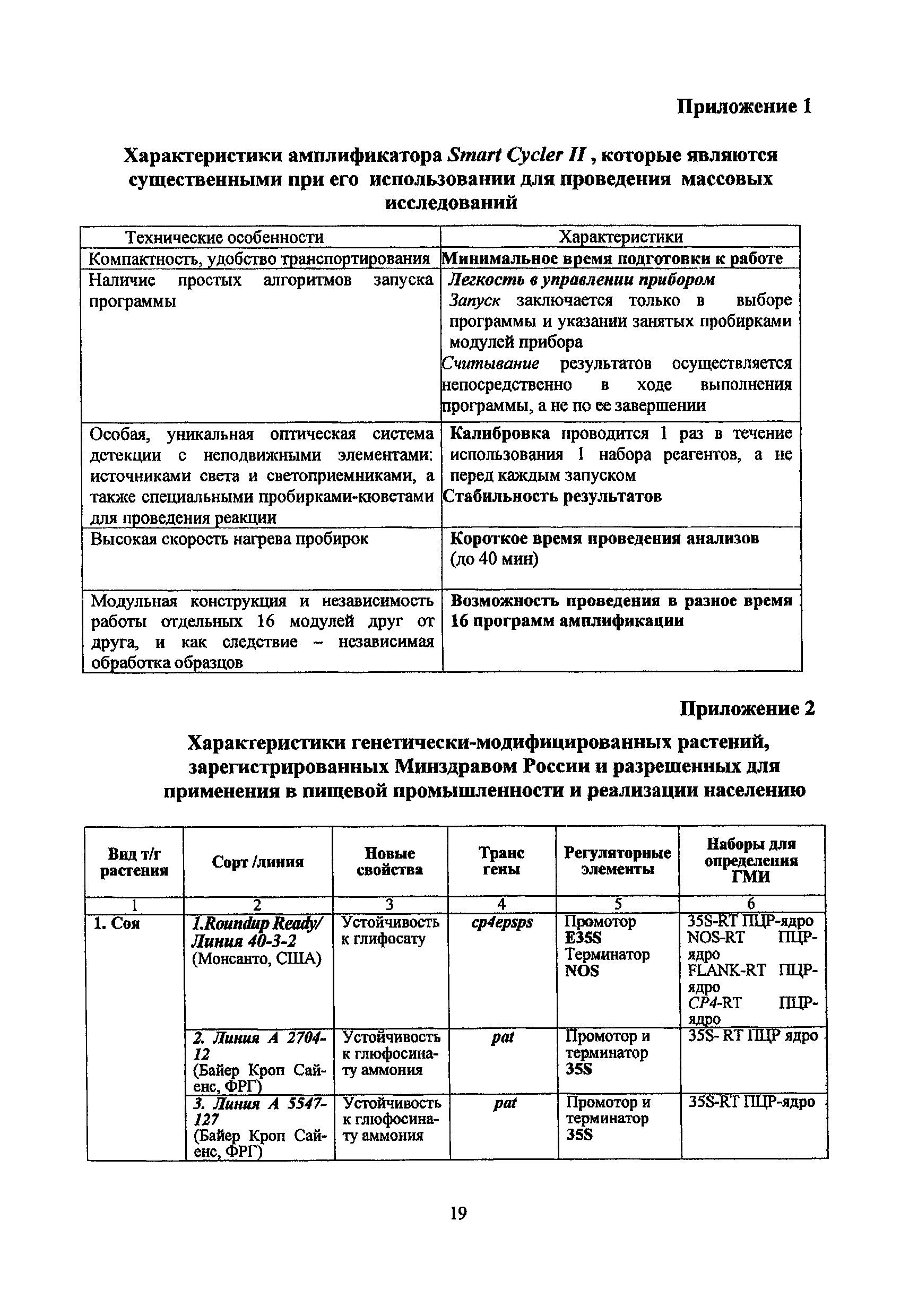
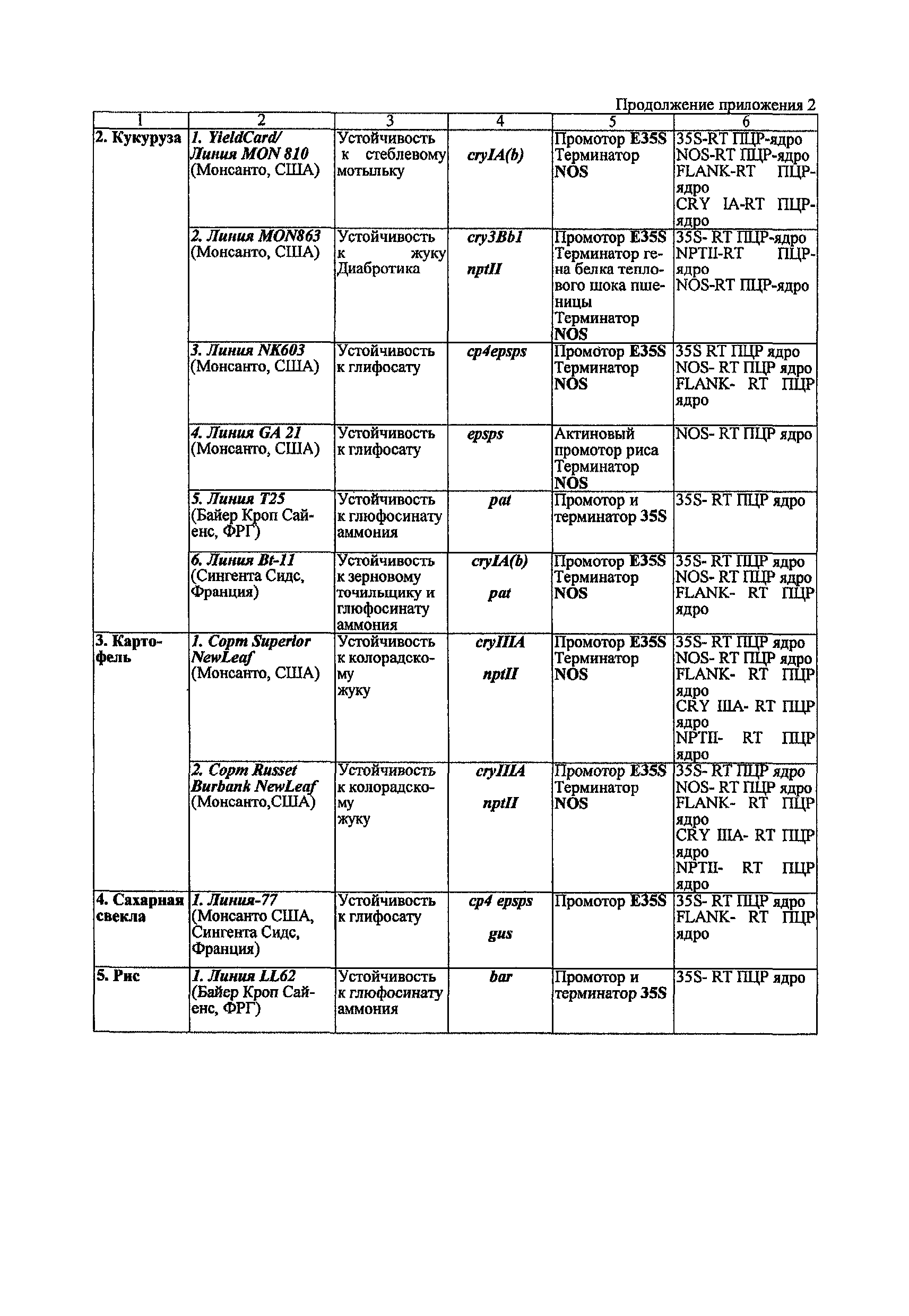


 Федеральный закон 52-ФЗ «О санитарно-эпидемиологическом благополучии населения»
Федеральный закон 52-ФЗ «О санитарно-эпидемиологическом благополучии населения»